Пищевое отравление Bacillus cereus и его лечение
Добавил пользователь Евгений Кузнецов Обновлено: 28.01.2026
Пищевое отравление ботулинотоксином (Clostridium botulinum) и его лечение
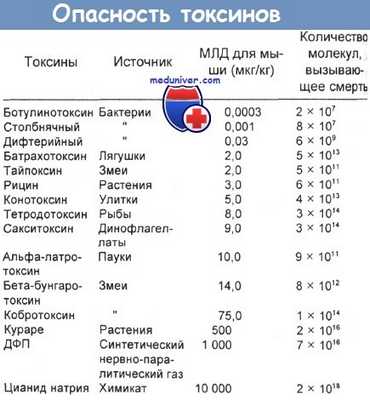
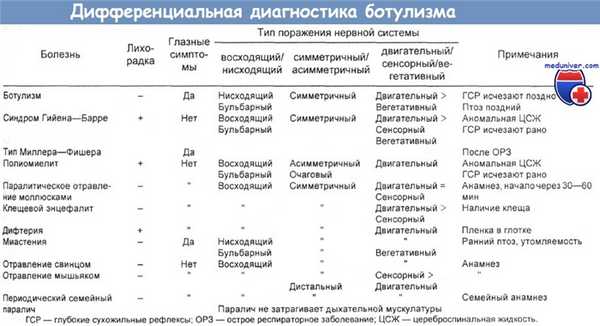
В таблице ниже приведены сравнительные данные по летальности ряда токсинов. Одну из схем дифференциальной диагностики ботулизма предложили Motenson и соавт..
а) Распространенность. В одной серии наблюдений токсин Clostridium botulinum типа А вызвал заболевание у 48 % пациентов, типа В — у 29 %, типа Е — у 23 %. Медиана инкубационного периода для всех пациентов составила 1 сут (общие диапазоны: 0 — 7 сут для типа А, 0 - 5 сут для типа В и 0 - 2 сут для типа Е).
б) Пробы кала. Невозможность выявить токсин в большинстве проб кала, полученных ранее или позднее 3 сут после перорального отравления, говорит о том, что за этот период вещество всасывается в пищеварительном тракте, расщепляется или выделяется. Влияет ли внутривенное введение антитоксина на исчезновение токсина из просвета кишечника, неизвестно.
в) Лабораторные данные. У каждого пациента с подозрением на ботулизм надо взять сыворотку, кал и, по возможности, желудочный аспират на выявление токсина и анаэробный посев. Однако, если при диагностике слишком большое значение придается только лабораторным данным, возможен ложноотрицательный результат.
г) Лечение отравление ботулинотоксином. Большинство вспышек пищевого ботулизма в США связано с потреблением неправильно приготовленных и/или плохо хранившихся домашних консервов, в основном овощных, прежде всего из спаржи, зеленой фасоли и паприки (Центры по борьбе с болезнями, неопубликованные данные).
Для консервирования овощей надо использовать автоклав, позволяющий в течение 10 мин поддерживать температуру выше 100 С: это убивает споры возбудителя, однако оптимальное время и давление такой термообработки зависят от конкретного пищевого продукта. Варенье можно без опасений "закатывать" и без автоклавирования, поскольку высокое содержание в нем сахара не позволяет размножаться Clostridium botulinum.
Инструкции по домашнему консервированию можно получить в окружных отделах службы здравоохранения. Прошедшую термообработку пищу нельзя хранить при температуре 4 — 60 °С более 4 ч. Кипячение продуктов в течение 10 мин перед едой уничтожает любой присутствующий в них токсин.
3,4-Диаминопиридин, испытанный двойным слепым методом с контролем-плацебо на больных ботулизмом А, не улучшает мышечной силы, дыхательной функции и сложного мышечного потенциала действия на электромиограмме.
Человеческий "ботулиновый" иммуноглобулин (БИГ) должен был выпускаться в Калифорнии с 1 января 1991 г., однако из-за войны в Заливе появился только 1 февраля 1992 г. Клинические испытания БИГ находятся в стадии уточнения эффективности (фаза И) и спонсируются Программой "лекарства для сирот" ("Orphan Drug Program") Управления FDA и Калифорнийским департаментом здравоохранения.
Накопленный опыт позволяет считать, что лучший результат в случае пищевого ботулизма достигается при скорейшем начале лечения. Врачи, подозревающие у пациентов детский ботулизм, могут получить БИГ в США, заказав его в любое время суток по телефону (510) 540-2646. Есть надежда, что применение БИГ существенно сократит продолжительность болезни и стоимость пребывания отравившихся младенцев в больнице.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Bacillus cereus у детей
В. cereus – название бактерий и болезней, которые ими вызваны. Инфекционный процесс может быть либо локализированным либо генерализированным. Чаще всего болезнь проходит как острый гастроэнтерит.
В группе риска находятся новорожденные, ослабленные, дети с иммунодефицитными состояниями, а также больные со злокачественными новообразованиями. В таких случаях Bacillus cereus сопровождается упорной бактериемией и нередко принимает форму сепсиса.
Эпидемиология. Бактерии рода Bacillus распространены во всех странах. Они «проживают» в почве, воздухе, на окружающих предметах и в воде. Инфекцию можно подхватить из пищевых продуктов, мединструментов, медаппаратуры, которые применяются для инвазивных лечений и исследований (клапанная аппаратура, системы для гемодиализа, катетеры и пр.). Пути передачи Bacillus cereus: алиментарный, контактный. Заболеваемость имеет спорадический характер (отдельные, не связанные, периодические случаи), но вспышки острого гастроэнтерита могут возникать при пищевом инфицировании.
Что провоцирует / Причины Bacillus cereus у детей:
В. census относятся к роду Bacillus. Они имеют палочковидную форму. Размер бактерий 2,2х 1,2—7 мкм, они подвижны, обладают имеют латерально расположенными жгутиками. По Граму окрашиваются положительно. Относятся к строгим аэробам, формируют эндоспоры. Bacillus подразделяются на 3 морфологические группы в зависимости от формы и раздувания клетки при спорообразовании. Возбудители болезни у детей, взрослых и животных относятся в основном к первой группе.
На данный момент науке известно примерно 20 серотипов данной бактерии. Их нельзя убить широко распространенными, традиционными дезинфицирующими растворами и препаратами.
В. cereus производят гемолизин, сходный со стрептолизином С, протсолитические ферменты, фосфолипазы, пенициллипазу, лецитиназу и пр.
Патогенез (что происходит?) во время Bacillus cereus у детей:
Инфекция проникает в организм черед ротоглотку, дыхательные пути или повреждения на коже. Большую роль играют инвазивные операции: ввод катетеров, клапанных аппаратов, шунтов, подключение системы гемодиализа и т. д. Такими путями В. cereus может попадать в кровь в большом количестве, находясь на инструментарии, перечисленном выше.
Если путь заражения алиментарный, данные бактерии приводят к острому гастроэнтериту. Энтеротоксин при этом приводит к поражению желудочно-кишечного тракта. Он же стимулирует систему циклических пуклеотидов в эпителиальных клетках тонкой кишки, вызывает повреждение слизистой оболочки желудка и тонкой кишки и нарушение сосудистой проницаемости. Из-за этого появляются такие симптомы как рвота и диарея.
От количества выработанного В. cereus пиогенного токсина зависит степень тяжести поражения ЖКТ и других органов. Данный токсин вызывает изъязвление эпителия дыхательных путей, деструкцию слизистой оболочки кишечника, абсцедирование (в том числе и ткани головного мозга).
Пищевое отравление В. cereus заканчивается благоприятно по причине локализации процесса. Инфекция, вызванная В. cereus, становится септической (и наблюдается упорная бактериемия) у ослабленных стрессами или иммунодефицитами детей, а также у новорожденных. В этих случаях морфологические изменения в органах (кишечник, легкие, мозг) выражаются в появлении острых воспалительных очагов с зонами некроза, фибриноидным некрозом артерий, в которых выявляются большие скопления В. cereus.
Симптомы Bacillus cereus у детей:
Инфекционный процесс, к которому приводят рассматриваемые бактерии, может проявляться разными симптомами. Пищевое отравление «выливается» острым гастроэнтеритом. При иных путях заражения наблюдается развитие менингита, бронхопневмонии, остеомиелита, абсцесса мозга, панофтальмита, эндокардит, сепсиса, бактериемии.
Инкубационный период при остром гастроэнтерите составляет от 1 до 16 часов. Болезнь имеет острое начало, ребенка тошнит, он жалуется на боли в животе. Повышения температуры обычно нет. Появляется рвота (возможно – многократная), а через несколько часов отмечают водянистую диарею. Отмечаются болезненные позывы на дефекацию («в туалет»). В некоторых случаях болезнь может проходить по аналогии с пищевой токсикоинфекции. Тогда, прежде всего, появляется профузная рвота, а диареи нет.
Острый гастроэнтерит может проходить в легкой или среднетяжелой форме. Тяжелые формы – очень большая редкость. Болезнь может длиться как несколько часов, так и 2 суток.
Пневмония, вызванная Bacillus cereus, начинается остро – появляется лихорадка и одышка. Появляются боли в области грудины. Рентген показывается Рентгенологически выявляется одно- или двусторонний инфильтративный процесс с поражением одной или нескольких долей легкого и вовлечением плевры. Пневмония может быть геморрагической, в таком случаи часты летальные исходы.
Менингит имеет острое начало, температура очень высокая, рвота повторная, развиваются менингеальные симптомы, повторные судороги. Состояние больного ребенка тяжелое. В спинномозговой жидкости обнаруживают значительный плеоцитоз, а лимфоциты и нейтрофилы наличествуют в равном количестве. В периферической крови может быть лейкоцитоз с нейтрофильным сдвигом. Симптомы проявляются довольно долго, не помогают препараты пенициллинового ряда.
Септицемия. Инфекционный процесс, вызванный Bacillus cereus, может проявляться септицемией с очагами воспаления или без них. Показательный симптом – упорная лихорадка, которая становится интермиттирующей (перемежающейся). Источник инфекции удается установиться не всегда (как и «входные ворота»). При данной форме инфекции В. cereus выделяется в чистой культуре.
Диагностика Bacillus cereus у детей:
Для точного диагноза используют только выделение возбудителя из биологического материала от заболевшего ребенка и доказательство патогенности выделенных бактерий. Для анализа используют кровь, рвотные массы, мокроту, мочу, испражнения, отделяемое из очага воспаления (гной, слизь). Диагностическое значение имеет большое количество бактерий при остром гастроэнтерите. При других поражениях необходимо получить высев микроба в повторных порциях крови.
Поскольку по клиническим проявлениям инфекцию, вызванную В. cereus, невозможно отличить от других инфекций, решающее значение придается повторному обнаружению В. cereus в больших количествах в материале от больного при отсутствии выделения других микроорганизмов. Однако необходимо учитывать, что В. cereus может вызывать патологический процесс совместно с другими инфекционными агентами, например, с протеем или эшерихиями.
Лечение Bacillus cereus у детей:
Острый гастроэнтерит, вызванный В. cereus, лечится назначением соответствующей диеты и оральной регидратации. Под регидратацией понимают восполнение обычного водного баланса в организме.
Тяжелые процессы (менингит, бронхопневмония, септицемия, остеомиелит) требуют назначение антибиотиков. В. cereus благодаря выработке р-лактамазы, устойчивы к пенициллину и препаратам на его основе. Но их можно уничтожить цефалослоринами 3-го и 4-го поколений.
Антибиотики применяют в дозах, соответствующих возрасту. Срок лечения составляет от 5 до 10 суток. Отменяют прием антибиотиков после санации от возбудителя, прихода в нормы температуры тема и ликвидации симптомов.
Применяют для лечения также колибактерин. Это препарат с антибактериальным и противодиарейным действием, он восстанавливает кишечную микрофлору и иммунную систему, борется с патогенными и условно-патогенными нефизиологичными микроорганизмами.
Профилактика Bacillus cereus у детей:
Специфической профилактики данной инфекции на данный момент не разработано. Следует предупредить попадание В. cereus на предметы ухода за новорожденными и ослабленными детьми, а также на медицинские инструменты, особенно те, которые используются для инвазивных методов лечения и обследования детей и взрослых.
Профилактика острого гастроэнтерита заключается в соблюдении элементарных гигиенических правил и полноценной термической обработке пищевых продуктов.
К каким докторам следует обращаться если у Вас Bacillus cereus у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Bacillus cereus у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Пищевые токсикоинфекции
Пищевые токсикоинфекции - острые инфекционные заболевания, вызываемые условно-патогенными бактериями, продуцирующими экзотоксины. При попадании микроорганизмов в пищевые продукты в них накапливаются токсины, которые могут вызывать отравления человека.
Краткие исторические сведения
На протяжении многих веков человечеству было известно, что употребление в пищу недоброкачественных продуктов, прежде всего мясных, может приводить к развитию рвоты и поноса. После описания П.Н. Лащенковым (1901) клинической картины стафилококковой пищевой интоксикации было установлено, что заболевания с синдромами диареи и интоксикации могут вызывать условно-патогенные бактерии. В результате работ отечественных исследователей эти заболевания отнесены к группе пищевых токсикоинфекций.
Что провоцирует / Причины Пищевых токсикоинфекций :
Пишевая токсикоинфекция вызывает большая группа бактерий; основные возбудители - Staphylococcus aureus, Proteus vulgaris, Bacillus cereus, Clostridium perfringens, Clostridium difficile, представители родов Klebsiella, Enterobacter, Citrobacter, Serratia, Enterococcus и др. Возбудители широко распространены в природе, обладают выраженной устойчивостью и способны размножаться в объектах внешней среды. Все они являются постоянными представителями нормальной микрофлоры кишечника человека и животных. Нередко у заболевших не удаётся выделить возбудитель, так как клиническую картину пищевых токсикоинфекций в основном определяет действие микробных токсических субстанций. Под действием различных факторов внешней среды условно-патогенные микроорганизмы изменяют такие биологические свойства, как вирулентность и устойчивость к антибактериальным препаратам.
Эпидемиология
Источник инфекции - различные животные и люди. Наиболее часто это лица, страдающие гнойными заболеваниями (панарициями, ангинами, фурункулёзом и др.); среди животных - коровы и овцы, болеющие маститами. Все они выделяют возбудитель (обычно стафилококки), попадающие в пищевые продукты в процессе их обработки, где и происходит размножение и накопление бактерий. Эпидемиологическую опасность представляют как больные, так и носители возбудителей. Период заразности больных небольшой; относительно сроков бактерионосительства данные противоречивы.
Возбудители других токсикоинфекций (С. perfringens, В. cereus и др.) люди и животные выделяют во внешнюю среду с испражнениями. Резервуаром ряда возбудителей могут являться почва, вода и другие объекты внешней среды, загрязнённые испражнениями животных и человека.
Механизм передачи - фекально-оральный, основной путь передачи - пищевой. Для возникновения пищевых токсикоинфекций, вызываемых условно-патогенными бактериями, необходима массивная доза возбудителей либо определённое время для его размножения в пищевых продуктах. Чаще всего пищевые токсикоинфекции связаны с контаминацией молока, молочных продуктов, рыбных консервов в масле, мясных, рыбных и овощных блюд, а также кондитерских изделий, содержащих крем (торты, пирожные). Основным продуктом, участвующим в передаче клостридий, является мясо (говядина, свинина, куры и др.). Приготовление некоторых мясных блюд и изделий (медленное охлаждение, многократное подогревание и др.), условия их реализации способствуют прорастанию спор и размножению вегетативных форм. В эстафетной передаче возбудителя участвуют различные объекты внешней среды: вода, почва, растения, предметы быта и ухода за больными. Продукты, содержащие стафилококковый и другие энтеротоксины, по внешнему виду, запаху и вкусу не отличаются от доброкачественных. Заболевания протекают в виде спорадических случаев и вспышек. Их чаще регистрируют в тёплое время года, когда создаются благоприятные условия для размножения возбудителей и накопления их токсинов.
Естественная восприимчивость людей высокая. Обычно заболевает большая часть лиц, употреблявших контаминированную пищу. Помимо свойств возбудителя (достаточная доза, высокая вирулентность) для развития заболевания требуется ряд способствующих факторов как со стороны микроорганизма, так и макроорганизма (сниженная сопротивляемость, наличие сопутствующих заболеваний и др.). Более восприимчивы индивидуумы из группы риска: новорождённые, ослабленные лица, пациенты после хирургических вмешательств либо длительно получавшие антибиотики и др.
Основные эпидемиологические признаки. Заболевания, вызываемые условно-патогенными микроорганизмами, распространены повсеместно. Вспышки носят семейный характер или при контаминации пищи на предприятиях общественного питания, заболевания могут быть рассеяны среди населения. Число заболевших определяет количество лиц, употреблявших контаминированный пищевой продукт, и может существенно варьировать. В частности, весьма характерны групповые заболевания среди пассажиров морских судов, туристов и членов детских и взрослых организованных коллективов. Вспышки обычно носят взрывной характер. Каких-либо особенностей по социально-возрастному и половому составу не выявлено. Заболевания чаще регистрируют в летнее время. В зависимости от вида пищевого продукта среди заболевших преобладают дети или взрослые. Кроме пищевых возможны и бытовые вспышки, в большинстве случаев возникающие в больничных условиях. Вспышки внутрибольничных инфекций, вызываемых С. difficile, связаны с длительным применением антибиотиков. При водных вспышках как следствие фекального загрязнения одновременно с условно-патогенными микроорганизмами выделяют и другие возбудители острых кишечных инфекций.
Патогенез (что происходит?) во время Пищевых токсикоинфекций :
Общее свойство для всех возбудителей пищевых токсикоинфекций - способность вырабатывать различные типы экзотоксинов (энтеротоксинов) и эндотоксинов (липополисахаридных комплексов). Именно благодаря особенностям действия этих токсинов отмечают определённое своеобразие в клинических проявлениях пищевых токсикоинфекций, обусловленных различными возбудителями. На исключительно важную роль бактериальных токсинов в развитии пищевых токсикоинфекций указывает и относительно короткий инкубационный период заболевания.
В зависимости от типов токсинов они могут вызывать гиперсекрецию жидкости в просвет кишечника, клинические проявления гастроэнтерита и системные проявления заболевания в виде синдрома интоксикации.
Токсины бактерий реализуют своё действие через выработку эндогенных медиаторов (цАМФ, ПГ, интерлейкинов, гистамина и др.), непосредственно регулирующих структурно-функциональные изменения органов и систем, выявляемые у больных с пищевой токсикоинфекцией.
Сходство патогенетических механизмов пищевых токсикоинфекций различной этиологии обусловливает общность основных принципов в подходах к лечебным мероприятиям при этих заболеваниях, а также при сальмонеллёзе и кампилобактериозе.
Симптомы Пищевых токсикоинфекций :
Инкубационный период. Составляет, как правило, несколько часов, однако в отдельных случаях он может укорачиваться до 30 мин или, наоборот, удлиняться до 24 ч и более.
Вместе с тем, клинические проявления пищевых токсикоинфекций имеют некоторые различия в зависимости от вида возбудителя. Стафилококковой инфекции свойственны короткий инкубационный период и бурное развитие симптомов заболевания. В клинической картине доминируют признаки гастрита: многократная рвота, резкие боли в эпигастральной области, напоминающие желудочные колики. Характер стула может не меняться. Температура тела в большинстве случаев остаётся нормальной или кратковременно повышается. Выраженное снижение артериального давления, цианоз и судороги можно наблюдать уже в первые часы заболевания, но в целом течение болезни кратковременное и благоприятное, поскольку изменения кардиогемодинамики не соответствуют степени водно-электролитных расстройств. В случаях пищевых токсикоинфекций, вызванных Clostridium perfringens, клиническая картина, сходная с таковой при стафилококковой инфекции, дополняется развитием диареи с характерным жидким кровянистым стулом, температура тела остаётся нормальной. При пищевых токсикоинфекциях, вызванных вульгарным протеем, стул приобретает зловонный характер.
Осложнения
Наблюдают крайне редко; наиболее часто - гиповолемический шок, острая сердечно-сосудистая недостаточность, сепсис и др.
Диагностика Пищевых токсикоинфекций :
Дифференциальная диагностика
Пищевые токсикоинфекции следует отличать от сальмонеллёза и других острых кишечных инфекций - вирусных гастроэнтеритов, шигеллёзов, кампилобактериоза, холеры и др., а также от хронических заболеваний ЖКТ, хирургической и гинекологической патологий, инфаркта миокарда. Поскольку основные патогенетические механизмы и клинические проявления пищевых токсикоинфекций мало отличимы от таковых при сальмонеллёзе, в клинической практике часто ставят обобщённый предварительный диагноз пищевых токсикоинфекций, а выделение сальмонеллёза из этой общей группы проводят в случае его бактериологического или серологического подтверждения.
Лабораторная диагностика
Основу составляет выделение возбудителя из рвотных масс, промывных вод желудка и испражнений. При высеве возбудителя необходимо изучение его токсигенных свойств. Однако в большинстве случаев выделяемость незначительна, а обнаружение конкретного микроорганизма у больного ещё не позволяет считать его виновником заболевания. При этом необходимо доказать его этиологическую роль либо с помощью серологических реакций с аутоштаммом, либо установлением идентичности возбудителей, выделенных из заражённого продукта и от лиц, употреблявших его.
Лечение Пищевых токсикоинфекций :
Лечение пищевых токикоинфекций аналогично таковому при сальмонеллёзе; показаны промывание желудка, сифонные клизмы, раннее назначение энтеросорбентов (активированный уголь и др.), витаминов. При необходимости проводят регидратационную терапию. Этиотропное лечение при неосложнённом течении пищевых токсикоинфекций не показано.
Профилактика Пищевых токсикоинфекций :
Эпидемиологический надзор следует проводить в рамках надзора за кишечными инфекциями и внутрибольничными инфекциями.
В основе профилактики заболеваний лежит соблюдение санитарно-гигиенического и технологического режима, норм и правил заготовки, приготовления, хранения и реализации пищевых продуктов. Необходимо обеспечить ветеринарно-санитарный контроль над животными, способными контаминировать почву, воду и окружающие предметы возбудителями. Для предупреждения стафилококковых отравлений проводят мероприятия, направленные на уменьшение носительства стафилококков у работников пищевых предприятий (санация носителей стафилококка в носоглотке и на кожных покровах, лечение хронических воспалительных заболеваний миндалин и верхних дыхательных путей). Необходимо отстранение от работы, непосредственно связанной с обработкой пищевых продуктов и их изготовлением, лиц с гнойничковыми заболеваниями кожи, фарингитами, ангинами и другими проявлениями стафилококковой инфекции. Большое значение имеют контроль за соблюдением санитарно-гигиенического режима на пищевых предприятиях и лечебно-профилактических учреждениях, соблюдение правил личной гигиены, постоянное проведение санитарно-просветительной работы. Важно правильно хранить пищевые продукты, исключить размножение в них возбудителей пищевых токсикоинфекций. Чрезвычайно важны термическая обработка пищевых продуктов, кипячение молока и соблюдение сроков их реализации.
Мероприятия в эпидемическом очаге
Аналогичны таковым при других острых кишечных инфекциях. Диспансерное наблюдение за переболевшими не регламентировано.
К каким докторам следует обращаться если у Вас Пищевые токсикоинфекции :
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Пищевых токсикоинфекций , ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Пищевое отравление Bacillus cereus и его лечение
Пищевое отравление Escherichia coli и его лечение
Патогенные штаммы Escherichia coli делятся на следующие категории:
1. Энтеротоксигенные Escherichia coli (ЕТЕС), вызывающие холе-роподобную диарею путешественников.
2. Энтеропатогенные для младенцев Escherichia coli (EDEC).
3. Энтероинвазивные штаммы (EITC), приводящие к дизентериеподобной клинической картине.
4. Энтерогеморрагические штаммы, вызывающие геморрагический колит и гемолитико-уремический синдром.
5. Энтероадгезивные Escherichia coli (ЕАЕС) — слабо охарактеризованная категория, связанная с диареей путешественников. Серогруппы еще не определены. Бактерии прилипают плотными группами к поверхности Нер-2-клеток. Дальнейшие исследования позволят установить, правомерно ли считать именно эти E.coli возбудителями диареи.
6. Диффузно адгезивные E.coli (DAEC) связываются со всей поверхностью клеток HeLa и НЕР-2 поодиночке. По поводу их патогенности и эпидемиологического значения существуют противоречивые мнения.
7. Энтероагрегационные E.coli (EAggEC) — скопления бактерий, прикрепленные к поверхности культуры эпителиальных клеток, выглядят "штабелями кирпичей".
8. Эти штаммы обнаруживались при острой и хронической диарее. Дизентериеподобный синдром напоминает инфекции, обусловленные Campylobacter, Yersinia и Shigella; холерный тип имитирует понос, вызываемый Vibrio и Bacillus се reus.
а) Источники. Вспышка пищевого отравления в январе 1993 г. привела к госпитализации многих детей, которым требовался диализ по поводу гемолитико-уремического синдрома. Трое младенцев умерли. Выяснилось, что патогенные бактерии находились в замороженных пирожках с говядиной, изготовленных одной из фирм по производству гамбургеров в штате Вашингтон. E.coli 0157:Н7 продуцирует 2 шигаподобных токсина, сходных с шигатоксином, образуемым Shigella dysenteriae.
Эти бактерии были обнаружены также в курятине, свинине, молочных и других пищевых продуктах. Другая широкомасштабная вспышка инфекции E.coli 0157-Н7 в штате Миссури в 1989 и 1990 гг.(243 заболевших) сопровождалась кровавым поносом или диареей с болью в животе. Четверо умерли, а у троих развился гемолитико-уремический синдром.
б) Симптоматика. После инфицирования кишечника E.coli 0157:Н7 может развиться гемолитико-уремический синдром, характеризующийся микроангиопатической гемолитической анемией, тромбоцитопенией и почечной дисфункцией. Диарейная фаза заболевания обычно предшествует гемолизу. Одной из причин постдиарейного гемолитико-уремического синдрома и тромбоцитопенической пурпуры является шигеллоподобный токсин, продуцируемый E.coli (например, E.coli:0111).
в) Диагностика. Микробиологические посевы кала позволяют выявить E.coli, однако, чтобы отличить инвазивные штаммы от токсигенных, необходимо дорогостоящее и в повседневной практике нерентабельное тестирование на животных. Одной из эффективных скрининговых процедур при геморрагическом колите или гемолитико-уремическом синдроме служит реакция сбраживания сорбита: E.coli 0157:Н7 в отличие от других E.coli сорбитотрицательным штаммом.
г) Профилактика. Туристы могут предупредить заражение, используя для питья только разлитые в бутылки напитки или очищенную воду. Самый надежный способ ее очистки — кипячение в течение нескольких минут. Альтернативный способ — 5 капель настойки йода на 1 л прозрачной воды за 30 мин до питья. Если вода холодная или мутная, надо добавить 10 капель на 1 л, а подождать после этого лучше несколько часов.
Некоторую защиту обеспечивают портативные фильтры для воды, однако достаточной бактериологической проверки они не проходили и Центры по борьбе с болезнями специальных рекомендаций по их использованию не распространяют. Туристы не должны глотать лед, пить непастеризованное молоко, есть неподвергнутую термообработке пищу и фрукты, которые нельзя очистить.
д) Лечение пищевого отравления Escherichia coli. Профилактическую антибиотикотерапию против диареи путешественников проводят только лицам с другими болезнями. Эффективны в этом плане триметоприм/сульфаметоксазол (160/800 мг/сут) или доксициклин (200 мг 2 раза в сутки).
Пепто-Бисмол в дозе 60 мг 4 раза в день снижает заболеваемость диареей путешественников на 60 %. Некоторые туристы принимают таблетки Пепто-Бисмола, содержащие, кроме 300 мг субсалицилата висмута, 350 мг карбоната кальция. Рекомендуемая доза 14 таблеток в день эквивалентна 4,9 г последнего вещества в сутки.
В определенных условиях (обезвоживание, почечная недостаточность, применение препаратов витамина D или тиазидных диуретиков, бессимптомный первичный гиперпаратиреоз) это чревато гиперкальциемией. Названные таблетки содержат также по 130 мг всасываемого салицилата каждая — следовательно, 14 штук эквивалентно 28 его гранам (5,6 обычных взрослых таблеток салицилата). Предупредить диарею путешественников, по-видимому, могут и более низкие дозы субсалицилата висмута (4 — 8 таблеток в сутки).
Серовары кишечной палочки - Escherichia coli
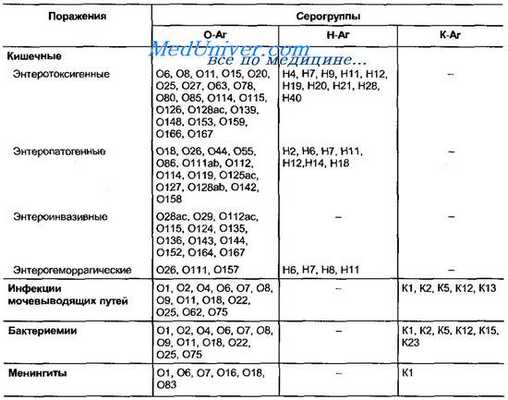
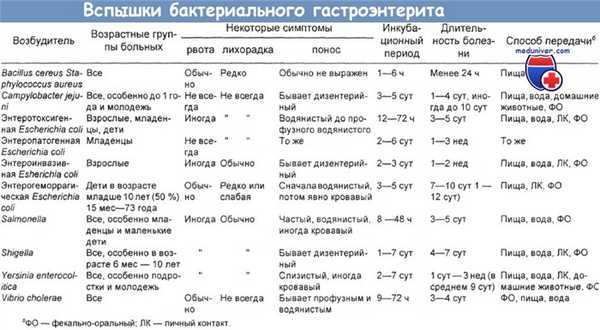
Токсикоинфекции пищевые
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Токсикоинфекции: причины появления, симптомы, диагностика и способы лечения.
Определение
Пищевые токсикоинфекции (ПТИ) – это острые кишечные инфекционные заболевания, возникающие после употребления в пищу продуктов, инфицированных различными условно-патогенными бактериями. Однако недостаточно просто съесть некачественный продукт, непременным условием развития клинической картины ПТИ является поступление в организм большого количество возбудителя и его токсинов.
Всемирная организация здравоохранения приводит данные о том, что ежегодно в результате употребления продуктов, содержащих условно-патогенную микрофлору, в мире заболевают порядка 600 млн человек. В группе наибольшего риска – дети младше пяти лет (около 40% всех пищевых отравлений).
Причины появления токсикоинфекций
Возбудители токсикоинфекций распространены в природе – их можно обнаружить в почве, воде, воздухе, на различных предметах. Кроме того, в незначительных количествах они являются постоянными представителями нормальной микрофлоры кишечника человека и животных. Заболевание манифестирует, если их количество значимо увеличивается.
Источником инфекции могут быть заболевшие люди, бактерионосители, сельскохозяйственные животные, птицы и даже рыба. Кроме того, продукты могут оказаться обсемененными микроорганизмами, если в их приготовлении участвовали люди с инфекционными болезнями кожи.
Механизм передачи – фекально-оральный, путь передачи – пищевой. Заболевает до 100% людей, употреблявших инфицированные продукты (молочные продукты, рыбные консервы в масле, мясные, рыбные блюда, кондитерские изделия с кремом и т.д.).
Для возникновения заболевания, которое вызывают условно-патогенные бактерии, необходима или массивная доза возбудителей, или определенное время для его размножения в пищевых продуктах, то есть возбудитель должен размножиться в пищевой массе до достаточного уровня, способного вызвать заболевание.

Поэтому в профилактике заболевания имеют значение условия хранения и сроки реализации пищевых продуктов. При размножении в пище микроорганизмы могут не изменять цвет, вкус и запах продукта.
Таким образом, возникновение токсикоинфекции возможно при наличии следующих условий:
- бактериальное загрязнение пищевого продукта;
- нарушение технологии приготовления (например, недостаточная термическая обработка);
- нарушение условий хранения продукта и несоблюдение сроков его реализации;
- биологическое соответствие состава пищевой массы видовым возможностям размножения возбудителя;
- присутствие возбудителя в пищевом продукте в значимых количествах.
- Staphylococcus aureus. Заболевание связано с употреблением в пищу салатов с майонезом, кремовых тортов и др., обсемененных золотистым стафилококком, который способен вырабатывать токсин, поражающий кишечник.
- Bacillus cereus. Заболевание обычно связано с употреблением блюд из риса, фарша, а также изделий, содержащих крахмал.
Классификация заболевания
По клиническим формам:
- гастритическая,
- энтеритическая,
- гастроэнтеритическая,
- гастроэнтероколитическая.
- легкая,
- средней тяжести,
- тяжелая.
Инкубационный период заболевания, то есть отрезок времени от момента попадания возбудителя в организм до появления симптомов, может составлять от несколько часов до суток. Клиническими проявлениями могут быть гастроэнтероколит, интоксикация и, как следствие, водно-электролитные расстройства.
Начало заболевания острое, характеризуется появлением тошноты, многократной рвоты, жидкого стула до 10-15 раз в сутки. Боль в животе может быть как незначительной, так и сильной, схваткообразной. Температура тела – 37-39°С. Больные жалуются на общую слабость, недомогание, ломоту в суставах и костях, головную боль, учащенное сердцебиение, снижение артериального давления, озноб.
Тяжесть состояния зависит от объема жидкости, теряемой больными при рвоте или диареи, то есть от степени обезвоживания организма. Продолжительность заболевания в большинстве случаев составляет 1-З дня.
Примерно 5% больных с токсикоинфекцией имеют клинику гастрита (боль в эпигастральной области, тошнота, рвота). У 95% развивается энтерит (боль в области пупка, частый и обильный жидкий стул). О возникновении колита свидетельствуют схваткообразные боли внизу живота, а также стул с примесью слизи и крови. При гастроэнтероколитическом варианте течения болезни в процесс последовательно вовлекаются желудок, тонкий и толстый кишечник.
Вид возбудителя токсикоинфекции также может влиять на симптоматику заболевания. Стафилококковая инфекция протекает с коротким инкубационным периодом, многократной рвотой, резкой болью в эпигастральной области, напоминающей желудочные колики. А вот характер стула может не меняться, и температура тела в большинстве случаев остается в пределах нормы или кратковременно повышается до субфебрильных значений. Течение болезни непродолжительное и благоприятное.
Для ПТИ, вызванной клостридиями, характерно тяжелое течение, которое может иметь три клинических варианта: острейший гастроэнтероколит с преобладанием интоксикационного синдрома и развитием анаэробного сепсиса; холероподобный с развитием обезвоживания II-III степени; развитие некротических процессов в тонкой кишке и перитонита.
При ПТИ, вызванной вульгарным протеем, в большинстве случаев наблюдается легкое течение, стул приобретает зловонный характер. Токсикоинфекции, вызываемые бактериями Aeromonas, проявляются в виде острого гастроэнтерита, как правило, у маленьких детей и людей с иммунодефицитами. Клинически аэромонадный гастроэнтерит может протекать в виде холероподобного заболевания или дизентерийного гастроэнтерита.
Самым опасным последствием заболевания является обезвоживание, которое возникает в результате значительной потери жидкости при поносе и/или рвоте.

Диагностика пищевой токсикоинфекции
Диагностика токсикоинфекции включает выделение возбудителя из рвотных масс, промывных вод и испражнений и изучение его токсигенных свойств для назначения корректной терапии.
- Раздельное определение токсина А и токсина В Clostridium difficile в кале, антигенный тест.
Читайте также:
- Нарушения гомеостаза при алкоголизме. Инфузионная терапия при алкоголизме
- Неотложная помощь при предсердной пароксизмальной тахикардии.
- Желудочковая тахикардия при ишемической болезни сердца (ИБС)
- Влияние фенотипа на активность генов. Аллельные детерминанты антител
- Оксигемометрические методы. Кюветный оксигемометр
