Побочные реакции на введение антибиотиков. Токсико-аллергические реакции на антибиотики
Добавил пользователь Алексей Ф. Обновлено: 29.01.2026
С.С ПОСТНИКОВ, д.м.н, профессор кафедры клинической фармакологии РГМУ, Москва К сожалению, безвредных лекарств нет и, более того, по-видимому, и быть не может. Поэтому мы продолжаем рассказывать о побочных эффектах одной из самой назначаемой группы препаратов - антибактериальных средств.
АМИНОГЛИКОЗИДЫ (АМГ)
К аминогликозидам относят соединения, в состав которых входят 2 или более аминосахаров, соединенных гликозидной связью с ядром молекулы - аминоциклитолом.
Большинство первых АМГ - природные АБ (грибки рода Streptomices и Micromonospore). Новейшие АМГ - амикацин (производное канамицина А) и нетилмицин (полусинтетическое производное гентамицина) получены путем химической модификации природных молекул.
АМГ играют важную роль в лечении инфекций, вызванных грамотрицательными организмами. Все АМГ как старые (стрептомицин, неомицин, мономицин, канамицин), так и новые (гентамицин, тобрамицин, сизомицин, амикацин, нетилмицин) обладают широким спектром действия, бактерицидностью, близкими фармакокинетическими свойствами, сходными особенностями побочных и токсических реакций (ото- и нефротоксичность) и синергидным взаимодействием с β-лактамами (Союзфармация, 1991).
При введении через рот АМГ всасываются плохо и поэтому для лечения инфекций вне кишечной трубки не используются.
Однако АМГ могут в значительной мере абсорбироваться (особенно у новорожденных) при местном применении с поверхности тела после ирригации или аппликации и оказывать нефро- и нейротоксическое действие (системный эффект).
АМГ проникают через плаценту, накапливаются у плода (около 50% материнской концентрации) с возможным развитием тотальной глухоты.
НЕФРОТОКСИЧНОСТЬ АМГ
АМГ почти не подвергаются биотрансформации и выводятся из организма в основном путем клубочковой фильтрации. Указывается также на их реабсорбцию проксимальными канальцами. Из-за преимущественно ренального пути элиминации все представители этой группы АБ потенциально нефротоксичны (вплоть до развития тубулярного некроза с ОПН), только в разной степени. По этому признаку АМГ могут быть расположены в следующем порядке: неомицин > гентамицина > тобрамицина > амикацина > нетилмицина (Е.М.Лукьянова, 2002).
Нефротоксичность АМГ (2-10%) чаще развивается в полярных возрастных группах (дети раннего возраста и пожилые люди) - возрастзависимый токсический эффект. Вероятность нефротоксичности также возрастает с увеличением суточной дозы, длительности лечения (более 10 дней), а также кратности введения, и зависит от предшествующей почечной дисфункции.
Наиболее информативными показателями поражения проксимальных канальцев (мишень для токсического воздействия АМГ) являются появление в моче микроглобулинов (β2-микроглобулина и α1-микроглобулина), которые в норме почти полностью реабсорбируются и катаболизируются проксимальными канальцами и энзимурия (повышение уровня N-ацетил-β-глюкозаминидазы), а также белков с молекулярной массой больше 33 КД, которые фильтруются клубочками. Как правило, эти маркеры обнаруживаются после 5-7 дней лечения, умеренно выражены и обратимы.
Нарушение азотовыделительной функции почек как проявление почечной недостаточности (повышение уровня мочевины и креатинина сыворотки более, чем на 20%) выявляется лишь при существенном поражении почек вследствие длительного применения АМГ в высоких дозах, потенциировании их нефротоксичности петлевыми диуретиками и/или амфотерицином В.
ГЕНТАМИЦИН: почками кумулируется около 40% АБ, распределяемого в тканях больного (в коре почек более 80% "почечного" АБ). В корковом слое почек концентрация гентамицина превышает наблюдаемой в сыворотке крови более чем в 100 раз. Следует подчеркнуть, что для гентамицина характерна более высокая степень канальцевой реабсорбции и большее накопление в корковом слое почек, чем у других АМГ. Гентамицин накапливается также (хотя и в меньших количествах) в мозговом слое и сосочках почек.
Гентамицин, поглощаясь проксимальными канальцами почек, накапливается в лизосомах клеток. Находясь в клетках, он ингибирует лизосомальную фосфолипазу и сфингомиелиназу, что вызывает лизосомальный фосфолипидоз, аккумуляцию миелодных частиц и клеточный некроз. При электронно-микроскопическом исследовании в эксперименте и биопсии почек у человека выявлено набухание проксимальных канальцев, исчезновение ворсинок щеточной каймы, изменения внутриклеточных органелл при введении гентамицина в средних терапевтических дозах. Лечение высокими (>7 мг/кг в день) дозами гентамицина может сопровождаться острым тубулярным некрозом с развитием ОПН и необходимостью гемодиализа в отдельных случаях, продолжительностью олигурической фазы около 10 дней, при этом, как правило, наблюдается полное восстановление функции почек после отмены препарата.
К факторам, повышающим возможность проявления нефротоксичности гентамицина, относятся: предшествующая несостоятельность почек, гиповолемия, одновременное использование других нефротоксических ЛС (гидрокортизона, индометацина, фуросемида и этакриновой кислоты, цефалоридина, циклоспорина, амфотерицина В), рентгеноконтрастных веществ; возраст больного.
Частота возникновения нефротоксических реакций при лечении гентамицином варьирует от 10-12 до 25% и даже 40% в зависимости от дозы и продолжительности лечения. Эти реакции чаще наблюдаются при максимальной концентрации АБ в крови 12-15 мкг/мл. Однако подчеркивается целесообразность определения минимальных (остаточных) концентраций, поскольку увеличение именно этих значений выше 1-2 мкг/мл перед каждым следующим введением является свидетельством кумуляции препарата и, следовательно, возможной нефротоксичности. Отсюда и необходимость лекарственного мониторинга для АМГ.
ОТОТОКСИЧНОСТЬ АМГ
При применении стрептомицина, гентамицина, тобрамицина чаще возникают вестибулярные расстройства, а канамицин и его производное амикацин преимущественно влияют на слух. Однако это избирательность сугубо относительна и у всех АМГ отмечается "широкий" спектр ототоксичности. Так, гентамицин проникает и длительно сохраняется в жидкости внутреннего уха, в клетках слухового и вестибулярного аппарата. Его концентрация в эндо- и перилимфе значительно выше, чем в других органах и приближается к концентрации крови, а на уровне 1 мкг/мл сохраняется там в течение 15 дней после прекращения лечения, вызывая дегенеративные изменения во внешних клетках мерцательного эпителия основной извилины улитки (Ю.Б.Белоусов, С.М.Шатунов, 2001). В клинической картине этим изменениям соответствует нарушение слуха в пределах высоких тонов, а по мере продвижения дегенерации к верхушке улитки - также средних и низких тонов. К ранним обратимым проявлением вестибулярных расстройств (через 3-5 дней от начала применения препарата) относится: головокружение, шум в ушах, нистагм, нарушение координации. При длительном применении АМГ (более 2-3-х недель) происходит замедление их выведения из организма с повышением концентрации во внутренним ухе, в результате чего могут развиться тяжелые инвалидизирующие изменения органов слуха и равновесия. Однако в случае с гентамицином не выявлено достаточной корреляции между его концентрацией во внутреннем ухе и степенью ототоксичности, и, в отличие от канамицина, мономицина и неомицина, глухота при лечении гентамицином практически не развивается. Вместе с этим существуют выраженные вариации среди АМГ в частоте возникновения этих нарушений. Так, в одном из исследований на 10000 больных было выявлено, что амикацин вызывает нарушение слуха в 13,9% случаев, гентамицин - у 8,3% больных, тобрамицин - у 6,3%, а неомицин - у 2,4%. Частота вестибулярных нарушений составляет соответственно 2,8; 3,2; 3,5 и 1,4%.
Ототоксические реакции при лечении гентамицином развиваются значительно реже у взрослых, чем у детей. Теоретически новорожденные являются группой повышенного риска по развитию ототоксических реакций в связи с незрелостью механизмов элиминации, меньшей скоростью клубочковой фильтрации. Однако, несмотря на широкое применение гентамицина у беременных и новорожденных, неонатальная ототоксичность наблюдается исключительно редко.
Слуховые и вестибулярные токсические эффекты тобрамицина также связываются с его передозировкой, длительностью лечения (>10 дней) и особенностями больных - нарушенная почечная функция, обезвоживание, получение других лекарств, также обладающих ототоксичностью или сдерживающих элиминацию АМГ.
У части больных ототоксичность может клинически не проявлять себя, в других случаях больные испытывают головокружение, шум в ушах, потерю остроты восприятия высоких тонов по мере прогрессирования ототоксичности. Признаки ототоксичности обычно начинают появляться спустя длительное время после отмены препарата - отсроченный эффект. Однако известен случай (В.С. Моисеев, 1995), когда ототоксичность развилась после однократного введения тобрамицина.
АМИКАЦИН. Наличие в 1-м положении молекулы амикацина - 4-амино-2-гидроксибутирил-масляной кислоты обеспечивает не только защиту АБ от разрушающего действия большинства ферментов, продуцируемых устойчивыми штаммами бактерий, но и является причиной меньшей ототоксичности по сравнению с другими АМГ (кроме метилмицина): слуховые - 5%, вестибулярные - 0,65% на 1500 лечившихся этим АБ. Однако в другой серии исследований (10000 больных) контролировавшихся аудиометрией, была показана близкая к гентамицину частота слуховых расстройств, хотя в эксперименте было установлено, что амикацин подобно другим АМГ проникает во внутреннее ухо и вызывает дегенеративные изменения волосяных клеток, однако, как и в случае с гентамицином, не было установлено зависимости между уровнем концентрации амикацина во внутреннем ухе и степенью ототоксичности. Показано также, что волосковые клетки слуховой и вестибулярной системы выживали и при том, что гентамицин обнаружился внутри клеток и через 11 месяцев после прекращения лечения. Это доказывает, что не существует простой корреляции между присутствием АМГ и повреждением органов слуха и равновесия. Именно поэтому было высказано предположение о наличии у отдельных больных генетической предрасположенности к повреждающему воздействию АМГ (М.Г. Абакаров, 2003). Подтверждением этому положению было открытие в 1993 году у 15 больных с тугоухостью из 3-х китайских семей (после лечения АМГ) генетической мутации A1555G позиции 12S РНК, кодирующей митохондриальные ферменты, которая не была обнаружена у 278 пациентов без тугоухости, также получавших АМГ. Это позволило сделать вывод о том, что применение АМГ является пусковым механизмом для фенотипического выявления этой мутации.
В последние годы приобретает все большую популярность новый режим дозирования АМГ - однократное введение всей суточной дозы гентамицина (7 мг/кг) или тобрамицина (1 мг/кг) в виде 30-60-минутной инфузии. При этом исходит из того, что АМГ обладают концентрационно-зависимым бактерицидным эффектом и поэтому отношение Cmax/ mic > 10 является адекватным предиктором клинико-бактериологического эффекта.
Эффективность нового способа введения АМГ была показана при инфекциях различной локализации - абдоминальных, респираторных, мочеполовых, кожных и мягкотканных, как острых по течению, так и хронических (муковисцидоз). Однако возникающие при таком режиме дозирования пиковые концентрации АМГ, нередко превышающие 20 мкг/мл, могут теоретически создавать угрозу нефро- и ототоксичности. Между тем исследования D. Nicolau, 1995; K. Kruger, 2001; T. Schroeter et al, 2001 показывают, что однократное введение АМГ не только не уступают, но даже превосходят по безопасности обычное 3-х разовое применение АМГ, возможно, за счет более длительного отмывочного периода.
ТЕТРАЦИКЛИНЫ
Тетрациклины - остеотропны и поэтому накапливаются в костной ткани, особенно молодой, пролиферирующей. В эксперименте у собак отмечено отложение тетрациклина и в постоянных зубах.
Вследствие своей липофильности тетрациклины проникают через плацентарный барьер и откладываются в костях плода (в виде лишенных биологической активности хелатных комплексов с кальцием), что может сопровождаться замедлением их роста.
Применение тетрациклиновых АБ у детей дошкольного возраста приводит в ряде случаев к отложению препаратов в зубной эмали и дентине, что вызывает гипоминерализацию зубов, их потемнение (дисколорацию), гипоплазию зубной эмали, увеличение частоты кариеса, выпадение зубов. Встречаемость этих осложнений при применении тетрациклинов составляет примерно 20%.
При неосторожном или ошибочном применении тетрациклинов в большой дозе (более 2 г в день) может развиться тубулотоксичность (тубулярный некроз) с клиникой ОПН и необходимостью, в отдельных случаях, гемодиализа.
Поэтому использование тетрациклинов у беременных, кормящих грудью (тетрациклин проникает в грудное молоко) и детей до 8 лет не рекомендуется.
Подводя итоги вышеизложенному, хочется еще раз подчеркнуть, что любое лекарство (а значит, и антибиотики) - это обоюдоострое оружие, что, кстати, было подмечено и отражено в древнерусском определении, где слово "зелье" употреблялось в двойном значении - и как лечебное, и как ядовитое средство. Поэтому, начиная фармакотерапию, нельзя в дальнейшем оставлять больного один на один с лекарством, говоря ему (как это еще нередко бывает в той же поликлинике) "попейте его (лекарство) с недельку-другую и потом приходите". Для некоторых больных это "потом" может и не наступить. Делая упор в своем врачебном сознании на терапевтический эффект, мы (может быть сами того не желая) умаляем значение другого важнейшего правила лечения - его безопасности. Такая потеря бдительности делает нас неготовыми к нужным действиям при возникновении неблагоприятных реакций, что может иногда привести к непоправимым последствиям.
Побочные реакции на введение антибиотиков. Токсико-аллергические реакции на антибиотики
Частота и характер осложнений зависит от свойств антибактериальных препаратов, от способа их введения, длительности применения, от индивидуальной чувствительности больных, от их исходного состояния и возраста. Осложнения при антибиотикотерапии чаще всего наблюдаются у больных пожилого и раннего возраста, у ослабленных длительным и тяжелым заболеванием. Повышенная чувствительность отмечается также у лиц после частого и повторного пользования антибиотиками, проявляясь особенно у тех, кто склонен к аллергиям и прежде лечился этими препаратами. Ранее применявшиеся антибиотики способствуют повышению чувствительности к ним.
Токсико-аллергические реакции чаще всего развиваются в начале второй недели лечения антибиотиками, но могут быть раньше и позже. Большое значение в сенсибилизации организма и развитии осложнений имеет, как уже сказано, повторное применение антибактериальных препаратов. Однако в литературе опубликованы случаи тяжелых осложнений, закончившихся даже смертельным исходом, наступивших после одноразового введения пенициллина.
Побочные действия отдельных антибиотиков в настоящее время хорошо изучены. Так, например, известно, что пенициллин, по сравнению с другими химиотерапевтическими средствами, отличается малой токсичностью, чаще всего он обусловливает аллергические реакции. Зато стрептомицин и особенно биомицин преимущественно вызывают токсические реакции (Г. Л. Александер, У. А. Аскаров и др.).
М. П. Николаев, суммируя имеющиеся в литературе сведения, приводит перечень осложнений, развивающихся на почве пенициллинотерапии. К ним относятся озноб с повышением или без повышения температуры, головная боль, общая разбитость, ощущение неприятного вкуса во рту, различные кожные поражения (эритемы, дерматиты), являющиеся наиболее распространенной реакцией, невриты, протекающие с двигательными и чувствительными расстройствами. Отмечаются и отдаленные реакции после применения пенициллина, которые сводятся к легкой лихорадке, умеренной тахикардии, к болям в суставах, сопровождающимся серозными выпотами в них. Очень редко после введения больших доз пенициллина наступает анафилактическая реакция, которая может закончиться неблагоприятным исходом.
Отмечены также гематурия, воспалительные явления со стороны почек и судороги. А. Л. Мясников считает, что большие дозы пенициллина при длительном применении действуют на сердечную мышцу. Иногда возникают явления сердечной декомпенсации как во время, так и после пенициллинотерапии. Имеются указания на то, что пенициллин вызывает уменьшение витаминного комплекса В. А. Л. Мясников, Л. X. Кечнер и Т. А. Танфй-лова рекомендуют совместное назначение больших доз пенициллина и витамина В1. При назначении витамина B1 биохимические процессы совершаются более благоприятно.
Отмечены также изменения со стороны крови после введения пенициллина (А. Е. Френкель). Эти изменения выразились в увеличении количества эозинофилов. Иногда наблюдается также тромбоцитопения и резкое уменьшение количества лейкоцитов.
Стрептомицин редко вызывает аллергические реакции; он относится к препаратам, обладающим слабо выраженными сенсибилизирующими свойствами. Аллергические реакции иногда наблюдаются после введения больших доз препарата. Побочные реакции стрептомицина сводятся к тому, что он оказывает нервно-токсическое действие, проявляющееся в поражении VIII пары нервов, ослаблении зрения, парестезиях и иногда судорогах. В результате поражения слухового нерва наступает тугоухость, глухота и нарушение координации движений. Нарушения слуха и функции вестибулярного аппарата наблюдались у больных туберкулезным менингитом после эндолюмбального введения больших количеств стрептомицина. При отогенном менингите это не наблюдалось.
Стрептомицин вызывает также нарушения со стороны крови в виде анемии, лейкопении и агранулоцитоза. Эти изменения, судя по литературным данным, наблюдаются очень редко.
Что касается побочных действий биомицина и тетрациклина, то они в основном вызывают токсические реакции и изменения слизистой полости рта, глотки и т. д.
При лечении антибиотиками следует помнить не только о возможности аллергических и токсических реакций кожи типа дерматита, крапивницы и других, но и возможности поражения слизистой оболочки полости рта, глотки и гортани. Эти токсико-аллергические реакции глотки и гортани имеют место при внутримышечном и особенно пероральном введении антибиотиков.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Аллергическая реакция на антибиотики
Наличие аллергической реакции на антибиотики становится довольно распространенным явлением, так как использование антибиотиков для лечения различных инфекций значительно возросло.
Антибиотики используются для профилактики, лечения и борьбы с инфекциями, вызываемыми различными бактериями.
Потребление антибиотиков практически для всех проблем со здоровьем стало нормальным способом борьбы с инфекциями и болезнями.
Слово «антибиотик» происходит от двух греческих слов: «анти» и «биос» означает «против» и «жизнь» соответственно.
Антибиотики полностью или частично получены из штаммов бактерий или плесени.
Когда бактерии проникают в организм, вызывая нарушения его функционирования, а иммунная система не в состоянии бороться с ним, назначаются мощные антибиотики, помогающие иммунной системе.
Они могут убивать бактерии или препятствовать их росту.
Следует иметь в виду, что антибиотики могут уменьшить инфекцию, вызванную бактериями, а не вирусами, вызывающими простуду и грипп.
При правильном использовании антибиотики могут спасти жизнь, но могут вызвать осложнения, если используются без разбора.
Тем не менее бывают случаи, когда организм производит нежелательные реакции на антибиотики, даже если их использовать осторожно.
Симптомы аллергии на антибиотики
Аллергические реакции на антибиотики в значительной степени зависят от типа и количества принимаемых антибиотиков.
В большинстве случаев симптомы аллергии на антибиотики начинаются в течение 24 часов.
Как долго длится аллергическая реакция — часто первый вопрос, который приходит на ум, когда у человека начинает развиваться аллергия.
Обычно это длится пару часов после немедленного лечения.
Следующие симптомы наблюдаются в случае аллергии на антибиотики.
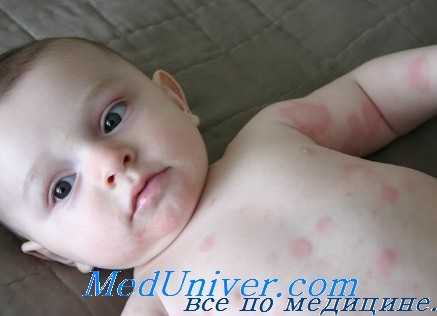
Это болезненные высыпания в простой форме либо в виде покраснения, отека и зуда.
Затруднение дыхания. Кашель и хрипы. Проблемы с глотанием пищи. Тошнота и рвота.
Анафилактический шок — очень серьезная аллергическая реакция, требующая немедленной медицинской помощи.
Это может привести к летальному исходу, если человек не стабилизируется и не получит соответствующую медицинскую помощь.
Аллергические реакции на антибиотики у детей также сходны с упомянутыми выше.
У них могут развиться приступы диареи и дискомфорта в животе.
Амоксициллин и ампициллин — два распространенных антибиотика, назначаемых маленьким детям. Они часто способны вызывать аллергические реакции.
Родители должны воздерживаться от назначения детям и младенцам антибиотиков без рецепта и немедленно сообщать врачу в случае возникновения аллергической реакции.
Также аллергию могут вызвать пенициллин, тетрациклин, хлорамфеникол, сульфонамиды (сульфаниламидные препараты), ванкомицин, нитрофурантоин, ципрофлоксацин и другие антибиотики.
У некоторых людей вероятность развития аллергии на антибиотики выше, чем у других людей. К ним относятся люди в возрастной группе 20-49 лет.
Лица с хроническими заболеваниями или члены семьи, страдающие аллергией на антибиотики, также подвержены таким аллергическим реакциям.
Диагностика аллергии на антибиотики
Диагностика аллергии на антибиотики проводится путем выполнения определенных тестов на чувствительном человеке.
Доктор спрашивает об истории болезни человека и любых предыдущих аллергических реакциях.
После осмотра он назначает одно из следующих испытаний.
Тест кожного пластыря: на кожу накладывают антибиотик и оставляют на 2 дня.
Позже его проверяют на наличие каких-либо аллергических реакций.
Тест на укол кожи: кожу предплечья осторожно укалывают иголкой и наносят небольшое количество антибиотика.
Препарат удаляется через некоторое время и отмечается любая наблюдаемая реакция.
Тест на антибиотик.
Пациенту вводят повышенные дозы антибиотика, чтобы проверить наличие признаков аллергии.
Интрадермальный тест: антибиотик в жидкой форме вводится внутрикожно (под поверхность кожи) для выявления аллергии на антибиотики.
Лечение аллергии на антибиотики
Первым шагом к лечению аллергии на антибиотики является прекращение приема антибиотиков и немедленная медицинская помощь.
Продолжительность и курс лечения зависит от тяжести симптомов аллергии.
Простые высыпания лечат антигистаминными препаратами или кортикостероидами в сочетании с успокаивающим смягчающим средством для контроля зуда и уменьшения воспаления и покраснения.
Для контроля кашля, хрипов и удушья врачи назначают ингаляторы.
Анафилактический шок обычно лечат инъекционным адреналином.
Аллергия на антибиотики
Антибиотики могут подходить не каждому человеку, что приводит к аллергическим реакциям различной степени тяжести.
Написал и проверил - автор статьи Черепенин Михаил Юрьевич
Изобретение антибиотиков в своё время позволило значительно сократить число смертельных исходов инфекционных заболеваний. Однако такой препарат может подходить не каждому человеку, что приводит к аллергическим реакциям различной степени тяжести. Если после приёма препаратов вы заметили нежелательные реакции, следует немедленно прекратить принимать его и обратиться к специалисту. В Бест Клиник приём ведут высшей квалификационной категории, которые проведут диагностику и назначат эффективную терапию.
Как распознать аллергию на антибиотики?
Аллергические реакции на антибиотики характеризуются следующей симптоматикой.
Анафилактический шок. Он проявляется отёком гортани, гипертермией (повышением температуры тела), острым зудом, нарушением работы сердца и острой гипотонией (резким понижением давления). Наступает анафилактический шок довольно быстро и требует экстренного оказания помощи больному, поскольку может привести к летальному исходу.
Сывороточноподобный синдром. Наступает не сразу: его признаки могут проявиться в течение 1–3 недель. Его проявления: гипертермия, боль в суставах, лимфатические узлыувеличены, а на коже появились высыпания.
Лекарственная лихорадка. Этот симптом, характеризующийся высокой температурой у больного, может держаться до 3 дней даже после прекращения приёма препарата. Отличием лекарственной лихорадки от обычной является отсутствие учащённого сердцебиения у пациента.
Синдром Лайела. Этот симптом встречается не так часто и сопровождается появлением у пациента пузырей с серозным содержимым, образующих после себя обширные раны. Другое название этого симптома — токсический эпидермальный некролиз.
Синдром . Проявляется в воспалении слизистых и кожи пациента, гипертермией.
Кроме перечисленных выше симптомов об аллергии на антибиотики могут свидетельствовать и местные кожные реакции.
- Фотосенсибилизация ( повышение чувствительности к ультрафиолетовому или видимому излучениям) — выражается в покраснении кожи, сопровождающемся зудом.
- Крапивница. На теле пациента появляются пятна красноватого оттенка. Участки поражения обширные и на них наблюдается сильный зуд.
- Сыпь. На отдельных участках кожи появляются прыщи (сыпь может поражать и весь кожный покров больного).
- Отёк Квинке. Покраснение и отёк обширного участка тела. При этом симптоме пациенту показана госпитализация: если отекает гортань, высок риск удушья.
На скорость развития аллергии влияют индивидуальная реакция организма на аллерген и способ приёма антибиотика: перорально, внутримышечно или внутривенно.
Существует ли возможность спрогнозировать возможную аллергическую реакцию?
Существенно увеличивают риск возникновения аллергии на антибиотики:
- наследственность;
- особенности конституции ( совокупность индивидуальных особенностей организма, сложившихся на основе наследственных и приобретённых свойств);
- длительный приём препаратов в большой дозировке (инъекционная форма);
- многократные повторные курсы одного и того же препарата;
- сопутствующие патологии (такие как ВИЧ, лимфолейкоз и пр.);
- аллергия на вещество или продукт другой группы аллергенов;
- ряд вирусных инфекций.
Диагностика
Чтобы диагностировать аллергию на антибиотики и назначить необходимое лечение, пациенту проводят следующие анализы:
- анализ крови. Если на препарат у пациента обнаружен иммуноглобулин Е, диагноз считают подтверждённым;
- кожные аллергологические пробы. При наличии кожных изменений непереносимость антибиотика доказана.
Проведение кожных аллергологических проб требует соблюдения некоторых условий. Например, их не применяют для пациентов, перенёсших синдром или Лайелла. Пробу проводят только с согласия пациента, которого информируют о возможных рисках. Если он согласен на проведение данного исследования, пробу должен проводить специалист, обладающий достаточным опытом и имеющий необходимую подготовку для оказания экстренной медицинской помощи в случае наступления у пациента анафилактического шока. Аллергологические пробы могут проводиться только в медицинских учреждениях, где имеется отделение реанимации и интенсивной терапии.
Результаты исследований позволяют установить предрасположенность к аллергической реакции и подобрать для пациента другие препараты.
В многопрофильном медицинском центре Бест Клиник вы можете пройти диагностику наличия аллергии для составления эффективного лечения.
Лечение
Лечение аллергии на антибиотики складывается по следующей схеме:
- отменяется принимаемый пациентом препарат;
- больному назначают терапию медикаментами, снижающими симптоматику аллергии;
- десенсибилизация (аллергенспецифическая иммунотерапия) — осуществляется посредством систематического введения препарата в минимальных дозировках (постепенно доводя их до терапевтической). Таким образом понижают чувствительность организма к аллергену.
Аллергия на антибиотики у детей
Симптомы аллергической реакции у детей, как правило, не так ярко выражены. В основном они заключаются в кожных реакциях. Врачи в таких случаях всегда стремятся подобрать щадящие препараты местного действия. Малышу в том числе показана диета с большим количеством овощей, фруктов, а также кисломолочных продуктов.
Зачастую аллергия на антибиотики сопровождается и другими формами аллергии. Поэтому при наличии у ребёнка аллергической реакции на продукты его родителям следует предельно внимательно относиться к тому, какие реакции вызывают у него те или иные лекарства.
Запишитесь на приём к Бест Клиник — для удобства наших пациентов мы работаем без выходных. Не забудьте рассказать врачу о прошлых реакциях на препараты — это существенно облегчит составление эффективного и безопасного лечения.
Антибиотики представляют собой самую многочисленную группу лекарственных средств. Так, в России в настоящее время используется 30 различных групп антибиотиков, а число препаратов (без учета неоригинальных) приближается к 200. Польза антибиотиков является неоспоримым фактом. Важно то, что они приносят пользу и даже могут спасти человеческую жизнь только в том случае, когда лекарственные препараты и другие виды лечения не помогают. Антибиотики способны препятствовать развитию практически всех видов микробов. Доля антибиотиков на рынке лекарственных препаратов в разных странах составляет от 6 до 21%, при этом имеется четкая тенденция к увеличению использования препаратов данной группы. Риск появления побочных явлений и осложнений определенно есть. В нашей статье мы поднимаем одну из актуальных проблем, такую как ошибки при использовании антибиотикотерапии.
5. Т.Ф. Одегова, О.Г. Олешко, Н.В. Новикова. Микробиология. Учебник для фармацевтических ВУЗов. – Л.: Типография ГОУ ВПО ПГФА 2009-377с.
6. Л. С. Страчунский, С.Н. Козлов. Антибиотики: клиническая фармакология. – Смол.: Амипресс 1994-208 с.
В настоящее время под термином антибиотики понимают продукты жизнедеятельности любых живых организмов, обладающих высокой биологической активностью по отношению к определенным группам микроорганизмов или клеткам злокачественных опухолей, избирательно задерживающих рост или полностью подавляя развитие.
Современная классификация антибиотиков разработана в Государственном центре по антибиотикам (С.М.Навашин, 1994), в соответствии с которой они характеризуются по механизму действия, химической структуре, противомикробному спектру, типу действия на клетку.
По химическому строению антибиотики делятся на:
1.Бета-лактамные антибиотики - включают большую группу препаратов, общим для которых является наличие бета-лактамного кольца. В зависимости от строения второй части бициклического кольца, бета-лактамные антибиотики разделяются на пеницилины, цефалоспорины, каропенемы, монобактамы.
а) Пенициллины. Родоначальником пеницилинов является бензилпенициллин-антибиотик природного происхождения, продукт жизнедеятельности грибов рода Pennicillum. Основой химической структурой пенициллинов является 6-аминопенициллиновая кислота. Классические пенициллины –это препараты с преимущественной активностью в отношении грамположительных бактерий .Модификацией молекулы путем присоединения к ней разных радикалов в положении 6 удалость получить полусинтетические антибиотики с более широким спектром действия и благоприятной фармакокинетикой. Недостатки: узкий спектр действия, большая частота аллергический реакцией, быстро выводятся из организма(кроме бициллина),быстро формируется устойчивость микробов за счет образования бета-лактамаз-ферментов, разрушающих бета-лактамное кольцо.[1]
В связи с широким распространением резистентных к антибактериальным препаратам микробов, вызванных продукцией ими бета-лактамаз, были созданы препараты, получившие название ингибиторы «бета-лактамаз». Они имеют свойство необратимо инактивировать широкий спектр бета-лактамаз, продуцируемых различными микроорганизмами. К ним относят клавулановую кислоту, сульбактам, тазобактам.[3]
К препаратам содержащим пенициллины и ингибиторы бета-лактамаз-защищенным пенициллинам-относят сочетания ампициллин/сульбактам, амоксициллин/клавуалановая кислота, тикарциллин/клавулановая кислота, пиперациллин/тазбактам. Эти препараты применяются для лечения инфекции различных локализаций (дыхательные пути, мочевыделительная система, кожа и мягкие ткани, брюшная полость, малый таз и др.),особенно при высоком риске наличия возбудителя, продуцирующих бета-лактамазы.
Наиболее частые осложнения при приеме пенициллинов это аллергические реакции. Иногда это кожные высыпания, дерматиты, лихорадка. Более тяжелые случаи характеризуются отеком слизистых оболочек, артриты, поражение почек. Наиболее тяжелым является анафилактический шок. Иногда анафилактический шок может закончится летально.
б) Цефалоспорины. Имеют в своей основе 7-аминоцефалоспориновую кислоту . Выделяют четыре поколения цефалоспоринов.
Цефалоспорины 1 поколения(цефазолин,цефалексин) активны преимущественно в отношении грамположительных кокков(стафилококков,стрептококков и др.)и некоторых грамотрицательных бактерий.
Цефалоспорины 2поколения(цефуроксим,цефаклор) обладают более широким спектром действия по сравнению с препаратами 1 поколения за счет наличия активности в отношении грамотрицательных бактерий.
Цефалоспорины 3 поколения(цефотаксим,цефтриаксон) имеют более высокую активность в отношении различных грамотрицательных бактерий (энтеробактерии, гемофилуса, гонококков, менингокков ) по сравнению с цефалоспоринами 2 поколения. кроме того, некоторые цефалоспорины 3 поколения (цефтазиди) активны в отношении синегнойной палочки.
Цефалоспорины 4 поколения (цефепим,цефпиром)-химической особенностью данных препаратов является их биполярна структура, что обеспечивает быстрое проникновение молекулы через наружную мембрану бактерий. Цефалоспорины 4 поколения характеризуются более широким спектром антимикробной активности по сравнению с цефалоспоринами 3 поколения. Они высокоактивны как в отношении большинства грамотрицательных бактерий, в том числе продуцирующих бета-лактамазы, включая синегнойную палочку, так и отношении грамположительных бактерий.
в)Карбапенемы (имипенем, меропенем) характеризуются наиболее широким спектром противомикробной активности среди всех бета-лактамных антибиотиков. Они в отношении грамположительных грамотрицательных аэробных бактерий ,анаэробов, более устойчивы к действию бета-лактамаз.
г)Монобактамы или моноциклические бета-лактамы, в клинической практике применяется один препарат-азтреонам, имеющий узкий спектр антибактериальной активности. Воздействует на аэробную грамотрицательную флору.
Бета-лактамные антибиотики применяются при инфекциях дыхательных путей, мочевыводящих путей, гнойных процессах различной локализации, внутрибольничных инфекциях.
2) Аминогликозиды. Среди этой группы выделяют препараты 3х поколений.
Аминогликозиды 1 поколения (стрептомицин, канамицин) в настоящие время применяются ограниченно, преимущественно во фтизиатрии.
Аминогликозиды 2 поколения (гентамицин, тобрамицин) и 3 поколения (амикацин) широко применяются в клинической практике.
Аминогликозиды обладают широким спектром противомикробной активности, но препараты слабо действуют на стрептакокки, не активны в отношении анаэробных бактерий. Эти антибиотики используются при лечении туберкулеза, инфекции дыхательных путей, септических состояний. Аминогликогзиды способны вызывать вестибулярные нарушения, нефротоксичность, нейромышечную блокаду и аллергические реакции [5]
3)Гликопептиды. К этой группе относятся природные антибиотики-ванкомицин и тейкопланин. Гликопептиды являются препаратами выбора при внутрибольничных инфекциях ,вызванных устойчивыми формами стафилококка ,энтерококка.
4) Липопептиды. Группа препаратов представлена, предложенным в последнее время антибиотиком даптомицином, который активен по отношению к грамположительным микробам, в том числе к устойчивым штаммам.
5)Макролиды. Это природные вещества или полусинтетические соединения, которые содержат 14,15 или 16-членное лактамное кольцо. Ранние макролиды активны, главным образом, по отношению к грамположительным и «атипичным» возбудителям ( хламидии, риккетсии, микоплазмы), обладают более высокой токсичностью (эритромицин ,рокситромицин). Новые макролидные антибиотики высокоактивны, реже вызывают побочные действия, более удобны в применении (кларитромицин, азатромицин). Эти антибиотики используются при лечении инфекций дыхательных путей, инфекций, передающихся половым путем.
6) Тетрациклины обладают широким спектром противомикробной активности. Наибольшее клиническое значение имеют тетрациклин и диксициклин, которые используются для лечения хламидиозов, риккетсиозов, некоторых зоонозов. Недостатки: гепатотоксичность, тератогенность, развитие резистентности бактерий, приобретенной в процессе их многолетнего использования. Антибиотики тетрациклинового ряда относительно малотоксичные препараты. Однако при длительном применение могу давай серьезные ослажнения. Накапливаясь в печени тетрациклины могу вызывать желтуху, гипопротромбинемию и нарушение свертываемости крови. Описаны тяжелые случаи некроза печени с летальным исходом . Способность тетрациклинов накапливаться в костях может привести к задержке роста костей в длину, нарушению развития зубов, окраска зубов в желто-коричневый вет и раннему кариесу у детй.
7) В группу линкозамидов входят природные антибиотики линкомицин и его полусинтетеческий аналог клиндамицин. Они активны по отношению г грамположительным бактериям, преимущественно к коккам. Используются в качестве препаратов резерва, когда неэффективны другие антибиотики.
8) Группа оксазолидинонов линезолид- первый представитель данного класса. Он проявляет высокую активность по отношению к грамположительным микроорганизмам( стафилококки, энерококки, превмококки). Также является препаратом резерва.
9) Группа полимиксинов характеризуется узким спектром активности и высокой токсичностью. Это соединения активны по отношению к грамотрицательным бактериям. Природной устойчивостью обладают грамотрицательные кокки и вся грамположительная флора. Препараты этой группы применяют при тяжелых инфекциях, вызванных синегнойной палочкой и резистентной грамотрицательной микрофлорой.
10) Группа левомицитина характеризуется широким спектром противомикробной активности, бактериостатическим действием. Недостатки: левомицитин угнетает кровообращение, у новорожденных вызывает «синдром серой асфиксии». В настоящее время имеет ограниченное применение, используется при бактериальном менингите, брюшном тифе. Левомицетин может нарушать зрение, слух, вызывать психические расстройства, а так же- вызывать аллергические реакции в виде сыпей на коже.
По спектру действия антибиотики делятся на:
1. Антибиотики узкого спектра действия (влияют преимущественно на грамположительные бактерии, например, пенициллин, эритромицин)
2. Антибиотки широкого спектра действия (угнетают рост грамположительных и грамотрицательных микроорганизмов, например, гентамицин, цефалоспорины 2-4 поколений)
3. Антибиотики со специфической активностью: противотуберкулезные, противогрипковые, антипротозойные, противоопухолевые)
Противомикробные препараты, или антимикотики, представляют собой обширный класс разнообразных химических соединений как природного происхождения, так и полученные синтетическим путем, которые обладают активностью в отношении патогенных грибов. В зависимости от их химической структуры они разделяются на несколько групп, отличающихся по спектру активности, фармакокинетике: полиены (нистатин, леворин, амфотерицин В), азолы (кетоконазол, флуконазол, итраконазол – для системного применения, клотримазол, миконазол – для местного применения), эхинокандины (каспофунгин), флюоропиримидины (флуцитозин), аллиламиды (тербинафин), препараты разных групп (гризеофульфин, аморолифин).
Говорить о принципах антибиотикотерапии –– это значит постулировать те вопросы, на которые должен обязательно ответить врач, когда выбирает лечебный препарат и его дозу.
Совершенно очевидно, что антимикробные препараты в разных клинических ситуациях не равноценны, одни полезны, а другие нет, одни опасны, другие безвредны, одни экономически целесообразны, другие недопустимо затратны. Вопросов много, но есть базовые, принципиальные, без ответа на которые антибиотикотерапии быть не может. Их многократно формулировали с разной степенью убедительности.[5]
Принципы рациональной антибиотикотерапии:
- Микробиологический: необходимо наличие показаний для использования антибиотиков; в терапии вирусных инфекций не целесообразно использовать антибиотики, обладающие способностью угнетать рост бактерий. Антибиотики необходимо назначать в соответствии с чувствительностью к ним конкретного возбудителя заболевания.
2. Фармакологический: назначение антибиотиков в соответствии с фармакокинетикой противомикробного средства. Препараты нужно назначать в такой дозе и вводить так часто, чтобы обеспечить его среднюю терапевтическую концентрацию в тканях и жидкостях макроорганизма на протяжении всего курса терапии. Путь введения определяется биодоступностью антибиотика, тяжестью заболевания, локализацией паталогического процесса. Применяется внутримышечное, внутривенное введение, per os, в виде ингаляций, местно (накожно, в виде глазных капель), per rectum, внутриполостное введение (в брюшную полость)
3. Клинический – выбор антибиотика, его дозы и способа введения производится с минимальным повреждающим действием препарата на макроорганизм. Следует определить переносимость антибиотика, учесть пол, возраст, сопутствующую патологию пациента.
4. Эпидемиологический: назначение антибактериального препарата с учетом устойчивости микроорганизма в среде, окружающей больного (в стационаре, географическом регионе).
5. Фармацевтический – назначение противомикробного средства с учетом соблюдений сроков годности и условий хранения.
6. Адекватное комбинирование. Необходимо правильно сочетать антибиотики разных групп с учетом их спектра и характера действия, побочных эффектов. Например, нельзя комбинировать пенициллины, оказывающих бактерицидное действие на клетку в фазе роста с тетрациклинами, задерживающих рост бактерий. Необходимо рационально сочетать антибиотики с другими лекарственными препаратами (пробиотиками, противогрибковыми средствами, витаминами).
7. Оценка эффективности действия антибиотиков: при проведении курса антибиотикотерапии оценивают динамику симптомов заболевания, динамику лабораторных и бактериологических показаний. Если в течении 2-3 дней отсутствует положительный эффект, следует отменить данный антибиотик и назначить другой.[5]
Сегодня в общественном сознании существует множество точек зрения, причем нередко взаимоисключающих друг друга, о том, что же такое антибиотики, когда и как их надо применять и насколько они опасны для человека. Предположение о том, что истина лежит где-то посередине между крайними точками зрения, вполне разумно, но нуждается в некоторой конкретизации. При длительном применении некоторые антибиотики могут оказывать токсическое действие на центральную нервную систему человека, подавлять его иммунитет, вызывать аллергические реакции. Однако по выраженности побочных явлений они не превосходят другие лекарственные средства.
Суммируя вышесказанное, необходимо подчеркнуть, что антибактериальные препараты являются важным, зачастую главным компонентом . Их рациональное и обоснованное применение в большинстве случаев определяет эффективность проводимого лечения.
Читайте также:
