Применение и токсикокинетика трициклических антидепрессантов (ТЦА)
Добавил пользователь Morpheus Обновлено: 09.01.2026
В настоящее время для лечения депрессии, особенно в амбулаторной практике, используются относительно новые антидепрессанты — селективные ингибиторы обратного захвата серотонина (СИОЗС), обладающие значительно меньшим количеством побочных эффектов, чем трициклические антидепрессанты, за счет избирательного влияния на обмен серотонина (избирательное торможение захвата
СИОЗС представлены такими препаратами как: флуоксетин (прозак), флувоксамин (феварин), сертралин (золофт, стимулотон, асентра), пароксетин (паксил, рексетин), ципрамил (циталопрам, ципралекс).
В отличие от ТЦА, особенностью действия серотонинергических антидепрессантов является их селективное влияние на серотонинергическую систему, первоначально выявленное в лабораторных исследованиях (Wong D.,с соавт., 1974; Fuller R., с соавт., 1977). Эффективность терапии депрессии СИОЗС, составляет не менее 65% (Mulrow D., с соавт., 2000)
Благодаря сродству этих препаратов и их активных метаболитов к серотониновым рецепторам происходит блокада обратного захвата серотонина на уровне пресинаптических окончаний, тем самым повышается концентрация медиатора в синаптической щели, что в свою очередь ведет к снижению синтеза и кругооборота серотонина (Stark Р., с соавт., 1985).
Избирательное, но неспецифическое для определенного подтипа рецепторов (Stahl S., 1993) действие СИОЗС не всегда повышает эффективность лечения, особенно если речь идет о терапии пациентов, страдающих тяжелой депрессией (Anderson I., Tomenson B., 1994; Burce M., Prescorn S., 1995).
Препараты группы СИОЗС имеют совершенно разную химическую структуру и отличаются друг от друга по фармакокинетическим параметрам, дозировкам и профилям побочных эффектов. Селективность подавления обратного захвата уменьшает количество побочных эффектов, улучшает переносимость и снижает частоту отказов от приема препаратов в сравнении с ТЦА (Anderson I., Tomenson T., 1994).
Таблица Сравнительная характеристика СИОЗС по интенсивность эффекта антидепрессанта
Препарат
Интенсивность эффекта
Пароксетин (рексетин, паксил)
Сертралин (стимулотон, золофт)
Ципрамил (ципралекс, циталопрам, целекса)
Флуоксетин (прозак, флуксал)
Примечание: +++— значительная интенсивность, ++— умеренная интенсивность , + — слабая выраженность эффекта.
Необходимо подчеркнуть относительную безопасность СИОЗС (меньшее число и выраженность побочных явлений) и большую комфортность лечения (возможность проведения терапии в амбулаторных условиях).
СИОЗС отличаются также низкой токсичностью (риск смертельного исхода при отравлении или передозировке практически равен нулю), а также возможностью использования препаратов этой группы у пациентов с противопоказаниям к применению ТЦА (нарушение сердечного ритма, затруднение мочеиспускания в связи с гипертрофией предстательной железы, закрытоугольная глаукома) (Машковский М.Д., 1997).
Следует отметить, что в литературе отмечены случаи центральных и переферических побочных эффектов в процессе лечения СИОЗС (Baldessarini R., 1989).
Эти препараты являются более дорогостоящими антидепрессантами, по сравнению с другими препаратами, использующимися для лечения депрессии.
Большинство из селективных ингибиторов обратного захвата серотонина (СИОЗС) являются пролонгами и используются в фиксированных дозах. Фармакокинетика различных представителей группы СИОЗС имеет свои особенности в зависимости от возраста пациентов и соматической отягощенности. Так период полураспада флувоксамина несколько увеличивается у пожилых пациентов и больных с патологией печени (Raghoebar M., Roseboom H., 1988). На продолжительность периода полураспада сертралина также оказывает влияние возраст (Warrington S.1988), а на эффекте флуоксетина достаточно существенно отражаются функциональные возможности печени (Bergstrom M., Lemberg L, с соавт., 1988).
Клинические испытания СИОЗС продемонстрировали, что они, как и ТЦА, являются эффективным средством при большинстве депрессивных состояний, включающих в себя тревогу, нарушения сна, психомоторную ажитацию и заторможенность. ( Levine S. с соавт., 1987, Dunlop S. с соавт., 1990, Claghorn J., 1992, Kiev A., 1992).
Таблица Сравнительная оценка дополнительного терапевтического эффекта СИОЗС
Терапевтический эффект
Анксиолитический, антифобический, вегетативно-стабилизирующий
Ципрамил (ципралекс, циталопрам)
Пароксетин (паксил, рексетин)
Показаниями к применению СИОЗС являются выраженные и средне тяжелые депрессии (типа простой) с нерезко выраженной тревогой и беспокойством (Pujynski S., с соавт., 1994;. Pujynski S, 1996). Кроме того СИОЗС могут использоваться для терапии личностных расстройств, включающих в себя реакции гнева и проявления импульсивности.
В медицинской литературе подчеркивается чувствительность витальных нарушений к действию этих антидепрессантов (Laakmann G. с соавт. 1988).
В ряде исследований описано, что пациенты, у которых в структуре синдрома преобладала тоска, демонстрировали хороший терапевтический ответ при применении СИОЗС (Reimherr F. et al., 1990, Tignol G. et al., 1992; Мосолов С.Н., Калинин В.В., 1994).
Учитывая, хорошую переносимость данных лекарственных средств их рекомендуют применять в пожилом возрасте.
В то же время большинство исследователей отмечают достаточно высокую анксиолитическую активность СИОЗС (Amin M. с соавт., 1989; Kiev А., 1992, , Бовин Р.Я., с соавт. 1995, Иванов М.В с соавт. 1995). На начальных этапах появления СИОЗС в отечественной литературе встречались указания на низкую эффективность, а иногда даже усиление тревоги при применении СИОЗС у больных с тревожной депрессией (Калинин В.В., Костюкова Е.Г., 1994, Лопухов И.Г. с соавт., 1994, Мосолов С.Н., с соавт., 1994).
В течение последних лет были проведены исследования, в которых представлены сравнительные оценки СИОЗС с ТЦА. Большинство авторов отмечает, что активность новых соединений сравнима с традиционными препаратами (Guelri J.. с соавт., 1983; Shaw D., с соавт., 1986; Hale A. С соавт., 1991, Fontaine R. С соавт., 1991). При сравнении СИОЗС с ТЦА, традиционно применяющемся при лечении тревожно-депрессивных состояний, как правило, указывается, что различия в эффективности исследуемых препаратов по способности купировать чувство тревоги не являются статистически значимыми (Feighner J., 1985, Laws D. С соавт., 1990, Авруцкий Г.Я., Мосолов С.Н., 1991, Doogan D., Gailard V., 1992).
По мнению многих авторов СИОЗС в ряде случаев эффективны тогда, когда применение ТЦА оказалось нерезультативным (Weilburg J.B. с соавт., 1989, Beasley C.M. с соавт.. 1990; Иванов М.В. с совт., 1991; Бовин Р.Я. с соавт., 1992; Серебрякова Т.В., 1994; Бовин Р.Я., с соавт. 1995). По данным Beasley C., Sayler M. (1990), пациенты, резистентные к ТЦА, в случаев оказываются чувствительными к новым препаратам.
Необходимо подчеркнуть большую по сравнению с ТЦА безопасность СИОЗС (меньшее число и выраженность побочных явлений), большую комфортность лечения (возможность проведения терапии в амбулаторных условиях) (Boyer W. Feighner J., 1996).
При приеме ТЦА 30% пациентов вынуждены отказаться от лечения из-за выраженности побочных действий, тогда как в случае назначения новых препаратов только у 15% больных приходится прерывать прием лекарств (Cooper G., 1988).
S. Montgomery, S. Kasper (1995) показали, что частота прекращения приема препаратов из-за побочных эффектов была у 14 % пациентов, лечившихся СИОЗС и у 19 % — ТЦА. Преимущество антидепрессантов второго поколения особенно важно в ходе длительной терапии (Medavar Т. с соавт., 1987).
Р.Я. Бовин (1989) указывает на возрастающую опасность возникновения суицида на ранних этапах терапии ТЦА. В то время как, в большинстве исследований, посвященым СИОЗС, авторы обращают внимание на высокую направленность этих препаратов против суицида (Fava M. с соавт., 1991; Cohn D. с соавт., 1990; Sacchetti E. с соавт., 1991).
Помимо терапии депрессии, все чаще предпринимаются попытки длительного применения антидепрессантов (флуоксетин, сертралин) для профилактики ее рецидивов.
Cohn G.N. с соавт., (1990), учитывая хорошую переносимость СА, рекомендуют их использование в геронтопсихиатрии.
Не существует единого мнения относительно скорости наступления эффекта при применении СИОЗС. По мнению иностранных авторов, клинический эффект СИОЗС обнаруживается позднее, чем ТЦА (Roose S, с соавт. 1994). В то же время отечественные ученые указывают, что у CИОЗС регистрируется тенденция к более быстрому наступлению терапевтического эффекта, по сравнению с другими антидепрессантами (Авруцкий Г.Я, Мосолов С.Н, 1991).
В группе СИОЗС различные препараты отличаются по силе действия на рецепторы и уровню селективности. Причем селективность и сила действия не совпадают. Было установлено, что пароксетин является более мощным ингибитором серотонинового возврата, в то время как циталопрам — более селективным. Различия в селективности и мощности действия на рецепторы определяют не только особенности терапевтического эффекта того или иного препарата, но и наличие побочных эффектов (Thopas D., с соавт., 1987; Hyttel G., 1993).
При прочих равных условиях рецидивы депрессии чаще отмечаются после терапии флуоксетином, чем пароксетином и после лечения циталопрамом, чем сертралином; при почти равном количестве рецидивов на фоне лечения сертралином и пароксетином.
Поскольку флувоксамин и пароксетин обладают выраженным седативным и противотревожным эффектом, то они по спектру своей активности приближаются к таким препаратам, как амитриптилин или доксепин. Большинство других препаратов, особенно флуоксетин, больше напоминают профиль имипрамина, так как обладают растормаживающим эффектом и могут усилить проявления тревоги и беспокойства (Caley Ch.,1993; Pujynski S., с соавт., 1994; Montgomery S., Johnson F., 1995). В отечественной литературе также имеются указания на низкую эффективность, а иногда даже усиление тревоги при применении СИОЗС у больных с тревожной депрессией (Калинин В.В., Костюкова Е.Г., 1994, Лопухов И.Г. с соавт., 1994, Мосолов С.Н., с соавт., 1994).
Вследствие растормаживающего эффекта подобные препараты не следует применять при тревоге, беспокойстве, двигательной расторможенности, бессоннице, суицидальных мыслях и тенденциях. По мнению, S. Pujynski (1996) относительным противопоказанием к применению СИОЗС являются психотические формы депрессии. Однако, Feighner J., Bouer W (1988), напротив, отмечают позитивный эффект данных препаратов даже при психотическом варианте депрессии.
Наиболее частыми побочными эффектами при приеме ингибиторов серотонина считаются гастроинтестинальные расстройства: тошнота и рвота, запоры и жидкий стул. У ряда больных отмечается снижение веса.
Таблица Сравнительная характеристика СИОЗС по выраженности побочных эффектов
Применение и токсикокинетика трициклических антидепрессантов (ТЦА)
а) Самоубийства и антидепрессанты. Около половины пациентов совершают суицид в депрессивном состоянии. Большинство таких пациентов не принимают антидепрессанты непосредственно перед смертью. Недостатки терапии (неполучение новых, менее токсичных антидепрессантов), по-видимому, являются более важной проблемой, чем токсичность антидепрессантов.
Данные исследований, проводившихся в Европе, показывают, что прием амитриптилина, имипрамина, нортриптилина и дезипрамина сопровождается большим числом случаев суицида, чем прием миансерина или тразодона.
б) Химические уникальные антидепрессанты. Тразодон — производное триазолопиридина, структурно и фармакологически отличающееся от антидепрессантов, описанных раннее. Кардиотоксичность, нейротоксичность и угнетение дыхания, часто отмечаемые в случаях передозировок трициклических антидепрессантов, не наблюдаются при передозировках тразодона.
Номифензин, необычное по химической структуре производное тетрагидроизохинолина, редко обусловливает судороги и кардиотоксичность; однако выявление тяжелых побочных реакций (таких, как летальная гемолитическая анемия, некроз печени, сердечные аритмии) побудило производителя добровольно отказаться от выпуска этого лекарства в 1986 г.
Зимелдин в 1983 г. был снят с продажи в Европе и в Америке в связи с тем, что его применение сопровождалось нарушением функции печени, потерей двигательного контроля, развитием синдрома Гийена—Барре и других невропатий и миалгий.

в) Острые токсичные дозы антидепрессантов. У 72-летней женщины, проглотившей 350 мг тразодона, отмечены гипонатриемия, гипертензия и припадки. У 63-летней женщины, проглотившей 3—4,5 г тразодона, развились летаргия, синусовая брадикардия, отмечены удлинение интервала Q—T, скорректированного на частоту сердечных сокращений (Q—Tc), и "пируэтное" нарушение ритма, что привело к остановке сердца, за которой последовали кома, почечная недостаточность и неустойчивость сердечной функции, приведшие к смерти пациентки.
При ее поступлении в больницу концентрация тразодона в сыворотке составляла 5680 нг/мл (терапевтическая концентрация равна 1600 нг/мл).
г) Токсикокинетика. Трициклические антидепрессанты (ТЦА), принимаемые в больших количествах при попытках суицида, обнаруживают измененную токсикокинетику. Их всасывание может быть задержано подавлением опорожнения желудка и перистальтики. Значительная энтерогепа-тическая рециркуляция задерживает окончательную элиминацию большой доли лекарства. Ферменты, обусловливающие бензилгидроксилирование ТЦА, могут стать насыщенными и, таким образом, вызвать снижение элиминации ТЦА до кинетики нулевого порядка.
Уровень ТЦА, не связанных с белками плазмы, может также увеличиться из-за ацидемии, развившейся вследствие угнетения дыхания после передозировок. Проглатывание других соединений при попытках суицида тоже сильно меняет токсикокинетику ТЦА.
- Распределение. Циклические антидепрессанты отличаются высокой липофильностью, и для них характерны большие и варьируемые объемы распределения (15—40 л/кг). После абсорбции эти лекарства быстро распределяются в тканях и обнаруживаются в высоких концентрациях в печени, почках, легких и миокарде. Обычно соотношение ткань: плазма превышает 10:1.
Амитриптилин распределяется преимущественно в плазме, нортриптилин — в красных кровяных тельцах. Дифференцированное распределение зависит от дозы и обусловлено более высокой степенью связывания амитриптилина с а1-кислотным гликопротеином по сравнению с нортриптилином. Идентификация уровня ТЦА в крови осуществляется посредством анализа их содержания в красных кровяных тельцах и плазме. Amitai и соавт. полагают, что содержание метаболитов ТЦА в красных кровяных тельцах служит лучшим маркером нарушенного внутрижелудочкового проведения.
- Выведение. Концентрации антидепрессантов в плазме, которые ме-таболизированы более чем на 95 %, не меняются при ослабленной функции почек. Концентрации антидепрессантов, которые экскретируются с мочой преимущественно в неизмененном виде, значительно повышаются у пациентов с ослабленной почечной функцией. Содержание метаболитов, составляющих 10 % и более от дозы исходного лекарства в моче, повышается при нарушении функции почек.
Гидроксилированные метаболиты. Трициклические и некоторые другие антидепрессанты входят в число психотропных средств, которые подвергаются реакции гидроксилирования. Гидроксилированные метаболиты (OHM) антидепрессантов фармакологически активны. Гепатическое гидроксилирование — основной метаболический путь ТЦА и других антидепрессантов. OHM менее липофильны, чем исходные соединения.
Возможно, этим объясняется их меньший объем распределения. Соотношение концентраций в спинномозговой жидкости и суммарных концентраций в плазме обычно выше для OHM, чем для соответствующих исходных соединений. Это может обусловливать значительное воздействие OHM на центральную нервную систему после применения ТЦА.
При терапевтических концентрациях степень деметилирования значительно варьирует у взрослых пациентов (по данным одного исследования, от 25 до 89 %). Это означает, что у разных лиц количества исходного лекарственного средства и активного метаболита могут также значительно варьировать при одной и той же дозе. Период полужизни амитриптилина при передозировках варьирует от 25 до 81 ч, тогда как период полужизни при передозировках имипрамина варьирует между 12 и 21 ч.
Вилоксазин. После перорального приема дозы 100 мг пиковая концентрация в крови 0,8—3,56 мкг/мл достигается примерно через 2 ч. Период полужизни 2— 5 ч. Для определения концентраций вилоксазина в плазме применяют метод газовой хроматографии с чувствительностью 0,1 мкг/мл. Вилоксазин метаболизируется главным образом путем гидроксилирования. Когда вилоксазин применяют одновременно с теофиллином или с карбамазепином, конкуренция из-за одних и тех же микросомальных ферментов печени, по-видимому, ингибирует выведение двух последних лекарственных средств, их концентрации в крови возрастают и их токсичность повышается.
д) Механизм действия трициклических антидепрессантов. Тразодон ингибирует поглощение серотонина и серотониновые рецепторы (5-НТ2), а также умеренно ингибирует а-адренергические рецепторы и обнаруживает некоторую антигистаминовую (Н1) активность. Его активный метаболит, m-хлорфенилпиперазин (mХФП), действует и как агонист, и как антагонист серотонинового рецептора, ингибирует повторное поглощение серотонина и взаимодействует с а-адренергическими, дофаминовыми, ацетилхолиновыми и b-адренергическими рецепторами.
При проведении исследования с участием пациентов, принимавших циклические антидепрессанты, были отмечены повышение уровня катехоламина и расширение комплекса QRS без соответственного изменения кровяного давления, что позволило сделать вывод о десенсибилизации адренергических рецепторов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Побочные эффекты ТЦА
Большое разнообразие эффектов выражается и в достаточно большом количестве побочных эффектов, возникающих в процессе терапии ТЦА. При приеме трициклических антидепрессантов 30% пациентов вынуждены отказаться от лечения из-за выраженности побочных действий, тогда как в случае назначения антидепрессантов, более поздних поколений только у 15% больных приходится прерывать прием лекарств. У пожилых больных ТЦА могут вызывать состояние спутанности сознания и миоклонические судороги.
Наиболее частым следствием холинолитического эффекта ТЦА являются сухость во рту, запоры, задержка мочи, ортостатическая гипотония, сонливость и вялость, реже отмечаются сердцебиение, а в ряде случаев и нарушение сознания. Наиболее выраженными побочными эффектами обладают амитриптилин и кломипрамин.
Антигистаминное действие выражается в увеличении массы тела, сонливости, понижении артериального давления (возможен ортостатический коллапс).
Воздействие на альфа-адренергические рецепторы также вызывает гипотензию и сонливость. Торможение захвата норадреналина проявляется тахикардией, мышечными подергиваниями, сексуальными дисфункциями: нарушением эрекции, эякуляции.
Следствием торможение захвата дофамина является двигательное возбуждение, обострение психопатологической симптоматики.
Торможение захвата серотонина проявляется снижением аппетита, тошнотой, диспепсией, ослабление эрекции, эякуляции, ухудшением зрения (при контактных линзах ощущение «песка в глазах»).
Большинство побочных эффектов со временем проходит, но в ряде случаев требуется снижение дозировки препарата или его замена. Однако, и сами пациенты могут уменьшить выраженность побочных эффектов, например, при сухости во рту советуют сосательные конфеты, не содержащие сахара или жевательную резинку.
Не рекомендуется давать ТЦА тем пациентам, которые высказывают суицидальные мысли, если больные в этот момент времени находятся вне стационара.
Общеизвестно токсическое влияние ТЦА на сердце, обычно проявляющееся в нарушении проводимости, ускорении ритма сердечных сокращений. При нарушении функции синусового узла возможно появление брадиаритмии при приеме ТЦА. При приеме данных препаратов нередко развивается феномен увеличения интервала QT на ЭКГ, вследствие вышесказанного возможно появление желудочковой тахикардии.
В случае повышенной чувствительности к этим медикаментам возможны нарушения со стороны кожных покровов, изменение функциональных возможностей печени, крови. Как отмечалось выше, влияние на центральную нервную систему может проявляться судорожными приступами.
Побочные эффекты, вызываемые ТЦА, часто ограничивают возможность применения адекватных доз, и значительное число пациентов вынуждено получать лечение недостаточными дозами, Так, по данным J. McCombs с соавт. (1990) до 80% пациентов получают лечение недостаточными для эффекта дозами препаратов. Кроме того, лечение низкими дозами создает опасность перехода острой фазы в хроническую (Бовин Р.Я., с соавт., 1989).
Резкая отмена TЦА может приводить к возникновению тревоги, беспокойства, бессонницы, выраженных вегетативных расстройств, появлению болях в мышцах, тошноты и рвоты (Dilsaver C., с соавт., 1987).
Классификация антидепрессантов и их токсичность
Антидепрессанты входят в число лекарственных средств, которые особенно часто являются причиной самоотравлений. К этим лекарствам относятся трициклические, тетрациклические, бициклические и моноциклические антидепрессанты, а также ингибиторы моноаминоксидазы (МАО) и селективные ингибиторы повторного поглощения серотонина (СИППС).
Из числа названных препаратов более сильную токсичность при передозировках обычно дают трициклические антидепрессанты (ТЦА), при этом максимальная токсичность проявляется в первые 6 ч после передозировки. Проявление интоксикации наиболее вероятно после передозировок классических ТЦА и классических ингибиторов МАО, за ними следуют новые циклические антидепрессанты.
Интоксикация редко наблюдается при применении новых ингибиторов MAO-A и СИППС, если эти средства применяют раздельно.
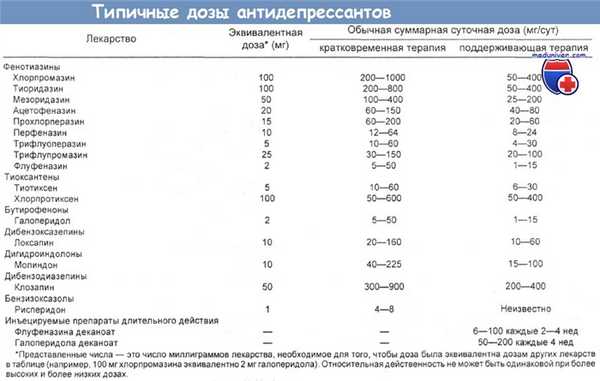
В таблицах ниже представлены классы психотропных средств, в частности "новые" лекарственные средства, приведены данные по фармакологическим эффектам антидепрессивных средств, дан перечень антидепрессантов, выпускаемых в США и Великобритании.

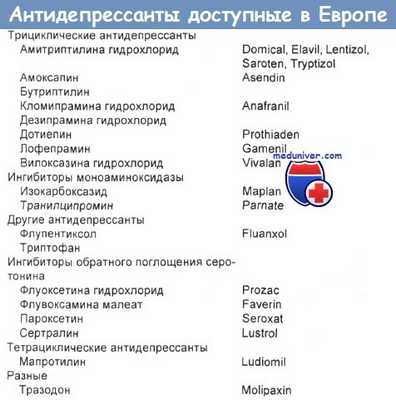
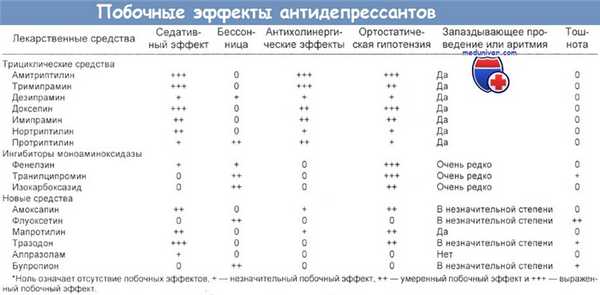
а) Терапевтическая доза. В таблице ниже приведены типичные дозы и данные об относительной действенности антипсихотических лекарственных средств, выпускаемых в США.
б) Индекс смертельной токсичности. На основе индекса смертельной токсичности (ИСТ) антидепрессанты классифицируют следующим образом: дотиэпин, амитриптилин и транилципромин — как средства с "недопустимым риском" (более 40 смертных случаев на 1 млн выписанных рецептов), мапротилин — как "очень опасное" средство (более 30 смертных случаев на 1 млн выписанных рецептов), фенелзин и имипрамин — как "очевидно опасные" (более 20 смертных случаев на 1 млн выписанных рецептов), кломипрамин, протриптилин и тразодон — как "потенциально опасные средства" (более 10 смертных случаев на 1 млн), лофепрамин, миансерин, флувоксамин, флуоксетин и вилоксазин — как "относительно безопасные" — менее 10 смертных случаев на 1 млн выписанных рецептов.
Используя аналогичную методологию, De Jonghe и Swinkels классифицировали флуоксетин, флувоксамин, миансерин, пароксетин и тразодон как "безопасные антидепрессанты", обосновывая это тем, что передозировки этих антидепрессантов при двухнедельном приеме лекарств переносятся пациентами без значительной интоксикации.
в) Токсикокинетика. Обобщенные данные по токсикокинетике антидепрессантов представлены в таблицах ниже. Следует обратить внимание на большой объем распределения и высокую степень связывания этих лекарств с белками плазмы. Вследствие этого экстракорпоральные методы элиминации могут оказаться малоэффективными.
г) Механизм действия. Антидепрессанты являются активными блокаторами адренергических, серотониновых, дофаминовых, гистаминовых Н1- и мускариновых рецепторов. Эти свойства отражены в их токсических эффектах.
НА — норадреналин (норэпинефрин). 5-НТ — 5-гидрокситриптамин (серотонин). Д — дофамин.
а1 — а1-адренергический рецептор. а2 — а2-адренергический рецептор.
Н1 — гистаминовый Н1-рецептор. МУСК — мускариновый (холинергический) рецептор.
0 — отсутствие эффекта. ± — неоднозначный эффект. + — слабый эффект.
++ —умеренный эффект. +++ — сильный эффект. ++++ — максимальный эффект.
д) Клиническая картина отравления антидепрессантами:
- Шизофрения. По имеющимся данным, ген дофамин-D2-рецептора (DRD2) — потенциальный ген шизофрении. Блокада дофамин-D2-рецептора обусловливает также экстрапирамидные синдромы, индуцируемые нейролептическими средствами.
- Синдром дефицита, индуцированный нейролептиками. Антипсихотические лекарственные средства (например, галоперидол) обусловливают развитие синдрома дефицита, для которого характерны седативный эффект, экстрапирамидные признаки, индифферентность к внутренним и внешним раздражителям, пассивность и снижение инициативности.
Такое нарушение когнитивной, социальной и эмоциональной функций обозначают термином "синдром дефицита", индуцированный нейролептиками (СДИН). Некоторые пациенты переключились на клозапин, применение которого характеризуется "пробуждающим" эффектом. Отграничение СДИН от других эффектов, таких как индуцированные лекарствами паркинсонизм и акатизия, седативный эффект и депрессивные проявления шизофрении, все еще остается серьезной проблемой.
Нарушение когнитивной функции, обусловленное глубинным заболеванием, может быть устранено посредством терапии, но за этим может последовать нарушение когнитивной функции, обусловленное действием нейролептических средств.
- Шизофрения типов I и II. Различают два синдрома шизофрении. Каждый может быть ассоциирован со специфическим патологическим процессом. Синдром типа I, эквивалентный острой шизофрении и характеризуемый позитивными симптомами (бредом, галлюцинациями и нарушением мышления), некоторым образом связан с изменениями дофаминергической передачи возбуждения.
Синдром типа II характеризуется негативными симптомами (аффективным уплощением и обеднением речи) и не связан с дофаминергической передачей нервного импульса, но может быть обусловлен расстройством интеллекта и, возможно, структурными изменениями в головном мозге. Симптомы шизофрении типа I обратимы; симптомы шизофрении типа II могут оказаться необратимыми. Синдром типа I предполагает потенциальную реакцию на нейролептические средства.
При синдроме типа II долгосрочный прогноз неблагоприятен. За проявлением симптомов типа I может последовать развитие синдрома типа II, возможно проявление обоих синдромов. Однако симптомы типа II определяют группу болезней с более серьезным прогнозом.
е) Лабораторные данные. При острых передозировках антидепрессантов необходимость идентификации и количественного анализа возникает только при применении ТЦА. Для количественного анализа других циклических антидепрессантов, например ингибиторов МАО-А или СИППС, нет оснований. Качественная идентификация ингибиторов МАО-А и СИППС может потребоваться, если есть подозрение, что эти лекарства принимали одновременно.


Фармакокинетические параметры антидепрессантов различных классов
| Фармакокинетический параметр | Трициклические антидепрессанты (ТЦА) | Селективные ингибиторы повторного поглощения серотонина (СИППС) | Бупропион | Тразодон | Ингибитор моноаминоксидазы |
| Tмакс | Достигается в пределах 1—3 ч для третично-аминных ТЦА и 4—8 ч для вторично-аминных ТЦА. Обусловливает седативный эффект, ортостатическую гипотензию и ухудшение внутрисердечного проведения. | Медленная скорость абсорбции: в типичных случаях 4—8 ч. В течение 1 ч после введения СИППС может отмечаться тошнота, что свидетельствует о прямом воздействии на желудок. Из-за длительного Тмакс изменение дозы с целью минимизации бессонницы, но всей вероятности, не поможет. | Достигается в течение 1—3ч. Вызывает тошноту (обусловленную воздействием на желудочно-кишечный тракт или на ЦНС) и возбуждающий эффект. Наибольшее число совпадений припадков с интервалом Тмакс. | Достигается в течение 1—2 ч. Вызывает седативный эффект. | Достигается в течение 1—3 ч. Во время этого интервала наблюдается наибольшее число некоторых неблагоприятных сердечно-сосудистых реакций. |
| Период полувыведения | У всех ТЦА период полувыведения равен 24 ч или больше у физически здоровых людей с нормальным метаболизмом, когда периоды полувыведения исходного лекарства и его активного метаболита рассматриваются в совокупности. Следовательно, ТЦА можно давать 1 раз в день, если только нет проблем с Смакс (например, у пациентов с сердечными заболеваниями). У большинства молодых, физически здоровых взрослых людей стационарное состояние устанавливается на протяжении 7 сут. | Среди СИППС отмечаются существенные различия: флуоксетин (2—4 сут), норфлуоксетин (7—15 сут), пароксетин в начальной дозе (1 сут, но увеличивается при более высоких дозах вследствие аутоингибирования), сертралин в диапазоне клинически целесообразных доз (1 сут). Время достижения стационарного состояния у молодых, физически здоровых взрослых людей: флуоксетин (10—20 сут), норфлуоксетин (35—75 сут),сертралин(7 сут), пароксетин (7 сут при 20 мг/сут и больше при более высоких дозах). Поскольку у флуоксетина и норфлуоксетина длительные периоды полувыведения, может происходить постепенное накопление эффектов за много недель, а также отмечаться длительная персистенция после прекращения приема лекарства. Титрование доз может вызвать затруднения. | Период полувыведения (средн. ± СО) бупропиона — 9,8 ± 6,8 ч; гидроксибупропиона — 22,2 + 5,6 ч; треогидробупропиона — 26,8 ± 9,4 и эритрогидробупропиона — 19,8 + 8,2 ч. Период полувыведения исходного лекарства в сочетании с проблемой частоты припадков и величины Смакс обусловливает необходимость многократного ежедневного применения доз для экстренной и поддерживающей терапии. | 5—9 ч. Короткий период полувыведения делает необходимым ежедневное многократное применение доз для индуцирования ремиссии. В отсутствие противопоказаний ежедневное многократное применение доз рекомендуется для поддерживающей терапии. Стационарное состояние достигается в течение 2—3 сут. | 2—4 ч. Длительный биологический эффект вследствие необратимой дезактивации фермента. Полная диссоциация кривой концентрация в плазме — реакция — время. |
| Активные метаболиты | ТЦА образуют многочисленные метаболиты, фармакологические профили которых могут быть клинически отличными от профиля исходного лекарства. Вторично-аминные ТЦА (например, дезипрамин, нортриптилин) являются метаболитами третично-аминных ТЦА (например, имипрамина, амитриптилина). Возможно, они более действенные антидепрессанты, чем третично-аминные ТЦА; однако они предпочтительнее по профилю побочных эффектов: у них менее выражены антихолинергический, антигистаминный, анти-а1-эдренергический эффекты и эффект прямой мембранной стабилизации. Имеются также гидроксилированные метаболиты. | СИППС значительно различаются между собой по данному показателю. Флуоксетин образует метаболит (норфлуоксетин). который равен по действенности исходному лекарству как в отношении ингибирования повторного поглощения серотонина, так и в отношении ингибирования гепатического изофермента IID6. Ни сертралин, ни пароксетин не образуют метаболитов, которые играли бы клинически значимую роль в ингибировании повторного поглощения серотонина. Оба образуют метаболиты, которые могут ингибировать фермент IID6; концентрации этих метаболитов и их действенность таковы, что не могут вызвать клинически значимых последствий. | Три биологически активных метаболита проявляют себя в большей степени как вещества, способные индуцировать припадки, чем как антидепрессанты. | ХФП — основной биологически активный метаболит, фармакологический профиль которого существенно отличается от фармакологического профиля тразодона. Для него характерны анксиогенный и другие эффекты. | Метаболиты структурно и фармакологически подобны амфетаминам и могут обусловливать некоторые стимулирующие эффекты МА-ОИ, которые проявляются вскоре после проглатывания лекарства (т. е. через 2—5 ч). |
| Взаимосвязь между дозой и концентрацией в плазме | В пределах клинически приемлемого диапазона доз у большинства пациентов наблюдалась линейная фармакокинетика ТЦА. Примерно у 7 % белых людей отмечается генетически обусловленный медленный метаболизм ТЦА вследствие функциональной недостаточности гепатического изофермента IID6. В связи с этим у таких пациентов увеличение дозы ТЦА вызывает непропорционально значительное повышение концентраций ТЦА в плазме. Возраст, болезни, одновременное применение других лекарственных средств и необычайно высокие дозы ТЦА тоже могут обусловить нелинейную фармакокинетику ТЦА. | Для сертралина характерна линейная фармакокинетика в пределах клинически приемлемого диапазона доз, тогда как у флуоксетина и пароксетина такая линейность отсутствует. Повышение доз последних сопровождается несоразмерно значительным увеличением концентраций в плазме и увеличением продолжительности периодов полувыведения. Их нелинейная фармакокинетика обусловлена их ингибирующим действием на изоферменты печени, катализирующие их биотрансформацию перед выведением. | Проблема недостаточно изучена, чтобы можно было делать категорические заключения. Проблема является потенциально клинически значимой в связи с зависящим от дозы (и, следовательно, зависящим от концентрации лекарства в плазме) риском возникновения припадков и сложным метаболизмом бупропиона. | Проблема недостаточно изучена, чтобы можно было делать определенные выводы. Возможны эффекты, сопряженные с Смакс. | Есть данные, позволяющие предполагать, что для МАОИ характерна нелинейная фармакокинетика в клинически приемлемом диапазоне доз, но данные о клинической значимости этого фактора отсутствуют. |
| Особые группы населения - Возраст | У пациентов в возрасте старше 60 лет концентрации ТЦА в плазме после применения одинаковых доз в 2 раза выше, чем у более молодых лиц, принимавших амитриптилин, нортриптилин и, предположительно, другие ТЦА. | Возраст практически не влияет на концентрацию сертралина в плазме, но в большей степени влияет на концентрации пароксетина и флуоксетина плюс норфлуоксетина. У физически здоровых пожилых (> 65 лет) лиц концентрации этих двух лекарств в плазме выше, чем у молодых людей. | Проблема изучена недостаточно. | С возрастом в связи с ухудшением функции почек происходит снижение клиренса m ХФП. | Информация о фармакокинетических различиях у детей, молодых и пожилых людей ничтожно мала. Рекомендуется соблюдать осторожность. |
| - Болезни | Нарушение функции левого желудочка сердца и функции печени снижает клиренс третично-аминных и вторично-аминных ТЦА. Нарушение почечной функции снижает клиренс гидроксилированных метаболитов ТЦА. | Систематического исследования по этой проблеме не проводилось. При значительном ухудшении функции печени периоды полувыведения флуоксетина и норфлуоксетина увеличиваются в 3 и 2 раза соответственно. Поскольку клиренс печени зависит от печеночного артериального кровотока, нарушение функции печени левого желудочка сердца приводит к снижению клиренса. | Проблема изучена недостаточно. Можно прогнозировать, что у пациентов с заболеванием почек будет отмечаться большее аккумулирование метаболитов. | Клиренс m ХФП зависит от функции почек и левого желудочка сердца. | Проблема изучена недостаточно. Сомнительно, что будут наблюдаться клинически значимые последствия. Возможны фармакодинамические последствия. |
| - В качестве запланированного лекарства | Метаболизм ТЦА может быть индуцирован и ингибирован различными лекарственными средствами. К числу индуцирующих лекарств относятся карбамазепин, фенобарбитал и фенитоин. Стационарные уровни ТЦА в плазме могут снизиться на 50 % или более, что обусловливает риск рецидива. В число ингибиторов входят флуоксетин, пароксетин, хинидин и нейролептики. Стационарные уровни ТЦА могут возрасти в 4—10 раз, что связано с риском тяжелой интоксикации (например, делирия, припадков, сердечных аритмий). Прекращение одновременного приема индуцирующих или ингибирующих лекарств приводит соответственно к увеличению или снижению концентраций ТЦА в плазме. | Флуоксетин и пароксетин ингибируют свой собственный метаболизм и поэтому, по всей вероятности, друг друга. Флуоксетин ингибирует метаболизм сертралина. Эффект пароксетина неизвестен. | Систематических исследований мало, имеются данные отдельных историй болезни. Вероятно, концентрации исходного лекарства и/или метаболитов снижаются под воздействием карбамазепина и близких к нему лекарств, индуцирующих активность Р450-изоферментов. Описан случай, когда флуоксетин вызвал значительное повышение уровня гидроксибупропиона и треогидробупропиона. Влияние пароксетина не изучалось, но его возможный эффект следует принимать во внимание. Уровни бупропиона и/или метаболитов могут также подвергаться воздействию циметидина и бета-адреноблокаторов. | Систематических исследований мало. Если принять во внимание большой терапевтический индекс и короткий период полувыведения, клинически значимое взаимодействие с другими лекарствами, ведущее к тяжелым последствиям, представляется маловероятным. | Данные о воздействии других лекарственных средств на фармакокинетику МАОИ неизвестны. |
| - В качестве лекарства-протагониста | Данные отсутствуют | Флуоксетин и пароксетин в дозе 20 мг/сут обнаруживают клинически значимое ингибирование гепатического изофермента IID6, что приводит к повышению в плазме концентраций лекарственных средств, метаболизируемых при посредстве этого фермента. Сертралин в дозе 50 мг/сут такого действия не оказывает. Эти различия усиливаются при повышении доз вследствие нелинейной фармакокинетики флуоксетина и пароксетина и линейной фармакокинетики сертралина, а у пожилых лиц эти различия усиливаются вследствие обусловленного возрастом снижения клиренса флуоксетина и пароксетина и минимального влияния возраста на клиренс сертралина. Флуоксетин, кроме того, ингибирует биотрансформацию алпразолама в 4-гидроксиалпразолам, которая зависит от гепатического изофермента IIIA4. Подобному воздействию должны подвергаться и другие лекарственные средства, зависящие от активности фермента IIIA4. | Нет никаких данных о том, что бупропион индуцирует или ингибирует метаболизм других лекарственных средств в клинически значимой степени. | Нет никаких данных о том, что тразодон индуцирует или ингибирует метаболизм других лекарственных средств в клинически значимой степени. | Нет данных о воздействии МАОИ на метаболизм или элиминацию других лекарственных средств, но они ингибируют один фермент и, таким образом, могут воздействовать на изоферменты печени. |
Антидепрессанты применяются при широком круге аффективных расстройств, наблюдающихся в общемедицинской сети — при нозогенных, соматогенных, невротических, реактивных, эндогенных депрессиях и дистимиях. Выбор препаратов зависит в первую очередь от типологической структуры депрессий (схема 5).
Систематика антидепрессантов в соответствии с типологией депрессивных расстройств
Лечение при типичных депрессиях
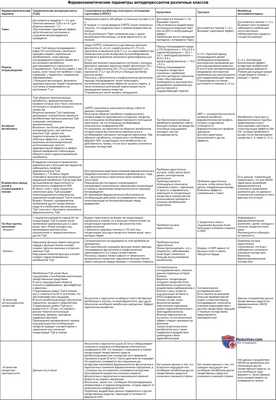
При типичных (витальных) депрессиях, психопатологические симптомокомплексы которых исчерпываются проявлениями позитивной эффективности, используется общее тимоаналептическое действие антидепрессантов, которым обладают все препараты этого класса. Как показано на рис. 7, на котором представлены данные сравнительного мета-анализа эффективности антидепрессантов различных групп, можно видеть, что линия тренда, объединяющая доли респондеров в каждой из тестируемых групп антидепрессантов, находится примерно на одном уровне и не обнаруживает существенных достоверных различий. Выбор психотропных средств в этих случаях зависит в первую очередь от тяжести состояния.
Положительный результат в процессе купирования аффективных расстройств большой выраженности (тяжелые депрессии) можно прогнозировать при применении антидепрессантов три- и гетероциклической структуры (имипрамин, кломипрамин, амитриптилин, мапротилин). Как показал опыт, накопленный в клинике по изучению пограничных состояний и психосоматических расстройств НЦПЗ РАМН, совпадающий с данными ряда европейских клиник [Kasper S., 1997; Anderson I. M., 2000] (схема б), купирование остро возникших депрессивных эпизодов (подавленность с чувством безнадежности и суицидальными мыслями (или тенденциями), тревога, достигающая степени ажитации, либо двигательное торможение с явлениями депрессивного ступора) проводится с помощью таких препаратов, как имипрамин, кломипрамин, амитриптилин и мапротилин, при необходимости вводимых парентерально (внутримышечно, внутривенно. капельно — см. с. 161: «Альтернативные способы введения психотропных средств»). В подтверждение более высокой эффективности ТЦА (и прежде всего амитриптилина) сравнительно с СИОЗС при терапии депрессий, требующих в связи с их тяжестью (меланхолический уровень расстройства, высокий риск суицидального поведения) госпитализации, приводятся данные мета-анализа, обобщающего материалы 102 исследований (свыше 10000 больных) [Anderson I. M., 2000].
Сопоставление эффективности антидепрессантов различных групп при витальных депрессиях: данные мета-анализа; n — число исследований. Разность между суммарными долями респондеров на тестируемую группу антидепрессантов и тимолептиками сравнения, % [Depression Guideline Panel. Depression in Primary Care, 1993]
Критерии выбора антидепрессантов при типичной депрессии [Kasper S., 1997; Смулевич А. Б. и др., 2001]
Трициклические (амитриптилин, имипрамин, кломипрамин) и гетероциклические (мапротилин) антидепрессанты наряду с тимоаналептическим обнаруживают и выраженное ноцицептивное (противоалгическое) действие, способствуя редукции острых и хронических болей различной этиологии [Fish bain D., 2000]. Соответственно препараты этой группы эффективны при депрессиях с явлениями фибромиалгии, а также при сочетании депрессии с болями в рамках соматической и/или неврологической патологии (невралгии, пояснично-крестцовый радикулит, артралгии). Использование ТЦА при терапии депрессий у онкологических больных снижает потребность в наркотических анальгетиках.
При легких депрессиях и депрессиях средней тяжести (тоска, сниженная самооценка, соматизированные и другие расстройства, выраженность которых варьирует в соответствии с патологическим циркадным ритмом — ранние пробуждения с пиком плохого самочувствия, приходящимся на утренние часы) применяются,(см. схемы 5 и 6) психотропные средства первого ряда (СИОЗС, ССОЗС, СИОЗСиН и др.), обладающие элективным действием (стимулирующим либо седативным). Выбор того или иного антидепрессанта в этих случаях производится с учетом возможных побочных эффектов, коморбидной соматической патологии, предпочтительной чувствительности к антидепрессантам, обнаружившейся в период лечения предшествующих депрессивных эпизодов, а также у других членов семьи. Эти препараты с успехом используют как при рекуррентных, так и при затяжных депрессиях.
Лечение атипичных депрессий
Лечение атипичных депрессий, формирующихся как путем акцентуации одной из облигатных составляющих аффективного синдрома — тревожная, ипохондрическая, самоистязающая депрессии, так и путем видоизменения психопатологических проявлений собственно гипотимии — апатическая, адинамическая, астеническая, анестетическая, деперсонализационная, депрессия с отчуждением соматочувственных влечений (см. соответственно депрессии типов bi и А, разд. III, с. 41-46) требует более дифференцированного подхода, учитывающего избирательную психотропную активность (элективный клинический эффект) антидепрессантов (см. схемы 5 и 6).
Атипичные депрессии типа Б 1
При атипичных депрессиях типа Б 1 протекающих с преобладанием тревожных, ипохондрических и других расстройств показаны препараты с элективной анксиолитической активностью.
Пиразидол — оригинальный отечественный препарат тетрациклической структуры (синтезирован во ВНИИХФИ М. Д. Машковским и Н. И. Андреевой в 1975 г.) показан при аффективных расстройствах с явлениями соматизированной тревоги, вегетативных, соматизированных депрессиях, а также при гипотимических состояниях с преобладанием анксиозных и фобических расстройств. Назначение препарата в суточных дозах 100-200 мг, как правило, не сопровождается побочными эффектами.
Широкое применение находит тианептин (коаксил) — антидепрессант новой генерации, по химической структуре относящийся к атипичным трициклическим тимоаналептикам. Механизм действия препарата уникален: тианептин не блокирует, а напротив, стимулирует обратный захват серотонина. В отличие от традиционных ТЦА, тианептин обладает селективностью: не оказывает клинически значимого влияния на рецепторы a1 - и a2 -адренергические, дофаминовые, серотониновые, имипраминовые, глютаминовые, бензодиазепиновые, мускариновые, гистаминовые, кальциевые каналы, что обеспечивает особенно благоприятную переносимость и безопасность препарата. Тианептин назначается в средних дозах 25-37,5 мг/сут.
В результате систематического анализа эффективности тианептина, проведенного в отделе по изучению пограничной психической патологии и психосоматических расстройств НЦПЗ РАМН и в межклиническом психосоматическом отделении ММА им. И. М. Сеченова, установлено, что препарат обладает широким спектром клинической активности (сочетание антидепрессивного, анксиолитического и рединамизирующего действия). Установлено также, что тианептин может применяться при коморбидности аффективных расстройств с тяжелыми соматическими заболеваниями.
По выраженности антидепрессивного действия при легких и умеренных депрессиях, которые преимущественно встречаются в общемедицинской практике, тианептин не уступает эталонным антидепрессантам. Эффективность тианептина при депрессивных состояниях с выраженными соматовегетативными, астеническими, алгическими и конверсионными расстройствами превышает 70 %. При этом длительная терапия приводит к снижению частоты обострений (до 6 % через б месяцев) и рецидивов депрессии (до 12 % через 18 месяцев) [Dale- гу 1 et al, 1997]. Одновременно проявляется характерная особенность действия тианептина — противотревожный анксиолитический эффект, отличающийся от сходных свойств стандартных ТЦА. Применение тианептина способствует быстрой — на протяжении первых же недель — редукции как психической, так и соматической тревоги. Если при использовании ТЦА купирование сопутствующей депрессии тревожной симптоматики сопровождается выраженными явлениями поведенческой токсичности (сонливость, психическая и двигательная заторможенность, нарушения внимания и пр.), то терапия тианептином приводит к редукции тревожных расстройств без побочных эффектов, а ее результаты клинически сопоставимы с действием транквилизаторов.
Тианептин безопасен при терапии депрессий у больных сердечнососудистой патологией [Дробижев М. Ю. и др., 1998]; эндокринологической (сахарный диабет) [Анциферов М. Б., Захарчук Т. А., 2001], дерматологической (псориаз, экзема) [Дороженок И. Ю., Белоусова Т. А., 2001]. Препарат практически не влияет на артериальное давление, число сердечных сокращений, не вызывает клинически значимой ортостатической гипотензии, не изменяет уровень сахара в крови, гематологические показатели.
Терапевтическое действие тианептина при аффективных расстройствах, сочетающихся с функциональными (синдром раздраженной толстой кишки) и органическими нарушениями ЖКТ, сказывается в первые же дни лечения и неуклонно нарастает на протяжении всего курса лечения [Смулевич А. Б. и др., 1999]. Параллельно тимоаналептическому обнаруживается и соматотропный эффект, проявляющийся в первую очередь редукцией вегетативных дисфункций и абдоминалгий. О безопасности тианептина свидетельствуют данные R. Mal ka с соавт. (1992), с успехом применявших препарат при тревожных депрессиях у больных с циррозом печени и гепатоцеллюлярной недостаточностью.
Тианептин эффективен и безопасен при депрессиях позднего возраста [Андрусенко М. П. и др., 1999] и, в частности, у женщин в период менопаузы [Chaby L et al., 1993].
Положительные результаты при лечении тревожных депрессий наблюдаются при применении СИОЗС. Это новая группа психотропных средств, тормозящих обратное проникновение серотонина из синаптической щели внутрь пресинаптического нейрона.
При сходстве механизма действия препараты группы СИОЗС дифференцируются по химической структуре и фармакокинетическим показателям, с чем, по-видимому, частично могут быть связаны различия клинических эффектов. Быстрой редукции как депрессивного, так и тревожного аффекта, сопровождающихся беспокойством, дисфорией и нарушениями сна, способствуют такие СИОЗС, как сертралин (золофт), флувоксамин (феварин), пароксетин (паксил).
Антидепрессанты группы СИОЗС эффективны при дистимиях (в рамках длительной, способствующей восстановлению витальных функций и улучшающей качество жизни, терапии [Ravindran A. V., 1999]), а также при невротических, циркулярных, реактивных и нозогенных депрессиях, при посттравматическом стрессовом расстройстве, органических поражениях ЦНС, соматических заболеваниях, при аффективных симптомокомплексах, возникающих в послеродовом периоде, а также в рамках синдрома предменструального дисфорического расстройства [Freeman E. W. et al., 2000].
Флуоксетин, а также другие препараты этой группы (пароксетин, сертралин, флувоксамин) применяются у ВИЧ-инфицированных. При хорошей переносимости эти медикаменты обнаруживают высокую эффективность при депрессиях, формирующихся на разных этапах заболевания. Доля респондеров при лечении флуоксетином депрессий, коморбидных ВИЧ-инфекции, по данным различных авторов, колеблется от 74 до 100 % [Penzak S. R. et at 2000].
Препараты этой группы значительно расширяют возможности терапии депрессий, коморбидных с соматическими (особенно сердечнососудистыми) заболеваниями, протекающими с нарушениями проводимости миокарда и явлениями ортостатической гипотензии.
Некоторые депрессии, протекающие с преобладанием анксиозных расстройств (особенно соматизированной тревоги), обнаруживают чувствительность не к серотонинергическим, но к норадренергическим антидепрессантам СБОЗН: миансерин (леривон), а также к НССА: миртазапин (ремерон), блокирующим пресинаптические а-ауто- и гетерорецепторы, а также серотонинергические (5НТ2 и 5НТз) рецепторы. Эти препараты уже в первые дни терапии купируют нарушения сна; наряду с этим редуцируются признаки ажитации и соматизированные расстройства [Мосолов С. Н., 1995]. Селективный блокатор обратного захвата норадреналина миансерин (леривон) по спектру психотропной активности относится к «малым» антидепрессантам [Мосолов С. Н., 1995]. Благодаря мягкому тимоаналептическому эффекту и удобству дозирования (назначается 1 раз в сутки, чаще перед сном, в дозах 15-60 мг) может применяться в амбулаторной практике (маскированные, соматизированные депрессии, инволюционная истерия с дисфорической симптоматикой — приливами, чувством жара, головными болями). Исследование миансерина, проведенное в отделе по изучению пограничной психической патологии и психосоматических расстройств [Смулевич А. Б. и др., 1997], а также данные других авторов свидетельствуют о возможности применения препарата для лечения депрессий у больных с соматической патологией (ИБС, гипертензия и др.), при функциональных расстройствах ЖКТ, протекающих с болями и другими неприятными ощущениями в абдоминальной области [Tanum Y., Malt U. F., 1996]. Миансерин не влияет на артериальное давление, частоту сердечных сокращений, в период терапии не отмечается значимых нежелательных взаимодействий с широким кругом соматотропных средств.
Миртазапин (ремерон) эффективен при депрессиях, протекающих с явлениями как генерализованной, так и соматизированной тревоги, при коморбидности аффективных расстройств с ТФР (панические атаки) [Carpenter L L et al, 1999]. Миртазапин используется при комбинированной терапии аффективных расстройствах, резистентных к психофармакологическим средствам [Carpenter L L. et al, 1999], а также в сочетании с другими антидепрессантами в качестве препарата, назначаемого в вечернее время и на ночь, купирующего нарушения, наблюдающиеся во всех фазах сна (затрудненное засыпание, прерывистый сон, раннее пробуждение). Препарат в отличие от СИОЗС способствует повышению массы тела и соответственно показан при депрессиях, протекающих с отчуждением витальных влечений в виде депрессивной анорексии.
Депрессии типа А
В случаях доминирования в клинической картине атипичной депрессии проявлений негативной эффективности — энергических расстройств, признаков утраты жизненного тонуса и психической активности, сознания невозможности концентрации внимания, обедненности воображения (см. разд. III, с. 41: депрессии типа А) — показаны СИОЗС: флуоксетин (прозак, продел, портал, профлузак) и циталопрам (ципрамил), являющиеся препаратами выбора при апатической и энергической депрессии, протекающей с явлениями ангедонии и психической анестезии [Бовин Р. Я. и др., 1992; Мосолов С. Н., 1995].
Флуоксетин эффективен при атипичных депрессиях, сопровождающихся падением физической энергии, достигающим иногда степени «паралича активности», когнитивными расстройствами (рассредоточенность, замедление течения мыслительных процессов, нарушения памяти), гиперсомнией, повышением аппетита [McGrath P. J. et al., 2000]1.
Широкое применение находит флуоксетин при затяжных депрессивных фазах, а также при поддерживающей терапии; ни низкие дозы препарата, используемые в этих случаях, ни даже длящийся в течение нескольких дней перерыв в лечении не приводят к экзацербации эффективных расстройств. Это связывают со свойственным флуоксетину длительным периодом полувыведения [Michel son D. et al, 2000].
Циталопрам рассматривается как новый стандарт селективности СИОЗС, что связано с фактическим отсутствием влияния препарата и его метаболитов на норадренергические и дофаминергические нейротрансмиттерные системы. Препарат эффективен при легких депрессиях и депрессиях умеренной тяжести с явлениями угнетенности, нарушением вовлеченности в события окружающей жизни, снижением побуждений к деятельности, заторможенностью, признаками психической анестезии и депрессивной деперсонализации [Дубницкая Э. Б., Андрющенко А. В., 1999а].
При выраженных аффективных расстройствах, а также при депрессиях с признаками резистентности к психофармакотерапии циталопрам назначается в сочетании с антидепрессантами других групп.
Наряду с тимолептическим, циталопрам обладает и соматотропным эффектом — обнаруживает антиноцицептивное действие при невропатиях диабетического происхождения [Дубницкая Э. Б., Андрющенко А. В., 1999а].
Показания к применению флуоксетина и циталопрам а расширяются за счет аффективных расстройств позднего возраста, в том числе сосудистых, постинсультных депрессий с преобладанием астении, растерянностью, насильственным плачем. Применение СИОЗС на протяжении первого года после инсульта достаточно безопасно и в 60-70 % случаев сопровождается редукцией аффективных расстройств [Wiart L et al, 2000].
Флуоксетин и циталопрам назначают в суточных дозах 20-40 мг. У лиц пожилого возраста необходимо очень медленно титровать дозу, причем эффективными могут оказаться вдвое меньшие, чем у лиц зрелого возраста, суточные количества препарата.
Существенные психофармакологические эффекты при воздействии на аффективные расстройства преимущественно энергического полюса обнаруживают антидепрессанты с двойным механизмом действия СИОЗСиН: милнаципран (иксел) и венлафаксин (эффексор).
В соответствии с результатами исследования, проведенного в клиническом отделе по изучению пограничных состояний и психосоматических расстройств НЦПЗ РАМН, совпадающими с данными других клинических центров (материалы мультицентрового исследования) [Аведисова А. С. и др., 2000] милнаципран (в дозах 50-150 мг/сут), обладая сбалансированным действием, наиболее эффективен при депрессиях с преобладанием астенических и адинамических расстройств. В процессе терапии редуцируются явления заторможенности, нарушения концентрации внимания, исчезают жалобы на потерю энергии, безразличие, усталость. Милнаципран в связи с отсутствием взаимодействия с другими рецепторными системами обладает благоприятным фармакологическим профилем, обеспечивая хорошую переносимость [Robert Ph., 2001]. Соответственно препарат может применяться при депрессиях, коморбидных с соматическими заболеваниями, а также у лиц пожилого возраста: милнаципран не обнаруживает существенного влияния на АД и показатели сердечного ритма [Leonard В., 2001].
Положительный эффект при лечении аффективных расстройств с преобладанием апатии, заторможенности и анергии наблюдается и при применении селективных ИМАО. В частности, это селективный ОИМАО-А моклобемид (аурорикс), отличающийся от традиционных ИМАО меньшей токсичностью. Клиническое действие препарата в дозе 300 мг/сут (для терапии резистентных депрессий используются значительно большие дозы — 450-600 мг/сут) обнаруживается на протяжении первых недель лечения. Наряду с характерным для ИМАО влиянием на негативную эффективность моклобемид эффективен при затяжных соматизированных депрессиях [Дробижев М. Ю. и др., 1993; Андрющенко А. В., Колесников Д. Б., 1998].
Депрессии типа Б2
Терапия атипичных депрессий, формирующихся путем присоединения психопатологических проявлений неэффективных регистров — депрессия с навязчивостями, с бредом, истерическая депрессия (см. разд. III, с. 47: депрессии типа Ба), требует использования комбинированных стратегий, выбор которых строится с учетом коморбидных соотношений собственно аффективных проявлений с расстройствами других регистров. Подробно этот аспект излагается ниже (см. с. 167, «Комбинированная психофармакотерапия»).
Читайте также:
