Примеры флюоресцентной ангиографии, гистологии солитарной врожденной гипертрофии пигментного эпителия сетчатки
Добавил пользователь Алексей Ф. Обновлено: 30.01.2026
Суть метода, в свойстве данного красителя – флуоресценции. Освещение голубым светом, имеющем длину волны примерно 490 нм, активирует молекулы флуоресцеина, которые начинают излучать волны иного спектра (примерно 530 нм), имеющие желто-зеленый цвет. В этот момент, специальной фундус-камерой фиксируются изображения глазного дна на разных этапах прохождения красителя по сосудам.
Флуоресцеин, попадая в крупные ретинальные, а также хориоидальные сосуды сетчатки, из-за эндотелия, который выстилает их изнутри, защищая сетчатую оболочку от токсинов и прочих активных веществ, не имеет возможности проникать в окружающие ткани. После крупных хориоидальных сосудов краситель попадает в капилляры, которые имеют тонкие стенки, перфорированные множеством отверстий (фенестрами), сквозь которые происходит обмен питательными веществами, а также продуктами жизнедеятельности с глубоко лежащими структурами сетчатки. Сквозь фенестры краситель попадает во внесосудистое пространство минуя мембрану Бруха. Дальнейшее его движение через ПЭС блокируется в норме плотным слоем клеток данной структуры.
Методика проведения
До проведения исследования, в глаз вносят капли, расширяющие зрачок. Пациента усаживают перед фундус-камерой и делают снимок глазного дна, который считается контрольным. Затем внутривенно болюсно вводят 5,0 мл раствора флуоресцеина (10%) и в течение 25-30с, практически ежесекундно выполняют фотографирование. Возможно выполнение и более поздних снимков при необходимости. После транзитной фазы, делают снимки сетчатки парного глаза.
Осложнения
При введении флуоресцеина, в ряде случаев могут наблюдаться следующие побочные действия и осложнения:
- Окраска кожных покровов (временная) в желто-коричневый цвет, видение объектов в красном цвете из-за фотовспышек, изменение цвета мочи.
- Тошнота и рвота, как правило преходящего характера, не нуждающаяся в терапии.
- Вазовагальные обмороки – не нуждаются в терапии, за исключением случаев резкой брадикардии, при которой требуется ввести атропин.
- Аллергические реакции: крапивница, гипотензия, бронхоспазм. Подобные состояния требуют введения супрастина, гидрокортизона, в ряде случаев адреналина, а также кислородной ингаляции.
- Остановка дыхания и сердечной деятельности при которых выполняется сердечно-легочная реанимация.
Показания к выполнению ФАГ
- Генетически обусловленные тапеторетинальные абиотрофии сетчатки (ТРА).
- Дистрофии сетчатки при преобладающих изменениях в макуле обусловленных нарушением кровообращения сосудисто-капиллярной пластинки (ВМД, центральная серозная ретинопатия).
- Диабетическая ретинопатия.
- Острые нарушения кровообращения сосудов сетчатки (тромбоз, эмболия центральной артерии или вены сетчатки, а также ее ветвей).
- Новообразования сосудистой оболочки (невус, меланоцитома, меланома, метастазирующие опухоли).
- Воспалительные процессы сосудистой и сетчатой оболочек.
- Изменения и поражения в диске зрительного нерва (псевдозастой, застойный диск, неврит).
Противопоказания к выполнению ФАГ
- Аллергические реакции (ангионевротический отек, крапивница, пирогенные реакции и пр.).
- Бронхиальная астма.
- Декомпенсация заболеваний сердечно-сосудистой системы.
- Болезни почек (острый или хронический гломерулонефрит в острой фазе, пиелонефрит, нефроптоз).
- Беременность (относительное противопоказание).
- При лактации нужно в течение четырех дней после проведения процедуры отказаться от кормления ребенка.
Оценка результатов
Интерпретацию феноменов флуоресценции производят основываясь на оценке гипофлуоресценции (низкой светимости) и гиперфлуоресценции (высокой светимости).
Примеры флюоресцентной ангиографии, гистологии солитарной врожденной гипертрофии пигментного эпителия сетчатки
Солитарная врожденная гипертрофия пигментного эпителия сетчатки: признаки, гистология, лечение, прогноз
Опухоли и схожие образования пигментного эпителия сетчатки включают в себя врожденную гипертрофию пигментного эпителия сетчатки (congenital hypertrophy of the retinal pigment epithelium - CHRPE), гиперпластические новообразования ПЭС, связанные с семейным аденоматозным полипозом (familial adenomatous polyposis - FAP), простую врожденную гамартому, макулопатию по типу «торпеды, комбинированную гамартому, псевдоканцерозную реактивную гиперплазию, доброкачественную эпителиому (аденому) и злокачественную эпителиому (аденокарциному). Врожденная гипертрофия ПЭС далее подразделяется на солитарный и мультифокальный варианты, последний также известен как врожденная очаговая пигментация или «медвежьи следы».
Солитарная врожденная гипертрофия ПЭС-широко известная аномалия глазного дна, которой в офтальмологической литературе уделяется много внимания (1-28). Хотя это состояние считается врожденным, средний возраст на момент постановки диагноза составляет 45 лет (1).
Поздняя диагностика, вероятно, обусловлена тем, что обычно эта аномалия протекает бессимптомно и локализуется на средней периферии или периферии глазного дна и при обычной офтальмоскопии может оставаться незамеченной. Как правило, она представляет собой солитарное новообразование; в отличие от невуса или меланомы хориоидеи (4), расовой предрасположенности не выявлено.
Термином врожденная гипертрофия пигментного эпителия сетчатки также обозначают несколько отличающиеся от описанных выше мультифокальные изменения глазного дна, часто сопутствующие семейному аденоматозному полипозу и раку толстой кишки (15,16); эту патологию мы обсудим ниже. Такую терминологию нельзя признать удачной, поскольку типичная солитарная врожденная гипертрофия ПЭС, очевидно, не связана с высокой частотой семейного аденоматозного полипоза или раковых опухолей желудочно-кишечного тракта (17).
а) Клиническая картина. В обзоре 330 случаев солитарной врожденной гипертрофии пигментного эпителия сетчатки представлено более подробное описание этого состояния (1). Клинически оно выглядит как четко отграниченная плоская или минимально проминирующая в стекловидное тело бляшка на глазном дне, от равномерно черной окраски до полностью беспигментной (1-28).
Как указывалось выше, большинство из этих аномалий локализуются на средней периферии или на периферии глазного дна. Только 2% из них развиваются в макулярной или перипапиллярной зоне. Новообразования в 88% случаев преимущественно пигментированные, в 12% случаев - непигментированные. Медиана максимального диаметра основания - 4,5 мм. В 43% случаев пигментированной врожденной гипертрофии ПЭС выявляются депигментированные очаги с четкими контурами, называемые лакунами. По краю большинства солитарных новообразований при врожденной гипертрофии ПЭС идет характерное беспигментное кольцо или «гало».
В 32% случаев в среднем через пять лет наблюдения отмечается увеличение лакун (1). В двух сериях наблюдений солитарной врожденной гиперплазии ПЭС при сроке наблюдения более пяти лет небольшое увеличение диаметра отмечалось в 74% и 83% случаев (1,3).
Касательно дифференциального диагноза, крупные новообразования, особенно на периферии глазного дна, могут быть очень похожи на меланому хориоидеи. При офтальмоскопии периферическое новообразование может субъективно создавать ложное впечатление значительно проминирующей в стекловидную полость опухоли.
В серии наблюдений из 330 случаев в 26% случаев диагноз направления был невус хориоидеи, в 15% случаев - меланома хориоидеи и в 48% случаев - неспецифическое новообразование глазного дна. Правильный диагноз врожденной гипертрофии ПЭС был поставлен в 9% случаев. Описанная в настоящей главе клиническая картина отличается от клинической картины невуса или меланомы и позволяет опытному врачу легко поставить диагноз клинически. В недавних публикациях, кроме того, описаны случаи роста узлового новообразования из очага солитарной врожденной гипертрофии ПЭС (18,19).
Частота развития и роста такого узлового новообразования в зоне врожденной гипертрофии ПЭС составляет, вероятно, около 1%. Постепенно у этих узловых новообразований появляются ретинальные сосуды-дренирующая вена и питающая артерия, развиваются желтые интрарегинальные экссудаты и экссудативная отслойка сетчатки (19). Эти изменения идентичны картине аденомы пигментного эпителия сетчатки, которую мы обсудим далее.
В одном случае была выполнена резекция глазной стенки, растущее амеланотическое узловое новообразование, развившееся из солитарной врожденной гипертрофии пигментного эпителия сетчатки, оказалось высокодифференцированной злокачественной эпителиомой (аденокарциномой) ПЭС (19). Эти опухоли описаны ниже в разделе, посвященном эпителиомам ПЭС.
СОЛИТАРНАЯ ВРОЖДЕННАЯ ГИПЕРТРОФИЯ ПИГМЕНТНОГО ЭПИТЕЛИЯ СЕТЧАТКИ: КЛИНИЧЕСКИЕ ВАРИАНТЫ
Отмечается значительная вариабельность окраски, размеров и формы очагов солитарной врожденной гипертрофии ПЭС.
Небольшой очаг солитарной врожденной гипертрофии пигментного эпителия сетчатки равномерной черной окраски у мужчины 54 лет. Более крупный очаг солитарной врожденной гипертрофии пигментного эпителия сетчатки у подростка 17 лет: отмечаются черная окраска центральной части новообразования и менее пигментированная периферическая зона. Очаг солитарной врожденной гипертрофии пигментного эпителия сетчатки у пациента 28 лет: определяются депигментированная лакуна и краевая светлая кайма. Образование имеет неправильную форму, но края у него ровные. Юкстапапиллярный очаг солитарной врожденной гипертрофии пигментного эпителия сетчатки у мужчины 40 лет: вид образования сходен с таковым периферического образования на рисунке выше. Это очень необычная локализация подобного очага. Очаг солитарной врожденной гипертрофии пигментного эпителия сетчатки возле экватора в нижнем квадранте у женщины средних лет. Обратите внимание на малозаметные лакуны в пределах новообразования. Крупный очаг солитарной врожденной гипертрофии пигментного эпителия сетчатки у пациента 17 лет, направленного для энуклеации в связи с подозрением на меланому хориоидеи. Однако была диагностирована врожденная гипертрофия ПЭС и от энуклеации решено воздержаться.
б) Диагностика. При флюоресцентной ангиографии и ангиографии с индоцианином зеленым обычно на протяжении всего исследования наблюдается экранирование флюоресценции. Также в течение всего исследования, как правило, отмечаются постоянная гипофлюоресценция пигментированных зон и флюоресценция хориоидеи сквозь зоны депигментации.
При ультразвуковом исследовании определяется новообразование толщиной около 0,5-1,0 мм, однако этот метод не имеет диагностического значения. Изменения поля зрения варьируют от небольшой относительной скотомы до абсолютного дефекта поля зрения, как правило, это зависит от размеров новообразования.
При оптической когерентной томографии определяются истончение покрывающей новообразование сетчатки, утрата фоторецепторов; на нижележащую хориоидею образование отбрасывает умеренно плотную относительную тень, однако диагностическое значение выявляемых изменений также невелико (5-9).
При исследовании аутофлюоресценции новообразование выглядит темным вследствие отсутствия липофусцина (10). Обычно это новообразование не выявляется при КТ и МРТ.
в) Патологическая анатомия. При гистологическом исследовании очага врожденной гипертрофии ПЭС определяются пигментные эпителиальные клетки, более высокие и более плотно упакованные сферическими меланосомами по сравнению с нормальными клетками ПЭС, содержащими мелкие несколько вытянутые меланосомы. Эти аномалии развиваются в результате комбинации клеточной гиперплазии и гипертрофии. Наблюдается атрофия вышележащих фоторецепторов (11, 12).
г) Лечение. Лечение солитарной врожденной гиперплазии ПЭС заключается в периодическом наблюдении. Если развивается небольшое узловое новообразование, зачастую оно также требует лишь наблюдения в течение некоторого периода времени, поскольку прогрессирует очень медленно и обычно не вызывает снижения зрительных функций.
Если такой узел сопровождается экссудацией или скоплением субретинальной жидкости, возможно проведение лазерокоагуляции или криотерапии. Если разрастающийся узел вызывает появление складок сетчатки и ретинопатию макулярной области, выполняется витрэктомия и пилинг мембран. Прогноз при врожденной гипертрофии пигментного эпителия сетчатки обычно благоприятный.
Клинические примеры солитарной врожденной гипертрофии пигментного эпителия сетчатки:
Редактор: Искандер Милевски. Дата публикации: 26.6.2020
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Мультифокальная врожденная гипертрофия пигментного эпителия сетчатки (ПЭС, медвежьи следы)
Мультифокальный вариант врожденной гипертрофии ПЭС также известен как врожденная очаговая групповая пигментация сетчатки или «медвежьи следы» (1-13). Обычно это ненаследуемое спорадическое состояние, но описан случай наличия этой аномалии у матери и у дочери (2).
Какая-либо другая сопутствующая патология глаз чаще всего отсутствует, но такие изменения описаны у пациентов с персистирующим гиперпластическим стекловидным телом на парном глазу (12), ретинобластомой, нейрофиброматозом и болезнью Коатса. Но, вероятно, такие сочетания случайны.
а) Клиническая картина. Мультифокальная врожденная гипертрофия пигментного эпителия сетчатки (ПЭС, медвежьи следы) характеризуется наличием нескольких групп четко отграниченных плоских лилово-серых очагов, обычно занимающих какой-либо сектор глазного дна.
Каждую группу образуют от трех до тридцати отдельных пигментированных очагов размером от 0,1 до 3 мм, более крупные очаги локализуются дальше к периферии. Каждый отдельный очаг очень похож на очаги, наблюдаемые при солитарной форме врожденной гипертрофии ПЭС, но, как правило, имеет меньшие размеры, чем при монофокальном типе, и не имеет ни светлых лакун, ни беспигментной каймы (гало). Иногда клинически эти очаги выглядят беспигментными, в таких случаях их называют «следами белого медведя» (1).
Типичные клинические признаки помогают дифференцировать эту патологию от других многочисленных состояний, сопровождающихся появлением на глазном дне множественных пигментированных очагов. При электрофизиологических исследованиях сетчатки пациентов с мультифокальной врожденной гипертрофией ПЭС патологических изменений не выявляется. Как правило, очаги остаются стабильными.
Как уже отмечалось выше, недавно была установлена тесная связь множественных мелких пигментированных новообразований глазного дна с семейным аденоматозным полипозом и синдромом Gardner-заболеваниями, характеризующимися семейным раком толстой кишки. Хотя эту аномалию глазного дна также относят к врожденной гипертрофии ПЭС, на самом деле она отличается от мультифокальной формы врожденной гипертрофии ПЭС тем, что такие новообразования двусторонние, более хаотично распределены по глазному дну и часто имеют более неровные или зазубренные края.
Как оказалось, связь между типичными формами врожденной гипертрофии ПЭС и упомянутыми синдромами рака отсутствует (4). Этот вопрос обсуждается ниже в отдельной статье на сайте.
МУЛЬТИФОКАЛЬНАЯ ВРОЖДЕННАЯ ГИПЕРТРОФИЯ ПИГМЕНТНОГО ЭПИТЕЛИЯ СЕТЧАТКИ
Мультифокальная врожденная гипертрофия ПЭС также известна как врожденная очаговая групповая пигментация сетчатки или «медвежьи следы». Не мультифокальные очаги гипертрофии клинически и гистологически идентичны солитарной врожденной гипертрофии ПЭС. Как и солитарная форма, групповые очаги могут быть пигментированными или беспигментными, но беспигментный вариант встречается реже. Часто эти очаги занимают сектор глазного дна, мелкие очаги локализуются ближе к диску зрительного нерва, а крупные - ближе к периферии глазного дна.
Типичная мультифокальная врожденная гипертрофия пигментного эпителия сетчатки у годовалого младенца. Беспигментная врожденная гипертрофия пигментного эпителия сетчатки у десятилетней девочки. Такие изменения иногда называют «следами белого медведя». Секторальная мультифокальная врожденная гипертрофия пигментного эпителия сетчатки у маленького мальчика. Семейный анамнез по раку толстой кишки не отягощен. Мультифокальная врожденная гипертрофия пигментного эпителия сетчатки у двухлетнего ребенка с ретинобластомой. На парном глазу наблюдались аналогичные изменения; после его энуклиации выполнено мофологическое исследование. Макросъемка пигментного эпителия сетчатки энуклеированного парного глаза того же пациента, что и на рисунке выше: отмечаются очаги гиперпигментации. При электронной микроскопии одного из очагов, показанных на рисунке выше, в цитоплазме клеток пигментного эпителия сетчатки определяются крупные, плотно упакованные меланосомы (х4000).
б) Диагностика. При флюоресцентной ангиографии наблюдается гипофлюоресценция. При ОКТ определяется плоский очаг с фокальной атрофией наружных слоев сетчатки (6, 7). При исследовании аутофлюоресценции глазного дна наблюдается гипоаутофлюоресценция этих очагов (8, 9).
в) Патологическая анатомия. Гистологические изменения при мультифокальной врожденной гипертрофии ПЭС очень похожи на картину изменений при солитарной врожденной гипертрофии ПЭС (10,11). Однако с помощью световой и электронной микроскопии установлено, что пигментные гранулы сохраняют свою нормальную эллипсоидную форму, а гипертрофия и гиперплазия не выражены (10, 11).
г) Лечение. Мультифокальная врожденная гипертрофия ПЭС не требует лечения и подлежит лишь наблюдению при плановых осмотрах у офтальмолога. Прогноз благоприятный.
© Н.Л.Маланова, И.Г.Терентьев, Т.А.Цыганова,
М.А.Мелехина, 2002 г.
УДК 617.7:543.542
Поступила 31.05.2002 г.
Н.Л.Маланова, И.Г.Терентьев, Т.А.Цыганова, М.А.Мелехина
Нижегородская государственная медицинская академия;
Областная клиническая больница им. Семашко, Нижний Новгород
Метод флюоресцентной ангиографии в офтальмологии
Флюоресцентная ангиография (ФАГ), предложенная в 1961 г. Novotny и Alvis, является ценной и информативной методикой для прижизненного исследования сосудов глазного дна. Сетчатку можно обследовать с помощью прямой и непрямой офтальмоскопии и биомикроскопии. Флюоресцентная ангиография является необходимым дополнением к этим клиническим методам исследования, предоставляя значительный объем дополнительной информации для диагностики и лечения патологических состояний сетчатки и зрительного нерва.
Метод ФАГ основан на способности флюоресцеина поглощать синий свет и излучать желто-зеленый. Этот краситель интенсивно флюоресцирует при нормальном значении pH крови (7,37—7,45). Он нетоксичен и достаточно безопасен для большинства пациентов. При поступлении флюоресцеина в кровь происходит поэтапное контрастирование сосудов, что можно зафиксировать фотографически. Для этой цели используются различные модели фундус-камер с высокой скоростью фотографирования. В нашей клинике применяется фундус-камера F450 ф. Zeiss. Контрастированные флюоресцеином сосуды на позитивных фотоснимках выглядят в виде светлых полос на фоне глазного дна, на негативах отношения обратные.
Исследование проводят следующим образом. До введения флюоресцеина делают несколько фотографий без фильтра, далее в синем свете производят контрольный снимок. После этого быстро вводят флюоресцеин (флюоресцеин-натрий 10%, 5,0 мл) в локтевую вену и через 5—7 с начинают серийную хронометрированную фотосъемку. Отдельные снимки делают с увеличением интервала. Возбуждающий (синий) и барьерный (желтый) светофильтры подбирают таким образом, чтобы они полностью поглощали все лучи, исходящие от источника возбуждения. По мере поступления вещества в сосудистое русло (время попадания флюоресцеина из вены в сосуды глаза составляет обычно 12—15 с) красителем заполняются собственно сосудистая оболочка и хориокапилляры. Это первая, преартериальная, фаза ангиограмм.
Пигментный эпителий сетчатки непроницаем для флюоресцеина, и краситель далее поэтапно поступает в артериальное русло (артериальная фаза), в капилляры и вены (артериовенозная и венозная фазы).
Венозная фаза продолжается до заполнения красителем вен. За этой фазой после первого прохождения через сосуды почек происходит возвращение крови, содержащей флюоресцеин, вновь в сосуды сетчатки. Это фаза рециркуляции. Концентрация красителя в крови уже значительно ниже, чем в предыдущие, поэтому фаза рециркуляции имеет большую диагностическую ценность. В течение 24 ч у пациентов с нормальной почечной фильтрацией флюоресцеин практически полностью элиминируется из кровяного русла. При этом наблюдается окрашивание склер и мочи.
Основной клинический симптом, выявляемый с помощью ФАГ, — патологическая флюоресценция. Требуется только оценить характер этих изменений (гипо– или гиперфлюоресценция) и их локализацию.
Гиперфлюоресценция чаще связана с патологическими процессами в пигментном эпителии сетчатки, что приводит к просачиванию красителя в сетчатку или субретинально либо флюоресценция видна сквозь пигментный эпителий. Описанные изменения могут наблюдаться при центральной серозной хориопатии, при наличии новообразованных сосудов (диабетическая ретинопатия, неопластический процесс, болезнь Коатса и др.), при дистрофиях пигментного эпителия.
Гипофлюоресценция проявляется полной или частичной блокадой свечения флюоресцирующих в норме структур. Так, например, блокада флюоресценции может быть связана со скоплением пигмента (невусы хориоидеи), со скоплением экссудата при нарушениях проходимости сосудов сетчатки (центральной вены сетчатки, центральной артерии сетчатки или их ветвей).
Очень информативна ФАГ при патологических состояниях зрительного нерва. Характерна ангиографическая картина при друзах зрительного нерва (друзы флюоресцируют еще до введения красителя — псевдофлюоресценция). Хорошо выявляется на ангиограммах отек диска зрительного нерва, как изолированный, так и в сочетании с воспалительным компонентом. Однако выявляемая картина гиперфлюоресценции неспецифична и должна оцениваться лишь в комплексе с офтальмоскопическими изменениями.
Особо ценной является возможность дифференциальной диагностики регматогенных и вторичных отслоек сетчатки и невусов хориоидеи. У пациентов с внутриглазными опухолями на флюоресцентных ангиограммах в раннюю преартериальную фазу выявляются собственные сосуды опухоли, при этом сосудистый рисунок резко отличается от сосудистого рисунка сетчатки над очагом. В раннюю артериальную фазу флюоресцеин интенсивно проходит из сосудов в опухоль и длительно задерживается опухолевым узлом в поздней фазе.
Если же отслойка сетчатки имеет регматогенный или экссудативный характер, флюоресцеин локально накапливается под пигментным эпителием в месте скопления субретинальной жидкости в виде полости.
При невусах хориоидеи картина ФАГ может быть вариабельна — от разной степени выраженности блокады хориоидальной флюоресценции с нечетко очерченными краями до гиперфлюоресценции за счет пропотевания красителя из очагов вторичных изменений сетчатки над невусом (кистозные изменения, друзы). Контрастированные сосуды сетчатки при этом не изменены. Нередко наблюдается и нормальная ангиографическая картина.
Полученные результаты заносятся в компьютеризированную систему архивирования, что позволяет оперативно и с высокой степенью точности проводить динамическое наблюдение за пациентами, что особенно важно при росте невусов, после органосохранного лечения меланом хориоиде, для контрольных осмотров при диабетической ретинопатии.
Таким образом, флюоресцентная ангиография сетчатки является ценным дополнительным методом исследования, значительно расширяющим возможности дифференциальной диагностики различных состояний глазного дна.
"Медикум"
новый научно-практический медицинский журнал, который будет издаваться на 2-х языках: русском и английском, в трех формах выпуска: печатная, интернет-версия, CD-версия.
Врождённая гипертрофия пигментного эпителия сетчатки ("след медведя")
При врожденной гипертрофии пигментного эпителия сетчатки речь идет о нарушении формирования этого слоя в период внутриутробной жизни. Проявляется заболевание сгруппированной пигментацией, которая имеет внешнее сходство со следом медведя.
До конца патогенез гипертрофии сетчатки не изучен. Некоторые ученые полагают, что в результате формирования в патологической сетчатке макромеланосом происходит изменение катаболической функции. В результате клетки пигментного эпителия погибают, а на их месте формируются лакуны, или очаги гипогигментации.
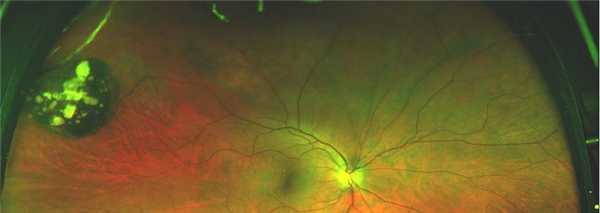
Клинические проявления гипертрофии
При врожденной гиперплазии пигментного слоя сетчатки возникает очаговая гиперпигментация. По своей форме очаги гиперпигментации напоминают медвежий след. Окраска этих пятен может быть светло-коричневой или черной. Форма пятен округлая, а края гладкие или фестончатые. Вокруг очагов гиперпигментации можно обнаружить довольно обширную плакоидную область. Лакуны, формирующиеся при гиперплазии, могут носить одиночный или множественный характер. Сгруппированные очаги гиперпигментации (маленькие пучки или скопления) называют следом медведя. Размер этих скоплений может быть с маленький диск, а иногда достигает целого квадранта глазного дна. Типичной локализации для этих патологических изменений не выявлено. Центральная область сетчатки, то есть макула, довольно редко вовлекается в патологический процесс.
Заболевание может протекать бессимптомно. Иногда очаги гиперплазии увеличиваются в размерах или озлокачествляются. При выполнении флуоресцентной ангиографии на ранних стадиях патологий можно рассмотреть крупные сосуды хориоидальной оболочки, которые пересекают лакуны. При этом слой хориокапилляров отсутствует. На всем протяжении гипертрофированного участка можно выявить гипофлуоресценцию.
Диагностика
Световая микроскопия
Слой гипертрофированного пигментного эпителия представляет собой большие пигментные гранулы овальной формы. Фоторецепторы, которые прилежат к этой зоне, подвергаются дистрофии (наружные и внутренние сегменты). Также имеется утоление мембраны Бруха, а в лакунах с гипопигментацией отсутствуют фоторецепторы и пигментные эпителиальные клетки. Сосудистая оболочка при этом заболевании не изменена.
Инструментальные исследования
Во время выполнения флуоресцентной ангиографии в зоне гиперпигментации можно заметить блокаду фоновой флуоресценции хориоидеи. В гипопигментированных лакунах хориоидальный кровоток сохранен. Сеть сосудов, которая покрывает очаг изменения, невидима. Иногда имеются признаки облитерации капилляров, микроаневризм, сосудистых шунтов, отмечается разреженность структур, флуоресцеин может просачиваться.
При исследовании поля зрения могут возникать относительные скотомы, которые увеличиваются с возрастом. ЭОГ и ЭРГ сохраняются в норме.
Дифференциальная диагностика
Следует отличать врожденную гипертрофию пигментного эпителиального слоя сетчатки от меланомы, невуса хориоидеи, меланоцитомы. Также дифференциальную диагностику нужно проводить с реактивной гиперплазией этого слоя сетчатки, которая возникает в результате травмы, кровоизлияния, воспаления или приема токсических веществ.
Лечение
Лечения этого заболевания не проводят.
Прогноз
При отсутствии патологических изменений в зоне макулы снижения остроты зрения не отмечается.
Читайте также:
