Примеры флюоресцентной ангиографии метастазов в хориоидею
Добавил пользователь Евгений Кузнецов Обновлено: 29.01.2026
Флюоресцентная ангиография (ФАГ) широко используется в современной офтальмологии для диагностики сосудистой патологии сетчатки более 40 лет и утвердилась в качестве стандартного метода обследования [1,5]. Из-за доступности новых методов лечения патологии сетчатки, в частности, хориоидальной неоваскуляризации (ХНВ), количество ангиографических исследований, выполняемых в специализированных центрах, выросло более чем в два раза. В свою очередь это усилило интерес к методу ФАГ, поскольку современные стратегии лечения и принятие решений о вмешательствах, как правило, основываются на использовании именно этого метода, являющегося «золотым стандартом» для классификации ХНВ, в соответствии с исследованием по лазеркоагуляции макулы (Macular Photocoagulation Study).
Несмотря на постоянное усовершенствование и внедрение различных современных и методов диагностики, в НУЗ «Центральная поликлиника» ОАО «РЖД» ФАГ ранее не применялась. Пациентам, нуждающимся в проведении ФАГ, обследование проводилось в специализированных глазных центрах с задержкой, в связи с чем они получали лечение несвоевременно или эмпирически.
ФАГ является минимально инвазионной процедурой, позволяет улучшить видимость мелких сосудов, а также оценить кровообращение в сосудистом ложе сетчатки и хориоидеи в целом. Кроме того, метод позволяет детально оценить размеры, локализацию, положение и тип (скрытый или классический) ХНВ.
В последние годы с появлением anti-VEGF терапии (ингибитора сосудистого эндотелиального фактора роста) метод стал применяться для лечения всех типов неоваскуляризаций и некоторые клиники стали пренебрегать проведением ФАГ, ограничиваясь в диагностике ХНВ только оптической когерентной томографией (ОКТ). Специалисты единогласны в мнении, что эти два исследования обеспечивают комплементарную информацию, и анатомические данные, полученные ОКТ, должны быть подтверждены доказательством, что активное просачивание существует и это может быть обеспечено только ФAГ [2,11].
ОКТ представляет собой неинвазивный метод обследования, имеющий отчетливое преимущество перед флюоресцентной ангиографией в отношении интерпретации патологии зоны витреоретинального контакта, а также для качественных и полуколичественных исследований макулярного отека в динамике. Но она не может заменить флюоресцентную ангиографию при принятии решения о лечении при трех наиболее распространенных заболеваний макулы, встречающихся в повседневной практике: возрастной макулярной дегенерации, диабетическом макулярном отеке и окклюзиях вен сетчатки.
Если не принимать во внимание появление цифровой фотографии, технические особенности флюоресцентной ангиографии остались в основном теми же, которые были описаны в самых первых публикациях [3,4]. При флюоресцентной ангиографии флюоресцирующее вещество вводится внутривенно; через короткий промежуток времени оно распространяется посредством кровотока по хориоидее и сосудам сетчатки [7]. Стимулирующий свет проникает в глаз через барьерный фильтр, а затем, как результат флюоресценции вещества, происходит излучение света, который можно сфотографировать, и/ или произвести его видеорегистрацию.
Из-за сравнительной безопасности процедуры и сложившейся тенденции неверного использования ангиографии в качестве метода документирования течения болезни в последние годы к флюоресцентной ангиографии стали прибегать неоправданно часто. Как и все прочие диагностические процедуры, флюоресцентная ангиография используется для установления диагноза, для определения необходимости лечения или для контроля динамики отдельных заболеваний. Несмотря на хорошую переносимость и высокий уровень безопасности флюоресцентная ангиография до сих пор является инвазивным методом, который потенциально может привести к серьезным побочным действиям. Поэтому следует избегать проведения ангиографии при отсутствии показаний к ней.
Ангиографию не следует проводить, если диагноз может быть поставлен и без нее, или если процедура не повлечет за собой никаких изменений в тактике лечения.
Ангиография также не показана в качестве «рутинного метода» контроля или только для целей документирования, например, при диабетическом макулярном отеке или макулярной дегенерации.
Ангиография часто назначается необоснованно, в частности, при заболеваниях, входящих в следующие группы:
- при возрастной макулярной дегенерации с бесспорным клиническим диагнозом без ожидаемых изменений в тактике лечения.;
- при диабетической ретинопатии для диагностики клинически выраженного макулярного отека или в качестве «рутинного контроля» [9];
- при необъяснимой потере остроты зрения в клинически нормальном состоянии макулы. В этом случае от ангиографии не следует ожидать какойлибо дополнительной информации;
- при меланоме хориоидеи. Ангиография в случаях подозрения на меланому хориоидеи предоставляет мало дополнительной информации;
- при окклюзии сосудов сетчатки; обычно диагноз установлен без ангиографии. Бесспорные заключения относительно характера лечения могут быть сделаны только в случаях окклюзии вен, и то лишь через несколько месяцев после окклюзии этих сосудов. До сих пор спорной является возможность установления с помощью ангиографии необходимости проведения панретинальной лазерной коагуляции при окклюзии вен сетчатки;
- при наследственных дистрофиях сетчатки. Исследование аутофлюоресценции глазного дна, как правило, предоставляет достаточно полную информацию даже раньше и подробнее, чем флюоресцентная ангиография, которая обоснована лишь в тех случаях, когда есть подозрения на наличие экссудативных осложнений.
Исследования в области оценки аутофлюоресценции глазного дна в последнее время продемонстрировали преимущество этой простой и неинвазивной технологии получения изображения при неэкссудативных поражениях глазного дна. Исследование аутофлюоресценции глазного дна отражает метаболическое состояние пигментного эпителия сетчатки (ПЭС), а также, кроме выявления поражений ПЭС, этот метод способствует визуализации участков, где происходят активные дегенеративные процессы. Анализ феномена аутофлюоресценции на глазном дне обещает стать одним из методов повседневной клинической практики, в частности, при неэкссудативной возрастной макулярной дегенерации, а также для раннего обнаружения наследственной и приобретенной дегенерации сетчатки. Основное преимущество данного метода заключается в раннем выявлении морфологических изменений, в то время как результаты офтальмоскопии все еще остаются нормальными [8]. В принципе, исследование аутофлюоресценции глазного дна может заменить инвазивную флюоресцентную ангиографию при всех неэкссудативных патологических процессах в сетчатке [10]. Аутофлюоресценция глазного дна может предоставить больший объем информации, чем флюоресцентная ангиография, и в некоторых случаях данный метод является единственным способом обнаружения морфологических поражений (например, при макулодистрофии, хлорохиновой ретинопатии), облегчая раннюю диагностику заболеваний сетчатки. Неинвазивность этого метода дает ему ощутимое преимущество перед флюоресцентной ангиографией, но для доказательства его ценности в клинической практике с целью принятия решения о лечении должны быть проведены более широкие клинические исследования.
Таким образом, ФАГ является источником уникальной информации, позволяет визуализировать ретинальную сосудистую сеть в мельчайших подробностях, детально изучить циркуляцию крови в структурах глазного дна и определить целостность гематоретинального барьера [6], что делает ФАГ незаменимым исследованием в офтальмологии.
Примеры флюоресцентной ангиографии метастазов в хориоидею
Метастатические опухоли сосудистой оболочки глаза, сетчатки и диска зрительного нерва
Метастатический рак, вероятно, является наиболее часто встречающейся интраокулярной злокачественной опухолью. По проблеме метастатического поражения внутриглазных структур опубликованы результаты многочисленных больших серий наблюдений, обзоры и клинические случаи, в настоящей статье мы цитируем лишь некоторые из них (1-53). Несмотря на то, что метастазы в сосудистой оболочке - наиболее часто встречающееся злокачественное внутриглазное новообразование, в практике офтальмоонколога эта патология встречается реже, чем меланома сосудистой оболочки, вероятно, потому, что у многих из этих больных уже имеется далеко зашедшее системное раковое поражение и такие больные не попадают в поле зрения офтальмолога.
Метастазы рака достигают интраокулярные структуры гематогенным путем и чаще всего поражают сосудистую оболочку, >90% из них локализуется в задней части хориоидеи, а
Чаще всего встречаются внутриглазные метастазы рака, метастазы сарком и меланом наблюдаются реже. Большинство метастазов в сосудистой оболочке - это метастазы рака молочной железы у женщин и метастазы легких у мужчин. Реже в роли первичной опухоли выступает рак желудочно-кишечного тракта, почек, щитовидной железы, поджелудочной железы, предстательной железы и других органов. Иногда в сосудистую оболочку метастазируют меланома кожи и карциноидные опухоли легких, такие поражения имеют характерные отличительные признаки.
Из всех пациентов, попадающих на прием к офтальмологу с метастазами в сосудистой оболочке, примерно у 25-30% в анамнезе отсутствуют сведения о системном раковом поражении (1). В ходе последующего системного обследования примерно у 17% пациентов первичную раковою опухоль выявить не удается, и она остается неустановленной (1). Поэтому клиницисту необходимо знать клинические проявления внутриглазного метастатического поражения.
а) Клиническая картина. Клиническая картина внутриглазных метастазов варьирует в зависимости от локализации опухоли (1-53). Проявления метастазов в радужке отличаются разнообразием (4,5). Они могут представлять собой единичные или множественные узелки в строме радужки желтого, белого или розового цвета. Они могут выглядеть как одна или несколько четко отграниченных опухолей или иметь рыхлую структуру и давать отсевы клеток в водянистую влагу, формируя картину внутриглазного воспаления и опухолевый псевдогипопион. Метастазы в цилиарном теле зачастую бывает сложно обнаружить клинически. Они могут выглядеть как солитарное объемное образование или вызывать симптомы воспаления, симулируя иридоциклит.
Метастазы хориоидеи обычно выглядят как одно или несколько желтых образований на глазном дне одного или обоих глаз. Отмечается предрасположенность к поражению задней части хориоидеи, часто метастазы локализуются в макулярной области. В отличие от метастазов в радужке и цилиарном теле, метастазы хориоидеи, как правило, не вызывают выраженных симптомов воспаления, но обычно сопровождаются вялотекущей вторичной отслойкой сетчатки. Хотя метастазы хориоидеи обычно имеют желтую окраску, метастазы меланомы зачастую имеют серый или коричневый цвет, а метастазы карциноидной опухоли, рака щитовидной железы и почечноклеточного рака часто бывают оранжевого цвета. Метастазы в сетчатке, встречающиеся крайне редко, могут симулировать окклюзивный васкулит и давать отсевы клеток в стекловидное тело.
Метастазы в стекловидном теле также встречаются редко и, вероятно, развиваются из поражений сетчатки. Обычно они проявляют себя появлением опухолевых клеток в стекловидном теле, что напоминает первичный воспалительный процесс или первичную лимфому. Метастатические поражения диска зрительного нерва могут развиваться вследствие разрастания юкстапапиллярных метастазов в хориоидее или же могут представлять собой изолированное поражение зрительного нерва; в последнем случае диск зрительного нерва пораженного глаза выступает в стекловидную полость (6). Часто развивается вторичная глаукома, особенно при опухолях радужки и цилиарного тела.
Метастазы рака легких в радужке с кровоизлиянием и вторичной гифемой. Метастаз карциноидной опухоли бронха в радужке: наблюдается характерная «мясная» розово-оранжевая окраска. Множественные метастазы мелкоклеточного рака легкого в радужке у женщины 78 лет. Тот же глаз, показанный на рисунке выше, после внешнего облучения: наблюдается регресс опухолей. Узловой метастаз рака желудка с псевдогипопионом, образовавшимся вследствие дисперсии клеток основной опухоли. Метастаз саркомы Юинга бедра в радужке у пациентки 19 лет. Отмечаются многочисленные опухолевые узелки на поверхности радужки и рыхлая опухоль, создающая картину «псевдогипопиона» в нижней части передней камеры.
МЕТАСТАЗЫ В ХОРИОИДЕЕ НЕВЫЯВЛЕННЫХ ПЕРВИЧНЫХ ОПУХОЛЕЙ, ДИАГНОСТИРОВАННЫЕ С ПОМОЩЬЮ ТОНКОИГОЛЬНОЙ АСПИРАЦИОННОЙ БИОПСИИ
Иногда у больного обнаруживают новообразование сосудистой оболочки, по своей картине соответствующее метастазу, но в результате системного обследования первичную опухоль выявить не удается, данные о раке в анамнезе больного также отсутствуют, и для подтверждения диагноза метастаза выполняется тонкоигольная аспирационная биопсия. В некоторых случаях на локализацию первичной опухоли могут указывать характерные цитопатологические признаки или результаты иммуногистохимического исследования. Однако у других пациентов цитопатологическое исследование подтверждает диагноз метастатического поражения, но локализация первичной опухоли так и остается неизвестной. Ниже проиллюстрировано несколько случаев, в каждом из которых диагноз ставился на основании цитопатологического исследования материала, полученного при тонкоигольной аспирационной биопсии, но первичная опухоль так и не была выявлена.
Метастаз в хориоидее кверху от диска зрительного нерва. Метастаз в хориоидее в макулярной зоне. Метастаз в хориоидее кверху от диска зрительного нерва. Метастаз в хориоидею макулярной зоны. Метастаз в хориоидее снизу от диска зрительного нерва с фиброзной метаплазией пигментного эпителия сетчатки. Метастаз в хориоидее, окружающий и прорастающий диск зрительного нерва.
б) Диагностика. Диагностика внутриглазных метастазов обычно включает в себя сбор анамнеза о ранее существовавших раковых опухолях и тщательную биомикроскопию на щелевой лампе и офтальмоскопию. Диагностике помогают дополнительные методы исследования, такие, как флюоресцентная ангиография и ультразвуковое исследование. При флюоресцентной ангиографии гиперфлюоресценция метастазов в хориоидее, как правило, начинается в позднюю венозную фазу, обычно позже, чем гиперфлюоресценция меланомы или гемангиомы хориоидеи. При ультразвуковом A-сканировании обычно отмечается высокая эхогенность ткани метастаза, а при В-сканировании - акустическая плотность образования; такая же картина наблюдается при гемангиоме хориоидеи. В редких случаях метастаз в хориоидее может принимать грибовидную форму, аналогично меланоме хориоидеи (19).
Оптическая когерентная томография с увеличенной глубиной сканирования (enhanced depth imaging optical coherence tomography-EDI-OCT) - новый метод, позволяющий выявлять субклинические метастазы глазного яблока, оценивать топографию поверхности опухоли и ее инвазивность. При ОКТ с увеличенной глубиной сканирования в большинстве случаев наблюдается сдавление мелкими хориоидальными метастазами слоя хориокапилляров, при этом новообразование имеет контур типа «кочек и ухабов». Также отмечается утрата фоторецепторов и скопление субретинальной жидкости (21). В сложных случаях, когда с помощью перечисленных выше методов обследования не удается поставить диагноз, выполняется тонкоигольная биопсия с цитологическим исследованием аспирированного материала (17).
в) Патологическая анатомия. В большинстве случаев диагноз внутриглазного метастаза ставится клинически, забор ткани для гистологического исследования не выполняется. Однако метастазы в сосудистой оболочке формируют классическую макроскопическую и микроскопическую картину. При макроскопическом исследовании эти злокачественные новообразования обычно имеют белую или желтую окраску, они могут быть диффузными или узловыми и иметь широкое основание. Гистологическое строение метастазов в сосудистой оболочке варьирует в широких пределах, оно зависит от типа и локализации первичной опухоли и степени ее дифференцировки (1-3).
Иногда опухоль настолько низко дифференцирована, что при исследовании тканей глаза локализацию первичной опухоли определить трудно. В таких случаях некоторую помощь в классификации новообразования и определении локализации первичной опухоли оказывает иммуногистохимическое исследование.
г) Лечение. Способы лечения при метастазах в сосудистой оболочке различаются в зависимости от клинической ситуации (1-8, 22-25). Мелкие бессимптомные опухоли или образования, реагирующие на проведенную ранее или проводимую во время выявления метастаза химиотерапию, могут не требовать немедленного лечения и подлежат лишь периодическому наблюдению. По поводу более крупных вызывающих жалобы опухолей проводится внешнее облучение или брахитерапия с применением аппликатора. Недавно был описан прекрасный эффект фотодинамической терапии при лечении мелких метастазов в задней части хориоидеи. Фотодинамическая терапия длится всего несколько минут, тогда как любая методика лучевой терапии требует гораздо больше времени (22, 24).
Системный прогноз зависит от типа опухоли. У больных с метастазами рака молочной железы в хориоидею прогноз зачастую более благоприятный, тогда как метастазы рака легких или меланомы характеризуются значительно худшим прогнозом. У пациентов с метастазами карциноидной опухоли прогноз зачастую гораздо более благоприятный, так как метастатические очаги этой опухоли могут оставаться относительно стабильными в течение месяцев или лет (1).
Клинические примеры метастатических опухолей сосудистой оболочки глаза, сетчатки и диска зрительного нерва:
Редактор: Искандер Милевски. Дата публикации: 11.6.2020
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
ФГБУ «Московский НИИ глазных болезней им. Гельмгольца» Минздрава России, Москва
ФГБУ "Московский НИИ глазных болезней им. Гельмгольца" Минздрава РФ
ФГБУ Московский научно-исследовательский институт глазных болезней им. Гельмгольца Минздрава РФ, Москва
Метастатическая карцинома хориоидеи: два клинических случая
Журнал: Вестник офтальмологии. 2013;129(2): 56‑60
Саакян С.В., Мякошина Е.Б., Юровская Н.Н., Рябина М.В. Метастатическая карцинома хориоидеи: два клинических случая. Вестник офтальмологии. 2013;129(2):56‑60.
Saakian SV, Miakoshina EB, Iurovskaia NN, Riabina MV. Metastatic choroidal carcinoma. Two clinical cases.. Vestnik Oftalmologii. 2013;129(2):56‑60. (In Russ.).
Представленные клинические случаи показывают значимость современных методов диагностики (флюоресцентной ангиографии и спектральной оптической когерентной томографии) в установлении в одном наблюдении и опровержении в другом метастатической карциномы хориоидеи с назначением адекватной терапии.
В последние годы появились сведения об увеличении частоты встречаемости внутриглазных метастазов до 67% [1]. Источником метастазирования могут быть опухоли любой локализации, но более 50% приходится на рак грудной железы и легкого [2, 4]. По данным литературы, у 12% больных при первом осмотре у офтальмолога отсутствовал онкологический анамнез [1], а у 3,3% так и не удалось выявить первичный опухолевый узел [2]. По результатам обращаемости больных в отдел офтальмоонкологии и радиологии ФГБУ «МНИИ глазных болезней им. Гельмгольца» среди всех внутриглазных новообразований на долю метастатических карцином хориоидеи приходится 11%.
В настоящее время существующие высокотехнологичные методы диагностики внутриглазных опухолей позволяют выявить ранние диагностические признаки метастатической карциномы хориоидеи [1, 3, 5, 7—10]. К таким методам относятся флюоресцентная ангиография, дающая возможность выявить признаки нарушения наружного и внутреннего гематоофтальмического барьера, проявляющиеся зонами гипер- и гипофлюоресценции [1, 5, 7], и спектральная оптическая когерентная томография (СОКТ), позволяющая провести прижизненную патоморфометрическую оценку сетчатки, хориоидеи и стекловидного тела с трехмерной визуализацией объекта [3, 6, 7—9]. Своевременное установление или опровержение диагноза увеального метастаза не только изменяет качество жизни больного, но и улучшает витальный прогноз.
Материал и методы
В настоящей статье представлены два клинических случая, в одном из которых демонстрируется установление диагноза метастатической карциномы, во втором — его опровержение с использованием комплекса современных диагностических исследований.
1. Пациенту К., 58 лет, в 2004 г. по месту жительства установили диагноз саркома Капоши — генерализованная форма с поражением кожи верхних и нижних конечностей, после чего проводилось комбинированное лечение, включающее системную полихимиотерапию (3 курса) и локальное лазерное лечение. Последний курс полихимиотерапии закончили в марте 2011 г.
В октябре 2011 г. появились жалобы на темное пятно перед левым глазом и пациент направлен в ФГБУ «МНИИ ГБ им. Гельмгольца» Минздрава РФ с диагнозом метастатическая карцинома хориоидеи левого глаза.
OD = 0,3 c sph +1,75 cyl +1,25 ax 170 гр = 0,7,
OS = 0,03 c sph +2,0 cyl +2,5 ax 15 гр = 0,3.
Внутриглазное давление: OU = 17 мм рт.ст.
Компьютерная периметрия: OD — скотом не выявлено, OS — несколько центральных относительных скотом в поле зрения.
Биомикроскопия: OU — передний отрезок не изменен, оптические среды прозрачны.
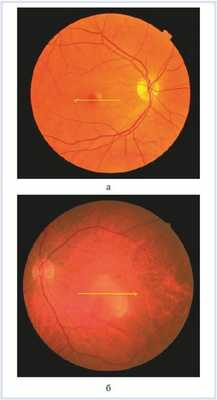
Офтальмоскопия: OD — в центральной зоне глазного дна единичные мелкие просовидные очажки округлой формы. На периферии очаговой патологии не выявлено (рис. 1, а). Рисунок 1. Офтальмоскопия друз (а) и проминирующего очага (б). Здесь и на рис. 4, а, б: желтой стрелкой указана зона глазного дна, на уровне которой проведен томографический срез методом СОКТ.
OS — в макулярной зоне в 1,5 pupilla diametr (PD) от диска зрительного нерва по меридианам с 14 до 16 ч определялся проминирующий желтый беспигментный очаг с гладкой поверхностью, нечеткими неровными границами, размером 2×2 PD (см. рис. 1, б).
Ультразвуковая эхография: OD — зон проминенции не выявлено.
OS — элевация опухоли — 1,1 мм, диаметр основания — 2,9 мм.
Для уточненной дифференциальной диагностики проведены флюоресцентная ангиография и спектральная оптическая когерентная томография.
Флюоресцентная ангиография: OD в венозную фазу — несколько мелких гиперфлюоресцирующих округлых фокусов (друзы).

OS — в макулярной зоне выраженная гипофлюоресценция очага с четкими границами, окруженная обширной зоной гиперфлюоресценции (отслойка нейроэпителия — НЭ). В парамакулярных зонах — очаги гипофлюоресценции (микроотслойки ретинального пигментного эпителия — РПЭ) и множественные мелкие гиперфлюоресцирующие округлые очаги (сливные друзы) (рис. 2). Рисунок 2. Флюоресцентная ангиография поздней стадии возрастной макулярной дегенерации, проявляющейся проминирующим очагом (объяснения в тексте).

Спектральная оптическая когерентная томография: OD — в макулярной зоне множественные отслойки РПЭ (рис. 3, а). Рисунок 3. СОКТ друз (а) и поздней стадии возрастной макулярной дегенерации, проявляющейся проминирующим очагом (б). Красная стрелка — отслойка РПЭ; синяя стрелка — отслойка НЭ; зеленая стрелка — ровный профиль мембраны Бруха (объяснения в тексте).
OS — в макулярной зоне высокая волнообразная отслойка РПЭ с отслойкой НЭ в сопредельных зонах, ровный профиль мембраны Бруха (см. рис. 3, б).
На основании совокупности результатов проведенных исследований диагностирована бинокулярная возрастная макулярная дегенерация (ранняя стадия — OD, поздняя стадия — OS).
Больному назначена анти-VEGF-терапия по месту жительства.
2. Пациентке Г., 39 лет, в 2010 г. по месту жительства установили диагноз рак молочной железы слева. Проведена радикальная мастэктомия с последующей системной химиотерапией, гормонотерапией и лучевой терапией. Комбинированное лечение закончила в сентябре 2011 г.
В январе 2012 г. появились жалобы на снижение зрения левого глаза и пациентка направлена в ФГБУ «МНИИ ГБ им. Гельмгольца» Минздрава РФ с диагнозом метастатическая карцинома хориоидеи левого глаза.
Внутриглазное давление: OD = 14 мм рт.ст., OS = 15 мм рт.ст.
Офтальмоскопия: OD — норма.
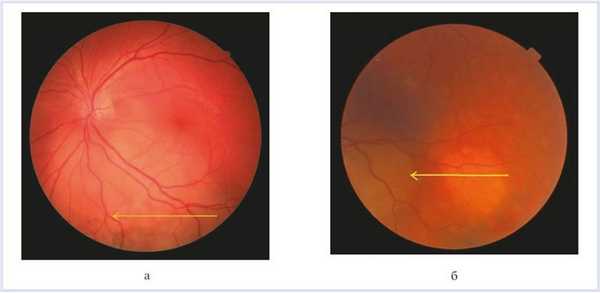
OS — макулярно и парамакулярно в 1,5 PD от диска зрительного нерва по меридианам с 14.30 до 20.30 часов определялся проминирующий желтый слабопигментированный очаг с бугристой поверхностью, нечеткими неровными границами, размером 4×5 PD (рис. 4, а). Рисунок 4. Офтальмоскопия юкстапапиллярного очага (а) и малого фокуса (б). Кнаружи от основного фокуса диагностирован слегка проминирующий очаг желто-коричневого цвета, с нечеткими неровными границами, с бугристой поверхностью (см. рис. 4, б).
OS — элевация опухоли — 2,0 мм, диаметр основания — 11,0 мм.
Флюоресцентная ангиография:
OS — в ранние фазы исследования определяется зона гипофлюоресценции в центральном отделе очага, в ранние венозные фазы — ангиопатия сосудов сетчатки, в средние венозные фазы — гиперфлюоресценция по периферии фокуса с формированием симптома «россыпи крупы», сохраняющегося до поздних фаз исследования.
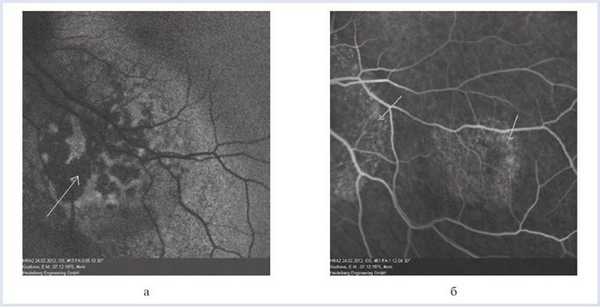
В зоне наружного очага — симптом «россыпи крупы», сохраняющийся до поздних фаз исследования (рис. 5). Рисунок 5. Флюоресцентная ангиография метастатической карциномы хориоидеи. Гипофлюоресценция в ранние фазы исследования — белая стрелка (а); «россыпь крупы» (стрелки) юкстапапиллярного очага и малого фокуса (б).
Спектральная оптическая когерентная томография:
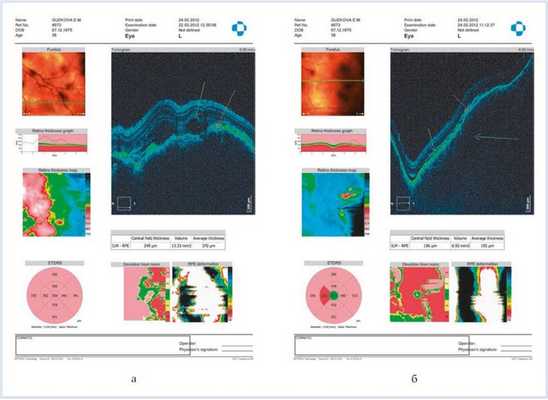
OS — над очагами мелко- и крупнобугристое изменение хориоидального профиля, ретиношизис, мелкие и крупные гиперрефлективные депозиты в слое нейроэпителия, сохранение анатомо-топографической структуры хориокапилляров. На уровне больших сосудов хориоидеи визуализируется низкорефлективная полоса, передняя и задняя границы очага, а также мелкие округлые гиперрефлективные включения во внутренних слоях хориоидеи (рис. 6). Рисунок 6. СОКТ метастатической карциномы хориоидеи юкстапапиллярного очага (а) и малого фокуса (б). Красная стрелка — мелкобугристое изменение хориоидального профиля; зеленая стрелка — интраретинальные депозиты; синяя стрелка — хориоидальный очаг с визуализацией хориокапилляров.
На основании совокупности результатов проведенных исследований диагностирована метастатическая карцинома хориоидеи. Больная направлена к онкологу для проведения повторного курса системной полихимиотерапии.
Результаты и обсуждение
Существовавшее ранее мнение о редкости внутриглазных метастатических опухолей в последние годы пересмотрено, что связано с большей концентрацией онкологических больных в специализированных клиниках и увеличившейся продолжительностью их жизни [1].
Приведенные два клинических случая интересны тем, что оба пациента имеют онкологический анамнез и у обоих на глазном дне офтальмоскопически выявлен желтый проминирующий очаг в постэкваториальной зоне, что может указывать на метастатический характер поражения глаза. Однако при тщательном обследовании с использованием методов флюоресцентной ангиографии и спектральной оптической когерентной томографии по совокупности томографических и ангиографических симптомов в одном случае диагноз метастаза снят, а в другом подтвержден.
В первом случае гипофлюоресценция в зоне очага с гиперфлюоресценцией по его периферии в совокупности с томографически выявленной отслойкой РПЭ и сохранением ровного профиля мембраны Бруха позволяют снять диагноз вторичной злокачественной опухоли хориоидеи и установить возрастную макулярную дегенерацию.
Во втором случае гипофлюоресценция в ранние фазы исследования, симптом «россыпи крупы» в совокупности с томографически определяемым мелкобугристым изменением хориоидального профиля, наличием депозитов в слоях сетчатки, ретиношизисом дают возможность установить диагноз метастатической карциномы хориоидеи.
Анализ описанных двух случаев диктует необходимость тщательного осмотра глаз при жалобах на снижение зрения как в момент первичной диагностики, так и при последующем динамическом наблюдении, особенно при наличии общих онкологических заболеваний.
Ранняя диагностика метастатической карциномы хориоидеи с последующей адекватной терапией обеспечивает не только улучшение качества жизни больного, но и лучший витальный прогноз.
Выводы
1. При общих онкологических заболеваниях и жалобах на снижение зрение обязательным является осмотр глазного дна с целью своевременного выявления метастатической карциномы хориоидеи.
2. Введение в алгоритм обследования больных с метастатической карциномой хориоидеи флюоресцентной ангиографии и спектральной оптической когерентной томографии позволяет поставить диагноз на ранних этапах развития и провести в дальнейшем своевременное адекватное лечение.
Частота определения сосудистой сети по ангиографии с индоцианином зеленым
Как свидетельствуют данные, представленные в табл. 3, при проведении ангиографии с индоцианином зеленым при меланоме хориоидеи собственная сосудистая сеть в ткани опухоли визуализировалась у 21 из 27 (77,8%) больных, при метастазе — у 3 из 4 пациентов и при гемангиоме — у всех больных. Результаты, представленные в табл. 3, наглядно отражают более высокую информативность данного метода в сравнении с методом УЗДГ при меланоме хориоидеи. Следует отметить, что в данной выборке больных с меланомами превалировали пациенты с меланомой малых размеров (до 3 мм высотой) — именно у данной категории больных отмечаются сложности дифференциальной диагностики с невусами, а при беспигментом характере — с метастатическим поражением хориоидеи и гемангиомами.
Невус хориоидеи при ангиографии с индоцианином зеленым характеризовался диффузной гипофлюоресценцией во всех фазах исследования с довольно четкой границей; сосуды хориоидеи, как правило, экранировались зоной невуса и были более размытыми по сравнению с окружающим свечением неизмененной собственно сосудистой оболочки. Площадь невуса, определяемая на ангиограмме, в некоторых случаях была больше, чем при офтальмоскопии. Трудности для диагностики представляют невусы, сопровождающиеся отслойкой нейроэпителия, отложениями на пигментном эпителии. Ангиография с индоцианином зеленым позволяет дифференцировать эти состояния. Для таких невусов характерно отсутствие патологических сосудов в проекции образования и постепенно появляющиеся в поздние фазы очаги гипо- и гиперфлюоресценции, соответствующие друзеноидным отложениям, отслойке нейроэпителия и деструктивным изменениям пигментного эпителия сетчатки. У всех пациентов данной группы кровоток по данным УЗДГ не выявлялся (рис. 1).
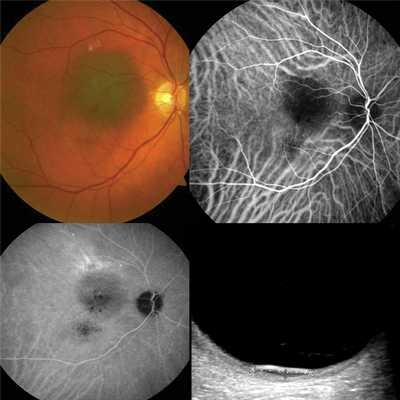
Рис. 1. Невус хориоидеи при УЗДГ и ангиографии с индоцианином зеленым: диффузная гипофлюоресценция во всех фазах исследования.
Размеры образования по данным УЗДС — 0,7×6,4 мм. Патологическая сосудистая сеть не определяется.
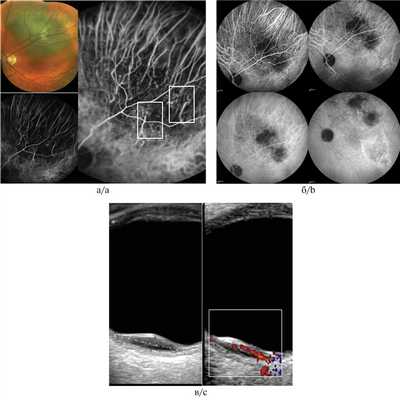
Рис. 2. Меланома хориоидеи при ангиографии с индоцианином зеленым.
а — на фоне гипофлюоресценции в опухоли в раннюю фазу исследования визуализируются собственные сосуды в виде вертикальных прямых паттернов (до 15 с); б — в поздние фазы исследования (до 30 мин от начала исследования) определяется нарастающая гиперфлюоресценция в опухоли вследствие просачивания и накопления красителя; в — УЗДГ-картина: среднескоростной, среднерезистентный кровоток в ткани опухоли (размер образования 2,1×12,0 мм).
При метастатическом поражении хориоидеи ангиографическая картина была разнообразна. Так, при метастазе кожной меланомы имело место выраженное свечение патологической неоваскулярной сети на фоне блокады фоновой флюоресценции, при проведении УЗДГ определялся низкоскоростной, среднерезистентный кровоток (рис. 3, а, б). Метастатическое поражение хориоидеи при первично не выявленном очаге, напротив, демонстрировало блок свечения сосудов хориоидеи соответственно размерам очага во всех фазах исследования при полном отсутствии идентификации признаков патологической неоваскуляризации (рис. 4, а, б).
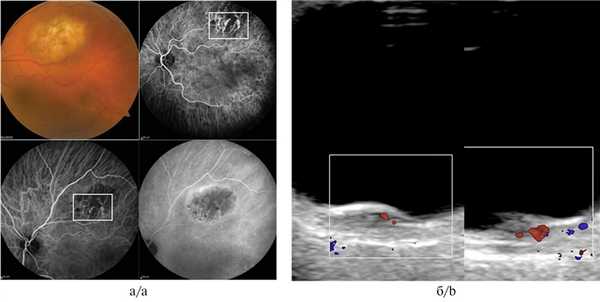
Рис. 3. Метастаз хориоидеи вследствие меланомы кожи при ангиографии с индоцианином зеленым.
а — выраженное свечение патологической неоваскулярной сети на фоне блокады фоновой флюоресценции. Визуализируются собственные сосуды в виде петлевых паттернов; б — УЗДГ-картина: низкоскоростной, среднерезистентный кровоток в ткани опухоли (размер образования 2,0×8,9 мм).
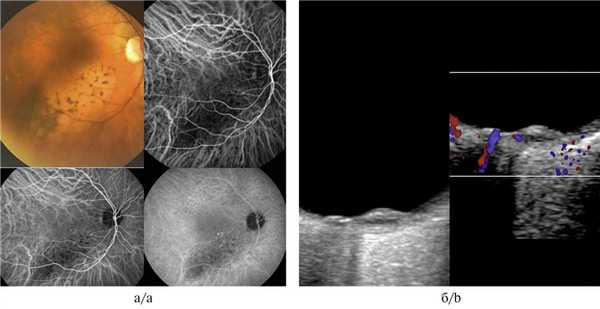
Рис. 4. Метастаз хориоидеи при первично не выявленном очаге.
а — ангиография с индоцианином зеленым: определяется блок свечения сосудов хориоидеи соответственно размерам очага во всех фазах исследования при полном отсутствии идентификации признаков патологической неоваскуляризации; б — УЗДГ-картина: отсутствие кровотока в ткани опухоли (размер образования 1,6×5,7 мм).
Гемангиома хориоидеи характеризовалась выраженными отличительными признаками как при проведении ангиографии с индоцианином зеленым, так и при УЗИ с ЦДК. Данную патологию отличали идентификация патогномоничных сосудистых паттернов в виде рисунка «рыбацкой сети», сети в виде «кружева» и гиперфлюоресценция на всех фазах исследования (рис. 5, а, б). При проведении УЗДГ выявлялся высокоскоростной и среднерезистентный кровоток (рис. 5, в).
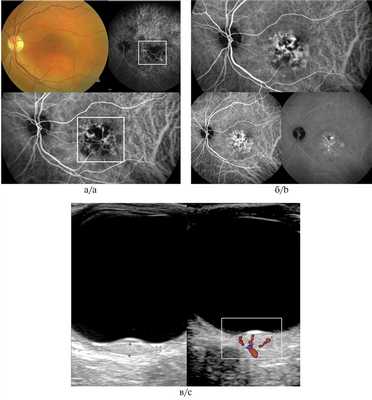
Рис. 5. Гемангиома хориоидеи при ангиографии с индоцианином зеленым.
а, б — сосудистые паттерны в виде рисунка «рыбацкой сети», сети в виде «кружева» и гиперфлюоресценция на всех фазах исследования; в — УЗДГ-картина: высокоскоростной и среднерезистентный кровоток в ткани опухоли (размер образования 1,8×9,2 мм).
Краситель индоцианин зеленый впервые синтезирован в 1950 г. компанией Eastman Kodak для производства инфракрасных фотографических материалов, в медицинской практике он нашел применение с начала 1970 г., когда K. Kogure и E. Chromokos при изучении гемодинамики мозга обезьяны обнаружили возможности визуализации сосудистой сети при его применении. Перспективность его использования в офтальмологии определяется тем, что индоцианин зеленый, являясь трикарбоцианиновым красителем, хорошо связывается с белками плазмы (98%), не диффундирует через фенестрированные капилляры, достигает своего пикового свечения при 835 нм, имеет pH 5,5—6,5, что определяет его хорошее проникновение через большинство глазных тканей, включая пигментный эпителий и ксантофилл макулярной области, а также долгую персистенцию в кровотоке. В 70-х годах прошлого века данная методика бурно развивалась в ряде стран, что обусловлено совершенствованием техники и прогрессом в области разработки современного оборудования, позволяющего проводить спектральную динамическую видеоангиографию [23].
В современных условиях для диагностики различных новообразований хориоидеи применяется мультимодальный подход с использованием таких методов, как спектральная оптическая когерентная томография, УЗИ с ЦДК, флюоресцентная ангиография, контрастная магнитно-резонансная томография, в сложных диагностических случаях — тонкоигольная аспирационная биопсия [24]. Как правило, данного арсенала диагностических средств бывает достаточно для верификации неопластического процесса, и основные сложности возникают в диагностике беспигментных первичных и вторичных опухолей хориоидеи [1, 13]. Как показывает данное исследование, применение ангиографии с индоцианином зеленым вкупе с УЗДГ является исключительно информативным при гемангиоме хориоидеи и может быть полезным в идентификации беспигментной меланомы и метастаза, что согласуется с мнением ряда авторов [5, 13, 25].
Как свидетельствуют полученные результаты, визуализация неоваскулярной сети меланом с помощью ангиографии с индоцианином зеленым возможна у 77,8% пациентов, а при применении метода УЗДГ — у 55,6%. Следует отметить, что в данном исследовании изучаемую выборку составили пациенты с малыми меланомами, что, возможно, ограничивало информативность ангиографии с индоцианином зеленым. Так, по данным A.J. Mueller и соавт. (1999), частота выявления сосудистой сети в меланомах хориоидеи высотой до 8 мм достигает 94% [26]. Следует отметить, что возможности данного метода лимитированы степенью пигментации опухоли: общеизвестно, что с увеличением степени пигментации меланомы хориоидеи снижается степень ее флюоресценции вплоть до полного блока [13].
Перспективность изучения применения ангиографии с индоцианином зеленым в настоящее время определяется возможностью идентификации васкулогенной мимикрии. Так, в исследованиях A.J. Mueller и соавт. [17] в 1998 г. у 16 (89%) из 18 пациентов при помощи ангиографии с индоцианином зеленым были идентифицированы опухолевые сосуды (петлевые структуры), которые в последующем были подтверждены исследованием гистологических срезов опухолей с помощью PAS-реакции. S. Frenkel и соавт. [21] в 2008 г. показали, что петлевые паттерны васкулогенной мимикрии, идентифицированные методом ангиографии с индоцианином зеленым, в гистологических срезах увеальной меланомы соединяются с кровеносными сосудами, выстланными эндотелиальными клетками, представляя альтернативный путь для питания опухоли. Учитывая, что выявленные ангиографические паттерны в виде петлевых структур, анастомозов и сетей определяют риски метастазирования процесса, представляется перспективным дальнейшее изучение данного метода [20, 27].
Выводы
1. Ангиография с индоцианином зеленым позволяет диагностировать сосудистую сеть у 77,8% больных с меланомами хориоидеи малых и средних размеров.
2. Ангиоархитектоника новообразований хориоидеи, визуализируемая при ангиографии с индоцианином зеленым, отличается вариабельностью паттернов, которые следует учитывать в дифференциальной диагностике различных патологических состояний.
© Н.Л.Маланова, И.Г.Терентьев, Т.А.Цыганова,
М.А.Мелехина, 2002 г.
УДК 617.7:543.542
Поступила 31.05.2002 г.
Н.Л.Маланова, И.Г.Терентьев, Т.А.Цыганова, М.А.Мелехина
Нижегородская государственная медицинская академия;
Областная клиническая больница им. Семашко, Нижний Новгород
Метод флюоресцентной ангиографии в офтальмологии
Флюоресцентная ангиография (ФАГ), предложенная в 1961 г. Novotny и Alvis, является ценной и информативной методикой для прижизненного исследования сосудов глазного дна. Сетчатку можно обследовать с помощью прямой и непрямой офтальмоскопии и биомикроскопии. Флюоресцентная ангиография является необходимым дополнением к этим клиническим методам исследования, предоставляя значительный объем дополнительной информации для диагностики и лечения патологических состояний сетчатки и зрительного нерва.
Метод ФАГ основан на способности флюоресцеина поглощать синий свет и излучать желто-зеленый. Этот краситель интенсивно флюоресцирует при нормальном значении pH крови (7,37—7,45). Он нетоксичен и достаточно безопасен для большинства пациентов. При поступлении флюоресцеина в кровь происходит поэтапное контрастирование сосудов, что можно зафиксировать фотографически. Для этой цели используются различные модели фундус-камер с высокой скоростью фотографирования. В нашей клинике применяется фундус-камера F450 ф. Zeiss. Контрастированные флюоресцеином сосуды на позитивных фотоснимках выглядят в виде светлых полос на фоне глазного дна, на негативах отношения обратные.
Исследование проводят следующим образом. До введения флюоресцеина делают несколько фотографий без фильтра, далее в синем свете производят контрольный снимок. После этого быстро вводят флюоресцеин (флюоресцеин-натрий 10%, 5,0 мл) в локтевую вену и через 5—7 с начинают серийную хронометрированную фотосъемку. Отдельные снимки делают с увеличением интервала. Возбуждающий (синий) и барьерный (желтый) светофильтры подбирают таким образом, чтобы они полностью поглощали все лучи, исходящие от источника возбуждения. По мере поступления вещества в сосудистое русло (время попадания флюоресцеина из вены в сосуды глаза составляет обычно 12—15 с) красителем заполняются собственно сосудистая оболочка и хориокапилляры. Это первая, преартериальная, фаза ангиограмм.
Пигментный эпителий сетчатки непроницаем для флюоресцеина, и краситель далее поэтапно поступает в артериальное русло (артериальная фаза), в капилляры и вены (артериовенозная и венозная фазы).
Венозная фаза продолжается до заполнения красителем вен. За этой фазой после первого прохождения через сосуды почек происходит возвращение крови, содержащей флюоресцеин, вновь в сосуды сетчатки. Это фаза рециркуляции. Концентрация красителя в крови уже значительно ниже, чем в предыдущие, поэтому фаза рециркуляции имеет большую диагностическую ценность. В течение 24 ч у пациентов с нормальной почечной фильтрацией флюоресцеин практически полностью элиминируется из кровяного русла. При этом наблюдается окрашивание склер и мочи.
Основной клинический симптом, выявляемый с помощью ФАГ, — патологическая флюоресценция. Требуется только оценить характер этих изменений (гипо– или гиперфлюоресценция) и их локализацию.
Гиперфлюоресценция чаще связана с патологическими процессами в пигментном эпителии сетчатки, что приводит к просачиванию красителя в сетчатку или субретинально либо флюоресценция видна сквозь пигментный эпителий. Описанные изменения могут наблюдаться при центральной серозной хориопатии, при наличии новообразованных сосудов (диабетическая ретинопатия, неопластический процесс, болезнь Коатса и др.), при дистрофиях пигментного эпителия.
Гипофлюоресценция проявляется полной или частичной блокадой свечения флюоресцирующих в норме структур. Так, например, блокада флюоресценции может быть связана со скоплением пигмента (невусы хориоидеи), со скоплением экссудата при нарушениях проходимости сосудов сетчатки (центральной вены сетчатки, центральной артерии сетчатки или их ветвей).
Очень информативна ФАГ при патологических состояниях зрительного нерва. Характерна ангиографическая картина при друзах зрительного нерва (друзы флюоресцируют еще до введения красителя — псевдофлюоресценция). Хорошо выявляется на ангиограммах отек диска зрительного нерва, как изолированный, так и в сочетании с воспалительным компонентом. Однако выявляемая картина гиперфлюоресценции неспецифична и должна оцениваться лишь в комплексе с офтальмоскопическими изменениями.
Особо ценной является возможность дифференциальной диагностики регматогенных и вторичных отслоек сетчатки и невусов хориоидеи. У пациентов с внутриглазными опухолями на флюоресцентных ангиограммах в раннюю преартериальную фазу выявляются собственные сосуды опухоли, при этом сосудистый рисунок резко отличается от сосудистого рисунка сетчатки над очагом. В раннюю артериальную фазу флюоресцеин интенсивно проходит из сосудов в опухоль и длительно задерживается опухолевым узлом в поздней фазе.
Если же отслойка сетчатки имеет регматогенный или экссудативный характер, флюоресцеин локально накапливается под пигментным эпителием в месте скопления субретинальной жидкости в виде полости.
При невусах хориоидеи картина ФАГ может быть вариабельна — от разной степени выраженности блокады хориоидальной флюоресценции с нечетко очерченными краями до гиперфлюоресценции за счет пропотевания красителя из очагов вторичных изменений сетчатки над невусом (кистозные изменения, друзы). Контрастированные сосуды сетчатки при этом не изменены. Нередко наблюдается и нормальная ангиографическая картина.
Полученные результаты заносятся в компьютеризированную систему архивирования, что позволяет оперативно и с высокой степенью точности проводить динамическое наблюдение за пациентами, что особенно важно при росте невусов, после органосохранного лечения меланом хориоиде, для контрольных осмотров при диабетической ретинопатии.
Таким образом, флюоресцентная ангиография сетчатки является ценным дополнительным методом исследования, значительно расширяющим возможности дифференциальной диагностики различных состояний глазного дна.
"Медикум"
новый научно-практический медицинский журнал, который будет издаваться на 2-х языках: русском и английском, в трех формах выпуска: печатная, интернет-версия, CD-версия.
Читайте также:
