Увеличение левого желудочка. Электрокардиограмма при увеличении левого желудочка
Добавил пользователь Владимир З. Обновлено: 29.01.2026
Разработать дополнительные чувствительные и специфичные электрокардиографические (ЭКГ) критерии для ранней диагностики гипертрофии левого желудочка (ГЛЖ).
МАТЕРИАЛ И МЕТОДЫ
Группу наблюдения составили 184 пациента мужского пола (средний возраст 53,0±7,5 года). Проведена эхокардиография (ЭХО-КГ) на аппарате Vivid q (GE Vingmed Ultrasound AS, Норвегия) для определения ГЛЖ, ЭКГ в 12 стандартных отведениях с использованием электрокардиографа CARDIOVIT АТ-10 (Schiller FG, Швейцария) для оценки индексов ГЛЖ. Выполнены статистическая обработка данных и ROC-анализ.
РЕЗУЛЬТАТЫ
ВЫВОДЫ
Установленные значения точек отреза (cut-off) в отношении ГЛЖ у мужчин для RaVL 4,5 мм и корнельского вольтажного индекса 15,5 мм позволяют прогнозировать наличие ГЛЖ у мужчин и осуществлять целенаправленную эхокардиографию.
ФБУН «Федеральный научный центр медико-профилактических технологий управления рисками здоровью населения» Роспотребнадзора
ФБУН «Федеральный научный центр медико-профилактических технологий управления рисками здоровью населения» Роспотребнадзора
ФБУН «Федеральный научный центр медико-профилактических технологий управления рисками здоровью населения»
ФБУН «Федеральный научный центр медико-профилактических технологий управления рисками здоровью населения»
Дата принятия в печать:
Введение
Гипертрофия левого желудочка (ГЛЖ) определяется у 16—19% населения, у 8,1% взрослых с артериальной гипертензией (АГ), чаще встречается у мужчин [1, 2]. Распространенность ГЛЖ в общей популяции по данным электрокардиографии (ЭКГ) составляет 3—10%, а по данным эхокардиографии (ЭХО-КГ) — 15—20% [3].
Своевременная диагностика ГЛЖ имеет не только клинический, но и трудовой прогноз, так как увеличение левого желудочка является неблагоприятным предиктором сердечно-сосудистых катастроф [3].
На раннем этапе ГЛЖ характеризуется увеличением размеров кардиомиоцитов, числа митохондрий, миофибрилл, и на этой стадии возможен обратный процесс. При прогрессировании ГЛЖ клетки миокарда погибают и замещаются соединительной тканью, соответственно выраженный регресс на этом этапе уже невозможен [4]. Диагностика ГЛЖ и своевременное лечение улучшают прогноз у пациентов и снижают риск кардиальных осложнений в 4 раза [5, 6].
Самым доступным методом диагностики ГЛЖ в практическом здравоохранении является стандартная 12-канальная ЭКГ. Этот метод исследования широко используется не только на догоспитальном этапе у пациентов, но и при скрининге сердечно-сосудистых заболеваний (ССЗ) у здоровых людей. Однако однозначно диагностировать ГЛЖ, особенно на ранних этапах ее развития, не представляется возможным и требуется верификация диагноза данными ЭХО-КГ. Реже всего диагностику ГЛЖ проводят с помощью магнитно-резонансной томографии (МРТ). Для преодоления существующих ограничений стандартной ЭКГ в диагностике ГЛЖ необходима разработка дополнительных критериев, применяемых в анализе данных.
Цель исследования — разработать дополнительные чувствительные и специфичные ЭКГ-критерии для ранней диагностики ГЛЖ.
Материал и методы
Группу наблюдения составили 184 пациента мужского пола (средний возраст 53,0±7,5 года). У 66 (35,9%) человек диагностирована АГ, у 14 (7,6%) — АГ, осложненная нарушением мозгового кровообращения, у 6 (3,3%) — ишемическая болезнь сердца (ИБС), у 18 (9,8%) — АГ в сочетании с сахарным диабетом 2-го типа (СД2 типа), у 37 (20,1%) — АГ в сочетании с ИБС, у 4 (2,2%) — гипертрофическая кардиомиопатия, у 4 (2,2%) — пороки сердца, у 2 (1,1%) — СД2 типа. Не было ССЗ у 33 (17,9%) пациентов. У 152 (82,6%) пациентов выявлена избыточная масса тела либо определено ожирение, у 32 (17,4%) индекс массы тела соответствовал норме.
В исследование не включены пациенты, перенесшие инфаркт миокарда, больные с хронической сердечной недостаточностью III—IV функционального класса, а также пациенты с фибрилляцией предсердий.
ЭХО-КГ проведена на аппарате экспертного класса Vivid q (GE Vingmed Ultrasound AS, Норвегия) с использованием секторного фазированного датчика (1,5—3,5 МГц) по стандартной методике. Массу миокарда левого желудочка (ММЛЖ) определяли по формуле американского эхокардиографического общества (ASE):
где КДР — конечный диастолический размер, см; ТЗСд — толщина задней стенки левого желудочка в диастоле, см; ТМЖПд — толщина межжелудочковой перегородки в диастоле, см.
ММЛЖ у пациентов с гипертрофической кардиомиопатией не рассчитывали.
Индекс массы миокарда левого желудочка (ИММЛЖ) у пациентов с избыточной массой тела и ожирением определяли по формуле:
ММЛЖ/рост 2, 7 (г/м 2,7 ), (2)
Наличие ГЛЖ у пациентов с избыточной массой тела устанавливали при значении индекса более 50 г/м 2,7 . У пациентов с нормальной массой тела ИММЛЖ рассчитывали по формуле:
где ППТ — площадь поверхности тела.
За ГЛЖ принимали значение ИММЛЖ более 115 г/м 2 [7].
ЭКГ в 12 стандартных отведениях выполняли с использованием электрокардиографа CARDIOVIT АТ-10 (Schiller FG, Швейцария). Рассчитывали ЭКГ-индексы ГЛЖ, рекомендованные к использованию в рамках актуальных клинических рекомендаций по АГ [7]:
— RaVL (норма менее 11 мм);
— корнельский вольтажный индекс: RaVL+SV3 (норма менее 28 мм);
— корнельское произведение: (RaVL+SV3) × QRS (норма менее 2440 мм × мс).
Статистическую обработку проводили с помощью программы SPSS 22. Выполняли построение моделей однофакторной и многофакторной логистической регрессии (методом Forward LR), описываемой формулой:
, (4)
где p — вероятность наличия у пациента ГЛЖ; e — основание натурального логарифма; х — независимый фактор; b0, b1,, bi — коэффициенты многофакторной математической модели.
В модель включены ЭКГ-критерии ГЛЖ. Порогом отсечения при бинарной классификации (ГЛЖ есть/ГЛЖ нет) для модели считали вероятность 0,5.
Выполнено построение ROC-кривой (receiver operating characteristic — ROC) для каждого тестируемого фактора, а также для массива прогнозной вероятности, определенной с помощью многофакторной логистической модели, с целью оценки качества бинарной классификации. Определяли площадь под ROC-кривой (area under the curve — AUC). Качество модели по AUC оценивали следующим образом: 0,9—1,0 — отличное; 0,8—0,9 — очень хорошее; 0,7—0,8 — хорошее; 0,6—0,7 — среднее; 0,5—0,6 — неудовлетворительное.
При использовании статистических процедур статистически значимым уровнем считали p
Настоящее исследование выполнено в соответствии с правилами ICHGCP, с соблюдением этических норм, изложенных в Хельсинкской декларации (редакция 2008 г.), Национальным стандартом Российской Федерации ГОСТ-Р 52379—2005 «Надлежащая клиническая практика» (ICH E6 GCP). Программа исследования одобрена этическим комитетом ФБУН «ФНЦ медико-профилактических технологий управления рисками здоровью населения» (протокол №105 от 17.06.19). Все пациенты информированы о цели проведения исследования, получено информированное добровольное согласие исследуемых.
Результаты
Параметры однофакторных логистических регрессионных моделей с ЭКГ-критериями ГЛЖ в качестве независимых переменных и наличием или отсутствием ГЛЖ по данным трансторакальной ЭХО-КГ представлены в табл. 1. Все анализируемые ЭКГ-критерии ГЛЖ показали статистически значимое влияние на вероятность наличия ГЛЖ по данным ЭХО-КГ, и при этом наибольшее повышение уровня правильной классификации показали RaVL (54,3—64,1%) и корнельский вольтажный индекс (54,3—65,8%). Данные индексы показали и наибольшее снижение значения —2Log likelihood: 253,7—235,3 и 253,7—217,2 соответственно. Следует отметить, что R 2 Найджелкерка для исследованных показателей составил 0,04—0,24, в то время как проверка согласия Хосмера—Лемешева показала значимость более 0,05 только для трех ЭКГ-критериев: RaVL, индекса Соколова—Лайона и корнельского вольтажного индекса. В случае корнельского произведения проверка согласия Хосмера—Лемешева показала значимость 0,022; это означает, что данная модель недостаточно хорошо описывает фактические данные.
Таблица 1. Параметры однофакторных логистических регрессионных моделей
Изменение доли правильной классификации от шага 0 к шагу 1,%
Изменение —2Log likelihood от шага 0 к шагу 1
Проверка согласия Хосмера—Лемешева
Корнельский вольтажный индекс
Включение ЭКГ-критериев в многофакторную логистическую регрессионную модель (метод Forward LR) позволило получить уравнение с двумя статистически значимыми независимыми переменными (табл. 2). В модель включены RaVL и корнельский вольтажный индекс, в то время как корнельское произведение и индекс Соколова—Лайона из модели исключены. Доля правильной классификации в целом для многофакторной модели составила 70,1%, а коэффициент R 2 Найджелкерка — 0,27. Критерий Хосмера—Лемешева, равный 0,22, позволяет говорить о том, что полученная модель хорошо описывает фактические данные.
Таблица 2. Параметры многофакторной логистической регрессионной модели
Изменение доли правильной классификации от шага 0 к шагу 1,%
Изменение —2Log likelihood от шага 0 к шагу 1
R 2 Найджелкерка
Проверка согласия Хосмера—Лемешева
Корнельский вольтажный индекс
Уравнение двухфакторной логистической регрессии вероятности наличия ГЛЖ на основании значения RaVL и корнельского вольтажного индекса выглядит следующим образом:
p=1/1+е –(–3,74+0,14× RaVL +0,18×корнельский вольтажный индекс) .
ROC-анализ для индексов RaVL и корнельского вольтажного индекса, а также предсказанной вероятности на основе многофакторной логистической модели и ГЛЖ, по данным трансторакальной ЭХО-КГ, представлен в табл. 3 и на рис. 1.
Таблица 3. Результаты ROC-анализа параметров регрессионной модели
Переменная результата проверки
Площадь под кривой (AUC)
Асимптотический 95% доверительный интервал
Корнельский вольтажный индекс
Примечание. * — в соответствии с непараметрическим предположением; ** — нулевая гипотеза: = действительная площадь =0,5.
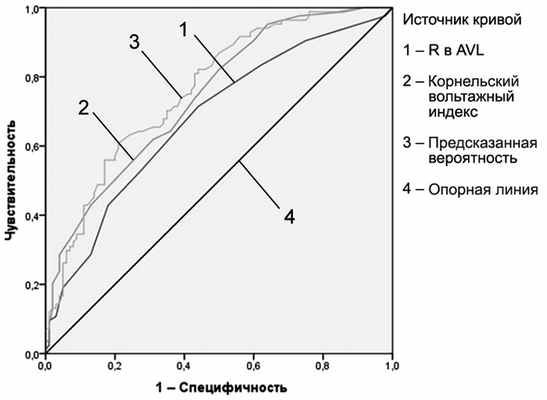
Рис. 1. ROC-кривые для индексов RaVL, корнельского вольтажного индекса, предсказанной вероятности на основе многофакторной логистической модели и гипертрофии левого желудочка по данным трансторакальной эхокардиографии.
Согласно полученным данным, хорошая прогностическая способность в отношении диагностики ГЛЖ показана для корнельского вольтажного индекса (AUC=0,744), средняя — для RaVL (AUC=0,679). Включение в логистическую модель обоих критериев позволило получить AUC=0,764, что характеризует хорошее качество двухфакторной модели.
Согласно матрице ROC-анализа, значение точки отреза (cut-off) для RaVL в отношении ГЛЖ составляет 4,5 мм с чувствительностью 71% и специфичностью 56% (для рекомендованного значения менее 11 мм расчетная чувствительность составила только 10% при 99% специфичности); для корнельского вольтажного индекса таковая составляет 15,5 мм с чувствительностью 74% и специфичностью 57% (для рекомендованного значения менее 28 мм расчетная чувствительность составила только 6% при 99% специфичности).
Следующим этапом работы была оценка методом ROC-анализа точки отреза (cut-off) ИММЛЖ по росту в степени 2,7 в отношении прогнозной принадлежности к группе ГЛЖ по данным двухфакторной логистической регрессионной модели. Результаты представлены на рис. 2. Получено значение AUC=0,704 (p=0,0001) и точки отреза ИММЛЖ с чувствительностью 68% и специфичностью 72%, равной 50 г/м 2,7 .
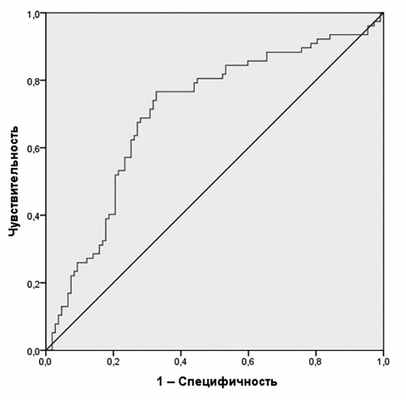
Рис. 2. ROC-кривая для индекса массы миокарда левого желудочка и предсказанной принадлежности к группе гипертрофии левого желудочка на основании двухфакторной логистической регрессионной модели.
Разработка высокочувствительных и специфичных критериев ранней диагностики ГЛЖ является актуальной задачей в связи с тем, что ГЛЖ служит ключевым признаком поражения сердца при различных заболеваниях. В настоящее время для диагностики ГЛЖ используют ЭКГ, ЭХО-КГ, МРТ, имеющие свои достоинства и недостатки [8].
Для диагностики ГЛЖ в практическом здравоохранении нашли широкое применение ЭКГ-критерии. Выделяют традиционные вольтажные ЭКГ-критерии ГЛЖ с чувствительностью 6,2—53,1% и специфичностью 82—100% и авторские критерии, например, критерии Romhilt—Estes с чувствительностью 62% и специфичностью 97% [9—11]. В руководстве Г.С. Вагнера выделяют множество авторских ЭКГ-критериев ГЛЖ [12]. Однако, как правило, это трудоемкие методики расчета, чаще используемые в научных клинических исследованиях. Рекомендованные для практического использования ЭКГ-критерии ГЛЖ [7] показывают высокую специфичность (71—100%), но имеют низкую чувствительность (0—37,5%). Помимо хорошо изученных ограничений ЭКГ диагностики ГЛЖ, существуют малоизученные — возрастные, половые, конституциональные, расовые факторы [13—15]. ЭКГ -диагностика позволяет выявить выраженную ГЛЖ, в то время как диагностика ранних стадий ГЛЖ представляет трудности [16, 17]. В настоящее время идеальный ЭКГ-критерий диагностики ГЛЖ не найден. В клинике завершающим этапом поиска ГЛЖ является ЭХО-КГ. Одной из задач скринингового ЭКГ-исследования является решение вопроса о необходимости продолжения диагностического поиска, в том числе направления на ЭХО-КГ. Не всегда пациент с неизмененной ЭКГ проходит исследование на ЭХО-КГ. ЭХО-КГ является более точным методом оценки ГЛЖ и хорошо коррелирует с данными МРТ — золотым стандартом прижизненной диагностики ГЛЖ [18, 19].
При АГ на ультразвуковом исследовании ГЛЖ удается выявить у 20—80% пациентов и у 50% взрослых лиц в общей популяции [3]. ЭХО-КГ позволяет выявить не только наличие ГЛЖ, но и определить степень выраженности и морфологический тип увеличения левого желудочка [20]. ЭХО-КГ-критерии ГЛЖ являются лучшим долгосрочным предиктором сердечно-сосудистого прогноза, чем ЭКГ- критерии ГЛЖ [21].
M.Y. van der Ende и соавт. в своем исследовании определили специфическую для пола чувствительность ЭКГ-критериев ГЛЖ и разработали новые критерии, используя МРТ. В исследуемой когорте (n=2724) разработаны ЭКГ-критерии ГЛЖ, зависящие от пола, путем исследования всех возможных сумм амплитуд QRS во всех 12 отведениях и выбора суммы с наибольшим псевдо-R2 и площадью под кривой для выявления ГЛЖ. Разработанный критерий Гронингена для женщин превзошел все ЭКГ-критерии ГЛЖ с чувствительностью 42%. У мужчин данный критерий был столь же чувствителен (44%). Предложенные критерии Гронингена, специфичные для пола, повысили чувствительность к выявлению ГЛЖ, особенно у женщин [15].
F. De la Garza-Salazar и соавт. выдвинули гипотезу о том, что алгоритм машинного вычисления может оптимизировать ЭКГ при прогнозировании ГЛЖ с помощью ЭХО-КГ, а также установить фенотипы ЭКГ-критериев ГЛЖ. В ходе исследования использована ЭХО-КГ в качестве стандартного диагностического инструмента для выявления ГЛЖ. Авторы включили 432 пациента (мощность 99%), из которых у 202 (46,7%) пациентов имелись ЭХО-КГ-критерии ГЛЖ, при этом 240 (55,6%) из 432 —мужчины. Данные разделены на обучающий/тестовый набор (80%/20%). Авторы применили логистический регрессионный анализ к измерениям ЭКГ. Модель логистической регрессии с наилучшей способностью идентифицировать ЭХО-КГ-критерии ГЛЖ исследователями включена в вычислительный алгоритм. Определено, что машинный алгоритм превзошел точность текущих критериев ЭКГ при обнаружении ЭХО-КГ-критериев ГЛЖ. Полученные новые критерии основаны на измерениях ЭКГ, которые идентифицируют пациентов с высоким риском развития ГЛЖ [22].
О.А. Комарова и соавт. в своей работе по оценке информативности критериев ГЛЖ у пациентов с АГ установили, что критерии Корнельского университета, а также отдельные показатели критериев Соколова—Лайона (RaVL и R1+S3) являются диагностически эффективными. Критерии Корнельского университета у мужчин при мягкой и умеренной АГ показали чувствительность 38%, специфичность — 92%, индекс Соколова—Лайона — чувствительность 45%, специфичность — 37%. Данные критерии рекомендованы для использования в практике при диспансеризации населения с АГ [23].
ЭКГ-критерии ГЛЖ и ЭХО-КГ-критерии ГЛЖ характеризуются различными диагностическими и прогностическими возможностями. Учитывая соотношение затрат, выгод и трудоемкость ЭХО-КГ, по-прежнему можно считать обоснованным использование ЭКГ в практическом здравоохранении, но требуется дальнейшая верификация ЭКГ-критериев ГЛЖ.
Результаты проведенного нами исследования показали, что ЭКГ-критерии ГЛЖ позволяют статистически значимо прогнозировать наличие ГЛЖ у мужчин по данным ЭХО-КГ. В то же время диагностическая значимость данных критериев неодинакова и варьирует от хорошей (корнельский вольтажный индекс) до средней (RaVL). Точка отреза (cut-off) для RaVL в отношении ГЛЖ составляет 4,5 мм с чувствительностью 71% и специфичностью 56%, а для корнельского вольтажного индекса — 15,5 мм с чувствительностью 74% и специфичностью 57%. Включение ЭКГ-критериев в многофакторную логистическую регрессионную модель позволило установить независимое статистически значимое влияние RaVL и корнельского вольтажного индекса на вероятность диагностики ГЛЖ у мужчин по данным ЭХО-КГ. Предложенная логистическая регрессионная модель позволяет с чувствительностью 68% и специфичностью 72% прогнозировать у мужчин ИММЛЖ более 50 г/м 2,7 .
Выводы
1. Стандартные электрокардиографические критерии гипертрофии левого желудочка у мужчин не обладают высокой чувствительностью и специфичностью в отношении диагностики гипертрофии левого желудочка.
2. Установленные значения точек отреза (cut-off) в отношении гипертрофии левого желудочка у мужчин для RaVL 4,5 мм и корнельского вольтажного индекса 15,5 мм позволяют с чувствительностью 71—74% и специфичностью 56—57% прогнозировать наличие гипертрофии левого желудочка у мужчин и осуществлять целенаправленную эхокардиографию.
3. Предложенная двухфакторная регрессионная модель характеризуется хорошей прогностической способностью и позволяет с чувствительностью 68% и специфичностью 72% прогнозировать у мужчин индекс массы миокарда левого желудочка более 50 г/м 2,7 .
Участие авторов: концепция и дизайн исследования — О.Ю. Устинова, А.Е. Носов; сбор и обработка материала — А.С. Байдина; статистический анализ данных — А.С. Байдина, А.Е. Носов; написание текста — А.С. Байдина, О.Ю. Горбушина; редактирование — О.Ю. Устинова, А.Е. Носов.
Гипертрофия левого желудочка: симптомы и диагностика в Киеве
Гипертрофия левого желудочка (ГЛЖ) – это увеличение толщины стенки и массы ЛЖ, вызванное физическими перегрузками, заболеваниями сердца и сосудов, наследственностью. В норме толщина желудочка не превышает 11 мм. Патология часто диагностируется у людей с гипертонической болезнью. ГЛЖ встречается у людей всех возрастов.
Гипертрофия левого желудочка не является болезнью. Это отклонение от нормы, которое возникает на фоне патологий сердца. ГЛЖ становится причиной нарушения ритма сердца и сердечной недостаточности. Лечение включает консервативную терапию и хирургическое вмешательство. Заболевание протекает бессимптомно, изредка возникают одышка, обмороки, учащенное сердцебиение.
Классификация гипертрофии левого желудочка
- эксцентрическая — увеличение мышечных волокон происходит больше в длину, чем в толщину, увеличивается сердце и камеры, незначительно утолщается мышца ЛЖ, замедляется пульс;
- концентрическая — сердечная мышца больше изменяется в толщину, чем в длину, увеличивается толщина стенок сердца. Человек жалуется на повышенное АД, одышку, боль.
По степени проявления различают:
- латентную форму гипертрофии левого желудочка — симптомы отсутствуют, диагностируется по ЭхоКГ, часто коррелирует с повышенным уровнем ТТГ в крови;
- явную форму — возникают симптомы гипертрофии левого желудочка, часто - симптомы гипотиреоза.
По причине возникновения ГЛЖ бывает:
- физиологическая — диагностируется у спортсменов и людей с регулярными физическими нагрузками;
- патологическая — развивается на фоне генетических или приобретенных заболеваний.
Патологическая гипертрофия левого желудочка сердца вызвана артериальной гипертензией, аортальным пороком сердца и другими заболеваниями.
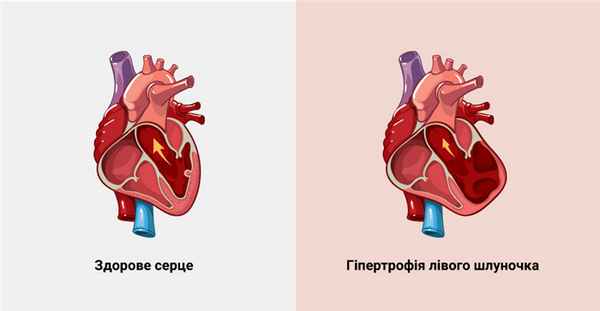
Этиология и патогенез
ГЛЖ – реакция сердца на чрезмерную нагрузку. Патология бывает приобретенной и врожденной.
Основные причины гипертрофии левого желудочка:
- занятие профессиональным спортом;
- кардиомиопатия;
- порок сердца (врожденный, приобретенный);
- кардиосклероз;
- патология почек;
- алкоголь;
- болезнь Фабри;
- ожирение;
- врожденная генная мутация;
- идиопатическая ГМЛЖ;
- ишемическая болезнь;
- малоподвижный образ жизни;
- артериальная гипертония;
- воспалительные процессы в организме;
- хронические болезни сердца и легких.
Ожирение и сахарный диабет вызывают метаболический синдром, который провоцирует увеличение и утолщение стенок ЛЖ. Патология может возникнуть также на фоне нескольких негативных факторов.
Прогрессирование гипертрофии левого желудочка приводит к несоответствию между растущей потребностью миокарда в кислороде и его нарушенной доставкой с кровью. Адаптивная (физиологическая) форма болезни перерастает в дезадаптивную (патологическую).
Стадии прогрессирования патологии:
- начальная — возникновения болезни;
- латентная — полная компенсация;
- стадия нарушенной компенсации с осложнениями — сердечная недостаточность, инфаркт, нарушение ритма сердца, внезапная смерть.
Изменения в сердце затрагивают всю сердечно-сосудистую систему. Возникает гипертрофия кардиомиоцитов, замещение мертвых кардиомиоцитов фиброзной тканью.
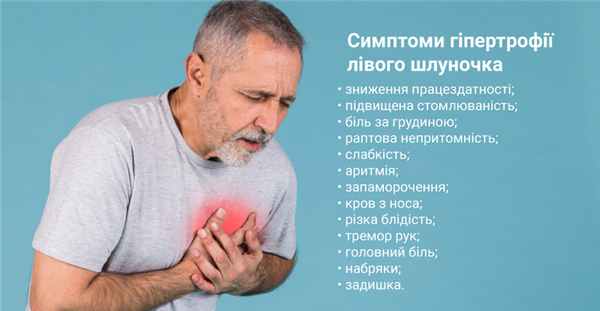
Симптомы и признаки гипертрофии левого желудочка
Заболевание на первых стадиях протекает бессимптомно. Признаки возникают, когда желудочек значительно увеличен.
Гипертрофия левого желудочка — симптомы:
- снижение работоспособности;
- повышенная утомляемость;
- боль за грудиной;
- внезапные обмороки;
- слабость;
- аритмия;
- головокружение;
- кровь из носа;
- резкая бледность;
- тремор рук;
- головная боль;
- отеки;
- одышка.
Стремительное увеличение ЛЖ может приводить к появлению мерцательной аритмии и стенокардии.
Особенности течения гипертрофии левого желудочка сердца у беременных
При гестации развиваются адаптивные изменения в сердечно-сосудистой системе. Повышаются сердечный выброс и частота сердечных сокращений, увеличивается объем циркулирующей крови, камер и ЛЖ без угнетения работы сердца. У беременных с сердечными патологиями нарушается адаптация левых отделов, что приводит к дисфункции, ухудшению маточно-плацентарного кровотока и нормального развития плода. Чтобы оценить риски, необходимо сделать ЭКГ и эхоКГ. В 80 % случаев беременность завершается благополучно.
Особенности ГЛЖ у детей
В период роста у ребенка увеличивается нагрузка на сердце. Нарастание массы ЛЖ вызвано врожденными патологиями или проблемами с кровообращением. Без лечения повреждаются сосуды легких, становятся жесткими, менее эластичными, усугубляя течение патологии. Заболевание может вызывать стеноз, чрезмерную нагрузку на сердце в утробе матери, аномалии строения перегородок. Симптомы гипертрофии левого желудочка появляются не сразу, поэтому рекомендуется сделать УЗИ сердца после рождения.
Гипертрофия левого желудочка: последствия и осложнения
Выраженная ГЛЖ опасна такими осложнениями:
- острая сердечная недостаточность;
- фибрилляция желудочка;
- внезапная смерть.
Развивается ишемия, мерцательная аритмия, инсульт.
Диагностика гипертрофии левого желудочка
Патология диагностируется в медицинском учреждении. Врач-кардиолог исследует сердечные камеры, направляет на дополнительное обследование, которое включает:
- УЗИ;
- холтеровское мониторирование;
- биохимию крови;
- магнитно-резонансную томографию;
- дуплексное сканирование аорты, измерение АД и пульса;
Лечение гипертрофии левого желудочка
Терапия направлена на устранение причин гипертрофии левого желудочка. Необходимо нормализовать рацион, режим дня, артериальное давление. Рекомендуется отказаться от вредных привычек и холестеринсодержащих продуктов питания. Показаны пешие прогулки, легкие физические упражнения.
Лечение гипертрофии левого желудочка включает прием таких групп препаратов:
- Блокаторы кальциевых каналов для устранения симптомов атеросклероза.
- Антиаритмические медикаменты, нормализующие сердечный ритм.
- Ингибиторы АПФ для снижения артериального давления.
- Сартаны, улучшающие работу мышцы.
- Бета-адреноблокаторы, которые снижают нагрузку на миокард.
Дозировка и длительность лечения определяется врачом.
Операции при гипертрофии левого желудочка
Если медикаментозное лечение не дало результатов, показано оперативное вмешательство:
- протезирование аорты для восстановления естественного просвета артерий;
- стентирование аорты — назначается при избытке атеросклеротических бляшек.
Перед операцией врач оценивает соотношение противопоказаний и необходимости хирургического вмешательства.
Контроль излеченности
Лечение гипертрофии левого желудочка считается успешным, если жизнь пациента продлена, уменьшены нарушения функционирования митрального клапана. Отсутствие прогресса болезни 6-9 месяцев говорит о правильно подобранном лечении. Если патологический процесс не сопровождается выраженными симптомами, стенка утолщена незначительно, терапия не требуется. Врач назначает корректировку образа жизни.
Профилактика гипертрофии левого желудочка
Чтобы избежать развития патологии, нужно уменьшить или отказаться полностью от кофе, спиртного, табачных изделий. Рекомендуется снизить количество употребляемой соли и жирной еды. Необходимо контролировать работу сердца, регулярно проходить обследование. Запрещены чрезмерные физические нагрузки, следует избегать стрессов и переживаний.
Советы и рекомендации
Специалисты советуют сбалансировать питание и включить в рацион такие продукты:
- сметану;
- кефир;
- злаковые;
- растительные жиры;
- молоко;
- курицу и рыбу;
- свежевыжатые соки, компоты.
Рекомендуется исключить из рациона соль, сладости, животные жиры, острые и пряные блюда. Питаться нужно дробно и часто. Ужин не позже чем за 3 часа до сна.
Статья носит информационно-ознакомительный характер. Пожалуйста, помните: самолечение может вредить вашему здоровью.
Гипертрофия левого желудочка при артериальной гипертензии и риск развития аритмий
Гипертрофия левого желудочка (ГЛЖ) является значимым независимым фактором риска не только общей и сердечно-сосудистой смертности, но и внезапной сердечной смерти. Вслед за повышением давления в гипертрофированном ЛЖ на фоне диастолической дисфункции миокарда очень быстро расширяется левое предсердие. Это приводит к возникновению наджелудочковой экстрасистолии, трепетанию и фибрилляции предсердий у 25%-50% пациентов с артериальной гипертонией (АГ). Связь между ГЛЖ, частотой и степенью выраженности желудочковых аритмий зависит от степени ГЛЖ и может отсутствовать на более близких к физиологическим ранних и средних стадиях. Ассоциация между ГЛЖ и спонтанно индуцированной желудочковой аритмией была подтверждена в хорошо контролируемых, экспериментальных исследованиях. К факторам аритмогенного риска у больных АГ с ГЛЖ относятся: поздние потенциалы желудочков, уменьшение вариабельности сердечного ритма, увеличение продолжительности QRS-комплекса и дисперсии интервала QT, а также альтернации Т-волны. Оценка риска развития аритмий у бессимптомных больных - трудная задача, которая может быть решена с помощью предложенного алгоритма.
Ключевые слова
Об авторах
Список литературы
1. Algra A., Tijssen J.G.P., Roelandt J.R.T.C., et al. Heart rate variability from 24-hour electrocardiography and the 2-year risk for sudden death. Circulation 1993; 88: 180-5.
2. Aronow W.S., Epstein S., Koenogsberg M., Schwartz K.S. Usefulnessof echocardiographic LVH ventricular tachycardia and complex ventricular arrhythmias in predicting ventricular fibrillation or sudden cardiac death in elderly patients. Am J Cardiol 1988; 62: 1124-5.
3. Aronson R. Mechanisms of arrhyihmias in ventricular hypertrophy. J Cardiovasc Eleclrophysiol 1991; 2: 249-61.
4. Brilla C.G., Matsubara L., Weber K.T. Advanced hypertensive heart disease in spontaneously hypertensive rat. Lisinopril-mediated regression of myocardial fibrosis. Hypertension 1996; 28: 269-75.
5. Chakko S., Mulintapang R.F., Huikuri H.V., et al. Alterations in heart rate variability and its circadian rhythm in hypertensive patients with left ventricular hypertrophy free of coronary artery disease. Am Heart J 1993; 126:1364-72.
7. Frohlich E.D. Risk mechanisms in hypertensive heart disease. Hypertension 1999; 34:782-9.
8. Lip G.Y.H., Felmeden D.C., Li-Saw-Hee F.L., Beevers D.G. Hypertensive heart disease. A complex syndrome or a hypertensive 'cardiomyopathy'? Eur Heart J 2000; 21: 1653-65.
9. Galinier M., Balanescu S., Fourcade J., et al. Prognostic value of arrhythmogenic markers in systemic hypertension. Eur Heart J 1997; 18:1484-91.
10. Ghali J.K., Kadakia S., Cooper R., Liao Y. Impact of LVH on ventricular arrhythmias in the absence of coronary artery disease. JACC 1991; 17:1277-82.
12. Gonzalez-Juanatey J.R., Garcia-Acuna J.M., Pose A., et al. Reduction of QL and QLc dispersion during long-term treatment of systemic hypertension with enalapril. Am J Cardiol 1998; 81: 170-4.
13. Hart G. Cellular electrophysiology in cardiac hypertrophy and failure. Cardhvasc Res 1994; 28: 933-46.
14. Hennersdorf M.G., Strauer B.E. Arterial hypertension and cardiac arrhythmias. J Hypertens 2001; 19: 167-77.
16. James M.A., Jones J.V. Ventricular arrhythmia in untreated newly presenting hypertensive patients compared with a matched normal population. J Hypertens 1989; 7:409-15.
17. Kannel W.B. Blood pressure as a cardiovascular risk factor. Engl J Med 1990; 322: 1561-6.
18. Kannel W.B. Prevalence and natural history of electrocardio-graphic left ventricular hypertrophy. Am J Med 1983; 75(Suppl. ЗА): 4-11.
19. Kaplan N.M. Systemic Hypertension: Mechanisms and Diagnosis. In: Heart Disease: Lextbook of Cardiovascular Medicine. BraunwaldE, ZipesD, Libby P. Eds.WB. Saunders Company 2001; 941-71.
20. Karpanou E.A., Vyssoulis G.P., Psichogios A., et al. Regression of left ventricular hypertrophy results in improvement of QL dispersion in patients with hypertension. Am Heart J 1998; 136: 765-8.
21. Kohya L., Yokoshiki H., Lohse N., et al. Regression of left ventricular hypertrophy prevents ischaemia-induced lethal arrhythmias. Beneficial effect of angiotensin II blockade. Circ Res 1995; 76: 892-9.
22. Koren M.J., Devereux R.B., Casale P.N., et al. Relation of left ventricular mass and geometry to morbidity and mortality in uncomplicated essential hypertension. Ann Intern Med 1991; 114: 345-52.
23. Kostis J.B., Lacy C.R., Shindler D.M., et al. Frequency of ventricular ectopic activity in isolated systolic systemic hypertension. Am J Cardiol 1992; 69: 557-9.
24. Krahn A.D., Manfreda J., Late R.B., et al. Lhe natural history of atrial fibrillation: incidence, risk factors, and prognosis in the Manitoba Follow-Up Study. Am J Med 1995; 98: 476-84.
25. Lavie C.J.Jr., Nunez B.D., Garavaglia G.E., Messerli F.H. Hypertensive concentric left ventricular hypertrophy: when is ventricular ectopic activity increased? South Med J 1988; 81: 696-700.
26. Levy D., Anderson K.M., Savane D.D., et al. Risk of ventricular arrhythmias in hypertension with left ventricular hypertrophy. Lhe Framingham Heart Study. Am J Cardiol 1987; 60: 560-5.
27. Lim P.O., Nys M., Naas A.A., et al. Irbesartan reduces QL dispersion in hypertensive individuals. Hypertension 1999; 33: 713-8.
28. Lindholm L.H., Dahlof B., Edelman J.E., et al. Effect of losartan on sudden cardiac death in people with diabetes: data from the LIFE study. Lancet 2003; 362: 619-20.
29. Lombardi H.C.A.F, Lerranova P., Hypertension and Concurrent Arrhythmias. Current Pharmaceutical Design 2003; 9(21): 1703-13.
31. Luque-Otero M., Perez Cascos F., Alcazar J. Increased ventricular arrhythmias in hypertension with left ventricular hypertrophy. J Hypertens 1986; 4(Suppl 6): 66-7.
32. Maimqvist K., Kahan T., Edner M., et al. Comparison of actions of irbesartan versus atenolol on cardiac repolarization in hypertensive left ventricular hypertrophy: results from the Swedish irbesartan left ventricular hypertrophy investigation versus atenolol (SILVHIA). Am J Cardiol 2002; 90: 1107-12.
33. Malerba M., Muiesan M.L., Zulli R., et al. Ventricular arrhythmias and changes in blood pressure and left ventricular mass induced by anti-hypertensive treatment in hypertensive patients. J Hypertens 1991; 9(Suppl. 6): SI62.
34. Manyari D.E., Patterson C., Johnson D., et al. Atrial and ventricular arrhythmias in asymptomatic active elderly subjects: correlation with left atrial size and left ventricular mass. Am Heart J 1990; 119: 1069-76.
35. Mayet J., Shahi M., McGrath K., et al. Left ventricular hypertrophy and QT dispersion in Hypertension. Hypertension 1996; 28: 791-6.
36. McLenachan J.M., Henderson E., Morris K.I., Dargie H.J. Ventricular arrhythmias in hypertensive left ventricular hypertrophy. N Engl J Med 1987; 317: 787-92.
38. Messerli F.H., Nunez B.D., Nunez M.M., et al. Hypertension and sudden death: disparate effects of calcium entry blocker and diuretic therapy on cardiac dysrhythmias. Arch Intern Med 1989; 149: 1263-7.
39. Messerli F.H. Hypertension and sudden cardiac death. Am J Hypertens 1999; 12: 181S-8.
40. Motz W., Vogt M., Rabenau D., et al. Evidence of endothelial dysfunction in coronary resistance vessels in patients with angina pectoris and normal coronary angiograms. Am J Cardiol 1991; 68:996-1003.
41. Novo S., Barbagallo M., Abrignani M.G., et al. Increased prevalence of cardiac arrhythmias and transient episodes of myocardial ischemia in hypertensives with left ventricular hypertrophy but without clinical history of coronary heart disease. Am J Hypertens 1997; 10: 843-51.
42. Pacifico A., Henry P.D. Structural pathways and prevention of heart failure and sudden death. J Cardiovasc Electrophysiol 2003; 14: 764-75.
43. Panza J.A., Quyami A.A., Brush J.E.Jr., Epstein S.E. Abnormal endothelium-dependent vascular relaxation in patients with essential hypertension. N Engl J Med 1990; 323: 22-7.
44. Perkiomaki J.S., Ikaheimo M.J., Pikkujamsa S.M., et al. Dispersion of the QT interval and autonomic modulation of the heart rate in hypertensive men with and without left ventricular hypertrophy. Hypertension 1996; 28: 16-21.
45. Pichard A.D., Gorlin R., Smith H., et al. Coronary flow studies in patients with left ventricular hypertrophy of the hypertensive type. Am J Cardiol 1981; 47: 547-54.
46. Rials S.J., Wu Y., Ford N., et al. Effect of left ventricular hypertrophy and its regression on ventricular electrophysiology and vulnerability to inducible arrhythmia in the feline heart. Circulation 1995;91:426-30.
47. Rosenbaum D.S., Jackson L.E., Smith J.M., et al. Electrical alternans and vulnerability to ventricular arrhythmias. N Engl J Med 1994; 330: 235-41.
49. Scheler S., Motz W., Strauer B.E. Transient myocardial ischemias in hypertensive patients. Z Kardiol 1990; 78: 197-203.
50. Schmieder R.E., Messerli F.H. Determinants of ventricular ectopy in hypertensive cardiac hypertrophy. Am Heart J 1992; 123: 89-95.
51. Schocn F.J. Systemic, (left-sided) hypertensive heart disease. In Pathologic Basis of Disease, Cotran R.S., Kumar V., Robbins S.L., Eds. W.B. Saunders Company Philadelphia 1994; 541-2.
52. Schwartzkopff B., Motz W., Frenzel H., et al. Structural and functional alterations of the intramyocardial coronary arterioles in patients with arterial hypertension. Circulation 1993; 88: 993-1003.
53. Siegel D., Cheitlin M.D., Black D.M., et al. Risk of ventricular arrhythmias in hypertensive men with left ventricular hypertrophy. Am J Cardiol 1990; 65: 742-7.
54. Singh J.P., Larson M.G., Tsuji H., et al. Reduced heart rate variability and new-onset Hypertension. Insight into pathogenesis of Hypertension: the Framingham Heart Study. Hypertension 1999; 32: 293-7.
55. Strauer B.E. The significance of coronary reserve in clinical heart disease. JACC 1990; 15: 774-83.
56. Strauer B.E. Hypertensive heart disease. Berlin-Heidelberg-New York-Tokyo: Springer-Verlag 1991.
57. Task Force of the European Society of Cardiology and the North American Society of Pacing and Electrophysiology. Heart Rate Variability. Standards of measurement physiological interpretation and clinical use. Circulation 1996; 93: 1043-65.
58. Kalian T., Bergfelt L. Left ventricular hypertrophy in hypertension: its arrhythmogenic potential. Heart 2005; 91: 250-6.
59. Verdecchia P., Angeli F., Borgioni C., et al. Changes in cardiovascular risk by reduction of left ventricular mass in hypertension: a meta-analysis. Am J Hypertens 2003; 11: 895-9.
60. Vester E.G., Kuhls S., Ochinlet-Vester J., et al. Electrophysiological and therapeutic implications of cardiac arrhythmias in hypertension. Eur Heart J 1992; 13(Suppl D): 70-81.
61. Vester E.G., Emschermann C., Stobbe U., et al. Late potentials and heart rate variability in heart muscle disease. Eur Heart J 1994; 15(SupplC): 25-33.
62. Wolk R. Arrhythmogenic mechanisms in left ventricular hypertrophy. Europace 2000; 2: 216-23.
63. Wolk R., Cobbe S.M. Cardiac arrhythmias in hypertrophy. In: Sheridan D.J., ed. Left Ventricular Hypertrophy. London: Churchill Livingstone 1998: 101-6.
64. Yokoshiki H., Kohya T., Tomita F., et al. Restoration of action potential duration and transient outward current by regression of left ventricular hypertrophy. J Moll Cell Cardiol 1997; 29: 1331-9.
65. Фомина И.Г., Шальнова C.A., Оганов P.Г. Артериальные гипертонии. В кн. Кардиология. Под ред. Оганова Р.Г., Фоминой И.Е Москва «Медицина» 2004; 266-306.
Гипертрофия левого желудочка сердца
Большая часть болезней сердечно-сосудистой системы сопровождается специфическим синдромом — гипертрофией левого желудочка. Состояние характеризуется увеличением массы сердца. Согласно медицинской статистике, за последние несколько лет возросло количество молодых пациентов с данной патологией. К тому же отмечается, что у таких больных опасность летального исхода выше, чем у престарелых. Мужчины с гипертрофией миокарда умирают в 7 раз чаще женщин. При чрезвычайной распространенности сердечно-сосудистых проблем важную роль в профилактике синдрома играют профилактические обследования.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обратиться к профильному специалисту.

Признаки гипертрофии левого желудочка на ЭКГ
Если у относительно здорового человека вес ЛЖ превышает ПЖ в среднем в 3 раза, то у больного соотношение увеличивается в несколько раз. Доступный и высокоточный метод обследования, электрокардиография, позволяет изучить функционирование сердца и имеющиеся отклонения. Гипертрофия ЛЖ проявляется на ЭКГ достаточно выраженно. Отмечаются следующие моменты:
- повышение зубца R в V6, V5, aVL;
- S-T ниже изоэлектрической линии;
- в V5 и V6 внутреннее уклонение увеличивается минимум на 0,05 с;
- двухфазность или инверсия зубца T в V6, V5, aVL и I.
Вышеуказанные проявления являются распространенными, но не единственными. Нередко отмечаются полные и неполные блокады. Больным с гипертрофией ЛЖ свойственна левограмма. Она подразумевает отклонение ЭОС влево. В момент возбуждения желудочка в правых грудных отведениях V1, V2 ЭКГ типа rS, в левых V5, V6 ЭКГ типа qR или qRs. При реполяризации:
- зубец TV6 ассиметричен и отрицателен;
- сегмент STV1 выше изолинии;
- STV6 ниже изолинии;
- TV1 положителен.
Подтверждение гипертрофии левого желудочка с назначением индивидуального лечения происходит при наличии высоких зубцов RV5, RV6 и глубоких SV1, SV2. Синдром TV1>TV6 сигнализирует о только начинающихся патологических изменениях. Помимо показателей кардиограммы, учитываются и общие признаки нездорового состояния:
- немотивированная слабость;
- ощущение биения сердца;
- нестабильное АД.
Причины эксцентрической, концентрической гипертрофии
Исходя из изменений структуры сердца выделяют два вида синдрома. Первый, эксцентрический, обусловлен расширением полости и стенок миокарда. Волокна мышц увеличиваются как в ширину, так и в длину. Эксцентрическая гипертрофия левого желудочка обусловливается:
- перегрузкой органа объемом;
- пороком сердца;
- инфарктом.
Если говорить о профессиональных спортсменах, то с такой проблемой сталкиваются пловцы, марафонцы, лыжники. Концентрическая гипертрофия сопровождается увеличением размеров миофибрилл и митохондрий без изменения объема полости. Возникает из-за:
- стойкого повышения АД;
- увеличения постнагрузки;
- высокого периферического сопротивления.
Часто сталкиваются с концентрическим синдромом спортсмены, занятые игровыми видами спорта, а также регулярно испытывающие статическую нагрузку. Концентрическая гипертрофия миокарда левого желудочка развивается у пациентов с:
- ИБС;
- кардиомиопатией;
- избыточным весом;
- нестабильным психоэмоциональным фоном;
- стенозом аорты;
- болезнями легких;
- пороками сердца.
К какому врачу обратиться?
Заболевание коварно своим скрытым развитием. Нередко первые стадии гипертрофии протекают для пациента незаметно. При повышенной утомляемости, постоянных или редких болях в груди, одышке и головокружениях необходимо обратиться к:
Электрокардиография
Стандартная электрокардиограмма представляет собой 12-векторное отображение электрической активности сердца как отражение разницы электрических потенциалов между положительными и отрицательными электродами, помещенными на конечности и грудную клетку. Шесть из данных отведений вертикальные (получаемые от фронтально расположенных электродов I, II и III и электродов, расположенных на конечностях – aVR, aVL, aVF) и 6 – горизонтальные (расположенные в прекардиальной области – V1, V2, V3, V4, V5, и V6). ЭКГ в 12 отведениях может быть решающим методом исследования для установления большого количества кардиологических диагнозов (см. таблицу Интерпретация изменений ЭКГ Интерпретация изменений ЭКГ ), включая
Гипертрофия желудочков (см. таблицу Критерии ЭКГ-диагностики гипертрофии левого желудочка Критерии ЭКГ-диагностики гипертрофии левого желудочка )
Для получения дополнительной информации по интерпретации ЭКГ, см. Обзор аритмий (Overview of Arrhythmias) Диагностика Здоровое сердце бьется регулярным, скоординированным образом благодаря тому, что электрические импульсы в сердце генерируются и распространяются миоцитами с уникальными электрическими свойствами. Прочитайте дополнительные сведенияСтандартные компоненты электрокардиографического комплекса
Общепринято деление кривой ЭКГ на зубец Р, интервал PR, комплекс QRS, интервал QТ, сегмент ST, зубец Т и зубец U (см. рисунок Волны ЭКГ Электрокардиографические (ЭКГ) волны ).
Электрокардиографические (ЭКГ) волны
Зубец Р = отражает деполяризацию предсердий. Интервал PR = временной интервал от начала деполяризации предсердий до начала деполяризации желудочков. Комплекс QRS = деполяризация желудочков, состоит из зубцов Q, R и S. Интервал Q-T = время между началом деполяризации желудочков и окончанием их реполяризации. Интервал R-R = временной интервал между двумя комплексами. Зубец Т = реполяризация желудочков. Сегмент ST + зубец T (ST-T) = реполяризация желудочков. Зубец U = вероятно, постдеполяризация (расслабление) желудочков.
Зубец Р
P-волна тражает деполяризацию предсердий. В большинстве отведений, за исключением aVR, он положительный. В отведениях II и V1 он может быть двухфазным; начальный сегмент зубца отражает возбуждение правого предсердия, конечный сегмент – левого предсердия.
Увеличение амплитуды любого из сегментов возникает при увеличении предсердий. Увеличение правого предсердия обуславливает появление зубца Р > 2 мм в отведениях ІІ, ІІІ и усиленном отведении от левой ноги (Р pulmonale); увеличение левого предсердия приводит к появлению широкого зубца P с двойным пиком в отведении ІІ (P mitrale). В норме ось зубца находится между 0 и 75 ° .
Интервал PR
Представляет собой промежуток от начала деполяризации предсердий до начала деполяризации желудочков. В норме он составляет 0,10–0,2 секунды; удлинение данного интервала свидетельствует об атриовентрикулярной блокаде I степени.
Комплекс QRS
Отражает деполяризацию желудочков.
Зубец Q представляет собой первый направленный вниз зубец комплекса. В норме зубец Q длится < 0,05 секунд во всех отведениях, за исключением V1–V3, в которых любой зубец Q считается патологическим и указывает на перенесенный или острый инфаркт.
Зубец R – первый направленный вверх компонент комплекса. Критерии его нормальной высоты и размера относительны, однако увеличение высоты зубцов R – признак гипертрофии желудочков. Второй положительный компонент комплекса QRS – зубец, обозначаемый R’.
Зубец S – 2-ой отрицательный компонент комплекса в том случае, если присутствует зубец, и 1-й, если его нет.
Комплекс может быть представлен изолированно зубцом, сегментами QS (без R), QR (без S), RS (без Q), а также комплексом RSR’ в зависимости от отведения, вектора сердца и наличия заболеваний органа.
В норме интервал QRS составляет 0,07–0,10 секунды. Продолжительность комплекса 0,10 – 0,11 секунды расценивают как неполную блокаду ножки пучка Гиса или неспецифическое замедление внутрижелудочкового проведения, в зависимости от изменений формы комплекса QRS. Длительность интервала ≥ 0,12 секунды указывает на полную блокаду ножки пучка Гиса или на замедление внутрижелудочковой проводимости.
В норме ось QRS находится между 90 и −30 ° . Значение электрической оси сердца от −30 ° до −90 ° рассматривается как отклонение электрической оси сердца влево и наблюдается при блокаде передней ветви левой ножки пучка Гиса (−60 ° ) и нижнем инфаркте миокарда.
Значение электрической оси сердца от 90 ° до 180 ° рассматривается, как отклонение электрической оси сердца вправо; оно наблюдается при любом состоянии, которое ведет к увеличению лёгочного давления и гипертрофии правого желудочка сердца (cor pulmonale, острая тромбоэмболия лёгочной артерии, лёгочная гипертензия), и иногда возникает при блокаде правой или задней ветви левой ножки пучка Гиса.
Интервал QT
Временной промежуток между началом деполяризации желудочков и окончанием их реполяризации. Интервал QT должен рассчитываться с учетом сердечного ритма при помощи формулы:
где QTc должное значение интервала QT, а R-R – временной интервал между двумя комплексами QRS. Все интервалы записываются в секундах. Удлинение интервала QTc имеет тесную связь с развитием тахикардии типа "пируэт" Синдром удлинённого интервала QT и двунаправленная желудочковая тахикардия Пируэтная тахикардия – это специфическая форма полиморфной ЖТ у пациентов с синдромом удлиненного интервала QT. Она характеризуется быстрыми нерегулярными QRS-комплексами, которые выглядят как. Прочитайте дополнительные сведения . Определить интервал QTc часто бывает непросто из-за того, что окончание зубца Т часто нечетко определено или за ним следует волна U. Существуют многочисленные препараты, приводящие к удлинению интервала QT (см. CredibleMeds).
Сегмент ST
Сегмент ST отражает окончание деполяризации миокарда желудочков. В норме он располагается горизонтально на изолинии аналогично интервалу P-R (или Т-Р) либо немного смещен с изолинии.
Подъем сегмента ST может быть вызван:
Гипертрофией левого желудочка
Ишемией и инфарктом миокарда
Аневризмой левого желудочка
Тромбоэмболией легочной артерии
Депрессия сегмента ST может быть вызвана:
Реципрокными изменениями при остром инфаркте миокарда
Зубец T
Отражает реполяризацию желудочков. В норме он имеет ту же направленность, что и комплекс QRS (конкордантен), обратная направленность (дискордантность) может свидетельствовать о текущем или перенесенном ИМ. Зубец Т обычно имеет сглаженную, закругленную форму, однако в условиях гипокалиемии и гипомагниемии он может иметь низкую амплитуду, а при гиперкалиемии и гипокальциемии заостренную форму.
Зубец U
Зубец U обычно появляется у больных с гипокалиемией, гипомагниемией или ишемией. Зубец U часто присутствует у здоровых людей.
Специальные электрокардиографические тесты
Стандартная ЭКГ в 12 отведениях отражает только отдельный короткий период сердечной активности, в то время как усовершенствованные методики позволяют получить дополнительную информацию.
Дополнительные грудные отведения
Дополнительные прекардиальные отведения используются для диагностики
Инфаркт правого желудочка
Инфаркт задней стенки
Электроды для правых грудных отведений накладывают на правую сторону грудной стенки зеркально стандартным левым грудным электродам. Их обозначают как V1R–V6R; иногда применяют только V4R, как наиболее чувствительное отведение для диагностики инфаркта миокарда правого желудочка.
Электроды для дополнительных однополюсных отведений могут размещаться в 5-ом межрёберном пространстве, V7 – возле заднеподмышечной линии, V8 – возле среднелопаточной линии и V9 – у левого края позвоночника. Эти отведения используют редко, но они могут быть особенно полезны для диагностики истинно заднего инфаркта миокарда.
Пищеводное отведение
Пищеводный электрод расположен значительно ближе к предсердию, чем наружные электроды. Его применяют, когда при стандартной ЭКГ зубец Р регистрируется неопределенно, а также если необходимо уточнение электрической активности предсердий при тахикардии с широким желудочковым комплексом (необходимость верификации ее предсердного или желудочкового варианта), либо при подозрении на атриовентрикулярную диссоциацию. Пищеводное отведение также можно использовать для интраоперационного мониторирования ишемии миокарда или выявления активности предсердий при кардио-плегии. Пациент проглатывает электрод, который затем присоединяют к обычному электрокардиографу, чаще всего к порту II отведения.
Анализ усредненной записи
Усреднение сигнала комплексов QRS образует цифровую структуру нескольких сотен сердечных циклов, позволяющую выявить высокочастотные, низкоамплитудные потенциалы и микротоки в терминальной части QRS-комплекса. Данные находки позволяют обнаружить зоны замедления проведения через аномальный мио-кард и, как следствие, выявить высокий риск развития желудочковой тахикардии с участием синдрома риентри.
Сигнал-усреднённая ЭКГ – всё ещё остается в основном экспериментальной техникой, однако иногда используется для оценки риска внезапной сердечной смерти (например, у пациентов с известным значимым заболеванием сердца). Данная техника кажется наиболее полезной для выявления пациентов с низким риском внезапной смерти. Не было обнаружено ценности этой методики для обнаружения пациентов с высоким риском внезапной сердечной смерти.
Усреднение сигнала также исследуется как метод диагностики при различных других заболеваниях сердца: от постинфарктного состояния и кардиомиопатий до синдрома Бругада и желудочковых аневризм, а также для оценки эффективности хирургической коррекции аритмий. Данная методика может быть полезной для оценки проаритмогенных эффектов антиаритмических препаратов и выявления отторжения сердечных трансплантатов.
Обнаружение изолированных изменений зубца помогает выявить пациентов с риском развития мерцательной аритмии.
Продолжительное мониторирование сегмента ST
Продолжительное мониторирование сегмента ST используют для выявления ишемии и тяжелых аритмий. Мониторирование может быть автоматизировано (существуют специальные электронные мониторы) или выполняться при клиническом анализе серии электрокардиограмм. Показания включают мониторирование в отделениях интенсивной терапии у больных с нарастающей стенокардией, состояние после чрескожной интервенции, интраоперационное мониторирование и послеоперационное наблюдение.
Дисперсия интервала QT
Дисперсия интервала QT (разность между самым длинным и самым коротким интервалом при ЭКГ-записи в 12 отведениях) предложена как метод оценки гетерогенности реполяризации миокарда. Увеличенная дисперсия (≥ 100 миллисекунд) свидетельствует об электрической гетерогенности миокарда, обусловленной ишемией или фиброзом, что повышает риск развития аритмий с механизмом риентри и внезапной смерти. Дисперсия может быть предиктором риска смерти, однако определяется редко, поскольку высока распространенность ошибки измерения и часто возможен перекрест значений у пациентов с заболеваниями сердца и здоровых, не существует границ возможной погрешности, а кроме того, существуют другие критерии риска данных состояний.
Вариабельность сердечного ритма
Отражает соотношение между симпатической и парасимпатической (вагусной) стимуляцией сердца. Сниженная вариабельность соответствует снижению влияния блуждающего нерва и повышению симпатического тонуса и является предиктором высокого риска развития аритмий и смерти. Наиболее распространенный метод исследования вариабельности сердечного ритма – расчет стандартного отклонения всех нормальных интервалов R-R при суточном ЭКГ-мониторировании.
Вариабельность сердечного ритма используется в основном в исследованиях. Данные свидетельствуют о том, что они предоставляют полезную информацию о дисфункции левого желудочка после инфаркта миокарда Острый инфаркт миокарда (ИМ) Острое поражение миокарда - это миокардиальный некроз в результате резкой обструкции коронарной артерии. Симптоматика данных состояний включает дискомфорт в грудной клетке, сопровождающийся. Прочитайте дополнительные сведения , и гипертрофической кардиомиопатии Гипертрофическая кардиомиопатия Гипертрофическая кардиомиопатия – врожденное или приобретенное заболевание, характеризующееся выраженной гипертрофией миокарда желудочков с диастолической дисфункцией, но без увеличенной постнагрузки. Прочитайте дополнительные сведенияХолтеровское мониторирование
Холтеровское мониторирование – длительное мониторирование и запись данных ЭКГ в течение 24–48 часов. Метод необходим для выявления преходящих аритмий, а также обнаружения артериальной гипертензии. Холтеровские мониторы портативны, позволяют пациенту сохранить обычный распорядок дня. Кроме того, их можно применять у больных, вынужденных занимать сидячее положение, на госпитальном этапе, в том случае если стационарный монитор невозможно использовать. Пациентов просят отмечать все ощущения и свою активность во время мониторирования, чтобы сопоставить эти данные с показателями на мониторе. Холтеровский монитор самостоятельно не анализирует данные ЭКГ; это выполняет врач после окончания исследования.
Регистратор событий
Использование датчиков событий позволяет проводить непрерывное наблюдение за больным до 30 дней, в течение которых можно выявить редкие нарушения ритма, пропускаемые при 24-часовом холтеровском мониторировании. Регистрирующее устройство может работать непрерывно или активируется самим пациентом в момент появления симптомов. Память прибора позволяет сохранять информацию о событиях за несколько секунд до и после активации. Пациент может передавать данные ЭКГ для расшифровки доктору как по телефону, так и при помощи спутниковой связи; некоторые регистраторы могут автоматически передавать данные о серьёзных событиях. Если у пациента значимые события (например, синкопе) происходят чаще, чем раз в 30 дней, то регистратор событий можно внедрить подкожно (имплантируемый петлевой регистратор). Он активируется при помощи маленького магнита. Срок службы батареи подкожного регистратора составляет несколько лет.
Беспроводной клеящийся кардиомонитор
Новый способ одноканального контроля ритма – небольшое, клеящееся, водостойкое, беспроводное и одноразовое устройство, которое крепится на груди. Один из типов такого устройства записывает сердечный ритм до 2 недель. Другое сходное устройство функционирует как регистратор событий. Для того, чтобы записать сохранённые данные ЭКГ за 45 секунд до и 15 секунд после события, пациент нажимает на кнопку на устройстве тогда, когда ощущает симптомы, потенциально связанные с аритмией (например, ощущение сильного сердцебиения, головокружение). Однако в отличие от регистратора событий, автоматизированный отчет в реальном времени недоступен.
Дополнительная информация
Ниже следуют некоторые англоязычные ресурсы, которые могут быть информативными. Обратите внимание, что The manual не несет ответственности за содержание этих ресурсов.
University of Utah ECG Learning Center: обеспечивает интерактивное учебное руководство по клинической электрокардиографии
CredibleMeds QTDrugs List: предоставляет информацию о препаратах, которые способствуют риску развития желудочковых аритмий, или подозреваются в этом
Авторское право © 2022 Merck & Co., Inc., Rahway, NJ, США и ее аффилированные лица. Все права сохранены.
Читайте также:
