Врожденная аплазия кожи у новорожденного
Добавил пользователь Alex Обновлено: 22.01.2026
Врожденная аплазия кожи у новорожденного
Врожденная аплазия кожи - гетерогенная группа заболеваний, общим признаком которых является врожденное отсутствие кожи. Хотя причина аплазии неизвестна, само состояние регистрируется вот уже более 250 лет.
В классической форме аплазия кожи проявляется одной или несколькими эрозиями или изъязвлениями, покрытыми коркой или тонкой оболочкой, на макушке волосистой части головы. Заживление в форме атрофических, лишенных волос рубцов происходит в течение 2-6 мес. в зависимости от размера и глубины изъязвлений (которые могут распространяться на всю глубину мягких тканей вплоть до кости).
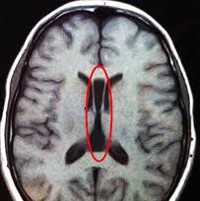
Это доброкачественное состояние может наследоваться по аутосомно-доминантному признаку или возникать спорадически. Реже встречается поражение туловища и конечностей, такие очаги могут ассоциироваться с дефектами конечностей, БЭ и хромосомными аномалиями. Очаг на волосистой части головы с кольцом окружающих его длинных темных волос (признак «волосяного воротничка») представляет собой дефект вследствие неполного заращения невральной трубки. Для оценки возможной связи с подлежащими участками мозга и кости показана МРТ.
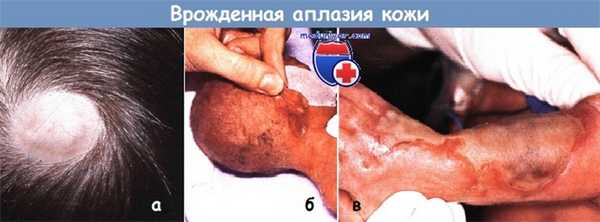
Врожденная аплазия кожи:
а - изолированный дефект кожи наблюдался на руке новорожденного
б - у этого недоношенного ребенка с небольшим дефектом на задней части шеи гемиатрофия правой стороны тела (синдром Адамса-Оливера).
При неосложненной врожденной аплазии кожи дефект корректируется простым иссечением в позднем детском или во взрослом возрасте. В случае крупных очагов может потребоваться поэтапное иссечение и применение тканевых экспандеров. У новорожденных необходимо оценить глубину дефекта, предупредить повреждение ткани и инфекцию и обследовать ребенка на наличие сочетанных аномалий.
Мягкие компрессы с физиологическим раствором, местное применение антибиотиков и наложение стерильных повязок являются адекватными терапевтическими мероприятиями для большинства пациентов. Для ведения пациентов с крупными дефектами применяются герметичные повязки (Duoderm®, Comfeel®). Иногда необходимо раннее хирургическое вмешательство.
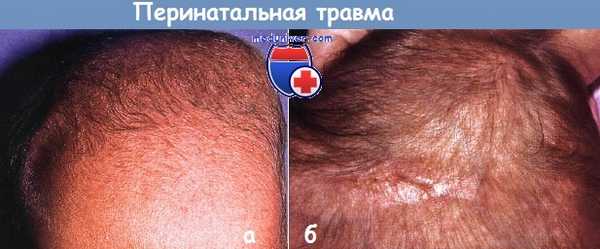
Перинатальная травма:
а - цефалогематома. Просачивание крови под надкостницу, обычно разрешается без особенностей.
б - редких случаях перинатальная травма приводит к образованию кольцевидного венчика на волосистой части головы с рубцеванием и перманентной утратой волос.
Перинатальная травма головы может привести к подобным дефектам, которые обнаруживают при рождении или в первый месяц жизни. Взятие крови в области волосистой части головы, электроды монитора и щипцы могут привести к образованию небольших язвочек, которые заживают с рубцеванием.
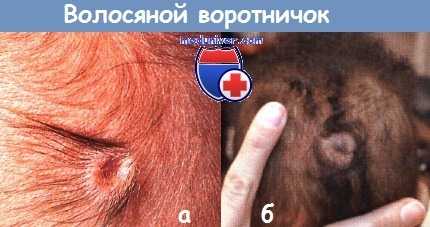
а - признак «волосяного воротничка» на волосистой части головы у новорожденного.
б - у этого здорового 4-месячного ребенка признак «волосяного воротничка».
МРТ не вывила никакой аномалии подлежащих структур.
Безволосый кольцевидный венчик на волосистой части головы - еще одна форма локализованной травмы головы, в редких случаях ассоциирующейся с родовой опухолью и цефалгематомой, которая иногда разрешается с рубцовой алопецией.
Врожденную аплазию кожи напоминают другие невоидные дефекты, часто проявляющиеся в форме лишенных волос пятен на волосистой части головы. Однако эти родимые пятна не покрываются коркой и не бывают атрофическими и обычно имеют характерные клинические признаки. Некоторые врожденные, слабо пигментированные пигментные невусы на волосистой части головы также могут имитировать врожденную аплазию кожи.
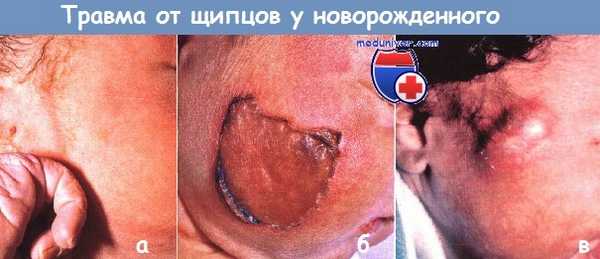
Дефекты, похожие на врожденную аплазию кожи:
а - травмы от щипцов чаще всего ассоциируются с образованием гематомы без нарушения кожных покровов.
Однако в редких случаях случается (б) поверхностный некроз и (в) жировой некроз.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Врожденная аплазия кожи
Врожденная аплазия кожи – группа состояний неясной этиологии, которые характеризуются очаговым нарушением формирования кожных покровов с развитием рубцов. Симптомы этого состояния выявляются сразу после рождения ребенка, у которого наблюдается одна или несколько эрозий или изъязвлений на коже головы или, очень редко, на других участках тела. Диагностика врожденной аплазии кожи осуществляется на основании данных осмотра дерматологом, гистологического изучения тканей в очаге поражения. Лечение только симптоматическое с целью недопущения развития вторичной инфекции, но возможна хирургическая коррекция рубцов для уменьшения косметического дефекта.
Общие сведения
Врожденная аплазия кожи – это очаговый дефект развития кожи, при котором нарушается формирование эпидермиса, дермы, придатков, а в особо тяжелых случаях и подкожной клетчатки. Это состояние известно человечеству уже более 250 лет, однако выявить причины его развития до сих пор не удалось, в дерматологии имеются лишь теории на этот счет. Встречаемость врожденной аплазии кожи точно неизвестна, большинство исследователей оценивают ее на уровне 1:10000. Иногда такое состояние сочетается с некоторыми генетическими заболеваниями, другими пороками внутриутробного развития. Врожденная аплазия кожи в большинстве случаев не приводит к тяжелым последствиям, однако косметический дефект в виде рубца на месте патологического очага остается у человека на всю жизнь.
Причины врожденной аплазии кожи
На сегодняшний день нет единой и общепризнанной теории, которая бы объясняла развитие этого врожденного дефекта развития кожи. Предполагается, что причиной врожденной аплазии кожи является целая группа различных патологических факторов, которые ведут к нарушению процесса закрытия нервной трубки или же тормозят развитие эмбриональных зачатков дермы и эпидермиса. Иногда удается выявить семейные формы этого состояния, при этом механизм его наследования, предположительно, аутосомно-доминантный. Но намного чаще встречаются спорадические формы врожденной аплазии кожи, причем иногда в сочетании с другими пороками развития, обусловленные генетическими заболеваниями или воздействием тератогенных факторов. Это дает повод рассматривать данное состояние как следствие влияния на формирующийся плод различных повреждающих факторов.
Симптомы врожденной аплазии кожи
Аплазия кожи выявляется сразу после рождения ребенка. Чаще всего на теменной области обнаруживается очаг округлой формы диаметром 1-3 сантиметра. Примерно в трети случаев возникает два очага, еще реже встречаются три и более участка аплазии кожи. Патологический участок представляет собой эрозию или язву, покрытую корочкой и грануляциями, волосяной покров на нем отсутствует. Однако вокруг язвы вырастают более длинные и темные волоски, что получило название симптома «волосяного воротничка». Цвет образования варьируется от розового до ярко-красного.
Со временем, при отсутствии осложнений (вторичной инфекции, например), участок врожденной аплазии кожи начинает разрешаться с образованием рубца белого цвета. На нем в дальнейшем также не вырастают волосы, и он остается у человека на всю жизнь. Помимо кожных симптомов, у ребенка с очагом врожденной аплазии кожи могут регистрироваться нарушения формирования более глубоко расположенных тканей и другие пороки развития – заячья губа, волчья пасть, атрофия глаз. У детей старшего возраста и взрослых на месте рубца иногда могут развиваться злокачественные новообразования.
Диагностика врожденной аплазии кожи
Распознавание этого заболевания обычно не представляет труда для врача-дерматолога – его симптоматика достаточно специфична, и спутать его с другими врожденными кожными состояниями довольно сложно. Однако в некоторых случаях похожую на врожденную аплазию кожи картину могут иметь и иные патологические процессы и состояния. Поэтому необходимо производить дифференциальную диагностику этой патологии с такими заболеваниями, как очаговая склеродермия, дискоидная красная волчанка, а также с последствиями перинатальной травмы (от щипцов и других акушерских инструментов). Очень похожи на аплазию семейные формы гипоплазии кожи лица, однако при этом атрофические очаги наблюдаются в области висков.
Наиболее точные диагностические данные может дать гистологическое изучение тканей патологического очага. При врожденной аплазии кожи наблюдается резкое уменьшение толщины (вплоть до 1-го слоя клеток) эпидермиса, дермы, иногда подкожной клетчатки. Признаков воспаления и лейкоцитарной инфильтрации (при отсутствии вторичной инфекции) не наблюдается, также не выявляют придатков кожи.
Лечение и прогноз врожденной аплазии кожи
Лечение врожденной аплазии кожи условно разделяется на два этапа. Первый производится непосредственно после рождения ребенка – в этот период показаны только профилактические и уходовые мероприятия (обработка эрозий антибактериальными мазями, увлажняющими средствами), наложение повязки для уменьшения риска травмирования. Через несколько недель на месте патологического очага сформируется рубец, который хоть и остается на всю жизнь, но может быть прикрыт окружающими волосами. Второй этап сводится к хирургическому устранению дефекта (чаще всего, по косметическим причинам), и проводить его можно в позднем детском или взрослом возрасте. При коррекции значительных по площади участков врожденной аплазии кожи может применяться пересадка кожи. Прогноз заболевания в целом благоприятный, некоторые исследователи указывают на необходимость ежегодного осмотра рубца у дерматолога из-за риска развития онкологических процессов.
Аномалии развития головного мозга ( Пороки развития головного мозга )
Аномалии развития головного мозга — это результат происходящих во внутриутробном периоде нарушений формирования отдельных церебральных структур или головного мозга в целом. Зачастую имеют неспецифическую клиническую симптоматику: преимущественно эпилептический синдром, задержку психического и умственного развития. Тяжесть клиники напрямую коррелирует со степенью поражения головного мозга. Диагностируются антенатально при проведении акушерского УЗИ, после рождения — при помощи ЭЭГ, нейросонографии и МРТ головного мозга. Лечение симптоматическое: противоэпилептическое, дегидратационное, метаболическое, психокоррегирующее.
МКБ-10
Причины
Наиболее весомой причиной сбоев внутриутробного развития является влияние на организм беременной и на плод, различных вредоносных факторов, обладающих тератогенным действием. Возникновение аномалии в результате моногенного наследования встречается лишь в 1% случаев. Наиболее влиятельной причиной пороков головного мозга считается экзогенный фактор. Тератогенным эффектом обладают многие активные химические соединения, радиоактивное загрязнение, отдельные биологические факторы. Немаловажное значение здесь имеет проблема загрязнения среды обитания людей, обуславливающая поступление в организм беременной токсических химических веществ.
Различные эмбриотоксические воздействия могут быть связаны с образом жизни самой беременной: например, с курением, алкоголизмом, наркоманией. Дисметаболические нарушения у беременной, такие как сахарный диабет, гипертиреоз и пр., могут также стать причиной церебральных аномалий плода. Тератогенным действием обладают и многие медикаменты, которые может принимать женщина в ранние сроки беременность, не подозревая о происходящих в ее организме процессах. Мощный тератогенный эффект оказывают инфекции, перенесенные беременной, или внутриутробные инфекции плода. Наиболее опасны цитомегалия, листериоз, краснуха, токсоплазмоз.
Патогенез
Дифференцировка нейробластов (зародышевых нервных клеток) приводит к образованию нейронов, формирующих серое вещество, и глиальных клеток, составляющих белое вещество. Серое вещество отвечает за высшие процессы нервной деятельности. В белом веществе проходят различные проводящие пути, связывающие церебральные структуры в единый функционирующий механизм. Рожденный в срок новорожденный имеет такое же число нейронов, как и взрослый человек. Но развитие его мозга продолжается, особенно интенсивно в первые 3 мес. жизни. Происходит увеличение глиальных клеток, разветвление нейрональных отростков и их миелинизация.
Сбои могут произойти на различных этапах формирования головного мозга. Если они возникают в первые 6 мес. беременности, то способны приводить к снижению числа сформированных нейронов, различным нарушениям в дифференцировке, гипоплазии различных отделов мозга. В более поздние сроки может возникать поражение и гибель нормально сформировавшегося церебрального вещества.
Виды аномалий мозга
Анэнцефалия — отсутствие головного мозга и акрания (отсутствие костей черепа). Место головного мозга занято соединительнотканными разрастаниями и кистозными полостями. Может быть покрыто кожей или обнажено. Патология несовместима с жизнью.
Энцефалоцеле — пролабирование церебральных тканей и оболочек через дефект костей черепа, обусловленный его незаращением. Как правило, формируется по средней линии, но бывает и асимметричным. Небольшое энцефалоцеле может имитировать кефалогематому. В таких случаях определить диагноз помогает рентгенография черепа. Прогноз зависит от размеров и содержимого энцефалоцеле. При небольших размерах выпячивания и наличии в его полости эктопированной нервной ткани эффективно хирургическое удаление энцефалоцеле.
Микроцефалия — уменьшение объема и массы головного мозга, обусловленное задержкой его развития. Встречается с частотой 1 случай на 5 тыс. новорожденных. Сопровождается уменьшенной окружностью головы и диспропорциональным соотношением лицевого/мозгового черепа с преобладанием первого. На долю микроцефалии приходится около 11% всех случаев олигофрении. При выраженной микроцефалии возможна идиотия. Зачастую наблюдается не только ЗПР, но и отставание в физическом развитии.
Макроцефалия — увеличение объема головного мозга и его массы. Гораздо менее распространена, чем микроцефалия. Макроцефалия обычно сочетается с нарушениями архитектоники мозга, очаговой гетеротопией белого вещества. Основное клиническое проявление — умственная отсталость. Может наблюдаться судорожный синдром. Встречается частичная макроцефалия с увеличением лишь одного из полушарий. Как правило, она сопровождается асимметрией мозгового отдела черепа.
Кистозная церебральная дисплазия — характеризуется множественными кистозными полостями головного мозга, обычно соединенными с желудочковой системой. Кисты могут иметь различный размер. Иногда локализуются только в одном полушарии. Множественные кисты головного мозга проявляются эпилепсией, устойчивой к антиконвульсантной терапии. Единичные кисты в зависимости от размера могут иметь субклиническое течение или сопровождаться внутричерепной гипертензией; зачастую отмечается их постепенное рассасывание.
Голопрозэнцефалия — отсутствие разделения полушарий, в результате чего они представлены единой полусферой. Боковые желудочки сформированы в единую полость. Сопровождается грубыми дисплазиями лицевого черепа и соматическими пороками. Отмечается мертворождение или гибель в первые сутки.
Агирия (гладкий мозг, лиссэнцефалия) — отставание развития извилин и тяжелое нарушение архитектоники коры. Клинически проявляется выраженным расстройством психического и моторного развития, парезами и различными формами судорог (в т. ч. синдромом Веста и синдромом Леннокса-Гасто). Обычно заканчивается летальным исходом на первом году жизни.
Пахигирия — укрупнение основных извилин при отсутствии третичных и вторичных. Сопровождается укорочением и выпрямлением борозд, нарушением архитектоники церебральной коры.
Микрополигирия — поверхность коры мозга представлена множеством мелких извилин. Кора имеет до 4-х слоев, тогда как в норме кора насчитывает 6 слоев. Может быть локальной или диффузной. Последняя, полимикрогирия, характеризуется плегией мимических, жевательных и глоточных мышц, эпилепсией с дебютом на 1-ом году жизни, олигофренией.
Гипоплазия/аплазия мозолистого тела. Часто встречается в виде синдрома Айкарди, описанного только у девочек. Характерны миоклонические пароксизмы и сгибательные спазмы, врожденные офтальмические пороки (колобомы, эктазия склеры, микрофтальм), множественные хориоретинальные дистрофические очаги, обнаруживаемые при офтальмоскопии.
Фокальная корковая дисплазия (ФКД) — наличие в коре головного мозга патологических участков с гигантскими нейронами и аномальными астроцитами. Излюбленное расположение — височные и лобные зоны мозга. Отличительной особенностью эпиприступов при ФКД является наличие кратковременных сложных пароксизмов с быстрой генерализацией, сопровождающихся в своей начальной фазе демонстративными двигательными феноменами в виде жестов, топтания на одном месте и т. п.
Гетеротопии — скопления нейронов, на этапе нейронной миграции задержавшихся на пути своего следования к коре. Гетеротопионы могут быть единичными и множественными, иметь узловую и ленточную форму. Их главное отличие от туберозного склероза — отсутствие способности накапливать контраст. Эти аномалии развития головного мозга проявляются эписиндромом и олигофренией, выраженность которых прямо коррелирует с числом и размером гетеротопионов. При одиночной гетеротопии эпиприступы, как правило, дебютируют после 10-летнего возраста.
Диагностика
Тяжелые аномалии развития головного мозга зачастую могут быть диагностированы при визуальном осмотре. В остальных случаях заподозрить церебральную аномалию позволяет ЗПР, гипотония мышц в неонатальном периоде, возникновение судорожного синдрома у детей первого года жизни. Исключить травматический или гипоксический характер поражения головного мозга можно при отсутствии в анамнезе данных о родовой травме новорожденного, гипоксии плода или асфиксии новорожденного. Пренатальная диагностика пороков развития плода осуществляется путем скринингового УЗИ при беременности. УЗИ в I триместре беременности позволяет предупредить рождение ребенка с тяжелой церебральной аномалией.
Одним из методов выявления пороков головного мозга у грудничков является нейросонография через родничок. Намного более точные данные у детей любого возраста и у взрослых получают при помощи МРТ головного мозга. МРТ позволяет определить характер и локализацию аномалии, размеры кист, гетеротопий и других аномальных участков, провести дифференциальную диагностику с гипоксическими, травматическими, опухолевыми, инфекционными поражениями мозга. Диагностика судорожного синдрома и подбор антиконвульсантной терапии осуществляется при помощи ЭЭГ, а также пролонгированного ЭЭГ-видеомониторинга. При наличии семейных случаев церебральных аномалий может быть полезна консультация генетика с проведением генеалогического исследования и ДНК-анализа. С целью выявления сочетанных аномалий проводится обследование соматических органов: УЗИ сердца, УЗИ брюшной полости, рентгенография органов грудной полости, УЗИ почек и пр.
Лечение аномалий мозга
Терапия пороков развития головного мозга преимущественно симптоматическая, осуществляется детским неврологом, неонатологом, педиатром, эпилептологом. При наличии судорожного синдрома проводится антиконвульсантная терапия (карбамазепин, леветирацетам, вальпроаты, нитразепам, ламотриджин и др.). Поскольку эпилепсия у детей, сопровождающая аномалии развития головного мозга, обычно резистентна к противосудорожной монотерапии, назначают комбинацию из 2 препаратов (например, леветирацетам с ламотриджином). При гидроцефалии осуществляют дегидратационную терапию, по показаниям прибегают к шунтирующим операциям. С целью улучшения метаболизма нормально функционирующих мозговых тканей, в какой-то степени компенсирующих имеющийся врожденный дефект, возможно проведение курсового нейрометаболического лечения с назначением глицина, витаминов гр. В и пр. Ноотропные препараты используются в лечении только при отсутствии эписиндрома.
При умеренных и относительно легких церебральных аномалиях рекомендована нейропсихологическая коррекция, занятия ребенка с психологом, комплексное психологическое сопровождение ребенка, детская арт-терапия, обучение детей старшего возраста в специализированных школах. Указанные методики помогают привить навыки самообслуживания, уменьшить степень выраженности олигофрении и по возможности социально адаптировать детей с церебральными пороками.
Прогноз и профилактика
Прогноз во многом определяется тяжестью церебральной аномалии. Неблагоприятным симптомом выступает ранее начало эпилепсии и ее резистентность к осуществляемой терапии. Осложняет прогноз наличие сочетанной врожденной соматической патологии. Эффективной мерой профилактики служит исключение эмбриотоксических и тератогенных влияний на женщину в период беременности. При планировании беременности будущим родителям следует избавиться от вредных привычек, пройти генетическое консультирование, обследование на наличие хронических инфекций.
Агенезия мозолистого тела
Агенезия мозолистого тела — это врожденное отсутствие мозолистого тела либо его части. Аномалия обусловлена генетическими нарушениями, сосудистыми мальформациями, тератогенными факторами. Основные признаки заболевания: двигательные расстройства, задержка психоречевого развития, судорожные приступы. При негрубом (частичном) варианте патологии возможно малосимптомное течение. Для диагностики состояния назначается церебральные КТ или МРТ, нейросонография у новорожденных, генетические исследования. Лечение симптоматическое: медикаментозная коррекция осложнений, реабилитационные программы.
Агенезия мозолистого тела (АМТ) — один из наиболее частых пороков нервной системы. Распространенность болезни в популяции составляет от 0,05% до 7% среди новорожденных, причем в группе детей с замедленным становлением психики агенезия встречается у 2,3%. Калифорнийская программа по изучению врожденных пороков предоставляет другие данные по частоте агенезии — 1,4 на 10000 живых новорожденных. Впервые состояние было описано в 1812 году в ходе аутопсии, проведенной немецким анатомом И. Рэйлем, и названо «природной моделью рассеченного мозга».
Точные этиологические факторы заболевания не установлены. В современной неврологии преобладает мультифакториальная теория, согласно которой для формирования врожденного порока ЦНС требуется комбинация неблагоприятных экзогенных и эндогенных причин. Ученые выделяют несколько наиболее вероятных предпосылок развития агенезии:
- Генетические аномалии. Повреждения мозолистого тела отмечаются при различных наследственных синдромах: Миллер-Дикера, Рубинштейна-Тауби, Доннаи-Кугана. Состояние входит в состав не менее 7 аутосомно-доминантных, 23 аутосомно-рецессивных, 12 Х-сцепленных врожденных заболеваний.
- Сосудистые нарушения. Причиной недоразвития мозолистого тела могут выступать артериовенозные мальформации или аневризмы, которые характеризуются отсутствием нормальной капиллярной сети. При этом возникает феномен обкрадывания, клетки МТ не получают должного количества кислорода, питательных веществ.
- Токсические влияния. Болезнь связана с действием тератогенных химических факторов: лекарственных препаратов, солей тяжелых металлов, пестицидов и бытовой химии. Негативное влияние на формирование ЦНС плода оказывает вдыхание табачного дыма (активное или пассивное курение) или прием беременной алкоголя во время гестации.
- Внутриутробные инфекции. Аномалии формирования неврологических структур, в том числе агенезия мозолистого тела, встречаются при проникновении возбудителей в организм плода на 2-3 месяце беременности. Нейротропные свойства демонстрируют герпетические инфекции, токсоплазмоз, цитомегаловирус.
Основным фактором риска выступает недоношенность. У новорожденных, родившихся до 27-недельного срока гестации МТ истончено в задних отделах, между 28 и 30 неделями — только в области валика. У рожденных после 30 недели в неонатальном периоде изменения не обнаруживаются, хотя при нейропсихологическом исследовании у школьников зачастую выявляется дефицит межполушарной передачи познавательной информации.
Агенезия возникает при нарушении дифференциации нервной трубки в период со 2 до 5 месяца внутриутробного развития. При полном отсутствии МТ третий мозговой желудочек остается открытым, не формируются столбы свода мозга, отсутствуют прозрачные перегородки. В 60% случаев при АМТ передней комиссуры нет вообще. В 10% она увеличена и берет на себя часть функций мозолистого тела у новорожденных, а также на следующих этапах постнатального периода.
Характерным анатомическим изменением является колпоцефалия, при которой расширены задние отделы боковых церебральных желудочков. Состояние не относится к истинной гидроцефалии новорожденных, а обусловлено уменьшением кортикальных ассоциативных путей. Еще один типичный признак порока — пучки Пробста, представляющие собой неправильно ориентированные аксоны, расположенные параллельно межполушарной щели.
Классификация
В практической неврологии состояние подразделяют на тотальное, когда орган полностью отсутствует, и частичное (парциальное), при котором визуализационные методы не обнаруживают отдельные участки МТ. Это имеет решающее значение для тяжести клинической картины, возможных осложнений. В соответствии с патогенетическими особенностями формирования врожденных пороков, выделяют следующие 3 формы болезни:
- Агенезия. Закладка эмбрионального зачатка МТ отсутствует полностью.
- Аплазия. Эмбриональный зачаток мозолистого тела есть, но не развивается.
- Гипоплазия. МТ недостаточно развито из-за нарушений на одном из этапов эмбриогенеза: размеры и масса органа уменьшены, его функциональная активность снижена.
Симптомы
Клиническая картина агенезии мозолистого тела широко варьирует от практически бессимптомных форм (при гипоплазии) до критических нервно-психических расстройств при его грубом недоразвитии, сопровождающемся другими врожденными пороками ЦНС. У новорожденных признаки патологии могут вовсе отсутствовать и проявляться по мере взросления младенца задержкой психомоторного развития.
Двигательные нарушения определяются у 35-40% пациентов. Они проявляются мышечной гипотонией или дистонией, гипер- или гипорефлексией, нарушением глотательного и сосательного рефлексов. Дети позже начинают держать голову, испытывают затруднения при обучении сидению, ползанию, ходьбе. Могут отмечаться координационные нарушения, неуклюжая походка. Из пароксизмальных расстройств у новорожденных и детей первого года жизни преобладают судороги.
Мозолистое тело поддерживает связь между церебральными зонами, формирует межполушарную организацию высших психических процессов. При его агенезии либо гипоплазии у детей выявляются когнитивные расстройства. У новорожденных пациентов и в раннем детстве наблюдается задержка речи, снижение динамического компонента игровой деятельности. В дошкольном и школьном возрасте возникают проблемы с концентрацией внимания, расстройства памяти, при тотальной АМТ снижен коэффициент интеллекта.
Осложнения
Около 65% случаев заболевания сопровождаются сопутствующими врожденными патологиями, среди которых преобладают мальформации кортикального развития (22,8%), межполушарные кисты (14,3%), голопрозэнцефалия (14,3%). К более редким сопутствующим аномалиям относят кисты и гипоплазию мозжечка, синдром Арнольда-Киари. До 20% новорожденных, кроме структур ЦНС, имеют пороки нескольких внутренних органов.
У 75% больных с тотальным поражением наблюдается симптоматическая эпилепсия височно-лобной локализации, в 66% случаев выражены когнитивные нарушения. У 16% пациентов формируются расстройства аутистического спектра. Изредка встречаются патологии органа зрения в виде хориоретинальных лакунарных очагов, сочетанной аномалии зрительных нервов.
В качестве первичного метода обследования в пренатальном периоде проводится акушерское УЗИ. У новорожденных для скрининговой диагностики используется нейросонография, однако этот метод не всегда показывает хорошую информативность, особенно при парциальной агенезии. Для верификации диагноза назначаются следующие методы исследования:
- КТ головного мозга. При компьютерной томографии определяются широко расставленные передние рога, высокое стояние третьего желудочка, параллельный ход медиальных стенок боковых желудочков. КТ производится в рамках постнатальной диагностики.
- МРТ головного мозга. Для максимально точной визуализации степени агенезии или гипоплазии мозолистого тела новорожденным выполняется магнитно-резонансная томография в трех плоскостях. По показаниям МРТ может рекомендоваться беременным женщинам для исключения несовместимых с жизнью сочетанных пороков ЦНС.
- Нейропсихологическое обследование. Для изучения когнитивных функций у детей применяется шкала интеллекта Векслера (WISC-Revised), адаптированное чтение и правописание (Schonnel Graded Reading and Spelling Tests), оценка вербальной беглости, тест контролируемых устных ассоциаций (Controlled Oral Word Association Test).
- Генетический анализ. Для подтверждения или исключения наследственных заболеваний, сопровождающихся агенезией мозолистого тела, показаны кариотипирование, секвенирование генома, проводимое как новорожденным, так и детям другого возраста. Исследования также проводят в антенатальном периоде для принятия решения о сохранении или прерывании беременности.
Лечение агенезии мозолистого тела
Специфическая терапия отсутствует. Медикаментозное лечение назначается неонатологом или педиатром индивидуально с учетом ведущих патологических синдромов: у новорожденных, детей раннего возраста используются антиконвульсанты, нейрометаболические препараты, дегидратационная терапия. Основу медицинской помощи составляет комплексная реабилитация, которая включает следующие составляющие:
- Нейрологопедические программы. Занятия с детским логопедом проводятся для становления речевой функции, ликвидации проявлений дизартрии, улучшения артикуляции.
- Дефектологические программы. Помощь коррекционных педагогов требуется детям с интеллектуальными нарушениями, которые не могут проходить обучение в обычных классах.
- Нейроакустические программы. Формирование и гармонизация высших психических функций производятся с помощью звуковой терапии, музыкотерапии.
Прогноз определяется видом врожденной аномалии мозолистого тела, наличием сопутствующих пороков развития ЦНС. Благоприятный исход наблюдается при частичной гипоплазии МТ, а в случае комбинированных церебральных пороков у новорожденных могут быть жизнеугрожающие осложнения. Профилактические меры включают медико-генетическое консультирование, исключение тератогенных влияний в гестационном периоде.
1. Эпилептические проявления когнитивные и аутистические расстройства у пациентов с агенезией мозолистого тела: результаты нейропсихологического тестирования/ О.А. Милованова, О.А. Комиссарова, Т.Ю. Тараканова, С.В. Бугрий// Эпилепсия и пароксизмальные состояния. — 2018. — №4.
2. Влияние особенностей строения мозолистого тела и доминирующего полушария на протекание психических процессов в юношеском возрасте/ У.С. Чернышова, Т.Ю. Хабарова, Д.А. Соколов// Центральный научный вестник. — 2016.
4. Молекулярная эмбриология: на пути каталогизации генов врожденных пороков развития головного мозга/ В.П. Пишак, М.А. Ризничук// Международный журнал педиатрии, акушерства и гинекологии. — 2014. — №5.
Дефект кожи головы - методы диагностики, лечения по Европейским рекомендациям
Синдром Адамса-Оливера включает врожденную аплазию кожи (ВАК) черепа с терминальным поперечным поражением конечностей с дефектом конечностей. Один из четырех случаев трисомии 13-15 проявляется врожденной аплазией кожи (ВАК).
Распространенность врожденной аплазии кожи (ВАК) в настоящее время неизвестна, хотя она была оценена в 3 случая на 10000 рождений. В 60% случаев, дефект ограничен волосистой частью головы, в то время как оставшиеся 40% могут быть рассеяны по телу или конечностям. Комбинированные поражения волосистой части головы и остальных частей тела обнаружены у 25% пациентов. Около 80% кожи головы занимают дефекты срединной линии, в основном на вершине черепа, хотя они могут занимать и боковое положение. Приблизительно 20% случаев ВАК головы связаны с подлежащим дефектом черепа.
Происхождение врожденной аплазии кожи (ВАК) головы остается неизвестным:
1. Некоторые авторы рассматривают это состояние как часть ДНТ и предполагают, что оно представляет форму дефекта закрытия нервной трубки, похожей на грыжу и менингоцеле.
2. Другие приписывают врожденную аплазию кожи (ВАК) головы нарушению слияния мезодермы, которое необходимо для нормального развития эктодермы.
3. Врожденная аплазия кожи (ВАК) также были отнесены к дефекту кровотока на вершине черепа (критическая зона для васкуляризации кожи головы) из-за скудного развития сосудов или к нарушению кровотока при перерастяжении кожи головы плода.
4. Врожденная аплазия кожи (ВАК) связывают и с ишемическими или тромботическими эпизодами в плаценте.
5. Другие относят эти дефекты к очаговым некрозам от давления как это происходит при амниотическом синдроме при клинически узком тазе.
6. Врожденная аплазия кожи (ВАК) и дефекты черепа также упоминаются в ассоциации с тератогенами (мизопростол, метимазол, аминоптерин, метотрексат и бензодиазепины), внутриутробными инфекциями (ветряная оспа или вирус простого герпеса) и злоупотреблением кокаином.
Диагностика врожденной аплазии кожи (ВАК) кожи головы выполняется при осмотре, мы рекомендуем использовать хорошее освещение и увеличительные лупы. Макроскопически поражения хорошо ограничены, имеют овальную или неправильную форму с размером 0,5-10 см по типу язвы неравной глубины. Когда повреждения заживают до рождения, они выглядят как врожденные шрамы. Микроскопически поражения состоят из атрофических кожных элементов без кожных придатков. Тщательное обследование новорожденных обязательно для исключения других кожных или системных аномалий.
Случаи с несколькими пороками развития предоставляются для соответствующих генетических исследований, такие состояния при нейрохирургической консультации, обычно требуют нейровизуализации. МРТ позволяет оценить состояние головного мозга. МР-ангиография и флебография используются для описания состояния магистральных сосудов и сагиттального синуса. Для оценки дефектов черепа используется КТ с трехмерной реконструкцией.
Дифференциальный диагноз устанавливается между атретической цефалоцеле, sinus pericranii и гетеротопической тканью. Некоторые поражениях кожи головы могут быть ошибочно отнесены к травматическим после вакуум-экстракции, применения щипцов или мониторинга электродами кожи головы плода.
Два основных варианта лечения врожденной аплазии кожи (ВАК) кожи головы:
1. Консервативное лечение. Маленький боковой или поверхностный дефект кожи (не связанный с черепом или твердой мозговой оболочкой) ведется консервативно в течение нескольких недель. Антибиотики используются только при наличии кожной инфекции.
2. Хирургическое лечение. Начало лечения зависит от следующих факторов:
а) локализация: дефекты срединной линии более склонны к развитию кровоизлияния или тромбоза сагиттального синуса.
б) размер поражения: мелкие дефекты кожи проще лечатся прямым закрытием или перемещением кожных лоскутов. Этот подход является предпочтительным, обеспечивая нормальный вид волосяного покрова.
в) глубина поражения: ВАК может поражать надкостницу, череп и твердую мозговую оболочку. Открытый мозг более подвержен менингиту, энцефалиту и кровотечению из сагиттального синуса. Большие дефекты требуют более сложных кожных лоскутов и даже пересадки кожи.
г) общее состояние и продолжительность жизни детей также должны быть приняты во внимание.
Время проведения хирургической коррекции определяется с учетом всех факторов. К участию в операции необходимо привлечь пластического хирурга. Прогноз при ВАК головы, как правило, хороший у большинства пациентов, и зависит от размеров поражения и сопутствующих аномалий, однако при больших и сложных поражениях смертность может превышать 50%.
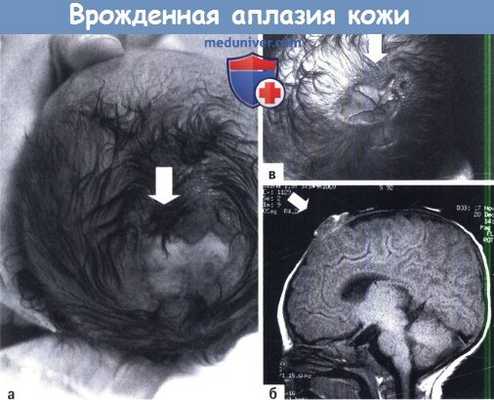
А, Б. Два случая врожденной аплазии кожи черепа (белая стрелка).
В. МРТ незаращенного повреждения врожденной аплазии, зарождение грыжи мозга (перепечатано с разрешения из Child’s Nervous System, Springer-Verlag).
Читайте также:
