У вич паразитарная основа
Понятие оппортунистических инфекций было введено в медицинскую литературу более двух веков назад вначале на примере условнопатогенных грибковых, а позже бактериальных инфекций. B настоящее время перечень оппортунистических инфекций включает более 100 нозоединиц, в том числе с недавнего времени (с начала трансплантации органов и тканей) также протозойную инфекцию - токсоплазмоз.
Постепенно было установлено, что непременным условием, способствующим условно-патогенным микроорганизмам проявлять свой патогенный потенциал при проникновении в организм человека, является наличие иммунодефицитного состояния. B зависимости от этиологии и патогенеза иммунодефицита манифестируют различные инфекции. При дефиците гуморального иммунитета преобладают бактериальные инфекции, при дефиците клеточного - вирусные, протозойные и грибковые.
Этиология иммунодефицитных состояний у человека разнообразна, она включает врожденные иммунодефициты, прием цитотоксических препаратов при лечении злокачественных новообразований, цитотоксическое воздействие радиации, длительную терапию кортикостероидами, а также препараты, используемые для предотвращения отторжения трансплантатов. Заметим, иммуносупрессивным воздействием обладают некоторые возбудители инфекций и инвазий (ЦМВ, ВЛ, многие гельминтозы).
Однако единственной инфекцией, которая разрушает клеточный иммунитет человека прогрессивно, вплоть до его полной анергии, является ВИЧ-инфекция. ВИЧ атакует клетки, несущие CD4 антиген, который выполняет функцию рецептора. Этот рецептор имеется на всех T4 лим- фоцитах-хелперах (помощниках), на 20% макрофагов, 10% моноцитов и примерно 5% В-лимфоцитов. B результате возникают благоприятные условия для развития инфекций, в защите от которых основную роль играет клеточный иммунитет. Возбудители-оппортунисты, которые лишены способности инфицировать индивидов с сохранной иммунной системой или вызывать у них лишь бессимптомный или самоог- раниченный инфекционный процесс, превращаются в патогенов, вызывающих тяжелые, потенциально смертельные заболевания.
Возбудители-оппортунисты, чей патогенный потенциал проявляется в основном на фоне дефицита клеточного иммунитета, инициированного ВИЧ, вызывают особую группу инфекций, получившую название СПИД-индикаторные, или СПИД-ассоциируемые. B эту группу давно входят протозойные инфекции: токсоплазмоз, криптоспоридиоз, пнев- моцистоз и изоспороз.
Имеется точка зрения, что хронически текущие паразитарные болезни (трипаносомозы, шистосомозы, филяриидозы) отличаются глубоким воздействием на иммунную систему больного и существенно изменяют ее ответ на не относящиеся к паразитам антигены, таким образом, что пациент становится более восприимчивым к инфекциям типа ВИЧ-инфекции. Следуя этому предположению, можно ожидать большей частоты ВИЧ-инфекции у больных с перечисленными и другими хроническими паразитарными болезнями, особенно в тропиках, где и паразитарные болезни, и ВИЧ/СПИД широко распространены. Некоторые наблюдения и обследования в какой-то степени подтверждают эту гипотезу.
Так, вагинальный трихомоноз у 1200 проституток в Абиджане обнаруживался в 27% у инфицированных ВИЧ против 17% у неинфициро- ванных. K сожалению, обследованные группы были неравноценны по риску заражения Trichomonas vaginalis. Кроме того, изучение реакции мононуклеаров на митогены у женщин в Xapape (Зимбабве) выявило сниженную реактивность на обычные митогены у женщин с трихомонозом. Таким образом, нет данных о наличии патогенетической связи между трихомонозом и СПИДом.
Амебиаз широко распространен среди мужчин-гомосексуалистов, очень немногие из них, даже инфицированные ВИЧ, имели явные симптомы амебиаза как болезни. B сельских районах Танзании поражен- ность Entamoeba histolytica ВИЧ-инфицированных жителей оказалась вдвое ниже, чем ВИЧ-негативных (12,5% против 25,1%), при том, что Cryptosporidium и Isospora обнаруживались существенно чаще как раз у ВИЧ/СПИД пациентов. Очевидно, что между амебиазом и СПИДом патогенетическая связь также отсутствует.
Малярия в аспекте ее ассоциируемости с ВИЧ/СПИД изучалась интенсивнее других протозойных инфекций. Установлено, что инфекция Plasmodium falciparum не была более распространенной и не протекала более тяжело у ВИЧ-инфицированных. Ни у взрослых, ни у детей не было обнаружено связи между ВИЧ/СПИД и пораженностью, интенсивностью паразитемии или податливостью лечению малярии. Наблюдения в Киншасе (Заир) за 1000 детьми с малярией и ВИЧ-ин- фекцией, получившими экстренные гемотрансфузии, показали отсутствие влияния прогрессирующей ВИЧ-инфекции на частоту тяжелого течения малярии, и наоборот, признаков влияния малярии на течение ВИЧ-инфекции.
Сонная болезнь, распространенная в очагах ВИЧ-инфекции в Африке, не претерпела в своем течении признаков взаимовоздействия Trypanosoma gambiense/rhodesiense на ВИЧ и обратно. Единственное, что было установлено - это меньшая податливость сонной болезни (равно как и висцерального лейшманиоза) этиологической химиотерапии у ВИЧ-инфицированных, т.е. на фоне иммунодефицита, инициированного ВИЧ.
Висцеральный лейшманиоз, протекающий хронически и сопровождаемый прогрессивным нарастанием клеточного иммунодефицита, стал часто сочетаться с ВИЧ-инфекцией даже в районах его ограниченного распространения. B средиземноморском регионе он вполне определенно проявляет себя как СПИД-ассоциируемая инфекция (см. главу 28). B районах совместного распространения кожных и висцерального лейшманиозов, только последний протекает у ВИЧ-инфицированных настолько своеобразно, что рассматривается как диагностический критерий наступления фазы СПИДа. Что касается кожных форм лейшманиозов, то никаких данных о наличии у них патогенетических связей со СПИДом до настоящего времени не обнаружено.
Акантамебиаз протекает либо как гранулематозный амебный энцефалит (ГАЭ), либо как диссеминированный пустулезный, узелковый, язвенный кожный синдром, не вовлекающий ЦНС и обнаруживающийся обычно у лиц с иммуносупрессией различной этиологии. Эти медленно развивающиеся формы поражения развиваются после относительно длинного инкубационного периода (>10 дней) - в резком отличии от первичного амебного менингоэнцефалита (ПАМ), вызываемого Naegleria fowleri и приводящего к смертельному поражению ЦНС в первые часы-сутки после заражения. У пациентов с иммунодефицитом, вызванным ВИЧ-инфекцией или применением препаратов иммуносупрессивного действия, диссеминированные формы акантамебиаза могут протекать остро. Другими словами, акантамебиаз проявляет себя как СПИД-ассоциируемая инфекция, по крайней мере в США, где регистрируется более половины всех известных случаев этой инфекции в мире.
Что касается микроспоридозов, то частота их обнаружения резко возросла параллельно росту ВИЧ-инфицированных, и они вполне обоснованно становятся кандидатами в перечень СПИД-ассоциируемых про- тозойных инфекций (см. ниже). Таким образом, достоверно диагностированные протозойные инфекции (группа из 6 нозоформ) остаются наглядным показателем перехода ВИЧ-инфекции в ее терминальную стадию, СПИД.
Чем эти 6 нозоформ отличаются от других протозойных инфекций, не являющихся критерием перехода ВИЧ-инфекции в терминальную стадию, СПИД? Часть этих отличий суммирована в таблице 25-1.
Сравнительные особенности возбудителей протозойных инфекций, отличающихся по их способности ассоциироваться со СПИДом

Как видно из таблицы 25-1, две особенности СПИД-ассоциируемых и не ассоциируемых со СПИДом протозойных инфекций достаточно четкие: первые всегда локализуются внутриклеточно, в том числе в им- мунокомпетентных клетках (токсоплазма и лейшмания - в макрофагах), и часто первично проявляют себя как эндогенные персистирующие инфекции, вторые локализуются внеклеточно (исключение - малярия, но ее возбудители локализуются в неиммунокомпетентных эритроцитах и являются исключительно экзогенньши).
Некоторые авторы заключают, что простейшим, проявляющим свой патогенный потенциал у больных СПИДом, присущи три свойства:
1. Персистировать в организме человека с рождения или с раннего детства, вызывая латентно протекающие эндогенные инфекции, которые реактивируются и генерализуются на фоне иммунодефицита;
2. Паразитировать внутриклеточно, особенно в иммунных клетках (макрофагах и др.);
3. Элиминироваться в норме Т-клетками или макрофагами во взаимодействии с Т-клетками.
Благодаря этим особенностям, СПИД-ассоциируемые протозойные инфекции протекают клинически неодинаково, в зависимости от иммунокомпетентности инфицированного индивида (табл. 25-2).
K другим особенностям протозойных инфекций у больных СПИДом следует отнести:
а) тенденцию к диссеминации возбудителей (к эктопической локали
б) трудности паразитологической и иммунологической диагностики;
в) слабую податливость антипротозойным препаратам и необходимость длительной поддерживающей (противорецидивной) терапии.
Более детально клинические и диагностические особенности этой группы инфекций рассматриваются в главах 26-30.
Другие инфекционные и паразитарные болезни при ВИЧ
Другие инфекционные и паразитарные болезни при ВИЧ
1. Криптоспоридиоз — кишечная протозойная инфекция, вызываемая внутриклеточным паразитом Cryptosporidium. Установлено, что сывороточные антитела существенной роли в процессе очищения при этой инфекции не играют, тогда как при поражении Т-клеток формируется затяжное течение. Вероятно, именно этот фактор имеет значение в развитии упорной диареи у ВИЧ-инфицированных, а сочетание развивающегося синдрома малабсорбции с повышенной секрецией жидкости и электролитов в просвет кишечника сопровождается значительной потерей массы тела больным.
2. Изоспороз — протозойное заболевание, вызываемое простейшими Isospora belli и Isospora natalensis.
3. Токсоплазмоз — протозойное зоонозное заболевание, вызываемое паразитом Toxoplasma gondii. При СПИДе на фоне выраженного иммунодефицита наступает активация токсоплазм, находящихся в клетках мозга. Кроме того, токсоплазмы получают возможность более активно распространяться по организму, в том числе и проникать в ЦНС.
Клиническая картина
1. Криптоспоридиоз.
О СПИДе можно говорить лишь при криптоспоридиозной диарее, продолжающейся 1 месяц и более, так как такой процесс уже не способен к самолимитированию. Диарея (постоянная или перемежающаяся) у больных СПИДом может продолжаться месяцы и даже годы, она сопровождается лихорадкой, болью в животе (иногда резкой), на этом фоне истощение может достигать критических степеней. У больных СПИДом диарея может сочетаться с катаральным синдромом, обусловленным размножением криптоспоридий в эпителии дыхательных путей. При аускультации легких в этих случаях выслушиваются рассеянные сухие и влажные хрипы, а рентгенография позволяет выявить данные, характерные для бронхита или пневмонии.
2. Изоспороз.
Размножение изоспор в эпителиальных клетках кишечника приводит к его повреждению, нарушению процессов всасывания жидкости и питательных веществ из просвета кишечника — развивается диарейный синдром, сопровождающийся схваткообразной болью в животе. Стул частый, водянистый, температура чаще субфебрильная. Процесс в иммунокомпетентном организме обычно протекает благоприятно, все явления стихают не позднее чем через 7 — 10 дней даже без лечения. У многих инфицированных диарейный синдром не развивается вообще, хотя изоспоры обнаруживаются в фекалиях. Однако у лиц с иммунодефицитом, в том числе и больных СПИДом, изоспороз приобретает затяжное течение — диарея может длиться месяцы, сопровождаясь малабсорбцией, приводя к истощению больного. Изоспороз с диареей более 1 месяца — индикатор СПИДа. Более того, при тяжелом длительном течении изоспороза возможна диссеминация изоспор.
3. Токсоплазмоз.
Размножение токсоплазм в ЦНС сопровождается развитием очаговых или диффузных поражений. Токсоплазмоз головного мозга у больных старше 1 месяца — маркер СПИДа. Возрастные ограничения (1 месяц) введены потому, что тяжелые поражения ЦНС с развитием гидроцефалии, микроцефалии и другой патологии могут быть следствием внутриутробного инфицирования токсоплазмами плода без признаков иммунодефицита; такой врожденный токсоплазмоз отчетливо проявится в течение 1-го месяца жизни ребенка. Симптоматика при поражении токсоплазмами головного мозга бывает очень пестрой. При диффузном поражении больных беспокоят головная боль, слабость, прогрессирующее снижение работоспособности. Эти явления быстро нарастают, и уже через несколько недель, а иногда и раньше у больных возникают спутанность сознания, дезориентация в окружающем, сонливость или возбуждение, а в дальнейшем наступают потеря сознания, судороги, кома. При очаговых поражениях клинические проявления определяются локализацией процесса. Часто возникает гемипарез, он может быть нерезко выражен и не всегда привлекает внимание из-за наличия других, более ярких симптомов. У больных могут выявляться поражение черепных нервов, афазия, атаксия, тремор и т. д. При поражении токсоплазмами спинного мозга развивается поперечный миелит. Токсоплазмы могут приводить к образованию внутримозговых абсцессов. У некоторых больных выявляют обширные зоны деструкции ткани мозга. Изменения, возникающие в ткани мозга, необратимы. Поражение ЦНС токсоплазмами у больных СПИДом сопровождается лихорадкой, упорной головной болью. Заболевание при отсутствии лечения быстро прогрессирует и может быть непосредственной причиной смерти. На фоне диссеминации токсоплазм при СПИДе возможны токсоплазмозные поражения различных органов: сердца, легких, мужских и женских половых органов (яички, придатки).
Диагностика
1. Криптоспоридиоз.
Диагноз подтверждают обнаружением криптоспоридий в исследуемом материале (обычно исследуют фекалии, при наличии соответствующей клиники — мокроту и дуоденальное содержимое). Существуют специальные методы обработки, хранения и окраски исследуемого материала. Методами РИФ, РЛА можно выявлять антигены криптоспоридий. Имеются серологические методы, позволяющие определять специфические антитела; хотя в борьбе с инфекцией они существенной роли не играют, но могут служить маркером инфекции.
2. Изоспороз.
Диагноз подтверждается обнаружением паразитов в фекалиях; применение метода обогащения повышает вероятность паразитологических находок.
3. Токсоплазмоз.
Токсоплазмозный генез энцефалита подтверждает обнаружение токсоплазм в биоптатах мозга и/или в спинномозговой жидкости. Серологические методы менее надежны, учитывая высокую степень инфицированности населения.
Паразитарные инфекции представляют собой разнообразный спектр симптомов и заболеваний, которые вызваны попаданием яиц или взрослой особи паразита в организм человека. Зачастую первые признаки заболевания невозможно обнаружить на протяжении нескольких дней, а в некоторых случаях нескольких месяцев и даже лет. Это связано с жизненным циклом паразитов и их основными функциями: хорошая маскировка и поддержание собственной жизни за счет получения питательных веществ от организма носителя.
Виды паразитов и их характеристика
Паразитарные инфекции в зависимости от определенных свойств их проявления делятся на три группы:
Основной локализацией служит поверхность тела человека. К ним относятся вши, блохи, клещи и клопы. Питаются преимущественно кровью человека, хотя в отдельных случаях, как, например, с клещами, которые вызывают демодекоз, основное питание – секрет сальных желез или отмершие клетки эпителия (кожи).
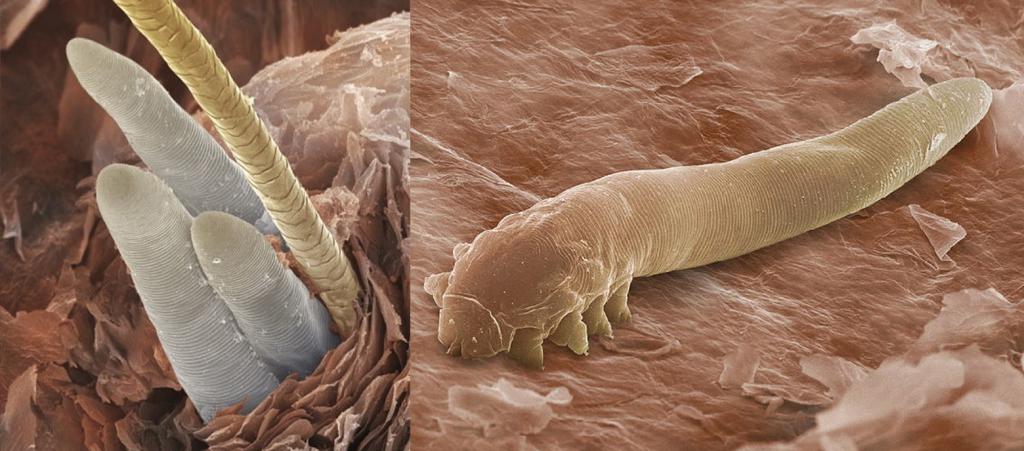
Первые признаки паразитарной инфекции достаточно легко распознать, так как они вызывают зуд и жжение в местах своего обитания. Некоторые эктопаразиты являются переносчиками серьезных заболеваний: тиф, сибирская язва, энцефалит и трипаносомоз. Они наносят огромный ущерб человеческому здоровью, вплоть до летального исхода.
2. Эндопаразиты (простейшие).
В основном поражают внутренние органы. По своей структуре являются одноклеточными, отсюда и название – простейшие. Несмотря на это, они способны привести к тяжелым формам болезней. Основными заболеваниями данной группы являются паразитарная инфекция крови, вызванная токсоплазмой, и кишечные инфекции, спровоцированные амебой или лямблиями.
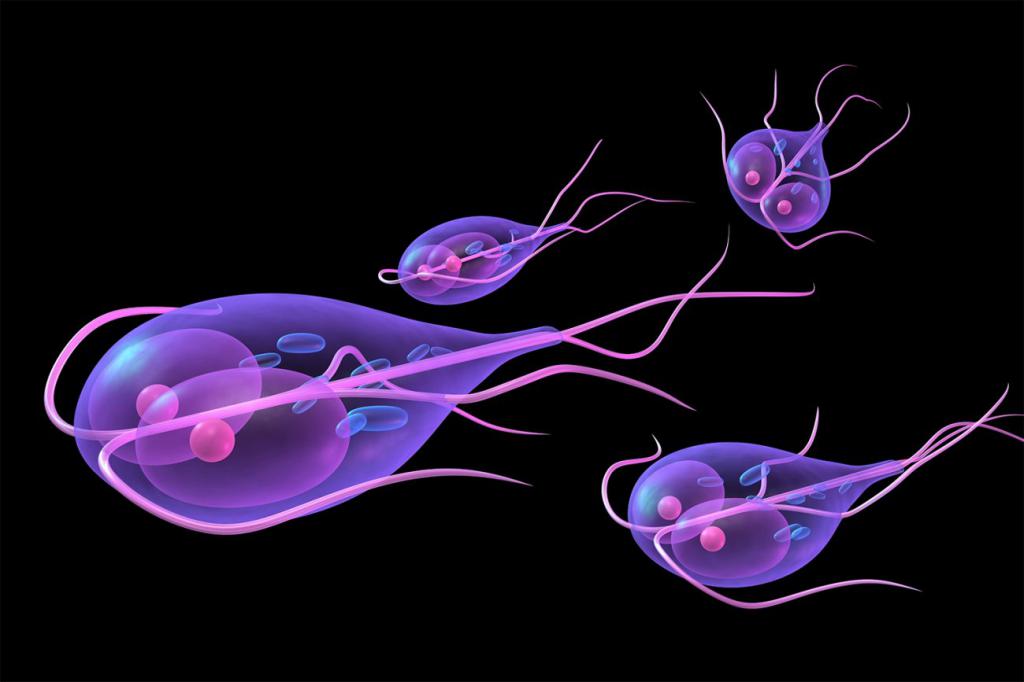
Являются возбудителями наиболее распространенных форм паразитарных инфекций. В организме человека их циклы развития в основном проходят в кишечнике и тканях, где и начинается проявление симптомов заболеваний.
Круглые черви (нематоды)
Это паразиты, тело которых в поперечном разрезе круглой формы. Легко различимы половые признаки. Самки, как правило, крупнее самцов. Но также у представителей данного класса встречаются гермафродиты. Все нематоды проходят стадии развития: яйцо, личинка, взрослая особь. К этому классу относятся:
- Острица. Вызывает заболевание энтеробиоз. Преимущественно поражает детей дошкольного и младшего школьного возраста.
- Власоглав. Вызывает заболевание трихоцефалез. Имеет отличительную форму тела. 2/3 длины тела имеет тонкий диаметр, напоминающий человеческие волосы или нить. Другой конец тела более крупного диаметра, в нем располагается кишечник.
- Аскарида. Вызывает заболевание аскаридоз. Взрослые особи достигают размеров 25 см (самцы) и 40 см (самки). После попадания личинки в организм человека она проходит желудок, попадает в тонкий кишечник. Оттуда через поры с током крови попадает в печень, далее в сердце и затем в легкие, где развивается в течение 7-10 дней. Затем личинки начинают подниматься к гортани. Достигнув ротовой полости, они повторно заглатываются. После попадания в тонкий кишечник личинки уже не могут повторно проникнуть через поры в кровоток из-за своего большого размера. Там они растут до взрослых особей в течение 2-3 месяцев. После этого начинается размножение и цикл повторяется. Самка может откладывать более 200 тыс. яиц за сутки.

Ленточные черви (цестоды)
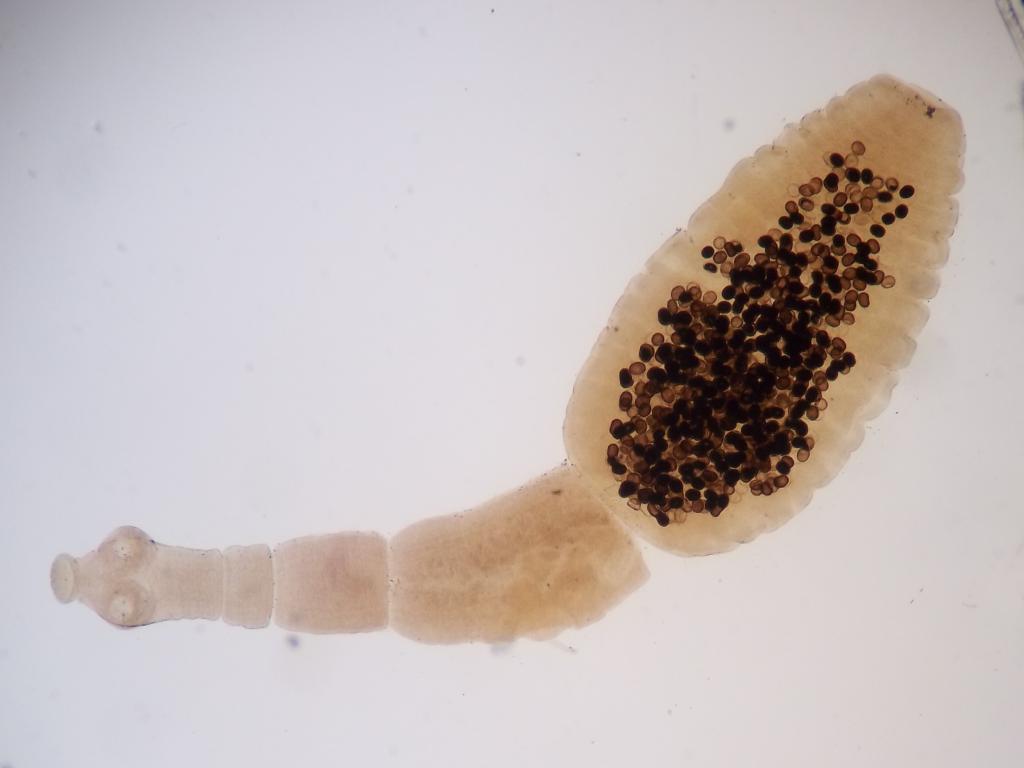
Это паразиты, тело которых напоминает форму ленты. Отличительной особенностью у данного класса является отсутствие пищеварительной системы. К ним относятся:
- Эхинококк. Вызывает заболевание эхинококкоз. Этот паразит имеет небольшой размер (2-9 мм) и состоит из нескольких члеников и присосок. В матке половозрелой особи содержится большое количество яиц, внутри которых находятся личинки. Основные места локализации эхинококка – печень и легкие. Там он вызывает хроническое заболевание, которое называется эхинококковой кистой.
- Бычий цепень. Вызывает заболевание тениаринхоз. На стадии личинки имеет промежуточного хозяина – крупнорогатый скот. Попадая в организм человека, развивается в тонком кишечнике до ленточной стадии. Тело взрослой особи паразита имеет до 1000 члеников, и в длину он может достигать 4-10 метров.
- Свиной цепень. Вызывает заболевание тениоз. Внешне очень похож на бычьего цепня. Также имеет промежуточных хозяев: свиньи, собаки, верблюды, зайцы и кролики. У человека паразитирует в кишечнике. Размеры взрослой особи в длину не превышают 4 метров.
- Лентец широкий. Вызывает заболевание дифиллоботриоз. Обитает в пресноводных водоемах. В качестве промежуточного хозяина использует рачков и рыб. В организме человека паразитирует в тонком кишечнике. В длину взрослая особь может достигать нескольких метров.
Плоские черви (трематоды)
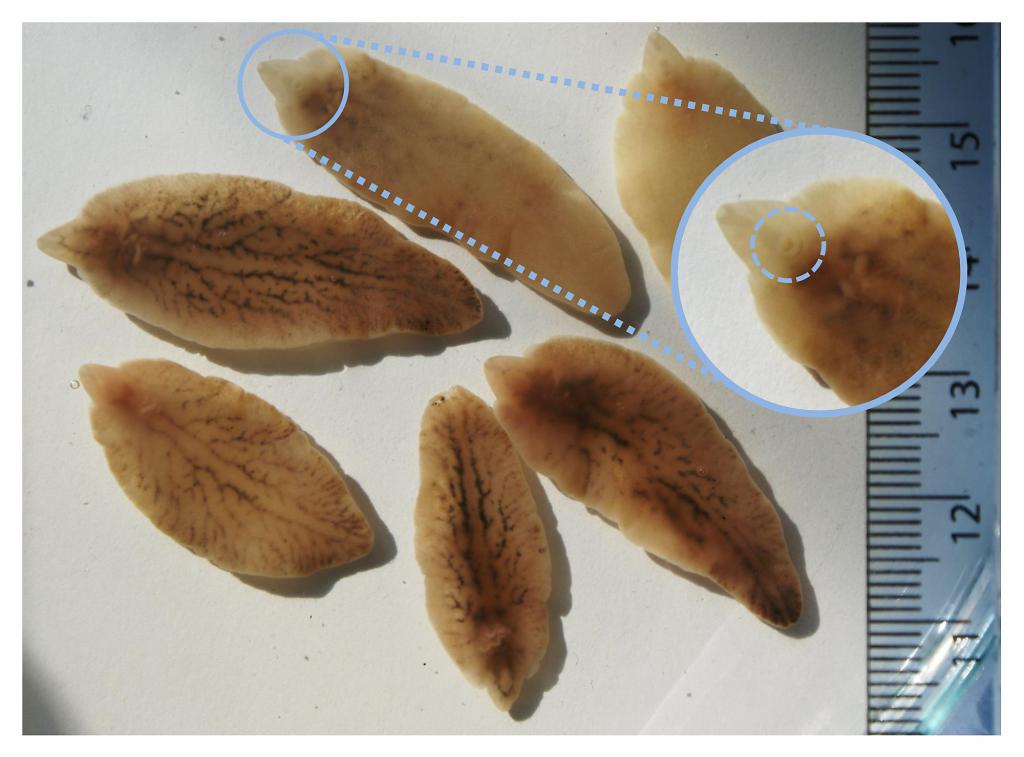
За свой жизненный цикл эти паразиты могут менять нескольких промежуточных хозяев. У человека могут паразитировать в любом органе. В данную группу входят:
- Шистосомы. Вызывают заболевание шистосомоз. В организм человека могут попасть при контакте с зараженным пресным водоемом. Паразит проникает через кожу и попадает в кровеносную систему, где начинает активно размножаться. В сутки самки могут производить от 300 до 3000 яиц. Далее, с током крови, яйца разносятся по всему организму и продолжают свое развитие в любом органе. Длина их тела не превышает 0,1-0,2 см.
- Печеночные сосальщики. Вызывают заболевание описторхоз. Длина взрослой особи колеблется от 3 до 5 см. При попадании в организм человека паразитирует в желчных протоках, желчном пузыре, печени и поджелудочной железе. Закрепляется в этих органах с помощью присосок, расположенных на теле.
Пути проникновения паразитов в организм человека
- Алиментарный путь заражения считается самым распространенным. Человек заражается паразитом при употреблении в пищу плохо промытых овощей и фруктов. Особенную опасность несет мясо, которое не прошло достаточную термическую обработку. Также заражение человека паразитарной инфекцией имеет место, если не соблюдать правила личной гигиены. Например, не помыть руки перед едой.
- Трансплацентарный путь. Паразитарная инфекция передается от беременной женщины через плаценту к ребенку. Например, это такие заболевания, как токсоплазмоз, малярия или анкилостомоз.
- Перкутанный путь. Паразит проникает в организм человека через кожу. В основном это шистосомы и анкилостомы.
- Контактный путь. Паразит передается через грязные руки, загрязненные личные принадлежности, белье. Так чаще всего передаются вши, чесоточный зудень, острицы.
- Трансмиссивный путь. Заражение происходит после укуса насекомых, которые являются носителями паразитов. Например, малярия.
Симптомы
Многие паразитарные заболевания на ранних стадиях не имеют симптоматики. Это связано со стадиями развития возбудителя. Каждый отдельный вид паразита по мере своего роста проявляет себя по-разному. К часто встречающимся общим симптомам паразитарной инфекции относятся:
- Зуд.
- Покраснение кожи по типу крапивницы.
- Диарея.
- Запор.
- Метеоризм.
- Тошнота, рвота.
- Спазмы и болезненные ощущения в желудочно-кишечном тракте.
- Снижение массы тела без применения диет и повышенных физических нагрузок
- Лихорадочное состояние.
- Высокая температура тела (38-40 ˚С) в течение продолжительного периода.
- Продолжительные приступы сухого кашля.
- Увеличение лимфатических узлов.
- Болезненные ощущения в мышцах.
- Нарушения психоэмоционального характера.
Диагностика

При подозрении на наличие паразитарных заболеваний необходимо сдать ряд анализов. Диагностика паразитарных инфекций позволяет определить наличие или отсутствие паразита, его вид и место локализации в организме. Полученные данные помогут врачу поставить правильный диагноз и назначить корректное лечение.
К методам диагностики относятся:
I. Исследование кала. Позволяет определить наличие большинства видов паразитов, которые обитают в кишечнике. С фекалиями выделяются их яйца, личинки и сегменты тела. Существует два вида анализа:
- Исследуется образец кала на яйца и личинки гельминтов. Анализ доставляется в лабораторию, где врач делает мазки и рассматривает их под микроскопом. Такой метод применяется часто, но он не является достаточно точным. Для того, чтобы поставить окончательный диагноз, пациенту необходимо сдавать этот анализ до трех раз с небольшими временными промежутками. Это связано с жизненным циклом паразитов и откладыванием яиц, которые обнаруживаются данным методом исследования.
- Соскоб (смыв) со складок анального прохода. Этот анализ применяют для обнаружения только одного вида гельминтов – остриц. У детей паразитарная инфекция встречается чаще, чем у взрослых. По этой причине такой анализ проводят преимущественно детям. Лаборант смачивает ватную или стеклянную глазную палочку в воде или глицерине и делает смыв с перианальных складок. Далее наносит полученный материал на предметное стекло и рассматривает под микроскопом. Также этот анализ делается другим методом: лаборант приклеивает кусочек липкой ленты к анальному проходу, прижимает и отклеивает. Затем липкая лента приклеивается к предметному стеклу и также рассматривается под микроскопом. Диагностируется паразит достаточно точно. Применяя эти методы, лаборанту удается рассмотреть не только яйца гельминтов, но иногда и взрослых особей.
II. Исследование спинномозговой жидкости, мокроты, дуоденального содержимого (желчи), мочи. Назначают по результатам опроса пациента с целью определения наличия паразита и определения его локализации. Анализ этих биологических жидкостей исследуют с применением микроскопии и макроскопии. Сначала полученный образец рассматривают на предмет наличия взрослых особей, а после проводят микроскопию для обнаружения яиц и личинок паразитов.
III. Исследование крови. Современные методы исследования крови на паразитарные инфекции позволяют определить наличие и вид возбудителя с высокой точностью. Применяются три вида такой диагностики:
- Серологические реакции. Позволяют определить наличие антител паразитов в сыворотке крови пациента. Этот метод считается высокоспецифичным, но уступает ПЦР-диагностике.
- ПЦР-диагностика. Данный метод основывается на выявлении ДНК паразитов в любой биологической жидкости, которую взяли для анализа.
- Генетическое исследование. Заключается в обнаружении генома паразита в образце крови пациента. Этот метод применяется гораздо реже всех остальных, но имеет высокую точность.
IV. Исследование биопсийного материала и лимфоузлов. Для этого анализа врач проводит иссечение небольшого участка органа, ткани или целый лимфатический узел и отправляет на гистологическое исследование. Таким образом диагностируется наличие или отсутствие паразитов.
Рекомендации по подготовке к сдаче анализов
Прежде чем сдавать анализы на паразитарные инфекции, необходимо правильно к ним подготовиться. При соблюдении рекомендаций повышается точность диагностики, так как в материале отсутствуют мешающие факторы, влияющие на эффективность методов исследования.
Подготовка к сдаче анализа кала:
- Следует прекратить прием антибиотиков, противовоспалительных средств и антацидов. Также недопустимо применение лекарственных и других препаратов, содержащих висмут и железо.
- Если проводилось рентгенологическое исследование с применением бария или колоноскопия, при которой проводилась очищающая кишечник клизма, то анализ кала можно будет сдавать только спустя 2-3 дня.
- Не рекомендуется сдавать кал в случае начала менструальных кровотечений или обострения геморроя.
Подготовка к сдаче анализа крови:
- Необходимо прекратить прием фармакологических препаратов, которые влияют на формулу крови.
- За три дня до сдачи анализа следует соблюдать легкую диету, не употреблять жирные продукты, отказаться от алкоголя.
- Анализ крови на паразитарные инфекции сдают натощак. Разрешается употребление небольшого количества чистой питьевой воды.
Для остальных анализов чаще всего не требуется особенная подготовка. Необходимо будет только соблюдать рекомендации врача.
Лечение
К сожалению, симптомы паразитарных инфекций не всегда можно обнаружить на начальных этапах заболевания. В таких случаях лечение начинается с опозданием. Важно понимать: чем дольше паразит находится в организме, тем сложнее будет от него избавиться.
Терапия инфекционных и паразитарных инфекций разделяется на два направления:
- Симптоматическое лечение. Направлено на устранение клинических проявлений заболевания. К ним относятся снижение температуры тела, избавление от покраснений и зуда, нормализация работы желудочно-кишечного тракта.
- Этиологическое лечение паразитарных инфекций направлено на избавление от возбудителя заболевания.
В некоторых случаях может возникнуть необходимость в хирургическом вмешательстве. Оно применимо при альвеококкозе, эхинококкозе и некоторых видах заражения трематодами.
Только врач может назначить лечение паразитарных инфекций, основываясь на данных лабораторных исследований и опроса пациента.
Профилактика
Очень важно соблюдать профилактику паразитарных инфекций. В большинстве случаев это поможет избежать попадания в организм болезнетворных возбудителей.

К профилактическим мерам относятся:
- Соблюдение правил личной гигиены: необходимо мыть руки перед употреблением пищи, после посещения туалетной комнаты, заходя домой с улицы.
- Следует хорошо промывать овощи и фрукты.
- Обязательно нужно проводить достаточную термическую обработку мяса, рыбы и морепродуктов.
- В качестве питьевой воды не стоит использовать воду из-под крана, так как она не всегда может быть очищена от паразитов. Не поможет в качестве дополнительной очистки применение домашних фильтров. Оптимальным вариантом будет употребление кипяченой или бутилированной воды.
- Если дома живут домашние животные, то им необходимо проводить дегельминтизацию один раз в полгода. Также следует ограничить контакт с питомцем при наличии у него признаков паразитарных заболеваний и обратиться в ветеринарную клинику.
- Следует гладить нижнее белье (особенно детское) после стирки.
- После посещения экзотических стран, при работе с землей, а также сотрудникам детских учреждений рекомендуется обследоваться раз в год на предмет наличия паразитарных инфекций и при необходимости проводить профилактику лекарственными средствами.

Лечение ВИЧ – это сложный процесс. Сложность, в основном, определяется малым сроком определения самой инфекции. ВИЧ впервые описали в 1981 году. Заболевание смертоносное. По этой причине силы на разработку методов лечения были брошены серьезные.
К 1986 году было представлено первое лекарственное средство, ныне имеющее название зидовудин. Это лекарство самостоятельно уже не применяется в силу привыкания. Однако оно применяется как часть метода ВААРТ, который впервые был обнародован в 1996 году.
Главная задача препаратов для лечения ВИЧ заключается в контроле воспроизводства (репликации) вируса иммунодефицита и замедления развития ВИЧ-ассоциированных заболеваний . Эти осложнения фактически являются причиной смертельного исхода.
При условии пожизненного применения препаратов ВААРТ заболевшему практически гарантируется естественный срок жизни. Более того, система лечения ВИЧ продолжает совершенствоваться. Возможно будет найдено решение по полному излечению.
Лечение ВИЧ инфекции – принципы
Основой лечения ВИЧ-инфекции являются схемы ВААРТ (высокоактивной антиретровирусной терапии). Лечение ВИЧ по схемам ВААРТ заключается в приеме комбинации из трех-четырех антиретровирусных средств.
Справочно. Лечение ВИЧ при помощи комбинированной терапии отличается высокой степенью эффективности и при своевременном назначении позволяет пациентам вести полноценный образ жизни.
Эффективность терапии зависит от стадии ВИЧ, на которой была начата терапия и количества CD4 клеток перед началом лечения. Согласно последним исследованиям, при уровне СD4 клеток свыше 350 кл/мм3 (перед началом лечения ВИЧ) продолжительность жизни пациента с ВИЧ может доходить до семидесяти лет.
Целью лечения ВИЧ-инфекции является:
- остановка воспроизведения (размножения) вируса в организме. Показателем эффективности проводимой терапии является уменьшение вирусной нагрузки в течение четырех недель – более чем в десять раз. В течение 16-24 недель вирусная нагрузка должна снизиться менее чем до 20-50 копий/мл. Антиретровирусная терапия должна максимально длительно удерживать вирусологическую нагрузку на минимальном уровне;
- восстановление состояния иммунной защиты пациента до нормального уровня. При эффективной антиретровирусной терапии происходит снижение вирусной нагрузки и восстановление количества СD4 лимфоцитарных клеток, за счет чего происходит нормализация иммунного ответа;
- увеличение продолжительности и качества жизни пациента. При своевременном назначении лечения ВИЧ-инфекции, риск развития СПИДа сводится к минимуму. Также, за счет резкого снижения вирусной нагрузки, уменьшается вероятность передачи инфекции при половом акте, заражения ребенка во время беременности.
ВИЧ диссиденты – кто это
ВИЧ диссиденты – это группа людей, которые отрицают существование ВИЧ и считают антиретровирусную терапию заговором фармацевтических компаний.
Эти люди представляют особую опасность для общества. 
Такие люди запрещают лечить своих детей (наибольший процент смертей от ВИЧ регистрируется у детей, не получавших лечение из-за родителей ВИЧ диссидентов). Не принимают лечение сами, и, как правило, не предохраняются при половых контактах, считая, что они здоровы (это приводит к увеличению количества заболевших ВИЧ).
Справочно. В качестве примера ВИЧ-диссидента можно привести Софью Мясковскую (орловская ВИЧ диссидентка). Она умерла от осложнения ВИЧ (двусторонней пневмонии). Также запрещала лечить своих детей, двое из которых умерли от осложнений ВИЧ в возрасте четырех лет и года.
Особенности лечения ВИЧ-инфицированных пациентов
Главной проблемой лечения пациентов с ВИЧ-инфекцией является высокая степень мутагенности вируса иммунодефицита. Вирус способен молниеносно мутировать и сохранять жизнеспособность и активность даже в неблагоприятных условиях.
Справочно. Лечение ВИЧ при помощи ВААРТ направленно на быстрое подавление вирусной нагрузки и профилактику развития резистентности вируса к препаратам.
При применении монотерапии (только один препарат) отмечается высокий риск быстрого развития устойчивости вируса. В связи с этим, лечение ВИЧ при помощи комбинированной терапии значительно превосходит по эффективности монотерапию.
Ранее, для лечения ВИЧ чаще всего назначали зидовудин, однако при такой монотерапии вирус быстро вырабатывал устойчивость. На данный момент, для профилактики развития устойчивости чаще всего применяют схемы, состоящие из трех-четырех антиретровирусных препаратов одновременно. Такие комбинированные схемы позволяют не только быстро и эффективно снизить вирусную нагрузку, но и уничтожить мутантные формы ВИЧ, появляющиеся во время прогрессирования заболевания.
Очень важно! Нужно понимание пациента, что эффективность лечения ВИЧ-инфекции напрямую зависит от его осознанного подхода к лечению. Самостоятельная коррекция назначенных дозировок, пропуск приема препарата, употребление спиртных напитков, могут привести к появлению мутантных, неподдающихся лечению штаммов ВИЧ инфекции.
Важно отметить, что лечение ВИЧ-инфекции оплачивается из федерального и регионального бюджета. Большая часть препаратов для лечения ВИЧ-инфекции внесены в список жизненно важных лекарственных средств. Препараты выдаются в специальных СПИД-центрах , инфекционных отделениях.
В свободном доступе в аптеках препараты для лечения ВИЧ отсутствуют.
При назначении антиретровирусной терапии учитывают:
- степень тяжести иммунодефицита до начала антиретровирусной терапии (оценивается вирусная нагрузка и количество СD4 лимфоцитарных клеток);
- риск развития устойчивости ВИЧ к проводимой терапии (оценивается эпидемическая ситуация в регионе и анамнез пациента (назначалась ли ему ранее АРТ));
- риски прогрессирования заболевания (прогноз зависит от исходного уровня CВ4 клеток и вирусной нагрузки);
- готовности пациента начать лечение и четко следовать рекомендациям врача и соблюдать назначенные схемы лечения;
- осведомленность пациента о возможных побочных эффектах проводимой антиретровирусной терапии;
- эффективность проводимой стартовой терапии, скорость достижения стойкого вирусологического ответа (снижение вирусной нагрузки, увеличение уровня СD4 клеток);
- фармакологическую целесообразность различных схем антиретровирусной терапии (все схемы антиретровирусной терапии должны подбираться индивидуально для каждого пациента).
Антиретровирусная терапия назначается согласно протоколам ВААРТ (схемы 1-го, 2-го и 3-го ряда).
Режим дозирования препаратов
Лечение ВИЧ инфекции требует четкого соблюдения назначенного режима дозирования. Чаще всего, все препараты принимаются одновременно и однократно. Такие схемы разработаны для удобства пациента и снижения риска пропуска приема препаратов.
Внимание. При пропуске назначенной дозы запрещено принимать увеличенные или сниженные дозировки средства, а также менять назначенные схемы лечения. Также запрещено сочетать прием антиретровирусной терапии со спиртными напитками.
- значительно снижает эффективность проводимой терапии;
- увеличивает риск быстрого мутирования ВИЧ и развития устойчивости к препаратам;
- повышает вероятность развития побочных эффектов от проводимой терапии;
- увеличивает риск быстрого прогрессирования заболевания в стадию СПИДа.
Диета при ВИЧ-инфекции
Специальной диеты для пациентов с ВИЧ-инфекцией не разработано. Однако, необходимо учитывать, что ВИЧ инфекция часто сочетается с хроническим гепатитом С, при котором требуется строгое соблюдение диетического питания.
Также следует отметить, что прием антиретровирусной терапии создает большую нагрузку на печень. 
В связи с этим, пациентам с ВИЧ-инфекцией рекомендовано соблюдать облегченную диету, богатую клетчаткой, белком и витаминами. Следует исключить из рациона жирные, жареные продукты, фаст-фуд, спиртные напитки.
Пациентам рекомендовано увеличить употребление нежирных сортов рыбы, овощей, фруктов, орехов.
Препараты для лечения ВИЧ инфекции
Для антиретровирусной терапии применяют группы:
- нуклеозидных/нуклеотидных ингибиторов обратных транскриптаз (к группе НИОТ относят препараты абакавир, зидовудин, ламивудин, диданозин, ставудин, фосфазид);
- ненуклеозидных ингибиторов обратной транскриптазы (к группе ННИОТ относят препараты ифавиренц (эфавиренз), невирапин, этравирин);
- ингибиторов протеаз (в группу ИП относят препараты атазанавир, индинавир, лопинавир/ритонавир, нелфинавир, фосампренавир, саквинавир, ритонавир, дарунавир);
- ингибиторов фузии (слияния) – препараты энфувиртида.
ВААРТ – показания
При наличии у пациента СПИД-индикаторных состояний или симптомов ВИЧ-инфекции ВААРТ назначают (или продолжают проводить) при любых значениях CD4 лимфоцитарных клеток и любой вирусной нагрузке. 
Пациентам с бессимптомным течением ВИЧ назначение ВААРТ показано при любом уровне вирусной нагрузки, при условии, что уровень CD4-лимфоцитарных клеток ниже 200 на 1 мкл.
Справочно. Пациентам с бессимптомным течением ВИЧ, при уровне лимфоцитарных клеток от 200 до 350 в 1 мкл и показателях вирусной нагрузки ниже 20 000 копий в 1 мл – многие специалисты рекомендуют отложить назначение ВААРТ, однако Европейское клиническое общество СПИДа рекомендует назначение ВААРТ вне зависимости от показателей вирусной нагрузки.
Этой же группе пациентов, при показателях вирусной нагрузки свыше 20 000 копий в 1 мл – следует начинать лечение ВИЧ при помощи ВААРТ.
Независимо от показателя вирусных нагрузок – лечение ВААРТ показано пациентам с высоким риском прогрессирования ВИЧ.
Показаниями для назначения ВААРТ у детей являются:
- клинические проявления ВИЧ инфекции (ВААРТ назначается независимо от уровня СD4 лимфоцитарных клеток показателей вирусной нагрузки);
- признаки умеренной или выраженной иммуносупрессии, также снижение абсолютного или относительного содержания уровня СD4 лимфоцитарных клеток.
Эффективность проведения ВААРТ у детей младше года не исследовалась, поэтому целесообразность проведения лечения ВИЧ в этой возрастной категории определяется индивидуально (на основании клинической симптоматики, а также данных иммунологической и вирусологической диагностики).
У детей старше года, при бессимптомном течении ВИЧ-инфекции, нормальном уровне СD4 лимфоцитарных клеток в анализах и низком риске прогрессирования ВИЧ, начало ВААРТ может быть отложено.
В таком случае проводится регулярный тщательный контроль вирусологической нагрузки и уровня СD4-лимфоцитарных клеток.
При повышении уровня вирусной нагрузки, быстром снижении СD4-лимфоцитарных клеток, а также появлении симптомов ВИЧ показано начало лечения ВИЧ-инфекции при помощи ВААРТ.
Необходимо понимать, что отсутствие показаний для проведения ВААРТ не означает отмену лечения ВИЧ. ВААРТ подразумевает одновременное применение трех-четырех препаратов против ВИЧ. А пациентам с низким риском прогрессирования ВИЧ и умеренной иммуносупрессией могут назначаться схемы с применением двух антиретровирусных препаратов.
Обследования перед назначением ВААРТ
Обязательные обследования будут назначены врачом исходя из предварительного собеседования.
К дополнительным обследованиям относятся:
- туберкулиновые пробы у пациентов без симптомов туберкулеза;
- микроскопия окрашенных мазков мокроты и проведение рентгенологического исследования органов грудной клетки у пациентов с симптомами туберкулеза;
- ЭКГ – показано для контроля состояния сердечно-сосудистой системы (применение ВААРТ повышает риски развития патологий сердечно-сосудистой системы);
- осмотры у невропатолога для своевременной диагностики периферических полинейропатий, ВИЧ-деменции.);
- осмотры у офтальмолога (при уровне CD4 лимфоцитарных клеток ниже 100 клеток в 1 мкл, следует проводить осмотр каждые три месяца, для своевременной диагностики цитомегаловирусных ретинитов);
- осмотры у гинеколога, проведение цитологических исследований Пап-мазка (мазки следует сдавать каждые шесть месяцев – для своевременной диагностики рака шейки матки, связанным с вирусом папилломы человека).
Схемы ВААРТ
Выбор схемы для лечения ВИЧ всегда индивидуален и зависит от таких факторов как:
- индивидуальные особенности пациента (его способность тщательно соблюдать назначенные схемы лечения, данные о злоупотреблении алкоголем или приеме психоактивных веществ в анамнезе, желание забеременеть у женщин);
- проводимая ранее терапия ВААРТ (учитывается эффективность проводимого ранее лечения, развитие или отсутствие устойчивости к препаратам против ВИЧ);
- наличие оппортунистических заболеваний;
- наличие и выраженность симптомов ВИЧ и СПИДа;
- наличие сопутствующих заболеваний (сахарный диабет, патологии печени);
- риск прогрессирования заболевания;
- уровень СD4 клеток и показатели вирусной нагрузки.
Назначение монотерапии нецелесообразно на любой стадии ВИЧ инфекции, поскольку последние исследования подтвердили ее низкую эффективность и высокие риски развития у вирусов иммунодефицита человека устойчивости к применяемому препарату в течение первых трех месяцев от начала терапии. 
Применение препаратов зидовудина в качестве монолечения ВИЧ оправдано только при полном отсутствии возможности провести комбинированную терапию ВИЧ (как минимум, с применением 2 нуклеозидных/нуклеотидных ингибиторов обратных транскриптаз).
Назначение схемы при помощи 2 нуклеозидных/нуклеотидных ингибиторов обратных транскриптаз (препараты зидовудина+диданозина или зидовудина+зальцитабина) рекомендовано пациентам с умеренным понижением уровня CD4 лимфоцитарных клеток (200 – 350 клеток в 1 мкл), а также при отсутствии возможности назначить схему ВААРТ из трех-четырех препаратов.
Справочно. Применение трехкомпонентных или четырехкомпонентных схем позволяет добиться максимальной эффективности от проводимой терапии и свести к минимуму риск развития у вируса резистентности к препаратам и прогрессирования ВИЧ до СПИДа.
Разработка схемы: 2 нуклеозидных/нуклеотидных ингибитора обратных транскриптаз + 1 ингибитор протеаз или 1 ненуклеозидный ингибитор обратной транскриптазы, позволила значительно улучшить качество жизни пациентов с ВИЧ и снизить частоту развития оппортунистических инфекций.
Также на фоне данной терапии отмечается обратное развитие саркомы Капоши и выраженное замедление прогрессирование симптомов нейроСПИДа .
Для терапии первого ряда показано применение 2 нуклеозидных/нуклеотидных ингибитора обратных транскриптаз + 1 ненуклеозидный ингибитор обратной транскриптазы.
Рекомендовано применение следующих схем:
- препараты зидовудина + ламивудина + (эфавиренза или невирапина);
- препараты тенофовира +эмтрицитабина (эфавиренза или невирапина);
- препараты абакавира + ламивудина (эфавиренза или невирапина).
В большинстве случаев, из препаратов ненуклеозидных ингибиторов обратных транскриптаз предпочтение отдается эфавирензу.
В качестве базы для ВААРТ первого ряда рассматривается комбинация двух препаратов нуклеозидных ингибиторов обратных транскриптаз. Эмтрицитабин в комбинированных схемах выступает как менее токсичный аналог ламивудина.
Также было доказано, что сочетание тенофовира и эмтрицитабина несколько эффективнее, чем сочетание зидовудина и ламивудина, при их комбинировании с препаратами эфавиренза.
Однако перед назначением тенофовира следует провести тщательное обследование функции почек.
Внимание. Препараты ставудина, на данный момент, исключены из большинства схем из-за низкого профиля безопасности и высокой частоты развития побочных эффектов от проводимой терапии.
При назначении ВААРТ важно учитывать ряд ограничений:
По показаниям, могут назначаться схемы, содержащие три нуклеозидных/нуклеотидных ингибитора обратных транскриптаз:
- препараты зидовудина+ ламивудина+абакавира;
- препараты зидовудина+ламивудина+тенофовира.
Такие схемы показаны пациентам с тяжелыми патологиями печени, непереносимостью препаратов ННИОТ, психическими нарушениями, ВИЧ2 инфекциями.
В схемах второго ряда предпочтение отдается сочетанию лопинавира и ритонавира, в редких случаях может применяться сочетание атазанавира и ритонавира, саквинавира и ритонавира. 

Профилактика развития ВИЧ
Профилактика развития ВИЧ инфекции включает:
- защищенные половые контакты (использование презерватива);
- регулярные обследования на заболевания, передающиеся половым путем;
- отказ от употребления наркотических средств;
- осознанный подход к собственному здоровью (высокий риск заражения отмечается при выполнении криминальных абортов, нанесении татуировок в заведениях без лицензии);
- тщательное обследование доноров;
- обследование беременных для исключения заражения плода и новорожденного при кормлении грудью.
Читайте также:


