Удалить шейку матки при вич
Вирус иммунодефицита человека (ВИЧ) разрушает специфические иммунные клетки и тем самым ослабляет иммунитет, делая его бесполезным в борьбе с инфекциями и болезнями. Нелеченная ВИЧ-инфекция прогрессирует к синдрому приобретенного иммунодефицита (СПИД), состояние, которое развивается в результате полного разрушения иммунитета вирусом.
Хотя возможно, что у ВИЧ-инфицированной женщины может и не быть никаких симптомов ВИЧ-инфекции, но в большинстве случаев женщина инфицированная ВИЧ испытывает некоторые симптомы, которые она не связывает с наличием ВИЧ в своём организме. В этом и коварство ВИЧ — он проникает в организм и тихо сидит и незаметно разрушает иммунную систему, чтобы она не смогла противостоять никаким заболеваниям. Потому что в норме, иммунная система постоянно защищает нас от множества болезнетворных возбудителей болезни, а мы этого не замечаем. Когда ВИЧ уничтожает иммунитет, то все эти инфекции вприпрыжку вторгаются в организм женщины беспрепятственно. Отсюда и разнообразие и неспецифичность симптомов. И главный критерии диагностики здесь — анализ крови на ВИЧ . Делайте его регулярно! Хотя бы как минимум 1 раз в год.
Хотя у мужчин и женщин признаки ВИЧ в основном похожие, но у женщин есть симптомы иммунодефицита, которые характерны только для них.
- Частые или тяжелые вагинальные инфекции.
- Атипичные результаты мазка на определение атипичных клеток (Папаниколау).
- Воспаление органов малого таза.
Если у Вас есть хотя бы один из вышеперечисленных состояний — немедленно обратитесь к врачу!
Другими, менее распространенными симптомами наличия ВИЧ в организме женщины являются:
- язвы, эрозии на половых органах,
- тяжелотекущие, плохо поддающиеся лечению герпес, грибковые инфекции (молочница).
- нарушения менструального цикла (изменение интенсивности выделений, пропуски цикла, очень тяжелый ПМС). Стресс и ЗППП, которые часто сопровождают ВИЧ-инфекцию, также могут быть причиной таких нарушений.
- боль внизу живота. Может быть признаком инфекции матки, яичников, фаллопиевых труб — воспалительного заболевания малого таза (ВЗОМТ). У части женщин, ВЗМОТ — это как красный сигнал светофора, кричащий о наличии ВИЧ в организме женщины.Также ВЗОМТ может проявляться: необычными выделениями из влагалища, температурой, нерегулярными менструациями, болью во время соития, болью в верхней части живота.
Для дополнительного чтения:
Описанные здесь симптомы не говорят, что у женщины 100% ВИЧ, а они говорят о том, что нужно обследоваться на ВИЧ.
Через какое время появляются первые симптомы ВИЧ у женщин?
Какие симптомы ВИЧ появляются у женщин на ранних стадиях во рту?
— На ранних стадиях ВИЧ во рту у женщин появляются белые налеты, белые бляшки (молочница, кандидоз). / Посмотреть фото признаков ВИЧ в ротовой полости /.
Какие симптомы ВИЧ появляются у женщины на ранних стадиях на коже?
— На ранних стадиях ВИЧ на коже у женщин появляется сыпь. / Прочитать более подробно о признаках ВИЧ/СПИДа на коже /.
Набор первых признаков наличия ВИЧ-инфекции у женщины в каждом случае может быть разным, они могут появляться уже через 2-4 недели после заражения, а иногда и через несколько лет. Поэтому так важно для Вас и Вашего полового партнера пройти тестирование на ВИЧ перед началом отношений. Чем раньше ВИЧ обнаружен у женщины, тем раньше можно назначить лечение и предотвратить развитие СПИДа и не заразить другого человека (потом он спасибо не скажет). Твитнуть Существуют различные симптомы ВИЧ-инфекции у женщин в зависимости от стадии заболевания:
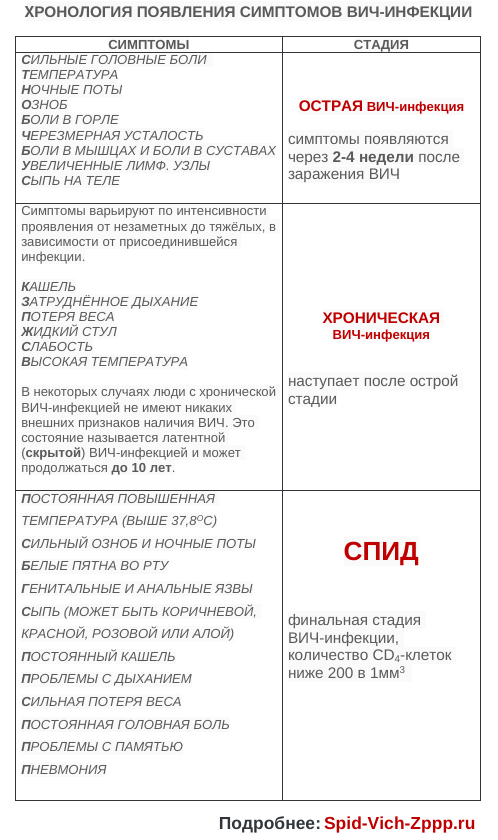
Первыми симптомами ВИЧ-инфекции у женщин в ранней стадии могут быть:
- сыпь на теле,
- лихорадка,
- боли в горле,
- сильные головные боли.
- увеличение лимфатических узлов,
- тошнота,
- усталость,
- язвы во рту,
- вагинальные инфекции, такие как дрожжевые инфекции и бактериальный вагиноз,
- ночные поты,
- рвота,
- боли в мышцах и боли в суставах.

Главные симптомы острой ВИЧ-инфекции
Во время острой стадии ВИЧ-инфекции, эти симптомы чаще всего длятся от одной до двух недель.
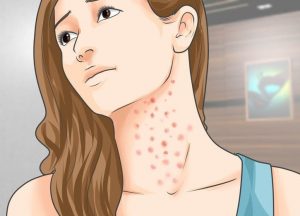
Специфичные симптомы ВИЧ — беспорядочные высыпания
Когда вышеупомянутые симптомы исчезают, тогда начинается бессимптомный период ВИЧ-инфекции. На этой стадии человек с ВИЧ не чувствует каких-либо признаков или симптомов ВИЧ-инфекции. ВИЧ может не вызывать никаких симптомов в течение нескольких месяцев или лет, но он присутствует в организме и активно размножается и начинает разрушать иммунную систему организма путем атаки на важные иммунные клетки. Вирус остается активным в течение этой стадии и по-прежнему может передаваться другим лицам, поэтому важно, вовремя пройти тестирование на ВИЧ-инфекцию, даже если Вы чувствуете себя хорошо.
Без лечения, для перехода ВИЧ-инфекции в СПИД требуются месяцы и годы в зависимости от степени разрушения вирусом иммунной системы женщины. Такое прогрессирование ВИЧ приводит к СПИДу (синдрому приобретенного иммунодефицита). Это последняя стадия ВИЧ-инфекции и она означает, что иммунная система организма сильно повреждена, в результате чего она становится более восприимчивой к другим инфекциям, женщина начинает болеть такими болезнями, которыми не болела при здоровой иммунной системе. Больные СПИДом женщины часто болеют простудами, гриппом, грибковыми заболеваниями.
Какие симптомы ВИЧ появляются у женщин на ранних стадиях в паху?
— На ранних стадиях ВИЧ в паху у женщин появляются увеличенные паховые лимфатические узлы.
Симптомы женщины в стадии СПИДа:
- постоянный понос,
- тошнота,
- рвота,
- быстрая беспричинная потеря веса,
- постоянная беспричинная усталость,
- эрозии или язвы во рту,
- вагинальные инфекции, такие как дрожжевые инфекции (молочница, кандидоз) и бактериальный вагиноз,
- воспалительные заболевания тазовых органов,
- периодическое повышение температуры (лихорадка),
- повторяющиеся ознобы,
- повторяющиеся ночные поты,
- сбивчивое дыхание,
- сухой кашель,
- стойкое или длительное увеличение лимфатических узлов,
- потеря памяти, спутанность сознания, неврологические расстройства.
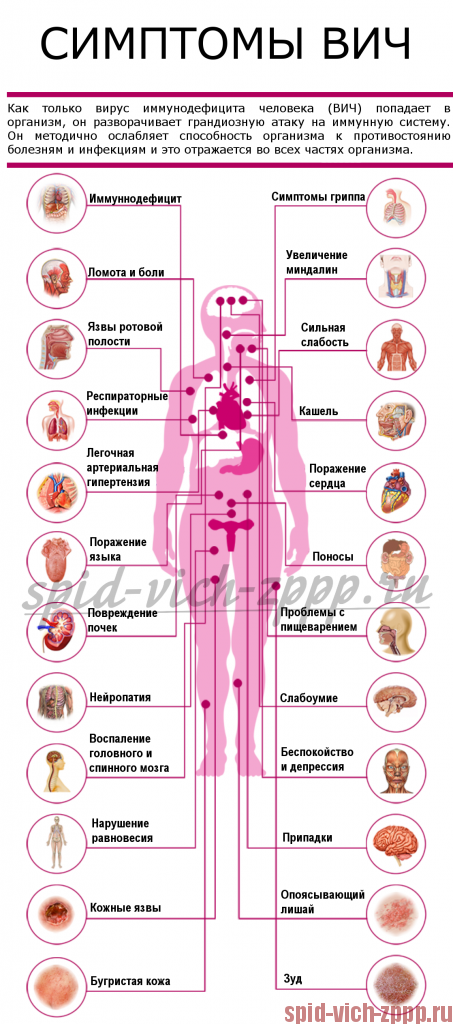
Симптомы ВИЧ, СПИДа
- молочница и другие вагинальные инфекции, бактериальный вагиноз,
- заболевания передающиеся через соитие: гонорея (трипер), хламидиоз, трихомониоз,
- воспаление тазовых органов (цистит (воспаление мочевого пузыря), уретрит (воспаление мочеиспускательного канала) и др.),
- инфекционное воспаление репродуктивных органов (эндометрит (воспаление слизистой матки), вульвовагинит (воспаление влагалища и вульвы), аднексит (воспаление яичников) и др.),
- нарушение менструального цикла (дисменорея),
- вирус папилломы человека, который вызывает бородавки на половых органах и ведет к раку шейки матки.
Еще одно отличие от ВИЧ-инфицированого мужчины в том, что ВИЧ плюс женщине труднее заметить пятнышки или другие изменения на половых органах.
У любой женщины, независимо от её ВИЧ статуса может появляться молочница. Но у женщин, которые ВИЧ плюс молочница возникает чаще и труднее поддается лечению.
- зуд вульвы,
- толстый белый налет на поверхности влагалища,
- жжение во время мочеиспускания,
- сухость влагалища и покраснение.
Болезненные ощущения во время полового акта. Женщины с молочницей должны избегать половых сношений, т.к. это может ухудшить течение болезни.
Вирус папилломы человека — это вирусная инфекция, которая разрушает клетки в половых органах, особенно в шейки матки. Существует много разных видов вируса папилломы человека (ВПЧ), есть очень вредные, которые вызывают рак и предраковые эрозии шейки матки.
Как показали исследования, у женщин инфицированных ВИЧ ВПЧ встречается в 10 раз чаще, чем у ВИЧ отрицательных женщин, особенно часто у ВИЧ-инфицированных женщин, у которых количество CD4-клеток менее 500 клеток/мкл. В другом исследовании было выявлено, что 77% ВИЧ-положительных женщин инфицированы ВПЧ.
ВПЧ очень сильно распространен среди ВИЧ плюс женщин. Поэтому его лечение должно быть начато незамедлительно, чтобы избежать распространение поражений вирусом и серьёзных осложнений.
У ВИЧ-инфицированных женщин вирус папилломы человека в 30 раз чаще вызывает рак шейки матки.
Обычно ВПЧ протекает бессимптомно, но иногда может проявляться белыми маленькими наростами (бородавками) или пятнами на влагалище или вокруг ануса. Также ВПЧ может сопровождаться дискомфортом, болезненными ощущениями во время полового соития. Врач обычно диагностирует ВПЧ делая мазок, биопсию, колпоскопию ( осмотр входа во влагалище, стенок влагалища и влагалищной части шейки матки с помощью увеличительных приборов ).
Бородавки могут быть удалены путем прижигания, замораживания, срезания, обработки химическими средствами (специально предназначенных для этой цели!), лечения лекарствами.
Воспаление органов малого таза (ВОМТ) — это очень серьезное осложнение (особенно у ВИЧ-инфицированных женщин, у которых очень сильно снижаются защитные силы организма), причиной которого является не леченная инфекция влагалища или шейки матки. Если не лечить, то бактерия может перейти с влагалища или шейки матки через мочеиспускательный канал и фаллопиевые трубы на яичники и окружающие ткани. ВОМТ может быть причиной нарушения (слипание фоллопиевых труб, что ведет к внематочной беременности) репродуктивной (способность к рождению) функции и даже может привести к смерти. Больше всего вызывают ВОМТ хламидии и гонорея.
Лечение ВОМТ требует очень строгого сильного курса антибиотиков и женщинам с ВИЧ часто требуется хирургическое вмешательство.
Главными симтомами ВОМТ являются:
- лихорадка,
- возрастающие неприятные ощущения во влагалище,
- волнообразные боли внизу живота от умеренных до сильных,
- кровотечения,
- тошнота,
- частые боли при мочеиспускании,
Но во многих случаях симптомы отсутствуют и женщина не подозревает, что воспаление прогрессирует.
Так как гинекологические инфекции это первая и наиболее распространенная проблема у ВИЧ-инфицированных женщин, поэтому необходимо регулярно проходить обследования влагалища и шейки матки.
Женщинам с ВИЧ не рекомендуется использовать ВМС (внутриматочную спираль) как противозачаточное средство, т.к. спираль это прямой путь к инфицированию и заболеванию органов малого таза.
ВИЧ также может передаваться от матери к ребенку во время родов (так называемый перинатальный ВИЧ) или через грудное вскармливание. Т.к. в России все беременные женщины должны проходят тестирование на ВИЧ на протяжении всей беременности, то выявление ВИЧ у женщины во время беременности помогает врачу вовремя назначить антиретровирусные препараты женщине и ребенку сразу после рождения, провести кесарево сечение для предотвращения передачи ВИЧ от матери к ребенку. При правильном назначении лекарств против ВИЧ риск инфицирования ВИЧом ребенка во время рождения от ВИЧ плюс матери можно снизить до менее 2%. Без лекарств риск родить больного ВИЧом ребёнка составляет около 40%.
Необходимо срочно посетить врача для осмотра, обследования, назначения анализов на ВИЧ , другие инфекции передающиеся половым путём.
Читать ещё личные истории ВИЧ-инфицированных:
Попова М.Ю., Танцурова К.С., Яковлева Ю.А.
Рак шейки матки у ВИЧ-инфицированных женщин
Попова М.Ю., Танцурова К.С., Яковлева Ю.А.
ФГБОУ ВО Южно-Уральский ГМУ Минздрава России
Кафедра акушерства и гинекологии
Рак шейки матки у ВИЧ-инфицированных женщин
Попова М.Ю., Танцурова К.С., Яковлева Ю.А.
ФГБОУ ВО Южно-Уральский ГМУ Минздрава России
Кафедра акушерства и гинекологии
Рак шейки матки у ВИЧ-инфицированных женщин
Попова М.Ю., Танцурова К.С., Яковлева Ю.А.
ФГБОУ ВО Южно-Уральский ГМУ Минздрава России
Кафедра акушерства и гинекологии
Актуальность. Рак шейки матки (РШМ) представляет собой одну из наиболее частых злокачественных опухолей̆ женской репродуктивной системы. Среди онкологических заболеваний у молодых женщин рак шейки матки имеет самые высокие показатели смертности. Источником раковой опухоли шейки матки служат нормальные клетки, покрывающие шейку матки. Ежегодно эту опухоль выявляют более чем у 600 тысяч пациенток [6]. Вирус иммунодефицита человека (ВИЧ) вызывает синдром приобретенного иммунодефицита (СПИД) и является одним из факторов риска развития плоскоклеточного интраэпителиального поражения или squamous intraepithelial lesion (SIL), возникающего в результате нарушения иммунного контроля. С течением времени SIL переходит в инвазивный рак шейки матки.
Цель работы. Изучить особенности возникновения, течения, диагностики, лечения рака шейки матки у ВИЧ- инфицированных женщин.
Задачи исследования. Установить взаимосвязь прогрессирования рака шейки матки у женщин с ВИЧ-положительным статусом.
Материалы и методы. По классификации выделяют LSIL, или Low grade SIL, или легкая степень и HSIL, или Hight grade SIL, или тяжелая степень. SIL должна своевременно лечиться (путем удаления или уничтожения внешних слоев клеток шейки
матки), чтобы не дать ей перерасти в инвазивный рак.
У ВИЧ инфицированных женщин переход SIL в рак шейки матки происходит намного быстрее, чем у здоровых женщин, вследствие поражения иммунной системы. ВИЧ поражает клетки крови человека, имеющие на своей поверхности CD4-рецепторы, а именно: Т-лимфоциты, макрофаги и дендритные клетки. Инфицированные Т-лимфоциты гибнут из-за разрушения вирусом, апоптоза и уничтожения цитотоксическими Т-лимфоцитами. Если число CD4+ T-лимфоцитов становится ниже 200 в одном микролитре крови, система клеточного иммунитета перестает защищать организм [3]. Исследования показали, что нелеченая неоплазия шейки матки с большей вероятностью переходит в инвазивный рак у ВИЧ-инфицированных женщин, чем у здоровых [4, 5].
При жидкостной цитологии забор материала проводится цитощетками, которые предназначены для взятия биологического материала с поверхности шейки матки и из цервикального канала для цитологических и бактериологических исследований, при этом образец не сразу переносится на стекло, а цитощетка с собранным материалом погружается в специальный раствор и затем с помощью прибора готовится образец для исследования. Цитощетка удобна в применении, атравматична для взятия материала. При необходимости рабочая часть может быть согнута под любым углом по отношению к рукоятке. Это позволяет адаптировать инструмент в зависимости от анатомических особенностей зоны, с которой выполняется забор материала.
Терапия требует чёткого соблюдения графика приёма. Недопустимо пропускать приемы препаратов, как и принимать уменьшенные или увеличенные дозы в случае пропуска.
Появление и развитие рака шейки матки — это многоступенчатый процесс. Этапы развития рака шейки матки представлены следующим образом: нормальный эпителий шейки матки => дисплазия эпителия (легкая, умеренная, тяжелая) => внутриэпителиальный рак (или рак 0 стадии, неинвазивный рак) => микроинвазивный рак => инвазивный рак. Самыми ранними проявлениями могут быть водянистые обильные выделения, кровянистые выделения, которые у женщин детородного возраста не связаны с менструациями, а у женщин в постменопаузе наблюдаются постоянно или периодически, выделения могут иметь неприятный запах. Выделение мочи и кала через влагалище свидетельство мочевлагалищных и прямокишечно-влагалищных свищей. При IV стадии появляются метастатические паховые и надключичные лимфоузлы.
Рак шейки матки делят на четыре стадии (I, II, III и IV), каждая из стадий делится на две подстадии (A и B), а каждая из подстадий IA и IB еще на две — IA1, IA2 и IB1, IB2. Выбор метода лечения рака шейки матки зависит от стадии заболевания. Хирургическое лечение используют при стадиях IA1, IA2, IB и реже IIA. Объем операции зависит от глубины инвазии, наличии метастазов в тазовых и парааортальных лимфоузлах. При стадии IA1 возможно выполнение конизации шейки матки (клиновидная биопсия, конусовидная эксцизия — ампутация конусовидного участка шейки матки, которая состоит в удалении части шейки матки в виде конуса) или простой экстирпации матки с придатками: трубами и яичниками. При стадиях IA2, IB1, IB2 и IIA показана радикальная экстирпация матки с удалением тазовых, а иногда и парааортальных лимфоузлов. Во время этой операции кроме матки с придатками и лимфоузлов удаляют еще и верхнюю треть влагалища, а также части связок матки и жировую клетчатку параметрия и клетчатку, окружающую шейку матки. При обнаружении метастазов в лимфоузлах, лечение после операции дополняют лучевой или одновременной химиолучевой терапией. Обычно комбинированное лечение (операция+лучевая терапия) проводят при стадиях IB и IIA. Иногда при инвазивном раке шейки матки (стадии IA2, IB1) выполняют сложную радикальную операцию, которая позволяет сохранить детородную функцию, под названием трахелэктомия. Во время операции удаляют только пораженную раком ткань шейки матки и окружающие лимфатические узлы [4]. Эффективность хирургического лечения и лучевой терапии при ранних стадиях инвазивного рака шейки матки практически одинаковая, лучевая терапия используется в виде дистанционной гамматерапии и брахитерапии. Длительность сочетанной лучевой терапии (дистанционной и брахитерапии) не должна превышать 55 дней. При стадиях IB2–IV стандартным лечением во всем мире признана одновременная химиолучевая терапия (раньше при этих стадиях проводили только лучевую терапию). При IVB стадии возможно применение только химиотерапию. Однако, женщины больные СПИДом и раком шейки матки одновременно, вылечиваются от рака не так успешно, как ВИЧ-отрицательные пациентки [5, 6].
Результаты исследования. Таким образом, в связи с большой вероятностью возникновения рака шейки матки у ВИЧ-инфицированных женщин и с целью раннего его выявления, им необходимо сделать ПАП-мазок, при отсутствии выявления атипичных клеток, необходимо повторить исследование через полгода, а затем, при отрицательных результатах, 1 раз в год. При обнаружении в ПАП-мазке всех видов SIL выполняется кольпоскопия с прицельной биопсией изменённых участков слизистой матки. Это позволяет не только выявить рак шейки матки на начальных стадиях, но также предупредить его развитие, путём диагностирования предопухолевых изменений эпителия шейки матки, лечение которых не позволяет развиться опухоли.
Выводы. СПИД-ассоциированный рак шейки матки развивается более стремительно, чем рак шейки матки ВИЧ-отрицательных женщин и приводит к многочисленным осложнениям. У женщин с положительным ВИЧ статусом предопухолевое состояние шейки матки с большей̆ вероятностью переходит в инвазивный рак, чем у ВИЧ-отрицательных женщин. Женщины, больные СПИД и ВИЧ-инфицированные женщины, должны находиться под постоянным наблюдением системой здравоохранения, так как имеют более высокий риск развития рака шейки матки.
Список литературы
1. У В.Н. Ошибки в лечении дисплазии шейки матки / В.Н. Беляковский // Иммунопатология, аллергология, инфектология. – 2008. – №1. – С. 83-87.
2. Биджиева Б.А. Генетическая нестабильность и аллельный полиморфизм у больных с дисплазиями и раком шейки матки, вызванными персистенцией ДНК вируса папилломы человека / Б.А. Биджиева. – М.: МИА, 2008. – 34 с.
3. Красногольский В.И. Патология влагалища и шейки матки / В.И. Красногольский. – М.: Медицина, 2007. – 172 с.
4. Прилепская В.Н., Роговская С.И., Межевитинова С.А. Кольпоскопия: практическое руководство / В.Н. Прилепская, С.И. Роговская, С.А. Межевитинова. – М.: МИА, 2001. – 100 с.
5. Садовникова В.Н., Вартапетова Н.В., Карпушкина A.B. Эпидемиологическая характеристика ВИЧ-инфекции у женщин / В.Н. Садовникова, Н.В. Вартапетова, А.В. Карпушкина // Эпидемиология и вакцинопрофилактика. – 2011. – №6. – С. 4-10.
6. Трушина О.И., Новикова Е.Г. Роль папилломавирусной инфекции в генезе рака шейки матки / О.И. Трушина, Е.Г. Новикова // Российский онкологический журнал. – 2009. – №1. – С. 45- 51.
Рак шейки матки (РШМ) занимает второе место в структуре смертности от онкологических заболеваний у женщин [3]. Диагностика и лечение патологии шейки матки остается одной из актуальных проблем гинекологии и, несмотря на успехи современной медицины, уровень заболеваемости имеет устойчивый восходящий тренд. Этиологическим фактором в развитии дисплазии шейки матки признано поражение вирусом папилломы человека (ВПЧ), а длительная персистенция ВПЧ способствует возникновению рецидивов и/или злокачественной трансформации поражений [4]. Особую актуальность представляет проблема заболеваний шейки матки у больных, пораженных вирусом иммунодефицита человека (ВИЧ). Это обусловлено тем, что повреждения шейки матки ВПЧ развиваются на фоне дисфункции иммунитета с нарушением противовирусного ответа [2], а наблюдение и обследование больных ВИЧ-инфекцией могут помочь смоделировать развитие интраэпителиальных повреждений в условиях иммунодефицита и разработать методы профилактики и лечения.
Накопленные данные исследователей всего мира показывают, что ВИЧ-инфицированные женщины отличаются более высоким уровнем хронического поражения ВПЧ, многообразием типов онкогенных вирусов, более частыми патологическими изменениями мазков по Папаниколау, агрессивностью течения РШМ по сравнению с этими данными у ВИЧ-отрицательных пациенток [64]. Выявлена прямая зависимость между продолжительностью заражения ВИЧ-инфекцией и возникновением патологии шейки матки [41]. Несмотря на успехи применения высокоактивной антиретровирусной терапии (ВААРТ), уровень поражения РШМ у ВИЧ-инфицированных остается выше, чем в популяции [13]. Длительное применение ВААРТ продлевает жизнь ВИЧ-инфицированных пациенток, следовательно, растет удельный вес ВПЧ-индуцированных заболеваний у этой категории больных [64].
ВИЧ-инфекция повышает риск поражения наружных половых органов ВПЧ [66], способствует более раннему [17] и более частому [37, 43] развитию тяжелой формы дисплазии и РШМ. При этом, чем выше степень иммунносупрессии и ниже уровень клеток СD4+, тем чаще выявляются высокоонкогенные штаммы ВПЧ и интраэпителиальные заболевания шейки матки, вплоть до рака [6, 18, 24, 45, 63].
Повреждения шейки матки способствуют гетеросексуальной и перинатальной передаче ВИЧ-инфекции [74]. У юных беременных, перинатально зараженных ВИЧ-инфекцией, при обследовании во время беременности чаще, чем в популяции, выявляли патологию шейки матки методом Папаниколау [15].
Мониторинг больных с дисплазией шейки матки показал значимое прогрессирование процесса у ВИЧ-инфицированных больных по сравнению с его течением у здоровых женщин [59, 63]. При обследовании больных с дисплазией шейки матки II-III степени выявлено, что у ВИЧ-инфицированных снижены показатели местного иммунного ответа [5]. ВПЧ высокого онкогенного риска, выявленный методом полимеразной цепной реакции из отделяемого цервикального канала, низкий уровень СD4+ и высокая вирусная нагрузка, являются факторами, способствующими возникновению дисплазии шейки матки, интраэпителиальной неоплазии [30, 37, 50, 73]. Напротив, при уровне СД4+ более 500 клеток/мл частота диагностики внутриэпителиальных повреждений у больных с ВИЧ-инфекцией не отличается от таковой у здоровых пациенток [81].
Частота выявления ВПЧ-инфекции быстро возрастает в течение первых лет после сероконверсии ВИЧ, по всей видимости, вследствие иммунной дисфункции слизистой оболочки шейки матки, характерной для ВИЧ-инфекции [79]. Хотя ВПЧ-инфицирование связано с передачей половым путем, у 22% ВИЧ-инфицированных больных с уровнем СD4+ менее 200 клеток/мл, не живущих половой жизнью, выявляли, по крайней мере, один тип ВПЧ [75].
В образцах, полученных при биопсии шейки матки, с нормальным эпителием и особенно с цервикальной интраэпителиальной неоплазией (CIN) у ВИЧ-инфицированных больных значительно чаще выявляли маркеры апоптоза [78].
ВИЧ-инфекция запускает патогенез плоскоклеточного РШМ у ВПЧ-пораженных больных [8, 38]. Уровень заболеваемости РШМ у лиц с ВИЧ или СПИДом имел стойкую тенденцию к увеличению в США за период с 1980 по 2007 г. [72]. В некоторых странах Африки РШМ является причиной самой высокой смертности [54]. Этот факт объясняется большим количеством ВИЧ-инфицированных женщин и отсутствием возможности цитологического исследования шейки матки [20]. Замечено, что РШМ чаще поражает больных, заразившихся половым путем [28], причем количество больных РШМ растет вместе с ростом числа ВИЧ-инфицированных [62].
У ВИЧ-инфицированных спектр ВПЧ более многообразен, чем у ВИЧ-негативных больных [24]. ВИЧ-инфицированные больные, пораженные РШМ, в среднем на 13 лет моложе ВИЧ-негативных [61]. Одни авторы указывают, что ВПЧ 16-го типа выявлялся у больных с ВИЧ-инфекцией, повреждениями шейки матки высокой степени тяжести и РШМ значительно чаще, чем у женщин с нормальными цитологическими мазками [24, 30, 44, 70]. Другие получили противоположный результат – ВПЧ
16-го типа чаще регистрируют у ВИЧ-инфицированных, однако у пациенток с внутриэпителиальными поражениями плоского эпителия высокой степени (high grade squamous intraepithelial lesions – HSIL) он встречается не чаще, чем во всей группе [22]. Нам встретилась публикация, в которой утверждалось, что 16-й и 18-й типы ВПЧ преобладали у ВИЧ-негативных женщин, а у ВИЧ-инфицированных с внутриэпителиальными поражениями плоского эпителия слабой степени (low grade squamous intraepithelial lesions – LSIL) чаще диагностировали 56-й и 53-й типы, с HSIL – 52-й и 58-й типы ВПЧ соответственно [34, 55], и, напротив, 52-й тип чаще диагностируют у женщин с нормальной цитологической картиной мазка или низкой степенью злокачественности [24]. В других работах у ВИЧ-инфицированных больных при исследовании патологии шейки матки чаще выявляли 58-й и 52-й типы [11, 26] или 62-й тип ВПЧ [69]. Подобное расхождение в диагностике типов ВПЧ связано с географическим местом исследования, в частности, в Камеруне чаще всего выявляли 45-й и 58-й типы ВПЧ [25].
При исследовании цитокинов (γIFN, IL-10, TNFα) в биоптатах шейки матки, пораженных ВПЧ 16-го и 18-го типов, выявлено, что ВПЧ 16-го типа может вызвать повреждение эпителия вне зависимости от статуса ВИЧ [29]. Иммуногистохимическое исследование образцов на р16(INK4а) может использоваться для выявления ВПЧ-поврежденных клеток, потенциальных для злокачественного перерождения [67].
В настоящее время обязательным является ежегодный осмотр пациентки, включающий цитологическое исследование (РАР-тест), кольпоскопию, типирование ВПЧ у ВИЧ-инфицированных больных [19, 46]. Часто ВИЧ-инфицированные пациентки не знают, что использование РАР-теста может помочь в предотвращении РШМ [65], поэтому цитологическое исследование шейки матки должно быть включено в стандарт оказания помощи ВИЧ-инфицированным больным [65, 73]. Обязательному цитологическому обследованию должны быть подвергнуты ВИЧ-инфицированные пациентки старше 30 лет, так как у них вероятность диагностики повреждений шейки матки высокой степени тяжести достигает более 70% [9], и пациентки с уровнем СD4+ менее 200 клеток/мл [31].
Помимо РАР-теста в настоящее время для скрининга применяют цитологическое исследование вагинальных смывов, типирование ВПЧ, методы прямой визуализации [42]. Тестирование ВПЧ может способствовать сокращению числа случаев прогрессирующего РШМ [71]. Цитологическое исследование вагинальных смывов может быть альтернативой РАР-тесту [36], но не имеет преимуществ перед тестом Папаниколау [76]. Использование количественной оценки уровня вирусной нагрузки ВПЧ как маркера повреждения шейки матки у ВИЧ-инфицированных пациенток [51] и уровня СD4+ может быть полезным в качестве индикатора риска прогрессирования процесса [63].
ВПЧ проявляет наибольшую активность при уровне СD4+ менее 200 клеток/мл и вирусной нагрузке более чем 100 000 копий/мл [31, 75]. Любой подозрительный участок должен быть подвергнут биопсии и гистологической экспертизе [27], так как у 14,3% ВИЧ-инфицированных с нормальной цитологической картиной шейки матки выявляли CIN [7]. Эта группа больных характеризовалась уровнем СD4+ менее 500 клеток/мкл и поражением ВПЧ. Биопсия шейки матки должна сочетаться с выскабливанием цервикального канала, так как при этом значительно чаще выявляется патология у серопозитивных женщин [16].
Чаще всего для лечения повреждения шейки матки используется петлевая эксцизия, так как данная процедура может быть выполнена амбулаторно, позволяет исключить инвазивную неоплазию, оценить края резекции, сохранить репродуктивную функцию, сопровождается минимальной кровопотерей и низким процентом послеоперационных осложнений [68]. Однако данное вмешательство у ВИЧ-инфицированных больных менее эффективно, чем у ВИЧ-негативных пациенток [9, 52]. Петлевая эксцизия, выполненная больным с HSIL, несмотря на свою эффективность в 15% случаев дает рецидив процесса [53]. Рецидивы CIN после конизации составляют от 20 до 75% [77]. Описаны случаи развития рака через 2 года после петлевой эксцизии, выполненной по поводу LSIL [36]. Одной из причин неудачи считается низкий иммунный статус: при уровне СD4+ меньше 200 клеток/мл и CIN II-III степени [56]. Напротив, при уровне СD4+ более 500 клеток/мл, 5-летний мониторинг после конизации или петлевой эксцизии, выполненной по поводу HSIL, не выявил различий в группах ВИЧ-позитивных и ВИЧ-негативных пациенток [33]. Еще одна причина рецидива в том, что дооперационная кольпоскопия не всегда в состоянии визуализировать всю зону преобразования, и у части больных было эндоцервикальное распространение поражения [32].
ВИЧ-инфицированные больные хуже поддаются лучевой терапии РШМ [35]. В результате применения сочетанного (дистанционное + внутриполостное) лучевого лечения больных РШМ IIB-III стадии 4-летняя выживаемость у ВИЧ-негативных и ВИЧ-инфицированных составила 46% и 0 соответственно [47]. Поэтому есть мнение, что более предпочтительны радикальные методы лечения, например, экстирпация матки с верхней третью влагалища при дисплазии шейки матки [1].
Профилактика РШМ у ВИЧ-инфицированных больных остается важной задачей [40]. Среди женщин с ВИЧ-инфекцией в проспективном исследовании, которое включало меры по профилактике РШМ, уровень последнего не превышал такового в группе сравнения ВИЧ-негативных женщин [57].
В настоящее время возникновение и развитие РШМ ассоциируют с наличием ВПЧ высокого онкогенного риска, в частности, с генотипами 16-й, 18-й и т.д. Разумеется, что выявление штаммов этих вирусов не всегда приводит к развитию РШМ, точно так же, как и отсутствие ВПЧ не является гарантией того, что женщина не заболеет РШМ. Следовательно, вполне естественно, что взаимоотношения между макроорганизмом и вирусом сложны и подчас непредсказуемы. Тем не менее мировой медицинской наукой и практикой доказано, что носительство ВПЧ является фактором риска развития РШМ. По существу, это беспрецедентный факт в онкологии, когда выявлена этиология злокачественного заболевания.
Достижения медицинской науки предопределили разработку превентивных мер против РШМ – это иммунизация определенными штаммами ВПЧ [23, 44]. Вместе с тем мнения специалистов об эффективности профилактической иммунизации не столь однозначны. Так, ряд авторов считают, что вакцины против ВПЧ, недавно ставшие доступными, не оказывают никакого терапевтического эффекта и не могут быть полезными в предотвращении РШМ [40]. Если принять во внимание, что разнообразие типов ВПЧ, выявляемое у ВИЧ-инфицированных, значительно больше, чем только 16-й и 18-й типы [58], использование ныне существующей вакцины неэффективно. ВПЧ 16-го и 18-го типов выявляли только у 8,2% при обследовании группы ВИЧ-инфицированных беременных, у 50% обследованных диагностируют ассоциацию различных типов ВПЧ [12]. Нет никакой уверенности, что вакцина, направленная против нескольких типов ВПЧ, может защитить от всего спектра вирусов [80].
Многие исследователи утверждают, что ВААРТ способствует снижению частоты, регрессу ВПЧ-повреждений шейки матки [60], предотвращению рецидива повреждений и РШМ [21, 39]. К примеру, ингибитор протеазы ВИЧ индинавир способен воздействовать на клетки, пораженные РШМ [48]. Следовательно, применение ВААРТ может быть приоритетом в профилактике РШМ по сравнению с вакциной.
Таким образом, большинство исследователей указывают на более высокую заболеваемость РШМ у ВИЧ-инфицированных больных по сравнению с таковой в общей популяции. Многие авторы обращают внимание на большую распространенность ВПЧ у этой категории больных.
В то же время существуют противоположные публикации, утверждающие, что вероятность более частого возникновения CIN и РШМ у больных ВИЧ-инфекцией не доказана [19], уровень клеток СD4+ у пораженных ВПЧ и ВПЧ-отрицательных не различается [19] и не влияет на возникновение интраэпителиальных повреждений [61]. Уровень повреждения эпителия шейки матки не зависит от продолжительности ВИЧ-инфекции, использования ВААРТ, вирусной нагрузки [30, 49, 59]. Уровень СD4+ до ВААРТ и после нее не имеет значения для прогнозирования течения РШМ [10]. Применение ВААРТ, увеличивая выживаемость за счет сокращения случаев смерти от оппортунистических инфекций, не влияет на продолжительность жизни больных раком шейки матки [14].
Таким образом, в мировой литературе нет единого мнения об особенностях патогенеза, терапии и профилактики интраэпителиальных повреждений у ВИЧ-инфицированных больных, и, следовательно, данная проблема ждет своего разрешения.
Читайте также:


