Вирус вич нобелевская премия
Нобелевская премия по физиологии и медицине – 2008

Харальд цур Хаузен родился в 1936 году в Гельзенкирхене (Германия). Он учился в Боннском, Гамбургском и Дюссельдорфском университетах. В Дюссельдорфском университете он получил степень доктора медицины и несколько лет работал в подчиненном университету Институте медицинской микробиологии. В середине шестидесятых цур Хаузер переехал в Филадельфию (США), где вначале работал в Лаборатории вирусологии знаменитой Детской больницы, а впоследствии преподавал в Пенсильванском университете. В 1969 году он вернулся в Германию и стал профессором в Вюрцбургском университете, затем работал в университетах в Эрлангене и Нюрнберге и во Фрайбурге в Брайсгау, а с 1983 года — в Германском центре исследования рака, который он возглавлял в течение 20 лет (1983–2003).

Вирусы папилломы человека (ВПЧ) передаются от человека к человеку. Некоторые разновидности ВПЧ безвредны, некоторые вызывают образование бородавок на коже, некоторые поражают половые органы (передаваясь половым путем). В середине семидесятых Харальд цур Хаузен обнаружил, что женщины, страдающие раком шейки матки, неизменно заражены ВПЧ. В то время многие специалисты полагали, что рак шейки матки вызывается вирусом простого герпеса (Herpes simplex virus), но цур Хаузен нашел в раковых клетках не вирусы герпеса, а вирусы папилломы, и предположил, что развитие рака происходит в результате заражения именно вирусом папилломы. Впоследствии ему и его коллегам удалось подтвердить эту гипотезу и установить, что большинство случаев рака шейки матки вызваны одним из двух типов этих вирусов: ВПЧ-16 и ВПЧ-18. Зараженные такими вирусами клетки с довольно большой вероятностью рано или поздно становятся раковыми, и из них развивается злокачественная опухоль.
Электронная микрофотография вируса папилломы человека (ВПЧ). Харальд цур Хаузен открыл, что рак шейки матки обычно возникает на основе папиллом, вызываемых некоторыми разновидностями этого вируса. Прививки против вируса папилломы позволяют свести риск заболевания раком шейки матки почти к нулю. Изображение с сайта commons.wikimedia.org
В середине восьмидесятых годов были начаты исследования, благодаря которым на сегодня уже получены и запущены в производство несколько вакцин, инъекция которых позволяет, по крайней мере на несколько лет, свести к нулю риск заражения определенными типами ВПЧ (в том числе 16 и 18). Таким образом, благодаря открытию цур Хаузена были разработаны высокоэффективные средства для предотвращения рака шейки матки.
Теперь первоочередная задача — внедрение этих средств. Около 5% всех случаев заболевания раком в мире приходится на рак шейки матки, и больше двухсот тысяч женщин умирают каждый год от этой болезни. Широкое распространение вакцинации от ВПЧ позволит спасти сотни тысяч женщин. Решение Нобелевского комитета наверняка принесет пользу делу: присужденная цур Хаузену премия, вероятно, поможет привлечь внимание людей во всём мире к проблеме предотвращения рака шейки матки и будет способствовать распространению спасительной вакцинации.
Франсуаза Барре-Синусси родилась в 1947 году в Париже, там же училась и в 1974 году получила докторскую степень. Объектом ее исследований стали ретровирусы (к которым относится и ВИЧ). Она изучала эту группу вирусов в Национальном институте здравоохранения и медицинских исследований (Inserm, Institut national de la santé et de la recherche médicale) и в Пастеровском институте, где продолжает трудиться и сегодня. В 1983 году Франсуаза Барре-Синусси работала под руководством Люка Монтанье и вместе с ним принимала участие в исследовании, позволившем впервые выделить и описать вирус иммунодефицита человека, вызывающий СПИД.
Люк Монтанье родился в 1932 году в коммуне Шабри в департаменте Эндр (Франция). Он учился в Пуатье и в Париже, некоторое время работал в Париже, а затем стажировался в ведущих вирусологических лабораториях Великобритании, где изучал, в частности, механизм репликации РНК-содержащих вирусов. Вернувшись в Париж, он вначале исследовал ретровирусы в Институте Кюри, а в 1972 году был приглашен Жаком Моно (Jaques Monod), выдающимся исследователем механизмов регуляции работы генов, в новообразованное отделение вирусологии Института Пастера, где Монтанье организовал и возглавил группу вирусной онкологии, которая проводила исследования, посвященные механизмам возникновения злокачественных опухолей в результате вирусных инфекций. Сотрудниками этой группы и был впервые выделен возбудитель СПИДа. В 1993 году Люк Монтанье и генеральный директор ЮНЕСКО Федерико Майор (Federico Mayor) учредили Всемирный фонд исследования и предупреждения СПИДа. Монтанье возглавил этот фонд и по сей день руководит им.
В 1982 году группа Люка Монтанье начала исследования с целью выявить возможного возбудителя недавно описанного необычного заболевания — синдрома приобретенного иммунодефицита, характеризующегося прогрессирующим ослаблением жизненно важной иммунной системы. В 1983 году вирус был выделен (поначалу он получил другое название, но сегодня он известен как ВИЧ — вирус иммунодефицита человека). Вскоре после открытия ВИЧ в Институте Пастера его выделили и в США, в группе Роберта Галло (Robert Gallo), сотрудничавшей с группой Монтанье, из образцов, полученных от французской группы. Претензия Роберта Галло на первенство в открытии и полученный им патент на методику анализа крови на ВИЧ вызвали многолетние споры между американской и французской сторонами. Эти споры в конечном итоге разрешились признанием приоритета группы Монтанье. К сожалению, споры о приоритете отняли у исследователей много времени и немало помешали работе в области изучения ВИЧ и поиска и внедрения средств, позволяющих выявлять, предупреждать и лечить ВИЧ-инфекцию.

С 1981 года, когда был впервые описан СПИД, от этой болезни умерло больше 25 миллионов человек. Больше 33 миллионов живущих сегодня людей заражены ВИЧ, и каждый год болезнь уносит новые миллионы жизней. СПИД называли чумой XX века. Давно наступил XXI век, а число людей, зараженных ВИЧ, продолжает расти, и порядка двух миллионов зараженных, значительную долю которых составляют дети, ежегодно умирают от СПИДа. К счастью, уже разработаны методы лечения, позволяющие на десятилетия отодвинуть смерть зараженного СПИДом человека. Но к сожалению, это лечение стоит дорого, и позволить его себе могут в основном лишь достаточно состоятельные люди. При этом СПИД более всего распространен как раз на самом бедном континенте — в Африке. Кроме того, до сих пор не удалось разработать, и неизвестно, удастся ли, ни способов полного выведения ВИЧ из зараженного организма, ни вакцины, прививка которой сводила бы к нулю (или хотя бы существенно уменьшала) риск заражения СПИДом. Но продолжаются интенсивные исследования, и в будущем меры борьбы со СПИДом наверняка станут доступнее и действеннее.
Открытие группой Люка Монтанье вируса, вызывающего СПИД, было сделано вскоре после открытия самой болезни. Быстрое выявление возбудителя СПИДа очень помогло последовавшей затем разработке способов борьбы с этим заболеванием.
Премия, по традиции, будет вручена лауреатам 10 декабря, в день смерти Альфреда Нобеля, в его родном городе — Стокгольме. В прошлом году Нобелевскую премию по физиологии и медицине получили Марио Капекки (Mario R. Capecchi) из Университета Юты (США), Оливер Смитис (Oliver Smithies) из Университета Северной Каролины (США) и Мартин Эванс (Sir Martin J. Evans) из Кардиффского университета (Великобритания) за изобретение метода нокаута генов (gene knockout).

СТОКГОЛЬМ, 6 окт - РИА Новости, Людмила Божко. Лауреатами Нобелевской премии по медицине в 2008 году, чьи имена были названы в понедельник в шведском Каролинском институте, стали ученые, открывшие вирус СПИДа и доказавшие, что другой вирус является причиной одной из самых распространенных форм рака.
Половину общей суммы премии получит немецкий ученый Харальд цур Хаузен за открытие вируса папилломы человека, приводящего к раку шейки матки. Вторую половину разделят французские биологи Франсуаза Баррэ-Синусси и Люк Монтанье, ставшие лауреатами за открытие вируса иммунодефицита человека, вызывающего СПИД.
Сумма Нобелевской премии в каждой номинации составляет в этом году 10 миллионов шведских крон (1 миллион 399 тысяч долларов).
Вирус, вызывающий рак
Харальд цур Хаузен из Центра изучения раковых заболеваний в Гейдельберге еще в 1970-х годах начал исследовать роль вируса папилломы человека в развитии рака шейки матки - это вторая по распространенности среди женщин разновидность рака, поражающая ежегодно около 500 тысяч человек.
Ученый предположил, что клетки опухоли, если они содержат онкогенный вирус, должны содержать вирусную ДНК, интегрированную в геном. В 1983 году ему удалось обнаружить разновидность ДНК вируса в опухоли и, следовательно, открыть канцерогенный тип вируса HPV16. В 1984 году он клонировал HPV16 и 18, взятые у больных раком шейки матки.
Как показали результаты исследований, вирус папилломы человека был обнаружен у 99,7% женщин, у которых был подтвержден диагноз рака шейки матки.
Открытие связи между вирусом и опухолью открыло дорогу к успешному лечению - достаточно вакцины от вируса, чтобы на 95% обеспечить защиту от инфекции.
"Сегодня для предотвращения рака во многих странах мира прививается много девочек. Лично мне кажется целесообразным введение всеобщей вакцинации как для мальчиков, так и для девочек", - говорит Томас Бергстрем, профессор клинической микробиологии Сальгренской медицинской академии Гетеборга, комментируя шведской "Дагенс Нюхетер" Нобелевскую премию 2008 года.
Ученый считает, что благодаря открытию цур Хаузена у медицинских работников появилась сегодня возможность делать прививки против вируса, вызывающего рак. "Сама концепция вакцины против рака - нечто совершенно новое", - говорит он.
Открытие чумы 20-го века
Вторая половина премии уйдет французским коллегам цур Хаузена - вирусологу из парижского института Пастера Франсуазе Баррэ-Синусси и сотруднику Всемирного фонда исследований и профилактики СПИДа Люку Монтанье, которые в 1983 году впервые выделили вирус иммунодефицита человека, вызывающий СПИД.
Однако примерно тогда же об открытии вируса заявили американские ученые, что вызвало споры о приоритете.
Баррэ-Синусси и Монтанье идентифицировали вирус человеческого иммунодефицита в лимфоцитах пациентов с увеличенными лимфоузлами на ранней стадии СПИДа и в крови пациентов на поздних стадиях болезни.
Они охарактеризовали этот ретровирус как первый известный лентивирус человека, основываясь на его морфологических, биохимических и иммунологических свойствах. Открытие было одной из предпосылок для нынешнего понимания биологии болезни, вызвавшей пандемию, поражающую миллионы людей ежегодно, и антиретровирусной терапии.
Профессор Каролинского института и исследователь в области ВИЧ Франческа Чиоди, комментируя награду французских исследователей, говорит, что награда этого года поможет по-новому обратить внимание общественности на исследования в сфере изучения ВИЧ.
"Премия этого года очень важна для всего мира, и хорошо, что среди лауреатов есть женщина", - говорит шведский исследователь.
Магнус Гисслен, доцент Сальгренской медицинской академии Гетеборга, сказал газете, что открытие французских коллег открыло много возможностей для исследований последующего поколения ученых.
"К сожалению, у нас нет пока вакцины против ВИЧ, но за последние 15-20 лет научные исследования привели к тому, что появились лекарства, тормозящие ВИЧ. Из болезни со смертельным исходом она превратилась сегодня в хроническое заболевание", - говорит Гисслен.
Церемония вручения премии пройдет в Стокгольме и Осло 10 декабря, в день кончины ее основателя - Альфреда Нобеля (1833-1896) - шведского изобретателя, промышленника, лингвиста, философа и гуманиста.
06 октября 2008
- 1973
- 1,6
- 0
- 0
Вирусы — неотъемлемый компонент живой природы, однако бороться с ними — дело благородное. По крайней мере, в случае ВПЧ и ВИЧ.
6 октября 2008 года Нобелевский комитет присудил Нобелевскую премию в области физиологии и медицины Гарольду цур Хаузену за открытие того, что вирус папилломы может вызывать рак шейки матки, и Франсуазе Барре-Синусси и Люку Монтанье за открытие вируса иммунодефицита человека.
Лауреаты
Гарольд цур Хаузен (Harald zur Hausen), родился в 1936 г. в Германии, на настоящий момент гражданин Германии, доктор медицины в Университете Дюссельдорфа. Заслуженный профессор и бывший заведующий и директор по науке Немецкого ракового центра в Гейдельберге.
Франсуаза Барре-Синусси (Françoise Barré-Sinoussi), родилась в 1947 г. во Франции, на настоящий момент гражданка Франции, кандидат наук (PhD) в области вирусологии. Профессор и директор подразделения ретровирусных инфекций Института Пастера в Париже. Кстати, Франсуаза стала восьмой женщиной в истории, удостоенной Нобелевской премии.
Люк Монтанье (Luc Montagnier), родился в 1932 г. во Франции, на настоящий момент гражданин Франции, кандидат наук (PhD) в области вирусологии. Почётный профессор и директор Мирового сообщества по изучению и предотвращению СПИДа в Париже.
Открытие вирусной природы рака шейки матки
Вопреки существовавшим в 1970-х представлениям о природе раковых заболеваний, Гарольд цур Хаузен (Harald zur Hausen) постулировал, что развитие рака шейки матки (по крайней мере, в некоторых случаях) связано с папилломавирусом человека (ВПЧ). Он предположил, что если опухолевые клетки содержат онкогенный вирус, то их геном должен включать и вирусную ДНК. Следовательно, активность вирусных генов, инициирующих злокачественный рост, может быть обнаружена при помощи специальных ДНК-тестов, ориентированных на вирусный генетический материал. Цур Хаузен более десяти лет продвигал свою идею и занимался поиском различных типов ВПЧ-инфекции, что затруднялось, в частности, тем обстоятельством, что вирусная ДНК лишь частично внедрялась в хромосомы хозяина (человека). В 1983 году ему удалось обнаружить ДНК папилломавируса в биопсии рака шейки матки, и это событие можно считать открытием онкогенного вируса ВПЧ-16. Годом позже он клонировал ДНК ВПЧ-16 и ВПЧ-18 в пациентах, больных раком шейки матки. Эти типы вируса обнаруживаются примерно в 70% случаях рака шейки матки.
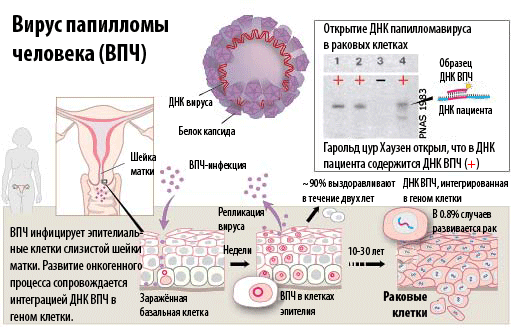
Рисунок 1. Вирус папилломы человека (ВПЧ). ВПЧ содержит двуцепочечную кольцевую молекулу ДНК, заключённую в капсид. Всего известно >100 видов ВПЧ. ВПЧ-16 и ВПЧ-18 являются причиной 70% случаев рака шейки матки.
Значение исследований вируса папилломы
Ущерб, наносимый папилломавирусом здоровью людей во всём мире, весьма значителен. Более 5% всех зарегистрированных случаев рака вызывается именно вирусами этой группы. Вирусы папилломы — одна из наиболее часто встречающихся инфекций, передающихся половым путём. Из более чем 100 известных разновидностей ВПЧ, около сорока инфицируют мочеполовую систему, и 15 из них создают повышенный риск заболевания раком шейки матки (но ВПЧ связывают и с другими разновидностями онкогенных процессов). Папилломавирус находят у 99,7% женщин с гистологически подтверждённым диагнозом рака шейки матки — что составляет около 500000 женщин в год.
Исследования Гарольда цур Хаузена в области ВПЧ-инфекции легли в основу понимания механизмов канцерогенеза, индуцированного вирусом папилломы. Впоследствии были разработаны вакцины, которые более чем в 95% случаев позволяют предотвратить инфекцию вирусами ВПЧ-16 и ВПЧ-18. Это лечение позволит сократить объем хирургического вмешательства и в целом снизить угрозу, представляемую раком шейки матки.
Открытие ВИЧа
В 1981-м появились медицинские описания новой формы синдрома иммунодефицита. Франсуаза Барре-Синусси (Françoise Barré-Sinoussi) и Люк Монтанье (Luc Montagnier) выделили и исследовали культуры лимфатических клеток людей, которым был поставлен диагноз начальной формы приобретённого иммунодефицита. В этих культурах им удалось обнаружить следы работы фермента обратной транскриптазы — прямого свидетельства инфекции ретровирусом и его репликации в заражённых клетках. Кроме того, они обнаружили непосредственно ретровирусные частицы, отпочковывающиеся от заражённых клеток. Выделенный вирус — получивший название вируса иммунодефицита человека (ВИЧ) — заражал и убивал лимфоциты как здоровых, так и больных людей, а также реагировал с антителами инфицированных пациентов. По сравнению с уже известными на тот момент канцерогенными вирусами, ВИЧ не вызывал неконтролируемой пролиферации клеток; вместо этого он использовал активацию клеточного метаболизма Т-лимфоцитов для собственного размножения. Этот факт позволил объяснить причину приобретённого иммунодефицита, поскольку Т-клетки выполняют очень важную роль в иммунной защите. К 1984 году Барре-Синусси и Монтанье уже имели несколько образцов нового человеческого ретровируса (который они отнесли к подгруппе лентивирусов), полученных из пациентов, заразившихся половым путём, при переливании крови или больных от рождения (в случае, когда инфекция передаётся от матери к ребёнку). Значение проделанной ими работы трудно переоценить, учитывая почти повсеместное распространение ВИЧа и эпидемию СПИДа, охватившую почти 1% населения Земли.
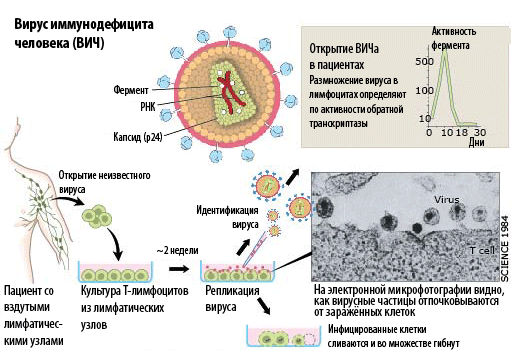
Значение исследований вируса иммунодефицита
ВИЧ стал причиной глобальной пандемии. Никогда прежде медицина и наука не реагировали на угрозу так же быстро, идентифицируя причину нового заболевания и предлагая методики лечения. Пусть не совершенные, на сегодня они обеспечивают практически такую же среднюю продолжительность жизни пациентов, как и у здоровых людей. Многочисленные разработки в области вирусологии этой инфекции всё-таки позволяют надеяться, что однажды человечество сможет полностью победить вирус иммунодефицита.
Первооткрыватели ВИЧ и папилломавируса удостоились Нобелевской премии по физиологии и медицине

С понедельника, шестого октября, началась Нобелевская неделя. В ближайшие дни будут названы имена авторов открытий и исследований, которые оказали существенное влияние на развитие человечества. И с важностью открытий, за которые была присуждена первая Нобелевская премия 2008 года, – по физиологии и медицине – трудно спорить. Лауреатами самой престижной научной награды стали открыватели вируса иммунодефицита человека (ВИЧ) и папилломавируса, который вызывает рак шейки матки.
Главное слово XX века
Сейчас трудно найти человека, который бы не слышал о ВИЧ (вирусе иммунодефицита человека) и СПИДе (синдроме приобретенного иммунодефицита). Но 27 лет назад врачи были озадачены увеличением числа пациентов с редкими заболеваниями, такими как саркома Капоши. Этот вид злокачественной опухоли, локализующийся в дерме (коже), до 1980-х годов встречался с частотой один-два случая на десять миллионов, причем все пациенты были старше 60 лет. Большинству новых заболевших еще не исполнилось 30 лет.
Кроме учащения случаев саркомы Капоши в больницы Европы и США стали поступать пациенты со злокачественной формой пневмоцистной пневмонии. Это заболевание вызывается грибком Pneumocystis jirovecii и крайне редко встречается у людей с нормальным иммунитетом.
У необычных пациентов встречались другие общие заболевания и симптомы, например, увеличенные лимфоузлы. Кроме того, их объединял еще один признак: большинство страдавших редкими заболеваниями были гомосексуалистами. Стандартное лечение не оказывало заметного эффекта на состояние пациентов, число которых росло. Кроме мужчин нетрадиционной ориентации, симптомы проявлялись у людей, страдающих гемофилией, наркоманов и пациентов после трансплантации органов. Через некоторое время врачи осознали, что все эти, на первый взгляд, несвязанные вещи определяются одной и той же причиной, но выявить ее не удавалось.
Ретровирусы – это класс вирусов, которые в ходе размножения "записывают" свою генетическую информацию в геном клетки-хозяина. То есть, зараженная клетка несет в себе вирус даже в том случае, если в данный момент он неактивен.
В 1982 году к поискам присоединилась группа исследователей из Института Пастера, которую возглавлял Люк Монтанье (Luc Montagnier). Одним из сотрудников Монтанье была Франсуаза Барр-Синусси (Francoise Barre-Sinoussi). К тому моменту, когда будущие нобелевские лауреаты занялись решением страшной загадки (пациентам не помогало лечение, и они быстро умирали), один из ученых, также пытавшийся понять причину нового симптомокомплекса, Вилли Розенбаум (Willy Rozenbaum) из клиники Биша в Париже, предположил, что все симптомы вызываются ретровирусом.
Розенбаум послал Монтанье образец ткани лимфоузла одного из пациентов с характерными для неизвестного заболевания симптомами. Монтанье и Барр-Синусси изолировали клетки лимфоузла и вырастили их культуру. Исследователи обнаружили в клетках активность фермента, который необходим ретровирусам для того, чтобы "вписать" свой геном в ДНК хозяина. Генетическая информация ретровирусов находится в форме РНК, а в ядрах зараженных клетки находится ДНК. Вирусный фермент обратная транскриптаза переводит геном вируса с "языка РНК" на "язык ДНК".
Обнаружение активности обратной транскриптазы само по себе является доказательством того, что в клетках "хозяйничает" ретровирус. Однако Монтанье и Барр-Синусси продолжили работу и обнаружили вирусные частицы, отпочковывающиеся от зараженных клеток. Исследователи добавили эти частицы к здоровым и уже зараженным клеткам и убедились, что вирусы убивают их.
К 1984 году Монтанье и Барр-Синусси удалось выделись аналогичные вирусные частицы из клеток людей, у которых симптомы появились после незащищенного секса, из клеток гемофиликов, а также из клеток пациентов с пересаженными органами и детей, родившихся от заболевших матерей. Вскоре нескольким группам удалось показать связь между наличием вируса и проявлением симптомокомплекса, известного как СПИД (хотя долгое время – и даже сейчас – некоторые исследователи считают, что этот факт не доказан).
Монтанье и Барр-Синусси назвали новый вирус вирусом, ассоциированным с лимфоаденопатией. Однако это название не прижилось. Спустя год американский исследователь Роберт Галло (Robert Gallo) подтвердил открытие команды Монтанье, но назвал выделенный вирус Т-лимфотропным вирусом человека второго типа. Еще через год, в 1986 году, научное сообщество постановило дать новому вирусу то имя, которое мы знаем сегодня, - вирус иммунодефицита человека. Выбор такого названия был определен основным симптомом, который "тянет" за собой остальные – ослаблением иммунной системы.
Доказательство того, что страшное заболевание вызывает ретровирус, и разработка технологии его выделения позволили ученым всего мира начать более "прицельное" изучение "чумы XX века". До тех пор, пока не стало ясно, что именно вызывает симптомы, лечить болезнь было невозможно. После того, как убийца был идентифицирован, исследования пошли значительно быстрее. В 1985 году была получена полная последовательность РНК вируса. Сейчас ученые знают очень многое о жизненном цикле ВИЧ (фактически, он является наиболее изученным из всех известных вирусов). Современные лекарства воздействуют на разные стадии процесса заражения и размножения вируса и позволяют пациентам долгое время вести нормальный образ жизни.
Почему исследователи решили, что Нобелевской премии достойны именно работы по открытию вируса иммунодефицита, понятно. Возникает вопрос, почему в число лауреатов не попал Роберт Галло, чьи работы во многом способствовали доказательству того, что ВИЧ является инфекционным агентом, вызывающим СПИД. Команды Галло и Монтанье опубликовали свои работы приблизительно в одно и то же время, однако в отношении некоторых экспериментов американского биохимика возникли сомнения (в частности, Галло обвиняли в использовании образцов ВИЧ из лаборатории Монтанье). В конце концов научный мир пришел к негласному заключению, что Монтанье и Барр-Синусси первыми выделили ВИЧ, а Галло первым показал его связь со СПИДом. Однако в официальном пресс-релизе, посвященном Нобелевской премии по физиологии и медицине 2008 года, имя Галло ни разу не упоминается.
Вторую половину Нобелевской премии (а это целых 650 тысяч долларов) получит немецкий вирусолог Харальд цур Хаузен (Harald zur Hausen). Можно сказать, что он получил эту награду за то, что "восстал против существовавшей догмы" (цитата из официального пресс-релиза). Еще в 1970-х годах цур Хаузен предположил, что вирус папилломы человека вызывает рак шейки матки, который занимает второе место по частоте встречаемости у женщин после рака груди. До этого времени ученые считали, что рак не является вирусным заболеванием. Немецкий вирусолог также заключил, что ДНК этого ретровируса может присутствовать в опухолевых клетках.
В течение десяти лет цур Хаузен пытался найти вирусную ДНК в раковых клетках. Это была совсем не простая задача для того времени, особенно если учесть, что в геном клетки встраивается не вся ДНК вируса. В 1983 году ученый обнаружил не встречавшуюся раньше ДНК папилломавируса в клетках рака шейки матки. Это ДНК принадлежала онкогенному штамму папилломавируса – HPV16. В 1984 году цур Хаузен выделил и клонировал HPV16 и еще один штамм - HPV18. Вместе эти два штамма "ответственны" за 70 процентов всех случаев рака шейки матки.
Работы цур Хаузена позволили лучше понять природу и механизмы распространения вируса папилломы человека, который вызывает около пяти процентов всех случаев рака. Благодаря его открытиям ученые смогли разработать лекарства, помогающие значительно снизить смертность и необходимость хирургического вмешательства при заболеваниях раком шейки матки.
В надежде на продолжение
В 2008 году Нобелевская премия была присуждена за открытия, сделанные четверть века назад. Как это не печально, но такой срок является обычным для этой премии. За это время ученым удалось значительно продвинуться в разработке лекарств против рака и СПИДа, однако так и не удалось полностью победить эти болезни. Возможно, научный мир так долго тянул с награждением первооткрывателей ВИЧ и папилломавируса в надежде, что предоставится возможность наградить тех, кто разработает панацею от этих напастей. Остается надеяться, что нынешние лауреаты смогут когда-нибудь поздравить ученых, закончивших то, что начали они.

Харальд цур Хаузен родился в 1936 году в Гельзенкирхене (Германия). Он учился в Боннском, Гамбургском и Дюссельдорфском университетах. В Дюссельдорфском университете он получил степень доктора медицины и несколько лет работал в подчиненном университету Институте медицинской микробиологии. В середине шестидесятых цур Хаузер переехал в Филадельфию (США), где вначале работал в Лаборатории вирусологии знаменитой Детской больницы, а впоследствии преподавал в Пенсильванском университете. В 1969 году он вернулся в Германию и стал профессором в Вюрцбургском университете, затем работал в университетах в Эрлангене и Нюрнберге и во Фрайбурге в Брайсгау, а с 1983 года — в Германском центре исследования рака, который он возглавлял в течение 20 лет (1983–2003).
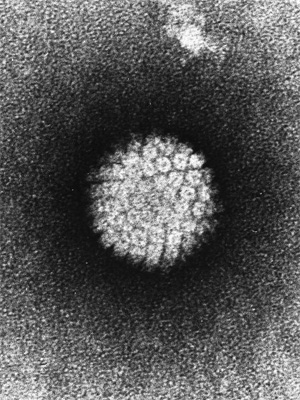
Вирусы папилломы человека (ВПЧ) передаются от человека к человеку. Некоторые разновидности ВПЧ безвредны, некоторые вызывают образование бородавок на коже, некоторые поражают половые органы (передаваясь половым путем). В середине семидесятых Харальд цур Хаузен обнаружил, что женщины, страдающие раком шейки матки, неизменно заражены ВПЧ. В то время многие специалисты полагали, что рак шейки матки вызывается вирусом простого герпеса (Herpes simplex virus), но цур Хаузен нашел в раковых клетках не вирусы герпеса, а вирусы папилломы, и предположил, что развитие рака происходит в результате заражения именно вирусом папилломы. Впоследствии ему и его коллегам удалось подтвердить эту гипотезу и установить, что большинство случаев рака шейки матки вызваны одним из двух типов этих вирусов: ВПЧ-16 и ВПЧ-18. Зараженные такими вирусами клетки с довольно большой вероятностью рано или поздно становятся раковыми, и из них развивается злокачественная опухоль.
В середине восьмидесятых годов были начаты исследования, благодаря которым на сегодня уже получены и запущены в производство несколько вакцин, инъекция которых позволяет, по крайней мере на несколько лет, свести к нулю риск заражения определенными типами ВПЧ (в том числе 16 и 18). Таким образом, благодаря открытию цур Хаузена были разработаны высокоэффективные средства для предотвращения рака шейки матки.
Теперь первоочередная задача — внедрение этих средств. Около 5% всех случаев заболевания раком в мире приходится на рак шейки матки, и больше двухсот тысяч женщин умирают каждый год от этой болезни. Широкое распространение вакцинации от ВПЧ позволит спасти сотни тысяч женщин. Решение Нобелевского комитета наверняка принесет пользу делу: присужденная цур Хаузену премия, вероятно, поможет привлечь внимание людей во всём мире к проблеме предотвращения рака шейки матки и будет способствовать распространению спасительной вакцинации.
Люк Монтанье родился в 1932 году в коммуне Шабри в департаменте Эндр (Франция). Он учился в Пуатье и в Париже, некоторое время работал в Париже, а затем стажировался в ведущих вирусологических лабораториях Великобритании, где изучал, в частности, механизм репликации РНК-содержащих вирусов. Вернувшись в Париж, он вначале исследовал ретровирусы в Институте Кюри, а в 1972 году был приглашен Жаком Моно (Jaques Monod), выдающимся исследователем механизмов регуляции работы генов, в новообразованное отделение вирусологии Института Пастера, где Монтанье организовал и возглавил группу вирусной онкологии, которая проводила исследования, посвященные механизмам возникновения злокачественных опухолей в результате вирусных инфекций. Сотрудниками этой группы и был впервые выделен возбудитель СПИДа. В 1993 году Люк Монтанье и генеральный директор ЮНЕСКО Федерико Майор (Federico Mayor) учредили Всемирный фонд исследования и предупреждения СПИДа. Монтанье возглавил этот фонд и по сей день руководит им.
В 1982 году группа Люка Монтанье начала исследования с целью выявить возможного возбудителя недавно описанного необычного заболевания — синдрома приобретенного иммунодефицита, характеризующегося прогрессирующим ослаблением жизненно важной иммунной системы. В 1983 году вирус был выделен (поначалу он получил другое название, но сегодня он известен как ВИЧ — вирус иммунодефицита человека). Вскоре после открытия ВИЧ в Институте Пастера его выделили и в США, в группе Роберта Галло (Robert Gallo), сотрудничавшей с группой Монтанье, из образцов, полученных от французской группы. Претензия Роберта Галло на первенство в открытии и полученный им патент на методику анализа крови на ВИЧ вызвали многолетние споры между американской и французской сторонами. Эти споры в конечном итоге разрешились признанием приоритета группы Монтанье. К сожалению, споры о приоритете отняли у исследователей много времени и немало помешали работе в области изучения ВИЧ и поиска и внедрения средств, позволяющих выявлять, предупреждать и лечить ВИЧ-инфекцию.

С 1981 года, когда был впервые описан СПИД, от этой болезни умерло больше 25 миллионов человек. Больше 33 миллионов живущих сегодня людей заражены ВИЧ, и каждый год болезнь уносит новые миллионы жизней. СПИД называли чумой XX века. Давно наступил XXI век, а число людей, зараженных ВИЧ, продолжает расти, и порядка двух миллионов зараженных, значительную долю которых составляют дети, ежегодно умирают от СПИДа. К счастью, уже разработаны методы лечения, позволяющие на десятилетия отодвинуть смерть зараженного СПИДом человека. Но к сожалению, это лечение стоит дорого, и позволить его себе могут в основном лишь достаточно состоятельные люди. При этом СПИД более всего распространен как раз на самом бедном континенте — в Африке. Кроме того, до сих пор не удалось разработать, и неизвестно, удастся ли, ни способов полного выведения ВИЧ из зараженного организма, ни вакцины, прививка которой сводила бы к нулю (или хотя бы существенно уменьшала) риск заражения СПИДом. Но продолжаются интенсивные исследования, и в будущем меры борьбы со СПИДом наверняка станут доступнее и действеннее.
Открытие группой Люка Монтанье вируса, вызывающего СПИД, было сделано вскоре после открытия самой болезни. Быстрое выявление возбудителя СПИДа очень помогло последовавшей затем разработке способов борьбы с этим заболеванием.
Премия, по традиции, будет вручена лауреатам 10 декабря, в день смерти Альфреда Нобеля, в его родном городе — Стокгольме. В прошлом году Нобелевскую премию по физиологии и медицине получили Марио Капекки (Mario R. Capecchi) из Университета Юты (США), Оливер Смитис (Oliver Smithies) из Университета Северной Каролины (США) и Мартин Эванс (Sir Martin J. Evans) из Кардиффского университета (Великобритания) за изобретение метода нокаута генов (gene knockout).
Читайте также:


