Бактериофаг против сальмонеллеза энтеритидис кур
Бактериофаг сальмонеллезный групп A, B, C, D, E: инструкция по применению и отзывы
Латинское название: Bacteriophagum Salmonellae gr. ABCDE
Действующее вещество: бактериофаг сальмонеллезный (Bacteriophagum Salmonellae)
Производитель: Микроген НПО, АО (Россия)
Актуализация описания и фото: 24.01.2019
Бактериофаг сальмонеллезный – иммуностимулирующее средство со специфическим антибактериальным действием в отношении сальмонелл групп A, B, C, D и E.
Форма выпуска и состав
- раствор для приема внутрь и местного применения: прозрачная жидкость желтого цвета различной интенсивности окрашивания (по 20 мл во флаконах, в картонной пачке 4 или 8 флаконов; по 100 мл во флаконах, в картонной пачке 1 флакон);
- таблетки с кислотоустойчивым покрытием: круглые, двояковыпуклые, Ø – 7 мм, светло-серого или светло-бежевого цвета различной интенсивности окрашивания, со светлыми включениями, допускается мраморность (по 50 шт. в стеклянных флаконах, в картонной пачке 10 флаконов).
В каждой пачке также содержится инструкция по применению Бактериофага сальмонеллезного.
Состав раствора в 1 флаконе:
- активное вещество: бактериофаг сальмонеллезный групп A, B, C, D, E жидкий – 20 или 100 мл;
- вспомогательный компонент (консервант): хинозол.
Состав 1 таблетки:
- активное вещество: бактериофаг сальмонеллезный групп A, B, C, D, E – 72 мг;
- вспомогательные компоненты: кальция стеарат, декстрозы моногидрат, кальция глюконат моногидрат, молоко обезжиренное (сухой остаток), тальк очищенный, пектин.
Фармакологические свойства
Бактериофаг сальмонеллезный групп A, B, C, D, E – микробиологическое средство, вызывающее лизис следующих сальмонелл:
- группа A – Salmonella paratyphi A;
- группа B – Salmonella Heidelberg, Salmonella paratyphi В, Salmonella typhimurium;
- группа C – Salmonella oranienburg, Salmonella choleraesuis, Salmonella infantis, Salmonella newport;
- группа D – Salmonella enteritidis, Salmonella dublin;
- группа E – Salmonella newlands, Salmonella analum.
Показания к применению
Бактериофаг сальмонеллезный предназначен для профилактики и лечения заболеваний, и бактерионосительства, вызванных сальмонеллами групп A, B, C, D, E.
Противопоказания
Ограничений к применению жидкого бактериофага в виде раствора нет.
В форме таблеток препарат противопоказан детям до 1 года.
Бактериофаг сальмонеллезный, инструкция по применению: способ и дозировка
Бактериофаг сальмонеллезный в форме раствора предназначен для перорального и ректального (в виде клизм после очищения кишечника) применения. Перед использованием флакон следует тщательно взбалтывать.
Внутрь препарат принимают за 1 ч до приема пищи 3 раза в сутки с первого дня выявления заболевания. Курс лечения составляет 7–10 дней.
При заболеваниях, сопровождающихся слабовыраженным колитическим синдромом, и в период выздоровления рекомендуется сочетать пероральный прием 2 раза в сутки с 1 ректальным применением.
Рекомендуемые разовые дозировки для перорального применения Бактериофага сальмонеллезного в зависимости от возраста пациента:
- 0–6 месяцев – 5 мл;
- 6–12 месяцев – 10–15 мл;
- 1–3 года – 15–20 мл;
- 3–8 лет – 20–30 мл;
- от 8 лет и старше – 30–40 мл.
Рекомендуемые разовые дозировки для ректального применения Бактериофага сальмонеллезного в зависимости от возраста пациента:
- 0–6 месяцев – 10 мл;
- 6–12 месяцев – 20 мл;
- 1–3 года – 20–30 мл;
- 3–8 лет – 30–40 мл;
- от 8 лет и старше – 50–60 мл.
В профилактических целях бактериофаг применяют для предупреждения бактерионосительства и развития внутрибольничной инфекции, а также для предупреждения инфицирования во время групповых заболеваний в семьях и организованных коллективах. В этом случае по 1 возрастной дозе следует принимать 1 раз в сутки. Продолжительность курса определяется условиями эпидемической ситуации.
Бактериофаг сальмонеллезный в форме таблеток следует принимать внутрь, за 1 ч до приема пищи 3 раза в сутки, с первого дня заболевания. Курс лечения – 7–10 дней.
При заболеваниях, сопровождающихся слабовыраженным колитическим синдромом, и в период выздоровления рекомендуется сочетать пероральный прием 2 раза в сутки с 1 ректальным применением жидкого бактериофага в виде клизм после опорожнения кишечника.
Рекомендуемые разовые дозировки Бактериофага сальмонеллезного в зависимости от возраста пациента:
- 1–3 года – 1 таблетка;
- 3–8 лет – 1–2 таблетки;
- от 8 лет и старше – 2–3 таблетки.
В профилактических целях бактериофаг принимают по 1 возрастной дозе 1 раз в сутки. Продолжительность курса определяется условиями эпидемической ситуации.
Побочные действия
До настоящего времени развитие побочных эффектов на фоне терапии препаратом выявлено не было.
Передозировка
Не поступали сообщения о случаях передозировки бактериофага.
Особые указания
Для проведения эффективной фаготерапии важно предварительное определение чувствительности возбудителя к препарату и раннее начало лечения.
Нельзя использовать жидкий бактериофаг в случае помутнения раствора.
Негативное влияние на психические и моторные способности человека не выявлено.
Применение при беременности и лактации
Бактериофаг сальмонеллезный может применяться во время беременности и лактации по соответствующим показаниям и по назначению врача.
Применение в детском возрасте
Раствор для приема внутрь и местного применения не имеет возрастных ограничений к применению. В форме таблеток препарат противопоказано использовать для лечения детей до 1 года.
Лекарственное взаимодействие
Бактериофаг сальмонеллезный не ограничивает применение других лекарственных средств, включая антибиотики.
Аналоги
Информация об аналогах Бактериофага сальмонеллезного отсутствует.
Сроки и условия хранения
Обе лекарственные формы препарата следует хранить при температуре 2–8 °С в защищенном от света, недоступном для детей, сухом месте.
Срок годности раствора и таблеток – 2 года.
Условия отпуска из аптек
Отпускается без рецепта.
Отзывы о Бактериофаге сальмонеллезном
Согласно отзывам, Бактериофаг сальмонеллезный – единственное средство, позволяющее вылечить заболевания, вызванные Salmonella серотипов A, B, C, D, E. Как указывают многие, наибольшая эффективность отмечается при сочетании перорального и ректального способов применения препарата. К дополнительным преимуществам относят возможность использования раствора у детей с рождения, а также хорошую переносимость бактериофага.
Недостатком считают высокую стоимость, однако, по мнению большинства, полное излечивание после одного курса терапии нивелирует этот негативный момент.
Цена на Бактериофаг сальмонеллезный в аптеках
В зависимости от региона продажи и аптечной сети цена на Бактериофаг сальмонеллезный за 1 флакон объемом 100 мл может составлять 586–845 руб.

Образование: Ростовский государственный медицинский университет, специальность "Лечебное дело".
Информация о препарате является обобщенной, предоставляется в ознакомительных целях и не заменяет официальную инструкцию. Самолечение опасно для здоровья!
При регулярном посещении солярия шанс заболеть раком кожи увеличивается на 60%.
Человек, принимающий антидепрессанты, в большинстве случаев снова будет страдать депрессией. Если же человек справился с подавленностью своими силами, он имеет все шансы навсегда забыть про это состояние.
В четырех дольках темного шоколада содержится порядка двухсот калорий. Так что если не хотите поправиться, лучше не есть больше двух долек в сутки.
Когда влюбленные целуются, каждый из них теряет 6,4 ккалорий в минуту, но при этом они обмениваются почти 300 видами различных бактерий.
По статистике, по понедельникам риск получения травм спины увеличивается на 25%, а риск сердечного приступа – на 33%. Будьте осторожны.
Существуют очень любопытные медицинские синдромы, например, навязчивое заглатывание предметов. В желудке одной пациентки, страдающей от этой мании, было обнаружено 2500 инородных предметов.
Люди, которые привыкли регулярно завтракать, гораздо реже страдают ожирением.
Образованный человек меньше подвержен заболеваниям мозга. Интеллектуальная активность способствует образованию дополнительной ткани, компенсирующей заболевшую.
В Великобритании есть закон, согласно которому хирург может отказаться делать пациенту операцию, если он курит или имеет избыточный вес. Человек должен отказаться от вредных привычек, и тогда, возможно, ему не потребуется оперативное вмешательство.
Самая высокая температура тела была зафиксирована у Уилли Джонса (США), который поступил в больницу с температурой 46,5°C.
Самое редкое заболевание – болезнь Куру. Болеют ей только представители племени фор в Новой Гвинее. Больной умирает от смеха. Считается, что причиной возникновения болезни является поедание человеческого мозга.
Даже если сердце человека не бьется, то он все равно может жить в течение долгого промежутка времени, что и продемонстрировал нам норвежский рыбак Ян Ревсдал. Его "мотор" остановился на 4 часа после того как рыбак заблудился и заснул в снегу.
Большинство женщин способно получать больше удовольствия от созерцания своего красивого тела в зеркале, чем от секса. Так что, женщины, стремитесь к стройности.
Согласно мнению многих ученых, витаминные комплексы практически бесполезны для человека.
Человеческие кости крепче бетона в четыре раза.
Всё большее количество пациентов из всего мира отправляются на лечение в Турцию. Сюда едут как из развитых государств, так и из стран с низким уровнем развития .
Использование: ветеринарная биотехнология, препарат для лечения и специфической профилактики сальмонеллеза кур. Сущность изобретения: препарат состоит из двух частей - бактериофага S.enteritidis с широким спектром литического действия, представляющего собой суспензию частиц штамма фага F-6 в культуральной среде, консервированной хинозолом, и вакцины, содержащей суспензию клеток фагоустойчивого аттенуированного штамма S.enteritidis ВГНКИ N 204 - R и сахарозо-желатиновый стабилизатор. Препарат способен предохранять 1-10-дневных цыплят от заболевания сальмоннелезом, обладает лечебным эффектом, санирует сальмонеллоносителей и создает иммунитет высокой напряженности. 2 с.п. ф-лы, 2 табл.
Изобретение относится к ветеринарной биотехнологи. Целью изобретения является создание препарата для эффективного лечения и специфической профилактики сальмонеллеза кур.
В последние годы наблюдается рост заболеваемости кур сальмонеллезом, вызываемым S. enteritidis. Возбудитель заболевания хорошо адаптировался к организму кур. Сальмонеллез энтеритидис вызывает значительную гибель цыплят и сопровождается длительным сальмонеллоносительством у взрослой птицы. Инфицированные S. enteritidis продукты птицеводства являются основным источником возбудителя токсикоинфекций человека.
Широкая распространенность S. enteritidis среди кур, значительный материальный ущерб, причиняемый птицеводству, опасность для человека, отсутствие эффективных лечебных препаратов, делают необходимым изыскание средств лечения и специфической профилактики этого заболевания.
Известна инактивированная вакцина против сальмонеллеза энтеритидис кур [1].
Однако эта вакцина низкоиммуногенна, особенно при интраперитонеальном способе введения.
Известна живая вакцина из термочувствительного мутанта S. enteritidis, не способного расти при 37 о С, но эффективно размножающегося при 25 о С [2]. Вакцина находится на стадии разработки и применялась на ограниченном поголовье птицы.
Использование вакцин в качестве средства борьбы с сальмонеллезом энтеритидис кур малоэффективно по следующим причинам.
Активный иммунитет у иммунизированных цыплят формируется лишь на 7-10-й день после вакцинации. Известно, что массовая гибель цыплят (достигающая 10-15% поголовья) приходится из цыплят до 10-дневного возраста, вследствие этого вакцинация не может предотвратить ущерб от заболевания в этом возрасте.
Вакцины не обладают лечебным эффектом. Вакцинация не способна ликвидировать сальмонеллоносительство у инфицированной птицы. Инфицированные продукты птицеводства являются источником возбудителя токсикоинфекций человека, что определяет весомую эпидемиологическую значимость сальмонеллеза энтеритидис.
Целью изобретения является создание эффективного препарата для лечения и специфической профилактики сальмонеллеза кур, а также разработка рационального способа лечения и профилактики заболевания.
Предлагаемый препарат в сравнении с имеющимися аналогами обладает следующими существенными отличиями: способен предохранять 1-10-дневных цыплят от заболевания сальмонеллезом; обладает лечебным эффектом и санирует сальмонеллоносителей.
Цель достигается созданием препарата, содержащего аттенуированный штамм. S. enteritidis и стабилизатор, отличающегося тем, что он дополнительно содержит суспензию фаговых частиц штамма Phagum enteritidis ВГНКИ N F-6 с концентрацией 1-10 млрд. БОЕ/см 3 в культуральной среде, консервированной хинозолом, из аттенуированных штаммов он содержит фагоустойчивый штамм S. enteritidis ВГНКИ N 204-R, а в качестве стабилизатора сахарозу и желатин, при следующем соотношении компонентов, об.%: Суспензия частиц штамма фага ВГНКИ N F-6 с концентрацией 1-10 млрд. БОЕ/см 3 в культуральной среде 45,0-50,0 Хинозол 0,005-0,01 Суспензия клеток фагоустойчивого штамма S. enteritidis ВГНКИ N 204-R с концентрацией 150-250 млрд. БОЕ/см 3 22,5-27,5 Сахароза 2,5-3,7 Желатин 0,75-1,0 Дистиллированная вода Остальное Способ лечения и профилактики сальмонеллеза кур предусматривает введение в организм цыплят 1-3-дневного возраста препарата, содержащего смесь суспензий фаговых частиц штамма фага ВГНКИ NF-6 и клеток фагоустойчивого штамма S. enteridis ВГНКИ N 204-R, консервант и стабилизатор, при следующем соотношении компонентов, об.%: Суспензия частиц штамма фага ВГНКИ N F-6 с концентрацией 1-10 млрд. БОЕ/см 3 45,0-50,0 Хинозол 0,005-0,01 Суспензия клеток фагоустойчивого штам- ма S. enteritidis ВГНКИ N 204-R с концентрацией 150-250 млрд. кл/см 3 22,5-27,5 Сахароза 2,5-3,7 Желатин 0,75-1,0 Дистиллированная вода Остальное из расчета по 100-200 млн. фаговых частиц и 0,5-1 млрд. клеток вакцинного штамма на одного цыпленка перорально, двукратно, с интервалом в 3 дня.
Штамм Phagum enteritidis F-6 депонирован в коллекции микроорганизмов Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов, имеет регистрационный N 6.
Штамм бактериофага обладает следующими свойствами.
Морфология вириона. Вирион бактериофага обладает бинальным типом симметрии, состоит из гексагональной головки размером 50х50 нм, длинного отростка размером 112 нм, имеет несокращающийся чехол отростка и базальную пластинку. Относится к IV морфологической группе по классификации А.С.Тихоненко.
Морфология негативных колоний. Бактериофаг формирует при посеве на штамме-хозяине в течение 18 ч культивирования при 37 о С негативные прозрачные круглые колонии, диаметром 1,5-2 мм, с четкими ровными краями.
Штамм фага обладает высокой литической активностью, титр фага, определенный методом Аппельмана, составляет 10 -9 . Оптимальная множественность инфицирования бактериальных клеток хозяина штаммом фага находится в диапазоне 0,01-0,1.
Бактериофаг характеризуется высокой урожайностью и скоростью роста. В стационарных условиях культивирования при 37 о С в течение 4 ч в 1 см 3 среды содержится 2,0-3,5 х 10 10 фаговых частиц.
Спектр литического действия. Штамм бактериофага обладает широким спектром литического действия по отношению к изолятам S. enteritidis, выделенным в неблагополучных по сальмонеллезу птицеводческих хозяйствах, лизирует 97% выделенных сальмонелл.
Штамм S. enteritidis 204-R получен целенаправленным снижением вирулентности путем внедрения транспозона Тп7 в геном устойчивого к рифампицину мутанта эпизоотического штамма, с последующей селекцией клонов, устойчивых к действию фага F-6.
Штамм S. enteritidis 204-R депонирован в коллекции микроорганизмов Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов.
Штамм обладает следующими свойствами.
Морфология - мелкие, грамотрицательные палочки без спор и капсул размером 2-3 х 0,6-0,7 мк, перитрих.
Ферментативные свойства - сбраживает с образованием кислоты и газа глюкозу, мальтозу, маннит, сорбит, левулезу, галактозу, декстрин глицерин, инозит, образует сероводород, не образует индол, нитриты редуцирует в нитраты.
Антигенная структура - агглютинируется монорецепторными сальмонеллезными "0" сыворотками: 1,9,12 и "Н" сыворотками: g,1,7.
Генетические маркеры - устойчив к стрептомицину (150 мкг/см 3 ), рифампицину (200 мкг/см 3 ), триметоприму (200 мкг/см 3 ). Маркеры стабильно сохраняются после 10-кратных пересевов на мясопептонном агаре и при 5-кратных пассажах на белых мышах и цыплятах.
Устойчив к действию штамма бактериофага F-6.
Вирулентность - ЛД50 для белых мышей линии Валв/с - 5,6х10 6 микробных клеток.
Иммуногенность - выживаемость белых мышей и цыплят, иммунизированных аттенурованным штаммом, после заражения 5-7 ЛД50вирулентного штамма составляет 80-95% от числа зараженных животных, при гибели в контроле 90-100%.
После наступления лизиса бактерий бактериофаг консервируют, добавляя 2% -ный раствор хинозола до его конечной концентрации в препарате 0,01-0,02%. Затем бактериофаг фильтруют через пластины марки СФ-300 в стерильный реактор и расфасовывают во флаконы.
Бактериофаг серии 1 имел следующий состав, об.%: Суспензия частиц штамма фага F-6 с концентрацией 1 млрд. БОЕ/см 3 в культуральной среде 99,9 Хинозол 0,01 Бактериофаг серии 2 имел следующий состав, об.%: Суспензия частиц штамма фага F-6 с концентрацией 10 млрд. БОЕ/см 3 в культуральной среде 99,9 Хинозол 0,01 Бактериофаг серии 3 имел следующий состав, об.%: Суспензия частиц штамма фага F-6 с концентрацией 1 млрд. БОЕ/см 3 в культуральной среде 99,8 Хинозол 0,02 П р и м е р 2. Изготовление вакцины.
Вакцина 3 изготовленных серий имела следующий компонентный состав, об.%: Серия 1 Серия 2 Серия 3 Суспензия клеток фагоустойчивого штамма S. enteritidis 204-R с концентрацией 150-250 млрд. кл/см 3 52,0 45,0 55,0 Сахароза 5,0 7,5 7,5 Желатин 2,0 1,5 2,0 Дистиллированная вода Остальное П р и м е р 3. Определяют эффективность фаговой части препарата для белых мышей. Используют белых мышей массой 14-16 г. Препарат вводят перорально в объеме 0,5 см 3 .
Первой группе мышей вводят препарат, полученный смешением фаговой и вакцинной частей из расчета 1 млрд. частиц фага и 1 млн. клеток аттенуированного штамма. Половину мышей опытной группы заражают 4-5 ЛД50вирулентного штамма S. enteritidis через 1 сутки, половину через 7 сут после введения препарата.
Второй группе мышей вводят только вакцинную часть препарата из расчета 1 млн. клеток аттенуированного штамма на голову.
Заражают животных в те сроки, что и мышей первой опытной группы. В качестве контроля используют неиммунизированных мышей.
Результаты представлены в табл.1.
Введение в состав препарата бактериофага предохраняет от гибели 85% животных при заражении их через 1 сутки. Гибель мышей, получивших только вакцину из аттенуированного штамма, зараженных в тот же срок, составляет 90%, неиммунизированных животных 95%.
Заражение мышей через 7 сут вызывает гибель животных контрольной группы в 88% случаях, при сохранении 91,6% животных, получивших фаг и вакцину, и 86% мышей получивших только вакцинную часть препарата.
П р и м е р 4. Определяют защитный эффект предлагаемого препарата для цыплят 1-3-дневного возраста. Цыплятам выпаивают препарат, полученный смешением фаговой и вакцинной частей из расчета: 100 млн. фаговых частиц и 0,5 млрд. живых микробных клеток фагоустойчивого вакцинного штамма на одного цыпленка. Препарат применяют перорально, двукратно, с интервалом в 3 дня. Половину цыплят опытной группы заражают 5 ЛД50 вирулентного штамма через 1 сутки, половину через 10 сут после введения препарата. В качестве контроля используют равное количество неиммунизированных цыплят, зараженных в те же сроки.
Результаты представлены в табл.2.
Препарат предохраняет от гибели 86% цыплят при заражении их через 1 сутки при падеже 92% цыплят в контрольной группе. Заражение цыплят через 10 сут вызывает гибель 84% цыплят контрольной группы при выживании 90% птицы в опытной группе.
Использование предлагаемого препарата в ветеринарной практике позволит повысить эффективность проводимых мероприятий по лечению и профилактике сальмонеллеза кур.
ПРЕПАРАТ ПРОТИВ САЛЬМОНЕЛЛЕЗА КУР И СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ САЛЬМОНЕЛЛЕЗА КУР.
Среди болезней сельскохозяйственных животных на первом месте стоят инфекционные заболевания, которые приносят существенный экономический ущерб из-за гибели животных и потери продуктивности, а также немалых затрат на организацию мер профилактики и борьбы. Особое значение имеют инфекции, которым наряду с животными подвержен и человек: сибирская язва, бешенство, бруцеллез, лептоспироз, сальмонеллез и т. д.
Одной из ключевых, наиболее активно развивающихся отраслей сельского хозяйства во многих странах мира сегодня является птицеводство. Ежегодно производится около 300 млн т мяса, для чего выращивается более 500 млрд бройлеров. И примерно 5 % этой птицы погибает, т. е. каждую секунду от различных болезней умирает более 800 цыплят! Одной из основных причин смертности сельскохозяйственной птицы служат болезнетворные бактерии, в том числе опасные для человека. Для нашей страны наиболее актуальны такие патогены, как листерии, иерсинии, сальмонеллы, кампилобактерии и некоторые штаммы кишечной палочки.
Нужно заметить, что с проблемой инфекционных болезней рано или поздно сталкивается любое животноводческое предприятие, вне зависимости от того, на чем оно специализируется, будь то крупный или мелкий рогатый скот, свиньи, пушные животные и т. д. Обеспечение здоровья животных и безопасности продуктов питания требует активного противодействия патогенным микроорганизмам. С момента открытия пенициллина в 1928 г. основным средством борьбы с бактериальными инфекциями стали антибиотики. Однако несмотря на постоянное появление на рынке все новых препаратов, появление мультирезистентных форм бактерий, устойчивых практически ко всем антибиотикам, стало серьезной проблемой не только в здравоохранении, но и в ветеринарии.
Но если мы ограничим применение антибиотиков для животных, не приведет ли это к росту заражения людей патогенными бактериями и, соответственно, росту потребления антибиотиков уже в человеческой популяции? Кроме того, сегодня известны механизмы, которые могут приводить к появлению у бактерий антибиотикорезистентности даже при отсутствии контакта с этими препаратами.
Сложная ситуация подогревает интерес к поиску новых терапевтических средств, которые могут заменить или дополнить антибиотики в борьбе с инфекционными заболеваниями. Поиски альтернативных путей лечения бактериальных инфекций сразу выдвинули на первое место фаготерапию и фагопрофилактику (Акимкин и др., 2010).
От лаборатории – к птицефабрике
Пионерами в использовании фагов для лечения животных можно считать английских ученых У. Смита и его коллег из Института исследования заболеваний животных (Smith et al., 1987). В своих исследованиях на лабораторных мышах, экспериментально зараженных кишечной палочкой, они обнаружили, что даже единичное введение препарата бактериофага значительно уменьшало количество жизнеспособных клеток E. coli в пищеварительном тракте. Позже они повторили этот опыт на телятах, ягнятах и морских свинках, зараженных вирулентным штаммом кишечной палочки, вызывающим диарею. И в этих случаях фаготерапия снижала численность бактерий в желудочно-кишечном тракте, а также смягчала такие связанные с инфекцией симптомы, как обезвоживание. В результате практически все инфицированные животные выжили.
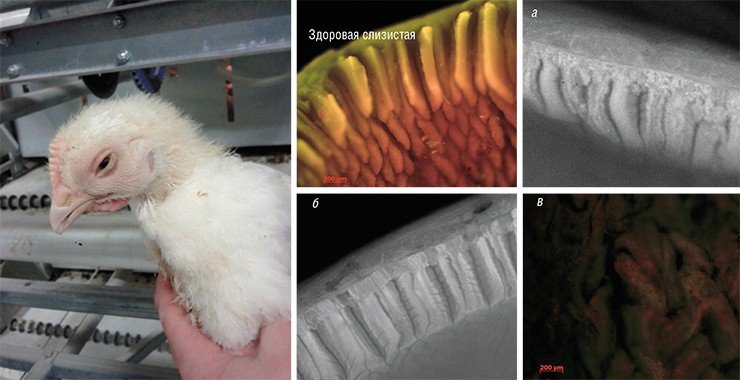
В наши дни становится технически и экономически возможным вести поиск бактериофагов и производство соответствующего биопрепарата для отдельно взятого предприятия. Уничтожить таким образом весь спектр патогенных бактерий нельзя, однако против наиболее важных в санитарном или эпидемическом плане бактерий вполне реально подобрать и применить эффективные бактериофаги.
На сегодня уже имеется успешный опыт применения препаратов бактериофагов против сальмонелл и кишечной палочки на крупных птицефабриках. Например, на одной из отечественных птицефабрик, где наблюдался аномально высокий (50—70 %) уровень инфицированности цыплят-бройлеров сальмонеллой, за несколько месяцев удалось снизить этот показатель до нерегистрируемых значений. К тому же на крупных птицефабриках и свинокомплексах, где имеется высокая скученность животных, распространение бактериофагов, вакцинных штаммов вирусов и полезных, пробиотических штаммов бактерий идет по типу эпидемического процесса, что значительно удешевляет и повышает эффективность борьбы с инфекциями.
В приведенном выше примере с сальмонеллой в процессе фаготерапии произошла смена серотипа бактерий, в результате чего появился новый штамм Infantis, оказавшийся устойчивым к используемому бактериофагу. Этот факт наводит на мысль, что бактериофаги могут выступать для бактерий как фактор межвидовой конкуренции. Ведь бактерии рода Salmonella встречаются в кишечнике в относительно низкой концентрации, и можно ожидать, что между разными видами и подвидами этого рода конкуренция будет отсутствовать (Antunes et al., 2016). Однако последовательная смена различных серотипов сальмонелл в популяциях кур позволяет предполагать неслучайный характер этого явления.
Для меньших братьев
В научной литературе достаточно широко освещены и явление полигостальной специфичности (способности заражать широкий спектр видов бактерий) в отношении разных видов бактерий, и феномен разной фагорезистентности у разных штаммов внутри одного вида бактерий по отношению к одному и тому же бактериофагу. Очевидно, что штамм бактерии, способный поддерживать существование бактериофага без гибели клетки-хозяина, может получить эволюционное преимущество, так как станет причиной гибели бактерий-конкурентов, чувствительных к бактериофагу. Этот пример показывает, как много различных биологических идей можно извлечь, наблюдая взаимоотношения бактерий с бактериофагами. Кроме того, изучая спонтанное распространение бактериофагов по птицефабрикам и свинофермам, мы можем совершенно безопасно моделировать эпидемии.

Безусловно, в ближайшем будущем бактериофаги не смогут заменить антибиотики. Но в ситуациях, когда антибиотики уже не помогают, а также, когда нужно снять риск возникновения антибиотико-устойчивых штаммов бактерий, бактериофаги должны занять свое законное место.
В ветеринарии использование бактериофагов намного перспективнее, чем в медицине. Ведь новые ветеринарные лекарства быстрее выводятся на рынок, чем лекарства для человека. К тому же в крупных животноводческих хозяйствах специалисты сталкиваются с меньшим разнообразием инфекций при диагностике, чем у людей, что упрощает этап формирования коллекций бактерий и подбора бактериальных вирусов.
Андреева И. С., Соловьянова Н. А., Афонюшкин В. Н. и др. Перспективы фаготерапии сальмонеллезов птицы в сельскохозяйственном производстве // Современное общество, образование и наука: Сб. науч. тр. по материалам Международной научно-практической конференции. 2013. С. 10—13.
Акимкин В. Г., Дарбеева О. С., Колков В. Ф. Бактериофаги: исторические и современные аспекты их применения: опыт и клинические перспективы // Клиническая практика. 2010. Т. 4. С. 48—54.
Antunes P., Mourão J., Campos J., Peixe L. Salmonellosis: the role of poultry meat // Clin. Microbiol Infect. 2016. V. 22. P. 110—121.
Klaas M. Pos, Trinity revealed: Stoichiometric complex assembly of a bacterial multidrug efflux pump // PNAS. V. 106. N. 17. P. 6893—6894, doi: 10.1073/pnas.0902837106
Бактериофаг IBР-1 против сальмонелла энтеритидис - инфекции кур
В Европе B 2004 году было зафиксировано около 400,000 случаев заболевания людей зоонозами. Около половины из них (48%) умерли от сальмонеллеза. В Великобритании Министр здравоохранения Е. Currie заявила, что яйца являются главным источником сальмонеллеза у людей, скандал привел к тому, что почти полностью остановилась потребление яиц. В США, приблизительно 40 000 случаев сальмонеллеза регистрируются каждый год, из них 25% вызваны S. enteritidis. B 24 из 50 штатов регистрировались случаи заболевания S. enteritidis. B 2000 - 2002 r r S. enteritidis и S. typhimurium, вместе составили 90% от всех выделенных сальмонелл от человека. 19 - 22 апреля 2012 г., Москва
В целом экономические убытки от сальмонеллеза B США оцениваются в 2 млрд. долларов, B Канаде - B 300 млн.долларов.
B странах СНГ за последние 15 лет заболеваемость людей и птицы сальмонеллезом возросла B 7 раз, при этом этиологическое значение S. enteritidis B заболевании людей возросло на 30%, у животных и птицы - на 75%, а случаи индикации возбудителя B продуктах питания увеличились на 50%.
В Российской федерации статистический мониторинг выявил возрастание числа неблагополучных пунктов по сальмонеллезу людей: от 60-ти в 1991 г. до 170-ти в 2001 г. В России B период с 2004 г. по 2008 г. вспышки сальмонеллеза были зафиксированы B Кемеровской, Нижегородской, Архангельской, Волгоградской, Челябинской, Новосибирской, Московской областях, Хакасии, Башкирии, Чувашии, Ставропольском, Красноярском, Приморском краях, Ханты- Мансийском, Таймырском автономных округах. В большинстве случаев пострадавшими оказывались дети дошкольного возраста.
В 2009 году B России от инфекционных болезней пало 2,1 млн. голов птицы, B результате получен ущерб B размере 60,7 млн. руб. При проведении микробиологического мониторинга B птицехозяйствах различного технологического направления установлено, что процент выделения S.enteritidis из патологического материала и помёта зависит от эпизоотической ситуации в каждом конкретном хозяйстве и составляет от 4,3% до 42,2%. По данным Росптицесоюза сальмонеллез занимает 0,23% от всех регистрируемых болезней птиц B России (2010 г).
Сальмонелла энтерэтидис настолько адаптировалась к организму кур, что является одним из основных возбудителей тяжело протекающих пищевых токсикоинфекций у человека. Из зарегистрированных вспышек пищевых токсикоинфекций - 76%, вызванные S. enteritidis связаны с потреблением мяса кур (10%), яиц (39%) или продуктов, содержащих яйца, таких как мороженое (2%).
По данным Росптицесоюза K 2012 году производтво мяса птицы будет доведено до 3,2 млн тонн в год, а яиц - до 43-47 млрд штук в год (прирост 3,6 млрд штук K показателю 2009 юда), в связи с такими перспективами проблема сальмонеллеза кур становится еще более актуальной.
Конечно, для решения проблемы сальмонеллезов применяется целая система мероприятий: дезинфекция птицеводческих предприятий, вакцинация птицепоголовья, применение пребиотиков и пробиотиков, но основным методом борьбы с сальмонеллезными инфекциями по-прежнему остаются антибиотики.
По этому поводу директор Всероссийского государственного научно- исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов (ФГУ ВГНКИ) Александр Панин сказал, что около 50% птицеводческой продукции не соответствует требованиям, он также заметил, что до 50% пти цеводческих хозяйств злоупотребляют антибиотиками. Кальницкая О.И. и Уша Б. В. также связывают попадание антибиотиков в продукты убоя птицы с их широким применением в лечебно-профилактических целях.
Но для ужесточения требований к остаточному содержанию антибиотиков в мясе разработан и действует новый микробиологический метод, с помощью которого можно определять до 50 антибиотиков. Этим методом ученые Московского государственного института прикладной биотехнологии выделили антибиотики из 27,9% исследованных проб продуктов убоя птицы импортного и отечественного производства. Такой метод, безусловно, будет способствовать тому, что в борьбе с инфекционными заболеваниями антибиотики станут применяться все реже и реже. Над этим уже давно работает Европейская Комиссия по Регулированию, которая установила правила для улучшения ситуации по сальмонеллезу, в частности Регулирование 1177/2006 запретило использование антибиотического лечения для сокращения или лечения сальмонеллезной инфекции.
Другое учреждение EFSA (Европейское ведомство по безопасности пищевых продуктов) выдвинуло ряд предложений для нормализации проблемы сальмонеллеза, а именно: компенсация фермерам, которым приходилось уничтожать их зараженные родительские стада и несушек, запрет на использование мяса после убоя от такой птицы, а также искоренение инфекции путем убоя зараженной домашней птицы.
В нашей стране ветеринарным законодательством все эти мероприятия предусмотрены, кроме конечно, материальной компенсации. Так, при подтверждении диагноза на заболевание птицы пуллорозомифом и сальмонеллезом антеритидис хозяйство (отделение, ферму) объявляют в установленном порядке неблагополучным и ВВОДЯТ ограничения, на основании чего запрещается: - вывоз инкубационных яиц и птиц в другие хозяйства для комплектования стад; - вывоз яиц от положительно реагирующей птицы в торговую сеть; - инкубация внутри хозяйства яиц неблагополучных птичников.
В племенных хозяйствах (зонально-опытные станции, экспериментальные хозяйства, племптицезаводы, племптицесовхозы, репродукторы первого и второго порядка) при обнаружении клинически больного пуллорозомтифом или сальмонеллезом энтеритидис ремонтного молодняка или больной взрослой птицы‚ а также птицы, реагирующей в ККРНГА; и при подтверждении диагноза бактерологическим методом всю птицу неблагополучного птичника убивают на мясо в убойном цехе (Ветеринарные правила ВП 13.4.1318-96).
В случае установления бактерионосительства (свыше 1% положительно реагирующих птиц) всю птицу мясных пород сдают на убой, а яйценоских - после удаления и убоя реагирующих птиц переводят в промышленное стадо для получения товарных яиц или убивают (Ветеринарные правила ВП 13.4.1318-96).
После каждого исследования всю реагирующую птицу немедленно убивают, а в птичнике проводят аэрозольную дезинфекцию согласно действующей Инструкции по проведению аэрозольной дезинфекции птицеводческих помещений в присутствии птиц; подстилку обновляют и добавляют в нее хлорную известь. Перед проведением аэрозольной дезинфекции птичника кормушки, поилки, гнезда, насесты очищают механически, Моют и дезинфицируют влажным методом. (Ветеринарные правила ВП 13.4.1318-96).
Яйца, предназначенные для инкубации, дезинфицируют парами формальдегида: не позднее 2 часов после снесения; при поступлении в инкубаторий (яйцесклад): после сортировки, через 6 часов после закладки в инкубаторы.
Известно, что Salmonella enteritidis может вызывать в неблагополучных фермах поголовное инфицирование и отход цыплят до 10-15% в первые дни их жизни. Взрослая птица переболевает бессимптомно и остается, также как и выжившие цыплята, носителем и выделителем сальмонелл, с преимущественной локализацией возбудителя в яичниках, печени, селезенке и толстом отделе кишечника.
Так что же предпринять ветеринарным врачам в условиях, когда возможности, продавать мясо и яйцо с остаточным количеством антибиотиков, нет, а проблема сальмонеллеза есть? Остается вакцинация в профилактических целях и применение бактериофагов в лечебных.
Для вакцинации птицы по всему миру применяются вакцины различных фирм. В настоящее время разрешены к применению на территории России пока только инактивированные вакцины, но иностранные компании уже готовят документы для ввоза живых сальмонеллезных вакцин. Конечно, вакцинация инактивированными вакцинами спасает положение и приносит свой ощутимый- вклад в оздоровление хозяйства, жаль только, что вакцинация слишком трудоемка и предусматривает от двух до трех-четырех вакцинаций родительского стада. Вакцинации же живыми вакцинами вообще не приведут к желаемому эффекту, т.к. все ветеринарные врачи знают, что от сальмонеллы энтеритидис даже подросший молодняк гибнет не всегда, а взрослая птица вообще является только носителем. Но мы-то говорим о проблеме пищевых токсикоинфекций y человека, а для этого не важно какая сальмонелла попала в продукт: от больной птицы, от носителя, или вакцинный штамм. И для сертифицированных лабораторий это также не играет никакой роли, они выявляют сальмонеллу и на этом ставят точку, определяя дальнейшие предписания в отношении того или иного птицехозяйства.
Читайте также:


