Клиника по лечению лейкоэнцефалопатии
Энцефалопатия (ЭП) – это синдром, обусловленный дистрофическими процессами со стороны головного мозга. Процесс имеет диффузный характер (затрагивает обширные части мозга). Возникает вследствие заболеваний и патологических состояний, прямо не связанных с повреждением нейронов. В нашей клинике проводится полная диагностика и лечение различных вариантов энцефалопатии.
Запись на консультацию, диагностику и лечение по телефону
Энцефалопатия многообразна. Все ее многочисленные разновидности объединяются в две большие группы: врожденная патология, а также приобретенная.
Причины энцефалопатии
У детей заболевание возникает как результат врожденного поражения мозга. Нередко обусловлено генетическими нарушениям, пороками развития, повреждением нервной системы вследствие внутриутробной гипоксии плода или травмы черепа при родах.
Приобретенная энцефалопатия развивается на фоне сторонних явлений разного рода, поэтому выделяют несколько ее разновидностей:
- посттравматическая;
- токсическая;
- лучевая (результат воздействия на организм радиации);
- метаболическая (дисциркуляторная, обменные нарушения при заболеваниях печени, почек, поджелудочной железы);
- сосудистая (атеросклеротическая, гипертоническая, венозная), развивающаяся при длительном заболевании сосудов.
Все виды ЭП развиваются по схожим механизмам. Возникает гипоксия головного мозга, в его веществе формируются многочисленные микро кровоизлияния. Такой процесс более усугубляется действием токсинов – алкоголя, никотина.
Как результат – вещество головного мозга диффузно засеивается очагами дистрофических процессов. Число нервных клеток уменьшается, происходят дегенеративные явления.
Симптоматика энцефалопатии
Проявления заболевания полиморфны. На ранних этапах снижается умственная активность, память, человек с трудом переключает внимание. Как правило, пациентов беспокоят:
- головные боли;
- шум в ушах и голове;
- перепады настроения;
- раздражительность;
- слабость;
- утомляемость.
Во время неврологического осмотра обнаруживается как общемозговая, так и очаговая симптоматика. У отдельных больных, ЭП проявляется в виде психических расстройств, судорожных синдромов.
Степени энцефалопатии
Патология разделяется на 3 степени, что определяется органическими изменениями со стороны головного мозга, тяжестью клинического течения.
Например, ЭП 2 степени, может характеризоваться не только явными клиническими проявлениями, но также четкими изменениями на МРТ, КТ. Иногда степени называют стадиями.
Установление диагноза и степени тяжести
В диагностике главную роль играют следующие виды обследований:
- тщательный сбор анамнеза больного, неврологический осмотр;
- электроэнцефалография, помогающая выявить очаги патологической активности;
- компьютерная томография, выявляющая опухоли, кровоизлияния, сосудистые нарушения, отек;
- биохимические анализы крови, позволяющие установить обменный характер нарушений.
Методы лечения энцефалопатии
Для назначения адекватного лечения врач должен тщательно оценить симптоматику пациента и проанализировать данные инструментальных исследований.
Первой линией назначаются препараты: улучшающие мозговое кровообращение, ноотропы, витамины, адаптогены. Медикаментозную терапию подкрепляют дополнительные методы лечения.
Проблема терапии ЭП до текущего момента представляет сложность, иногда удается лишь несколько стабилизировать состояние больного.
Энцефалопатия у детей, лечение. Терапию пациентов детского возраста необходимо проводить с учетом функциональных особенностей их организма.
Клиника восстановительной неврологии обладает опытом 25 лет лечения такой патологии у детей. Положительные результаты достигаем у пациентов с перинатальной энцефалопатией.
Кроме классических медикаментозных методик лечения, мы применяем индивидуально подобранною комплексную терапию.
Практикуем такие методики, как транскраниальная магнитная, зрительная, слуховая стимуляция, биорезонансная активация мозга и БОС, эрготерапия.
Серьезное внимание уделяется гирудотерапии, рефлексотерапии, массажу, ЛФК. Это позволяет нам добиваться заметных результатов, справляться как с первичным заболеванием, вызвавшем энцефалопатию, так и с ее патогенетическими механизмами.
Запись на консультацию, диагностику и лечение по телефону
Подписка на рассылку
Согласен (-на)с политикой конфиденциальности и обработки персональных данных
Была ли эта статья полезна?
Вы можете подписаться на нашу рассылку и узнать много интересного о лечение заболевания, научных достижений и инновационных решений:
Как можно улучшить эту статью?
Лейкоэнцефалопатия головного мозга может поразить человека любого возраста. Чаще всего возникновение и развитие этой болезни связывают со стабильно повышенным давлением, эпизодами кислородного голодания и распространением полиомавируса.

Лекарственных препаратов, способных остановить развитие заболевания, в настоящее время не существует.
Описание
Лейкоэнцефалопатия – заболевание, характеризующееся стойким разрушением в головном мозге белого вещества. Болезнь развивается быстро и практически всегда приводит к летальному исходу.
Патология впервые описана Людвигом Бинсвангером в 1964 г., поэтому иногда ее называют болезнью Бинсвангера.
Причины
Принято выделять 3 основные причины, приводящие к лейконэнцефалопатии. Это гипоксия, стабильно высокое давление и вирусы. Провоцируют ее возникновение следующие заболевания и состояния:
- эндокринные нарушения;
- гипертония;
- атеросклероз;
- злокачественные опухоли;
- туберкулез;
- ВИЧ и СПИД;
- патологии позвоночника;
- генетический фактор;
- вредные привычки;
- родовая травма;
- прием препаратов, снижающих иммунную реакцию организма.
Провоцирующее действие вредоносных факторов ведет к демиелинизации пучков нервных волокон. Белое вещество уменьшается в объеме, размягчается, изменяет структуру. В нем появляются кровоизлияния, очаги поражения, кисты.

Часто демиелинизацию вызывают полиомавирусы. В неактивном состоянии они присутствуют в жизни человека постоянно, сохраняясь в почках, костном мозге, селезенке. Ослабление иммунитета приводит к активизации вирусов. Лейкоциты переносят их в центральную нервную систему, где они находят благоприятную среду в мозге, поселяются в нем и разрушают его.
Обычно необратимым изменениям подвергается только белое вещество. Однако есть данные и о том, что, вероятно, перивентрикулярный вид лейкоэнцефалопатии ведет также к поражению серого вещества.
Классификация
Определение основной причины патологии и характера ее течения позволяет выделять несколько типов лейкоэнцефалопатии.
Основной причиной появления и развития мелкоочаговой лейкоэнцефалопатии сосудистого генеза является поражение сосудов мозга, вызванное гипертонией, травмами, появлением атеросклеротических бляшек, эндокринными заболеваниями, болезнями позвоночника. Кровообращение нарушается из-за сгущения крови и закупорки сосудов. Ухудшающим состояние фактором является алкоголизм и ожирение. Считается, что болезнь развивается при наличии отягчающих наследственных факторов.
Данную патологию называют также прогрессирующей сосудистой лейкоэнцефалопатией. Сначала появляются небольшие очаги поражения сосудов, потом они увеличиваются в размерах, вызывая ухудшение состояния больного. С течением времени нарастают признаки патологии, заметные окружающим. Ухудшается память, снижается интеллект, возникают психоэмоциональные расстройства.
Больной жалуется на тошноту, головную боль, постоянную усталость. Сосудистая мелкоочаговая энцефалопатия характеризуется скачками давления. Человек не может глотать, с трудом пережевывает пищу. Появляется тремор, отличающий болезнь Паркинсона. Утрачивается способность контролировать процессы мочеиспускания и дефекации.
Очаговая энцефалопатия сосудистого генеза регистрируется в основном у мужчин после 55 лет. Ранее данное нарушение было включено в список МКБ, но в дальнейшем его исключили.
Главной особенностью этого типа нарушения считается появление большого количества очагов повреждения. Вызывают воспаление полиомавирус человека 2 (JC polyomavirus). Он обнаруживается у 80% жителей Земли. В скрытом состоянии живет в организме несколько лет, но при ослаблении иммунитета активируется и, попадая в ЦНС, вызывает воспаление.
Провоцирующими заболевание факторами являются СПИД, ВИЧ-инфицирование, длительное применение иммунодепрессантов и лекарств, предназначенных для лечения онкологических заболеваний. Прогрессирующая мультифокальная энцефалопатия диагностируется у половины пациентов со СПИДом и 5% людей с ВИЧ-инфекцией.

Поражение часто имеет асимметричный характер. Признаками ПМЛ являются параличи, парезы, ригидность мышц, тремор, напоминающий болезнь Паркинсона. Лицо приобретает вид маски. Возможна потеря зрения. Проявляются тяжелые когнитивные нарушения, снижение внимания.
Мультифокальная лейкоэнцефалопатия не лечится. Для улучшения состояния больного убирают препараты, подавляющие иммунитет. Если заболевание вызвано пересадкой органа, он подлежит удалению.
Лейкопатию головного мозга у ребенка вызывает гипоксия, возникшая при родах. Инструментальные методы диагностики позволяют увидеть участки гибели ткани, преимущественно рядом с мозговыми желудочками. Перивентрикулярные волокна несут ответственность за двигательную активность, и их поражение ведет к детскому церебральному параличу. Очаги поражения возникают симметрично, в особо тяжелых случаях обнаруживаются во всех центральных зонах мозга. Поражение характеризуется прохождением 3 стадий:
- возникновение;
- развитие, приводящее к структурным изменениям;
- образование кисты или рубца.
Перивентрикулярная лейкоэнцефалопатия характеризуется 3 степенями заболевания. Легкая степень характеризуется незначительной выраженностью симптомов. Обычно они проходят через неделю после рождения. Для средней степени характерно повышение внутричерепного давления, возникают судороги. При тяжелой ребенок находится в коме.
Симптомы появляются не сразу, некоторые из них можно заметить только через 6 месяцев после рождения ребенка. Чаще всего обращают на себя внимание парезы и парализация. Наблюдается косоглазие, заторможенность, гиперактивность.
Лечение включает массаж, физиопроцедуры, специальные комплексы упражнений.
Основной причиной этого заболевания являются мутации генов, подавляющие белковый синтез. Чаще всего появляется у детей, преимущественно в возрасте от двух до шести лет. К провоцирующим факторам относят сильное психическое напряжение, вызванное травмой или тяжелой болезнью.
Версия: Справочник заболеваний MedElement
Общая информация
Примечание. Из данной подрубрики исключена "Субкортикальная сосудистая деменция (F01.2).
Этиология и патогенез
Описаны семейные случаи заболевания с началом до 40 лет, без артериальной гипертензии. Более чем в 80% случаев болезнь дебютирует в возрастном промежутке от 50 до 70 лет.
Страдают также и более крупные артерии диаметром до 500 мкм, и все микроциркуляторное русло.
Эпидемиология
Болезнь (энцефалопатия) Бинсвангера встречается довольно часто. По данным клинико-компьютерно-томографического исследования, она составляет около 1/3 всех случаев сосудистой деменции.
Возраст. Более чем в 80% случаев болезнь дебютирует в возрастном промежутке от 50 до 70 лет.
Факторы и группы риска
Клиническая картина
Клиническая картина болезни Бинсвангера характеризуется прогрессирующими когнитивными нарушениями, нарушениями функции ходьбы и тазовыми расстройствами. На последнем этапе заболевания клиническая картина представлена слабоумием, полной беспомощностью больных (не ходят, не обслуживают себя, не контролируют функцию тазовых органов).
Картина слабоумия может значительно варьироваться по степени тяжести и особенностям симптоматики.
В целом для болезни Бинсвангера характерно неуклонно-прогредиентное течение, но возможны и периоды длительной стабилизации. Причинами слабоумия в этих случаях считаются разобщение корково-подкорковых связей, наступающее в результате поражения подкоркового белого вещества, а также дисфункция базальных ганглиев и таламуса.
Основные характеристики лобной диспраксии ходьбы, связанной с дезавтоматизацией ходьбы, следующие:
• замедление ходьбы;
• укорочение шага;
• затруднение в начале ходьбы (инициация ходьбы);
• неустойчивость при поворотах (постуральная дисфункция);
• расширение базы опоры;
• снижение длины шагов.
Двигательные нарушения могут также характеризоваться (помимо нарушения ходьбы): другой экстрапирамидной патологией в виде паркинсоноподобной симптоматики, а также легкими или умеренными центральными моно- или гемипарезами, часто быстро регрессирующими (регресс очаговой двигательной симптоматики становится неполным по мере прогрессирования заболевания). Характерен псевдобульбарный синдром.
Эмоционально-волевые нарушения представлены астеническим, неврозоподобным или астено-депрессивным синдром. По мере прогрессирования заболевания на первый план выходят не астения и депрессия, а нарастание эмоционального оскудения, сужение круга интересов и спонтанности.
В критериях подчеркивается, что у пациента должны отсутствовать множественные или двухсторонние корковые очаги по данным КТ и МРТ, и тяжелая деменция.
Диагностика
Осложнения
- 1) Транзиторная ишемическая атака .
Транзиторные ишемические атаки (ТИА, преходящие нарушения мозгового кровообращения) характеризуются кратковременными симптомами локальной ишемии мозга.
ТИА обычно связаны с гемодинамической недостаточностью, возникающей при выраженном атеросклеротическом стенозе сонных или позвоночных артерий в их дистальных ветвях или артериальной эмболией.
В большинстве случаев транзиторные ишемические атаки разрешаются в течение 5-20 минут.
Клиническое значение ТИА состоит в том, что они служат предвестниками не только инсульта, но и инфаркта миокарда и представляют собой сигналы опасности, требующие от врача быстрых действий. Больных с ТИА необходимо госпитализировать в инсультное отделение для наблюдения, всестороннего обследования и проведения профилактики ишемического инсульта.
ТИА часто проявляются при снижении АД, физической нагрузке, натуживании, приеме пищи; при этом очаговые неврологические симптомы нередко проявляются на фоне предобморочного состояния, иногда по нескольку раз в день. Больные часто жалуются на предобморочное состояние, головокружение, нарушения зрения, слабость в конечностях, тошноту и рвоту, нарушения памяти, шум в ушах, нарушения чувствительности, неожиданную утрату равновесия.
2) Инсульты - острые нарушения мозгового кровообращения (ОНМК) .
Различают инсульты - ишемический инсульт и внутримозговое (паренхиматозное) кровоизлияние .
Ишемический инсульт возникает в результате критического снижения или прекращения кровоснабжения участка мозга с последующим развитием очага некроза мозговой ткани.
Внутримозговое кровоизлияние возникает в результате разрыва патологически измененных сосудов мозга, приводящего к кровоизлияниям.
Классическая лейкоэнцефалопатия – это хроническое прогрессирующее заболевание центральной нервной системы, вызванное инфекцией полиомавирусом человека 2-го типа, поражающее преимущественно белое вещество головного мозга и сопровождающееся демиелинизацией – разрушением миелиновой оболочки нервных волокон. Оно возникает у людей с иммунодефицитами.
Выраженная лейкоэнцефалопатия проявляется психическими, неврологическими расстройствами и симптомами интоксикации на фоне размножения вируса. Клиника также проявляется общемозговыми и менингеальными симптомами.
Впервые вирус, вызвавший заболевание, был выявлен в 1971 году. Как самостоятельное заболевание прогрессирующая лейкоэнцефалопатия была выделена в 1958 году. Вирус JC, названный в честь первого пациента John Cunningham, носят порядка 80% населения планеты. Однако из-за нормальной работы иммунной системы инфекция не проявляется и протекает в латентном состоянии.
В середине XX столетия частота заболеваемости составляла 1 случай на 1 миллион населения. К концу 90-х годов встречаемость снизилась до одного случая на 200 тысяч населения. После введения нового метода лечения ВААРТ (высокоактивная антиретровирусная терапия) прогрессирующая лейкоэнцефалопатия головного мозга стала встречается у одного пациента с ВИЧ-инфекцией из 1000.
Причины
В основе развития лейкоэнцефалопатии лежит реактивация вируса вследствие ухудшения работы иммунитета. У 80% пациентов, которым поставлен диагноз лейкоэнцефалопатии, болеют СПИДом или являются переносчиками ВИЧ-инфекции. 20% остальных пациентов страдают злокачественными опухолями, ходжкинскими и неходжскинскими лимфомами.
Вирус JC – оппортунистическая инфекция. Это значит, что у здоровых людей она не проявляется, а начинает размножаться при условии сниженного иммунитета. Вирус передается воздушно-капельным и фекально-оральным путем, что говорит об его распространенности среди населения планеты.
Когда работа иммунной системы ухудшилась, например, человек заразился ВИЧ-инфекцией, общая и специфическая резистентность иммунных механизмов падает. Начинается реактивация вируса. Он активно размножается и попадает в ток крови, откуда через гематоэнцефалический барьер переносится в белое вещество головного мозга. Он живет в олигодендроцитах и астроцитах, которые, в результате своей жизнедеятельности, разрушает. В клетку вирус JC попадет через связывание с клеточными рецепторами – серотониновый 5-гидрокситриптамин-2А рецептор. После разрушения олигодендроцитов начинается активный процесс демиелинизации, развивается мультифокальная энцефалопатия головного мозга.
Прогрессирующая многоочаговая лейкоэнцефалопатия под микроскопом проявляется разрушением олигодендроцитов. В клетках обнаруживаются остатки вирусов и увеличенные ядра. Астроциты увеличиваются в размере. На разрезе в мозге обнаруживаются очаги демиелинизации. В этих же участках наблюдаются небольшие полости.

Классификация
Белое вещество разрушается не только в результате вирусной инфекции или иммуносупрессии.
Энцефалопатия в общем понимании – это постепенное разрушение вещества головного мозга вследствие нарушения кровообращения, часто на фоне сосудистых патологией: артериальной гипертензии и атеросклероза. Энцефалопатия сопровождается масштабными изменениями вещества. В спектр поражения также входит белое вещество мозга. Чаще это диффузная лейкоэнцефалопатия. Она характеризуется разрушением белового вещества в большей части головного мозга.
Лейкоэнцефалопатия головного мозга сосудистого генеза сопровождается образованием мелких инфарктов белого вещества. В процессе развития болезни возникают очаги демиелинизации, погибают олигодендроциты и астроциты. В этих же областях на месте микроинфаркта обнаруживаются кисты и отек вокруг сосудов в результате воспаления.
Мелкоочаговая лейкоэнцефалопатия вероятно сосудистого генеза в последствии сопровождается глиозом – замещением нормальной рабочей нервной ткани аналогом соединительной ткани. Глиоз – это очаги мало- или вовсе нефункциональной ткани.
Подвид дисциркуляторной энцефалопатии – микроангиопатическая лейкоэнцефалопатия. Белая ткань разрушается вследствие поражения или закупорки мелких сосудов: артериол и капилляров.
Современное название патологии – перивентрикулярная лейкомаляция. Заболевание сопровождается образованием очагов омертвелой ткани в белом веществе мозга. Встречается у детей и является одной из причин детского церебрального паралича. Лейкоэнцефалопатия головного мозга у детей встречается обычно у мертворожденных.
Лейкомаляция, или размягчение белого вещества, возникает вследствие гипоксии и ишемии головного мозга. Обычно ассоциируется с пониженным артериальным давлением у ребенка, нарушением дыхания сразу после родов или осложнениями в виде инфекции. Перивентрикулярная лейкоэнцефалопатия головного мозга у ребенка может развиться вследствие недоношенности или вредных привычек матери, из-за чего у ребенка в период внутриутробного развития была интоксикация.
У мертвого ребенка может встречается комбинированный вариант – многоочаговая и перивентрикулярная лейкоэнцефалопатия сосудистого генеза. Это сочетание сосудистых нарушений, например, врожденных пороков сердца и нарушения дыхания после рождения.
Развивается вследствие приема токсических веществ, например, инъекционных наркотиков или вследствие интоксикации продуктами распада. Также может возникнуть в результате заболеваний печени, при которых в головной мозг проникает продукты метаболизма токсических веществ, разрушающих белое вещество. Разновидность – задняя обратимая лейкоэнцефалопатия. Это вторичная реакция на нарушение циркуляции, обычно на фоне резкого изменения кровяного давления с последующим застоем крови в головном мозгу. В результате возникает гиперперфузия. Развивается отек мозга, локализирующийся в области затылка.
Это генетически обусловленное заболевание, вызванное мутацией генов группы EIF. В норме они кодируют синтез белка, однако после мутации их функция теряется и количество синтезируемого белка снижается на 70%. Обнаруживается у детей.
Классификация по масштабу:
- Мелкоочаговая неспецифическая лейкоэнцефалопатия. В белом веществе возникают мелкие очаги или микроинфаркты.
- Многоочаговая лейкоэнцефалопатия. То же, что и предыдущее, однако очаги достигают больших размеров и их много.
- Диффузная лейкоэнцефалопатия. Характеризуется слабовыраженным поражением белого вещества по всей области головного мозга.

Симптомы
Клиническая картина классической прогрессирующей мультифокальной энцефалопатии состоит из неврологических, психических, инфекционных и общемозговых симптомов. Интоксикационный синдром сопровождается головными болями, усталостью, раздражительностью и лихорадкой. Неврологические симптомы лейкоэнцефалопатии:
- раздражение оболочек головного мозга: светобоязнь, головные боли, тошнота и рвота, ригидность мускулов шеи и специфическая поза лягавой собаки;
- ослабление или полное исчезновение мышечной силы на конечностях одной стороны тела;
- одностороннее выпадение зрения или снижение его точности;
- нарушение сознания и коматозное состояние.
К нервнопсихическим расстройствам относится деменция. У больных рассеивается внимания, снижается объем кратковременной памяти. Пациенты становятся апатичными, вялыми, безучастными. Со временем у них вовсе утрачивается интерес к внешнему миру. У 20% больных встречаются судорожные припадки.
Клиническая картина может дополняться воспалением ткани головного мозга и очаговой симптоматикой. Так, например, единичные неспецифические очаги лейкоэнцефалопатии в лобных долях может сопровождаться расторможением поведения и трудностями в контроле эмоциональных реакций. Родственники и близкие часто жалуются на странные и импульсивные поступки больного, не имеющие адекватного объяснения.
Лейкоэнцефалопатия с исчезающим белым веществом клинически разделяется на такие стадии:
Младенческий вариант диагностируется до первого года жизни. После рождения объективно выявляются неврологические нарушения и сочетающиеся приобретенные или врожденные поражения внутренних органов.
Детская форма встречается в возрасте от 2 до 6 лет. Она возникает вследствие внешних факторов, чаще это нейроинфекции или стресс. Клиническая картина характеризуется быстрым нарастанием дефицитарной неврологической симптоматикой, понижением артериального давления и нарушением сознания, вплоть до коматозного состояния.
Поздняя лейкоэнцефалопатия диагностируется после 16 лет. Проявляется преимущественно неврологической симптоматикой: нарушается работа мозжечка и пирамидного тракта. Позднее наслаивается эпилепсия. К старости формируется слабоумие. У больных отмечаются и психические расстройства: депрессия, инволюционные психозы, мигрень и резкое снижение либидо. У женщин поздний вариант сопровождается гормональными нарушениями. Фиксируется дисменорея, бесплодие, ранняя менопауза. Диагностика затрудняется тем, что у женщин на первый план выступают именно неврологические нарушения, а не общемозговые и неврологические симптомы.
Признаки сосудистой лейкоэнцефалопатии:
- Нейропсихологические расстройства. Сюда входит нарушение поведения, расстройство когнитивных функций, нарушение эмоционально-волевой сферы.
- Двигательные расстройства. Нарушаются сложные осознанные движения, также может наблюдаться очаговая симптоматика в виде гемипареза или гемиплегии.
- Вегетативные расстройства: снижение аппетита, гипергидроз, диарея или запор, одышка, сердцебиение, головокружение.
Диагностика
В основе диагностики классической лейкоэнцефалопатии – выявление ДНК вируса путем полимеразной цепной реакции. В диагностику также включается магнитно-резонансная томография и исследование спинномозговой жидкости. Однако изменения цереброспинального ликвора неспецифичны и часто отражают типовые изменения при воспалении.
На МРТ обнаруживаются очаги повышенной интенсивности, располагающиеся асимметрично в области белого вещества лобных и затылочных долей. МР картина перивентрикулярной мелкоочаговой лейкоэнцефалопатии: на Т1 режиме очаги низкой интенсивности. Очаги также обнаруживаются в коре головного мозга, стволовых отделах и мозжечке.
Способы лечения
Лечения, устраняющего причину болезни, нет. Основная цель терапии – воздействовать на патологический процесс при помощи глюкокортикоидов и цитотоксических средств. Лечение также дополняется препаратами, которые стимулируют работу иммунной системы. Вторая ветка терапии – устранение симптомов.
Прогноз
Прогноз неблагоприятный. Сколько живут: с момента постановки диагноза больные живут в среднем от 3 до 20 месяцев.
Профилактика
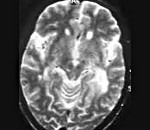
Прогрессирующая мультифокальная лейкоэнцефалопатия — редкое демиелинизирующее заболевание, обусловленное реактивацией находящегося в организме большинства людей вируса JC. Патология возникает на фоне угнетения иммунитета у больных СПИДом, гемобластозами, наследственными иммунодефицитами, у пациентов, получающих иммуносупрессивную терапию. Диагностика базируется на клинических данных, результатах томографии головного мозга, ПЦР-исследования ликвора на вирусную ДНК, гистологии церебральных биоптатов. Специфическая терапия не разработана.
Общие сведения
Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) ассоциирована с JC-вирусом (JCV), возникает у иммунокомпрометированных пациентов, 85% из которых составляют ВИЧ-инфицированные. Заболевание относится к оппортунистическим инфекциям, носителями вируса являются 90% человечества. До 90-х годов ХХ века заболеваемость ПМЛ не превышала 1 случая на 100 тыс. населения. С ростом числа больных СПИДом этот показатель увеличился до 1 на 20 тыс. человек. Сегодня прогрессирующая лейкоэнцефалопатия наблюдается у 5% больных СПИДом. Некоторые авторы сообщают о снижении заболеваемости за последнее десятилетие в связи с успешным применением антиретровирусной терапии. Одновременно отмечается увеличение распространённости ПМЛ среди лиц с аутоиммунными заболеваниями, что обусловлено использованием в их лечении агрессивной иммунотерапии.

Причины ПМЛ
Прогрессирующая мультифокальная лейкоэнцефалопатия развивается в результате реактивации полиомавируса JC. Вирус распространён повсеместно. Источником инфекции является человек, заражение происходит воздушно-капельным, алиментарным путём. Подавляющее большинство людей заражаются в детстве, являются здоровыми носителями. В течение жизни вирус находится в латентном состоянии, персистирует в почках, селезёнке, костном мозге. Реактивация возбудителя происходит на фоне резко сниженного иммунитета. В группу риска развития заболевания входят следующие состояния:
- ВИЧ-инфецирование. Протекающая в виде СПИДа ВИЧ-инфекция сопровождается угнетением клеточного иммунитета. Выступает самой частой причиной ПМЛ.
- Гемобластозы. Миелопролиферативные (лейкемия) и лимфопролиферативные (лимфомы) процессы приводят к развитию иммунодефицита.
- Аутоиммунная патология: системная красная волчанка, склеродермия, ревматоидный артрит. Иммунодефицит формируется на фоне активного иммуносупрессивного лечения, особенно препаратами моноклональных антител.
- Наследственные заболевания с иммунодефицитом: синдром Ди Джорджи, Вискотта-Олдрича, атаксия-телеангиэктазия.
- Иммуносупрессия на фоне трансплантации органов.
- Вторичный иммунодефицит в результате цитостатической терапии при онкологических заболеваниях.
Патогенез
Расстройство клеточного иммунитета провоцирует перестройку последовательности ДНК JC-вируса, приводит к его активации. Вирус обладает тропностью к клеточным элементам нейроглии (олигодендроцитам, астроцитам), поражение которых сопровождается разрушением миелина. В результате в веществе головного мозга происходит мультифокальная прогрессирующая демиелинизация с ростом и слиянием очагов поражения. Микроскопически обнаруживается увеличение астроцитов, деформация их ядер, окрашивание олигодендроцитов выявляет ядерные включения — скопления частиц JCV. Первостепенную роль в иммунной антивирусной реакции играют цитотоксические Т-лимфоциты, убивающие инфицированные активным вирусом клетки. Снижение выработки специфических Т-лимфоцитов вследствие иммунодефицита обуславливает развитие ПМЛ.
Симптомы ПМЛ
Дебют заболевания носит подострый (2-3 дня) или постепенный (1-3 недели) характер. На первый план выходит патопсихологическая симптоматика и очаговый неврологический дефицит. В типичном варианте прогрессирующая мультифокальная лейкоэнцефалопатия протекает без свойственных нейроинфекциям общемозговых симптомов, менингеального синдрома. Отмечается изменение поведения, агрессивность, эмоциональная лабильность, подозрительность, прогрессирующее ослабление когнитивной сферы (памяти, мышления, внимания). Очаговый дефицит представлен мышечной слабостью конечностей одной половины тела (гемипарезом), афазией, гемианопсией, атаксией, парестезиями в паретичных конечностях. Вначале гемипарез может отсутствовать, в дальнейшем наблюдается у 75% больных. 20% случаев протекают с пароксизмами эпилепсии. Психические расстройства отмечаются у 38% пациентов. Прогрессирование когнитивного дефицита приводит к деменции.
В редких случаях мультифокальная лейкоэнцефалопатия протекает в атипичной форме. К атипичным вариантам относятся JC-менингоэнцефалит, JC-энцефалопатия, гранулярно-клеточная невропатия. Менингоэнцефалитическая форма характеризуется наличием менингеальных симптомов. При JC-энцефалопатии отсутствует очаговый неврологический дефицит. Клиника гранулярно-клеточного варианта представлена изолированным мозжечковым синдромом.
Диагностика
Прогрессирующая лейкоэнцефалопатия диагностируется специалистами в области неврологии на основании клинических данных, результатов нейровизуализирующего исследования, обнаружения специфической ДНК. Диагностический алгоритм включает:
- Осмотр невролога. В классическом варианте в неврологическом статусе определяется гемипарез, гемигипестезия, шаткость, неустойчивость в позе Ромберга, дискоординация, сенсомоторная афазия, когнитивные нарушения. Наблюдается лабильность психики, психопатологические симптомы, возможно неадекватное поведение.
- Осмотр офтальмолога. У большинства пациентов диагностируют снижение зрения, периметрия выявляет гомонимную гемианопсию.
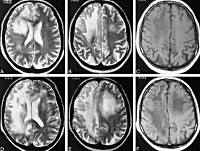
- МРТ головного мозга. Обнаруживается диффузная мультифокальная демиелинизация, очаги имеют различный размер, асимметрично располагаются в белом веществе, таламусе, базальных ядрах.
- ПЦР-исследование. Направлено на выявление ДНК вируса JC в цереброспинальной жидкости, полученной путём люмбальной пункции. Специфичность анализа 90-100%, чувствительность — 70-90%. Проведение антиретровирусной терапии больным СПИДом понижает чувствительность исследования до 58%, отрицательный результат не исключает наличие заболевания.
- Биопсию мозговых тканей. Инвазивная методика, проводится в диагностически затруднительных случаях. Гистологическое исследование образцов церебральных тканей позволяет подтвердить специфические для лейкоэнцефалопатии морфологические изменения.
Лечение ПМЛ
В настоящее время не существует препаратов для лечения прогрессирующей лейкоэнцефалопатии с доказанной эффективностью. Специфическая терапия находится в стадии разработки. Попытки лечения интерфероном, иммуностимуляторами, цитарабином, их комбинациями оказались безрезультатными. Окончились неудачей клинические испытания препарата цидофовир, показывающего анти-JC эффективность на опытах с мышами. Недавно был предложен кардинально новый метод лечения антидепрессантом миртазапином, блокирующим распространение JCV благодаря связыванию рецепторов, через которые вирус инфицирует клетки нейроглии. Способ требует клинических испытаний.
Прогноз и профилактика
Прогрессирующая мультифокальная лейкоэнцефалопатия отличается неуклонно усугубляющимся течением с исходом в кому. Продолжительность жизни варьирует от 1 мес. (острая форма) до 10-12 мес. с момента заболевания. Профилактика подразумевает меры предупреждения инфицирования ВИЧ, осторожное проведение терапии аутоиммунных заболеваний, мониторинг неврологической симптоматики у больных, получающих лечение моноклональными препаратами.
Читайте также:


