Подострый склерозирующий панэнцефалит что это такое
Описание
Панэнцефалит подострый склерозирующий – тяжелое инфекционное невротическое заболевание, с медленно прогрессирующим течением.
В медицине данный вид энцефалита называют несколькими наименованиями: энцефалит с включениями Даусона, лейкоэнцефалит Ван-Богарта, узелковый панэнцефалит Петте-Деринга.

Возбуждает панэнцефалит подострый склерозирующий корьевой вирус в измененной форме или подобный ему, имеющий разрушительное воздействие на клетки и мозговые нейроны, и способность накапливаться в них.
В современной медицине данное заболевание относится к числу самых редко встречающихся на земле болезней. Снижение заболевания происходит из-за массового проведения антикорьевой вакцинации.
Подвергаются поражению данным заболеванием в большинстве случаев, дети в возрастной группе до двух лет после перенесения кори или корьевой краснухи. Латентный период панэнцефалита доится более шести лет.
Симптомы
Симптоматика панэнцефалита подострого склерозирующего является острой. Начинается он резкой сменой настроения, снижением активного познания ребенка, нарушением внимания, невозможностью сконцентрироваться, провалами в памяти, чрезмерной утомляемостью и изменением личности.

Поскольку заболевание относится к разряду прогрессирующих, то с его течением появляются припадки эпилептические, трофические, вегетативные, падает зрение, меняется тонус в мышцах, активно развиваются различные двигательные нарушения.
Эта стадия заболевания может длиться до двенадцати месяцев. Затем начинается вторая стадия болезни, при которой проявляются расстройства экстрапирамидной системы. У пациента начинается тремор конечностей, миоклонические припадки.
Поскольку при панэнцефалите подостром склерозирующем поражается лобная доля коры головного мозга и мозжечка, то среди проявлений можно отметить локомоторную и статическую атаксию.
Третья стадия данного заболевания характеризуется нарастающей мышечной регидностью, структурными мышечными изменениями, появлением спазмов, судорог децеребрального вида. Эта стадия может продолжаться в течение пяти – семи месяцев.
Коматозная стадия панэнцефалита подострого склерозирующего , последняя. Ее проявления – это полное разрушение функций психики пациента, стойкая децеребральная ригидность, общее истощение организма. Все это приводит к смерти.

Поскольку панэнцефалит подострый склерозирующий может протекать в трех формах – острой, хронической и подострой, то от формы течения в прямой зависимости находится продолжительность течения болезни – от полугода до семи лет.
Диагностика
Диагностирование панэнцефалита подострого склерозирующего основывается на результатах анализа сыворотки крови и спинномозговой жидкости. При лабораторном исследовании этих материалов выявляется аномально высокое содержание в них антител, вызванных вирусом кори.
Обязательно проводится электроэнцефалограмма, при которой можно зарегистрировать периодические разряды, которые чередуются с подавлением активности.

Так же для полного уточнения и подтверждения диагноза назначаются магнитно-резонансная и компьютерная томография (при этом выявляются атрофия коры головного мозга, необструктивная гидроцефалия и очаги поражения белого мозгового вещества).
После смерти больного проводится патологоанатомическое исследование, которое помогает увидеть разрушенные мертвые нейроны коры головного мозга, ядерные стволовые образования и подкорковые узлы.
Профилактика
Профилактикой панэнцефалита склерозирующего подострого является своевременная вакцинация и грамотное лечение кори, оспы, полиомиелита, корьевой краснухи, и других вирусных инфекционных заболеваний острого характера.
Так же к профилактическим методам данного заболевания можно отнести и систематическое закаливание организма с раннего детского возраста.
Лечение
На данный момент в медицине не существует методов лечения панэнцефалита подострого склерозирующего .
Большинство случаев хронических энцефалитов у детей развиваются в виде первичных энцефалитов с выявлением этиологических агентов в ЦНС; они формируют гетерогенную группу, которая включает хорошо определенные типы (например, подострый склерозирующий панэнцефалит, краснушный панэнцефалит, энцефалопатия при ВИЧ-инфекции, лимфотропный Т-клеточный вирус, вирусный миелит и прионовые болезни) и плохо понимаемые причины, вероятно, напрямую не связанные с вирусной инфекцией. Механизмы хронического вирусного энцефалита сложны и могут варьировать в зависимости от взаимодействия инфекционного агента с иммунной системой хозяина. Хорошо определенные типы будут описаны ниже.
Подострый склерозирующий панэнцефалит (ПСПЭ) — деструктивное длительно текущее дегенеративное осложнение в результате продолжения абберантной репликации вируса кори в тканях ЦНС после первичной инфекции (Connolly et al., 1967). Возникает приблизительно в двух случаях из 100000 спонтанный инфекций с инкубационным периодом более семи лет; заболевание более характерно для детей, перенесших первичную корь в возрасте до двух лет. По сравнению с вакцинированными детьми уровень встречаемости 1:100000, с инкубационным периодом 3-4 года. Однако большинство случаев ПСПЭ у вакцинированных были вызваны дикими типами невакцинных штаммов кори (Jin et al., 2002, Miller et al, 2004).
Ранняя диагностика сложна из-за слабо прогрессирующих симптомов в течение первой стадии заболевания (Honarmand et al., 2004). В 2/3 случаев наблюдаются тонкие изменения личности и расстройство интеллекта с преобладанием афазии, апраксии и агнозии. Зачастую такие дети страдают от психологических проблем и направляются в психиатрические клиники. У четверти пациентов среди первых проявлений отмечают неврологические признаки и припадки, которые могут быть атоническими, миоклоническими или даже парциальными (Kornberg et al., 1991).
Непроизвольные движения могут появиться через 2-3 месяца и характеризуют начало второй стадии. Движения могут быть в виде миоклонических судорог. Чаще всего они являются сложными, с последовательным участием нескольких сегментов в повторяющихся схемах. Начало каждого движения внезапное, а продолжительность больше, чем при обычных миоклонических судорогах, часто занимая несколько секунд. Патологические движения встречаются периодически, хотя промежутки между двумя приступами не одинаковы и могут варьировать в разные дни у одного и того же пациента. Движения обычно двусторонние, но могут встречаться строго односторонние судороги. Они отсутствуют во время сна и могут исчезать и появляться без видимой причины.
У некоторых пациентов движения могут быть заменены (или предшествовать) периодическими проявлениями, более типичными для эпилепсии, в частности, атоническими судорогами с кивательными движениями головы или полным ее недержанием, или, реже, типичными миоклониями. Генерализованные эпилептические припадки, подобные абсансам приступы или частичные припадки не характерны (Andermann, 1967, Kornberg et al., 1991). В третьей стадии преобладающими становятся экстрапирамидные и/или пирамидные дисфункции или и те, и другие. Могут появляться экстрапирамидные дискинезии и часто паркинсоническая ригидность. Деменция при этом тяжелая, и ребенок оказывается прикованным к постели. В терминальной стадии прогрессирующая иммунологическая толерантность с усилением гипотонии и децеребральной ригидности сопровождается ухудшающимися трудностями при глотании и дыхании и вегетативными нарушениями.
Средняя длительность заболевания — около 12 месяцев, течение обычно постоянно прогрессирующее. Иногда встречаются подострые формы с летальным исходом менее чем через шесть недель (Nihei et al., 1977). И наоборот, можно наблюдать длительные периоды остановки развития. Периоды спонтанной ремиссии могут длиться до нескольких лет (Risk и Haddad, 1979).
Среди зрительных проявлений, главным образом, выделяют хориоретинит с преобладающим поражением макулярной области, с чем может быть связана бледность диска зрительного нерва. Эти симптомы могут появляться за месяцы или даже годы до классических проявлений заболевания (Robb и Watters, 1970). Корковая слепота не характерна, но часто происходит атрофия зрительного нерва. При транзиторном повышении ВЧД может быть обнаружен отек сосочка зрительного нерва. Показания электроретинографии остаются нормальными, а вызванные зрительные потенциалы нарушены.
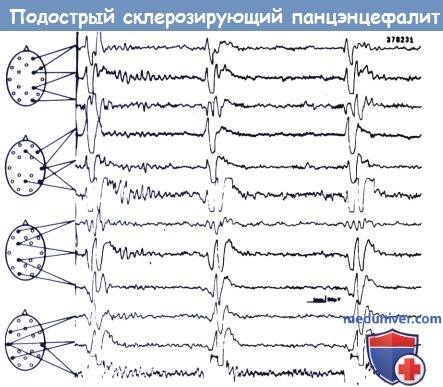
Подострый склерозирующий панэнцефалит: псевдопериодические ЭЭГ комплексы.
Заметно, что комплексы одинаковы в любом отведении.
Случаи с латерализацией или другими очаговыми особенностями могут создать проблемы при диагностике. Развиваются спастическая гемиплегия и односторонние спазмы. Могут ввести в заблуждение проявления в некоторых случаях кортикальной слепоты и гемианопии. Изредка признаки повышенного внутричерепного давления, сопуствующие очаговым изменениям могут ошибочно приниматься за опухолевый процесс (Glowacki и Goscinski, 1973).
Характерные аномалии на ЭЭГ можно обнаружить до любых клинических проявлений (Wulff, 1982). Пароксизмальные ЭЭГ комплексы типично формируются из высоко-вольтажных медленных волн периодически повторяющихся во время клинических судорог. Они, как правило, идентичной формы в любом отведении. Они могут встречаться при отсутствии клинических проявлений и на некоторых стадиях представлены у 80% пациентов.
В некоторых случаях вспышки активности волны потенциала действия могут замещать типичные комплексы. Фоновый рисунок может изначально быть нормальным, но постепенно замедляется с уменьшением амплитуды. Диагноз ПСПЭ подтверждается выявлением высоких титров антител против кори (IgG) в ликворе и плазме крови, с очень высоким соотношением титров антител СМЖ и плазмы крови. В ликворе не обнаруживаются клетки, а общий белок в пределах нормы или несколько повышен. Вирус обычно не выделяется из СМЖ, в то же время вирусный геном может амплифицироваться из ткани мозга.
Результаты КТ, как правило, нормальные в первые недели после начала заболевания. Может отмечаться диффузное набухание мозга со сдавлением желудочков. Редко можно увидеть очаговые снижения плотности. Позднее развивается атрофия мозга и белое вещество внешне выглядит гиподенсивным. На ранних стадиях данные МРТ могут быть в норме или указывать на поражения, обычно асимметрично поражающие корково-подкорковые зоны теменно-затылочных долей.
Со временем симметричные перивентрикулярные изменения белого вещества становятся более заметными, но явной корреляции между клиническими стадиями и результатами МРТ не обнаружено (Ozturk et al., 2002).
Несмотря на многочисленные попытки, удовлетворительного метода для лечения ПСПЭ не разработано. Изопринозин, возможно, способен вызвать ремиссию в некоторых случаях (DuRant et al., 1982). Имеются сообщения о повышении частоты ремиссий с 5-10% до 45% при комбинировании внутрижелудочкового интерферона и изопринозина (Yalaz et al., 1992, Gascon et al., 1993), но после ремиссии в течение нескольких лет могут возникать поздние рецидивы (Anlar et al., 1997).
В небольшом рандомизированном контролируемом исследовании проводилось сравнение использования только отдельно принимаемого перорально изопринозина и комбинации перорального приема изопринозина и внутрижелудочкового интерферона-альфа-2b. При сравнении клинической классификации исходов ни коэффициент выживаемости Каплана-Мейера, ни заболеваемость не показали статистически значимых различий между группами.
Тем не менее, наблюдающийся уровень удовлетворительных исходов (стабилизация или улучшение) около 35% был выше, чем спонтанные ремиссии в 5-10% случаев, указываемых в литературе, что подтверждает эффективность лечения по сравнению с его отсутствием (Gascon, 2003).
Другие комбинации лечения включали использование рибавирина (как внутрижелудочковое, так и внутривенное) с изопринозином (Aydin et al., 2003, Hosoya et al., 2004).
Редактор: Искандер Милевски. Дата публикации: 22.12.2018

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Подострый склерозирующий панэнцефалит (синонимы: лейкоэнцефалит Ван-Богарта, узелковый панэнцефалит Петте-Деринга, энцефалит с включениями Даусона).
Код по МКБ-10
А81.1. Подострый склерозирующий панэнцефалит.
Эпидемиология подострого склерозирующего панэнцефалита
Возраст заболевших составляет от 4 до 20 лет, преобладают лица мужского пола. Основным профилактическим мероприятием служит вакцинация против кори. У привитых частота подострого склерозирущего панэнцефалита снижается в 20 раз.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12], [13], [14], [15], [16]
Что вызывает подострый склерозирующий панэнцефалит?
Подострый склерозирущий панэнцефалит вызывается вирусом кори, который был обнаружен в мозговой ткани больных. Таким энцефалитом болеют дети и подростки, перенёсшие корь в первые 15 мес жизни. Заболеваемость составляет 1 случай на 1 млн населения.
Патогенез подострого склерозирующего панэнцефалита
Симптомы подострого склерозирующего панэнцефалита
Инкубационный период подострого склерозирующего панэнцефалита от 3 до 15 лет и дольше. Подострый склерозирующий панэнцефалит развивается обычно в возрасте от 4 до 20 лет. Неврологический статус характеризуется двигательными нарушениями в виде гиперкинезов, изменений мышечного тонуса, трофическими нарушениями, вегетативными расстройствами и эпилептическими припадками. Наряду с этим развивается быстро прогрессирующее слабоумие.
Выделяют 4 стадии заболевания.
- I стадию (длится 2-3 мес) характеризует недомогание, эмоциональная лабильность, неврозоподобные симптомы подострого склерозирующего панэнцефалита в виде повышенной раздражительности, тревожности, а также нарушения сна. У больного меняется поведение (уходы из дома, психопатоподобные реакции). К концу этой стадии нарастает сонливость, выявляют расстройства речи (дизартрию и афазию); нарушения координации движений - апраксию, расстройства письма - аграфию, агнозию, постепенно снижается уровень интеллекта, прогрессирует утрата памяти.
- II стадия болезни проявляется разными формами гиперкинезов в виде подёргиваний всего туловища, головы, конечностей, миоклонии. Затем к этим расстройствам присоединяются генерализованные эпилептические припадки и пирамидная симптоматика. Появляются следующие симптомы подострого склерозирующего панэнцефалита: диплопия, гиперкинезы, спастические параличи, больной перестаёт узнавать предметы, возможна потеря зрения.
- III стадию болезни (6-8 мес от начала болезни), характеризуют прежде всего тяжёлые нарушения дыхания, глотания, гипертермия и непроизвольные крик, плач, смех.
- IV стадия: присоединяются такие симптомы подострого склерозирующего панэнцефалита, как опистотонус, децеребрационная ригидность, сгибательные контрактуры, а также слепота.
В финале болезни больной впадает в коматозное состояние, появляются трофические расстройства. Болезнь заканчивается летальным исходом, который наступает не позднее 2 лет от её начала. Хронические формы более редки. В этих случаях в течение 4-7 лет выявляют разные формы гиперкинезов нарастающей тяжести и явления слабоумия.
Примерные сроки нетрудоспособности - со времени манифестации болезни.

[17], [18], [19]
Подострый склерозирующий панэнцефалит — медленная инфекция, вызванная вирусом кори. Латентный период составляет до 8 лет. Подострый коревой панэнцефалит дебютирует расстройствами личности и поведения, затем появляются прогрессирующие мышечно-тонические, двигательные, зрительные, когнитивные нарушения, пароксизмальные состояния. Основные методы диагностики: электроэнцефалография, КТ/МРТ головного мозга, анализ цереброспинальной жидкости, выявление антител к кори в крови, ликворе. Этиотропная терапия осуществляется антивирусными фармпрепаратами, симптоматическое лечение проводится противоэпилептическими средствами.
МКБ-10
Общие сведения

Причины ПСП
Патология является классической медленной инфекцией ЦНС. Инфекционным агентом выступает вирус кори, сохраняющийся в организме в персистирующем состоянии после перенесённой естественной коревой инфекции. В большинстве случаев ПСП наблюдается у детей, переболевших корью в возрасте до двух лет. Латентный период продолжается 6-8 лет, по истечении которых развивается быстро прогрессирующий коревой панэнцефалит. Факторы, обуславливающие вирусную персистенцию, остаются неизвестными. Отдельные авторы предполагают, что в основе лежит изменённая иммунологическая реактивность организма, обуславливающая неполную элиминацию вируса.
Патогенез
Этиопатогенетические механизмы не изучены, вызывающие активацию вируса триггеры не определены. После многолетнего латентного периода персистирующие в церебральных клетках вирусы кори начинают активную репликацию, что обуславливает тотальные воспалительные изменения тканей головного мозга — подострый панэнцефалит. В воспалительный процесс вовлекаются белое вещество, подкорковые ганглии, кора, мозговые оболочки. Очаги поражения распределяются неравномерно, в них происходит гибель нейронов, компенсаторно разрастается глиальная ткань. На поздних стадиях склерозирующий панэнцефалит характеризуется диффузной демиелинизацией в сочетании с глиозом. Микроскопически в поражённых нейронах обнаруживаются специфические включения. Исследование при помощи меченых антител выявляет в них наличие антигенов коревого вируса.
Классификация
Клиническая симптоматика ПСП весьма вариабельна, однако у всех пациентов прослеживается стадийное течение. Понимание фазы заболевания имеет клиническое и прогностическое значение, в связи с чем подострый склерозирующий панэнцефалит классифицируют на 4 основные стадии:
- I стадия (начальная, психотическая) характеризуется нарастающими изменениями в характере, поведении, интеллектуальных способностях больного. До появления мышечно-тонических нарушений часто ошибочно диагностируется как психиатрическая патология. Продолжается 2-12 месяцев.
- II стадия начинается с появления двигательных расстройств (гиперкинезов), пароксизмальных эпизодов (судорожных приступов, абсансов, атонических падений). В дальнейшем присоединяется различная неврологическая симптоматика. Стадия продолжается 6-12 месяцев.
- III стадия протекает с быстрым прогрессированием деменции, нарастанием мышечной ригидности, ослаблением судорожного синдрома. Длится несколько месяцев.
- IV стадия (терминальная, коматозная) — полный распад психических функций, децеребрационная ригидность, кахексия. Пациенты впадают в кому с последующим летальным исходом.
Симптомы ПСП
Подострый склерозирующий панэнцефалит дебютирует постепенно усугубляющимися отклонениями в поведении: больной становится неряшлив, упрям, агрессивен, раздражителен, равнодушен к окружающим. Начинают преобладать примитивные качества: жадность, эгоизм. Появляются психопатоподобные реакции, нарушения сна, у школьников возникают сложности в обучении. К концу начального периода наблюдаются прогрессирующие мнестические расстройства, интеллектуальное снижение, нарушения речи (дизартрия, афазия).
Постепенно гиперкинезы сменяются симптоматикой паркинсонизма, смешанные изменения тонуса переходят в тотальную ригидность. Экстрапирамидные расстройства сочетаются с вегетативной симптоматикой: повышенной сальностью кожи, гипергидрозом, лабильностью давления, гиперсаливацией. Нарастающая децеребрационная ригидность приводит к постепенному исчезновению судорожных пароксизмов. Отмечается полный распад личности, насильственный смех/плач, гипертермические кризы, расстройства глотания, дыхания. В терминальной стадии конечности пациента согнуты, имеются сгибательные контрактуры, продуктивный контакт отсутствует, угнетение сознания доходит до стадии комы, возникают трофические изменения тканей.
Осложнения
Прогрессирование зрительных нарушений приводит к амаврозу. Лежачее положение больного на последних стадиях ПСП может вызвать образование пролежней. Инфицирование последних ведёт к местным воспалительным изменениям, попадание инфекции в кровоток — к возникновению сепсиса. Обездвиженность пациента, дыхательные расстройства центрального генеза способствуют возникновению застойной пневмонии. Дисфагия опасна попаданием пищи в дыхательные пути с развитием аспирационной пневмонии. Перечисленные инфекционные осложнения выступают наиболее частыми причинами гибели больных.
Диагностика
Полиморфизм, неспецифичность симптоматики, изолированные психотические проявления начального периода, редкая встречаемость обуславливают позднее диагностирование заболевания. В ходе диагностики невролог опирается на анамнестические сведения о перенесённой в детстве кори, изменения неврологического статуса, данные ЭЭГ и нейровизуализации, результаты исследований на противокоревые антитела. Биопсия головного мозга не показательна, поскольку мозаицизм церебрального поражения делает возможным забор материала из неизменённого участка мозговых тканей. Перечень необходимых дополнительных обследований включает:
- Электроэнцефалографию. Типична картина повышенной медленноволновой активности, возникающая с интервалом 6-8 с и чередующаяся с периодами сниженной биоэлектрической активности. Регистрируемые комплексы носят двусторонний характер, симметричны, синхронны.
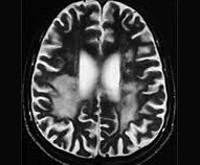
- Нейровизуализацию. Проводится методами компьютерной или магнитно-резонансной томографии. МРТ, КТ головного мозга диагностируют диффузное множественное поражение церебральных тканей, атрофические изменения коры, в ряде случаев — гидроцефалию. Изменения в белом веществе наблюдаются спустя 4 месяца от дебюта ПСП. В 50% случаев поражения базальных ганглиев определяются уже на 2-ой стадии.
- Исследование цереброспинальной жидкости. Ликвор для анализа получают путём люмбальной пункции. Исследование выявляет умеренное повышение концентрации белка со значительным нарастанием относительного содержания гамма-глобулинов, наличие специфических олигоклональных IgG. Резкое нарастание титра антикоревых антител свидетельствует о коревой этиологии поражения.
- Анализ крови на противокоревые антитела. Определяет повышение антител в сыворотке до 1:4 — 1:128. В норме титр составляет 1:200 – 1:500. Выявление повышенного титра в крови и цереброспинальной жидкости является важнейшим диагностическим признаком.
Выделение вируса кори из поражённых тканей мозга редко применяется в клинической практике по причине сложности выполнения. В начальной стадии подострый склерозирующий панэнцефалит необходимо дифференцировать от психических расстройств: неврастении, шизофрении, истерии. В последующем дифдиагноз осуществляется с опухолью головного мозга, прогрессирующим краснушным панэнцефалитом, клещевым энцефалитом, болезнью Крейтцфельдта-Якоба.
Лечение ПСП
Специфическая терапия не разработана. Большое значение имеет правильный уход за больным, предупреждение инфекционных осложнений. Проводится этиотропное лечение противовирусными средствами (рибавирин, инозин пранобекс), препаратами интерферона, но оно малорезультативно. В качестве симптоматической терапии назначают антиконвульсанты, эффективные в отношении миоклоний (диазепам, производные вальпроевой кислоты). Для снятия спастического гипертонуса применяют миорелаксанты (толперизон, баклофен). Нарушения дыхания на заключительных стадиях заболевания являются показанием к переводу пациентов на ИВЛ. Тщательный уход и симптоматическое лечение позволяют продлить жизнь больного.
Прогноз и профилактика
В 80% случаев подострый склерозирующий панэнцефалит имеет длительность 1-3 года и приводит к летальному исходу. У 10% пациентов наблюдается молниеносное течение. В 10% случаев удаётся увеличить продолжительность жизни больного, иногда до 10 лет. Наилучшими превентивными мерами, позволяющими предупредить возникновение ПСП, являются мероприятия по предупреждению заболевания корью. Специфическая профилактика проводится путём плановой вакцинации против кори детей в возрасте 12 месяцев.
Подострый склерозирующий панэнцефалит
Син.: подострый энцефалит Даусона, инклюзионный панэнцефалит Петте – Деринга, подострый склерозирующий лейкоэнцефалит Ван-Богарта
Подострый склерозирующий панэнцефалит (ПСПЭ) – медленная, всегда смертельная вирусная инфекция, характеризующаяся прогредиентным поражением ЦНС с неуклонно прогрессирующим снижением интеллекта и двигательными расстройствами.
Эпидемиология. Подострый склерозирующий панэнцефалит – редкое заболевание, встречается с частотой 0,2 случая на 1 000 000 популяции в целом и 1 случай на 1 000 000 детей. Абсолютно точных данных о распространенности и частоте заболевания нет из-за трудности диагноза и всеобъемлющей регистрации. Считается, что мужчины болеют чаще женщин (соотношение 1:2—4), что около 85 % случаев ПСПЭ выявляется в сельской местности, что средний возраст заболевших составляет 5—15 лет с колебаниями от 1 года до 58 лет и более. В целом надо признать, что эпидемиология этого заболевания изучена пока недостаточно.
Патогенез и патологоанатомическая картина. В патогенезе ПСПЭ, несмотря на значительный прогресс в его изучении, за последние 15—20 лет остается много неясного и дискуссионного. Центральным и бесспорным обстоятельством является факт пожизненной персистенции вируса кори в организме перенесшего коревую инфекцию (в лимфатических узлах, органах, богатых лимфоидной тканью, и в клетках ЦНС). Наименее изучен жизненный цикл возбудителя в клетках головного мозга. О.Г. Анджапаридзе и Н.Н.Богомолова (1983) считают, что в патогенезе ПСПЭ большое значение имеет слабовыраженная, но постоянная антигенная стимуляция иммунокомпетентных клеток, которая приводит к гиперпродукции антител, которые в свою очередь нейтрализуют поверхностные вирусспецифические белки, но сохраняют при этом недоступность клетки для цитотоксических лимфоцитов или иммунного лизиса комплементом.
При патологоанатомическом вскрытии выявляются отек головного мозга, признаки дегенерации нейронов и их выпадение, практически во всех отделах головного мозга – пролиферативные реакции глии и мезенхимально-глиальной реакции сосудов, что морфологически описывается как склерозирующий панэнцефалит. В сером веществе происходит демиелинизация волокон. Именно в сером веществе головного мозга развиваются первичные поражения, изменения в белом веществе считаются вторичными.
Клиническая картина. Интервал между перенесенной корью и развитием ПСПЭ составляет в среднем 6—8 лет. Ранние признаки ПСПЭ абсолютно неспецифичны: недомогание, снижение аппетита до анорексии, головокружения, головные боли.
Выделяют 4 стадии развития заболевания. В первой стадии ребенок или подросток становится раздражительным, забывчивым, плохо воспринимает новые знания и плохо их воспроизводит, постепенно утрачивая всякую способность к обучению – развиваются симптомы расстройства умственной деятельности. У взрослых больных ослабляется память, развивается безразличие к окружающему, к людям, даже самым близким, могут появляться странности в поведении.
Во второй стадии к этим симптомам присоединяются двигательные расстройства в виде пирамидных и экстрапирамидных нарушений. Появляются и прогрессируют афазия (расстройства речи), аграфия (нарушение письма), диплопия, атаксия (дискоординация сложных двигательных актов), нарушается походка. Возможны клинический тремор конечностей, судорожные подергивания мышц.
Третья стадия характеризуется усугублением мозговых расстройств вплоть до спастических парезов и гиперкинезов, агнозии, слепоты, недержания мочи, хореоатетоза.
В четвертой стадии развиваются кахексия и мозговая кома.
Общая продолжительность заболевания около 3 лет, у взрослых благодаря ремиссиям иногда достигает 7—8 лет, у детей, напротив, течение ПСПЭ еще более трагично: почти половина из них умирают в течение года с момента появления первых признаков заболевания.
Прогноз. ПСПЭ – абсолютно смертельное заболевание, как и все другие медленные инфекции.
Диагностика. Распознавание болезни затруднено. Появление описанной симптоматики расстройств умственной, психической деятельности и двигательных нарушений требует проведения электроэнцефалографии. На ЭЭГ при ПСПЭ периодически регистрируются широкие волны высокого вольтажа, которые появляются через 3,5—20 с и обычно совпадают с приступами миоклонических судорог. Выявление такого рода изменений служит показанием к серологическому обследованию для определения уровня противокоревых антител в сыворотке крови и цереброспинальной жидкости. Они необычайно высоки и, как правило, превышают титры антител при естественной коревой инфекции и тем более у привитых противокоревой вакциной. В сыворотке крови титры антител достигают 1:16000 и более, а в цереброспинальной жидкости —1:124—1:248.
Лечение. Применяют лейкоцитарный интерферон в возрастающих дозах с внутрижелудочковым его введением в течение 6 мес. У единичных больных удается достигнуть ремиссии, однако улучшение состояния всегда оказывается временным.
В стратегическом плане важны сведения о том, что абсолютное большинство больных ПСПЭ перенесли корь в очень раннем возрасте, в среднем в 15 мес жизни, реже – в возрасте до 1 года.
Данный текст является ознакомительным фрагментом.
Читайте также:


