Возбудитель ботулизма токсинообразование типы токсина
Глава 36. Возбудитель ботулизма
Clostridium botulinum (от лат. botulus - колбаса) были открыты Ван-Эрменгеном в 1896 г. Выделены они были из ветчины, послужившей причиной массового отравления.
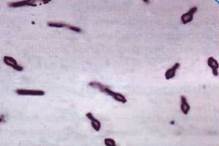
Морфология. Возбудители ботулизма - палочки размером 4-9 × 0,6-1 мкм с закругленными концами. Палочки полиморфны: встречаются короткие формы и длинные нити. Возбудители ботулизма образуют споры, располагающиеся субтерминально. Споры шире палочки и поэтому палочка со спорой имеют вид теннисной ракетки. С. botulinum не имеют капсул. Подвижны - перитрихи. Молодые культуры окрашиваются грамположительно.
Культивирование. С. botulinum - строгие анаэробы. Растут при температуре 25-37° С и рН среды 7,3-7,6. Культивируют их на казеиновых, мясных и других средах. На глюкозокровяном агаре микробы дают неправильной формы колонии с нитевидными отростками. В агаре столбиком колонии напоминают комочки ваты, иногда колонии имеют вид чечевичных зерен. На кровяном агаре в чашках Петри вырастают колонии в виде росинок с блестящей поверхностью и ровными или изрезанными краями (R-форма). На печеночном бульоне клостридии растут с образованием мути и последующим выпадением осадка, при этом бульон просветляется.
Ферментативные свойства (см. табл. 51). Сахаролитические свойства: расщепляют лактозу, глюкозу, мальтозу и глицерин с образованием кислоты и газа. Протеолитические свойства: расплавляют кусочки печени, расщепляют яичный белок, разжижают желатин, пептонизируют молоко, образуют сероводород и аммиак.
Токсинообразование. С. Botulinum продуцируют яд, самый сильный из всех биологических токсинов (в 1 мкг ботулинического токсина содержится 100000000 смертельных доз для белой мыши). Токсин состоит из двух компонентов: нейротоксина и гемагглютинина.
Антигенная структура. По антигенным свойствам нейротоксина все штаммы делят на семь сероваров: А, В, С, D, E, F и G. Каждый серовар характеризуется специфической иммуногенностью. Наиболее частой причиной заболевания ботулизмом являются токсины сероваров А, В и E, реже встречаются заболевания, вызываемые сероварами С, D и F. Токсины серовара G мало изучены.
Устойчивость к факторам окружающей среды. Вегетативные формы C. botulinum погибают при 80° С через 30 мин. Споры устойчивы. Они выдерживают кипячение в течение нескольких часов (до 5 ч). В больших кусках мяса, консервных банках большой емкости споры сохраняются даже после автоклавирования. В 5% растворе фенола споры сохраняются сутки. Ботулинический экзотоксин выдерживает кипячение в течение 10 мин. Он устойчив к действию солнечного света, низким температурам и к дезинфицирующим веществам.
Восприимчивость животных. К возбудителям ботулизма чувствительны мелкий и крупный рогатый скот, лошади, грызуны и птицы. Из экспериментальных животных чувствительны белые мыши, морские свинки, кролики, кошки.
Источники инфекции. Возбудители ботулизма широко распространены в природе: почве, воде, куда они попадают с фекалиями животных и рыб. В почве C. botulinum живут и размножаются. Человек заражается при употреблении продуктов, содержащих возбудителей и экзотоксин.
Пути передачи. Пищевой (при употреблении в пищу зараженных мясных, овощных и рыбных консервов, грибов, осетровых рыб и т. д.). Особенно опасны консервированные продукты, приготовленные в домашних условиях.
Патогенез. Входные ворота - слизистая оболочка кишечного тракта. Нейротоксин, образующийся при размножении вегетативных форм возбудителей ботулизма, не чувствителен к протеолитическим ферментам желудочно-кишечного тракта. Патологический процесс обусловливается нейротоксином, который через кишечник всасывается в кровь, разносится по всему организму, поражая центральную нервную систему. В основном поражаются: клетки (ядра) продолговатого мозга, сердечно-сосудистая система. У больных отмечают изменения со стороны органов зрения, расстройство дыхательных и глотательных функций.
Иммунитет. Естественной резистентности нет. Человек высокочувствителен к токсину C. botulinum. Перенесенное заболевание не оставляет иммунитета.
Профилактика. Предупреждение возможности загрязнения пищевых продуктов, правильная технология производства изготовления консервов и других продуктов. Профилактика ботулизма в быту: продукты домашнего консервирования перед употреблением следует кипятить в водяной бане (или кастрюле) в течение 15-20 мин.
Специфическая профилактика и лечение. Людям, употреблявшим продукты, где возможно содержится возбудитель ботулизма или ботулинический токсин, вводят противоботулиническую поливалентную антитоксическую сыворотку типов А, В, Е. После установления типа токсина вводят противоботулиническую сыворотку того типа, который соответствует типу выделенного штамма.
Цель исследования: обнаружение C. botulinum, ботулинического токсина, определение серовара.

Ботулизм - пищевая токсико-инфекционная болезнь, характеризующаяся поражением центральной нервной системы и парезами двигательной мускулатуры, прежде всего глотки, языка и нижней челюсти.
Токсигенность. Ботулизм возникает в результате поступлении в желудочно-кишечный тракт с пищей токсина C. botulinum. Раневой ботулизм. Токсины C. botulinum состоят из нескольких токсических факторов: нейротоксина, гемолизина, липазы и протеазы. Из них основным токсином для всех типов возбудителя, который имеет решающее значение в интоксикации организма, является нейротоксин. Протеолитические ферменты желудочно-кишечного тракта не разрушают токсины типа A, B, C, F, G и усиливают активность токсина типа Е. Усиление токсина типа Е под действием протеолитических ферментов объясняется тем, что он в основном вырабатывается микробной клеткой в виде протоксина.
Все шесть серологических типов экзотоксина обладают иммунологической специфичностью, выявляемой в реакции нейтрализации. Специфичность токсинов типов А, В и Е очень высока, С и D несколько ограничена. Токсины этих двух типов не нейтрализуются антитоксинами А, В и Е, но небольшие дозы токсинов С и D перекрестно нейтрализуются большими количествами антитоксинов D и С.
Патогенез. Ботулинический токсин передается не только через пищу, но и через воду. Водный путь передачи ботулинического токсина характерен для птиц. Известны многочисленные случаи массового заболевания и гибели водоплавающих птиц в природных условиях во всех частях света от ботулинического токсина типа С, который образуется в стоячей воде, где имеются гниющие растительные остатки или трупы павших животных.
При наличии соответствующих условий анаэробиоза, влажности и тепла C. botulinum активно размножается в органических субстратах с продукцией токсина.
В патогенезе ботулизма большое значение имеет феномен Беринга, который заключается в многократном повышении чувствительности животных к повторному поступлению в организм ботулинического токсина в небольших дозах. При этом животные погибают от небольших доз токсина.
Попавший в желудочно-кишечный тракт токсин при кислой реакции среды сохраняется в его верхних отделах 18…20 ч, не снижая своей активности. Из пищеварительного тракта он поступает в кровь, где его обнаруживают на второй-третий день и позже после проявления болезни, что указывает на образование его в организме. Циркуляция токсина в крови длится 24…48 ч. При этом поражается эндотелий капилляров и токсин проникает в клетки организма, прежде всего, вызывая повреждение моторных центров передних рогов спинного и продолговатого мозга, что является причиной развития паралитического синдрома.
Клинические признаки. Инкубационный период при ботулизме длится от нескольких часов до 2…3 недель и зависит от первоначальной дозы токсина, поступившего в организм с кормом, и сопротивляемости организма, но обычно он составляет 12…48 ч. Чем больше токсина имелось в корме, тем короче инкубационный период и острее течение болезни.
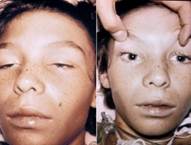
Характерными признаками заболевания ботулизмом являются прогрессирующая слабость, нарушение иннервации мышечной системы, особенно бульбарной (относящийся к продолговатому мозгу) паралич: паралич жевательного и глотательного аппарата. Аппетит и жажда у больных сохраняются. Нередко отмечается паралич языка и нижней челюсти, Наблюдаются расстройство зрения, слюнотечение, нарушение секреторной и моторной функций желудочно-кишечного тракта. Температура тела больных обычно нормальная или субнормальная. При остром течении болезни летальность достигает 90 %.
В зависимости от количества токсина, попавшего в организм животного, болезнь протекает молниеносно, остро и хронически. Диагностировать молниеносную форму болезни очень трудно — ввиду отсутствия характерных признаков болезни.
Острое течение болезни длится 2…3 суток. При этом наиболее четко выражен симптомокомплекс болезни, особенно паралич языка, который торчит изо рта или свободно висит при опущенной парализованной нижней челюсти. Хроническое течение болезни, которое нередко отмечается у лошадей, длится 10 и более дней и характеризуется параличом языка и глотки. Основные признаки болезни — затрудненность движений и неуверенность походки.
Возбудитель ботулизма широко распространен в природе и часто обнаруживается в почве, силосе, в иле водоемов, на корнеплодах, на фруктах и овощах. Являясь нормальными обитателями кишечника млекопитающих (теплокровных животных, человека) и рыб (особенно осетровых), клостридии ботулизма с испражнениями выделяются в почву и воду, где длительно сохраняются в виде спор. Отсюда возможно попадание микробов в сырье животного и растительного происхождения, используемое для приготовления различных консервов.
Споры возбудителя, попадающие в консервы с частицами почвы, при недостаточной термической обработке в условиях герметизации прорастают и выделяют токсин. Очень большую опасность для заражения представляют пластинчатые и трубчатые грибы, так как полное освобождение их от частиц почвы затруднено из-за особенностей строения шляпок.
Человек заболевает при употреблении пищи, содержащей токсин и живых микробов, с размножением которых количество токсина увеличивается. Продукты, послужившие причиной отравления, могут быть различными. В основном это растительные консервы, особенно с низкой кислотностью, сырокопченые окорока, мясные и рыбные сла-бозасоленные, вяленые и копченые продукты.
Для предупреждения возникновения ботулизма на пищевых предприятиях следует строго выполнять санитарно-гигиенические правила, не допускать обсеменения пищевых продуктов возбудителем.
В консервном производстве необходимо строго соблюдать технологические режимы стерилизации. Все подозрительные продукты перед их употреблением необходимо подвергать тепловой обработке.
Отравление через продукцию промышленного производства -редкое явление. Известны случаи ботулизма при употреблении консервов (фруктовых, овощных, грибных) домашнего изготовления, а также рыбных продуктов домашнего приготовления. БАЙКАЛЬСКИЙ ОМУЛЬ.
Ботулизм— острое инфекционное заболевание, характеризующееся интоксикацией организма с преимущественным поражением центральной нервной системы. Болезнь возникает в результате употребления пищевых продуктов, содержащих токсины Clostridium botulinum.
Таксономия. Возбудитель ботулизма относится к отделу Firmicutes, роду Clostridium.
Морфологические и тинкториальные свойства. C.botulinum — грамположительные палочки с закругленными концами, образуют споры и имеют вид веретена. Капсулой не обладают, перитрихи.
Культуральные свойства. Строгий анаэроб. Оптимальными для его роста являются температура 30С. На кровяном агаре образует небольшие прозрачные колонии. В столбике сахарного агара можно обнаружить R-формы формы зерен чечевицы и S-формы – пушинок.
Биохимическая активность. Выделяют 4 группы: бактерии I группы – выраженные протеолитические свойства, гидролизуют желатину, ферментируют глк. и мальтозу; II группы – проявляют сахаролитическую активность, протеолитической – нет. III группа – проявляют липазную активность, гидролизуют желатину. VI – гидролизуют желатину, не проявляют сахаролитических свойств.
Все типы образуют желатиназу, лецитиназу, H2S.Бактерии типа А, В, Е, F – ферментируют глк., фруктозу, мальтозу, сахарозу. Типа С,D – глк, мальтозу.
Антигенные свойства. Имеются группоспецифические жгутиковые – Н и типоспецифические О-АГ бактерий, не проявляющие токсических свойств. По структуре экзотоксинов бактерии разделяют на 8 сероваров: А, В, С1,С2, D, E, F и G.
Факторы патогенности. Выделяет экзотоксин, самый сильный из всех биологических ядов. Ботулинический экзотоксин обладает нейротоксическим действием. Его особенностью является высокая устойчивость к нагреванию (сохраняется в течение 10—15 мин при 100 °С), к кислой среде, высоким концентрациям поваренной соли, замораживанию, пищеварительным ферментам.
Резистентность. Споры обладают очень большой резистентностью к высокой температуре (выдерживают кипячение в течение 3—5 ч).
Эпидемиология. Широко распространен в природе. Его обнаруживают в организме животных, рыб, откуда он попадает в почву и воду. В почве C.botulinum долгое время сохраняется в виде спор и даже может размножаться, что позволяет отнести ботулизм к сапронозным инфекциям. Из почвы возбудитель попадает в пищевые продукты и при наличии анаэробных условий размножается там и выделяет экзотоксин. Путь заражения ботулизмом — пищевой. Чаще всего фактором передачи этой инфекции являются консервы (как правило, домашнего приготовления) — грибные, овощные, мясные, рыбные.
Патогенез. Ботулинический токсин попадает с пищей в ЖКТ. Устойчивый к действию пищеварительных ферментов и хлористоводородной кислоты, токсин всасывается через стенку кишечника в кровь и обусловливает длительную токсинемию. Токсин связывается нервными клетками и блокирует передачу импульсов через нервно-мышечные синапсы. В результате развивается паралич мышц гортани, глотки, дыхательных мышц, что приводит к нарушению глотания и дыхания; наблюдаются изменения со стороны органа зрения.
Клиника. Инкубационный период продолжается от 6—24 ч до 2—6 дней и более. Чем короче инкубационный период, тем тяжелее протекает болезнь. Обычно болезнь начинается остро, но температура тела остается нормальной. Возможны различные варианты ботулизма — с преобладанием симптомов поражения ЖКТ, зрения, глотания, речи или дыхательной функции. В первом случае болезнь начинается с появления сухости во рту, тошноты, рвоты, поноса, во втором — начальные проявления болезни связаны с нарушениями со стороны зрения (снижение остроты зрения, двоение). В результате паралича мышц гортани появляется осиплость, а затем голос пропадает.
Иммунитет. После перенесенной болезни иммунитет не формируется. Однако введение ботулинических анатоксинов создает прочный искусственный вариантоспецифический антитоксический иммунитет.
Микробиологическая диагностика. Исследуют промывные воды желудка, рвотные массы, остатки пищи, кровь. Применяют бактериологический метод, биологический (реакцию нейтрализации токсина антитоксином), с помощью реакции обратной непрямой гемагглютинации, и серологический (РПГА) методы, позволяющие выявить в исследуемом материале ботулинический токсин.
Лечение. Антитоксические противоботулинические гетерологичные сыворотки и гомологичные иммуноглобулины.
Профилактика. Соблюдение правил приготовления продуктов, домашних консервов. Для специфической активной профилактики ботулизма разработаны и применяются по показаниям тетра- и трианатоксины, в состав которых входят ботулинические анатоксины типов А, В и Е. Для экстренной пассивной профилактики используют противоботулинические антитоксические сыворотки.
Не нашли то, что искали? Воспользуйтесь поиском:
С. botulinum — довольно крупные полиморфные палочки с закругленными концами, длиной 4—9 мкм, диаметром 0,5—1,5 мкм, иногда образуются укороченные формы; располагаются беспорядочно, иногда парами или в виде коротких цепочек; в старых культурах могут образовывать длинные нити; грамположительны, подвижны, имеют перитрихиальные жгутики. Капсулы не образуют, споры овальные, располагаются субтерминально, придавая палочке форму, напоминающую теннисную ракетку (рис. 106). Споры в культурах появляются через 24—48 ч от начала инкубации. С. botulinum не размножается в продуктах при кислой реакции (рН 3,0—4,0) и при концентрации NaCl выше 10 %.
С. botulinum образует 8 типов токсинов: А, В, Cl, C2, D, E, F, G, различающихся по антигенной специфичности.
Структура, активация, механизм действия ботулотоксина.
С. botulinum может продуцировать несколько типов токсических комплексов. Функции нетоксических негемагглю-тинирующих, как и гемагглютинирующих белков (их идентифицировано три типа: 15 кД, 35 кД и 70 кД), пока не установлены.
Нейротоксические компоненты любого серотипа ботулинических токсинов и любого типа токсического комплекса имеют сходную структуру и биологические свойства. Они синтезируются в виде единой полипептидной цепи с м. м. 150 кД (7S-токсин), которая не обладает значительной токсической активностью. Эта полипептидная цепь превращается в активный нейротоксин только после ее разрезания бактериальной протеазой или протеазами кишечного тракта человека. В результате точечного гидролиза возникает структура, состоящая из двух связанных между собой дисульфидными связями цепей — тяжелой, с м. м. 100 кД (Н-цепь), и легкой, с м. м. 50 кД (L-цепь). Н-цепь ответственна за прикрепление нейротоксина к рецепторам мембраны клеток, а L-цепь осуществляет специфическое блокирующее действие нейротоксина на холинергическую передачу возбуждения в синапсах.
Ботулизм, патогенез, микробиологическая диагностика
Особенности патогенеза и клиники. Ботулизм протекает как токсикоинфекция. Организм поражается не только токсином, содержащимся в пищевом продукте, но и токсином, который образуется в пищеварительном тракте и тканях в связи с проникновением туда возбудителя. Люди чрезвычайно чувствительны к ботулиническим токсинам типов А, В, С, Е и F. Заболевания наблюдались даже тогда, когда человек брал в рот зараженный продукт, но не проглатывал его. Смертельная доза токсина для человека составляет 1 нг/кг массы тела. Ботулинический токсин быстро всасывается в желудке и кишечнике, проникает в кровь и избирательно действует на ядра продолговатого мозга и ганглиозные клетки спинного мозга. Следует отметить, что, попадая в пищеварительный тракт человека или животного, клостридии ботулизма размножаются, проникают в кровь и оттуда во все органы, продуцируя при этом токсины. Инкубационный период у людей варьирует от двух часов до 10 дней, но чаще всего он составляет 18—24 ч. Чем больше инфицирующая доза, тем короче инкубационный период и тем тяжелее протекает заболевание.
Лабораторная диагностика. Материалом для исследования служат: от больного — промывные воды желудка, испражнения, кровь, моча, рвотные массы; от трупа — содержимое желудка, тонких и толстых кишок, лимфатические узлы, а также головной и спинной мозг. Исследованию подвергают и продукт, послуживший причиной отравления. Исследования проводят с целью обнаружения и идентификации С. botulinum или, чаще всего, с целью обнаружения ботулинического токсина и установления его серотипа. Для выделения культуры С. botulinum материал засевают на плотные среды и накопительную среду Китта—Тароцци (часть пробирок при этом прогревают при температуре 85 °С в течение 20 мин для уничтожения неспорогенных бактерий). Из жидких культур после инкубирования делают посевы на плотные среды с целью получения изолированных колоний, а затем и чистых культур, которые идентифицируют по морфологическим, культуральным, биохимическим и токсигенным свойствам. Для обнаружения ботулинического токсина в исследуемом материале или в фильтрате полученной культуры можно использовать следующие три способа.
1. Биологическая проба на мышах. Для этого берут не менее 5 мышей. Одну из них заражают только исследуемым материалом, а каждую из остальных четырех — смесью материала с 200 АЕ антитоксической сыворотки соответствующего типа — А, В, С и Е. Смесь при комнатной температуре выдерживают 40 мин для нейтрализации токсина антитоксином. При наличии в исследуемом материале ботулинического токсина погибают все мыши, кроме той, которой была введена смесь материала с антитоксической сывороткой, нейтрализовавшей действие гомологичного типа токсина.
2. Использование РПГА с антительным диагностикумом, т. е. эритроцитами, сенсибилизированными антитоксинами соответствующих типов.
3. Высокочувствительный и специфический метод обнаружения ботулинического токсина основан на его способности подавлять активность фагоцитов. В присутствии соответствующей антитоксической сыворотки лейкотоксическое свойство токсина нейтрализуется.
1. Возбудитель дифтерии. Характеристика морфологических, культуральных и биохимических свойств. Типы дифтерийной палочки. Токсин, структура, механизм действия, генетический контроль синтеза токсина. Патогенез дифтерии. Специфическая профилактика.
Дифтерия — острое инфекционное заболевание преимущественно детского возраста, которое проявляется глубокой интоксикацией организма дифтерийным токсином и характерным фибринозным воспалением в месте локализации возбудителя. Название болезни происходит от греческого слова diphthera — кожа, пленка, так как в месте размножения возбудителя образуется плотная, серовато-белого цвета пленка.
Возбудитель дифтерии — Corynebacterium diphtheriae — был обнаружен впервые в 1883 г. Э. Клебсом в срезах из пленки, получен в чистой культуре в 1884 г. Ф. Леф- флером. В 1888 г. Э. Ру и А. Иерсен обнаружили его способность продуцировать экзотоксин, играющий главную роль в этиологии и патогенезе дифтерии. Получение в 1892 г. антитоксической сыворотки Э. Берингом и использование ее с 1894 г. для лечения дифтерии позволило значительно снизить летальность. Успешное наступление на эту болезнь началось после 1923 г. в связи с разработкой Г. Районом метода получения дифтерийного анатоксина.
Возбудитель дифтерии относится к роду Corynebacterium (класс Actinobacteria). В морфологическом отношении характеризуется тем, что клетки булавовидно утолщены на концах (греч. согупе — булава), образуют ветвление, особенно в старых культурах, и содержат зернистые включения.
В состав рода Corynebacterium входит большое число видов, которые делят на три группы.
1)Коринебактерии — паразиты человека и животных и патогенные для них.
2)Коринебактерии, патогенные для растений.
3)Непатогенные коринебактерии. Многие виды коринебактерий являются нормальными обитателями кожи, слизистых зева, носоглотки, глаз, дыхательных путей, уретры и половых органов.
С. diphtheriae — прямые или слегка изогнутые неподвижные палочки длиной 1,0-8,0 мкм и диаметром 0,3-0,8 мкм, спор и капсул не образуют. Очень часто они имеют вздутия на одном или обоих концах, часто содержат метахроматические гранулы — зерна волютина (полиметафосфаты), которые при окрашивании метилено- вым синим приобретают голубовато-пурпурный цвет. Для их обнаружения предложен особый метод окрашивания по Нейссеру. При этом палочки окрашиваются в соломенно-желтый, а зерна волютина — в темно-коричневый цвет, и располагаются обычно по полюсам. С. diphtheriae хорошо окрашивает ся анилиновыми красителями, грамположительна, но в старых культурах нередко обесцвечивается и имеет отрицательную окраску по Граму. Для нее характерен выраженный полиморфизм, особенно в старых культурах и под влиянием антибиотиков (см. рис. 102.1). Содержание Г + Ц в ДНК около 60 мол %.
Дифтерийная палочка является аэробом или факультативным анаэробом, температурный оптимум для роста 35—37 °С (границы роста 15—40 °С), оптимальная рН 7,6—7,8. К питательным средам не очень требовательна, но лучше растет на средах, содержащих сыворотку или кровь. Избирательными для дифтерийных бактерий являются свернутые сывороточные среды Ру или Леффлера, рост на них появляется через 8—12 ч в виде выпуклых, величиной с булавочную головку колоний серовато-белого или желтовато-кремового цвета. Поверхность их гладкая или слегка зернистая, на периферии колонии несколько более прозрачные, чем в центре. Колонии не сливаются, вследствие чего культура приобретает вид шагреневой кожи. На бульоне рост проявляется в виде равномерного помутнения, либо бульон остается прозрачным, а на его поверхности образуется нежная пленка, которая постепенно утолщается, крошится и хлопьями оседает на дно.
Особенностью дифтерийных бактерий является их хороший рост на кровяных и сывороточных средах, содержащих такие концентрации теллурита калия, которые подавляют рост других видов бактерий. Это связано с тем, что С. diphtheriae восстанавливают теллурит калия до металлического теллура, который, откладываясь в микробных клетках, придает колониям характерный темно-серый или черный цвет. Применение таких сред повышает процент высеваемости дифтерийных бактерий (рис. 103).
С. diphtheriae ферментируют глюкозу, мальтозу, галактозу с образованием кислоты без газа, но не ферментируют (как правило) сахарозу, имеют цистиназу, не имеют уреазы и не образуют индола. По этим признакам они отличаются от тех коринеформ- ных бактерий (дифтероидов), которые чаще других встречаются на слизистой оболочке глаза (С. xerosus) и носоглотки (С. pseudodiphtheriticum) и от других дифтероидов (табл. 44).
В природе существуют три основных варианта (биотипа) дифтерийной палочки: gravis, intermedins и mitis. Они различаются по морфологическим, культуральным, биохимическим и другим свойствам.
Экзотоксин синтезируется в виде неактивного предшественника - единой полипептидной цепи с м. м. 61 кД. Его активация осуществляется собственной бактериальной протеазой, которая разрезает полипептид на два связанные между собой ди- сульфидными связями пептида: А (м. м. 21 кД) и В (м. м. 39 кД). Пептид В выполняет акцепторную функцию — он распознает рецептор, связывается с ним и формирует внутримембранный канал, через который проникает в клетку пептид А и реализует биологическую активность токсина. Пептид А представляет собой фермент АДФ- Рибозилтрансферазу, который обеспечивает перенос аденозиндифосфатрибозы из НАД на один из аминокислотных остатков (гистидина) белкового фактора элонгации EF-2. В результате модификации EF-2 утрачивает свою активность, и это приводит подавлению синтеза белка рибосомами на стадии транслокации. Токсин синтезируют только такие С. diphtheriae, которые несут в своей хромосоме гены умеренного конвертирующего профага. Оперон, кодирующий синтез токсина, является моноци- стронным, он состоит из 1,9 тыс. пар нуклеотидов и имеет промотор toxP и 3 участ-ка: toxS, toxA и toxB. Участок toxS кодирует 25 аминокислотных остатков сигнального пептида (он обеспечивает выход токсина через мембрану в периплазматическое пространство бактериальной клетки), toxA — 193 аминокислотных остатка пептида А, и toxB — 342 аминокислотных остатка пептида В токсина. Утрата клеткой профага или мутации в tox-опероне делают клетку малотоксигенной. Напротив, лизогениза- ция нетоксигенных С. diphtheriae конвертирующим фагом превращает их в токсиген- ные бактерии. Это доказано однозначно: токсигенность дифтерийных бактерий зависит от лизогенизации их конвертирующими tox-коринефагами. Коринефаги интегрируются в хромосому коринебактерий с помощью механизма сайт-специфической рекомбинации, причем штаммы дифтерийных бактерий могут содержать в своих хромосомах по 2 сайта рекомбинации (attB), и коринефаги интегрируются в каждый из них с одинаковой частотой.
В связи с тем, что дифтерийный токсин в организме больных оказывает избирательное и специфическое воздействие на определенные системы (поражаются в основном симпатико-адреналовая система, сердце, сосуды и периферические нервы), то очевидно, он не только угнетает биосинтез белка в клетках, но и вызывает другие нарушения их метаболизма.
Особенности патогенеза и клиники. К дифтерии восприимчивы люди любого возраста. Возбудитель может проникнуть в организм человека через слизистые оболочки различных органов или через поврежденную кожу. В зависимости от локализации процесса различают дифтерию зева, носа, гортани, уха, глаза, половых органов и кожи. Возможны смешанные формы, например дифтерия зева и кожи и т. п. Инкубационный период — 2—10 дней. При клинически выраженной форме дифтерии в месте локализации возбудителя развивается характерное фибринозное воспаление слизистой оболочки. Токсин, вырабатываемый возбудителем, сначала поражает эпителиальные клетки, а затем близлежащие кровеносные сосуды, повышая их проницаемость. В выходящем экссудате содержится фибриноген, свертывание которого приводит к образованию на поверхности слизистой оболочки серовато-белого Цвета пленчатых налетов, которые плотно спаяны с подлежащей тканью и при отрыве От нее вызывают кровотечение. Следствием поражения кровеносных сосудов может быть развитие местного отека. Особенно опасной является дифтерия зева, так к ак она может стать причиной дифтерийного крупа вследствие отека слизистой оболочки гортани и голосовых связок, от которого раньше погибало в результате ас- фиксии 50—60 % больных дифтерией детей. Дифтерийный токсин, поступая в кровь, вызывает общую глубокую интоксикацию. Он поражает преимущественно сердечно-сосудистую, симпатико-адреналовую системы и периферические нервы, аким образом, клиника дифтерии складывается из сочетания местных симптомов, зависящих от локализации входных ворот, и общих симптомов, обусловленных отравлением токсином и проявляющихся в виде адинамии, вялости, бледности кожных покровов, понижения кровяного давления, миокардита, паралича периферических нервов и других нарушений. Дифтерия у привитых детей, если и наблюдается, протекает, как правило, в легкой форме и без осложнений. Летальность в период до применения серотерапии и антибиотиков составляла 50—60 %, ныне — 3—6 %.
Специфическая профилактика. Основным методом борьбы с дифтерией является массовая плановая вакцинация населения. С этой целью используют различные варианты вакцин, в том числе комбинированные, т. е. направленные на одновременное создание иммунитета против нескольких возбудителей. Наибольшее распространение в России получила вакцина АКДС. Она представляет собой адсорбированную на гидроокиси алюминия взвесь коклюшных бактерий, убитых формалином или мертиолятом (20 млрд в 1 мл), и содержит дифтерийный анатоксин в дозе 30 флоккулирующих единиц и 10 единиц связывания столбнячного анатоксина в 1 мл. Вакцинируют детей с 3-месячного возраста, а затем проводят ревакцинации: первую через 1,5—2 года, последующие в возрасте 9 и 16 лет, а далее через каждые 10 лет.
2. Микобактерии и их характеристика. Классификация микобактерий. Палочка туберкулеза, ее основные свойства, факторы патогенности. Бактериоскопическая диагностика туберкулеза.
Возбудитель туберкулеза — Mycobacterium tuberculosis —Морфологически характеризуются способностью образовывать нитевидные и ветвящиеся формы, особенно в старых культурах. Кроме того, они отличаются от других микроорганизмов более высокой устойчивостью к кислотам, щелочам и спирту.
По патогенным свойствам род Mycobacterium подразделяют на две группы:
1) патогенные и условно-патогенные (потенциально патогенные)
2) сапрофита. Для их ускоренной предварительной дифференциации учитывают прежде всего три признака: а) скорость и условия роста; б) способность к пигментообразованию; в) способность синтезировать никотиновую кислоту (ниацин).
По скорости роста род Mycobacterium подразделяют на три группы:
1) Быстрорастущие — крупные видимые колонии появляются ранее 7-го дня инкубации (18 видов).
2) Медленнорастущие — крупные видимые колонии появляются после 7-ми и более дней инкубации (20 видов).
3) Микобактерии, которые требуют специальных условий для роста или не растут на искусственных питательных средах. К этой группе относятся два вида: М. leprae и М. lepraemurium.
По способности к пигментообразованию микобактерии также делят на 3 группы:
1) Фотохромогенные — образуют пигмент лимонно-желтого цвета при росте на свету.
2) Скотохромогенные — образуют пигмент оранжево-желтого цвета при инкубировании в темноте.
3) Нефотохромогенные — пигмента не образуют (независимо от наличия света), иногда культуры имеют светло-желтоватую окраску.
К патогенным и потенциально патогенным относится 24 вида.
Многие биологические свойства микобактерий объясняются высоким содержанием липидов, составляющих до 40 % сухого остатка клеток.
Высокое содержание липидов определяет следующие свойства туберкулезных палочек.
1)Устойчивость к кислотам, щелочам и спирту.
2)Трудная окрашиваемость красителями. Для их окрашивания применяют интенсивные методы. Например, по способу Циля—Нильсена окрашивают концентрированным раствором карболового фуксина при подогревании.
С липидами, состоящими из нейтральных жиров, восков, стеринов, фосфатидов, сульфатидов и содержащими такие жирные кислоты, как фтиоидная, миколовая, туберкулостеариновая, пальмитиновая и др., связаны патогенные свойства туберкулезной палочки и те биологические реакции, которыми ткани отвечают на их внедрение. Главным фактором патогенности является токсический гликолипид (корд-фактор), который располагается на поверхности и в толще клеточной стенки.
Для диагностики туберкулеза применяют все методы: бактериоскопический, бактериологический, серологический, биологический, аллергические пробы, ПЦР.
При бактериоскопическом исследовании исходного материала (мокрота, моча, гной, спинномозговая жидкость, испражнения) необходимо учитывать, что содержание в нем микобактерий может быть незначительным, выделение их эпизодическим и в нем могут быть измененные варианты возбудителя, в том числе L-формы. Поэтому для повышения вероятности обнаружения микобактерий туберкулеза используют методы концентрирования их с помощью центрифугирования или флотации, а также фазово-контрастной (для обнаружения L-форм) и люминесцентной микроскопии (в качестве флуорохромов используют аурамин, аурамин-родамин, акридиновый оранжевый и др.).
СПИРОХЕТЫ, ГРИБЫ, ПРОСТЕЙШИЕ
Последнее изменение этой страницы: 2016-09-05; Нарушение авторского права страницы
Читайте также:


