Кишечная нервная система кишечная ней

Более 150 лет в физиологии и медицине изучается энтеральная нервная система (ЭНС). Все исследования можно разделить на три этапа:
Первый этап – анатомическое исследование внутренних систем человека, включая нервную систему. Начинается в 1850 г. с исследований анатомов Ауэрбаха и Мейсснера, открывших две тончайшие нейронные сети, видимые лишь под микроскопом, расположенные в стенке и в подслизистом слое кишечника.
Второй этап – физиология нервной системы внутренних органов. Начинается он с конца ХIХ века с работ двух английских физиологов из Лондона – Бейлиса и Старлинга, а позднее немецкого фармаколога Ульриха Тренделенбурга, открывших перистальтический рефлекс.
Третий этап – понимание функциональной автономности ЭНС. Этот этап активно развивается на протяжении последних тридцати лет. В сследованиях заняты более трехсот ученых из различных стран мира. Среди них Гершон Михаэль (США), Марчело Коста (Австралия), Михаэль Шенеманн (Германия), Эмерен Майер и Антонио Дамазио (США).
В общем плане нервная система состоит из центральной (ЦНС) и периферической нервной системы (ПНС), которые тесно взаимосвязаны друг с другом и следуют точным правилам. Вне этих правил находятся нервные сплетения желудочно-кишечного тракта (ЖКТ), клетки которых расположены в два ряда на протяжении всего пищеварительного тракта, длиной около 9 м у взрослого человека – своего рода чулок, охватывающий пищевод, желудок и кишечник (рис. 1). В начале ХХ века английский физиолог Ньюпорт Ленгли подсчитал количество нервных клеток в желудке и кишечнике – 100 миллионов [1]. Это больше, чем в спинном мозге и периферической нервной системе [2].
На данный момент в категории многочисленных были получены разнообразные данные о строении и функциони ровании ЭНС. В ней присутствует более 30 нейромедиаторов, подобных тем, что присутствуют в головном мозге. Многочисленность нейромедиаторов позволяет предположить, что информация, которой обмениваются клетки ЭНС, очень богата и разнообразна и сходна с той, которой обмениваются клетки головного мозга. Многие психоактивные вещества, вырабатываемые ЭНС, оказывают сильнейшее влияние на высшие органы ЦНС и на психические процессы [5].
Некоторые нейроны ЭНС секретируют гормоны [6]. ЭНС обеспечивает на 70% работу иммунной системы организма. Было доказано, что взаимодействия между ЭНС и местными иммуноцитами ответственны за адаптивные функциональные изменения, включая подвижность и секрецию, а энтеральные нейроны вовлечены в регуляцию воспалительного процесса и могут косвенно влиять на местные нейроиммунные реакции [7].
Как и головной мозг, брюшной мозг погружается в состояние, аналогичное сну, в котором выделяются и стадии быстрого сна, сопровождающиеся появлением соответствующих волн, мышечных сокращений.
У ЭНС есть свои рефлексы и ощущения, что позволяет ей контролировать поведение человека независимо от головного мозга [8]. Выработка условных энтеро-энтеральных рефлексов дает основания говорить о механизмах памяти [9]. При этом к ЭНС не относят сознательные мысли или сознательный процесс принятия решений.
Абсолютно независимо от вышеуказанных исследований А. Менегетти представитель онтопсихологического направления в психологии еще тридцать лет назад в своих работах писал об этом отделе нервной системы. Интересен тот факт, что в 80-х гг. Менегетти описывал этот феномен практически теми же словами, что и современные исследователи.
В качестве заключения хотелось бы отметить, что если раньше существовала тенденция искать линейную зависимость между причиной и заболеванием (как еще постулировал Кох в 1882 г., открыв взаимосвязь между инфекцией туберкулеза и заболеванием), то сегодня рассматривается многофакторность большинства заболеваний с характерными для них факторами риска. Признается, что грань, разделяющая физиологические реакции от патологических, размыта, и многие функциональные расстройства пищеварительного тракта могут представлять собой плохо садаптированный ответ на стимулы окружающей среды [21].
* - Виктория Александровна Дмитриева, кандидат психологических наук, психолог-консультант, и.о. зав. кафедрой онтопсихологии факультета психологии СПбГУ.
** - Вероника Викторовна Одинцова, к. мед. наук, психотерапевт-онтопсихолог, преподаватель САО.


Тело человека удивительно. Даже самые стойкие люди со стальными нервами могут быть внешне невозмутимыми, но испытывать чувство, что живот свело или скрутило от стресса. В основе этого ощущения лежит работа огромной сети нейронов, расположенных в кишечнике.
Нервная система кишечника — зачем она нужна?
Как хронический стресс влияет на иммунитет (и кишечник)?
При затянувшемся стрессе ситуация меняется: происходит длительное выделение химических передатчиков сигнала в структурах мозга (гипоталамусе и гипофизе), а также выброс кортизола надпочечниками. Это вызывает подавление работы иммунной системы и нарушение функции одного из ее важных звеньев — Т-клеток (Т-лимфоцитов) 3 . Они выделяют меньше биологически активных веществ и в итоге происходит не только снижение иммунитета, но и нарушение моторики желудка и кишечника. Такой тип реакции сходен с теми изменениями, которые происходят при хронических инфекциях 3 . Также при хроническом стрессе мозг посылает постоянные сообщения органам, в том числе кишечнику, что что-то пошло не так.

Почему кишечник бывает раздраженным?
Раздраженный кишечник — результат аномальных движений мышечных стенок желудочно-кишечного тракта, повышения чувствительности к боли и сложных взаимодействий между мозгом и желудочно-кишечным трактом.
Основные факторы риска этого состояния — стрессы, также свою роль играет неправильное питание (злоупотребление фастфудом, алкоголем), избыточный бактериальный рост в тонком кишечнике, перенесенные вирусные или бактериальные инфекции кишечника (инфекционные гастроэнтериты), курение, малоподвижный образ жизни.
Самые частые симптомы — спастические или колющие боли в животе (они, как правило, уменьшаются после похода в туалет и усиливаются перед едой), избыточное газообразование, вздутие живота, изменение формы стула, чередование периодов диареи и запоров. Эти признаки чаще усиливаются на фоне тревоги.
Как не ошибиться с диагнозом?
Для постановки диагноза обычно используют тщательный сбор анамнеза, лабораторные и эндоскопические тесты. Также помогут Римские критерии 4 , согласно которым функциональное расстройство наиболее вероятно, если имеется повторяющаяся боль в животе. Она должна возникать в среднем не реже раза в неделю последние три месяца и сопровождаться двумя или более дополнительными симптомами: должна быть связана с дефекацией (походом в туалет), изменением частоты стула, изменением формы или внешнего вида стула.
Зачем нужна йога и диета Fodmap?
Учитывая сложные взаимосвязи между кишечником и мозгом и значительную роль стресса, к лечению раздраженного кишечника необходим комплексный подход. Конечно, нужно снизить уровень стресса. Например, с помощью физических упражнений, в том числе занятий йогой. Кроме повышения гибкости, асаны способствуют установлению более осознанной связи с телом. Мышцы и связки посылают сигналы в мозг, вызывая выработку эндорфинов. Это приводит не только к расслаблению мышц, но и к стабилизации эмоционального фона. Подобным образом действуют и медитации. Они позволяют уменьшить напряжение поперечно-полосатых и гладких мышц кишечника и снять общее напряжение.

Еще один способ улучшения состояния при раздраженном кишечнике — диета с низким содержанием FODMAP 5 .
Название произошло от первых букв продуктов, которые следует избегать: Fermentable (ферментируемые или сбраживаемые), Oligosaccharides (олигосахариды), Disaccharides (дисахариды), Monosaccharides (моносахариды) and Polyols (полиолы).
Диета разработана в Австралии и предполагает уменьшение количества различных природных сахаров, искусственных подсластителей. Эти вещества обладают свойством задерживать воду и ферментируются бактериями, во время этого процесса выделяется большое количество метана и углекислого газа, что приводит к метеоризму и болям в животе. Диета означает уменьшение в рационе:
- олигосахаридов: продуктов на основе пшеницы, ржи, ячменя (хлеб, выпечка, крупы), красной фасоли и сои, гороха, свеклы. Таких фруктов, как персики, хурма, нектарины, а также сухофруктов (особенно чернослива), арбузов;
- дисахаридов: продуктов с лактозой, например, молока;
- моносахаридов: яблок, груш, манго, вишни, фруктовых соков с высоким содержанием фруктозы, кукурузного сиропа, меда;
- полиолов: грибов, цветной капусты, зеленого горошка.
Место этих продуктов в рационе занимают цитрусовые, дыня, маракуйя, ягоды, овощи (морковь, огурцы, капуста, тыква), крупы (гречневая, сорго, киноа), орехи, нежирные мясо, рыба, птица, яйца, безлактозное, миндальное или рисовое молоко, твердый сыр, фета, творог.
По данным недавнего исследования, 86% людей на фоне диеты отметили улучшение состояния при раздраженном кишечнике 5 . У них уменьшились боль, вздутие, стали меньше беспокоить запор/диарея.
Залог успеха — комплексное лечение
Для достижения результатов при раздраженном кишечнике необходима медикаментозная поддержка. Поэтому целесообразен прием препаратов, снимающих спазм и координирующих работу гладкой мускулатуры кишечника. Важно, чтобы лекарство было селективным, то есть действовало именно в кишечнике, не влияя на другие системы организма.
Так работает Дюспаталин ® 135 мг, разработанный для специально для лечения раздраженного кишечника 6 . Дюспаталин ® 135 мг уже через 15 минут 7 начинает действовать, помогая снимать боль и спазм. При курсовом приеме от 28 дней 8 Дюспаталин ® борется с комплексом симптомов, устраняя боль и нормализуя работу кишечника.
Работая только в кишечнике, он действует напрямую на гладкомышечные клетки, потому не имеет системных побочных эффектов и может применяться неограниченно долго. Эффект препарата сохраняется 6 месяцев 8 .
Мозг и кишечник неразрывно связаны, и когда в кишечнике неполадки, это отражается на работе всего организма. Если раздраженный кишечник мешает жить, то это время задуматься о занятиях йогой, специальной диете и приеме препаратов, созданных как раз для его лечения. Таких, как Дюспаталин ® 135 мг. С ним Ваш кишечник невозмутим.

Регистрационный номер RUS237535, 05 ноября 2019 года.
Источники
Минушкин О.Н., Елизаветина Г.А., Ардатская М.Д. Лекарственная терапия функциональных расстройств кишечника и желчевыводящей системы, протекающих преимущественно с абдоминальными болями и метеоризмом. Клиническая фармакология и терапия. 2002;1:24-26.
- Здоровье и наука

Новости нейронауки: в 2018 году в результате исследований в области нейробиологии сделан ряд потрясающих открытий. Вот одно из них, взрывающее наши умы: здоровье нашего мозга зависит от микрофлоры кишечника. И, чтобы повлиять на него, нужно поменять свой рацион питания.
Взаимосвязь нашего мозга и микрофлоры кишечника
Кроме того, энтеральная нервная система осуществляет контроль за перевариванием пищи в желудке, ее прохождением по кишечнику, а также иннервирует мускулатуру и сфинктеры внутренних органов, регулирует выработку ферментов и желудочной кислоты, необходимых для процесса переваривания.
Американским ученым удалось доказать, что нервная сеть пищеварительного тракта не только выполняет команды головного мозга (это было известно много десятилетий назад), но представляет собой достаточно самостоятельную систему, приспособленную реализовывать пищеварительную деятельность организма, даже тогда, когда прервано её соединение со спинным и головным мозгом.
Современные исследования ученых в области генетики и тканей на молекулярном уровне выявили в кишечнике человека тысячи различных типов бактерий, состав которых у здоровых людей относительно постоянный. А вот во время стресса или изменения привычного рациона правильного питания, а также с возрастом, микрофлора кишечника значительно изменяется и негативно влияет на здоровье мозга, связанного с кишечником посредством эндокринной, нервной, иммунной систем и не специфического природного иммунитета.
Исследователи – нейробиологи признают факт связи дисбактериоза – дисбаланса микрофлоры, с симптомами, вызванными стрессом. Воспаление слизистой кишечника и накопление токсинов в крови повышает уровень тревожности у человека.
Кишечник может спровоцировать депрессию
Ученые все больше понимают, что кишечник может способствовать беспокойству, депрессии или, что более спорно, познанию.
В прошлом году ученые обнаружили новый набор информационных магистралей, которые напрямую связывают кишечник с мозгом. В кишечнике энтероэндокринные клетки откачивают гормоны, которые запускают пищеварение и подавляют голод. Эти клетки имеют небольшие выступы, похожие на ступни, которые удивительно похожи на синапсы – место контакта между двумя нейронами для передачи импульсов или разговора друг с другом с помощью химических веществ.
Исследователи обнаружили, что энтероэндокринные клетки напрямую связываются с нейронами блуждающего нерва – гигантского нерва, который проходит от мозга к жизненно важным органам, таким как сердце и легкие. Более того, они общаются со своими партнерами с помощью классических нейромедиаторов головного мозга, включая глутамат и серотонин, которые работают намного быстрее гормонов.
Другое исследование показало, что кишечник напрямую связан с центрами вознаграждения мозга через блуждающий нерв. С помощью лазеров ученые обнаружили повышенный уровень дофамина в мозге мышей, стимулирующий настроение.
Эти новые связи могут объяснить, почему стимуляция блуждающего нерва потенциально полезна для людей с тяжелой депрессией. Этим также объясняется, почему насыщаясь пищей мы ощущаем себя теплыми и пушистыми.
Новость нейронауки – раскрытие связи кишечник-мозг набирает обороты в исследовательской области. В конце концов, результаты могут привести к новым методам лечения расстройств, связанных с нарушением работы кишечника—например, ожирение, расстройства питания, депрессия или даже аутизм.
Вместо заключения
Отсюда следует ожидать, что в будущем возможно эффективное лечение депрессии и других патологических симптомов нарушения нервной системы с помощью средств для восстановления микрофлоры кишечника – пробиотиков.
Так что, ешьте больше растительной пищи и пробиотиков в виде квашеных овощей для хорошего самочувствия и здоровья мозга!
По количеству нервных клеток кишечник сопоставим со спинным мозгом. Речь пойдет об энтеральной неврной системе.
Наша пищеварительная система имеет собственную, местную нервную систему, причем достаточно автономную. Мы же не задумываемся каждую секунду, о том, сколько нам нужно для пищеварения желудочного сока, через какое время пища из него должна пойти дальше, как и на каком участке кишечник должен расслабиться а в каком сократиться. Мы вообще об этом не думаем. Все происходит автоматически.
Как открывали энтеральную нервную систему
С появлением микроскопии ученые старались рассмотреть под большим увеличением практически все: микромир все больше открывался любознательным. Первым, кто описал микроскопические ганглии в стенке глотки и желудка был Ремак (Remak) в 1840 году. Но в своих наблюдениях он не принял их за нервное сплетение. Более полные исследования принадлежат следующим ученым: Мейсснеру , Бильроту и Ауэрбаху. Подробные описания и зарисовки этих ученых, основанных на довольно примитивных методах окраски нервной ткани были без изменений практически до 1930 года
Те самые, которые не восстанавливаются
Действительно, нервные клетки — нейроны, утратили (за редким исключением) способность к делению. Природа забрала эту способность у них, наделив другими уникальным свойством: нейроны способны быстро принимать, передавать и обрабатывать информацию.
Все знают, что такое эстафета: бегун передает палочку следующему спортсмену, полному сил. В древности предупреждали о приближении вражеского войска при помощи сигнала от одного поста к другому, разжигая костер. Увидев дым от него, видевшие его воины разжигали свой и предупреждали следующий пост. Так информация об опасности быстро достигала командования.
Итак, кишечник имеет свою собственную нервную систему, которая, подобно кружевному чулку, оплетает пищеварительную трубку практически от глотки до внутреннего сфинктера.
Нервная система, которая встроена в кишечную стенку, находится у всех представителей царства животных, даже у такого более примитивного существа как гидра (Shimizu, 2004 год).
Ее изучают на уроках зоологии в школе. Поразительная способность к регенерации: она может восстановиться из одной сотой части тела (из каждого кусочка будет новая гидра). У нее тоже имеются простейшая энтеральная нервная система
Сейчас ученые считают, что примитивный мозг червей, а конечном итоге мозг высших животных и нас с вами, произошли от нервной системы внутри кишечной трубки. Так что энтеральная нервная система — древний прародитель более развитой, современной центральной нервной системы.
Александр Станиславович Догель
Являясь одним из основоположников нейрогистологии, среди множества работ профессора Догеля были и работы по изучению нервной системы кишечника. Он описал различные виды нервных клеток в кишечной стенке, выделил три разных их типа: 
Эти клетки непосредственно отдают команды исполняемым клеткам (секреторным или мышечным) 
Нейроны Догеля 2 типа — это клетки, воспринимающие все то что происходит в полости кишки: кислотность содержимого, его состав, ну и конечно же — давление и степень растяжения кишечной стенки 
Как устроена нервная система кишечника
Основные ее компоненты — межмышечное сплетение (Ауэрбахово) — располагается между продольным и циркулярным мышечным слоем и подслизистое нервное сплетение (сплетение Мейсснера), расположенное под слизистой оболочкой кишки. 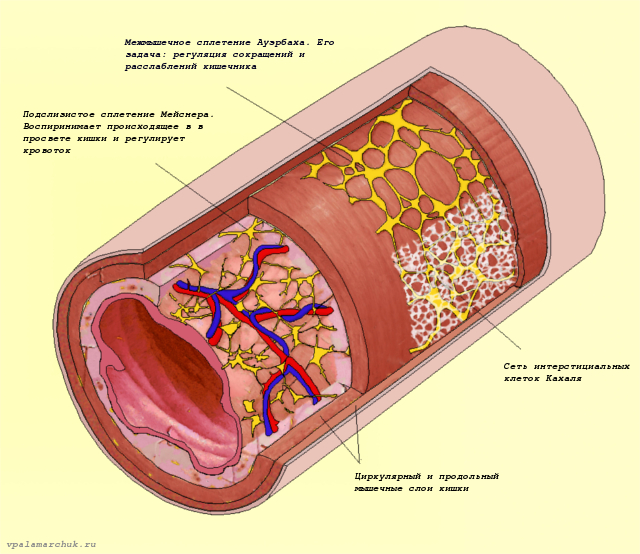
Ауэрбахово сплетение более развито и его задача — координированное расслабление и сокращение гладкой мускулатуры кишки.
В межмышечном сплетении располагается большая часть мотонейронов и клеток посредников — интернейронов.
Сплетение Мейсснера воспринимает происходящее в просвете кишечника и регулирует выделение кишечных соков и кровообращение. Здесь в основном определяются большие нейроны 2 типа
Теперь о нейронах посредниках. На рисунке они зеленые. Одни из них активируют моторный нейрон, другие наоборот, приводят к его торможению.
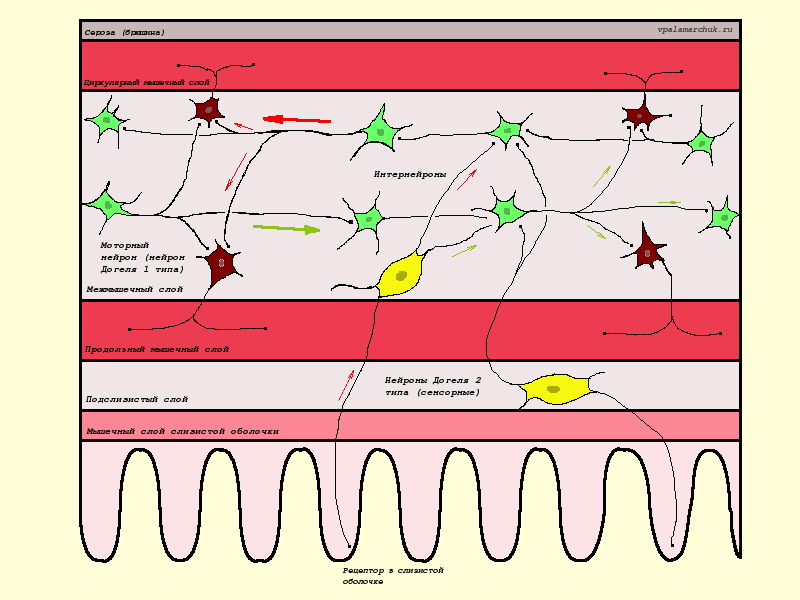
Желтые — воспринимающие нейроны, зеленые — интернейроны, красные — нейроны моторные.Стрелками показаны пути стимулирующие (красная) и тормозящие (зеленая). Или парасимпатическое и симпатическое сплетение соответственно. Сенсорные нейроны могут действовать и на тот и на другой путь.
Видов медиаторов более тридцати. Ключевые: ацетилхолин — медиатор, который стимулирует мотонейрон (следовательно, кишка будет сокращаться, будет вырабатываться кишкой слизь, будет усиливаться кровообращение) и норадреналин, который действует взаимно противоположно (кишечник расслабляется, ослабляется кровоток, снижается выработка кишечных соков).
Симпатика — норадреналин, парасимпатика — ацетилхолин. 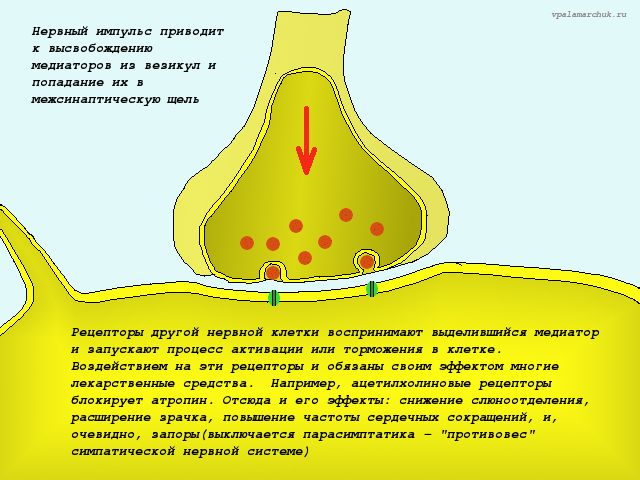
В заключение
Если уж быть объективным, то почти половина всех медицинских препаратов и связана с воздействием на на синаптическую передачу. Есть в кишечнике и опиатные рецепторы. Поэтому у страдающих наркотической зависимостью могут наблюдаться тяжелейшие запоры. В 50 годах прошлого века для купирования стула после проктологической операции (стула не было до 5 суток) применялся морфин. Нарушение нервно-мышечной передачи у пациентов с болезнью Паркинсона приводит к упорным запорам. Запоры наблюдаются у душевно больных людей после приема нейролептиков. А вот никотин способен стимулировать ацетилхолиновые рецепторы, поэтому после курения может захотеться в туалет.
Врожденное недоразвитие нервных ганглиев приводит к болезни Гиршпрунга и интестинальной нейронной дисплазии.
Теперь об одной из основных функций: перистальтике.
Если вы нашли опечатку в тексте, пожалуйста, сообщите мне об этом. Выделите фрагмент текста и нажмите Ctrl+Enter.
Чуете нутром? То у вас порхают в животе бабочки, то некто сосет под ложечкой от страха, то развивается медвежья болезнь при сильной тревоге. Знакомо? Сегодня мы поговорим о связи мозга и кишечника. Да-да, в кишечнике есть много нервных клеток, много бактерий, которые влияют на наш мозг намного сильнее, чем мы с вами думаем. Средний человек имеет около 1,5 килограммов бактерий кишечника.
Что такое ось кишечник-мозг?
Ось “кишечник-мозг” – воображаемая связная линия и один из новых горизонтов комплекса нейронаук. Микробиота кишечника (иначе, микрофлора), которую часто теперь называют “вторым геномом” и “вторым мозгом”, может влиять на наше настроение посредством механизмов, которые ученые только начинают понимать. И, в отличие от генов, которые мы наследуем, микрофлору можно изменить и даже вырастить. По мере того, как исследования переходят с мышей не людей, мы получаем все больше понимания связей микрофлоры с нашим мозгом, становятся видны важные связи с ментальным (или душевным) здоровьем. Одного японского магната однажды спросили, как он узнает, стоит ли ему вступать в сделку, и он ответил: "Я проглатываю это, и, если мне нравится ощущения в моем животе, я вступаю в сделку". Наш кишечник сам себе голова, но при этом непрерывно разговаривает с нашим мозгом.
Пищеварение — сложный процесс, поэтому нет ничего удивительного в том, что для его регуляции существует отдельная нейронная сеть. Пищеварительная нервная система отвечает за процессы механического перемешивания пищи в желудке, координирует сокращение круговой мускулатуры и всех сфинктеров на протяжении кишечника для того чтобы обеспечивать поступательное продвижение пищи, она также поддерживает разную биохимическую среду и уровень кислотности внутри каждой отдельной секции пищеварительного тракта, обеспечивая ферментам необходимые условия для их работы.
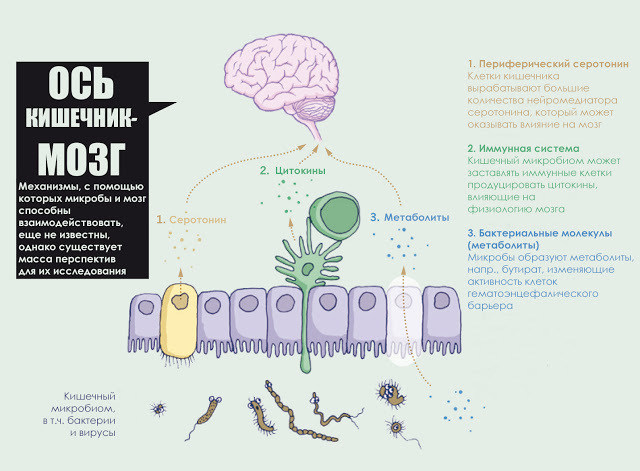
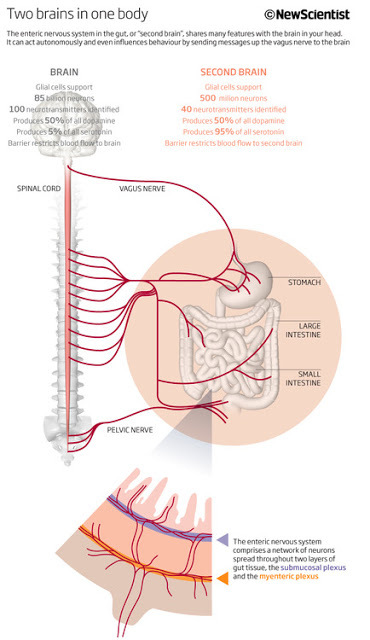
Спустя десятилетие после выхода в свет популярнейшего произведения "Второй мозг" американский ученый подтверждает предположение, что нервная система кишечника - это не тупое скопление узлов и тканей, выполняющих команды центральной нервной системы, как гласит старая медицинская доктрина, а уникальная сеть, способная осуществлять сложные процессы самостоятельно.
Примечательно, что кишечник продолжает функционировать, даже когда отсутствует связь с головным и спинным мозгом. Кишечный мозг самостоятельно решает все аспекты пищеварения на всем протяжении желудочно-кишечного тракта - от пищевода до кишечника и прямой кишки. При этом им используются те же инструменты, что и "благородным" мозгом: целой паутиной нейронных цепочек, нейропередатчиков и протеинов. Эволюция свидетельствует о своей проницательности: вместо того, чтобы заставлять голову жестоко напрягаться работой миллионов нервных клеток для связи с удаленным участком организма, она предпочла передоверить управление центру, расположенному в контролируемых им зонах.
Согласно современным представлениям, нейромедиаторы, вырабатываемые нейронами желудочно-кишечного тракта, не способны попасть в головной мозг, однако теоретически они, все-таки могут проникнуть в небольшие области мозга, где уровень проницаемости гематоэнцефалического барьера выше, например, в гипоталамус. Как бы там ни было, нервные сигналы, посылаемые из желудочно-кишечного тракта в головной мозг, бесспорно, затрагивают настроение. Исследователи начали расшифровывать способы, которыми бактерии кишечника могут подавать сигналы мозгу. Петерсон и другие показали, что у взрослых мышей микробные метаболиты влияют на основную физиологию гематоэнцефалического барьера. Кишечные микробы расщепляют сложные углеводы до короткоцепочечных жирных кислот с образованием массы эффектов: бутираты жирных кислот, например, укрепляют гематоэнцефалический барьер, “затягивая” соединения между клетками.
Сосуществование симбионтной микрофлоры и ее носителя, по большей части, взаимовыгодно. В частности, присутствие симбионтов принципиально для функционирования нашей иммунной системы, переработки питательных веществ и для других аспектов здоровой физиологии. Используя самые современные инструменты для изучения генетики и тканей организма на молекулярном уровне, ученые смогли продемонстрировать, что в кишечнике представлены несколько типов бактерий, и что симбионтные популяции характеризуются большим разнообразием: можно выделить до тысячи разных видов. В дополнение к этому, на формирование индивидуальной микрофлоры постоянно влияют такие факторы как пол, генетика, возраст, тип питания .
У здоровых людей бактериологическое разнообразие существенно больше, но при этом, изучая микрофлору таких людей в разные моменты времени (с промежутком в несколько месяцев, можно увидеть, что состав едва ли меняется. А вот в стрессовых ситуациях или в ответ на физиологические или диетические изменения, микрофлора может сама измениться, создавая дисбаланс во взаимодействии между микрофлорой и ее носителем. И такие изменения могут влиять на состояние здоровья человека.
Взаимонаправленные связи между кишечником и мозгом осуществляются посредством эндокринной, нервной, иммунной систем и неспецифического природного иммунитета. Кишечная микрофлора как активный участник кишечно-мозговой оси не только оказывает влияние на кишечные функции, но также стимулирует развитие ЦНС в перинатальном периоде и взаимодействует с высшими нервными центрами, вызывая депрессию и когнитивные расстройства при патологии. Особая роль принадлежит микроглии кишечника. Помимо механической (защитной) и трофической функции для кишечных нейронов, глия осуществляет нейротрансмиттерную, иммунологическую, барьерную и моторную функции в кишечнике. Существует взаимосвязь между барьерной функцией кишечника и регуляцией гематоэнцефалического барьера.
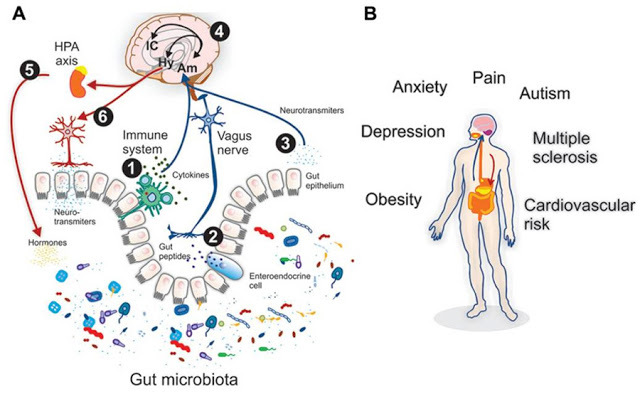
Хроническая эндотоксинемия (высокий уровень токсинов в крови) как результат дисфункции кишечного барьера формирует устойчивое воспалительное состояние в околожелудочковых зонах мозга с последующей дестабилизацией гемато-энцефалического барьера и распространением воспаления на другие участки мозга, следствием чего является развитие нейродегенерации.
Установлено, что микробиота, оказывающая действие на барьерную функцию слизистой оболочки и вызывающая иммунный и нейроэндокринный ответ, может давать прямые и непрямые эффекты на функцию и даже морфологию мышечных и нервных клеток кишечника. Исследования показали наличие взаимосвязей между воспалением слизистой оболочки и моторной и сенсорной функциями кишки, нарушение ее барьерной функции при модификации микробиоты и последствия изменений целостности слизистой оболочки для хозяина. Иммунный ответ, индуцированный микроорганизмами, привлекает к себе повышенное внимание исследователей, учитывая возможный вклад воспаления в патогенез моторной дисфункции при различных заболеваниях.
Например, сегодня уже известно, что в депрессии есть воспалительный компонент и многие полезные бактерии в кишечнике вырабатывают короткоцепочечные жирные кислоты, такие как бутират, способствующие питанию клеток, выстилающих кишечник, чтобы уменьшить воспаление. Микробиом связали с депрессией совсем недавно, когда было обнаружено, что бактерии Oscillibacter вырабатывают химическое вещество, действующее как естественный транквилизатор, имитирующий действие нейромедиатора ГАМК (этот нейродиметиатор — гамма-аминомасляная кислота — понижает нервную активность мозга и может привести к депрессии). Способность почвенных микробов, например микобактерии вакка (Mycobacterium vaccae), модулировать иммунную систему человека давно известна, и некоторые исследователи даже предполагают, что это свойство можно использовать для создания вакцины против стресса и депрессии.
В частности, Грэм Рук из Университетского колледжа Лондона утверждает, что недостаточный контакт с нашими старыми друзьями — почвенными микробами, воздействию которых мы подвергались на протяжении всей истории, но теперь, в своем неумеренном стремлении к чистоте, свели к нулю, — это причина распространения многих заболеваний, в том числе диабета, артрита и депрессии.
Анорексия и микрофлора
Поскольку кишечная микрофлора играет ключевую роль в развитии иммунитета, можно считать, что у стерильных мышей воспалительные процессы всегда тихие. Когда мы рассматриваем связь между воспалением и тревожным поведением, мы можем наблюдать, что низкая тревожность обнаруживается там же, где и воспалительные процессы не выражены сильно, а вот более сильное воспаление ведет к повышению тревожности.
Например, инфицирование мышей паразитом Trichuris muris ведет к воспалению в кишечнике и возрастанию уровня тревожности. В дополнение к этому, химически спровоцированное воспаление (колит) также приводит к повышению тревожности. В тех же исследованиях предоставляются и доказательства в пользу того, что микрофлора выступает в роли модулятора этой тревожности в поведении, связываемой с иммунной реакцией: в отчетах говорится, что “лечение” пробиотической культурой Bifidobacterium longum уменьшало эту тревожность. Эти наблюдения предполагают, что назначение пробиотиков может оказаться перспективным при лечении воспалительных процессов или связанных с ними симптомами “тревожности”.
Одно из первых исследований, рассматривающих связь стресса и микрофлоры показало, что у стерильных мышей стрессовая реакция излишне интенсивная. А другое, более свежее исследование показало, что подверженность стрессу крыс “в юности” вызывает нарушения в составе микрофлоры и ведет к более интенсивным стрессовым реакциям в зрелости. Важно, что в этом исследовании обнаружили: если крысятам давать пробиотик (бактерии Lactobacillus sp) это нормализует уровень гормонов стресса. Стресс на ранних этапах жизни ведет к более депрессивному поведению у зрелых крыс. Другое похожее исследование показало, что если крысиному молодняку, подверженному стрессу, давать пробиотики (бактерии Bifiodo infantis), то уменьшаются признаки депрессии в зрелости.
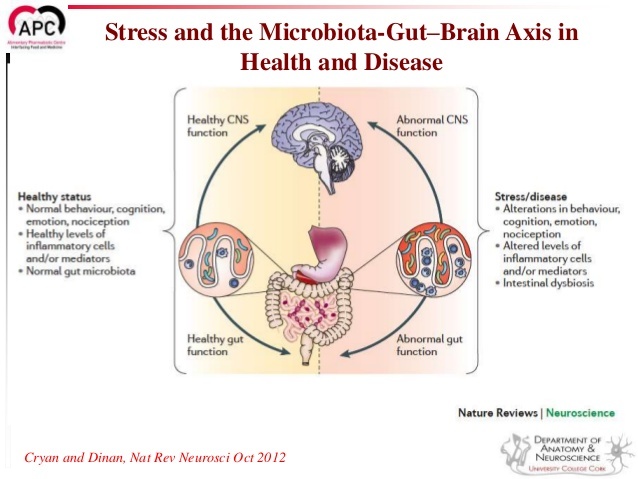
Вместе эти исследования наводят на вывод о том, что нужно признать связь между дисбалансом микрофлоры (дисбактериозом), изменениями в поведении в связи с влиянием стресса и стрессовой реакцией. Также напрашивается вывод, что использование пробиотиков может быть эффективно в лечении симптомов, связанных со стрессом.
В ходе небольшого исследования, участниками которого стали молодые здоровые мужчины, ученые из Университетского колледжа Корка (University College Cork), Ирландия, выявили, что прием пробиотических препаратов, содержащих штамм Bifidobacterium longum (B. longum), способствует снижению уровня физиологического и психологического стресса и улучшает состояние памяти. Доклад об этой работе представил руководитель исследования доктор Джерард Кларк (Gerard Clarke) на ежегодном собрании Сообщества нейронауки (Society for Neuroscience — SfN). Он отметил, что основой для ее проведения стали доклинические эксперименты, в ходе которых стало известно, что штамм B. longum оказывает позитивное воздействие на когнитивные функции лабораторных мышей и уменьшает выраженность физиологических и поведенческих проявлений стресса. 
В данной работе приняли участие 22 волонтера (мужчины, средний возраст — 25,5 года), которые в течение 4 нед принимали препарат, содержащий штамм B. longum NCIMB 41676, а затем следующие 4 нед — плацебо. В начале работы и по окончании каждого 4-недельного периода ученые оценивали уровень острого стресса у частников, используя холодовой прессорный тест и измеряя уровень кортизола — гормона стресса, а ежедневного — с помощью Шкалы воспринимаемого стресса Коэна (Cohen Perceived Stress). Состояние когнитивных функций у волонтеров определяли, исходя из показателей неврологической активности и результатов нейропсихологических тестов.
Проанализировав полученные результаты, авторы исследования отметили, что прием препарата, содержащего пробиотический штамм B. longum NCIMB 41676, приводил к снижению уровня кортизола и субъективному уменьшению уровня тревожности. Участники констатировали, что во время приема препарата они чувствовали себя менее напряженными, чем в начале исследования, а их зрительная память значительно улучшилась.
Кишечная микрофлора (микробиота) – огромная популяция, важная для здорового обмена веществ и функционирования головного мозга, а коммуникация между кишечником и мозгом проходит в т.ч. через нейронные связи. Кишечная микрофлора очень важна в раннем возрасте и может оказывать влияние на то, какие реакции на стресс будут вырабатываться в мозгу
Пробиотики (исследования на людях и животных показали что пробиотики или, иначе говоря, “хорошие бактерии”, оказывают положительное воздействие на настроение. И хотя это очень многообещающие открытия, не нужно спешить и думать, что мы уже нашли решение для клинических ситуаций (расстройств поведения и настроения). Конечно, микрофлора является важным модулятором здоровья и ее следует считать составляющей сложной, многогранной системы коммуникации, которая необходима для установления здорового баланса для развития и здоровой работы мозга.
Но! Критерием здоровья кишечника является не только некий один пробиотик, а именно разнообразие микрофлоры.Поэтому важна нормализация питания в целом! Увы, уникального пробиотика не существует. Что делать для улучшения микрофлоры, напишу потом. опубликовано econet.ru
Понравилась статья? Напишите свое мнение в комментариях.
Подпишитесь на наш ФБ:
Читайте также:


