Поражение периферической нервной системы при боррелиозе
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.

Читайте в новом номере
Лайм-боррелиоз (ЛБ), или болезнь Лайма (Lyme disease), Лаймовский боррелиоз, или иксодовый клещевой боррелиоз – это инфекционное природно-очаговое трансмиссивное мультисистемное инфекционное полиорганное воспалительное заболевание, вызываемое спирохетами рода Borrelia, переносчиками которых являются иксодовые клещи. ЛБ характеризуется стадийностью, склонностью к хронизации и рецидивирующему течению [1].
Особое место в клинической картине болезни занимает поражение нервной системы, или нейроборрелиоз, частота выявления которого зависит от географической зоны, наблюдается в России у 10–60% больных [5]. Колебание в частоте его развития связано с особенностью геновидов боррелии и недостаточной изученностью проблемы в ряде регионов. Наиболее высокая частота поражения нервной системы наблюдается на Северо-Западе и в Центре России – 43–64%.
Широкий спектр клинических симптомов и синдромов при нейроборрелиозе объясняется способностью Воrreliа burgdorferi поражать все отделы нервной системы на любой стадии болезни [6, 7]. При нейроборрелиозе описаны:
- сенестонейропатии, нейропатии и радикулопатии;
- поражения черепно-мозговых нервов (ЧМН): моно(поли)неврит (лицевого, языкоглоточного, блуждающего нервов, зрительного, слухового нервов);
- синдром Банавартца (менингорадикулоневрит);
- периферические невриты, плексит. У 1/3 больных выявляется периферический судорожный синдром (тремор кистей рук и судороги в мышцах голеней);
- миелит;
- миелорадикулоневрит;
- лимфоцитарный менингит;
- очаговый или диффузный энцефалит;
- пароксизмальные расстройства сознания;
- эпилептические припадки, церебральный васкулит;
- прогрессирующий энцефаломиелит.
Хронический боррелиоз, или III стадия ЛБ, развивается у 10% больных через 6 мес. – 2 года после острого периода [8]. Наиболее изученными в этом периоде являются хронические неврологические синдромы, напоминающие по срокам развития третичный период нейросифилиса, названные хроническим нейроборрелиозом. При этом развиваются хронический энцефаломиелит, спастический парапарез, некоторые расстройства памяти, деменция, хроническая аксональная полирадикулопатия. Эта стадия характеризуется чередованием ремиссий и рецидивов, однако в некоторых случаях болезнь имеет непрерывно рецидивирующий характер.
Частота развития хронических форм нейроборрелиоза, по данным разных авторов, составляет от 4 до 20% всех больных ЛБ. Однако имеются данные о том, что реальный показатель может быть значительно выше и после перенесенной безэритематозной формы заболевания достигать 85% [9–11]. Считается, что диагностика этих форм заболевания затруднена в связи с отсутствием общепринятых критериев диагностики и недоступных для широкой практики методов идентификации инфекции [12].
Для хронической нейроинфекции наиболее характерно постепенное поражение нервной системы с развитием патологического процесса, имитирующим другие нозологические формы, в частности рассеянный склероз, рассеянный энцефаломиелит. Большинство больных c хронической нейроинфекцией не указывают на предшествующую мигрирующую эритему или укус клеща. Полагают, что укусы самцов и незрелых особей клещей часто проходят незаметно для людей [13]. Кроме того, могут встречаться безэритематозные формы ЛБ в 2–20% случаев [14–15]. Известно, что в 6–8% случаев возможно субклиническое течение боррелиозной инфекции, при этом отсутствуют клинические проявления болезни. Отсутствие симптомов болезни не исключает развития в последующем II и III стадий заболевания. Все это является фактором риска развития хронической нейроинфекции, т. к. обусловливает отсроченную диагностику [16–18]. Латентный период инфекции при позднем нейроборрелиозе может составлять от 1,5 до 17 лет. Столь длительное латентное течение заболевания связывают с возможным переходом боррелии в неактивные L-формы с последующей их активацией [19–21].
Впервые хронический боррелиозный энцефаломиелит был описан R. Ackermann et al. в 1985 г. [23]. Позже была изучена группа из 44 больных, у которых встречались преимущественно церебральные проявления, напоминающие мультифокальный энцефалит, или спинальные симптомы. В настоящее время частота выявления энцефаломиелита при ЛБ невысока и составляет в среднем 4–5% от всех случаев нейроборрелиоза. Хроническое течение ЛБ в России изучено мало, что связано с отсутствием общепринятых критериев диагностики и недоступных для широкой практики методов идентификации инфекции [24].
В литературе выделяют разные варианты течения нейроинфекции при хроническом ЛБ, включая прогрессирующий энцефаломиелит, хроническую радикулополиневропатию, хронический лимфоцитарный менингит, церебральный васкулит, энцефалопатию и др. Прогрессирующий энцефаломиелит при ЛБ нередко имитирует рассеянный склероз [25, 26]. Согласно наблюдению ряда исследователей, при хроническом ЛБ процесс носит генерализованный характер поражения нервной системы, несмотря на то, что клинически определяется изолированное поражение какого-либо нерва [27, 28]. Пo данным магнитно-резонансной томографии (МРТ) отмечаются поражения очагового характера преимущественно белого вещества головного мозга [29], которые могут определяться после длительного латентного периода.
Ведущие симптомы прогрессирующего боррелиозного энцефаломиелита – это спастические пара- и тетрапарезы, атаксия, дисфункция тазовых органов, когнитивные расстройства в виде снижения памяти и концентрации внимания. Больше чем у 50% больных ЛБ с поражением ЦНС наблюдаются сопутствующее поражение корешков и периферических нервов, множественные парезы черепных нервов, преимущественно вестибулокохлеарного.
- Наличие признаков поражения ЦНС при боррелиозе после перенесенных I и II стадий заболевания.
- Развитие неврологической симптоматики позднее 6 мес. от появления мигрирующей эритемы и/или факта присасывания клеща или сохранение симптоматики на протяжении более 6 мес.
- Обнаружение умеренных или высокоположительных титров антител к Borrelia burgdorferi в сыворотке крови больного при двукратном обследовании.
- Исключение другой этиологии патологического процесса, протекающего в нервной системе, который мог явиться причиной развития имеющейся у больного клинической симптоматики.
Поражение нервной системы на поздних стадиях ЛБ у 40% больных бывает изолированным и почти в 60% сочетается с экстраневрональными проявлениями ЛБ [6, 30]. Наиболее часто отмечаются поражения опорно-двигательного аппарата в виде артралгии, миалгии и других проявлений. В связи с развитием ревматических синдромов до 30% больных с ЛБ ежегодно обращаются к ревматологам.
Особая сложность диагностики наблюдается при отсроченном развитии поражения нервной системы, когда трудно определить связь развития поражения нервной системы с фактом присасывания клеща, особенно в случае безэритематозных форм. Также позитивность по антителам к Borrelia burgdorferi в ликворе выявляется только у 18% больных ЛБ [31–35].
В патогенезе хронического нейроборрелиоза играют роль проникновение инфекции и лимфоцитов в ткани нервной системы, чему способствуют активация или повреждение эндотелиальных клеток, нарастание уровня растворимой формы одной из основных клеточных молекул адгезии – ICAM-1, металлопротеиназы-9 [32]. В ряде исследований имеются доказательства развития аутоиммунных процессов в виде обнаружения антител, направленных против протеинов Borrelia burgdorferi и белков нервной ткани, вызывающих воспаление и демиелинизацию [33]. Высказывается предположение о возможном участии боррелии в инициации аутоиммунного процесса в результате активации миелин-специфичных Т-клеток и обнаружения аутореактивных антител к миелину и компонентам миелина при ЛБ [34]. По мере прогрессирования заболевания расширяется спектр антител ко многим белкам боррелии, что может приводить к перекрестному реагированию иммунной системы с антигенами боррелии и макроорганизма. Ведущая роль в этом отводится длительной персистенции возбудителя в тканях и его внутриклеточному расположению [35].
Комплексная оценка эпидемиологических, клинико-лабораторных и инструментальных данных, отражающих поражения нервной системы при хроническом ЛБ, демонстрирует отличие клинической картины хронической нейроинфекции в России от таковой в Европе в виде более частого поражения периферической нервной системы (радикулополиневропатии) и энцефалопатии, а также отсутствия сочетания полиневропатии с хроническим атрофическим акродерматитом.
Факторами риска развития хронического нейроборрелиоза названы: множественные присасывания клещей, отсутствие у больных мигрирующей эритемы на месте присасывания клеща в острый период ЛБ, раннее развитие признаков диссеминации, отсроченный и неполный курс лечения в острый период заболевания.
Спектр редких проявлений хронического нейроборрелиоза включает изолированное поражение черепных нервов, множественные мононевропатии, церебральный васкулит, синдромы паркинсонизма и бокового амиотрофического склероза, описан миастеноподобный синдром как проявление хронического ЛБ [36].
Представляют клинический интерес особенности течения хронической микст-инфекции ЛБ с клещевым энцефалитом и эрлихиозом, анаплазмозом. Так, в единичных случаях возможно хроническое течение клещевой микст-инфекции с характерными клинико-лабораторными проявлениями данных заболеваний. Показано, что в единичных случаях возможно хроническое течение клещевого энцефалита и ЛБ с типичными клиническими проявлениями последних. В случае возможной хронической микст-инфекции ЛБ и эрлихиоза по сравнению с изолированным течением ЛБ преобладает системность проявлений в сочетании с общеинфекционным синдромом и изменением лабораторных показателей крови (лейкопения, повышение уровня трансаминаз).
Диагностика и течение ЛБ в целом и нейроборрелиоза в частности при ревматических заболеваниях осложняется некоторым атипизмом клинический картины и скоростью прогрессирования ее проявлений, связанных со скомпрометированностью иммунной системы этой группы пациентов на фоне терапии высокими дозами глюкокортикоидов (ГК) и цитостатиками.
Пациент Г., 1972 г. р. Анамнез болезни: считает себя больным с июля 2013 г., когда без объективной причины возникли повышение температуры до 37,4°С, параорбитальный отек, первые признаки мышечной слабости, утомляемость, боли в области правого тазобедренного сустава. При обследовании (июль 2013 г.) в общем анализе крови: гемоглобин – 148 г/л, скорость оседания эритроцитов (СОЭ) – 8 мм/ч, лейкопения – 2,82х109 (норма 4,0–9,0), тромбоцитопения, аспартатаминотрансфераза (АСТ) – 49 Ед/л (норма до 35 Ед/л), аланинаминотрансфераза (АЛТ) – 26,2 Ед/л, показатели креатинфосфокиназы (КФК) не исследовали. Белковые фракции: альбумины – 57,3%, (норма 55,7–66,1%), α1 – 6,3% (норма 2,9–11,8%), α2 – 9,1% (норма 7,1–11,8%), β1 – 5,5% (норма 4,7–7,2%), β2 – 5,9% (норма 3,2–6,5%), γ – 15,9% (норма 11,1–18,8%). Общий анализ мочи – без особенностей.
С августа 2013 г. – нарастание параорбитального отека, эритема на лице, груди (в зоне декольте), шее, лихорадка, общая слабость, утомляемость, появление признаков мышечной слабости преимущественно нижних конечностей. При обследовании в сентябре 2013 г. впервые выявлено повышение КФК до 841 Ед/л, лактатдегидрогеназы (ЛДГ) – до 657 Ед/л, креатинина – до 118 мкмоль/л (61–115), сохранялись тромбоцитопения (150х109) и лейкопения (2,8х109).
С учетом наличия в клинической картине параорбитального отека, эритемы на лице и в зоне декольте, проксимальной мышечной слабости, миопатических изменений по данным игольчатой электромиографии, повышения уровня КФК у больного диагностирован дерматомиозит (ДМ), начата терапия ГК в дозе 40 мг/сут, на фоне которой отмечены нормализация температуры тела и уменьшение отека вокруг глаз, снижение уровня КФК, АСТ, АЛТ, нормализации уровня лейкоцитов и тромбоцитов. Однако через 2 нед., на фоне быстрого снижения ГК, при достижении дозы преднизолона 30 мг/сут вновь отмечались возобновление лихорадки, усиление выраженности параорбитального отека, появление и нарастание признаков язвенно-некротического васкулита параорбитальной области (рис. 1 а, б). В связи с обострением заболевания и нарастанием признаков язвенно-некротического васкулита параорбитальной области было назначено повышение дозы ГК до 60 мг/сут, к терапии добавлен циклофосфамид 1000 мг в сочетании с метилпреднизолоном 500 мг в/в капельно 1 р./мес.
За период наблюдения пациенту проведен онкопоиск, включающий КТ грудной клетки, консультации специалистов, в т. ч. уролога – патологии не выявлено. Тогда же (до начала терапии циклофосфамидом в октябре 2013 г.) больному впервые выполнена МРТ головного мозга, каких-либо изменений не выявлено.
На фоне вышеуказанной терапии наблюдались: нормализация температуры тела, заживление язвенно-некротических изменений (рис. 2), нарастание мышечной силы, снижение КФК – 145 Ед/л, ЛДГ– 256 Ел/л, АСТ – 26 Ед/л, АЛТ – 35 Ед/л. Показатели гемоглобина и СОЭ, как и в начале заболевания, сохранялись в пределах нормы.
В январе 2014 г. проведена повторная МРТ головного мозга, при которой выявлено появление множественных инфильтративных очагов в кортикальном слое лобных областей, левой теменной области, супраорбитальный области, признаков отека мозга, нарушение гемодинамики (рис. 4 а–г).
Обсуждение возможности активизации латентно протекающей ранее инфекции привело к дополнительным исследованиям: реакция непрямой гемагглютинации на псевдотуберкулез – отрицательно, Yersinia enterocolitica IgG, IgМ – отрицательно; HSV (Herpes simplex virus) IgM – отрицательно, VZV (Varicella-Zoster virus) IgM – отрицательно, CMV (Сytomegalovirus) IgG – 80,4 Ед/мл, IgМ Литература
Только для зарегистрированных пользователей
Нейроборрелиоз (Лайм-боррелиоз)
Лайм-боррелиоз - зоонозное природно-очаговое заболевание с преимущественным поражением кожи, нервной системы, сердечно-сосудистой системы и опорно-двигательного аппарата, склонное к хроническому течению.
Частота
В России заболеваемость составляет 1,7-3,5 на 100 000 населения в год повсемество. Чаще болеют дети до 15 лет и взрослые в возрасте 25-44 года.
Этиология
Возбудители - 3 вида боррелий: Borrelia burgdorferi, Borrelia garinii и Borrelia a f zelii.
Эпидемиология
Источник инфекции и резервуар - многие виды диких и домашних животных (грызуны, белохвостые олени, лоси и др.). В природных очагах возбудители циркулируют между клещами и дикими животными. Переносчики - Ixodes ricinus, Ixodes persulcatus. Путь передачи - через укусы клеща с его слюной (трансмиссивный), с фекалиями (при их втирании в месте укуса при расчёсах) , реже алиментарный (при употреблении сырого козьего молока). Характерна сезонность (с мая по сентябрь).
Клиническая картина
Инкубационный период продолжается от 1 до 50 дней, в среднем 10-12 сут. У половины инфицированных 1 стадия (локальная инфекция) держится в течение первого месяца после укуса клеща. Характерно острое или подострое начало, гриппоподобное течение с лихорадкой, головной болью, недомоганием, болями в мышцах и суставах, общей слабостью, иногда с выраженным ознобом.
Повышенная температура тела (от 37 до 39-40 ° С) продолжается до 10-12 сут.
Иногда бывают тошнота, рвота. Возможны лимфаденопатия, увеличение печени и селезёнки, менингизм (без изменений ликвора). Патогномоничный признак - мигрирующая кольцевидная эритема способная быть единственным проявлением первой стадии болезни (20% больных).
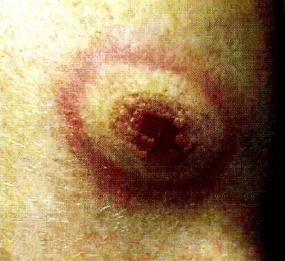
Сначала в месте укуса клеща возникает пятно или папула (участок гомогенной гиперемии), постепенно поражение равномерно увеличивается до десятков сантиметров в диаметре. Края пятна чёткие, ярко-красные, приподняты над уровнем кожи. У части больных в центре пятна эритема постепенно бледнеет и превращается в кольцевидную, при обретает цианотичный оттенок. В зоне пятна возникают зуд и умеренная болезненность. При лечении эта эритема держится несколько дней, а без лечения - до 2 мес и более. После её исчезновения остаются слабая пигментация, шелушение и атрофические изменения кожи в виде папиросной бумаги (рис. 31-2).
Рис. 31-2. Мигрирующая эритема при эритемной форме иксодового клещевого боррелиоза у взрослого человека в поздней стадии развития.
У 10-15% инфицированных через несколько недель развивается вторая стадия (диссеминация боррелий). Присоединяются серозный менингит (головная боль, тошнота, рвота, светобоязнь в сочетании с невропатией лицевого нерва или других ЧН; в ликворе - умеренный лимфоцитарный плеоцитоз, увеличение содержания белка, лёгкое снижение концентрации глюкозы) и/или другие признаки поражения нервной системы (периферической и центральной) в виде вялотекущего энцефалита, миелита, радикулоневрита или мононеврита, менингорадикулита с характерными симптомами нарушения функций этих структур нервной системы (интенсивные корешковые боли, наруmения чувствительности, периферические и центральные парезы, менингеальные знаки и т.п.). Возможно сочетание с признаками поражения сердца и сосудистой системы (кардиалгия, сердцебиение, артериальная гипертензия, миокардит, нарушения проводимости вплоть до атриовентрикулярной блокады), печени (безжелтушный нетяжёлый гепатит) и редко конъюнктивиты, ангины, бронхиты, орхиты, нефриты.
Третья стадия (персистенции) формируется через 1-3 мес (иногда через 6-12 мес) после окончания первых 2 фаз. Болезнь приобретает длительное рецидивирующее течение. Клиническая картина про является головной болью, нарушениями сна, повышенной утомляемостью, слабостью, лёгкой возбудимостью, раздражительностью или депрессией (астеновегетативный синдром), миалгиями, мигрирующими артралгиями. У 10% больных развиваются признаки хронического энцефаломиелита с парезами конечностей (центрального или смешанного типа) , проводниковыми нарушениями чувствительности, множественными мононевритами, расстройствами памяти и других когнитивных функций. Возможны кератиты, передние увеиты, невриты зрительных нервов, ретинальные васкулиты и др.
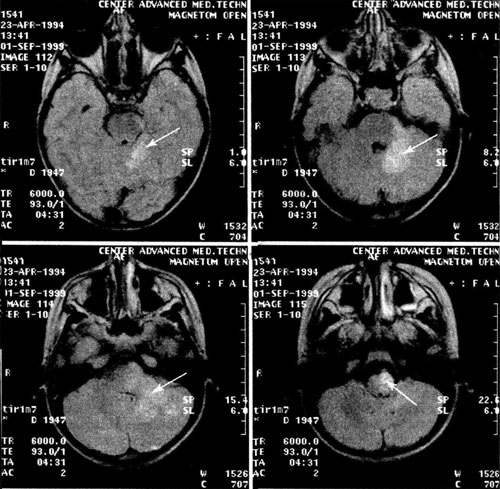
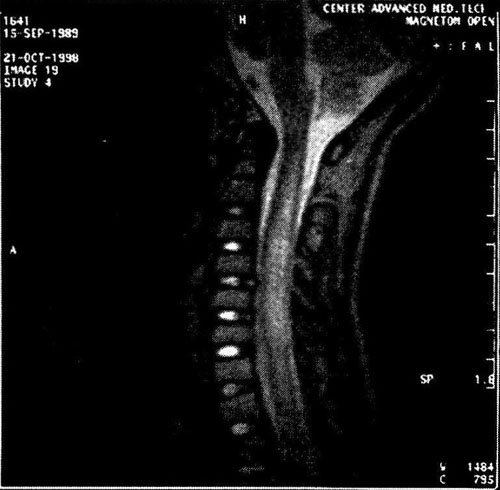
Изменения вещества головного и спинного мозга обнаруживают при МРТ (рис. 31-4, 31-5).
Рис. 31-4. Больная Г., 5 лет. Диагноз: иксодовый клещевой боррелиоз с поражением ЦНС (энцефалит), острое течение. МРТ головного мозга (FLAIR). Очаги патологического сигнала в мозжечке, ножках мозжечка, мосту, продолговатом мозге (указаны стрелками).
Рис. 31-5. Больной Г., 8 лет. Диагноз: диссеминированный миелит, вызванный боррелиями, острое течение. МРТ спинного мозга. Очаг воспаления в шейных сегментах.
Диагностика
Кроме типичной клинической картины и выявления фазности её течения помогают диагностике реакция непрямой иммунофлюоресценции для выявления антител к боррелиям, а также полимеразная цепная реакция для выявления ДНК боррелий в сыворотке, ликворе, синовиальной жидкости, тканях. Дифференциальную диагностику проводят с клещевым энцефалитом, рассеянным склерозом, другими вирусными нейроинфекциями.
Лечение
Этиотропная терапия заключается в раннем назначении антибактериальных средств широкого спектра действия, предпочтительно из группы цефалоспоринов III поколения с последующим использованием пролонгированных пенициллинов (бензатина бензи.riпенициллин, бензатнна бензилпенициллин + бензилпенициллин прокаина) 1 раз в 7-14 дней в течение 1-6 мес в зависимости от тяжести заболевания и характера течения. Лечение хронического иксодового клещевого боррелиоза про водят цефалоспоринами III поколения в течение 14 дней с последующим введением бензатина бензилпенициллина на протяжении 6 мес.
Течение и прогноз
Раннее начало антибактериальной терапии позволяет сократить длительность клинического течения и предупредить развитие поздних стадий боррелиоза с неврологическими проявлениями. Если имеются признаки поражения нервной системы, прогноз малоблагоприятный.
Профилактика
Неспецифические меры профилактики направлены на то, чтобы предотвратить нападение клещей. Профилактическая антибактериальная терапия после укуса клеща целесообразна при раннем обследовании клеща (методом иммуноферментного анализа или полимеразной цепной реакции) и при обнаружении боррелий. у взрослых использование Доксициклина по 0,1 мг 1 раз в сут в течение 5 дней, а также цефтриаксона по 1 г 1 раз в сут 3 дня - довольно эффективная мера предотвращения иксодового клещевого боррелиоза.
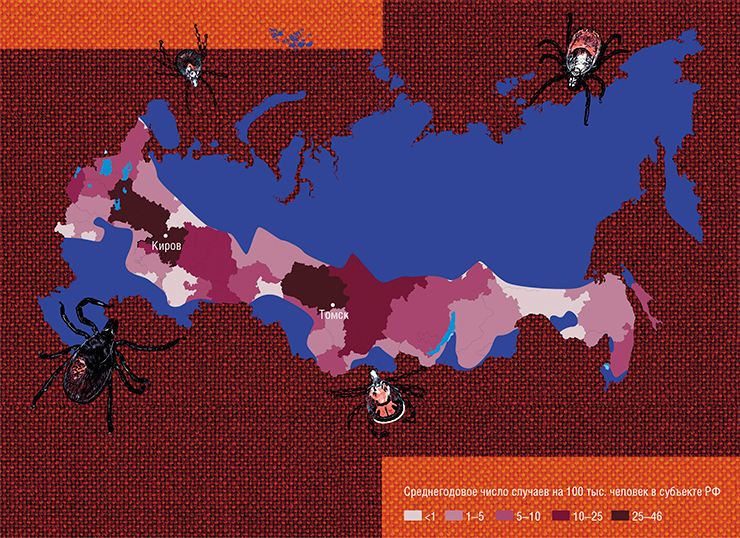
Клещевым боррелиозом (болезнью Лайма) ежегодно заражаются тысячи людей в разных странах мира, в первую очередь в России и США. Так, в 2017 г. в США было официально зарегистрировано около 60 тыс. случаев заболевания клещевыми инфекциями, и в 82 % это была болезнь Лайма. Однако, по некоторым оценкам, истинная заболеваемость клещевым боррелиозом может быть на порядок выше. В большинстве случаев заболевшие успешно излечиваются антибиотиками, однако у 10–20 % болезнь переходит в тяжелую хроническую форму. Почему это происходит, специалисты не могут понять до сих пор. Трудность диагностики клещевого боррелиоза и широкий спектр симптомов приводят к тому, что врачи порой затрудняются с постановкой диагноза и своевременным назначением лечения больным, которые обращаются за медицинской помощью
Клещевой боррелиоз, или болезнь Лайма, – это переносимое иксодовыми клещами мультисистемное инфекционное заболевание с самыми разными проявлениями: кожными, суставными, неврологическими, кардиологическими и т. д. Первые симптомы возникают в течение нескольких дней или недель после укуса клеща, а поздние могут проявиться через месяцы и годы после заражения. При этом как симптомы, так и само течение болезни у разных людей могут значительно варьировать.
В месте укуса инфицированного клеща через несколько дней может образоваться покраснение, которое расширяется в виде кольца и мигрирует по телу. Это так называемая мигрирующая эритема – яркое свидетельство локального размножения и распространения возбудителей инфекции, бактерий спирохет. Однако такое характерное покраснение развивается далеко не у всех заболевших, поэтому отсутствие эритемы не означает меньший риск развития болезни у человека, укушенного клещом. При этом 30—40 % таких больных даже не замечают укус клеща, который стал причиной болезни.
В любом случае постановка клинического диагноза в ряде случаев невозможна без лабораторного подтверждения. Однако применяющиеся сегодня иммуноферментные тесты для диагностики боррелиоза несовершенны. Стандартный иммуноферментный тест регистрирует не самих боррелий, а антитела, вырабатываемые против них организмом, которые появляются лишь спустя 3—4 недели после заражения. Поэтому такие тесты часто оказываются ложноотрицательными, в первую очередь у пациентов, иммунная система которых не дала сильного иммунного ответа. Эти тест-системы нередко дают и ложноположительные результаты. Более трудоемкие анализы, основанные на определении нескольких бактериальных белков, также не дают абсолютно достоверных результатов.
Таким образом, лабораторные тесты могут подтвердить диагноз, но отрицательный результат не может считаться доказательством отсутствия боррелиоза. Поэтому врач должен проанализировать всю картину заболевания у конкретного пациента. Сделать это непросто, так как, к примеру, симптомы поражения головного мозга при боррелиозе похожи на симптомы нескольких нейродегенеративных заболеваний. А такие признаки, как слабость и головная боль, могут сопутствовать самым разным болезням, и не только инфекционным.
Считается, что у людей с нормально функционирующей иммунной системой заражение боррелиями вызывает активный иммунный ответ, так что бактерии могут погибнуть даже без стандартной для этого заболевания терапии. Для лечения болезни Лайма сегодня применяют антибиотики, наилучшие результаты дают цефтриаксон и доксициклин. Современная медицина предусматривает профилактическое применение антибиотиков для людей с высокой вероятностью заражения (укушенных клещом, с мигрирующей эритемой и т. п.) и двух-трехнедельный курс антибиотикотерапии при развитии заболевания.
Несмотря на все эти меры, у некоторых больных болезнь переходит в хроническую форму, при которой не помогают даже повторные курсы антибиотиков. И здесь возникает трудность, связанная с определением причин этого болезненного состояния. Недостаточность знаний о механизмах повреждения организма в результате инфицирования боррелиями, об устойчивости бактерий к лекарствам, а также ненадежность современных методов клинической диагностики привели к появлению разных, полярных точек зрения на эту проблему.
Болезнь или синдром?
О проблеме клещевого боррелиоза спорят не только доктора – нет единства и среди ученых.
Согласно одной из точек зрения, с помощью стандартной антибиотикотерапии не удается уничтожить всех возбудителей болезни в организме пациентов со слабой иммунной системой. Это мнение подтверждается экспериментами на лабораторных животных: живые боррелии обнаруживались после лечения антибиотиками в организме инфицированных лабораторных мышей и обезьян. Результаты некоторых исследований говорят о том, что колонии боррелий, возможно, продолжают жить в органах и тканях в составе так называемых биопленок – сообществ микроорганизмов, заключенных в продуцируемый ими полимерный матрикс. В таком виде боррелии становятся практически недоступными для лекарств и клеток иммунной системы.

На ранней стадии заболевания клещевым боррелиозом люди могут испытывать самые разнообразные простудоподобные симптомы: лихорадку, усталость, нарушения сна, увеличение лимфатических узлов. В дальнейшем, при отсутствии лечения, могут отекать и болеть суставы, особенно коленные. Возникают неврологические проблемы (энцефалит, менингит, временный паралич лицевых мышц), а также нарушения функций мускулатуры, миозиты.
На поздних стадиях заболевания симптомы сильно варьируют. У некоторых больных появляются нарушения сердечного ритма, наблюдаются воспаления глаз, печени, появляется сильная слабость. Среди неврологических осложнений – тяжелая депрессия, нарушения памяти, бессонница, частая головная боль, непереносимость света или звуков, галлюцинации, энцефаломиелит и т. п.
Согласно другой точке зрения, после курса антибиотикотерапии в организме не остается живых боррелий. Однако за время болезни бактерии успевают вызвать нарушения в работе иммунной системы, которые проявляются еще долгое время в виде аутоиммунных поражений. Сильными иммуногенами являются, к примеру, пептидогликаны клеточной стенки бактерий, которые могут долго сохраняться в организме. Долгосрочные токсические эффекты могут вызывать и остатки биопленок с погибшими боррелиями. Все эти бактериальные компоненты провоцируют воспалительные процессы, затрагивающие различные органы и ткани, что приводит, например, к артриту. Подобное болезненное состояние назвали пост-Лайм синдромом (Blaut-Jurkowska, Jurkowski, 2016).
Кстати сказать, ряд специалистов считает, что хроническая болезнь Лайма развивается в случае, когда пациент поражается одновременно боррелиями и другими патогенами, переносимыми клещами (например, риккетсиями). Клещи очень часто переносят одновременно возбудителей разных инфекций, и некоторые из них вызывают симптомы, клинически трудно различимые.
Скрестили шпаги
С такой позицией не согласны тысячи людей в США, годами страдающие от тяжелых заболеваний, которые они связывают с последствиями клещевых инфекций. Хроническая болезнь Лайма впервые была отмечена в США еще 45 лет назад: по некоторым оценкам, число таких больных сегодня достигает 400 тыс. человек. Эти люди совместно с некоторыми врачами организовали Международное общество борьбы с болезнью Лайма и ассоциированными заболеваниями, которое предлагает применять агрессивную антибиотикотерапию при подозрении на то, что наблюдаемые болезненные симптомы вызваны боррелиозной инфекцией.
Защитники официальной точки зрения считают, что сама хроническая болезнь Лайма выдумана недобросовестными врачами, эксплуатирующими отчаянное состояние пациентов с неопределенным диагнозом. По их мнению, те пациенты, у которых современные методы диагностики не выявляют боррелий, нуждаются не в дополнительном лечении, а в помощи психиатра. В результате люди, считающие себя хроническими больными, вынуждены обращаться к врачам, несогласным с позицией медицинских властей, и лечиться за свой счет.
Истина где-то посередине?
К примеру, недавно были получены экспериментальные доказательства, что пациенты с пост-Лайм синдромом страдают не какими-то психологическими расстройствами, а вполне конкретными поражениями головного мозга. В их крови, а также в восьми отделах мозга было обнаружено повышенное содержание белка, служащего маркером воспалительного процесса. При этом в течение полугода после курса антибиотикотерапии эти люди ощущали сильную слабость, неспособность концентрировать внимание; страдали нарушениями памяти и когнитивных функций (Coughlin, Yang, Rebman et al., 2018). Из-за воспалительных процессов и повреждений, связанных с боррелиозной инфекцией, подобные неврологические симптомы могут сохраняться неделями и месяцами даже после длительного начального курса антибиотиков.
Однако в редких случаях хронического боррелиоза дополнительная антибиотикотерапия все же оказывалась эффективной. Вероятно, у некоторых пациентов в организме после стандартного либо запоздалого или неполного курса лечения действительно могут сохраняться живые боррелии, т. е. речь идет именно о хронической инфекции. Напомним, что лабораторная диагностика боррелиоза сегодня ненадежна. Кроме того, в случае хронического боррелиоза инфекционные агенты могут находиться в основном внутри нейронов, т. е. за гематоэнцефалическим барьером. А диагностические системы обладают низкой чувствительностью и непригодны для использования у пациентов, у которых количество бактерий в крови невелико.
Так что все зависит от ситуации, и в некоторых случаях речь может идти о реальном хроническом инфекционном заболевании, а в некоторых – о развитии пост-Лайм синдрома после перенесенной болезни.
Биосенсор – для клеща, ПЦР – для людей
Одна из главных проблем с клещевым боррелиозом связана с его диагностикой на ранних стадиях развития болезни. Ведь чем раньше можно начать лечение, тем больше будет шансов избежать перехода болезни в хроническую форму.
Сегодня существует прямой метод обнаружения боррелий в крови на ранней стадии развития инфекции. Это ПЦР-диагностика, детекция бактериальной ДНК с помощью полимеразной цепной реакции. Однако простые варианты этого метода недостаточно чувствительны, а высокочувствительные, основанные на комбинации ПЦР и масс-спектрометрии, слишком сложны и дороги для применения в клинике. Недавно американская компания Ceres Nanosciences разработала еще один прямой метод обнаружения боррелий в организме. Для этого используются специальные наночастицы, на которые осаждаются бактериальные молекулы-антигены из больших объемов мочи пациента. После такого концентрирования антигены могут определяться с помощью обычного иммунного анализа (Magni, Espina, Shah et al., 2015).
Команда студентов Московского государственного университета имени М. В. Ломоносова совместно со специалистами из Института молекулярной биологии имени В. А. Энгельгардта РАН (Москва) и других исследовательских организаций приступила к разработке экспресс-диагностики зараженности боррелиозом самого переносчика болезни – иксодового клеща.
БОРРЕЛИОЗ – ПРИЧИНА НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ? Группа американских исследователей выдвинула гипотезу о связи между заражением боррелиозом и развитием нейродегенеративных заболеваний. Их натолкнуло на эту мысль сходство симптомов, наблюдаемых на поздних стадиях заболевания болезнью Лайма, с симптомами, характерными для болезни Альцгеймера, болезни Паркинсона и даже аутизма (MacDonald, 2006; Miklossy, 2008, 2015). В пользу этой гипотезы говорит и тот факт, что боррелии, как и их близкие родственники трепонемы – возбудители сифилиса, способны проникать в мозг и приводить к поражениям, характеризующимся как нейроборрелиоз (Lapenta, 2018).
Боррелии были действительно обнаружены в тонких срезах мозга пациентов, умерших от нейродегенеративных заболеваний. По мнению авторов этой работы, биопленки боррелий находились внутри амилоидных бляшек, аналогичных тем, что наблюдаются у пациентов с болезнью Альцгеймера (Miklossy, 2016). Было выдвинуто предположение, что именно иммунный ответ на эти биопленки и приводит к развитию болезни Альцгеймера, при этом человек может быть инфицирован трепонемами или боррелиями задолго до поражения мозга. Однако убедительных подтверждений эти предположения не получили.
Исследования в Национальных институтах здоровья США не выявили маркеров боррелиоза у таких больных. Но главным аргументом стал анализ распространения болезней по территории страны, так как болезнь Лайма, в отличие от нейродегенеративных болезней, встречается лишь в нескольких штатах на Восточном побережье США (Forrester, Kugeler, Perea et al., 2015). Не было получено убедительных данных и о связи боррелиоза с другими нейродегенеративными заболеваниями
До сих пор клеща, снятого с тела, приносят в специализированную лабораторию, где инфекционный агент детектируется с помощью ПЦР или иммуноферментного анализа. Анализ занимает несколько часов и может быть выполнен только в условиях лаборатории. Принцип действия нового биосенсора основан на поиске ДНК боррелий в образце с помощью молекулярных генно-инженерных конструкций, созданных на базе системы, сконструированной из компонентов известного молекулярного комплекса для редактирования генома CRISPR/Cas.
В состав этой бинарной системы входят две молекулы РНК, комплементарные двум соседним последовательностям в бактериальной ДНК. Эти РНК несут два белка, которые являются составными частями фермента бета-лактамазы. Если в исследуемом образце есть ДНК боррелий, РНК свяжутся с ней, и белковые субъединицы сблизятся, сформировав комплекс с ферментативной активностью, в результате чего в присутствии определенного субстрата в растворе будет синтезироваться красящее вещество. Окрашивание раствора можно зарегистрировать с помощью простейшего портативного спектрофотометра.
На сегодня ситуация с хроническим боррелиозом остается тревожной. Слишком много нерешенных вопросов, связанных с диагностикой и рекомендациями по терапии пациентов, заболевших этой клещевой инфекцией.
Один из наиболее спорных вопросов: надо ли спешить с применением антибиотиков после укуса клеща. Среди официальных рекомендаций есть и такая: если клещ присасывался менее чем на сутки, опасности инфекции практически нет. Но все дело в том, что заболевшие боррелиозом порой вообще не помнят контакта с клещом – заразить могут и нимфы, которых можно просто не заметить, и самцы, которые наносят лишь кратковременные укусы. При этом большинство врачей в США и европейских странах считают, что если характерные симптомы заболевания в первые дни после заражения отсутствуют, то и антибиотикотерапию проводить не следует. С этим трудно согласиться, учитывая, что развитие инфекции может привести к долговременным нарушениям работы многих систем организма.

Ответы на все эти вопросы мы получим лишь тогда, когда ученые разберутся со сложными загадками коварной бактерии. До этих пор шарлатаны могут обирать пациентов, а страховые компании – уклоняться от выплат больным. Но для проведения полноценных научных исследований клещевых инфекций, разработки эффективных средств диагностики и терапии требуется достаточное финансирование.
В США сами больные совместными усилиями пытаются через Конгресс повлиять на ситуацию с финансированием работ по изучению болезни Лайма. Подобное движение в свое время возникло из-за эпидемии СПИДа, и в результате были приняты действенные меры по организации интенсивных исследований ВИЧ. И сегодня эта болезнь уже не является смертельным приговором. Если приложить аналогичные усилия к изучению клещевого боррелиоза, то очень скоро он уже не будет представлять такую угрозу для нашего здоровья, как сейчас.
Фоменко Н. В. Клещевой боррелиоз: болезнь на всю жизнь? // НАУКА из первых рук. 2007. Т. 15. № 3. С. 44–51.
Ливанова Н. Н. Восьминогие вампиры // НАУКА из первых рук. 2006. Т. 11. № 5. С. 106–109.
Embers M. E., Narasimhan S. Vaccination against Lyme disease: past, present, and future // Frontiers in Cellular and Infection Microbology. 2013. V. 3(6). DOI: 10.3389/fcimb.2013.00006
Forrester J. D., Kugeler K. J., Perea A. E. et al. Geographic Correlation between Lyme Disease and Death Due to 4 Neurodegenerative Disorders, United States, 2001–2010 //Emerg Infect Dis. 2015. V. 21(11). P. 2036–2039.
Blaut-Jurkowska J., Jurkowski M. Post-Lyme disease syndrome //Pol Merkur Lekarski. 2016. V. 40(236). P. 129–133.
Miklossy J. Historic evidence to support a causal relationship between spirochetal infections and Alzheimer’s disease // Front Aging Neurosci. 2015. V. 7(46).
Lapenta J. M. Lyme Disease and Dementia, Alzheimer, Parkinson, Autism, an Easy Way to Destroy your Brain //Investigative Dermatology and Venereology Research. 2018. V. 4. N. 1. P. 30–43.
Coughlin J. M., Yang T., Rebman A. W. et al. Imaging glial activation in patients with post-treatment Lyme dis-ease symptoms: a pilot study using [11C]DPA-713 PET // Journal of Neuroinflammation. 2018. V. 15(1). DOI: 10.1186/s12974-018-1381-4.
Читайте также: