Спазм мышц денервация нервов
а) Определения:
• Вторичное повреждение мышц, вызванное их денервацией вследствие повреждения нерва
б) Визуализация:
1. Общие характеристики:
• Наиболее значимый диагностический признак:
о Диффузное усиление интенсивности сигнала в Т2, STIR при сохранении целостности мышечных волокон
• Размеры:
о Острая денервация: ± увеличение объема мышцы вследствие отека
о Хроническая денервация: атрофия мышцы
2. КТ при денервации мышц:
• При острой денервации мышцы выглядят нормально
• ± минимальное увеличение объема мышцы ± контрастное усиление (острая денервация)
• Снижение объема, гиподенсная жировая перестройка (хроническая денервация)
4. Другие методы исследования:
• Игольная электромиография (ЭМГ):
о Изменения электрической активности мышцы обычно появляются только через три недели после травмы иннервирующего ее нерва
5. Рекомендации по визуализации:
• Наиболее оптимальный метод диагностики:
о МРТ
• Протокол исследования:
о Плоскости сканирования необходимо выбирать таким образом, чтобы видеть поперечные сечения мышц
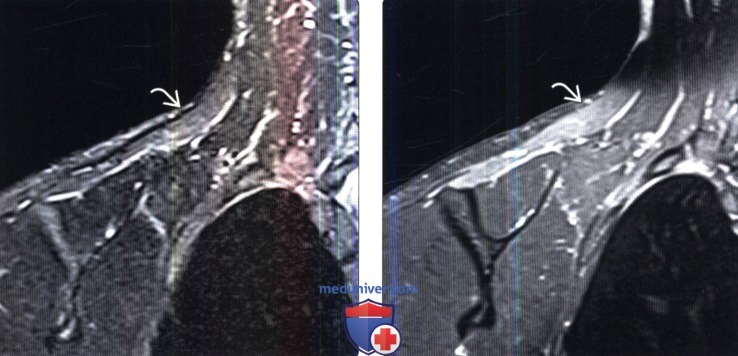
(Слева) На фронтальном STIR МР-И определяются признаки денервационного отека трапециевидной мышцы, иннервируемой спинальными корешками добавочного нерва. Этот нерв может быть травмирован при ношении на плече тяжелого груза.
(Справа) На фронтальном FS Т1-ВИ с КУ у этого же пациента отмечается равномерное контрастное усиление пораженной мышцы. Разрывы мышцы в отличие от подобной картины характеризуются неоднородной картиной.
в) Дифференциальная диагностика денервации мышц:
1. Атрофия от неиспользования:
• Жировая атрофия мышцы
• Отек обычно отсутствует
2. Травма мышцы:
• Разрыв/нарушение целостности мышечных волокон
• Гематома обычно характеризуется неоднородностью сигнала в Т2, STIR
3. Разрыв сухожилия:
• Разрывы сухожилий мышц в конечном итоге также ведут к атрофии мышцы
4. Воспалительные изменения или инфекционное поражение мышцы:
• Патологические изменения Т2-сигнала и контрастное усиление выглядят более неравномерно
• Различные причины:
о Полимиозит/дерматомиозит
о Инфекционный миозит
о Диабетический мионекроз
о Рабдомиолиз
о Серповидноклеточный криз
5. Постлучевая миопатия:
• Васкулит, повреждение тканей → гомогенный отек мышцы
• Четкие границы отека, соответствующие области облучения
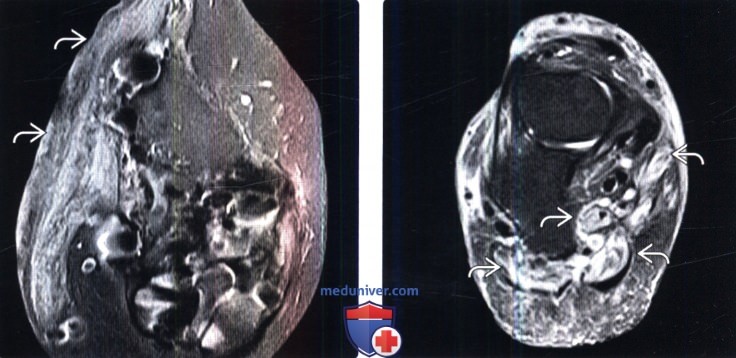
(Слева) Аксиальный срез, FS Т2-ВИ: свободный мышечный лоскут голени. Мышца с признаками выраженного диффузного отека и минимальным числом жировых включений. Это вполне ожидаемая картина, которую не следует путать с инфекционным поражением.
(Справа) Нa фронтальном FS Т2-ВИ определяются признаки денервационного отека собственных мышц стопы. Денервационный отек на фоне сахарного диабета характеризуется поражением в первую очередь мышц стопы. Мышцы в этой ситуации выглядят более исчерченными и менее гомогенными, чем при денервации другой этиологии.
г) Патология. Общие характеристики:
• Этиология:
о Опухоль нерва, инфекция, аутоиммунный неврит, периферическая нейропатия или травма
д) Клинические особенности:
1. Клиническая картина:
• Наиболее распространенные симптомы/признаки:
о Слабость, снижение объема мышц в зоне иннервации поврежденного нерва
о Может сопровождаться болевым синдромом
2. Течение заболевания и прогноз:
• При острой денервации в зависимости от тяжести повреждения нерва может наступать частичное или полное восстановление
• При хронической денервации изменения носят перманентный характер
3. Лечение денервации мышц:
• Лечение причин нарушения нервной проводимости, если это возможно
• Физиотерапия, направленная на укрепление сохранившихся мышечных групп
е) Диагностическая памятка. Советы по интерпретации изображений:
• Локализация изменений мышц напрямую говорит о локализации повреждения нерва
ж) Список использованной литературы:
1. Gupta A et al: MRI diagnosis of muscle denervation from herpes zoster with discordant distribution of the skin rash. Skeletal Radiol. 43 (10):1481 -5, 2014
2. Mosole S et al: Long-term high-level exercise promotes muscle reinnervation with age. J Neuropathol Exp Neurol. 73(4):284-94, 2014
3. Ohana M et al: Current and future imaging of the peripheral nervous system. Diagn Interv Imaging. 95(1):17-26, 2014
4. Hu ZJ et al: Effect and possible mechanism of muscle-splitting approach on multifidus muscle injury and atrophy after posterior lumbar spine surgery. J Bone Joint Surg Am. 95(24):e192(1-9), 2013
5. Sedano MJ et al: Muscle MRI in severe Guillain-Barre syndrome with motor nerve inexcitability. J Neurol. 260(6): 1 624-30, 2013
6. BercianoJ et al: Magnetic resonance imaging of lower limb musculature in acute motor axonal neuropathy. J Neurol. 259(6): 1 111-6, 2012
7. Viddeleer AR et al: Seguential MR imaging of denervated and reinnervated skeletal muscle as correlated to functional outcome. Radiology. 264(2):522-30, 2012
8. Kim SJ et al: MR imaging mapping of skeletal muscle denervation in entrapment and compressive neuropathies. Radiographics. 31(2):319-32, 2011
9. Haig AJ: Paraspinal denervation and the spinal degenerative cascade. Spine J. 2(5):372-80, 2002
- Вернуться в оглавление раздела "Лучевая медицина"
Редактор: Искандер Милевски. Дата публикации: 10.9.2019
В клинической практике Д. используется как метод лечения невритов и невралгий (напр., при некупирующейся невралгии тройничного нерва), каузалгии, фантомных болей, кишечных и бескаменных желчных колик, расстройств трофики (трофические язвы конечностей) и периферического кровообращения (ангионевроз, болезнь Рейно) и др. В физиол, исследованиях Д. используют для изучения зависимости каких-либо органов от влияния нервной системы и в целях раздельного изучения нервных и гуморальных влияний. Д. является одним из основных методов исследования эволюции функций. Применение этого метода, в частности, позволило Л. А. Орбели (1934) сформулировать положение об эволюции мышечной ткани, согласно к-рому мышца, лишенная моторной иннервации, возвращается к более примитивному состоянию, сходному с эмбриональным.
Д. достигается путем перерезки всех видимых нервных ветвей, применения различных хим. веществ (никотин, атропин, новокаин, этиловый спирт, фенол, декаметоний, тубокурарин и др.), физ. воздействий, нарушающих проведение возбуждения по нервным волокнам и в синапсах (напр., холодовый блок), использованием иммунологических методов и др.
В исследованиях, проведенных на гладких и скелетных мышцах, железах, сердце, нейронах вегетативных ганглиев, спинного и головного мозга различных животных было обнаружено, что через нек-рое время после Д. органы и ткани приобретают повышенную чувствительность к действию хим. веществ и поступающих нервных импульсов.
У. Кеннон сформулировал закон денервации (1935), позднее расширенный Розенблютом и Гарсией Рамосом (A. S. Rosenblueth, J. Garsia Ramos, 1945). По этому закону, если одно из звеньев функциональной цепи нейронов прервано, то общая или частичная Д. последующих звеньев в цепи приводит к повышению чувствительности всех дистальных элементов (включая и денервированные структуры и эффекторы); повышение чувствительности больше в звеньях, которые непосредственно примыкают к перерезанным нейронам, и меньше в более отдаленных элементах. Такое повышение чувствительности обусловлено многими механизмами. Так, после Д. мышечных волокон отмечается появление холинорецепторов на всей поверхности волокна; выявляются также изменения во взаимном расположении холинорецепторов. Д. сопровождается глубокими биохим, и структурными изменениями денервированного органа. Клинически Д. может проявляться в виде различных двигательных (параличи, контрактуры, гиперкинезы), трофических (трофические язвы, дистрофия, изменение потоотделения) и чувствительных нарушений. Одними из тяжелейших видов повышения и извращения чувствительности являются каузалгии и фантомные боли.
Г. Н. Сорохтиным и его сотр. (исследования в 1945—1973 гг.) показано, что в результате обратимой или необратимой Д. в различных органах и тканях, таких как скелетная мышца, слюнная железа, симпатический ганглий, дыхательный центр и другие, возникает особое состояние (так наз. дефицит возбуждения), связанное с прекращением поступления нервных импульсов. Оно характеризуется развитием состояния пассивной гиперполяризации и в зависимости от морфол, и функциональных особенностей структуры органов и тканей сопровождается повышенной или пониженной возбудимостью.
Библиография: Кеннон В. и Розенблют А. Повышение чувствительности денервированных структур, Закон денервации, пер. с англ., М., 1951; Михель-сонМ. Я. иЗеймаль Э. В. Ацетилхолин, о молекулярном механизме действия, Л., 1970, библиогр.; Орбели Л. А. Избранные труды, т. 1,с. 59, М.—Л., 1961; Сорохтин Г. Н. Реакция возбудимых систем на дефицит возбуждения, М., 1968; Физиология сенсорных систем, ч. 3, Физиология механорецепторов, под ред. О. Б. Ильинского, Л, 1975.
При денервации в тканях возникают биохимические, структурные и функциональные изменения.
Патогенные воздействия на периферический нерв всегда сопровождаются изменением обмена веществ в соответствующем органе. Это касается углеводов, жиров, белков, нуклеиновых кислот и т. д. Наблюдаются не только количественные, но и качественные изменения. Так, миозин в денервированной мышце утрачивает свои АТФазные свойства, а гликоген по своей структуре становится проще, элементарнее. Наблюдается перестройка ферментативных процессов. Так, изоферментный спектр лактатдегидрогеназы меняется в пользу ЛДГ4 и ЛДГ5, т. е. тех ферментов, которые адаптированы к анаэробным условиям. Падает активность такого фермента, как сукциндегидрогеназа. Общая же тенденция изменений метаболизма состоит в том, что он приобретает "эмбриональный" характер, т. е. в нем начинают преобладать гликолитические процессы, тогда как окислительные падают. Ослабевает мощность цикла Кребса, уменьшается выход макроэргов, понижается энергетический потенциал.
В тканях при нарушении иннервации возникают существенные морфологические изменения. Если речь идет о роговице, о коже или слизистых, то здесь последовательно развиваются все стадии воспаления. Устранение инфекции, травмы, высыхания не предотвращает процесс, но замедляет его развитие. В итоге развивается язва, не имеющая тенденции к заживлению(трофическая язва). Исследование тонкой структуры показало изменение органелл. Митохондрии уменьшаются в количестве, их матрикс просветляется, в результате снижаются энергетические возможности клетки. В денервированных тканях снижается и митотическая активность.
Что касается функциональных расстройств при развитии нейродистрофического процесса, то последствия денервации будут разными в зависимости от того, о какой ткани идет речь. Например, скелетная мышца при денервации утрачивает свою главную функцию – способность сокращаться. Сердечная мышца сокращается даже при перерезке всех экстракардиальных нервов. Слюнная железа будет секретировать слюну, но характер ее уже не будет зависеть от вида пищи.
Гораздо интереснее то обстоятельство, что денервированная ткань реагирует на многие гуморальные факторы иначе, чем нормальная. Речь идет прежде всего о медиаторах нервной системы. Установлено, что скелетные мышцы, лишенные симпатических нервов, реагируют на адреналин не меньше, а больше, чем в норме, те же мышцы, отъединенные от моторных (холинэргических) нервов, реагируют на ацетилхолин сильнее, чем в норме. Так был открыт закон денервации, что означает повышенную чувствительность денервированных структур. В частности, это связано с тем, что холинорецепторы, которые в нормальных мышцах сосредоточены только в области мионевральных синапсов, после денервации появляются на всей поверхности мембраны миоцита. Теперь известно, что необычность ответа денервированных структур состоит не только в повышении, но и в извращении, когда, например, вместо расслабления сосудистых мышц получается их сокращение.
При денервации в мышце и других тканях появляются свойства, присущие ранним, в частности, эмбриональным стадиям развития. Это явление возникает как результат патологического растормаживания супрессированных в норме генов.
Нарушения двигательной функции. Гипокинезии. Параличи и парезы. Причины возникновения. Сравнительная характеристика центральных и периферических параличей. Паркинсонизм.
При участии нервной системы происходят осуществление и регуляция двигательной активности – какнепроизвольной (рефлекторной), так и произвольной.
Как известно, сокращение скелетных мышц, его сила, продолжительность, скорость зависят от уровня возбуждения α-мотонейронов спинного мозга. К каждому мотонейрону поступают многочисленные импульсы от чувствительных нервов, нейронов, расположенных в различных сегментах спинного мозга, стволе головного мозга, мозжечке, базальных ядрах, коре головного мозга. Эти нервные структуры регулируют активность мотонейронов как непосредственно, так и влияя на интернейроны спинного мозга и γ-мотонейроны. При возбуждении γ-мотонейронов возбуждение передается через чувствительные нейроны на α-мотонейроны, вследствие чего возникает тоническое сокращение мышц. Большинство регулирующих влияний в различных разделах нервной системы на тонус мышц осуществляется посредством γ-мотонейронов. Эти влияния регулируют осанку и координируют деятельность различных групп мышц при выполнении целенаправленного двигательного акта.
Двигательные расстройства возникают вследствие повреждения указанных отделов ЦНС, а также нарушения проведения импульсов по двигательным нервам, передачи импульсов с нерва на мышцу.
Нарушения двигательной активности сопровождаются различными симптомами гипокинезии и гиперкинезии.
Гипокинезии (в том числе акинезия)-нейрогенные расстройства движений, характеризующийся ограничением объёма, количества и скорости движений, которые проявляются наличием параличей, парезов, скованностью активных движений.
По выраженности ограничения произвольных движений гипокинезии подразделяются на парезы и параличи.
Дата добавления: 2018-08-06 ; просмотров: 1310 ;
Вопрос о влиянии периферической электростимуляции на восстановление нормальной функции мышц переплетается с вопросом о роли периферических факторов вообще в восстановлении функции мышц после денервации.
Известно, что денервированная мышца в значительной мере определяет реиннервацию, т.к. по современным воззрениям, нервное окончание и иннервируемая структура представляет единую энзимохимическую систему.
Поскольку регенерация нерва бывает эффективнее в начальные фазы атрофии мышцы, необходимо предохранять мышцу от атрофии в этот период.
Воздействие на мышцы, сопровождающееся их сокращением, раздражает механорецепторы, хеморецепторы, барорецепторы сосудов, рецепторы сухожилий, связок. При частичных повреждениях периферических нервов эти эффекты оказывают огромное влияние на регуляцию мышечного кровообращения, оказывают определенное влияние на общее кровообращение, усиливают деятельность сердца и дыхательного центра и т.д.
В зависимости от масштабов поражений и степени воздействия (в определенных случаях могут стимулироваться симметричные здоровые мышцы, антагонисты и другие группы, создающие необходимую координацию в работе мышц тела), это воздействие на ткани и сосуды может иметь решающее значение.
Наиболее эффективным методом предупреждения или замедления развития различных атрофий оказалась электростимуляция. В пользу положительной оценки электростимуляции говорят многие экспериментальные исследования конца 30-х середины 60 гг.
А.Н. Студитский считает, что на всех стадиях развития и регенерации у всех обследованных животных в качестве первого условия восстановления соматической мускулатуры выступает натяжение. Применив это положение к бездеятельной мышце, можно сказать, что непременным условием замедления ее атрофии является сокращение.
Как справедливо отмечал П.М. Зубенко сокращением мышцы не исчерпываются все условия для ее нормального существования, но активность является одним из этих существенных условий. Ряд авторов показал весовые различия стимулируемых и нестимулируемых денервированных мышц. Как выяснилось, электростимуляция значительно задерживала прогрессирующую атрофию мышц, которая следует за денервацией.
Работоспособность денервированных мышц, подвергавшихся электростимуляции, гораздо выше, а утомление при работе наступает значительно позже, чем денервированных, но нестимулированных.
Если одну из денервированных мышц раздражать до полного утомления и оставить в покое, то после короткого отдыха стимулированная мышца, несмотря на то, что она предварительно выполнила большую работу, сокращается сильней и больше, чем нестимулированная. П.М.Зубенко говорит, что стимулированная мышца быстрее восстанавливает свою работоспособность потому, что процессы реституции в ней совершаются быстрее.
Электростимуляция денервированной мышцы значительно увеличивает ее кровоснабжение. Содержание миоглобина в денервированной мышце значительно снижено по сравнению с такой же, но стимулированной. Снижена также и доставка кислорода к бездеятельной мышце.
Стимуляция денервированных мышц приводит к увеличению содержания в них креатина, креатинфосфата, АТФ, гликогена, задерживает изменения в белках, уменьшает снижение активности АТФ-фазы, АТФ-креатинфосфоферазы, дегидразы, замедляет повышение активности протеаз. Таким образом, стимуляция, изменяя течение биохимических процессов в мышцах, тем самым задерживает ее атрофию, увеличивает ее работоспособность.
С увеличением времени благоприятное влияние стимуляции на замедление развития атрофии выявляется еще ярче. Так, например, через 3 месяца после операции разница в весе между стимулированными мышцами составляла 19,5%, через 6 месяцев - 53,5%, а через 9 - 93,6%.
Однако, как уже отмечалось, остается не решенным вопрос о продолжительности, частоте и количестве сеансов и числе сокращений или длительности каждого сеанса.
J. Eccles нашел, что стимуляция продолжительностью от 10 сек. до 2 часов предотвращала общую атрофию от бездействия.
Osborne et all сообщили, что электростимуляция по 10 минут, на протяжении 6 дней в неделю задерживает и даже предотвращает атрофию мышц от бездействия; пришли к выводу, что стимуляция 2 раза в день по 30 мин дает больший эффект, чем стимуляция по 5 мин. через каждые 0,5 часа на протяжении рабочего дня.
Нужно отметить, что стимуляция денервированной мышцы электрическим током не полностью задерживает ее атрофию. Здесь, очевидно, имеют существенное значение трофические импульсы нервной системы, которые в условиях целостного организма поступают практически на протяжении всей жизни.
И.П. Павлов в работе "О трофической иннервации" говорит, что это определенные нервные импульсы, которые ведут к регуляции интимного обмена веществ между тканью и окружающей средой. Речь идет о регуляции тонких процессов, которые могут осуществляться и без нервов, но интенсивность и скорость обмена регулируется нервной системой.
При наступлении реинервации мышцы в срок до 12-14 дней электростимуляции не влияет на ее скорость, лишь замедляет атрофию. При более поздней реинервации электростимуляция уже ведет к ускорению этого процесса.
Детальное изучение влияния электростимуляции на денервированные мышцы показало, что предохранение мышцы от атрофии не означает при этом устранения всех вредных последствий денервации. В частности, у стимулируемых мышц, как и у контрольных падает сила сокращения, появляется высокая чувствительность к ацетилхолину и контрактурное сокращение на его воздействие. Эти изменения специфически связаны с утерей трофического воздействия нервной системы на мышцы.
Поддержание на должном уровне обменных процессов в мышцах является фактором, содействующим реиннервации. С этой точки зрения особенно важна для мышцы систематическая работа, независимо от причины, ее обеспечивающей.
Регенерация нерва представляет собой конечный результат сложной цепи процессов и взаимодействий как между различными частями самого нейрона, так и между нейроном и окружающими его тканями, не принадлежащими к нервной системе. Любые изменения каждого из многочисленных условий, играющих роль в проявлении этого конечного результата будут влиять на интенсивность регенерации нерва.
Hyden, раздражая дорсальные корешки спинного мозга "умеренным током" от 1 до 10 минут, нашел, что реакция клеток ганглия на этот ток варьировала в зависимости от продолжительности воздействия и в основном заключалась в повышении количества нисельевского вещества.
Hoffman, раздражая электрическим током корешки спинного мозга, обнаружили ускорение роста нерва. Автор полагает, что под влиянием электрораздражения происходит усиление плазматического синтеза в клеточном ядре. Отсюда вновь образовавшийся материал перемещается на периферию.
Масса нейрона в каждый момент определяется состоянием между этим локальным образованием и повсеместным раздражением и потреблением компонентов протоплазмы. Нейроплазма переходит из перикариона в аксон под влиянием нагнетающего механизма, действующего в центробежном направлении по длине аксона. Движущая сила этого механизма на сегодняшний день не известна.
Weiss говорит, что скорость синтеза нейроплазмы регулируется влиянием с периферии: она повышается или понижается с увеличением или уменьшением массы иннервируемой ткани. После полной пере резки аксона она снижается до минимума.
Т.Н.Несмеянова показала, что систематическое применение кожных электрических и механических раздражений, начатое вскоре после пере резки у собаки спинного мозга, ведет к поддержанию стойкости выработанных спинномозговых рефлексов.
Кроме того, после пере резки спинного мозга у собаки с помощью электрической стимуляции задних лап при максимальном сокращении и потом расслаблении (начиная с 8-10 дня после операции) удалось вызвать различные спинальные рефлексы.
Оперированные и стимулированные собаки могли стоять, самостоятельно вставать и даже передвигаться. Контрольные же собаки обычно, лишь ползали и не могли удержаться в стоячем положении. Морфологические исследования показали, что электрическая стимуляция, начатая вскоре после перерезки спинного мозга, препятствует в какой-то мере, развитию дистрофических процессов в клетках его дистального отрезка.
Через 3, 6 и 12 месяцев после перерезки не наблюдалось видимых изменений основной массы нервных клеток заднего рога. Данные говорят об ответственной роли в рефлекторной дуге афферентного звена. По заключению этих авторов, полученные ими результаты с применением электрической стимуляции позволяют говорить о том, что электростимуляция, помимо благотворного влияния на периферические аппараты, способствует поддержанию клеток спинного мозга в хорошем состоянии.
Как было детально рассмотрено в главе 4, А.В.Паладин, Н.Н.Яковлев и другие показали, что тренировка мышц повышает содержание в них веществ, поставляющих энергию для работы. При этом повышается активность ферментов, что обеспечивает более высокую утилизацию питательных веществ. Д.Л.Фердман с положительным результатом применял для борьбы с атрофией денервированных мышц небольшие дозы монокальциевой соли АТФ.
Одним словом, любые методы воздействия, предохраняющие мышцы от атрофии, содействуют регенерации. Но эффективность этих средств в обеспечении регенерации разная. Поскольку электростимуляцию мы считаем наиболее эффективным средством не только в обеспечении регенерации, но и вообще для воздействия с периферии, мы и обратились к изучению ее воздействия при периферических травмах.
В наших исследованиях главное внимание уделялось мышцам, участвующим в выполнении нарушенных движений. Наложение электродов на кожу над пораженными мышцами предполагало возбуждение кожных афферентов, участвующих избирательно в активации этих мышц по принципу местных рефлексов Шеррингтона. В зависимости от состояния кожи и мышц возбуждающее влияние на них было различным.
При электрической стимуляции атрофирующихся мышц, когда нерв травмирован сдавливанием, неполным разрывом или как-то иначе, но сохраняет часть волокон, можно всегда подобрать такую интенсивность раздражения, которая вызываем возбуждение даже самых высокопороговых волокон. При периферических травмах, осложненных рубцовой тканью и при других повреждениях мы чаще всего сталкиваемся с известным явлением, частичного сохранения некоторых функций, главным образом трофических.
Электрическая стимуляция помимо воздействия на мышцу, оказывает влияние на сохранившиеся нервные волокна. Восстанавливая до нормального уровня трофику кожи, сосудистые реакции, электростимуляция обеспечивает вторично более эффективное возбуждение самих мышц, а через их афференты - центральных структур.
Известно, что электрическое раздражение чувствительных волокон группы С вызывает сильное расширение сосудов, причем даже единственный электрический стимул, достаточный для возбуждения С - волокон, вызывает длительно удерживающееся почти максимальное их расширение. По В.М.Хаютину, именно волокна группы С имеют значение в местных изменениях кровоснабжения поврежденной кожи.
Видимо, раздражение нервных волокон группы С и расширением кожных сосудов можно объяснить постепенное восстановление трофики кожи при электростимуляции. С восстановлением нормальной функции кожи в раздражение с периферии включается у-система, обеспечивающая восстановление трофики мышц и другие процессы.
Воздействие на мышцы, сопровождающиеся их сокращением, раздражает механорецепторы, хеморецепторы, барорецепторы сосудов, рецепторы сухожилий, связок. При частичных повреждениях периферических нервов эти эффекты оказывают огромное влияние на регуляцию мышечного кровообращения, оказывают определенное влияние на общее кровообращение, усиливают деятельность сердца и дыхательного центра и т.д.
В зависимости от масштабов поражений и степени воздействия (в определенных случаях могут стимулироваться симметричные здоровые мышцы, антагонисты и др. группы, создающие необходимую координацию в работе мышц тела), это воздействие на ткани и сосуды может иметь решающее значение.
Дистония — это общий медицинский термин, объединяющий ряд двигательных расстройств, вызывающих мышечные спазмы и сокращения, или же судороги.
Судороги и спазмы могут быть либо замедленными, либо приходящими и уходящими, то есть периодическими. Кроме того, пациентам с дистонией причиняет неудобства положение тела — конечности и голова подвергаются тремору, позы болезненны и неестественны для здорового человека. Тремор является симптомом лишь определенного типа дистонии, этот симптом несвойственен всем подтипам заболевания.
Дистония относится к неврологическим заболеваниям (вызванным проблемами с мозгом и нервной системой). Однако в большинстве случаев функции мозга, такие как интеллект, память, речь и другие – остаются неизменными.
Типы мышечных дистоний
Дистония может воздействовать только на одну мышцу или группу мышц.
Существует пять основных типов дистонии:
- Фокусная.
Затрагивает только одну мышцу или часть тела, например, руки или глаза. К такому типу относится блефароспазм — аномальное подергивание одного века или обоих век, цервикальный спазм, писчий спазм или спазм мышц руки, отвечающих за правильное удерживание ручки или карандаша. В целом, если спазм и судорога охватывает один определенный участок, этот тип дистонии называется фокусной.
- Цервикальная.
- Сегментная.
Относится к двум и более областям тела. Например, шее и ноге, двум ногам, двум рукам и т.д.
- Черепная.
Задействованы мышцы нижней челюсти, языка, подбородка. Вызывает затруднения в процессе глотания пищи, воды, слюны. Может влиять на тембр голоса, общую способность говорить.
- Мультифокальная.
Охвачены два или более участка тела, причем не обязательно связанные между собой.
- Обобщенная.
Локализуется следующим образом: мышцы позвоночника и минимум две конечности или какие-либо два участка тела. Мышцы ног не всегда поражены.
- Гемидистония.
Поражение одной половины тела.
- Медикаментозная.
Может вызывать различные типы дистоний, например, фокусную или мультифокальную. Хорошо поддается лечению. Были зафиксированы случаи, при которых медикаментозная дистония самопроизвольно исчезала за несколько дней при отмене лекарства, вызывающего мышечные спазмы.
- Семейная, несемейная.
Наследственный тип дистонии называется семейным, может наследоваться любой тип из описанных выше. Несемейная означает, что даже при полностью здоровых близких родственниках заболевание проявляется либо с рождения, либо в более поздний период. Причинами такого проявления могут быть различные состояния и синдромы.
- Идиопатическая.
Развивается без очевидных причин, спонтанно.
Различают также классификацию дистонии по типу конечностей или частей тела, которые они поражает.
Примерно 90% случаев всех проявленных дистоний — это цервикальная дистония, затрагивающая мышцы шеи или блефароспазм (веки). Оба подтипа в действительности являются подтипами фокальной дистонии, развиваются в более зрелом возрасте, а не в раннем детстве, и могут поддаваться лечению при своевременной диагностике и комплексном терапевтическом подходе.
Причины дистонии мышц, диагностика
В большинстве случаев мышечная дистония не имеет конкретной причины. Дистония — следствие нарушений работы базальных ганглиев мозга. Эта область мозга отвечает за инициирование сокращения мышц. Основная проблема при данном состоянии — это нарушение сообщения нервных импульсов с мышцами.
Приобретенная дистония всегда является следствием повреждения базальных ганглиев.
Кроме того, причины дистонии могут быть следующими:
- травма мозга;
- инсульт;
- опухоль мозга;
- кислородное голодание;
- инфекционное заболевание (энцефалит, менингит инфекционного характера);
- реакция на медикаменты;
- отравление свинцом;
- токсический эффект монооксида углерода.
Если идентифицируемой причины дистонии нет, она называется первичной.
Вторичная мышечная дистония развивается как симптом основного заболевания или последствие травмы. Общие причины вторичной дистонии это:
- черепно-мозговая травма;
- энцефалит;
- болезнь Паркинсона;
- инсульт;
- менингит.
Тип заболевания определяют по области спастичности. Запущенные состояния диагностируются исходя из внешних признаков, без дополнительных диагностических манипуляций. Для точной диагностики необходимы:
- анализ крови;
- анализ мочи;
- МРТ;
- генетическая экспертиза;
- физический осмотр.
Симптомы дистонии, факторы риска
Симптомы дистонии варьируются в зависимости от типа заболевания и возраста, в котором оно развивается. При раннем начале симптомы проявляются в детстве или подростковом возрасте. Обычно первыми страдают ноги и руки, либо мышцы верхней части тела.
Типы мышц, которые чаще всего поражаются при дистонии:
- мышцы шеи;
- мышцы ног и рук;
- мышцы спины.
Дистония, начинающаяся во взрослом возрасте, поражает шею, руки или голову.
Симптомы ранней мышечной дистонии:
Практически все типы мышечной дистонии схожи по своим симптомам и проявляются интенсивнее при стрессе, плохом самочувствии, усталости, заболеваниях, не связанных с мышцами.
Факторы риска или факторы, из-за которых мышечная дистония усиливается, это:
- стресс;
- бессонница;
- усталость;
- эмоциональная перегрузка;
- большое количество новой информации;
- инфекционные заболевания;
- неврологические нарушения;
- употребление алкоголя;
- употребление кофе и продуктов с кофеином;
- употребление психоактивных веществ;
- наркотическое опьянение.
Методы лечения дистонии мышц, прогноз
Лечение дистонии определяется типом заболевания и точной клинической картиной. Однако существует четыре основных метода лечения, применяемых практически при всех типах:
- ботулинический токсин; широко используется для лечения неврологических состояний, к которым относятся аномальные сокращения мышц, токсин вводится прямо в пораженные мышцы, чтобы временно ослабить или уменьшить спазмы;
- лекарственные препараты; например, антихолинергические препараты, баклофен и миорелаксанты;
- физиотерапия; специальные программы упражнений для улучшения мышечного тонуса и положения тела в пространстве, а также для предотвращения мышечной слабости;
- хирургическое лечение; применяется в том случае, когда другие методы лечения не оказывают ожидаемого эффекта. При таком лечении нервы, контролирующие мышцы, подвергаются селективной периферической денервации.
Еще один метод лечения — временное имплантирование электродов в головной мозг с устройством, похожим на кардиостимулятор (метод глубокой стимуляции мозга).
Препараты, уменьшающие проявления дистонии:
- Леводопа;
- Проциклидина гидрохлорид;
- Диазепам;
- Лоразепам;
- Клоназепам;
- Баклофен.
Прогноз
Дистония — непредсказуемое заболевание. Она имеет тенденцию медленно прогрессировать, и тяжесть симптомов у пациента зависит как от индивидуальных причин, общего состояния здоровья, степени прогресса и общих факторов. Фокальная дистония прогрессирует медленно в течение примерно 5 лет, а затем наступает резкое ухудшение состояния здоровья.
Иногда состояние больного спонтанно улучшается, а симптомы практически или полностью исчезают. Это состояние называется полной ремиссией, происходит оно примерно у 5-10% пациентов. Общая ремиссия свойственна людям с вторичной дистонией, появившейся как следствие приема лекарственных препаратов или стресса, травмы или других факторов. При болезни Паркинсона, например, симптомы высокого мышечного тонуса сохраняются до конца жизни.
Читайте также:


