Гигантские многоядерные клетки при герпесе
Распространенность носительства вируса герпеса в среднем составляет около 20% населения, но только у 5% инфицированных имеются клинические проявления генитального герпеса, в остальных случаях он протекает субклинически или бессимптомно.
Идентифицировано два серотипа вируса простого герпеса (ВПГ) ВПГ-1 и ВПГ-2. Большинство случаев генитального герпеса вызывается ВПГ-2 (70-80%).Однако ввиду широкого распространения орально-генитальных контактов происходит смешение обоих типов герпеса и в 20-30% случаев эта инфекция может обусловливаться ВПГ-1,а ВПГ-2 может вызывать ротоглоточные инфекции
Входными воротами для вируса являются слизистые губ, ротовой полости, носоглотки,
гениталий, ануса, конъюктивы глаза. Наиболее частые пути инфицирования взрослых - половой (все виды половых контактов) и орально-оральный (поцелуи). При традиционном половом контакте риск заражения приблизительно 75 % ,если у полового партнера есть клинические проявления герпеса.
Для детей характерен контакно-бытовой (инфицирование через предметы загрязненные мочой и (или) слюной больного и воздушно-капельный (через инфицированную слюну) пути заражения. Также возможно заражение ребенка внутриутробно (через материнскую кровь) и при родах при прохождении через инфицированные родовые пути. Риск внутриутробного заражения плода может достигать 50% при развитии первичного герпеса у беременной до месяца перед родами
Также возможны и другие пути инфицирования - гемотрансфузионный (при переливании крови и в том числе и при использовании медицинского инструментария) и трансплантационный - при пересадке органов и тканей.
Для течения герпеса характерно несколько стадий ( этапов)
Первичное инфицирование
Развивается после заражения ранее неинфицированного человека. Клинически первичное инфицирование проявляется так называемым первым эпизодом с появлением характерных или атипичных признаков герпеса. Различают
Субклиническую инфекцию, при которой отмечается бессимптомное течение
Инфекцию с одиночным внедрением вируса, при которой выявляется ограниченная область поражения
Инфекцию с множественными входными воротами - поражение происходит одновременно в разных локализациях.
Латентная инфекция
Неактивная стадия, при которой вирус не обнаруживается в биологических материалах, но сохраняется в нервных ганглиях. Может наступать непосредственно после первичного инфицирования либо после первого эпизода герпеса.
Рецидив герпеса
Повторное появление клинических симптомов герпеса после периода латентного (скрытого) течения.
Типичная форма генитальной герпетической инфекции - для типичной формы характерны определенные стадии:
Продромальный период : зуд ,жжение, боли, покалывание. Длительность 24-48 часов
Период высыпаний: Продолжительность от 3 до 7 дней
Период регресса: образование корочек ,а затем участков проходящей гиперпигментации (от 2 дней до недели).
Локализация герпетической инфекции так называемого "нижнего пояса" довольно разнообразна. Наиболее часто поражаются слизистые и кожа головки и крайней плоти у мужчин, область больших, малых половых губ и преддверия влагалища у женщин. для герпеса характерно высыпание сгруппированных пузырьков, быстро превращающихся в поверхностные эрозии на фоне гиперемированной и отечной кожи.
Малосимптомная и атипичная формы
В настоящее время в большинстве случаев генитальный герпес протекает асимптомно т.е. без типичных везикул (пузырьков).Отмечается покраснение и отек пораженных участков с умеренными субъективными ощущениями. В других случаях при отсутствии выраженных кожных поражений отмечается значительный болевой синдром с иррадиацией в близлежащие участки кожи и органы. Реже встречается только незначительная эритема в местах поражения. Сроки течения асимптомных форм также короче, чем у типичной формы. Многие больные просто не замечают у себя проявления таких форм герпеса
Материалом для исследования может служить любой биоматериал: содержимое герпетических пузырьков, отделяемое из уретры, влагалища, шейки матки, моча, слюна, сперма, кровь, ликвор, мазки-отпечатки с высыпаний, биопсийные материалы. В основном применяют следующие методы диагностики:
Культуральное исследование - выделение вирусов в клеточной культуре. Дорогой и длительный по срокам метод. Применяется в основном в научных целях
Иммуноферментный анализ (ИФА) - в основном применяется для определения антител класса M,G. Широко распространен, но большого практического значения не имеет, так как антитела класса G к герпесу выявляются у значительной части здорового населения ( контакт организма с вирусом герпеса в прошлом)
Полимеразная цепная реакция ПЦР - самый точный и достоверный метод детекции вируса в организме.
Цитологическая диагностика - метод мазков отпечатков с очагов поражения и определения многоядерных клеток Тцанка - также довольно достоверный метод диагностики герпеса. Проба Цанка - содержимое свежей, невскрывшейся везикулы тонким слоем наносят на предметное стекло. Когда мазок подсохнет, его окрашивают по Райту или Гимзе. Проба Цанка считается положительной, если в мазке обнаружены гигантские многоядерные клетки (кератиноциты). В острой стадии результат положите- лен у 75% больных, как при первичном герпесе, так и при рецидивах.
Единственной группой препаратов, которые эффективны для лечения генитального герпеса, являются аномальные нуклеозиды (нуклеотиды). Наиболее распространенным в клинической практике являются ацикловир, его производные и фамцикловир
Эффективность и безопасность применения препаратов ликопид, амиксин, панавир, индинол, виферон, циклоферон, имунофан для лечения генитального герпеса не доказана и эти препараты в мировой медицинской практике не применяются
Разработка герпетической вакцины ведется уже более 90 лет, но различные модификации вакцины продемонстрировали примерно 37.5% ее эффективности, так что в настоящий момент в мировой практике эффективной вакцины не существует.
[youtube.player]Медицинский эксперт статьи

Инфекция, вызванная вирусом простого герпеса, может иметь несколько клинических форм, но чаще всего бессимптомна. Обычными клиническими проявлениями бывают везикулярные высыпания на коже и слизистых оболочках. Иногда может быть тяжелый кератит, менингоэнцефалит или диссеминированное заболевание новорожденных. Вирус простого герпеса патогенен для многих видов животных - мышей, крыс, хомячков, морских свинок, кроликов, собак, обезьян, у которых обычно вызывает лихорадку и энцефалит (при внутримозговом заражении), а у кроликов также кератоконъюнктивит.
Так как вирус обладает дермонейротропным действием, то у выживших животных и инфицированных людей он может длительно сохраняться в латентном состоянии в мозге, эпителиальных клетках, ганглиях тройничного и других нервов в виде двунитевых кольцевых форм ДНК.
Вирус хорошо размножается в хорион-аллантоисной оболочке куриных эмбрионов, где через 2-3 сут. после заражения образует выпуклые белые бляшки, видимые невооруженным глазом. В препаратах-отпечатках из них видны гигантские клетки с внутриядерными включениями. Вирус легко размножается почти во всех широко используемых культурах клеток, образуя в монослоях бляшки. В зараженных клетках образуются тельца-включения, появляются гигантские многоядерные клетки, которые далее некротизируются (цитопатический эффект). Особенно пригодна для заражения первичная культура клеток почек кролика.

[1], [2], [3], [4], [5], [6], [7], [8], [9]
Патогенез и симптомы простого герпеса
При инфицировании вирусом первичная его репродукция происходит в эпителии слизистой оболочки рта, глотки или половых органов. Далее вирус лимфогенным путем проникает в кровь (генерализованная инфекция) и, пройдя через гематоэнцефалический барьер, может вызвать менингит или энцефалит. При генерализованной герпес-инфекции у новорожденных наступает смерть, к которой приводят множественные мелкоточечные некрозы и воспалительные очаги во внутренних органах. В случае выздоровления устанавливается состояние вирусоносительства, изменяющееся в течение всей жизни и проявляющееся преходящими герпетическими атаками, которые могут быть спровоцированы различными агентами (солнечная радиация, лихорадка, стресс, острая пища и др.).
Вирус герпеса типа 1 может вызвать развитие следующих клинических форм заболевания:
- острый герпетический (афтозный) стоматит развивается чаще у первично инфицированных детей, инкубационный период 3-5 дней, повреждения слизистой заживают через 2-3 нед.;
- герпетическая экзема (сыпь Капоши, сходная с сыпью при ветряной оспе) сопровождается лихорадкой и пузырьковыми высыпаниями на большей части поверхности тела, иногда наблюдается летальный исход;
- кератоконъюнктивит; при частых рецидивах может наблюдаться необратимое помутнение роговицы и слепота;
- менингоэнцефалит; летальность довольно высокая, в случае выздоровления - стойкие остаточные неврологические изменения;
- герпес губной (лабиалис) - наиболее частая форма; на границе слизистой и кожи на губах появляются гроздья сливающихся пузырьков, превращающиеся в язвочки, заживающие без рубцов.
Вирус герпеса типа 2 вызывает две основные клинические формы заболевания: генитальный герпес (характеризуется пузырьково-язвенными высыпаниями на коже и слизистой половых органов, частыми рецидивами) и герпес новорожденных (ребенок инфицируется при родах от больной матери, проявление - от стертых форм до генерализации с летальным исходом). Возможна иная локализация высыпаний (раны, пальцы у стоматологов и др.). Трансплацентарное заражение плода вирусом простого герпеса бывает редко и вызывает развитие врожденных уродств.
Иммунитет при простом герпесе
Ребенок первых 6 мес. жизни имеет, как правило, антитела к вирусу, приобретенные пассивно от матери. Далее они утрачиваются, ребенок наиболее восприимчив к герпетической инфекции в возрасте от 6 мес. до 2 лет. В крови переболевших обнаруживаются антитела, нейтрализующие вирус, а также специфические IgA на слизистых, но они не препятствуют персистированию вируса и развитию латентной инфекции.
Эпидемиология вирусов типов 1 и 2
Имеются данные, что до 70- 90 % людей инфицированы вирусом герпеса типа 1 и что он присутствует в организме человека более постоянно, чем любой другой вирус. Первичное инфицирование происходит в раннем периоде жизни. После исчезновения материнских антител инфекция протекает в виде везикулярного или афтозного стоматита. Вирус уже не удаляется из организма, так как не доступен действию антител. Вирус герпеса типа 1 передается прямым контактом через слюну или через посуду, загрязненную слюной носителя. Источником заражения детей обычно является один из родителей с активной формой герпеса.
Вирус простого герпеса типа 2 передается половым путем или во время родов от больной матери. Распространяется как типичная венерическая болезнь. Источник инфекции - только человек.

[10], [11], [12], [13], [14], [15], [16], [17]
Лабораторная диагностика простого герпеса
Диагностика простого герпеса может использовать вирусоскопический, вирусологический и серологический методы. Материалом для исследования служат соскобы с роговой оболочки, содержимое пузырьков, слюна и др. Соскобы и мазки, взятые из основания свежих герпетических высыпаний и окрашенные по Романовскому-Еимзе после немедленной фиксации в абсолютном спирте, содержат гигантские многоядерные клетки с внутриядерными включениями (тельца Каудри).
Для выделения вируса используют культуры клеток, куриные эмбрионы и лабораторных животных. В зараженных культурах клеток обнаруживают бляшки и характерный цитопатический эффект, в куриных эмбрионах при заражении на хориналлантоисную оболочку обнаруживают бляшки, причем бляшки, образованные вирусом герпеса типа 2, крупнее бляшек, образованных вирусом типа 1. При заражении новорожденных мышей в мозг симптомы энцефалита развиваются на 2-6-й день. Очень чувствительно и специфично для вируса герпеса заражение на скарифицированную роговицу кролика. Окончательную идентификацию производят в реакции нейтрализации на мышах, куриных эмбрионах или клеточных культурах с использованием стандартных противогерпетических иммунных сывороток животных, а также в реакции иммунофлуоресценции (РИФ).
При серодиагностике важно решить, первичное это заболевание или обострение хронической инфекции. Поэтому используют парные сыворотки, которые исследуют с помощью РСК, РИФ и ИФМ.
Лечение простого герпеса
Специфическое лечение простого герпеса основано на использовании химиопрепаратов - модифицированные нуклеозиды, подавляющие репликацию вируса, но обладающие токсичностью и способствующие появлению резистентных к ним штаммов вируса (аденинарабинозид, 5-йод-2-дезоксиуридин, ацикловир и др.). Эффективны, особенно в случае острого течения заболевания, индукторы интерферона.
Профилактика простого герпеса
Для лечебных целей в тяжелых случаях, а также для профилактики простого герпеса при частых рецидивах используют убитую культуральную герпетическую вакцину.
[youtube.player]Методические указания для студентов к практическому занятию № 6.
Тема: Лабораторная диагностика герпесвирусных инфекций.
Цель: Изучение лабораторной диагностики герпесвирусных инфекций.
Модуль 3. Общая и специальная вирусология.
Содержательный модуль 16. Специальная вирусология.
Тема 6:Лабораторная диагностика герпесвирусных инфекций.
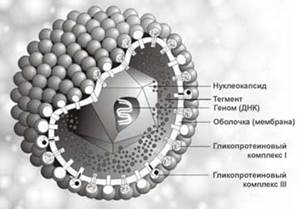
Актуальность темы:
Вирус простого герпеса – одна из самых распространенных вирусных инфекций человека, характеризующаяся лихорадочным состоянием и пузырьковыми высыпаниями, которые чаще всего локализуются на коже и слизистых оболочках. Важными особенностями герпетической инфекции являются пожизненное носительство вируса и частые рецидивы болезни.
Вирусная природа простого герпеса установлена в 1912 г. У. Грютером.
(Трёхмерное изображение вируса герпеса).
Герпесвирусы и вызываемые ими заболевания
| Типы вирусов герпеса | Вызываемые заболевания |
| ВПГ-1 (вирус простого герпеса типа 1) | Поражение: кожи, слизистой оболочки ротовой полости, конъюнктивы или роговицы глаза, энцефалиты |
| ВПГ-2 (вирус простого герпеса типа 2) | Поражение слизистых оболочек гениталий, у новорожденных - центральной нервной системы |
| ВЗВ (вирус ветрянки) | Ветряная оспа, опоясывающий лишай, постгерпетическая невралгия; язвенно-некротическая форма опоясывающего герпеса - СПИД-индикаторный признак заболевания |
| ЦМВ (цитомегаловирус) | Патологии новорожденных; осложнения после трансплантации органов и костного мозга: интерстициальная пневмония, гастроинтестинальные расстройства, гепатиты |
| ВЭБ (вирус Эпштейна-Барра) | Инфекционный мононуклеоз, лимфома Беркитта, рак носоглотки |
| ВГ-6 | Вирус, вызывающий фатальные интерстициальные пневмонии и инфекционные розеолы новорожденных |
| ВГ-7 | Вирус, выделенный от больных с синдромом хронической усталости |
| ВГ-8 | Вирус, выделенный из биоптата больного саркомой Капоши, ассоциированный с лимфопролиферативными заболеваниями |
| Примечание. ВГ - вирус герпеса. |
Таксономия, морфология, химический состав. Возбудитель простого герпеса - ДНК-содержащий вирус, относится к семейству Herpesviridae, роду Simplexvirus. По морфологии и химическому составу не отличается от вирусов ветряной оспы и опоясывающего герпеса.

Культивирование. Вирус простого герпеса (ВПГ) культивируют в куриных эмбрионах, культурах клеток и организме лабораторных животных. На хорионаллантоисной оболочке куриных эмбрионов вирус образует мелкие белые плотные узелки-бляшки; в зараженных культурах - вызывает цитопатический эффект: образование гигантских многоядерных клеток с внутриядерными включениями.
Антигенная структура. Вирус содержит ряд антигенов, связанных как с внутренними белками, так и с гликопротеидами наружной оболочки. Последние являются основными иммуногенами, индуцирующими выработку антител и клеточный иммунитет. Существует два серотипа вируса: ВПГ типа 1 и ВПГ типа 2.
Резистентность. Вирус может выживать на поверхности предметов при комнатной температуре в течение нескольких часов, чувствителен к УФ-лучам, обычным дезинфицирующим средствам, жирорастворителям, термолабилен.
Восприимчивость животных. Вирус простого герпеса патогенен для многих животных, у которых вызывает энцефалит при введении возбудителя в мозг или местный воспалительный процесс при заражении в глаз. В естественных условиях животные не болеют.
Эпидемиология. Простой герпес - одна из самых распространенных инфекций, которая поражает различные возрастные группы людей, чаще в осенне-зимний период. Отмечаются спорадические случаи заболевания, иногда небольшие вспышки в семьях, детских коллективах, больницах. Эпидемий не наблюдается.
Источником инфекции являются больные и носители. Основной механизм передачи - контактный, аэрогенный. Заражение происходит при попадании вирусов на поврежденные кожные покровы или слизистые оболочки.
Эпидемиология герпеса, вызванного вирусами типов 1 и 2, различна. ВПГ типа 1 передается через слюну, зараженные слюной руки и предметы быта, а ВПГ типа 2 - половым путем. Возможно заражение плода через плаценту.
Патогенез и клиническая картина. По клиническим проявлениям различают первичный и рецидивирующий герпес. Входными воротами возбудителя при первичной герпетической инфекции являются поврежденные участки кожи и слизистых оболочек рта, глаз, носа, мочеполового тракта, где вирусы репродуцируются. Затем по лимфатическим сосудам вирусы попадают в кровь и заносятся в различные органы и ткани.
Инкубационный период при первичном герпесе составляет в среднем 6-7 дней. Заболевание начинается с жжения, зуда, покраснения, отека на ограниченных участках кожи и слизистых оболочек, затем на этом месте появляются пузырьковые высыпания, наполненные жидкостью. Иногда заболевание сопровождается повышением температуры тела и нарушением общего состояния. При подсыхании пузырьков рубцов не образуется. Первичный герпес у новорожденных протекает тяжело и нередко заканчивается смертью. Однако у большинства людей первичная инфекция остается нераспознанной, так как протекает бессимптомно.
После первичной инфекции (явной и бессимптомной) 70-90 % людей остаются пожизненными носителями вируса, который сохраняется в латентном состоянии в нервных клетках чувствительных ганглиев. Нередко у носителей появляются рецидивы болезни в результате переохлаждения, перегревания, менструации, интоксикации, различных инфекционных заболеваний, стрессов, нервно-психических расстройств. Для рецидивирующего герпеса характерны повторные высыпания на коже и слизистых оболочках, нередко в тех же местах. Наиболее частой локализацией рецидивирующего герпеса, вызванного ВПГ типа 1, являются губы, крылья носа, полость рта, конъюнктива глаз. ВПГ типа 2 поражает мочеполовую систему и вызывает герпес новорожденных. Доказана роль ВПГ типа 2 в развитии рака шейки матки. Сравнительно редко встречаются генерализованные формы рецидивирующего герпеса, в частности поражения нервной системы и внутренних органов.
Иммунитет. В результате первичной герпетической инфекции в организме образуются сывороточные и секреторные антитела, которые обусловливают иммунитет к первичному герпесу, но не препятствуют сохранению вируса и возникновению рецидивов. Рецидивирующий герпес возникает при высоком уровне антител к вирусу герпеса. Основное значение в развитии рецидивирующего герпеса имеет состояние клеточного иммунитета.
Лабораторная диагностика. Материалом для исследования являются содержимое герпетических пузырьков, слюна, соскобы с роговой оболочки глаза, кровь, цереброспинальная жидкость, в летальных случаях . кусочки головного и спинного мозга.
Экспресс-диагностика заключается в обнаружении гигантских многоядерных клеток с внутриядерными включениями в мазках-отпечатках из высыпаний, окрашенных по Романовскому-Гимзе. Для дифференциации от других вирусов, принадлежащих к этому семейству, используют РИФ, ИФА, РИА, ПЦР. Выделение вируса проводят на куриных эмбрионах, культуре клеток и на лабораторных животных (мыши-сосунки), идентифицируют вирус с помощью РИФ или РН. В последние годы в диагностике простого герпеса начали применять моноклональные антитела, что дает возможность определить серотип вируса. Для серодиагностики заболевания используют РСК, РН, РИФ, ИФА.
Специфическая профилактика и лечение. Для профилактики тяжелых форм рецидивирующего герпеса в период ремиссии применяют многократное введение инактивированной, культуральной герпетической вакцины. Вакцинация, а также применение иммуномодуляторов, например реаферона, удлиняют межрецидивный период и облегчают течение последующих рецидивов. В остром периоде с лечебной целью используют химиотерапевтические препараты (виразол, ацикловир, оксолиновую, тебро-феновую, флореналовую мази, бонафтон), интерфероны и индукторы интерферона.
Вирус цитомегалии

Цитомегалия - инфекционное заболевание, возбудителем которого является цитомегаловирус (ЦМВ) Cytomegalovirus hominis (от греч. cytys - клетка, megas - большой). Вирус вызывает цитомегаловирусную инфекцию человека, характеризующуюся поражением почти всех органов (преимущественно слюнных желез) с образованием в них гигантских клеток с внутриядерными включениями, протекающую в различных формах - от бессимптомного носительства до тяжелой генерализованной формы, заканчивающейся летальным исходом.
Вирус впервые выделен К. Смитом в 1956 г.
Таксономия, морфология, антигенная структура. Возбудитель цитомегалии - ДНК-содержащий вирус, относится к семейству Herpesviridae, роду Cytomegalovirus.
Морфология, химический состав типичны для семейства герпесвирусов. Диаметр вирусной частицы (вириона) около 180 нм. В центре вириона находится двенадцатигранный нуклеокапсид, содержащий генетическую информацию - двухнитевую ДНК-вируса. Установлено 2 антигенных серотипа вируса.
Резистентность. Вирус термолабилен, чувствителен к дезинфицирующим средствам и жирорастворителям.
Эпидемиология. Цитомегаловирусная инфекция широко распространена на земном шаре. Источником вируса является больной человек или носитель. Вирус выделяется со слюной, мочой, секретами организма, реже фекалиями. Предполагается, что ведущий механизм передачи инфекции - контактно-бытовой, возможны аэрогенный и фекально-оральный механизмы передачи. Цитомегаловирус обладает высокой способностью проникать через плаценту (вертикальная передача), вызывая внутриутробную патологию плода.
Патогенез и клиническая картина. Патогенез не вполне выяснен. Инфекция связана с длительным носительством вируса, который в латентном состоянии сохраняется в слюнных железах, почках и других органах. Активация латентной инфекции происходит при иммунодефицитных состояниях, иммунодепрессивной терапии. Вирус поражает ЦНС, костный мозг, почки, печень, клетки крови. У беременных женщин цитомегалия может приводить к недоношенности, мертворождению, развитию аномалий у плода.
Иммунитет. У больных независимо от клинической формы инфекции, а также у носителей образуются антитела, которые, однако, не препятствуют сохранению вируса в организме и выделению его в окружающую среду. Интенсивность развития болезни находится под контролем клеточной иммунной системы хозяина.
Лабораторная диагностика. Обследованию на цитомегалию в первую очередь подлежат дети с поражением ЦНС и врожденными уродствами, а также женщины с неблагополучно протекающей беременностью. Исследуемый материал - слюна, моча, мокрота, цереброспинальная жидкость, кровь, пунктат печени.
Специфическая профилактика и лечение. Разработана живая аттенуированная вакцина. Для лечения применяют химиотерапевтические препараты (ганцикловир, фоскорнет натрия), иммуномодуляторы, интерферон.
Не нашли то, что искали? Воспользуйтесь поиском:
[youtube.player]Проблеме диагностики герпесвирусных инфекций посвящено множество научных публикаций, однако в последнее время все более возрастает интерес к этому вопросу со стороны клиницистов разных специальностей. По данным литературы, вирусом простого герпеса инфицировано 65-90 % взрослого и детского населения планеты. Местом локализации первичной герпесвирусной инфекции чаще всего является слизистая оболочка полости рта.
Несмотря на широкое и разностороннее изучение данной патологии, отмечается тенденция к росту распространенности герпетических стоматитов, особенно среди детского населения. Наделю герпетической инфекции среди всех поражений слизистой полости рта у детей приходится около 80 %, у 8-20% пациентов заболевание принимает рецидивирующий характер. При этом вирус может поражать практически все органы и ткани человеческого организма. У детей грудного и раннего возраста, после исчезновения антител, полученных интерплацентарно от матери, герпетическая инфекция, как правило,протекает в виде острого герпетического стоматита. Хроническая герпетическая инфекция в полости рта проявляется в виде рецидивирующего герпетического стоматитаили герпеса губ.
Современные наблюдения специалистов позволяют говорить о изменении клинической картины герпетического стоматита и выделении атипичных форм заболевания, а именно геморрагической, геморагически-некротической, язвенной, отечной, элефанзиазоподобной, рупеоидной, зудящей, эритематозной и папулезной, герпетиформной экземы Капоши, генерализованного герпеса. В литературе упоминается импетигоподобная форма герпеса, при которой высыпания на слизистой оболочке полости рта сочетаются со стрептококковым импетиго в периоральной зоне. Атипичные формы заболевания затрудняют диагностику. Таким образом, высокая инфицированность населения и распространенность заболевания, наличие атипичных форм и отсутствие четких диагностических алгоритмов свидетельствуют об актуальности этой проблемы.

Материалом для исследования при герпетической инфекции полости рта являются:
Соскоб и мазок-отпечаток с элементов поражения, слюна, кровь.
На сегодняшний день существует большое количество лабораторных методов диагностики герпесвирусных инфекций.
Выделяют три основных диагностических подхода:
1). изоляция и идентификация вирусаиз клинического материала;
2). непосредственное исследование материала на наличие вируса, вирусного антигена или нуклеиновых кислот
3). серологическая диагностика, основанная на установлении значительного прироста вирусных антител в течение болезни.
В настоящее время применяется ускоренный вирусологический метод выявления вирусов. При этом методе материал, полученный от больных, культивируется совместно с культурой клеток Vero в течение 24-х часов. После предварительной обработки применяется реакция непрямой иммунофлюорисценциии результаты оценивают под люминисцентным микроскопом.Этот метод позволяет выбрать антивирусный препарат для лечения герпетической инфекции и оценить эффективность противовирусной терапии через 1,5-2 месяца после окончания лечения. Результаты обследования готовы через 2-е суток.
Биологическая проба состоит в заражении чувствительных лабораторных животных (белых мышей или кроликов) биоматериалом, полученным от больного. Метод рекомендуют использовать в спорных случаях герпесвирусной инфекции и для диагностики атипичных форм.
Микроскопические методы исследования герпеса:

включают цитологическую диагностику и электронную микроскопию. Исследуемый материал для микроскопических методов получают путем соскоба или мазка-отпечатка с пораженных участков слизистой и кожи.
Цитологический метод простой, доступный, рассматривается как экспресс-метод, так как результаты исследования получают через 2-3 часа. Его чувствительность и специфичность не превышают 70-75 %. Метод нашел широкое применение в стоматологической практикедля проведения дифференциальной диагностики в сложных случаях и оценки эффективности лечебных мероприятий.
К методам экспресс-диагностики герпеса относится:
Электронная микроскопия. Метод позволяет выявить вирусные частицы в исследуемом образце. Для успешного определения вируса его концентрация в пробе должна быть примерно 1ˑ10 6 частиц в 1 мл. Но поскольку концентрация возбудителя в материале обычно незначительна, то требуется предварительное центрифугирование. Однако метод электронной микроскопии не позволяет дифференцировать вирусы простого герпеса и ветряной оспы, цитомегалии, поскольку они морфологически практически одинаковы. Использование метода ограничивается его трудоемкостью, малодоступностью, дороговизной, поэтому он применяется в основном в научных целях. Для получения результатов метода электронной микроскопии необходимо около 3-х часов, чувствительность метода составляет 70 %, специфичность около 100 %.
В настоящее время главенствующую роль в верификации герпесвирусных инфекций играют методы ДНК-диагностики, в частности полимеразная цепная реакция (ПЦР) и ДНК-гибридизация.
Гибридизация ДНК – высокоспецифичный метод, позволяющий идентифицировать геном вируса после его специфического связывания (гибридизации) с меченой комплементарной молекулой ДНК-диагностикума. В качестве маркера применяют ферменты (пероксидазу, щелочную фосфатазу) и изотопы. Недостатком метода является его длительное время выполнения- в среднем 5-7 суток, а также высокая частота ложноотрицательных результатов при низком количестве вирусной ДНК в исследуемой пробе.
Наиболее широко используемым методом диагностики герпетической инфекции является полимеразная цепная реакция (ПЦР), предложенная Мюллисом в 1983 году. В основе метода лежит катализируемая ферментом ДНК-полимеразой многократное образование копий (ампликация) определенного участка ДНК, представляющего диагностический интерес. Для ампликации отбирают уникальный ген, который наиболее четко отличает определяемый патоген от прочих.
Различают качественный, полуколичественный и количественный варианты метода. При проведении качественной ПЦР определяют лишь факт присутствия вируса, однако не возможным является оценка его репродуктивной активности, что не позволяет провести дифференциальную диагностику между латентными, персистирующими и реактивными формами инфекции. Полуколичественная ПЦР дает информацию о содержании копий вирусных ДНК в виде условных обозначений (+, ++, +++, ++++). Методом, позволяющим получить числовые значения, отражающие репродуктивную активность вируса является количественная ПЦР. Полученный количественный результат не соответствует истинному содержанию ДНК возбудителя в исследуемой пробе. При этом существует определенная пропорциональность между исходным количеством ДНК вируса и конечным результатом исследования. Такая пропорциональность соблюдается лишь при проведениидиагностики в стандартных условиях с использованием одних и тех же реактивов, поэтому сравнительный анализ полученных результатов в динамике проводят при обследовании пациента в одной лаборатории.
Ложноотрицательные результаты возможны при несоблюдении технологий и использовании некачественных реактивов. Ложноположительные данные возможны при подсчете результатов методом электрофореза, что обусловлено контаминацией воздушной среды рабочего пространства ампликонами при предварительных постановках, поэтому используют открытые методики подсчета результатов с надлежащей вентиляцией помещений и закрытые, которые являются более предпочтительными, так как предполагают отсутствие прямогоконтактамежду продуктами реакции и воздушной средой.
Наиболее точной является методика ПЦР в реальном времени (real time ПЦР). Ее особенностью является подсчет количества амплифицированных ДНК по мере их накопления после каждого цикла, а не в конце постановки ПЦР.
Даже количественная ПЦР не всегда позволяет отдифференцировать латентную и реактивированную инфекции. В этом случае рекомендуют использовать ПЦР обратной транскрипции, с помощью которой подсчитывают количество вирусной м-РНК, которое свидетельствует об интенсивности экспрессии вирусных генов. ПЦР является точным методом, так как для получения результата достаточно иметь в пробе всего одну молекулу ДНК возбудителя. Чувствительность ПЦР составляет 98%, а специфичность – 94 %. РезультатыПЦР можно получить уже через 3-6 часов после начала проведения.В стоматологической практике ПЦР широко применяется в диагностических целях. Установлена зависимость уровня вирусной активности в ротовой жидкости от степени тяжести герпетической инфекции.
Определения вирусных антигенов возможно при помощи реакции иммунофлюорисценции.
Этот метод основан на использовании иммуноглобулинов, меченных красителями и дающих зеленовато-желтую или красную флюорисценцию. Результаты метода учитывают при люминисцентой микроскопии препаратов обработанных меченными антителами. Метод иммунофлюорисценции используют в двух вариантах: прямой (ПИФ) и непрямой (НИФ). При прямом методе красителями метят антитела, непосредственно взаимодействующие с антигеном. При непрямом методе с исследуемым антигеном взаимодействуют специфические антитела, а уже с ними антивидовые антитела, меченые флюорохромом. Эти методы в какой то мере дублируют результаты ПЦР и могут быть полезны для исключения ложноположительных или ложноотрицательных результатов ДНК-диагностики. Чувствительность метода – 55-75 %, специфичность – 90 %. Метод нашел широкое применение в стоматологической практике для уточнения диагноза.
Серологические методы диагностики герпеса:
(реакции нейтрализации, связывания комплемента, гемагглютинации, иммунофлюорисценции и др.) позволяют оценить характер и напряженность специфического гуморального иммунитета. Все эти методы позволяют с разной степенью достоверности установить факт инфицирования пациента с вирусом. Диагностика основывается на наличии противогерпетическихIg M и Ig G. Наличие специфического Ig M свидетельствует об остроте процесса (первичная инфекция, реинфекция, реактивация). При первичной герпесвирусной инфекции противогерпетический Ig M появляется на 7-14 сутки после инфицирования и циркулирует 1-3 месяца. У отдельных лиц может сохраняться на протяжении длительного времени, давая ложную информацию об остроте процесса. Противогрепетические Ig G являются антителами вторичного иммунного ответа. При первичной инфекции выявляются во второй половине инфекционного процесса, а также при латентной, персистирующей инфекции и реактивации вируса. Рекомендуют применять метод парных сывороток, оценивая титр специфических антител с промежутком в 2-3 недели. Однако четырехкратное повышение титра специфическогоIg G является диагностическим критерием лишь при первичном инфицировании. Проведение серологических исследований позволяет оценить иммунный статус организма. Так, расхождение между показателями ПЦР, свидетельствующими о высокой репродуктивнойактивности вируса, и данными серологических исследований, показывающими низкий титр специфических антител, свидетельствует о недостаточности специфического гуморального иммунного ответа и является показанием к назначению заместительной терапии (препаратов специфических иммуноглобулинов) или средств, повышающих антителогенез (полиоксидоний, спленин и др.).
Иммунологические исследования являются обязательными при манифестных формах инфекции, так как вирус способен оказывать иммуносупрессивное действие на зараженный организм. Результаты таких исследований позволяют выявить иммунный дефект и назначить рациональную терапию. Метод применяется для выбора средств иммунотерапии и оценки их эффективности при лечении герпетических стоматитов.
Таким образом, диагностическими критериями герпетической инфекции полости рта являются:
-выявление вирусных агентов в крови, слюне, соскобах и мазках-отпечатках с элементов поражения достоверными методами: ПЦР, методом иммунофлюорисценции;
- в спорных случаях для экспресс-диагностики необходимо проводить цитологическое исследование с целью выявления клеток Тцанка;
- для диагностики первичной герпетической инфекции важным является выявление вирус-специфических иммуноглобулинов M и G.
При постановке диагноза обязательно учитывают наличие клинических признаков герпетической инфекции (типичных элементов поражения).
Для назначения рациональной противовирусной и иммунотерапии рекомендуется проведение следующих исследований:
- определение противогерпетических антител классаM, G и А для оценки напряженности специфического гуморального иммунитета;
- иммунологическое исследование проводят при тяжелом или атипичном течении и частых рецидивах герпетической инфекции, при низкой чувствительности к лечению ацикловиром и его аналогами.
[youtube.player]Читайте также:


