Медицинские статьи о лечении герпеса

В своей практической деятельности врачи многих специальностей встречаются с заболеваниями, вызванными вирусами семейства Herpesviridae, которые широко распространены в человеческой популяции. Они способны поражать практически все органы и системы организма хозяина, вызывая латентную, острую и хроническую формы инфекции при этом, спектр клинических проявлений, развитие которых они обусловливают, чрезвычайно широк [7]. Особого внимания заслуживает рецидивирующая форма герпетической инфекции (ГИ), относящаяся к числу наиболее распространенных психосоматических кожных заболеваний. Хроническое течение, зуд, частая локализация и характер высыпаний на лице или интимно значимых участках кожного покрова сопровождаются изменениями эмоциональной сферы. В свою очередь, состояния стресса, восприятие самим пациентом проявлений болезни оказывает влияние на интенсивность и частоту рецидивов простого герпеса (ПГ) [24].
Многочисленные исследования в области проблемы ГИ, особенно вызванные вирусами простого герпеса (ВПГ) 1 и 2 типов, не теряют своей актуальности в настоящее время [21, 16].
Серьёзной проблемой является высокая инфицированность здорового населения, преимущественно молодого, трудоспособного возраста. В мире ежегодно заражаются от 16 до 800, а в России – от 40 до 80 человек на 100 тыс. населения. В настоящее время заболеваемость ПГ крайне высока, по статистике ВОЗ, она занимает второе место среди вирусных поражений, уступая лишь гриппу. ВПГ-1 инфицировано около 90 % взрослого населения планеты, распространенность ВПГ-2 колеблется от 7 до 40 %. В США ежегодно регистрируется до 98 млн случаев лабиального герпеса и 20 млн случаев рецидивирующего герпеса гениталий, 500 тыс. случаев офтальмогерпеса и более 5 тыс. случаев герпетического энцефалита, около 1 тыс. случаев герпеса новорожденных. По мнению ведущих специалистов, в нашей стране ежегодная заболеваемость герпесом губ составляет 10 млн, герпесом кожи – 1 млн, офтальмогерпесом – 250 тыс. случаев. Рецидивирующими формами герпеса страдают от 10 до 20 % населения, а ежегодный прирост увеличивается на 15–17 % [3, 13, 23].
Литературные данные свидетельствуют, что большинство населения Земли инфицировано ВПГ-1, ВПГ-2 или тем и другим вирусом одновременно. Первичная инфекция, ассоциированная с ВПГ-1 или ВПГ-2, может протекать в клинически выраженной форме в очаге инфицирования (например, в орофациальной или генитальной области) либо как бессимптомная или нераспознанная инфекция. Генитальная форма простого герпеса может быть связана с ВПГ-1, так же как и лабиальная форма – с ВПГ-2. После первичного инфицирования у 50–75 % больных отмечается рецидивирующее течение простого герпеса. В течение первых 12 месяцев после инфицирования ВПГ-2 рецидив возникает у 80 % пациентов, ВПГ-1 – у 55 % [15, 26].
Современная медицина не располагает методами лечения, позволяющими элиминировать ВПГ из организма человека. Целью лечения герпеса является: 1) подавление репродукции ВПГ в период обострения (купирование рецидива); 2) снижение частоты и длительности рецидивов заболевания, тяжести их течения; 3) формирование адекватного иммунного ответа и его длительное сохранение с целью блокирования реактивации ВПГ в очагах персистенции.
Всё разнообразие методов терапии и профилактики обострения герпесвирусных инфекций можно сгруппировать в направления этиотропного, патогенетического и симптоматического лечения с применением химиотерапии, иммунотерапии и комплексного лечения [1, 7, 11].
Большое внимание уделяется антигерпетическим соединениям растительного происхождения, природным антиоксидантам, адаптогенам из лекарственного растительного сырья и витаминно-минеральным комплексам, ввиду изменения иммунного статуса пациентов [14, 19].
Патогенетическая терапия направлена на нормализацию функции иммунной системы организма, в том числе на активацию системы интерфероновой защиты, как правило, связанная с применением интерферонов (ИФН), индукторов ИФН и иммуномодуляторов. Специфическая иммунотерапия состоит в применении герпетической вакцины, хотя ряд исследователей считает, что надежды, возлагаемые на специфическую вакцинопрофилактику, не оправдали себя [11, 19]. Иммунотропные препараты, обладающие активностью против вируса герпеса, разнообразны и представлены в таблице.
Иммунотропные препараты, обладающие активностью против вируса герпеса
Использование противовирусной химиотерапии велико при лечении рецидивирующих форм простого герпеса с поражением кожи и слизистых оболочек. В лечении простого герпеса с применением противогерпетических химиопрепаратов можно выделить два принципиально отличающихся друг от друга подхода: 1) эпизодическое лечение – прием ациклических нуклеозидов (АН) в момент рецидива в терапевтических дозах при соблюдении кратности и длительности лечения; 2) супрессивная терапия – длительный, иногда многолетний, постоянный прием препаратов АН вне рецидива в более низких дозах [9, 25].
Согласно проведенным исследованиям, биодоступность (per os) противогерпетических препаратов из группы ациклических нуклеозидов возрастает следующим образом: ацикловир – 20 %, валацикловир – 54 % и фамцикловир – 77 % [24]. Тем не менее применение ацикловира по-прежнему остаётся востребованным среди врачей и пациентов в настоящее время, и одновременно ведутся исследования по увеличению растворимости ацикловира [5] и синтезу его производных [8].
В разные годы предпринимались многочисленные попытки повысить эффективность лечения ПГ путем комбинированной терапии. С этой целью использовались различные сочетания средств иммунного влияния, а также препаратов, отличающихся по этиопатогенетическому механизму действия [20].
Возможно сочетанное использование противовирусной терапии и глюкокортикостероидов. Выявлено, что такая комбинация эффективнее монотерапии противовирусными препаратами, особенно для лечения острой боли и коррекции различных аспектов качества жизни пациентов. Комбинация ацикловир + преднизолон значительно быстрее купирует острую боль и возвращает пациента к обычной жизнедеятельности в случае постгерпетической невралгии [2].
Наружные средства дополняют системную противовирусную терапию. Многочисленные наблюдения подтверждают, что в случае назначения таблетированных форм ациклических нуклеозидов на стадии предвестников в сочетании с наружной противовирусной терапией значительно чаще удается полностью прервать дальнейшее развитие рецидива или наблюдать его абортивное течение [20].
Местная терапия противовирусных лекарственных средств при герпесе кожи и слизистых оболочек требуется для уменьшения отёка, экссудации, боли и зуда, ускорения заживления язвочек и эрозий и сокращения длительности выделения вируса на участках поражения [22]. Применение данных лекарственных форм начинают при появлении первых признаков активации инфекции (чувство жжения, зуд и т.д.) и продолжают вплоть до эпителизации эрозий. Рано начатое местное лечение может предотвратить развитие везикул.
В комплексную терапию пациентов с простым герпесом необходимо включать местные противовирусные средства, способствующие стабилизации и разрешению процесса [12].
При анализе ассортимента противовирусных средств на российском рынке установлено, что большинство противовирусных препаратов выпускается в виде твёрдых лекарственных форм – 66 %, в виде мягких лекарственных форм – 22 %, а в форме жидких – 12 % [22], лидером же является ацикловир [6].
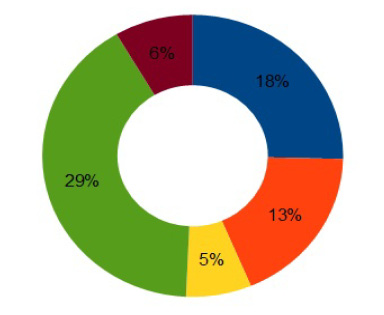

Ассортимент лекарственных форм, содержащих ацикловир
Следует отметить, что современная фармакотерапия герпеса эффективно уменьшает его клинические проявления, положительно влияет на психическое состояние пациентов и приобретает комплексный подход. Несмотря на различные достижения в лечении герпеса, ацикловир по-прежнему играет значительную роль в данном направлении и привлекает внимание исследователей по созданию комбинированных препаратов. В связи с чем актуальными являются исследования по разработке лекарственной формы комбинированного состава, обладающей противогерпесным эффектом – медицинские карандаши.
Рецензенты:
Степанова Э.Ф., д.фарм.н., профессор, профессор кафедры технологии лекарств ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск;
Хаджиева З.Д., д.фарм.н., профессор, профессор кафедры технологии лекарств ПМФИ – филиала ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.

Причиной возникновения сгруппированных болезненных мелких пузырьков на губах является первичное заражение или активация дремавшей внутриклеточной инфекции —вируса герпеса.
Вариантов клинических проявлений герпетической инфекции огромное множество. Зависит всё от состояния иммунной системы и разновидности вируса (по-научному, его антигенного типа). Наиболее тяжёлое течение заболевания отмечается после первого контакта с вирусом, когда у заболевшего отсутствуют специфические антитела к нему, например, у детей раннего возраста с незрелой иммунной системой или при иммунодефицитных состояниях (ВИЧ, больные после химиотерапии).
Первый контакт
Заражение герпесом происходит несколькими путями. Основной — это прямой контакт с больным человеком (поцелуи, половой контакт), через предметы обихода и гигиены (общие полотенца, зубные щётки, бритвенные приборы). Воздушно-капельным путём в организм проникает вирус опоясывающего герпеса, вызывающий опоясывающий лишай и ветряную оспу (ветрянку). Ещё один возможный путь заражения — вертикальный: от матери к плоду во время родов. В США ежегодно регистрируется 6-10 млн случаев генитального герпеса; около 2% беременных сталкиваются с его обострением, что становится серьезной проблемой для акушеров-гинекологов, поскольку пузырьковые поражения кожи гениталий повышают риск инфицирования плода в родах до 40-60%!
Излюбленные места дислокации
Видовое разнообразие
В большую группу герпесвирусных инфекций входят восемь различных типов возбудителя:
- вирусы простого герпеса 1 и 2 типа;
- вирус опоясывающего герпеса, вызывающий также и ветряную оспу;
- цитомегаловирус;
- вирус Эпштейна-Барр;
- вирусы герпеса человека 6, 7, 8 типа.
Два типа вируса простого герпеса:
Губная форма вируса простого герпеса (1 тип). Самой распространенной и одновременно заметной формой герпетической инфекции является герпес 1 типа. Чаще всего герпетические высыпания локализуются на красной кайме губ, крыльях носа, в ротовой полости (герпетический стоматит), на слизистой половых органов. Результатом повреждения является образование везикул (пузырьков) с лимфатической жидкостью, которые с течением времени ссыхаются, и на их месте образуется твердая корочка. В большинстве случаев для герпеса 1 типа не требуется лечения. Допускается проведение терапии в острый период, для уменьшения неприятной симптоматики (боль, зуд, жжение в месте будущих высыпаний, температура, головная боль, слабость) для чего предусмотрено применение противогерпетических мазей, инъекций или таблеток, использование природных антиоксидантов (витамины Е и С), иммуностимулирующих средств.
Менструальный герпес часто связывают с опоясывающим лишаем (герпесом 3 типа), но это не так. Это разновидность генитального герпеса, проявляющаяся высыпаниями в области поясницы и ягодиц незадолго до или во время менструации. Лечится это заболевание под контролем инфекциониста противовирусными препаратами. Также необходимо проконсультироваться у эндокринолога на предмет заболеваний щитовидной железы.
Опоясывающий герпес (3 тип) (Herpes zoster, син. опоясывающий лишай)
Двуликий вирус герпеса 3 типа вызывает два разных заболевания: при первой встрече с ним в молодом возрасте развивается ветряная оспа, так многим известная из детства. Герпес зостер передается воздушно-капельным путем. Вирус попадает в дыхательные пути, где происходит его размножение. В дальнейшем вирус распространяется внутри организма гематогенным, лимфогенным и нейрогенным путями, инфицирует ганглии вегетативной нервной системы. Инкубационный (скрытый) период болезни — 10-20 дней. У детей болезнь проявляется одновременно повышением температуры и сыпью. У взрослых сыпь на несколько дней запаздывает. Зудящая сыпь начинается с лица и головы, переходит на туловище; конечности поражаются редко.
При определённых условиях персистирующий в организме герпес зостер способен активироваться с развитием другого заболевания — опоясывающего лишая, характеризующегося высыпаниями на грудной клетке по ходу отдельных чувствительных нервов в виде нечётких розоватых пятен (диаметром 3-5 см), на фоне которых примерно через сутки образуются группы болезненных везикул. Поражения исчезают в течение 2-4 недели, боль (невралгия) может сохраняться в течение недель и даже месяцев. Опоясывающий лишай заразен с момента появления сыпи и до отпадения корок. Заболевание может осложняться вторичной бактериальной инфекцией кожи, а также энцефалитом, менингитом, миокардитом, гломерулонефритом. Самым грозным осложнением является пневмония, повышающая риск смертности у взрослых до 5-10%. Наблюдение за больными с опоясывающим лишаем осуществляют врачи дерматовенеролог и невролог, назначая противогерпетические и симптоматические препараты.
Герпес 4 типа (вирус Эпштейна-Барр)
У вируса Эпштейна-Барр есть некоторые территориальные особенности: так, у жителей южных регионов Китая, Юго-восточной Азии, Северной Африки и эскимосов он вызывает рак носоглотки. У молодых людей, живущих на Африканском континенте, вирус может вызвать лимфому Беркета — злокачественную опухоль верхней челюсти.
Герпес 5 типа (цитомегаловирус)
В зависимости от состояния иммунной системы заражение цитомегаловирусом (ЦМВ) может вызывать различные изменения: от бессимптомного течения и легкого мононуклеозоподобного синдрома до тяжелых системных инфекций с поражением легких, печени, почек и других органов. Заражение вирусом происходит половым, воздушно-капельным путями, при переливании крови и чрез молоко матери при грудном кормлении ребёнка. Особенно опасно заражение ЦМВ для беременной, так внутриутробное инфицирование плода на сроке до 12 недель, обычно заканчивается выкидышем, после 12 недель у ребенка может развиться тяжелое врожденное заболевание – цитомегалия, проявляющаяся недоношенностью, и нарушением работы внутренних органов. У детей, перенесших внутриутробно цитомегаловирусную инфекцию и избежавших генерализации процесса, в последующем могут возникнуть неврологические проблемы, нарушение слуха и зрения. Вирусоносительство и мононуклеозоподобный синдром у лиц с нормальным иммунитетом лечения не требует. При выявлении различных генерализованных форм инфекции требуется специализированное лечение.
Герпес 6 типа состоит из 2 видов 6А и 6В. Об этом типе герпеса не до конца все понятно: в частности, неясно какими путями происходит заражение и механизм его распространения. На данный момент основными путями распространения считают – воздушно-капельный и оральный. Кроме этого, вирус может быть передан при использовании зараженных им медицинских инструментов, гемотрансфузиях и при трансплантации органов. Вирус герпеса 6А часто встречается у пациентов с нейровоспалительным заболеванием – рассеянным склерозом. Вирус герпеса 6В, поражает чаще всего детей в возрасте от 6 месяцев до 3 лет, и является причиной детской розеолы, известной также как внезапная экзантема или шестая болезнь, проявляющейся высокой температурой и распространённой сыпью. Специфического лечения не разработано, проходит самостоятельно.
Герпес 8 типа смертельно опасен людям со стойким сниженным иммунитетом (в основном это больные СПИДом, реже больные после лучевой терапии и трансплантации органов). Данный тип герпеса связан с развитием саркомы Капоши — злокачественном опухолевом заболевании кожи.
Не хочешь болеть, вакцинируйся!

Дата публикации: 17.12.2018 2018-12-17
Статья просмотрена: 458 раз
В данной статье рассмотрены проблемы герпес-вирусной инфекции. Основное содержание исследования составляет выявление особенностей клинического течения у пациентов разного пола с герпес-вирусной инфекцией, статистическое выявление половозрастного состава пациентов с герпес-вирусной инфекцией, выявление наиболее часто встречаемых осложнений. Был выполнен подбор медицинских карт стационарных больных с заболеваниями, вызванными Herpes Zoster и анализ полученной информации статистическим, аналитическим, расчетным методами исследования.
Ключевые слова: Herpes Zoster, герпес-вирусная инфекция, осложнения герпес-вирусной инфекции, опоясывающий герпес, ветряная оспа.
Актуальность: На сегодняшний день герпес-вирусная инфекция остается одной из наиболее актуальных проблем для врачей всех специальностей. Вирус герпеса 3 типа представляет особый интерес для специалистов, так как заболевания, им инициированные, вызывают ряд серьезных неврологических осложнений. Последствия опоясывающего лишая и ветряной оспы заключаются в формировании невралгий, радикулита, энцефалита, поражения тройничного нерва головы и органа зрения. Предсказать взаимодействие между ВГЧ 3 типа и определенным организмом не представляется возможным. Существует 8 видов вируса герпеса и объединяет их склонность к латенции и бессимптомному носительству. Именно такими характеристиками обладает и Herpes Zoster — возбудитель ветряной оспы, который после перенесенной инфекции остается с человеком на всю жизнь в виде носительства и может в некоторых случаях проявляться повторно в виде такого заболевания, как опоясывающий лишай. Опоясывающий герпес является одной из распространенных вирусных инфекций человека. Частота в популяции повсеместно растет и достигает 200 случаев на 100000 населения в год (ВОЗ,2002). У лиц, переболевших ветряной оспой риск развития опоясывающего лишая составляет примерно 10–20 %. Группами риска тяжелого течения являются пациенты ВИЧ-инфицированные и с онкологической патологией. У большинства пациентов с опоясывающим лишаем развивается постгерпетическая невралгия, которая плохо поддается лечению и приводит к значительному снижению качества жизни пациентов. При этом выявление осложнений связано с трудностями диагностики, которая требует больших материальных и финансовых затрат, современного оборудования и квалифицированного персонала. Таким образом, герпес инфекция сопряжена со значительными экономическими потерями для общества — преимущественно ввиду утраты больными трудоспособности, ограничения повседневной активности вследствие выраженной невропатической боли, необходимости длительного приема медикаментов. Все это позволяет определить обширную проблему не только как актуальную медицинскую, но и социально-экономически значимую.
Цель работы: Выявление особенностей клинического течения у пациентов разного пола с герпес-вирусной инфекцией, статистическое выявления половозрастного состава пациентов с герпес-вирусной инфекцией, выявление наиболее часто встречаемых осложнений.
- Подбор медицинских карт стационарных больных с заболеваниями, вызванными Herpes Zoster.
- Анализ полученной информации статистическим, аналитическим, расчетным методами исследования
- Формулировка выводов
Материалы и методы исследования: Материалами исследования являются истории болезни на базе Краевой клинической инфекционной больницы. Методы исследования: статистический, аналитический, расчетный. Использовались программы: Microsoft Office 2010, Microsoft Excel 2010.
Полученные результаты: Из 52 историй болезни 2016–2017года с диагнозами герпес-вирусная инфекция было выявлено 42 истории болезни с герпес зостер, это составляет 80 %. Из 42 историй: мужчины составили 18(43 %), женщин 24 (57 %). Во внимание вошел возраст пациентов до 45 лет и 45 лет и старше, что в первом случае составило 20(47 %), во втором 22(53 %). Подтвержденные диагнозы лабораторно (ПЦР, ИФА): 35 (83 %) пациентов обнаружен ВПГ, и примерно у стольких же имеется ЦМВ. Лабораторного подтверждения диагноза у 7 пациентов отсутствовало. Из клиники: Поражение кожи головы: у 5 пациентов, поражение лица: у 19 пациентов, поражение ротоглотки: у 5 пациентов, поражение шеи: у 2 пациентов, поражение грудной клетки: у 13 пациентов, поражение межлопаточной области: у 2 пациентов, поражение живота: у 7 пациентов, поясничной области: у 5 пациентов, бедер, ягодиц: у 3, поражение всего тела: у 1 пациента.
Выводы: Из проведенных исследований выявлено, женщины болеют чаще, чем мужчины. Чаще поражаются вирусом герпеса пациенты старше 45 лет. На основе лабораторных данных можно сделать вывод, что герпес-вирус практически в 80 % сочетается с ЦМВ. Редко встречаются изолированные формы, чаще поражение затрагивает 2–3 области. Чаще затрагиваются область лица, сопровождающаяся невритом тройничного нерва и область грудной клетки, сопровождающаяся ганглионевритом Th1-Th12. Высыпания сопровождаются выраженным болевым синдромом. Имеет место интоксикационный синдром, длящийся не более 3 суток (подъем температуры тела до 38–39`С, слабость, недомогание, ломота в теле). Исходя из статистических данных нашего исследования в 47 % случаев развиваются постгерпетические невриты пораженных областей.

Как, согласно новым взглядам, надо бороться с этой инфекцией? Слово – экспертам.
Не снаружи, а изнутри

Научный руководитель Центра вирусной патологии кожи г. Москвы, доктор медицинских наук, профессор Алексей Халдин:
Этот коварный вирус также может поражать почки, желудок, прямую кишку, печень. Мало кто знает о герпетическом гепатите, а ведь он существует. У детей герпес чаще стартует во рту – в виде стоматита. А у многих взрослых может протекать и без внешних признаков, маскируясь под синдром хронической усталости.
Словом, проявления герпеса на коже – это лишь видимая часть айсберга. Поэтому нужно воздействовать на него не снаружи, только мазями и гелями, а изнутри. Для этого существуют современные схемы профилактики и лечения. Тогда вам удастся держать герпес под контролем – то есть уживаться с ним без снижения качества жизни и не заражать им окружающих.

Подавляющая терапия
– В России герпетическую болезнь сегодня лечат точно так же, как и во всём прогрессивном мире. Существует два современных подхода. Первый – это лечение каждого конкретного обострения, поэтому он так и называется – эпизодическая терапия. Такой подход годится, когда герпес обостряется не чаще шести раз в год.
Едва почувствовав признаки обострения (например, характерные ощущения на губе), человек начинает принимать специальный препарат. А именно одно из трёх противовирусных лекарств, действующих именно на семейство герпесов: ацикловир, валацикловир или фамцикловир. Каждый из них блокирует деление вирусов.
Но если обострения случаются чаще (каждые один-два месяца), применяется другая схема. Она носит название подавляющей терапии. В этом случае человек принимает противогерпетический препарат постоянно в малой дозе. Например, валацикловир по 500 мг раз в день. При таком режиме лечения число эпизодов герпеса уменьшается в 10 раз. Многократно снижается и риск передачи вируса окружающим.
Подавляющее лечение длится год, затем делается перерыв. Мы наблюдаем, как будут развиваться события. И во многих случаях новой вспышки инфекции не происходит.

Профилактический приём

Профессор кафедры дерматовенерологии Санкт-Петербургского государственного медицинского университета им. И. П. Павлова, доктор медицинских наук Елена Аравийская:
– Есть и ещё один подход к обузданию герпеса – профилактический. Его смысл в том, чтобы предотвратить обострение, когда его риск повышен. Например, перед проведением медицинских вмешательств в организм, при которых повреждаются глубокие слои кожи. Ведь любая травма приводит к снижению защитных свойств кожи и общего иммунитета и потому способна разбудить спящий вирус.
Делаете ли вы эстетическую операцию на лице, удаляете ли зубы – во всех подобных ситуациях мы рекомендуем профилактический приём валацикловира. Его начинают за 2–3 дня до вмешательства и продолжают ещё 7–8 дней после.
Если же планируется целая серия процедур, значит, защитные свойства кожи будут нарушены на более долгий срок. И тогда противовирусное лечение удлиняется до целого месяца.

Импульсная схема

Профессор кафедры нервных болезней Первого МГМУ им. И. М. Сеченова, исполнительный директор Ассоциации междисциплинарной медицины, доктор медицинских наук Алексей Данилов:
– Самые тяжёлые осложнения герпетической инфекции – опоясывающий лишай и постгерпетическая невралгия.
Вирус герпеса деформирует нервную систему на периферическом уровне, и вначале это проявляется в виде высыпаний. Но через несколько недель, месяцев или даже лет, откуда ни возьмись, возникает выраженная боль – чаще в области грудных нервов. Справиться с ней самостоятельно подчас невозможно годами. Причина этой проблемы – резкая активация живущего в организме вируса. Обычно на фоне сниженного иммунитета, после 50 лет.
К сожалению, многим пациентам в такой ситуации ошибочно назначают анальгетики, но они при этом типе боли совершенно неэффективны. Пользу же принесут специальные противовирусные препараты от герпеса.
Если же невралгия уже проявилась, также понадобятся особые препараты из группы антиконвульсантов и антидепрессантов.
Слово " герпес " (гр. - ползти) используется почти 25 веков. Лихорадочный герпес был описан римским врачом Геродотом в 100 году до н.э. О генитальном герпесе впервые сообщил французский врач J. Astruc в 1736 г.
Генитальный герпес поражает все популяционные группы. 98% взрослого населения во всем мире имеют антитела к ВПГ-1 или 2. В 7% генитальный герпес протекает бессимптомно. ВПГ-2 в 80% является возбудителем генитального и неонатального герпеса, в 20% - ВПГ-1.
Первичный эпизод генитального герпеса обычно возникает после интимного контакта с инфицированным лицом. Инкубационный период длится в среднем 1-3 недели. У женщин чаще всего поражаются половые губы, вход во влагалище, устье мочеиспускательного канала, но могут возникать и экстрагенитальные поражения промежности, перианальной области, бедер и ягодиц, причем у 70-90% женщин диагностируется цервицит.
Первичный герпетический вульвовагинит характеризуется развитием выраженного отека и гиперемии больших и малых половых губ, влагалища, области промежности. На фоне гиперемии появляются сгруппированные пузырьки. После их вскрытия образуются мокнущие эрозии, часть из них постепенно сливается между собой, образуя неглубокие болезненные язвочки. Эрозивно-язвенные дефекты эпителизируются с образованием пигментных пятен.
У мужчин в воспалительный процесс обычно вовлекается головка, крайняя плоть, кожа полового члена, мошонки, реже - внутренняя поверхность бедер и ягодиц.
При первичном эпизоде генитального герпеса высыпания сопровождаются выраженными местными симптомами (болью, жжением, зудом, покалыванием), могут беспокоить боли по ходу седалищного нерва, дизурические явления, выделения из влагалища, уретры, паховый лимфаденит. Рецидивы простого герпеса возникают с разной частотой - от 1-2 раз в год до нескольких эпизодов в месяц. Провоцирующими факторами рецидивов часто служат другие инфекционные заболевания, сопровождающиеся лихорадкой, длительные переохлаждения, УФ-облучение, психические или физические стрессы, острые дисфункции или циклические (менструации) изменения гормонального статуса.
Стоит также отметить роль ВПГ как Ко-фактора в развитии канцерогенеза женской половой сферы. В последние два десятилетия учеными обсуждается вопрос о возможной роли вируса простого герпеса в этиопатогенезе рака шейки матки. Однако, прямых доказательств нет. Считается, что ВПГ-инфекция сопровождается развитием фоновых процессов шейки матки (в 30%).
Установление вирус-специфических антигенов в материалах от женщин с предраковыми состояниями эпителия шейки матки указывают на нахождение в них генома вируса простого герпеса, имеющего в структуре ДНК онкогены. Об онкогенной активности ВПГ и его возможном участии в этиологии и патогенезе рака шейки матки свидетельствует способность вируса, его ДНК или ее фрагментов трансформировать клетки фибробластов эмбрионов хомячка, мышей, которые при имплантации соответствующим животным вызывают у них метастазирующие опухоли. В сыворотке крови этих животных появляются вирус-нейтрализующие антитела, реагирующие с вирус-специфическими антигенами трансформированных клеток. Все вышесказанное свидетельствует о возможной роли вируса простого герпеса типа 2 в этиологии некоторых злокачественных новообразований. Заслуживает внимания тот факт, что частота обнаружения с применением ИФ, РСК ранних вирус-индуцированных антигенов ВНГ-2 в опухолевых клетках раковых больных значительно выше, чем частота выявления вирусного антигена или инфекционного вируса. Выявление герпетических антигенов в опухолях человека представляет интерес в изучении роли вируса простого герпеса типа 2 в происхождении злокачественных новообразований, а также для разработки методов специфической иммунодиагностики и иммунопрофилактики. Антитела к ВПГ обнаруживаются у 76,9% женщин с дисплазией в РСК и у 96,2% - в РН, при начальном раке (1 стадия) - у 68 и 93,6%, при выраженном (2,3 стадии) - у 90 и 100% соответственно.
В настоящее время для лечения герпетической инфекции используется противовирусная терапия, иммунотерапия и комбинация этих методов в зависимости от фазы и тяжести течения заболевания.
Наружное назначение противовирусных препаратов при герпесвирусной инфекции кожи и слизистых оболочек необходимо для уменьшения клинических проявлений в очаге поражения, ускорения эпителизации и сокращения длительности выделения вируса из очага.
Традиционно основу местной терапии на всех стадиях герпетического процесса составляли мази с ацикловиром, что связано с их прямым противовирусным действием. Однако, как известно, в последние годы появляется все большее число штаммов вируса герпеса, которые оказались частично или полностью устойчивыми к ацикловиру.
Среди основных механизмов резистентности к ацикловиру в настоящее время описаны отсутствие индукции вирусом специфической тимидинкиназы. Другим механизмом является наличие генетического дефекта этого фермента при нормальном уровне его продукции, что приводит к невозможности фосфорилирования ацикловира. Третий механизм связан с мутацией в гене ДНК-полимеразы, в результате чего снижается чувствительность к тормозящему действию ацикловир-трифосфата. Вследствие этого применение ацикловирсодержащих противовирусных средств не прерывает репликации вируса. Поэтому поиск новых или альтернативных средств терапии герпесвирусной инфекции человека является одной из актуальных проблем.
Компания "Вертекс" выпустила на рынок новую форму рибавирина для лечения генитального герпеса, не имеющую аналога в России: в виде крема для наружного применения - Девирс.
На сегодняшний день рибавирин обладает наиболее широким спектром прямой противовирусной активности против большинства РНК- и ДНК-вирусов. Наиболее чувствительны к рибавирину ДНК-вирусы, в особенности вирус простого герпеса. Установлено, что рибавиринтрифосфат (РТФ) является мощным ингибитором инозинмонофосфатдегидрогеназы (ИМФ-дегидрогеназы). Рибавирин также встраивается в вирусный геном, вызывая летальные мутации, с последующим снижением патогенности вируса. Рибавирин ингибирует репликацию новых вирионов, что обеспечивает снижение вирусной нагрузки, селективно ингибирует синтез вирусной ДНК, не подавляя синтез ДНК в нормально функционирующих клетках, что принципиально отличает его от механизма действия ацикловира.
Клиническая эффективность рибавирина в виде крема для лечения генитального герпеса подтверждена международными исследованиями.
Zertuche H.F., Perches R.D. (1977) опубликовали данные об использовании рибавирина у 390 больных в Мексике для лечения различных вирусных инфекций. Исследование продемонстрировало клиническую эффективность и отсутствие серьезных токсических эффектов.
В исследовании (двойное слепое рандомизированное плацебо-контролируемое) Fernandez et al. (1980) выявлена эффективность сочетанного применения рибавирина при наружном (5% мазь) и внутреннем (капсулы 800 мг внутрь) способах введения при опоясывающем герпесе, развившемся на фоне химиотерапии у 74 пациентов.
Исследования, проведенные в Бразилии [Lorenco R., 1977] и в Южной Корее [Sung K.J. Kim K.J., 1980], также показали эффективность рибавирина при herpes zoster. В обоих исследованиях препарат назначался перорально в дозе 800 мг в сутки в течение 10 дней. Получено достоверное значимое уменьшение продолжительности болевого синдрома и времени формирования корок.
Клиническое исследование, проведенное в Дерматологическом центре Пасхи (Romero, Navarette, 2000) продемонстрировало высокую эффективность сочетанного применения рибавирина при приеме per os (капсулы) и per cutis (7,5% крем) по сравнению с плацебо при лечении постгерпетической невралгии, являющейся нередким осложнением herpes zoster (20% больных). В этом исследовании применение рибавирина приводило к статистически достоверному уменьшению интенсивности болевого синдрома более чем в 5 раз по сравнению с плацебо.
В исследовании S.M. Bierman, W. Kirkpatrick (1981) показана эффективность перорального приема рибавирина (капсулы 800 мг) у 48 пациентов при опоясывающем герпесе, что выражалось в уменьшении болевого синдрома, ускорении заживления и формирования корок на месте везикул.
В исследовании Nicollini et al. (1996) подтверждена клиническая эффективность рибавирина при сочетанном приеме внутрь (капсулы 800 мг) и наружно (крем 8%) у пациентов с генитальным и/или опоясывающим герпесом на фоне химиотерапии острых лейкозов.
Еще одно клиническое исследование, проведенное в Италии [M. Marchesi et al., 1999], показало эффективность наружного применения 7,5%-го крема рибавирина в виде аппликаций на участки кожи и слизистых, пораженные генитальным герпесом. Почти 35% больных отмечали снижение выраженности болевого синдрома и зуда на 10-14-й дни терапии, 23% отметили образование стойких кожных корочек, свидетельствующих о заживлении. Однако в этом же исследовании комбинация перорального и перкутанного применения рибавирина приводила к более выраженному результату, выражавшемуся в уменьшении степени выраженности боли и зуда у 63% пациентов и ускоренном формировании поствезикулярных корочек у 58% больных к 8-9-м суткам от начала терапии рибавирином. Тем не менее результаты данного исследования свидетельствуют о целесообразности назначения рибавирина в качестве средства монотерапии для наружного применения (7,5%-й крем) при лечении генитального герпеса. Вероятно, такая терапия больше подходит при легких и малораспространенных герпетических поражениях слизистой половых органов, проявляющихся преимущественно зудом или чувством жжения/дискомфорта.
K. Reinchart, B. Gehgolnt (1998) опубликовали исследование, в котором оценивалась эффективность и безопасность наружного применения рибавирина (крем 7,5%) у пациентов с генитальным герпесом на фоне доказанного путем проведения иммунологического исследования крови относительного дефицита гуморального иммунитета. Из 45 пациентов, принимавших участие в исследовании, лишь треть субъективно отметила снижение выраженности боли и зуда в области гениталий к 16-му дню терапии, почти половина обследуемых имели сформированные корочки в области везикул к 24-26-му дням лечения. Вероятно, на результаты данного исследования наложил отпечаток факт наличия у испытуемых относительного иммунодефицита, доказанного лабораторными методами. В отношении безопасности препарата авторы указывают, что 5 (11%) из 45 пациентов отмечали чувство покалывания при первом нанесении крема. 2 (4,4%) пациента выбыли из исследования по причине развития местной аллергической реакции с образованием на фоне герпетических везикул уртикарных высыпаний на коже в 1-й день терапии.
Применение Девирса при генитальном герпесе уменьшает клинические проявления в очаге поражения, ускоряет эпителизацию и сокращает длительность выделения вируса из очага. Девирс ингибирует репликацию новых вирусов, что обеспечивает снижение вирусной нагрузки, селективно ингибирует синтез вирусного генома, не подавляя синтез ДНК в нормально функционирующих клетках. Важно, что Девирс, обеспечивая мощное противовирусное действие в очаге поражения, не оказывает резорбтивного действия.
Противовирусная активность Девирса связана с блокадой гуанозин-зависимых ферментов - Девирс ингибирует фермент инозинмонофосфатдегидрогеназу (ИМФДГ), что приводит к нарушению синтеза гуанозинтрифосфата и нуклеиновых кислот. Таким образом, противовирусное действие Девирса не перекликается с механизмом действия ацикловира, что обуславливает потенцирование противовирусного эффекта ацикловира
Девирс имеет значительную цитокинную активность и индуцирует переход иммунного ответа, стимулируя Th1 ответ и подавляя Th2 ответ. Подтип Th1 иммунного ответа обусловливает мощную антивирусную реакцию. Девирс запускает пролиферацию Th1 клеток, которые продуцируют интерлейкин 2 (IL-2), фактор некроза опухоли (TNFα) и интерферон гамма (IFNγ), а они отвечают в свою очередь прежде всего за клеточно-опосредованный иммунитет. Это ведет к запуску цитотоксической реакции и к гибели клетки, инфицированной вирусом. При этом Девирс блокирует подтип Th2 иммуного ответа, который ассоциируется с персистенцией вируса в организме и может представлять собой механизм ускользания вируса от иммунного ответа хозяина.
Стоит также отметить, что, помимо монотерапии, крем Девирс может применяться и в комбинации с другими лекарственными формами рибавирина, предназначенными для парентерального и перорального применения, а также в сочетании с иммунокорригирующей терапией, создавая синергический эффект в отношении вируса и преодолевая резистентность к системной терапии.
Добавление Девирса в терапию генитального герпеса обеспечивает быстрое купирование рецидива и сокращение сроков лечения.
Таким образом, обзор клинических исследований с применением рибавирина в форме для наружного применения крем в концентрации 7,5% свидетельствует о его эффективности, безопасности и хорошей переносимости у пациентов с генитальной формой герпеса, что делает его препаратом выбора в лечении данной нозологии по сравнению с другими антивирусными нуклеозидами.
Читайте также:


