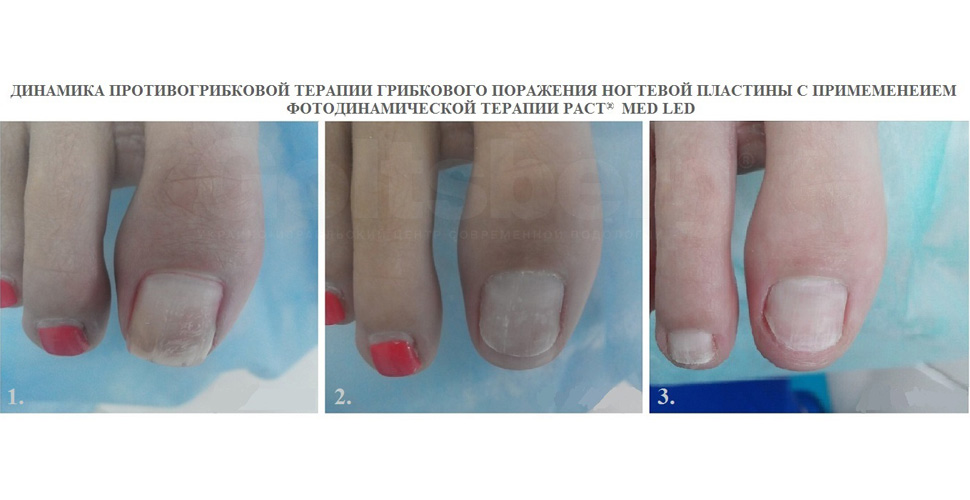
Фотодинамическая терапия лечение микоза
PACT ТЕРАПИЯ – РЕВОЛЮЦИЯ В ИЗБАВЛЕНИИ ОТ ОНИХОМИКОЗА
Появившись в России всего несколько лет назад, PACT терапия быстро набирает обороты и становится популярной. Явные успехи применения этой новинки побуждают многих клиентов, отчаявшихся избавится от онихомикоза, еще раз побороться за свое здоровье. Но информации об этом виде терапии мало и несмотря на накопленную статистику успешного применения в России, мало кто из мастеров и тем более клиентов, хорошо понимает, что представляет собой эта методика и что вообще означает это слово? Давайте разбираться))

После доказанного успешного применения для уничтожения патогенной микрофлоры, в том числе бактерий, неподвластных антибиотикам, методика стала тестироваться для применения против грибковых инфекций и успешно развиваться в этом направлении. Фирма Hahn Medical (Германия) в сотрудничестве с кафедрой микробиологии Университета Тюбинген (Германия) применила технологию для фотодинамической обработки онихомикозов и разработала соответствующую методику лечения. В 2012 году был выпущен прибор PACTmed, который с мая 2012 года появился в России и начал завоевывать доверие как медиков, так и мастеров аппаратного педикюра.
Лазер представляет собой монохроматического когерентное излучение, которое широко применяется в медицине и косметологии (бескровные скальпели, лазерная коррекция зрения, лазерные эпиляция, пилинг и тп). Несмотря на отличия в применяемых видах лазеров, которые заключаются в способе получения и длине луча, продолжительности импульса, технологии охлаждения кожного покрова и передаваемой энергии излучения, которая проходя по коже, сетчатке, стержню волоса или другой цели преобразуется в тепловую они все повреждают цель излучения. Нагрев разрушает клетки, которые являлись мишенью лазера. Не вдаваясь в подробности, мы акценируем внимание на том, что лазерное излучение носит разрушительный характер.
PACTmed излучатель – представляет собой светодиод с длиной волны 630-640 нм, площадью 0,5 см2, мощностью 1Вт. Такое излучение совершенно недостаточно для ожога и повреждения кожи. На шкале видимого спектра соответствует красному цвету и не имеет никакого отношения к инфракрасному излучению. Прибор не имеет никаких скрытых излучений. Вентилятор, встроенный в прибор предназначен для охлаждения самого светодиода, а не кожного покрова, как при лазерном излучении.
Однако само по себе излучение совершенно безвредно для ВСЕХ клеток, в том числе клеток грибов. Нужна вторая составляющая – хлорид толлония – толлудиновый синий.
Это действующее вещество активно используется в медицине в качестве маркера. Его вводят в кровь в специальных исследованиях и оно имеет свойство накапливаться в тканях. То есть сам по себе маркер толлудиновый синий – абсолютно безопасное и безвредное вещество. В гидрогеле, который используется для проведения процедуры кроме хлорида толлония присутствует основа, консервант и вещество, облегчающее пенетрацию (проникновение в ткани) и никаких противогрибковых компонентов.
Итак, мы имеем безопасный излучатель нужной нам мощности и длины волны и безопасный гель с маркером. При облучении маркера начинается интенсивная химическая реакция с образованием активного кислорода O-, который обладает цитологическим действием и губителен ДЛЯ ОПРЕДЕЛЕННОГО ВИДА клеток. Упрощенно говоря, человеческие клетки обладают толстой проницаемой мембраной, которая пропускает активный кислород О- без каких бы то ни было повреждений. А вот клетки грибов и бактерий имеют хрупкую клеточную стенку, состоящую из хитина и для активного О- эта стенка непроницаема. Активные О-, как нам известно из курса школьной химии, стремятся навстречу друг другу, чтобы соединится в стабильную форму О2, на всякий случай, заметим, абсолютно безопасную форму :))
В своем стремлении к объединению, О- проносятся безопасно через мембрану клеток, никак ее не повреждая и разрушают на своем пути хрупкие хитиновые стенки клеток грибов, что очевидно вызывает их гибель. Вот так, абсолютно безопасно и предельно точно истребляются ТОЛЬКО клетки грибов!
С уверенностью можно сказать, что PACT Med - революция в работе с грибковыми ногтями. Фотодинамика настолько проста и безопасна в применении, что может использоваться как в медицинском учреждении, так и квалифицированным мастером педикюра, подологом. В отличие от распространенных в мире методик, фотодинамика сочетает безопасность местной терапии и эффективность системной, не неся при этом никаких побочных эффектов.
Таким образом при индивидуальном подходе к лечению, учитывающем все особенности состояния здоровья пациента, при соблюдении графика посещений и грамотном проведении процедуры – PACT терапия, пожалуй, лучшая на сегодняшний день методика, безопасная, простая, физиологичная и эффективная.
Если Вы столкнулись с такой проблемой, как грибок ногтей (онихомикоз), очень важно своевременно обратиться к специалисту, а так же выбрать лучший метод терапии и приступить к лечению грибка.
Современная медицина предлагает множество способов лечения грибка ногтей на руках и ногах, вот самые популярные из них:
- Местное лечение грибка ногтей с применением аптечных противогрибковых средств (мазей, кремов, лаков и т.д.). Низкая эффективность данного метода связана с тем, что аптечные средства, в отличие от грибковой инфекции, не проникают в глубокие слои ногтевой пластины, а так же, могут вызывать привыкание, что значительно усложняет последующее лечение грибка ногтей;
- Медикаментозный способ лечения грибка ногтей на ногах или руках предполагает системный прием антимикотиков и гепатопротекторов пульс-терапией. Вещества проникают глубоко в организм. Основные минусы данного метода – высокая токсичность для организма и множество противопоказаний;
- Хирургическое лечение грибка ногтей (частичное или полное удаление ногтевой пластины). Данный метод является малоэффективным, т.к. велика вероятность отрастания деформированного и зараженного ногтя в будущем. Среди минусов метода так же его травматичность, болезненность и длительный период восстановления;
- Лазерное лечение грибка ногтей. Метод лечения лазером имеет ряд противопоказаний и побочных эффектов, является травматичным и болезненным за счет термического воздействия горячим лазерным лучом на ноготь, околоногтевые ткани, зону роста ногтевой пластины;
- Фотодинамическая терапия PACT® (блокировка грибковой инфекции путем напитки ногтевой пластины и околоногтевых тканей комплексом противогрибковых и противоинфекционных препаратов при помощи холодного светового луча PACT® Med Led) - инновационный метод противогрибковой терапии, базирующийся на применении фотосенсибилизаторов (PACT-красителей). Грибковые инфекции становятся чувствительны к свету за счет того, что происходит прокрашивание клеточных стенок. Под действием света PACT® грибковые инфекции и бактерии погибают в течение нескольких минут. Фотодинамическая терапия абсолютно безболезненна и не имеет побочных эффектов и противопоказаний.
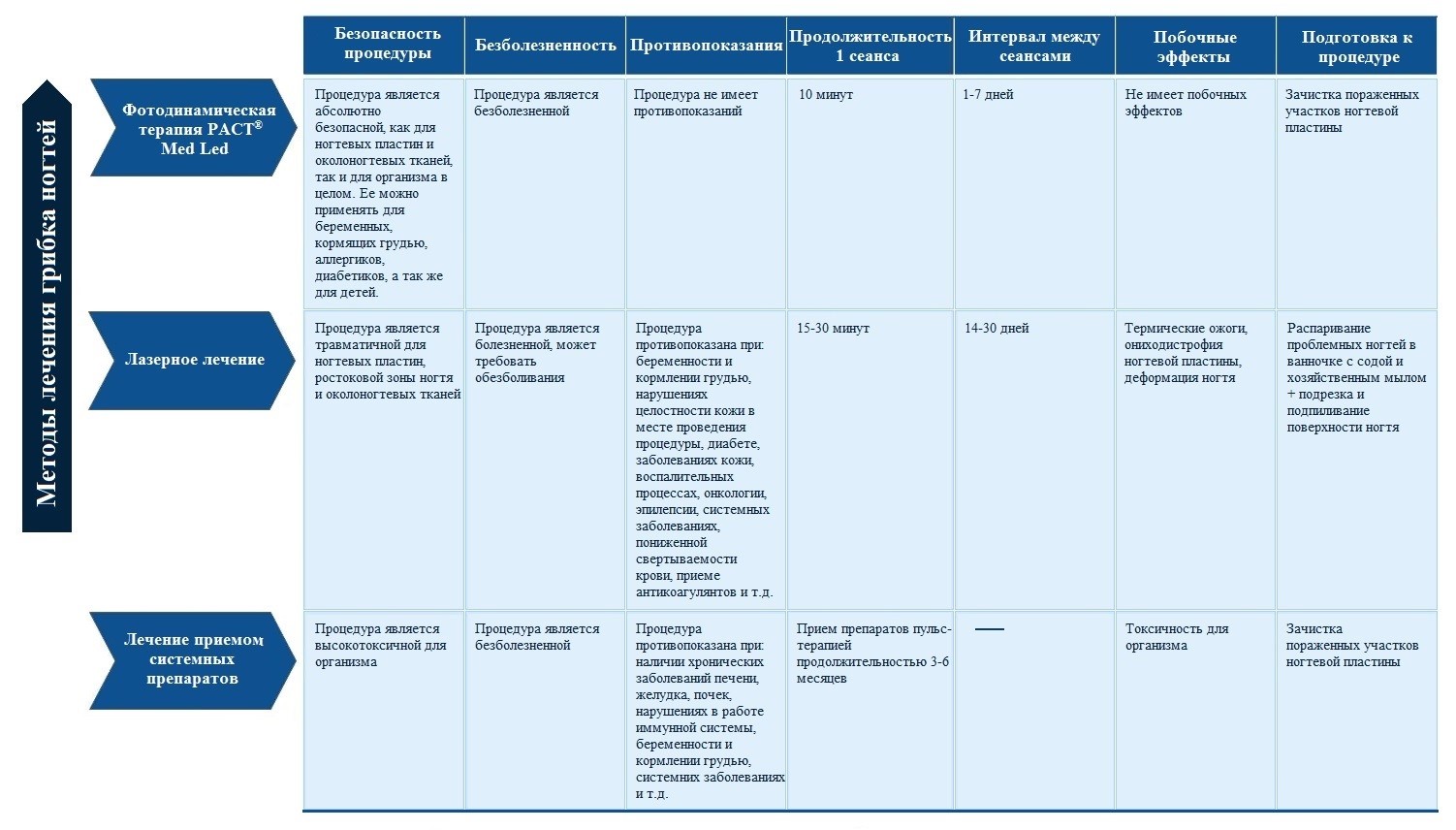
Ниже приведена таблица сравнения наиболее популярных методов лечения грибковой инфекции ногтевых пластин:
Метод Фотодинамической терапии PACT® Med Led впервые представлен немецкими учеными компании Hahn Medical в 2013 году после 14-летнего сотрудничества с кафедрой микробиологии Университета Тюбинген, доказал на практике свою эффективность и безопасность. Именно поэтому Украино-израильский Центр современной подологии Goltsberg® выбрал метод противогрибковой Фотодинамической терапии PACT® Med Led для помощи нашим клиентам в борьбе с грибковыми поражениями ногтевых пластин на пальцах рук и ног, а так же воспалительными процессами!
- Как работает PACT® Med Led?
Принцип действия Фотодинамической терапии PACT® основан на разнице в строении клеток грибка и здоровых клеток человека. Во время сеанса Фотодинамической противогрибковой терапии на ногтевую пластину наносится специальный гель, который проникает глубоко в ногтевую пластину и делает мембраны клеток грибка чувствительными к свету определенной длины волны. При воздействии на пораженный участок ногтя световыми волнами пигмент, содержащийся в геле и прокрашивающий стенки клеток грибка, распадается, образуя при этом активный кислород, который разрушает клетки грибка.
Огромное преимущество метода Фотодинамической терапии PACT® в том, что он позволяет воздействовать на грибок и блокировать инфекцию без вреда для здоровья!
-
Почему мы рекомендуем PACT® Med Led?
При стандартной схеме лечения у врача-дерматолога пациентам назначается прием антимикотиков (противогрибковых таблеток), которые оказывают негативное воздействие на желудочно-кишечный тракт, печень и почки, или болезненное лечение горячим лазером, травмирующее ростковую зону ногтя. Мы рекомендуем Фотодинамическую терапию PACT®, потому что понимаем, что на сегодняшний день это практически единственный абсолютно безопасный и безболезненный способ избавления от грибка ногтей.
Метод Фотодинамической терапии PACT®:
- Абсолютно безопасен для здоровья, его можно применять при беременности, грудном вскармливании, склонности к аллергиям, сахарном диабете и т.д.
- Блокирует любые типы грибковых инфекций, а так же стойкие к действию антибиотиков бактерии;
- Не причиняет болевых ощущений или дискомфорта в виде покалывания, стягивания или любых других неприятных ощущений;
- Сеанс длится минимум времени.
- Как проходит сеанс Фотодинамической терапии PACT®?
Сеансы Фотодинамической терапии возможно проводить при любом состоянии здоровья, проведение сеанса не требует предварительной подготовки со стороны клиента. Количество необходимых сеансов PACT® определяет специалист-подолог с учетом стадии, сложности и обширности грибкового поражения. Процедура проходит следующим образом: перед сеансом Фотодинамической терапии PACT® специалист проводит зачистку пораженных участков ногтевой пластины, после чего на ногтевую пластину наносится специальный гель PACT® и проводится сеанс воздействия световыми волнами PACT® на пораженный участок в течение 9–9,5 минут. После процедуры специалист назначает дату следующего сеанса. Между сеансами специалист-подолог может назначить применение местных противогрибковых средств (не аптечных) или средства для стимулирования быстрого срастания и укрепления ногтевой пластины. После окончания курса Фотодинамической терапии PACT® Вам необходимо посещать подолога для осуществления контроля за ростом ногтевой пластины на протяжении всего периода срастания ногтя (для ногтей на пальцах рук – в среднем, до 6 месяцев, на пальцах ног – в среднем, до 12 месяцев). В запущенных случаях, когда грибковая инфекция прогрессирует, избавление от грибка ногтей может занимать более длительный период и может требовать повторных процедур Фотодинамической терапии PACT®.
Доверьте восстановление здоровья и красоты Ваших ногтей специалистам Центра современной подологии Goltsberg!
Доверьте лечение грибковой инфекции лучшим специалистам!
Быстрое лечение ногтей, или как убить грибок за три месяца
Новейшие противогрибковые препараты не только активно действуют на грибок, останавливая развитие микоза. Они еще и надолго задерживаются в ногтях, что позволяет сократить срок лечения. Современные противогрибковые препараты обычно принимают в течение 2–4 месяцев (вместо 6–12), а в наиболее прогрессивных схемах (пульс-терапия) – и того меньше – несколько недель. Это делает лечение намного более удобным и доступным для пациентов. Однако напомним еще раз, что эти противогрибковые средства назначает только врач. При некоторых поражениях ногтей стандартная схема не работает. Но не все врачи подбирают дозу и продолжительность лечения правильно.
Местная и комбинированная терапия онихомикоза
Новые формы наружных противогрибковых средств пришлись как нельзя кстати. В виде противогрибковых лаков для ногтей появилась возможность местного лечения онихомикоза, нанося препарат всего 1–2 раза в неделю. Для тяжелых форм онихомикоза предусмотрено сочетание новых наружных форм с системной терапией (лечение капсулами или таблетками). Появились такие комбинированные препараты, где противогрибковые компоненты сочетаются с кератолитическими, то есть размягчающими роговые массы. Это позволяет бороться с утолщением ногтей.
С последней задачей справляются также появившиеся в последнее время устройства для аппаратной обработки – видоизмененные бормашины с особыми фрезами для ногтей. Следует заметить, что такие машинки начали использовать в СССР еще в 1930х гг., но после войны этот метод забыли. А сегодня некоторые специалисты выдают это за иностранную технологию, позволяющую радикально избавиться от грибка ногтей за пару сеансов. Это неверно. Инфекция не лечится в педикюрном салоне.
Лечение грибка лазером и фотодинамическая терапия ногтей
Современные способы борьбы с грибком без использования химических веществ - лекарственных препаратов - были разработаны на основе физического воздействия (интенсивного светового излучения) на грибок. К таким новым методикам, уже показавшим свою эффективность, можно отнести фотодинамическую обработку пораженных грибком ногтевых пластин и лазерное лечение грибка на специальных "ногтевых" лазерах. Они отличаются от косметологических и хирургических лазеров особыми режимами работы. Применение лазера и ФДТ в сочетании с противогрибковым лечением позволяет существенно сократить сроки излечения от грибка ногтей. Но и лазер не является панацеей. Если Вам обещают победить грибок "без лекарств" любым аппаратом или устройством, то, скорее всего, Вас вводят в заблуждение. Более того, врачи за рубежом и в нашей стране еще спорят, какие лазеры и фотоустановки можно и нужно применять при онихомикозе. Этот вопрос еще не решен, а чья-то реклама уже кричит о победе над грибком!
Как выбрать подходящий метод лечения ногтевого грибка?
Многообразие проявлений онихомикоза делает невозможным его универсальное лечение каким-либо одним методом или противогрибковым средством. Есть такие разновидности ногтевого грибка, для которых больше подходят растворы, лаки и другие местные средства. Есть поражения ногтей, где требуется назначение препаратов внутрь, или необходима чистка ногтей или даже их удаление. Определить это может только квалифицированный врач.
Именно это – отсутствие правильно подобранного метода лечения – объясняет неудачи самолечения онихомикозов. Даже врач не сразу определяет, какой именно метод лечения выбрать, сколько нужно принимать тот или иной противогрибковый препарат, какие дополнительные методы лечения следует привлечь. Это устанавливается в ходе обследования пациента и выяснения особенностей заболевания. Для этого могут потребоваться дополнительные анализы – например, установление вида грибка, или показаний/противопоказаний к назначению конкретного препарата.
Программа Национальной академии микологии с 2003 года по борьбе с массовыми заразными грибковыми заболеваниями в России
Одной из наиболее актуальных задач современной дерматологии является изучение механизмов развития, разработка ранних критериев диагностики и дальнейшее совершенствование методов лечения злокачественных Т-лимфом. Среди них наибольший удельный вес приходит
Одной из наиболее актуальных задач современной дерматологии является изучение механизмов развития, разработка ранних критериев диагностики и дальнейшее совершенствование методов лечения злокачественных Т-лимфом. Среди них наибольший удельный вес приходится на грибовидный микоз (ГМ). Согласно современным взглядам, биологическая сущность ГМ, вне зависимости от клинических проявлений и стадии процесса, определяется как пролиферация трансформированных Т-лимфоцитов [3, 6]. Причем ГМ относится к лимфомам низкой степени злокачественности.
Разнообразие клинических проявлений, отсутствие единых критериев систематизации патологического процесса, а также изменение представлений о кроветворении объясняют разнообразие различных классификаций злокачественных лимфом кожи. Так, L. Fuks оценивает степень тяжести ГМ следующим образом: I стадия — поражение только кожи; II стадия — поражение кожи и дерматопатический лимфаденит; III стадия — поражение кожи, регионарных лимфоузлов и/или селезенки; IV стадия — кожные и внекожные поражения с или без вовлечения в патологический процесс лимфоузлов и селезенки. Группа исследователей из ФРГ выделяет 5 стадий ГМ: I–III стадии — кожный ГМ (I — экзематоидные очаги поражения, II — папулы и бляшки, III — опухолевидные очаги поражения); IV стадия — кожный ГМ с лимфоаденопатией; V стадия — любые клинические проявления при наличии поражения внутренних органов. В основу классификации, применяемой в США, положена оценка степени выраженности следующих элементов лимфопролиферативного процесса: клиническая характеристика кожного процесса (T — tumor); наличие или отсутствие клинической и гистологической патологии лимфоузлов (N — nodus); наличие или отсутствие патологии внутренних органов (M — metastasis). Каждый элемент имеет несколько градаций, обозначаемых цифрами, которые отражают степень или распространенность патологического процесса. Учитывая несовершенство многочисленных классификаций ГМ, до настоящего времени в дерматологии широко применяется деление ГМ на 3 стадии: экзематоидно-эритродермическую, инфильтративно-бляшечную и туморозную [4, 5].
Таким образом, анализ литературного материала показал, что ГМ выделяется в самостоятельную нозологию и рассматривается как экстранодальная, поражающая преимущественно кожу, эпидермотропная лимфома, представленная инфильтрацией Т-хелперных клеток, имеющая своеобразную клинику, течение и патогистологическую картину.
Этиология и патогенетические механизмы ГМ до сих пор не ясны. До настоящего времени не известны побудительные мотивы неконтролируемой Т-клеточной пролиферации. Предполагается, что возникновение ГМ может быть связано с персестирующей вирусной инфекцией. Так, в ряде работ сообщается о выявлении в первичной клеточной культуре, полученной из лимфоузла больного в инфильтративно-бляшечной стадии ГМ, вирусных частиц, морфологически характерных для ретровирусов типа С [15]. Кроме того, в ДНК первичных клеточных культур, полученных от больных ГМ, выявлено наличие последовательности, родственной гену gag HTLV-1.
Определенную роль в возникновении злокачественных лимфом отводят генетическим факторам. Доказано, что развитие различных видов солидных опухолей и лейкемий связано с появлением и дальнейшим нарастанием хромосомных аномалий. В последние годы появились публикации о хромосомных перестройках при ГМ, которые способствуют активации онкогенов и инактивации генов опухолевой супрессии при развитии лимфопролиферативного процесса. В настоящее время в литературе широко обсуждается положение о том, что значимые патогенетические факторы ГМ могут быть носителями ксеногенной информации, приводящей к патологическим сбоям в функционировании различных систем и клеток макроорганизма [13]. В первую очередь такие изменения наблюдались со стороны иммунокомпетентных клеток, эпидермоцитов, макрофагальных элементов кожи, рецепторного аппарата кожи и продукции цитокинов. Имеющиеся в отечественной и зарубежной литературе сведения о состоянии иммунного гомеостаза убедительно свидетельствуют о стойких патологических сдвигах как в клеточном, так и в гуморальном звеньях иммунитета. Анализ иммунного статуса показал, что у большинства больных ГМ при нормальном количестве в сосудистом русле В-лимфоцитов среднее содержание Т-клеток значительно снижено по сравнению с показателями здоровых доноров. Отмечено снижение как Т-супрессорных, так и Т-хелперных лимфоцитов, причем количество последних снижается более существенно. Относительную лимфопению многие авторы рассматривают как наиболее часто встречающийся гематологический признак ГМ. Другие, кроме того, отмечают наличие абсолютной лимфопении в опухолевой стадии заболевания. Функциональная активность лимфоцитов у больных ГМ, по данным ряда авторов, снижена. Другие сообщают об отсутствии достоверных различий в характере пролиферации лимфоцитов периферической крови больных и здоровых лиц. Установлено, что течение патологического процесса при ГМ сопровождается снижением активности естественных киллеров.
Разноречивы результаты исследований состояния гуморального звена иммунитета. В ряде работ не выявлено существенных нарушений в продукции В-лимфоцитами иммуноглобулинов. Вместе с тем есть указания на наличие при ГМ явного IgМ- и скрытого IgA- и IgG-дефицита антителообразования. Другие исследователи выявили увеличение в крови больных ГМ количества IgA, IgМ, а также значительный рост концентрации IgG. При этом увеличение уровня иммуноглобулинов объясняют хелперным фенотипом опухолевого субстрата при ГМ. Таким образом, изменения показателей иммунного статуса у больных ГМ характеризуются значительной вариабельностью и отсутствием признаков, имеющих безусловное диагностическое значение.
В последние годы достигнут значительный прогресс в терапии ГМ, однако лечение больных с этим тяжелым, неуклонно прогрессирующим заболеванием представляет значительные сложности. Ситуация усложняется еще и тем, что не существует лабораторных критериев, позволяющих четко определить дозы, сроки или эффективные комбинации препаратов. Руководствуясь принципом интенсивной терапии опухолевых процессов, для лечения ГМ используют различные полихимиотерапевтические схемы: ЦОП — блео (циклофосфан, винкристин, преднизолон, блеомицин), ЦХОП (циклофосфан, винкристин, доксорубицин, преднизолон), МОПП (мехлорэтамин, винкристин, прокарбазин, преднизолон). Противоопухолевые средства, вошедшие в практику лечения ГМ, относятся к различным группам: антиметаболиты (метотрексат, метотрексат лахема, метотрексат-эбеве, меркаптопурин, пури-нетол), замедляющие нуклеиновый обмен и рост активно пролиферирующих тканей; алкилирующие агенты (циклофосфан, циклофосфамид-тева, циклофосфан-ЛЭНС, тиофосфамид), действующие непосредственно на ДНК клетки; вещества растительного происхождения (винкристин, винкристин ликвид-рихтер, винбластин, винбластин-рихтер), блокирующие деление клеток на стадии метафазы; синтетические противоопухолевые антибиотики (спиробромин, проспидин); противоопухолевые антибиотики (адриамицин, блеомицин, брунеомицин).
Препараты назначались в общепринятых для лечения онкологических заболеваний дозировках и режимах введения. Однако различные осложнения (чаще всего угнетение костно-мозгового кроветворения), а также недостаточная эффективность явились основанием для исключения из практики ряда цитостатических препаратов.
Высокой терапевтической эффективностью в сочетании с небольшими дозами кортикостероидов при лечении ГМ обладает проспидин. Существенным достоинством проспидинотерапии, отличающим ее от лечения другими химиопрепаратами, является отсутствие серьезных побочных эффектов. Это связано с тем, что основной мишенью действия проспидина являются не ДНК клеток, а их мембраны. Однако длительное применение препарата приводит к привыканию, в связи с чем эффективность терапии заметно снижается.
Для лечения больных ГМ широко используется ПУВА-терапия, основанная на применении фотосенсибилизаторов в комбинации с УФ-облучением в области А [7, 11]. Учитывая тот факт, что зона воздействия УФА-света находится в пределах эпидермиса и верхней трети дермы, целесообразно применение данного метода в доопухолевых стадиях заболевания. В опухолевой стадии ГМ обычно используют сочетание УФ-облучения с полихимиотерапией или рентгеновским облучением. Для лечения больных ГМ применяется также электронно-лучевая терапия, основанная на облучении быстрыми электронами. Данная методика позволяет воздействовать на опухолевый субстрат в глубоких отделах кожи, что значительно повышает эффективность лечебных мероприятий при ГМ. На ранних стадиях ГМ часто используются ретиноиды (изотретиноин, этретинат, тигазон), действие которых направлено на процессы созревания Т-хелперов [12].
В последние годы большое внимание уделяется разработке иммунокоррегирующих методов лечения ГМ. Иммуномодулирующее воздействие гемосорбции, плазмафереза, лейкофереза, фотофореза при ГМ позволяет сократить разовые и курсовые дозы цитостатиков, что в определенной степени способствует снижению частоты побочных эффектов химиотерапии. Мы изучали влияние тимодепрессина на состояние иммунного статуса у 12 больных ТМ. Препарат вводился ежедневно всем по 2 мл в течение 3 семидневных курсов лечения с недельным перерывом. Изучение иммунного статуса больных ГМ показало, что тимодепрессин сдерживает развитие пула атипичных Т-лимфоцитов, устраняя воспалительные и пролиферативные изменения в эпидермодермальном пространстве пораженных участков кожи. После окончания терапии состояние клинической ремиссии было достигнуто у 5 больных, значительное клиническое улучшение — у 6 пациентов, в течение года состояние клинической ремиссии сохранялось у 4 больных, еще у 4 больных возникли рецидивы ГМ спустя 3–6 мес после лечения. Повторное назначение тимодепрессина во всех случаях позволило купировать патологический процесс.
В терапевтические схемы лечения ГМ нередко включаются гормоны тимуса: Т-активин, тимопоэтин, тимозин, тималин, тимоген и др. Применяется также леакадин, обладающий противоопухолевым и иммуномодулирующим действием. Широко используются при лечении ГМ интерфероны [8, 14]. Они обладают выраженной противоопухолевой активностью, обусловленной не только прямым цитостатическим действием на опухолевые клетки, но и модуляцией механизмов гуморальной регуляции иммунного ответа. Установлено, что препараты данной группы (α-интерферон — виферон, реальдирон, вэллферон; β-интерферон — ребиф 22, бетаферон, лейкинферон; γ-интерферон — имукин) активируют макрофагальную и комплементарную системы организма, нормализуют продукцию провоспалительных цитокинов, воздействуют на экспрессию генов и антигенов главного комплекса гистосовместимости.
Сравнительный анализ терапевтических возможностей различных методов лечения ГМ позволил американской медицинской ассоциации рекомендовать следующую тактику ведения больных ГМ. На ранних стадиях лимфопролиферативного процесса показаны наружное применение кортикостероидов (локоид, полькортолон, фторокорт, целестодерм-в, флуцинар, элоком, адвантан, кутивейт, дермовейт), ПУВА-терапия, локально наносимые цитостатики, радиотерапия быстрыми электронами и мягколучевая рентгенотерапия. При прогрессировании ГМ используется системная терапия в виде комбинации ПУВА-терапии с ретиноидами или рекомбинантным α-интерфероном. При эритродермической форме ГМ рекомендован экстракорпоральный фотофорез в сочетании с α-интерфероном или ретиноидами. Таким образом, анализ литературного материала убедительно показал целесообразность дальнейшего изучения биологической сущности ГМ и разработки более эффективных схем его лечения.
- Гостева И. В. Фотофорез в комплексной терапии Т-клеточных злокачественных лимфом кожи: Автореф. дис. . канд. мед. наук. — 1995. — С. 22.
- Вавилов А. М., Лезвинская Е. М. Иммунокомпетентные структуры кожи и их роль в развитии первичных кожных лимфом//Архив патологии. 1996. — № 6. — С. 7–2.
- Ершов В. И., Бочкарникова О. В., Соколова И. Я. Кожные лимфомы//Актуальные вопросы внутренней медицины и педагогики: Сб. науч. тр. — 2000. — C. 232–240.
- Ламоткин И. А. Типы клинического течения грибовидного микоза// Междунар. мед. журн. — 2001. — № 5. — С. 427–428.
- Кутасевич Я. Ф. Особенности патогенеза, методы ранней диагностики и рациональной терапии грибовидного микоза: Автореф. дис. . докт. мед. наук, 1989. — С. 33.
- Трофимова И. Б. Т-клеточные злокачественные лимфомы кожи: иммунофенотипические особенности и терапия// Автореф. дис. . докт. мед. наук, 1994. — С. 34.
- Самсонов В. А., Вавилов А. М., Васина Н. И. Эффективность фотохимиотерапии в сочетании с лейкинфероном на различных стадиях Т-клеточных злокачественных лимфом кожи: Сб. науч. тр. — Астрахань, 1998. — С. 117–118.
- Самсонов В. А., Чистякова И. А., Аверина Л. В. Гаммаферон в терапии больных грибовидным микозом// Вестник дерматологии и венерологии, 1995. — № 5. — С. 4 — 6.
- Хасан Хамад А., Попова О. Н., Силуянова С. Н., Белушкина Н. Н. Исследование апоптоза лимфоцитов периферической крови больных с Т-клеточной лимфомой кожи и ангиитами кожи// Вопр. биол. мед. и фармац. химии. — 2000. —№ 4. — С. 22 — 25.
- Чиарион В., Бонони А., Форнаса К. Вторая фаза исследования применения интерферона-альфа с ПУВА-терапией у больных Т-клеточной лимфомой кожи// Журнал клинической онкологии. — 2002. — № 15. — С. 2876 — 2880.
- Carretero C. D., Fivenson D. P. A complement and durable response to denileukin diftitoх in a patient with micosis fungoides. J. Acadam Dermatol., 2003; 48, 275 — 276.
- Eichmuller S., Usener D. Tumor-specific antigens in cutaneous T-cell lymphoma. Int. J. Cancer. — 2003; 104. Р. 482 — 487.
- Kim Y., Martines G. Topical nitrogen mutard in management of micosis fungoides. Arch.Dermatol. — 2003; 139. Р. 165 — 173.
- Ferenczi K. Increased CCR4 expression in cutaneous T cell lymphoma. J. Invest Dermatol. 2002; 119; 1405 — 1410.
- Mucher J. Vaccination therapy for cutaneous T-cell lymphoma. Clin Exp. Dermatol. 2002; 27; 602 — 607.
- Rook A., Wysocka M. Citokines and other biologic agents as immunotherapeutics for cutaneous T-cell lymphoma. Adv. Dermatol. 2002; 18; 29 — 43.
Н. Г. Короткий, доктор медицинских наук, профессор
М. В. Уджуху
РГМУ, Москва
Читайте также: