Диагностика паразитарных заболеваний у животных
Основой диагностики паразитарных болезней, в частности гельминтозов, являются результаты лабораторных исследований, которые выявляют непосредственно возбудителей, их антигены или антитела к ним.
Гельминтозы развиваются в результате инвазии (заражения) организма окончательного хозяина (человека или животного), используемого как место обитания гельминтов и источника их питания. Часто болезни протекают без выраженных специфических клинических симптомов, что не всегда позволяет поставить диагноз по клинической картине.
Диагностика гельминтозов должна быть комплексной и основываться на данных эпидемиологического анамнеза, клиники заболевания и лабораторных исследований.
Специфика биологии каждого конкретного вида гельминта диктует необходимость различной тактики лабораторных исследований, которая направлена на обнаружение в одних случаях гельминтов или их фрагментов, а в других – их личинок, яиц или специфических иммуноглобулинов.
Материал для исследования берется в зависимости от подозрения на наличие у больного того или иного гельминтоза, так как пути выделения яиц, личинок или фрагментов паразитов из организма человека могут быть разными.
Для геогельминтов характерен кишечный (интестинальный) путь выделения яиц и личинок из организма больного человека. Большинство гельминтов, яйца которых выводятся через кишечник, паразитируют в пищеводе, желудке, кишечнике, а также попадают в кишечник при миграции через легкие, бронхи, трахеи, гортань, когда происходит заглатывание яиц и личинок со слизью при кашле. Этот путь присущ трематодам, цестодам и многим нематодам (в частности, геогельминтам). Материалом для исследования служат фекалии (кал). При исследовании проб фекалий обнаруживаются яйца и личинки многих гельминтов.
Паразитологические методы лабораторных исследований применяются:
- с диагностической целью;
- для контроля эффективности лечения;
- для оценки качества проведенного комплекса лечебно-профилактических мероприятий;
- для установления уровня пораженности населения (при профосмотрах)
Лабораторная диагностика является важным методом при паразитарных заболеваниях. В то же время качество лабораторной диагностики зависит от множества факторов, таких как надлежащая подготовка пациента к лабораторному обследованию, правильный забор материала для исследования и выбор оптимальной методики, квалификация и опыт специалиста-лаборанта.
Для верификации диагноза важно обеспечить следующее:
- сбор данных эпидемиологического анамнеза;
- определение соответствующего материала для исследования, правильно собранного и доставленного вовремя;
- выбор и применение соответствующего метода идентификации паразита;
- правильная идентификация паразита;
- правильная интерпретация результатов исследования.
Cбор материала для гельминтологических исследований включает следующие шаги:
- Для исследования собирают фекалии из любой чистой емкости немедленно после дефекации.
- Не допускается сбор образцов фекалий из унитаза.
- Для детей возможен сбор образца с пеленки, подгузника или горшка.
- Используя ложку в крышке контейнера, собрать не менее чем из трех точек стула.
- Испражнения для анализов должны доставляться в лабораторию не позднее одних суток после дефекации, а при подозрении на стронгилоидоз – немедленно.
- Если по каким-либо причинам доставка в лабораторию затруднена, то необходимо хранить материал при температуре +4–8 °C. Рекомендуется использование консерванта, и тогда исследование можно проводить в течение 3–10 дней после дефекации.
Методы лабораторной диагностики гельминтозов
Методы гельминтологических исследований делятся на прямые и опосредованные (косвенные).
Прямые методы: выявление самих гельминтов, их фрагментов, яиц, личинок в фекалиях, моче, дуоденальном секрете, мокроте и др.
Опосредованные (косвенные) методы: выявление вторичных изменений, возникающих в организме человека в результате жизнедеятельности паразита, путем серологических реакций, общего исследования крови, мочи.
Основным методом лабораторной диагностики глистных инвазий является обнаружение яиц или личинок гельминтов в фекалиях. Наиболее распространенными методами исследования фекалий являются гельминтокопроскопические.
Гельминтокопроскопия – это совокупность методов взятия, обработки и исследования (макро- и микроскопического) проб фекалий человека с целью обнаружения в них яиц, личинок гельминтов, их фрагментов. Она включает следующие виды исследований:
- копроовоскопия (исследование фекалий на яйца гельминтов);
- копроларвоскопия (исследование фекалий на личинки гельминтов);
- макроскопия фекалий (обнаружение фрагментов или зрелых гельминтов в фекалиях).
Микроскопические методы подразделяются на простые, сложные и специальные.
К простым относятся метод нативного мазка и метод толстого мазка под целлофаном по Като – Кац.
Сложные методы, или методы обогащения, основаны на феномене разных удельных весов яиц гельминтов и применяемых реагентов. При обработке фекалий этими растворами происходит концентрация яиц на поверхности раствора или в осадке, в результате чего увеличивается эффективность поиска.
Различают следующие методы обогащения:
- флотационные (когда используют солевые растворы, удельный вес которых выше удельного веса яиц гельминтов, в результате чего они всплывают в поверхностную пленку, которую и исследуют);
- седиментационные (когда используют растворы, удельный вес которых меньше удельного веса яиц гельминтов, в результате чего они оседают, образуя осадок).
Методом седиментации возможно определить следующие гельминтозы: описторхоз, клонорхоз, фасциолез, дикроцелиоз, метагонимоз, нанофиетоз, дифиллоботриоз, гименолепидоз, аскаридоз, трихоцефалез, анкилостомидозы, стронгилоидоз, трихостронгилез, некатороз, шистосомоз, кишечные протозоозы (лямблиоз,криптоспоридиоз, изоспороз)
Специальные методы чаще всего необходимы для обнаружения личинок гельминтов. Группа специальных методов направлена на диагностику конкретного геогельминтоза, применяемый метод специфичен только для данного гельминта.
Модификация эфир-формалинового метода седиментации
одноразовыми системами для проведения копрологического исследования
С развитием паразитологии в лечебную практику стали применяться одноразовые системы для копрологического исследования, предназначенные для эффективного концентрирования яиц и личинок гельминтов модифицированным эфир-формалиновым методом.
Системы для копрологического исследования являются одноразовыми и состоят из нескольких элементов:
- пробирка для образца, в которую имеется готовая смесь для фиксации образца фекалий и последующей седиментации
- пробирка с системой фильтров и шпателем для забора образца;
- коническая емкость для сбора отфильтрованного материала.
Система фильтров способствует оседанию грубых частиц непереваренной пищи и клетчатки в смесительной камере, а жидкая часть с выделившимися в нее паразитами, яйцами паразитов под давлением фильтруется и центрифугируется в конической пробирке.
После получения взвеси систему помещают в центрифугу и центрифугируют при скорости 2500–3000 об/мин в течение 1–3 минут, при скорости 1500 об/мин – 5 минут. В конической части пробирки остается жидкая часть пробы с выделившимися в нее яйцами гельминтов, цистами простейших. Отсоединяют модуль с фильтром и утилизируют после обеззараживания. Коническая часть пробирки остается для микроскопирования. Для этого из нижней части пробирки с помощью пипетки переносят на предметное стекло 2 капли пробы осадка. Микроскопируют при увеличении: окуляр x10, объективы x10, x40.
Преимущества использования одноразовых систем для копрологических исследований:
- повышает выявляемость возбудителей;
- уменьшает расход реагентов;
- снижает опасность контаминации, исключая контакт персонала с исследуемыми образцами;
- улучшает стандартизацию метода, повышает достоверность анализа;
- исключает подготовку и повторную обработку посуды, а также сокращает количество отходов в процессе проведения исследования
Эктопаразиты
Эктопаразиты – все паразиты, живущие на поверхности тела животного, к ним относятся - иксодовые клещи, блохи, вши, власоеды, комары.
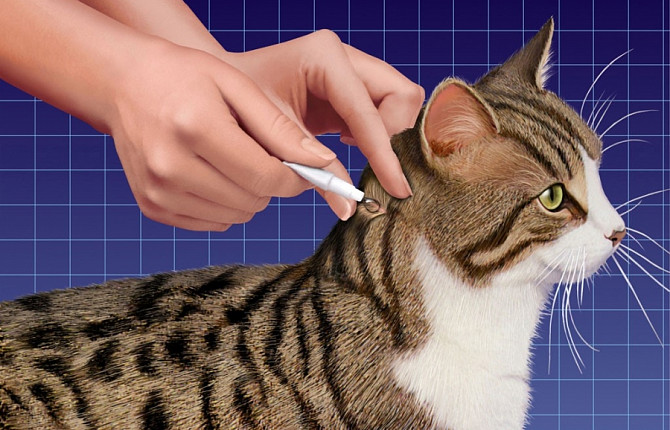
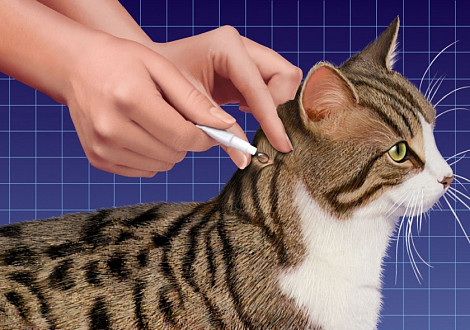
Иксодовые клещи – кровососущие паразиты, являющиеся переносчиками возбудителей кровопаразитарных заболеваний (в том числе болезнь Лайма и пироплазмоз у собак). Для борьбы с клещами имеется большое количество антипаразитарных препаратов в виде капель, спреев, ошейников и других средств наружного применения (Фронтлайн, Адвантикс, Стронхолд и др.).
Профилактика – обработка животных противопаразитарными препаратами, указанными выше. Дополнительно в качестве профилактики необходимо использовать средства защиты в виде комбинезонов, полностью защищающих животное. При дворовом содержании животных, можно обрабатывать садовый участок или двор инсектицидами - средствами от насекомых и вредителей (Интавир, Арриво, Цимбуш, Микрон и др.).
Вши и власоеды – кровососущие эктопаразиты переносят возбудителей заразных болезней, вызывающих дерматиты и зуд у животных.
Профилактикой является применение антипаразитарных препаратов, перечисленных выше, обработка животного растворами бутокса или энтомазана. При массовых поражениях в питомниках и хозяйствах возможно обтирание животных препаратами бутокс, ивамек, обработка помещений дезинсектицидами, проглаживание подстилок утюгом и т.д.
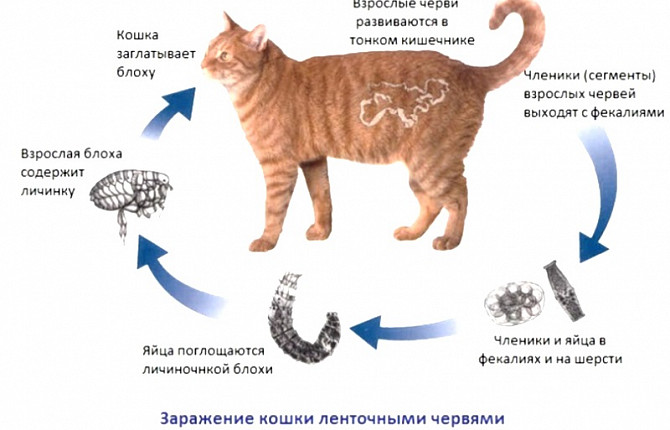
Блохи - долгосрочные кровососущие эктопаразиты, являются переносчиками различных заболеваний животных и человека. Они являются промежуточными хозяевами огуречного цепня (гельминта очень распространенного среди кошек). Вызывают атопический дерматит, зуд, сыпь, перхоть, выпадение шерсти у животных.
Профилактика - обработка животного инсектицидами (Фронтлайн, Адвантикс, Стронхолд и др.) в виде капель, спреев, ошейников.
На фотографии представлена собака дворового содержания, с внешним видом характерным для поражения эктопаразитами и глистной инвазией.
Эндопаразиты
Эндопаразиты – паразиты, обитающие во внутренних органах, в том числе и в клетках животного.
Они делятся на - внутриполостные, паразитирующие в просвете внутренних органов (гельминты, простейшие, патогенные бактерии); тканевые паразиты – поражающие мышечную, нервную, соединительную ткань и лимфу (гельминты, протозоозы); внутриклеточные - паразитирующие в клетках организма (пироплазма, протозоозы).
В подавляющем большинстве переносчиками эндопаразитов (гельминтозов, пироплазмоза, дирофиляриоза) являются эктопаразиты (клещи, блохи и др.).
Поэтому профилактикой борьбы с ними является дегельминтизация и обработка животных от эктопаразитов (блох, комаров, клещей, гельминтов и т.д.). Следует отметить, что, если в нашей стране обязательная дегельминтизация кошек и собак проводится ежегодно перед вакцинацией, то в Европейских странах эта процедура обязательна каждые 2-3 месяца (с непременной отметкой в ветеринарном паспорте животного).
Простейшие
Другой группой паразитов, с которыми ведется борьба и профилактика, являются простейшие, заболевания, которые они вызывают, называются протозоозы. К ним относятся токсоплазмоз, пироплазмоз, изоспороз.
Простейшие паразитируют в крови, пищеварительном тракте, головном мозгу, ретикулоэндотелиальной системе, мускулатуре и других органах, наиболее опасной для человека является токсоплазмоз.
Профилактикой заболеваний являются санитарно-гигиенические мероприятия – содержание животных в чистых помещениях кормление только вареным мясом и продуктами.
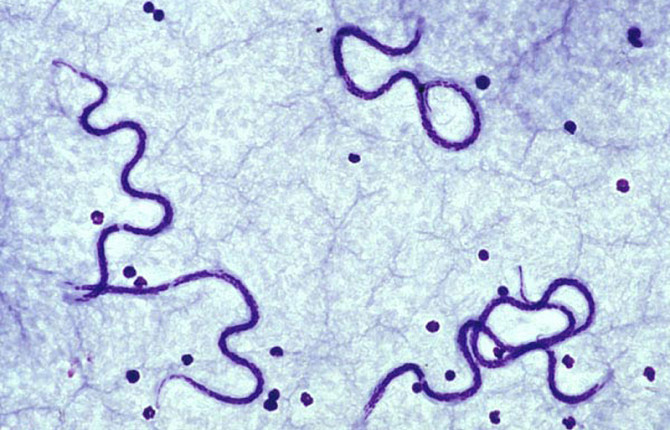
Пироплазмоз - поражает только животных семейства песьих (лисы, еноты). Заболевание тяжелое, может заканчиваться летальным исходом. Диагноз ставится на основании изучения мазка животного, при заболевании выявляются бабезии (пироплазмы) паразитирующие в эритроцитах.
Профилактика – для борьбы с иксодовыми клещами, применяют противопаразитарные препараты в виде капель на холку, спреев, суспензий, ошейников (Фронтлайн, Адвантикс, Стронхолд, Болфо др.). Обработка проводится с наступлением таяния снега в средней полосе России до первых заморозков. Использование препаратов необходимо повторять через 1-1,5 месяца, строго соблюдая дозировку и инструкцию по применению. В последние годы для профилактики пироплазмоза предлагают вакцину, однако, она не дает абсолютной гарантии от возникновения заболевания. По нашему опыту эффективность ее применения составляет около 60%.
Изоспороз - протозойное заболевание, характеризующееся паразитированием изоспор в тонком кишечнике. При тяжелом течении и поздней диагностике может быть летальный исход. Диагноз ставится на основе исследования ретикулоэндотелия и фекалий.
Профилактика – соблюдение санитарно-гигиенических мер содержания животного.
Токсоплазмоз – протозойное заболевание человека и животного. При этом заболевании поражается ретикулоэндотелиальная система, поэтому токсоплазмы могут паразитировать в головном мозге, скелетной мускулатуре и органах желудочно-кишечного тракта человека и животного и любых других органах и системах. Заболевание очень часто протекает бессимптомно или под маской других болезней.
Заражение токсоплазмозом происходит, как правило, от кошек. Очень редко от других животных (при употреблении в пищу не прожаренного мяса, сырых яиц). А также через кровососущих насекомых или через ранки на коже или акне, через укусы больных животных (мышей). Бывают случаи внутриутробного заражения (при заражении во время беременности), что приводит к формированию уродств у плода. Поэтому особенно опасен токсоплазмоз для беременных женщин. В случаях беременности женщин в доме, где проживают кошки обязательно необходимо проводить их проверку на токсоплазмоз, независимо от отсутствия у них клинических проявлений заболевания.
Клинические проявления токсоплазмоза выражены не всегда, так как при попадании в организм небольшого количества токсоплазм они защищают себя и превращаются в цисты и не представляют опасность для человека. В ином случае развиваются нарушения зрения, судороги и т.д.
Механизм заболевания токсоплазмозом кошки и человека. У токсоплазмы есть два вида размножения – половое и бесполое.
Токсоплазмозом болеют различные виды животных, однако только в тонком кишечнике кошки токсоплазмы находят благоприятные условия для активного полового размножения. Промежуточным хозяином токсоплазмы являются мыши, в организме которых и происходит бесполое размножение токсоплазмы. При заражении мышка становится очень активной и бесстрашной и попадает в лапы кошки, кошка съедает мышку и токсоплазма достигает намеченной цели – тонкого кишечника, где она активно размножается и заражает человека и других животных.
Далее, при тесном контакте кошки и человека (спит в одной постели, ест со стола и пр.) от кошки заражаются люди и животные.
Диагноз ставится при лабораторном исследовании крови. Методом ПЦР – определяют наличие возбудителя (токсоплазмы). Методом иммуноферментного анализа (ИФА) – определяют наличие антител. Если при ИФА в крови выявляют иммуноглобулины IgM, то считают, что заражение произошло недавно, т.к. эти иммуноглобулины нестойкие и со временем разрушаются. Вместо них появляются иммуноглобулины IgG, которые сохраняются пожизненно. Появление иммуноглобулинов IgM или впервые выявленные иммуноглобулины IgG свидетельствуют о заболевании.
Профилактика заключается в соблюдении санитарно-эпидемического режима - нельзя употреблять в пищу сырого мяса и не допускать близкого контакта с больными животными.
По всем вопросам, связанным с лечением и профилактикой паразитарных заболеваний животных, вы можете обратиться к специалистам московской ветеринарной клиники СанаВет. Схема проезда.
Телефоны администратора: +7 (495) 784-43-43, +7 (495) 437-54-54 (ежедневно, круглосуточно).
Телефон выездной службы: + 7 (925) 658-20-11 (ежедневно, круглосуточно).
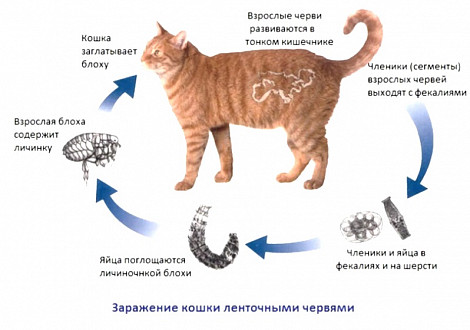
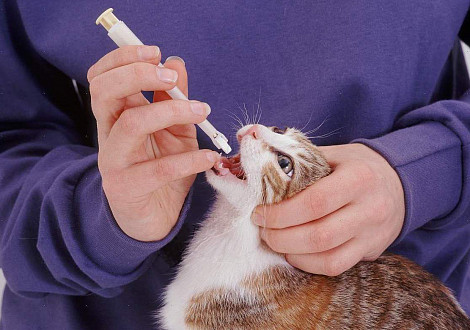
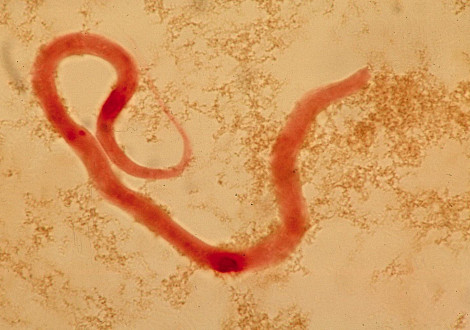
Инвазионными называют паразитарные заболевания собак и кошек, которые вызываются гельминтами, простейшими, насекомыми и т.д.
Заражение происходит, как правило, орально с инфицированными каловыми массами, при контакте с инвазированными животными, предметами ухода, подстилками, а также внутриутробно от матери к плоду и при выкармливании молодняка молоком.
К источникам паразитарной инвазии у собак и кошек относят больных животных, почву, воду, предметы ухода за питомцами.
Многие насекомые могут выступать в качестве переносчиков гельминтов и простейших.
Клиническая картина заражения может быть разнообразна и зависит от возраста животного, количества паразитов и размера самого питомца. Как правило, у взрослых кошек и собак глистная инвазия проходит без ярко выраженных симптомов. Наиболее опасно паразитирование у маленьких котят и щенят.
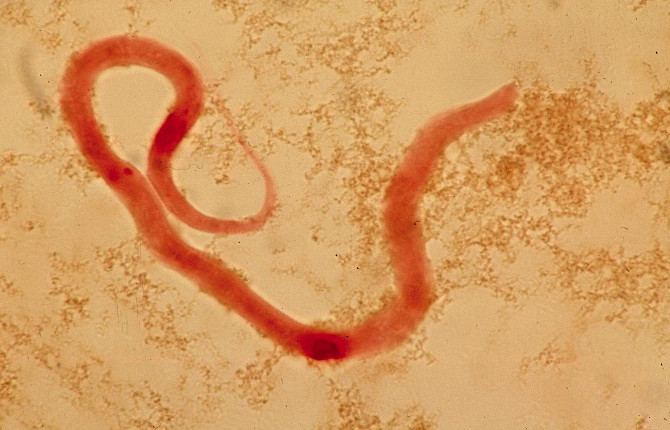
Самым очевидным признаком нахождения гельминтов в организме питомца, безусловно, является их обнаружение в фекалиях. Это говорит о высокой степени инвазии.
Чаще всего паразитарная инвазия у кошек и собак проявляется следующими признаками:
• Неоформленная консистенция стула;
• Возможно нахождение мертвых гельминтов в кале;
• Слизь и/или примесь крови в кале;
• Вздутие живота;
• Зуд в области анального отверстия;
• Отставание в росте, неполноценная усвояемость питательных веществ, недостаток витаминов (особенно группы В) у котят/щенков;
• При ряде патологий гельминты могут способствовать развитию анемии;
• Для прохождения паразитом цикла своего развития часто гельминты совершают ряд метаморфоз в организме животного. Они могут мигрировать по органам и тканям, вызывая нарушение их работы;
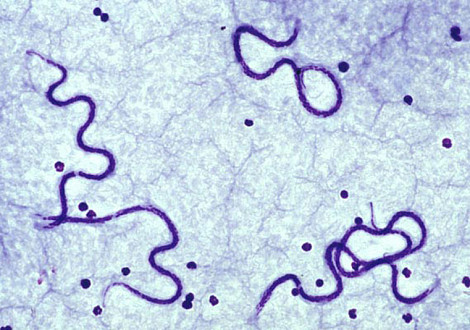
• Отдельно можно отметить один из видов паразитов, например, дирофилярии, которые обитают в камерах сердца, нарушая его работу и способствуя развитию у животного сердечной недостаточности.
Зачастую инвазия может осложнять течение и терапию многих инфекционных и неинфекционных патологий, поэтому своевременная обработка собак и кошек от эндопаразитов является для каждого владельца обязательным пунктом для выполнения.
Вид диагностики определяется в зависимости от подозреваемой паразитарной инвазии. Некоторые виды гельминтов и простейших можно обнаружить при микроскопическом исследовании кала. Данные паразиты имеют свой цикл развития и выделяются не с каждой порцией фекалий, поэтому данный метод не всегда достоверен для утверждения отсутствия паразитов.
Имеются специфические анализы для определенных видов паразитов. Например, экспресс-тесты, выявление гена паразита в материале, но, к сожалению, количество данных анализов крайне мало.
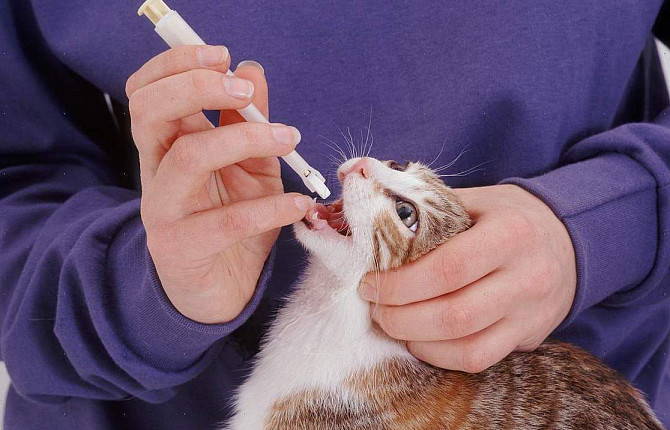
Если речь идет о заражении питомца гельминтами, то в лечебной порядке проводят минимум 2–3 обработки от паразитов с интервалом в 2 недели специальными препаратами широкого спектра действия.
Если речь идет о возможном нахождении простейших микроорганизмов, то необходимо сдать анализ кала для общего исследования и обнаружения цист простейших. Важно понимать, что как яйца гельминтов, так и простейшие микроорганизмы выделяются не с каждой порцией кала. Зачастую необходимо сделать до 3 и более исследований. На основании полученных после исследования кала данных подбирается специфическое лечение.
В идеале контроль лечения осуществляется повторной сдачей анализа кала до получения отрицательного результата по яйцам гельминтов и простейшим и хорошего общего анализа кала, по результатам которого врач сможет понять о степени переваривания корма, его усвояемости, наличии или отсутствии скрытой крови и т.д.
Профилактика заключается в систематической дегельминтизации питомца.
Собак, подбирающих предметы на улицы или поедающих чужие фекалии, следует выгуливать в наморднике.
Питомцев, гуляющих на улице (выезжающих на дачу), питающихся кормами домашнего производства (натуральная диета), следует дегельминтизировать четыре раза в год (каждый квартал). Одна из обработок производится перед вакцинацией питомца.
Питомцев, не выходящих за пределы квартиры и питающихся кормам промышленного производства, следует дегельминтизировать минимум 2 раза в год. Одна из обработок проводится перед вакцинацией.
Важно помнить, что если дома проживает несколько домашних животных (кошки и/или собаки), обработку проходят одновременно все питомцы, а также их владельцы, поскольку многие паразитические организмы могут использовать как животных, так и человека, как среду своего обитания.
Проводить дегельминтизацию можно только клинически здоровым животным и в соответствии с рекомендациями по весу и возрасту. Если у собаки/кошки имеются гельминты, после приема препарата они в процессе гибели выделяют токсины и продукты своей жизнедеятельности, что может усугубить уже имеющиеся симптомы инвазии, поэтому в день приема противогельминтного препарата рекомендуется дать питомцу какой-либо сорбент (например, энтеросгель).
Своевременная и точная диагностика является той основой, на которой зиждется эффективная система терапии и профилактики паразитарных болезней животных. Основными методами диагностики в ветеринарной паразитологии являются лабораторные методы исследований, многие из которых предполагают обнаружение и дифференциацию возбудителя болезни, изучение его свойств и чувствительности к тем или иным препаратам.
Существуют прижизненные и посмертные методы диагностики паразитозов.
При различных паразитарных болезнях применяют разные методы диагностики, основанные на современных научных достижениях и накопленном опыте практических специалистов. Определение возбудителя может проводиться или прямым путем (при осмотре животных, путем микроскопирования мазков крови, просмотра под микроскопом проб фекалий, соскобов с кожи и т. д.), или косвенным путем (при аллергической диагностике с известным антигеном и др.). При всех известных способах диагностики паразитарных болезней ставится совершенно определенная цель — установить возбудителя и определить степень пораженности им животного.
В настоящее время при постановке диагноза на паразитозы важным является выяснить не только экстенс-, но и интенсинвазированность животных паразитами. Не менее важным является также определение состава паразитоценоза, в том числе гельминтов, клещей, насекомых, простейших и других организмов.
Известно, что человек, животные и окружающая их среда экологически взаимосвязаны. Поэтому происходит циркуляция возбудителей паразитарных болезней в природе и обществе. Вот почему важным является изучение зараженности паразитами человека и животных (особенно зоонозами), распространения возбудителей этих болезней в окружающей среде.
В условиях индустриализации и урбанизации нашей планеты важно изучить закономерности распространения паразитозов, выяснить пути сохранения организмов в постоянно меняющихся условиях среды.
Все это определяет методологические подходы к диагностике паразитарных болезней, в связи с чем, в последнее время все больше внимания уделяется применению современных методов и средств диагностики: электронной микроскопии, внедрению иммуноферментных методов исследований, использованию радиодиагностических наборов и др.
ДИАГНОСТИКА ПРОТОЗООЗОВ ЖИВОТНЫХ
Перед обследованием животных с целью обнаружения в их организме патогенных простейших необходимо провести работы по подготовке материалов.
Для этой цели готовят предметные и покровные стекла. Лучше использовать новые, не бывшие в употреблении, которые тщательно моют в теплой воде с мылом. После этого их промывают чистой водой, насухо вытирают и помещают в банку с притертой пробкой, в которую перед этим наливают абсолютный спирт или смесь равных объемов спирта и эфира (смесь Никифорова). Перед употреблением стекла насухо вытирают чистой салфеткой.
В полевых условиях для обезжиривания предметных стекол применяют следующий способ. Сначала их протирают чистой салфеткой и после этого хорошо покрывают хозяйственным мылом. Затем стекла повторно протирают сухой чистой салфеткой или полотенцем до полного удаления мыла.
Взятие крови у животных. Пробы крови у животных берут в тех случаях, когда необходимо заразить ею подопытных животных, для серологического исследования или для приготовления препаратов.
Для биопробы или серологических исследований кровь у крупного рогатого скота, лошадей и мелких жвачных берут из яремной вены, у птиц — из подкрыльцовой вены. Для обнаружения простейших кровь у млекопитающих берут из сосудов кончика уха, у птиц — из гребня или подкрыльцовой вены.
Приготовление мазков крови и пунктата органов. На чистое предметное стекло наносят первую каплю крови, взятой у животного (в ней находится больше паразитов) и специально отшлифованным стеклом делают мазок. Во избежание загрязнения пылевыми частицами воздуха предметное стекло поворачивают сразу же мазком книзу. Через 10—15 с инъекционной иглой или карандашом ставят на предметном стекле номер или кличку животного и дату приготовления препарата. После этого мазок просушивают 10—12 мин.
Если препараты готовятся в зимнее время, предметные стекла перед нанесением на них капли крови следует подогревать до температуры 20—25 °С.
Для приготовления препарата толстой капли кровь наносят на предметное стекло, размазывают круговым движением толстым круглым слоем и помещают в термостат на 5—10 мин для высыхания. После этого на препарат наносят несколько капель дистиллированной воды (для гемолиза эритроцитов), осторожно сливают ее после того как препарат станет прозрачным. Препарат подсушивают и красят. Для фиксации мазков крови применяют различные химические вещества, среди которых — метиловый спирт, этиловый спирт, денатурированный спирт, реже применяют смесь Никифорова и др.
Для этой же цели можно применять и жидкость Завесина и Белокура (1950). Для ее получения необходимо на физиологическом растворе (рН 6,8—7,0) приготовить 4%-ный раствор чистой карболовой кислоты. Готовый раствор фильтруют и хранят в темном месте в течение 10—15 дней в банке из темного стекла с притертой пробкой. Длительность фиксации мазков крови — 5с. Мазок вынимают из фиксирующей жидкости пинцетом, ставят вертикально на полоску фильтровальной бумаги на 8—10 мин для сушки и потом окрашивают.
Окраска простейших. Осуществляется различными методами, однако наиболее приемлемыми являются следующие:
Окраска мазков крови и пунктатов из органов по Романовскому-Гимза. Поступающие в ветеринарные лаборатории основные растворы краски Романовского-Гимза не всегда бывают одинаковыми по своим красящим свойствам. Поэтому необходимо предварительно подбирать наилучшие сочетания количества вещества и сроков окрашивания при определенном объеме и рН воды.
Обычно для окрашивания препаратов основной раствор краски разбавляют из расчета 1 капля на 1 мл воды. Но иногда на 1 мл воды приходится расходовать 2—3 капли краски, но не более, так как в более концентрированных растворах она выпадает в осадок. Рабочий раствор готовится перед употреблением. Для получения хорошего качества рабочего раствора краски маточный раствор необходимо разводить дистиллированной водой (рН 7,0-7,2). В крайнем случае можно использовать прокипяченную профильтрованную проточную воду указанной реакции. Для разведения краски необходимо пользоваться одной и той же чистой посудой из стекла нейтральной реакции. При приготовлении рабочего раствора в сосуд с водой необходимо вносить по каплям требуемое количество краски и постоянно слегка помешивать, так как большое количество маточного раствора и грубое встряхивание могут привести к выпадению осадка. Маточный раствор краски хранят в темном сухом месте с постоянной температурой (20—22 °С). Если красящая способность раствора снизилась, ее необходимо подогреть в водяной бане до 60 °С в течение 15 мин.
Для окрашивания препаратов их помещают на дно чашки Петри мазком вниз на тонкие плоские стекла, чтобы расстояние между дном чашки и предметным стеклом составляло 0,3—0,5 см. После этого под предметные стекла осторожно подслаивают свежеприготовленную краску. Продолжительность окраски может быть от 15—20 мин до часа, но в среднем 30—40 мин. Свежие препараты окрашиваются быстрее и лучше. Нефиксированные мазки крови можно сохранять не более 1—2 недель, так как через месяц они теряют способность окрашиваться. Фиксированные препараты (мазки крови, пунктаты органов и т. д.) можно сохранять до окраски 1—2 мес. Перед применением краску нужно подогреть в термостате до 37 °С. После окраски мазки крови промывают дистиллированной водой и ставят в вертикальном положении на полоски фильтровальной бумаги. Хорошо промытое предметное стекло с мазком крови не должно оставлять на фильтровальной бумаге следов краски.
При хорошей окраске препараты имеют розово-фиолетовый цвет, эритроциты в тонких мазках крови окрашиваются в красный или розовый цвет, протоплазма паразитов и лейкоциты — в синий, ядра простейших и зернистость эозинофилов — в красный, а ядра лейкоцитов — в фиолетовый цвет. В перекрашенных мазках крови эритроциты имеют синий цвет и в них трудно различать паразитов.
Если мазки крови перекрашены, их погружают на 1—2 с в 80°-ный этиловый спирт, слегка подкисленный уксусной кислотой, или в подкисленную дистиллированную воду (на 100 мл спирта или воды добавляют 2 капли ледяной уксусной кислоты). После того как предметные стекла с мазками вынут из подкисленной воды или спирта, их немедленно промывают дистиллированной водой, высушивают и микроскопируют или оставляют на хранение.
Ускоренная окраска мазков крови по Романовскому-Гимза. Нефиксированный мазок помещают в чашку Петри и подслаивают смесь из неразведенной краски Романовского-Гимза и ацетона в равных количествах. Через минуту в чашку Петри в расчете на каждый миллилитр смеси краски и ацетона добавляют 10 мл дистиллированной воды и смешивают их легким покачиванием чашки. Через 10 мин мазок промывают водой, сушат и микроскопируют.
Окраска мазков крови по Филипсону. Одну часть рабочего раствора краски Романовского-Гимза смешивают с тремя частями этилового спирта и 1 мл приготовленной смеси наносят на нефиксированный мазок крови. Через 1—1,5 мин к краске добавляют 1 мл дистиллированной воды, перемешивают и оставляют на 30 мин для окрашивания. После этого краску смывают водой, мазок просушивают и микроскопируют.
Окраска мазков крови по Мансону. Берут 5 г буры и 2 г метиленового синего и растворяют их в дистиллированной воде (80 °С), выдерживают 2 ч в кипящей водяной бане, охлаждают и фильтруют. После этого для созревания помещают в термостат при температуре 37 °С. Для приготовления рабочего раствора берут каплю краски на 3—4 мл воды. Окраску мазков крови проводят в течение 1 мин. Затем препарат высушивают и микроскопируют. Окрашенный препарат имеет матово-зеленый цвет, эритроциты окрашиваются в светло- или сине-зеленый цвет, ядра лейкоцитов — в темно-синий, протоплазма — в светло-зеленый цвет. Паразиты имеют темно-синее ядро и светло-синюю протоплазму.
Окраска мазков крови по Ш. Д. Мошковскому. Готовят основной раствор метиленовой сини: на 100 мл дистиллированной воды берут 1 г метиленовой сини и 2,5 г буры. Раствор кипятят, охлаждают и фильтруют. Фиксированный мазок крови помещают на 10—20 с в разбавленный дистиллированной водой (1 : 10) основной раствор метиленовой сини. После этого мазок промывают водой, затем погружают на 5 с в 8—10%-ный раствор танина, повторно промывают, подсушивают и микроскопируют.
Окраска мазков крови по Нохту. Готовят растворы: азур II разводят дистиллированной водой в соотношении 1 :1000, аналогично готовят раствор эозина ВА. Краски хранят в склянках из оранжевого стекла в темном сухом месте. Перед окраской готовят рабочие растворы. Для этого в 4 мл дистиллированной воды (рН 7,0) разводят 2 мл 0,1 %-ного раствора эозина и к 4 мл воды добавляют 2 мл 0,1 %-ного раствора азура. Краски смешивают. Мазки крови помещают в чашку Петри, подслаивают краску и выдерживают 30—40 мин. После этого мазки подсушивают и микроскопируют.
Окраска мазков крови по Шуренковой и Межанской. Вначале готовят раствор А. Для этого берут 1 г метиленового синего и растворяют в 75 мл кипяченой воды; 1,5 г марганцово-кислого калия также растворяют в 75 мл кипяченой воды. Оба раствора сливают в колбу (вследствие этого образуется осадок), помещают ее в водяную баню и выдерживают при 100°С 40 мин, считая с начала кипения воды. После этого дают раствору остынуть и фильтруют.
Затем готовят раствор Б. Для этого берут 1 часть раствора А и добавляют 2 части подкисленной кипяченой воды (ее готовят путем добавления на 200 мл дистиллированной воды 15 капель разведенной соляной кислоты). При этом получают раствор № 1. После растворения в 200 мл кипяченой воды 0,2 г эозина водорастворимого получают раствор № 2.
При скоростном способе окрашивания фиксированный мазок погружают на 15—20 с в раствор № 2, прополаскивают водой и на 45 с погружают в раствор № 1, повторно промывают водой, подсушивают мазок на фильтровальной бумаге и микроскопируют.
Для массовой окраски мазков применяют длительный способ. Фиксированный мазок помещают на 5—10 мин в краску Б, разведенную 1 : 10 дистиллированной водой. После этого мазки промывают водой и заливают на 15— 20 мин краской А, также разведенной 1 : 10 водой. Мазки повторно промывают водой, подсушивают и микроскопируют. Обычно хорошо окрашенный мазок имеет сиреневый цвет. Ядра лейкоцитов окрашиваются в фиолетовый цвет, протоплазма простейших — в голубой, а ядро — в вишнево-красный цвет. Если мазки перекрашены эозином и имеют ярко-красную окраску, их на несколько секунд погружают в раствор № 1, слишком синие мазки погружают на несколько секунд в раствор № 2.
Окраска трихомонад: а) метод Романовского. Мазки фиксируют метиловым спиртом в течение 10 мин. После этого их окрашивают 45 мин краской Романовского-Гимза, разведенной 1: 15 нейтральной или слабощелочной дистиллированной водой; б) метод Шуренковой и Межанской. Мазки фиксируют в течение 10 мин метиловым спиртом. После этого их окрашивают 2 мин в растворе № 2, а затем в течение 1 мин — в растворе А; в) метод Милорадовича. Вначале готовят раствор № 1. Для этого 1 г основного фуксина смешивают с 10 мл 95°-ного этилового спирта и ставят в термостат при температуре 37 °С на 48 ч. После растворения фуксина к нему добавляют 100 мл 5%-ного раствора карболовой кислоты, смешивают и фильтруют. Полученный раствор разводят 1 : 50 дистиллированной водой. Перед употреблением на каждый миллилитр рабочего раствора добавляют по капле насыщенного раствора танина.
Раствор № 2 получают путем смешивания равных объемов 1%-ного раствора ауранция и 0,5%-ного раствора эозина.
Оба раствора готовят на 2%-ной карболовой кислоте. После фиксации и ополаскивания мазка на него наносят раствор № 1. Через минуту его сливают и сразу же наносят раствор № 2. Через 20 с препарат прополаскивают водой, просушивают и микроскопируют.
Окраска толстых капель крови: а) метод Шуренковой и Межанской. При скоростном способе окраски препарат в течение 15—20 с несколько раз погружают в раствор А. После того как капля крови на предметном стекле окрасится из зеленого в прозрачно-голубой цвет, препарат промывают водой, погружают в раствор № 2 и сразу же ополаскивают, высушивают и микроскопируют.
Если проводят массовую окраску, тогда применяют длительный способ: на 10-15 мин заливают разведенной (1:10) водой краской А. Затем ее сливают, препарат промывают водой и покрывают на 1-2 мин краской № 2, также разведенной (1:10) водой. После этого препарат промывают водой, просушивают и микроскопируют;
б) метод Иоффе. Готовят краску: берут 4 мл 1%-ного раствора метиленовой сини, 1 мл 1%-ного раствора фуксина на 50%-ном этиловом спирте, сюда же добавляют 4 мл 1 %-ной уксусной кислоты и 40 мл дистиллированной воды.
На нефиксированный препарат наносят краску. Через 15 мин ее осторожно смывают водой, препарат подсушивают и микроскопируют. При этом методе окраски эритроциты растворяются.
Методы исследования патогенных простейших. Методы исследования простейших, изучение их морфологии и биологии, а также диагностика вызываемых ими болезней животных предполагают использование микроскопических, серологических, аллергических, культуральных и других исследований в ветеринарной протозоологии. В связи с тем, что все указанные методы исследований имеют свои достоинства и недостатки, только проведение комплексных исследований дает наиболее высокую эффективность при постановке диагноза на данное заболевание или следует провести дифференциальную диагностику.
Для эффективной диагностики эймериозов необходимо правильно отобрать материал для исследований. Так как для эймерий характерным является видовая специфичность возбудителя и они имеют свои определенные места обитания в организме, важным является исследование определенных органов при постановке диагноза на эймериоз.
Для обнаружения ооцист эймерий исследуют фекалии животных, для выявления неполовозрелых форм шизогонии и гаметогонии исследуют кусочки пораженных органов.
Прижизненная диагностика эймериозов. Прижизненная диагностика предполагает обнаружение в фекалиях больных животных ооцист эймерий. Их обнаруживают путем исследования фекалий животных методом нативного мазка или флотационными методами.
Метод нативного мазка состоит в том, что на чистое предметное стекло помещают около 0,5 г фекалий и тщательно размешивают стеклянной палочкой с небольшим количеством смеси воды и глицерина в равных частях. После этого крупные частицы фекалий снимают пинцетом или препаровальной иглой, а оставшуюся массу покрывают стеклом и микроскопируют.
Флотационные методы являются более эффективными, чем метод нативного мазка. Для диагностики эймериозов применяются методы Г. А. Котельникова и В. М. Хренова (1974) с использованием растворов аммиачной или натриевой селитры, методы Фюллеборна, Дарлинга и др.
Культивирование эймерий проводится с целью изучения спорогонии у них. Для этого берут пробу фекалий, помещают в чашки Петри и смешивают их с мелкоистолоченным древесным углем и с 5%-ным раствором двухромово-кислого калия с целью предохранения фекалий от плесени. Чашки Петри с фекалиями помещают в теплое место и периодически перемешивают для лучшей аэрации. При необходимости пробы фекалий микроскопируют для определения сроков развития эймерий.
Посмертная диагностика эймериозов. Для исследования берут содержимое кишечника, соскоб слизистой оболочки кишки в местах с наибольшим поражением, кусочки пораженных паренхиматозных органов. Из отобранного материала готовят препараты (раздавленные капли, нативные мазки) для исследования живых эймерий, а также мазки или кляч-препараты для окраски паразитов.
Для обнаружения живых эймерий на различных стадиях берут кусочек содержимого из эймериозного узелка, помещают на предметное стекло в каплю физиологического раствора в смеси с белком куриного яйца. Содержимое узелка препаровальными иглами расчленяют на мелкие части, покрывают покровным стеклом и микроскопируют. Мерозоиты и шизонты хорошо заметны в затемненном поле зрения. При этом учитывают, что внедрившиеся в эпителиальную клетку спорозоиты имеют округлую форму с ядром в центре, а более зрелые макрогаметы – зернистость, они овальной формы и покрыты однослойной оболочкой , на одном из полюсов которой находится микропиле (табл.3-7).
Таблица 3. Эймерии крупного рогатого скота (по И. И. Вершинину, 1982)
Читайте также:


