Аплазия-гипоплазия улиткового нерва и канала улиткового нерва - лучевая диагностика
Добавил пользователь Владимир З. Обновлено: 28.01.2026

Аномалии развития внутреннего уха и кохлеарная имплантация
В.Е. Кузовков, Ю.К. Янов, С.В. Левин
Санкт-Петербургский научно-исследовательский институт уха, горла, носа и речи
Кохлеарная имплантация (КИ) в настоящее время является общепризнанным в мировой практике и наиболее перспективным направлением реабилитации лиц, страдающих сенсоневральной тугоухостью высокой степени и глухотой, с последующей интеграцией их в среду слышащих. В современной литературе достаточно широко освещены вопросы классификации аномалий развития внутреннего уха, в том числе применительно к КИ, описаны хирургические методики проведения КИ при данной патологии. Мировой опыт КИ у лиц с аномалиями развития внутреннего уха насчитывает более 10 лет. В то же время в отечественной литературе отсутствуют работы по данной тематике.
В Санкт-Петербургском НИИ уха, горла, носа и речи впервые в России стала выполняться КИ у лиц, имеющих аномалии развития внутреннего уха. Трехлетний опыт подобных операций, наличие успешных результатов таких вмешательств, а также недостаточное количество литературы по данному вопросу, послужили причиной выполнения данной работы.
Классификация аномалий развития внутреннего уха. Современное состояние вопроса.
С появлением в конце 80-х - начале 90-х г.г. компьютерной томографии (КТ) высокого разрешения и магнитно-резонансной томографии (МРТ) данные методики стали широко применяться для диагностики наследственной тугоухости и глухоты, особенно при определении показаний к КИ. С помощью этих прогрессивных и высокоточных методик были выявлены новые аномалии, которые не укладывались в существовавшие классификации F. Siebenmann [5] и K. Terrahe [7]. В результате чего R.K. Jackler [1, 2] были предложена новая классификация, расширенная и модифицированная N. Marangos [4] и L. Sennaroglu [5]. Однако, следует отметить, что, в частности, МРТ в настоящее время выявляет настолько тонкие детали, что обнаруживаемые мальформации бывает трудно классифицировать [3, 4].
В своей классификации аномалий развития внутреннего уха, основанной на данных обычной рентгенографии и первых данных КТ, R.K. Jackler [1] принимал во внимание отдельное развитие преддверно-полукружной и преддверно-улитковой частей единой системы. Автор предположил, что различные типы аномалий появляются в результате задержки или нарушения развития на определенной стадии последнего. Таким образом, обнаруживаемые типы мальформаций соотносятся с временем нарушения. Позже автор рекомендовал относить комбинированные аномалии к категории А, и предположил связь таких аномалий с наличием расширенного водопровода преддверия (табл.1).
В классификации N. Marangos [3] включены неполное или аберрантное развитие лабиринта (табл. 2, пункт 5).
Таблица 2
Классификация аномалий развития внутреннего уха по N. Marangos
| Категория | Подгруппа |
| А = неполное эмбриональное развитие | 1. Полная аплазия внутреннего уха (аномалия Michel) 2. Общая полость (отоцист) 3. Аплазия/гипоплазия улитки (нормальный «задний» лабиринт) 4. Аплазия/гипоплазия «заднего лабиринта» (нормальная улитка) 5. Гипоплазия всего лабиринта 6. Дисплазия Mondini |
| В = аберрантное эмбриональное развитие | 1. Расширенный водопровод преддверия 2. Узкий внутренний слуховой проход (внутрикостный диаметр менее 2 мм) 3. Длинный поперечный гребень (crista transversa) 4. Внутренний слуховой проход, разделенный на 3 части 5. Неполное кохлеомеатальное разделение (внутреннего слухового прохода и улитки) |
| С = изолированные наследственные аномалии | Х-связанная тугоухость |
| D | Аномалии при наследственных синдромах |
Таким образом, описаны четыре категории (A-D) аномалий развития внутреннего уха. Расширенным водопровод преддверия автор считает, если межкостное расстояние в средней части превышает 2 мм, тогда как другие авторы приводят цифру в 1,5 мм.
L. Sennaroglu [4] дифференцирует 5 основных групп (табл. 3): аномалии развития улитки, преддверия, полукружных каналов, внутреннего слухового прохода и водопровода преддверия или улитки.
Основные группы и конфигурации кохлеовестибулярных аномалий по L. Sennaroglu
| Основные группы | Конфигурация |
| Кохлеарные аномалии | Аномалия Michel / аплазия улитки / общая полость / неполное разделение тип I / гипоплазия улитки / неполное разделение тип II / нормальная улитка |
| Вестибулярные аномалии | Преддверие: отсутствие / гипоплазия / расширение (включая аномалию Michel и общую полость) |
| Аномалии полукружных каналов | Отсутствие / гипоплазия / увеличенные размеры |
| Аномалии внутреннего слухового прохода | Отсутствие / узкий / расширенный |
| Аномалии водопроводов преддверия и улитки | Расширенный / нормальный |
Кохлеарные мальформации (табл. 4) были разделены автором по степени выраженности на шесть категорий в зависимости от времени нарушения нормального хода эмбрионального развития. Эта классификация аномалий развития улитки включает неполное разделение I и II типов.
Таблица 4
Классификация аномалий улитки по времени нарушения внутриутробного развития по L. Sennaroglu
| Кохлеарные мальформации | Описание |
| Аномалия Michel (3-я неделя) | Полное отсутствие кохлеовестибулярных структур, часто - апластичный внутренний слуховой проход, чаще всего - нормальный водопровод преддверия |
| Аплазия улитки (конец 3-ей недели) | Улитка отсутствует, нормальное, расширенное или гипопластическое преддверие, и система полукружных каналов, часто - расширенный внутренний слуховой проход, чаще всего - нормальный водопровод преддверия |
| Общая полость (4-ая неделя) | Улитка и преддверие - единое пространство без внутренней архитектуры, нормальная или деформированная система полукружных каналов, либо ее отсутствие; внутренний слуховой проход чаще расширен, чем сужен; чаще всего - нормальный водопровод преддверия |
| Неполное разделение тип II (5-ая неделя) | Улитка представлена единой полостью без внутренней архитектуры; расширенное преддверие; чаще всего - расширенный внутренний слуховой проход; отсутствующая, расширенная или нормальная система полукружных каналов; нормальный водопровод преддверия |
| Гипоплазия улитки (6-ая неделя) | Четкое разделение кохлеарных и вестибулярных структур, улитка в виде пузырька небольших размеров; отсутствие или гипоплазия преддверия и системы полукружных каналов; суженный или нормальный внутренний слуховой проход; нормальный водопровод преддверия |
| Неполное разделение, тип II (аномалия Мондини) (7-ая неделя) | Улитка в 1,5 завитка, кистозно расширенные средний и апикальный завитки; размеры улитки близки к норме; незначительно расширенное преддверие; нормальная система полукружных каналов, расширенный водопровод преддверия |
Учитывая вышеизложенные современные представления о видах кохлеовестибулярных нарушений, мы используем классификации R.K. Jackler и L. Sennaroglu, как наиболее соответствующие находкам, встречающимся в собственной практике.
Принимая во внимание небольшое число прооперированных пациентов, ниже представлен один случай успешной КИ при аномалии развития внутреннего уха.
Случай из практики.
В СПб НИИ ЛОР в марте 2007 года обратились родители пациентки К., 2005 года рождения с жалобами на отсутствие у ребенка реакции на звуки и отсутствие речи. В ходе обследования был установлен диагноз: Хроническая двухсторонняя сенсоневральная тугоухость IV степени, врожденной этиологии. Вторичное расстройство рецептивной и экспрессивной речи. Последствия перенесенной внутриутробной цитомегаловирусной инфекции, внутриутробного поражения центральной нервной системы. Резидуально-органическое поражение центральной нервной системы. Левосторонний спастический верхний монопарез. Аплазия I пальца левой кисти. Дисплазия тазобедренных суставов. Спастическая кривошея. Тазовая дистопия гипоплазированной правой почки. Задержка психомоторного развития.
По заключению детского психолога - познавательные способности ребенка в пределах возрастной нормы, интеллект сохранен.

При проведении игровой аудиометрии в слуховых аппаратах выявлены реакции на звуки интенсивностью 80-95 дБ в диапазоне частот от 250 до 1000 Гц.
КТ височных костей выявила наличие двухсторонней аномалии развития улитки в виде неполного разделения I типа (табл. 4). При этом данное утверждение верно как для левого, так и для правого уха, несмотря на различную, на первый взгляд, картину (рис.1).
Рис. 1. Данные КТ пациентки К.

Примечание: Так, справа (1) улитка представлена небольшой полостью, максимальный размер которой составляет не более 5 мм, преддверие и полукружные каналы отсутствуют. Слева (2) улитка представлена единой полостью без внутренней архитектуры, отмечается наличие расширенного преддверия (рис. 2, стрелка); расширенная система полукружных каналов (рис. 3, стрелка).
Рис.2. Расширенное преддверие слева

Рис. 3. Расширенная и деформированная система полукружных каналов слева
После обследования пациентке проведена КИ на левом ухе классическим доступом через антромастоидотомию и заднюю тимпанотомию, с введением электрода через кохлеостому. Для операции использовался специальный укороченный электрод (Med-El, Австрия), имеющий рабочую длину активного электрода около 12 мм, специально разработанный для применения в случаях аномалии или оссификации улитки.
Несмотря на сохранные слуховые косточки и сухожилие стременной мышцы, акустические рефлексы со стременной мышцы в ходе операции зафиксированы не были. Однако, при проведении телеметрии нервного ответа, были получены четкие ответы при стимуляции 7 электродов из 12.

Послеоперационная трансорбитальная рентгенография улиток выявила, что активный электрод импланта находится в общей полости (рис. 4, стрелка), приняв форму идеальной окружности.
Рис. 4. Трансорбитальная рентгенография. Укороченный электрод в общей полости.
При контрольном аудиологическом обследовании через год после операции у пациентки обнаружены реакции в свободном звуковом поле на звуки интенсивностью в 15-20 дБ в диапазоне частот от 250 до 4000 Гц. Речь пациентки представлена одно- и двусложными словами («мама», «дай», «пить», «киса» и др.), простой фразой из не более двух одно- или двусложных слов. Учитывая то, что возраст пациентки на момент повторного обследования составлял менее 3 лет, результаты слухоречевой реабилитации в данном случае следует считать отличными.
Современная классификация аномалий развития внутреннего уха не только дает представление о многообразии такой патологии и времени появления дефекта в процессе внутриутробного развития, но и является полезной при определении показаний к проведению кохлеарной имплантации, в процессе выбора тактики для проведения вмешательства. Представленное в работе наблюдение позволяет оценить возможности кохлеарной имплантации, как средства реабилитации, в сложных случаях, расширяет представления о показаниях к проведению имплантации.
Синдром Мебиуса ( Врождённый окулофасциальный паралич , Фациальная диплегия )
Синдром Мебиуса — это врождённое сочетанное недоразвитие ядер V, VI, IX, XII пар черепных нервов, носящее преимущественно двусторонний характер. Проявляется с рождения отсутствием мимики, неполным закрытием глаз, нарушением сосания, глотания, артикуляции. В большинстве случаев сочетается с аномалиями лицевого черепа, конечностей. Диагностика включает неврологическое, нейропсихологическое обследование, церебральную МРТ, ЭНМГ, генетическое консультирование. Консервативное и хирургическое лечение направлено на коррекцию врождённых пороков, восстановление речи, социальную адаптацию пациентов.
МКБ-10
Общие сведения
Синдром Мебиуса представляет собой врождённую аномалию лицевого нерва (VII пара) в сочетании с патологией отводящего (VI), языкоглоточного (IX), подъязычного (XII), реже — тройничного (V), преддверно-улиткового (VIII) нервов. Впервые описан немецким неврологом П. Мебиусом в 1888 году. В современной неврологии встречаются следующие синонимичные названия: «фациальная диплегия», «врождённый окулофасциальный паралич». Распространённость патологии составляет 1 случай на 150 тыс. новорождённых, мальчики и девочки заболевают одинаково часто. Известны наследственные и спорадические случаи болезни.
Причины
Фациальная диплегия считается мультифакторным заболеванием. Генетическая детерминированность подтверждается семейными случаями с аутосомно-доминантным и аутосомно-рецессивным наследованием. Однако наследственный анамнез прослеживается не всегда. Спорадические случаи обусловлены неблагоприятным воздействием на плод в период внутриутробного развития. Этиофакторами возникновения синдрома могут выступать:
- Заболевания матери. Инфекции (краснуха, грипп), перенесённые женщиной в период вынашивания плода, различные хронические болезни (кардиомиопатия, бронхоэктатическая болезнь), эндокринная патология (гестационный диабет) создают неблагоприятные условия внутриутробного развития. Следствием последних становятся различные нарушения эмбриогенеза, в том числе синдром Мебиуса.
- Гипоксия плода. Кислородное голодание возникает при фетоплацентарной недостаточности, резус-конфликте, аномалиях пуповины, внутриутробных инфекциях. Длительная гипоксия приводит к общей задержке внутриутробного развития или нарушению отдельных его этапов. Задержка формирования черепно-мозговых нервов является причиной их конгенитальной гипоплазии.
- Токсические воздействия. Провоцировать сбои в процессе эмбриогенеза может приём тератогенных фармпрепаратов на ранних сроках беременности, наркомания, алкоголизм беременной. Результатом становится недоразвитие черепных нервов, их ядер, другая врождённая патология.
Патогенез
Генетическая детерминированность, неблагоприятные антенатальные условия потенцируют различные нарушения, задержку формирования ядер и корешков черепно-мозговых нервов на уровне ствола головного мозга. В первую очередь страдают лицевой и отводящий нервы. Из-за нарушения иннервации мимической мускулатуры лица возникает амимия. Денервация мышцы, поворачивающей глазное яблоко наружу, обуславливает сходящееся косоглазие. Зачастую синдром Мебиуса включает недоразвитие прочих расположенных в стволе черепных нервов. Гипоплазия языкоглоточного, блуждающего, подъязычного нервов приводит к расстройству сосания, глотания, голосообразования, артикуляции. При недоразвитии VIII пары выявляется тугоухость, V пары — отсутствие чувствительности кожи лица.
Симптомы
Первыми клиническими проявлениями синдрома становятся амимия лица, косоглазие, расстройство сосания, глотания. Обращает на себя внимание отсутствие мимики у новорождённого. Характерен внешний вид ребёнка: лицо неподвижное, уголки рта опущены, рот приоткрыт, наблюдается лагофтальм (неполное смыкание век). Отсутствуют плач, улыбка, слёзотечение. Синдром Мебиуса часто сочетается с иными врождёнными пороками различных структур головы: расщелиной твёрдого нёба, микрогнатией, аномалиями зубных рядов, дисплазией ушных раковин, микрофтальмом, У 50% больных имеются конгенитальные аномалии конечностей: синдактилия, полидактилия, косолапость, деформации стоп. Часто встречается синдром Поланда: аплазия большой грудной мышцы, молочной железы и соска, дисплазия рёбер, брахидактилия.
Нарушение иннервации мышц глотки, гортани, языка, круговой мышцы рта, щёк приводит к проблемам с кормлением грудничка. Ребёнок плохо сосёт, попёрхивается едой. При наличии расщелины нёба во время еды пища забрасывается с полость носа. С введением прикорма возникают сложности пережёвывания, из-за слабой подвижности языка остатки пищи скапливаются за зубами. В последующем отмечаются нарушения речи в виде дизартрии: речь смазанная, нечленораздельная, требует от ребёнка значительных усилий. Дизартрия сочетается с дисфонией, проявляющейся тихим осиплым голосом. У многих больных наблюдается снижение слуха вплоть до выраженной тугоухости. Нарушение интеллектуального развития определяется в 10% случаев, его выраженность варьируется от пограничного интеллектуального снижения до тяжёлой олигофрении.
Осложнения
Расстройства глотания опасны попаданием пищи в дыхательные пути с асфиксией. Скопление остатков пищи в полости рта создаёт благоприятные условия для развития кариеса и прочих стоматологических заболеваний. Вследствие нарушений строения и функционирования верхних дыхательных путей (носоглотки, гортани) часто возникают респираторные инфекции, которые могут осложниться пневмонией. Наличие особенностей строения уха обуславливает частые отиты у детей. Осложнением лагофтальма является повышенная сухость глаза (ксерофтальмия) и связанные с ней воспалительные процессы (конъюнктивиты, кератиты).
Лицевой паралич, речевые затруднения резко ограничивают способность больного выражать свои эмоции, наблюдаются сложности общения и приобретения социальных навыков. Вследствие этого пациенты склонны к депрессии, имеют трудности обучения. Дизартрия и тугоухость приводят к формированию общего недоразвития речи, без должной коррекции становятся причиной задержки психического развития. Диспластические изменения конечностей вызывают определённые ограничения в двигательной сфере, при отсутствии лечения развиваются контрактуры суставов.
Диагностика
Диагностический поиск направлен на оценку состояния черепных нервов, мышц лица, языка, глотки, исключение морфологического субстрата патологии (неоплазии, гематомы, врождённой гидроцефалии, церебральной кисты), определение возможностей хирургического лечения. Диагностика сопутствующих аномалий проводится с участием стоматолога, челюстно-лицевого хирурга, ортопеда, офтальмолога, оториноларинголога. Перечень необходимых диагностических обследований включает:
- Осмотр невролога. В неврологическом статусе отмечается лицевой паралич, атрофия языка, снижение глоточного рефлекса. При патологии тройничного нерва обнаруживается гипестезия кожи лица. Как правило, патологические изменения носят двусторонний характер.
- МРТ головного мозга. Позволяет выявить гипоплазию черепных нервов. С помощью МРТ можно исключить опухоль и пороки развития головного мозга, послеродовую гематому, врождённую кисту. Проведение КТоо детям не рекомендовано из-за опасности лучевой нагрузки.
- Электронейромиографию. Исследование определяет резкое снижение или полный блок проведения нервных импульсов по лицевому нерву. Количество возбуждаемых мышечных волокон уменьшено, что свидетельствует об атрофических изменениях.
- Нейропсихологическое обследование. Производится исследование реакции на появление матери, наличие слежения взглядом за игрушкой, соответствие психомоторного развития возрастным нормам. В старшем возрасте когнитивная и психологическая сферы оцениваются при помощи тестирования.
- Консультацию генетика. Составление генеалогического древа необходимо для выявления наследственного характера синдрома, установления типа наследования. ДНК-диагностика не получила широкого распространения из-за большого числа спорадических случаев.
Дифференцировать синдром Мебиуса необходимо от опухолевых процессов, энцефалита с поражением мозгового ствола, болезни Дауна, прогрессирующего бульбарного паралича, нервно-мышечных заболеваний. В редких случаях, когда синдром Мебиуса протекает с односторонним лицевым параличом, следует отличать патологию от внутримозговых гематом, образовавшихся вследствие внутричерепной родовой травмы.
Лечение синдрома Мебиуса
В отношении заболевания проводится комплексная терапия, направленная на коррекцию имеющихся врождённых аномалий, поддержание функционирования головного мозга, костно-мышечной системы, психологическую поддержку больного и его близких. Питание осуществляется при помощи специального шприца, через зонд, при необходимости — парентерально. Ребёнка консультируют педиатр, детский хирург, пластический хирург, офтальмолог, психолог, ортодонт. Лечение включает следующие составляющие:
- Неврологическую. Проводится поддерживающая нейротропная фармакотерапия аминокислотами, ноотропными, сосудистыми, витаминными препаратами. Коррекция амимии выполняется хирургически, операция заключается в пересадке мышечного трансплантата с бедра на лицо.
- Офтальмологическую. С целью предупреждения осложнений ксерофтальмии производится постоянное закапывание увлажняющих глазных капель. При развитии воспаления назначают антибактериальные капли. Для защиты роговицы показана частичная тарзорафия — ушивание краёв век. Косоглазие требует хирургического лечения.
- Ортопедическую. Предполагает хирургическую коррекцию пороков развития конечностей: разделение пальцев при синдактилии, устранение косолапости, операции на костях и суставах стопы. Рекомендовано ношение ортопедической обуви, регулярные занятия ЛФК, физиотерапия, массаж.
- Стоматологическую. Осуществляется закрытие расщелины нёба, ортодонтическое лечение нарушений прикуса, выравнивание зубных рядов. В тяжёлых случаях проводится лечение методами челюстно-лицевой хирургии.
- Логопедическую. Применяется артикуляционная гимнастика, логопедический массаж. Назначаются регулярные занятия с логопедом по коррекции дизартрии, ОНР.
- Психологическую. Большое значение в комплексном лечении имеют занятия ребёнка с психологом, детская психотерапия, арт-терапия, психологическое консультирование родителей. С целью социальной адаптации дети старшего возраста принимают участие в групповых психологических тренингах.
Прогноз и профилактика
Синдром Мебиуса отличается стабильностью течения. Прогноз зависит от тяжести врожденных пороков. Комплексное лечение позволяет минимизировать нарушения, обеспечить достаточно высокое качество жизни пациентов. Возможны затруднения адаптации в социуме. Дети с олигофренией имеют более серьёзный прогноз. Мерами профилактики являются планирование беременности в оптимальном репродуктивном возрасте, отказ от деторождения при наличии тяжёлой наследственной патологии, улучшение экологической обстановки, здоровый образ жизни родителей. Предупредить осложнения гестации, способные спровоцировать синдром Мебиуса, позволяет правильное ведение беременности, своевременная коррекция нарушений маточно-плацентарного кровотока, дисметаболических расстройств.
2. Синдромы с одновременным поражением органа зрения, полости рта и зубо-челюстной системы/ Ярцева Н.С, Барер Г.М., Гаджиева Н.С. - 2003.
3. The Mobius sequence/ Miller M.T., Stromland K.// J. Am Assoc Pediatr Ophthalmol. Strabismus. - 1999. - V. 3.
Гипоплазия зрительного нерва
Гипоплазия зрительного нерва - врожденная аномалия, характеризующаяся уменьшением количества аксонов в структуре пораженного нерва. Клиническая симптоматика представлена снижением остроты зрения, нистагмом, косоглазием, повышенной утомляемостью. Диагностика основывается на проведении прямой офтальмоскопии, электроретинографии, КТ головы, визометрии, гистологического и микроскопического исследования. Пациентам показана электростимуляция зрительного нерва, лазерная плеоптика, компенсация депривации, а также симптоматическая терапия страбизма и нистагма.
Гипоплазия зрительного нерва впервые была описана британским офтальмологом В. Ньюменом в 1864 году. Заболевание диагностируют у 50% детей с диагнозом фетального алкогольного синдрома. Согласно статистическим данным, в возрасте от 5 до 15 лет 5,9% от всех случаев слепоты обусловлены этой аномалией развития глаза. Около 90% детей с этой патологией страдают страбизмом или нистагмом. У 46-53% больных помимо недоразвития оптических волокон диагностируют агенезию мозолистого тела и прозрачной перегородки. У 12-45% пациентов удается выявить ряд мальформаций центральной нервной системы. Заболевание с одинаковой частотой встречается среди лиц мужского и женского пола.
Причины гипоплазии зрительного нерва
Иногда при недоразвитии оптических волокон обнаруживается мутация гена РАХ6 в локусе 11р13, которая обычно сочетается с помутнением хрусталика и аниридией. Установлен аутосомно-доминантный тип наследования. К пусковым факторам относятся:
- Воздействие тератогенных факторов. Экспериментальным путем было доказано, что прием спиртных напитков, потребление наркотических средств (кокаин) и курение в период беременности достоверно повышает вероятность возникновения заболевания.
- Метаболические расстройства. Патологию часто диагностируют у детей, рожденных от матерей с сахарным диабетом 1 типа, гипотиреозом в анамнезе.
- Влияние лекарственных средств. Поражение оптических нервных волокон у плода вызывает прием матерью фенобарбитала, антидепрессантов, хинина во время беременности.
- Внутриутробные инфекции. Развитие болезни часто провоцирует инфицирование плода цитомегаловирусом, герпетической инфекцией.
Патогенетический механизм напрямую связан с нарушением деления ганглиозных клеток внутренней оболочки глаза на 4-6 неделе эмбриогенеза. Амакриновые и горизонтальные клетки не поражаются. Согласно другой патогенетической теории, заболевание вызвано феноменом аксональной регрессии на 16-31 гестационной неделе. При сочетании болезни с другими аномалиями развития головного мозга ведущая роль в формировании дефектов отводится ретроградной дегенерации, обусловленной преобладанием энцефалокластических процессов. Нарушение дифференциации структур полушарий и оптических волокон зачастую связано с патологией регуляторных процессов. Механическая теория базируется на компрессии зрительного пути злокачественным новообразованием, организовавшимся экссудатом, сгустками крови.
Симптомы гипоплазии зрительного нерва
В случае тяжелого течения первые клинические проявления родители наблюдают уже в период новорожденности. У детей рано развивается косоглазие, нистагм, нарушение ориентации в пространстве. В старшем возрасте пациенты предъявляют жалобы на двоение перед глазами, головокружение, затруднения при фиксации взгляда, которые проявляются мелкоразмашистыми движениями. Симптоматика усиливается при волнении, усталости, в стрессовых ситуациях. При длительной концентрации взгляда возникает головная боль, затуманивание зрения, повышенная утомляемость. Нарушение остроты зрения варьирует от незначительного снижения до полной слепоты.
Патология может иметь одно- или двухсторонний характер. При односторонней или асимметричной форме нарушается бинокулярное зрение. При закрытии больного глаза симптомы исчезают. Часто дети пытаются ограничить участие пораженного глазного яблока в акте зрения. С целью компенсировать зрительную дисфункцию пациенты наклоняют голову под углом наиболее четкого видения. Для двухсторонней формы характерна девиация глаза, которая проявляется постоянным отклонением глазных яблок в определенную сторону. При этом создается впечатление, что человек всегда смотрит в одном направлении. У большинства пациентов выявляется афферентный зрачковый дефект. Из-за несимметричного положения радужной оболочки и зрачка часто наблюдаются затруднения адаптации в социуме.
Гипоплазия зрительного нерва часто осложняется выраженным снижением зрения вплоть по амавроза. Пациенты с данной патологией в анамнезе более склонны к присоединению инфекционных и воспалительных заболеваний глаз (пан- и эндофтальм, склерит), что связано с нарушением регионального кровоснабжения и трофики. Как правило, вторичное вовлечение в патологический процесс сетчатой оболочки и увеального тракта ведет к развитию ретинита, переднего и заднего увеита. При сопутствующем поражении оптических трактов возникает гемианопсия. Заболевание нередко сочетается со злокачественными новообразованиями головного мозга (супраселлярные опухоли, тератома).
Для постановки диагноза применяют физикальный осмотр и специальное офтальмологическое обследование. При наличии патологии у родителей или близких родственников на 16 неделе внутриутробного развития осуществляют генетический скрининг. В постнатальном периоде диагностика базируется на проведении:
Дополнительно показан расчет отношения расстояния между ДЗН и макулой к диаметру диска, который в норме составляет менее 3. Дифференциальная диагностика проводится с аплазией и атрофией оптического нерва. Характерные офтальмоскопические признаки атрофии - восковый оттенок ДЗН, экскавация его поверхности, сужение и уменьшение числа сосудов сетчатки. При аплазии определяется полное отсутствие диска зрительного нерва на фоне слабо выраженной пигментации внутренней оболочки глазного яблока. Макула не подлежит дифференциации. Визуализируются только сосуды хориоидеи.
Лечение гипоплазии зрительного нерва
Терапия результативна только при раннем проведении лечебных мероприятий. Это связано с тем, что в на первом году жизни пре- и постгеникулярные пути, латеральное коленчатое тело и корковые центры находятся на стадии формирования. Лечение включает в себя:
- Чрескожную электростимуляцию зрительного нерва. Эффективность метода напрямую зависит от исходной остроты зрения. Электростимуляция назначается курсами. В среднем проводится от 3 до 5 курсов.
- Компенсацию глазной депривации. Для компенсации этого явления ребёнку проводят очковую и контактную коррекцию остроты зрения. Профилактика развития амблиопии предполагает использование дозированной окклюзии лучше видящего глаза.
- Лазерную плеоптику. Методика основывается на применении лазерного излучения низкой интенсивности, которое позволяет улучшить микроциркуляцию и метаболические процессы в окружающих тканях, повышает активность ДНК, РНК и ферментов, благотворно влияет на энергетический потенциал клеток и трофические процессы.
Симптоматическая терапия базируется на хирургическом лечении нистагма и страбизма. Оперативные способы коррекции косоглазия используются в возрасте до 5 лет. В зависимости от типа страбизма назначают операции, которые ослабляют или усиливают функции глазодвигательных мышц. Цель лечения при нистагме - формирование позиции относительного покоя путем восстановления физиологического положения мышц. По индивидуальным показаниям осуществляют инъекции ботокса в глазничную полость для уменьшения амплитуды мелкоразмашистых движений глазных яблок. Дополнительно проводят коррекцию нейроэндокринных нарушений (неонатальная гипогликемия, пангипопитуитаризм, вторичный гипотиреоз).
Прогноз определяется степенью выраженности гипоплазии. Незначительный дефект строения зрительного нерва может долгое время оставаться незамеченным. Своевременно начатое лечение приводит к положительным результатам. Специфическая профилактика этой аномалии развития не разработана. Неспецифические превентивные меры сводятся к предупреждению воздействия тератогенных факторов (спиртные напитки, наркотические средства, ионизирующее излучение). При высоком риске возникновения болезни показано проведение перинатальной диагностики и специфической терапии с периода новорожденности.
Краниовертебральные аномалии ( аномалии краниовертебрального перехода )
Краниовертебральные аномалии — отклонения в анатомическом взаиморасположении и строении структур области соприкосновения черепной коробки и позвоночника. Зачастую не имеют клинических проявлений. В клинически значимых случаях манифестируют синдромами внутричерепной гипертензии, поражения позвоночной артерии, сдавления корешка, спинного мозга или ствола; у маленьких детей возможны расстройства дыхания. Диагностируются краниовертебральные аномалии при помощи краниографии, МРТ или КТ краниовертебральной области. Необходимо наблюдение невролога, по показаниям — нейрохирургическое лечение.
Краниовертебральный переход включает образованное затылочной костью основание черепа и первые 2 шейных позвонка (атлант и аксис). Это зона соединения неподвижной черепной коробки и мобильного позвоночника. Нарушения правильного анатомического строения и положения костных образований, лежащие в основе краниовертебральных аномалий (КВА), зачастую отражаются на расположенных в этой области структурах головного и спинного мозга, что влечет появление соответствующей неврологической симптоматики. Последняя носит довольно вариативный характер, связана в основном с компрессией верхнешейных сегментов спинного мозга и спинальных корешков, ствола мозга, мозжечка, IX-XII черепно-мозговых нервов, позвоночных артерий; нарушением циркуляции цереброспинальной жидкости. Краниовертебральные аномалии легкой степени выраженности протекают субклинически, однако их выявление имеет важное значение в клинической неврологии, особенно, когда речь идет о проведении мануальной терапии.
Причины краниовертебральных аномалий
Врожденные аномалии краниовертебрального перехода возникают как результат нарушения эмбриогенеза при воздействии на плод вариабельных негативных факторов. К последним относят повышенный радиоактивный фон, внутриутробные инфекции, интоксикации при дисметаболических заболеваниях, профессиональных вредностях или зависимостях (наркомании, курении, алкоголизме) беременной. В ряде семей прослеживается значительно более высокая частота аномалий, чем в общем по популяции, что говорит в пользу наследственной передачи КВА, имеющей, вероятно, мультифакторный характер.
Приобретенные краниовертебральные аномалии могут формироваться в результате травм позвоночника в шейном отделе или черепно-мозговых травм, в том числе и родовых травм новорожденного. Кроме того, травмы часто служат триггером, провоцирующим клинические проявления ранее бессимптомно протекающей аномалии. Деформации краниовертебральной зоны возможны вследствие остеопороза, причиной которого могут выступать рахит, гиперпаратиреоз, деформирующий остеит, остеомаляция. Приобретенные краниовертебральные аномалии могут возникать в связи с разрушением костных структур краниовертебрального перехода при остеомиелите, опухолях костей, туберкулезе, актиномикозе, сифилисе.
Признаки краниовертебральных аномалий
Клиническая картина аномалий краниовертебрального перехода весьма вариабельна: от субклинического течения до возникновения грубых неврологических расстройств. Она обусловлена видом и степенью имеющихся костных дефектов. Визуальные признаки, характеризующие краниовертебральные аномалии, включают: низкий рост волос на затылке, укороченную шею, ограничение подвижности головы, увеличенный шейный лордоз, кривошею, измененную посадку головы. Манифестация клиники зависит от тяжести аномалии. При грубых деформация она, как правило, происходит в раннем детском возрасте, при умеренных и легких — возможна в любой возрастной период, но обычно является отсроченной.
Клиническая симптоматика бывает представлена синдромом позвоночной артерии и хронической ишемией головного мозга, обмороками, гидроцефалией и внутричерепной гипертензией, в тяжелых случаях — синдромом вклинения ствола и миндалин мозжечка в затылочное отверстие. У детей раннего возраста краниовертебральные аномалии могут быть причиной синдрома сонных апноэ, стридора и пр. дыхательных нарушений.
Виды краниовертебральных аномалий
Проатлант — рудиментарный костный элемент в области затылочной кости. Врожденная патология, связанная с нарушением редуцирования соединительнотканного тяжа, образующегося с вентральной стороны позвонков в ходе онтогенеза. При отсутствии сращений рудиментарного элемента с окружающими костными структурами говорят о свободном проатланте. При его слиянии с передним краем большого затылочного отверстия употребляют термин «третий мыщелок», при срастании с задним краем — термин «околозатылочный отросток».
Гипоплазия и аплазия задней дуги атланта. В первом случае клинические проявления отсутствуют, порок диагностируется рентгенологически. Аномалия встречается у 5-9% населения. Во втором случае в детском возрасте или пубертате возникает сдавление дистальной части ствола и верхних отделов спинного мозга. Характерно быстрое усугубление симптоматики. Встречаемость порока составляет 0,5-1%.
Ассимиляция атланта — сращение 1-го шейного позвонка и затылочной кости. Может быть полным и неполным, одно- и двусторонним. Частота аномалии не превышает 2%. Ассимиляция атланта манифестирует клинически после 20-летнего возраста головными болями с вегетативной симптоматикой. Возможен ликворно-гипертензионный синдром, легкие диссоциированные сенсорные нарушения, расстройства функции нижних черепно-мозговых нервов.
Аномалии зубовидного отростка по различным данным встречаются у 0,5-9% населения. Включают гипо- и аплазию, а также гипертрофию отростка, которые протекают без клинических проявлений. Неврологическая симптоматика возникает в случаях, когда зубовидный отросток не сращен с аксисом, а формирует отдельную зубовидную кость. В таких условиях отмечается хронический атланто-аксиальный подвывих, возможна компрессия проксимальных отделов спинного мозга.
Платибазия — уплощение основания черепной коробки. Клинически платибазия проявляется только при III степени уплощения, сопровождающейся существенным уменьшением размеров задней черепной ямки, влекущим за собой внутричерепную гипертензию, сдавление мозжечка и IX-XII пар черепных нервов.
Базилярная импрессия — вдавление основания черепа в его полость. В популяции встречается с частотой 1-2%. При базилярной импрессии симптомы, обусловленные уменьшением задней черепной ямки, сочетаются с признаками сдавления спинальных корешков первых шейных сегментов. В этих сегментах возможно возникновение компрессионной миелопатии с центральным тетрапарезом. Крайняя выраженность аномалии (вворачивание основания внутрь полости черепа) носит название конвексобазия.
Аномалия Киммерли связана с наличием дополнительной дужки атланта, ограничивающей позвоночную артерию. Аномалия Киммерли бывает полная и неполная, одно- и двусторонняя. Клинически значима лишь у четверти носителей порока. Проявляется синдромом позвоночной артерии, обмороками, ТИА, в тяжелых случаях вероятен ишемический инсульт.
Аномалия Киари — врожденный порок развития, при котором часть структур задней черепной ямки пролабирует в затылочное отверстие. У 80% пациентов имеется сирингомиелия. Выделяют 4 типа аномалии Киари, которые отличаются возрастом дебюта и клинической симптоматикой.
Синдром Клиппеля-Фейля — редкая врожденная аномалия (частота 0,2-0,8%) в виде уменьшения числа шейных позвонков и/или их сращении. Может иметь наследственный или спорадический характер. Синдром Клиппеля-Фейля часто сочетается с др. пороками развития (расщеплением позвоночника, полидактилией, волчьей пастью, аномалиями зубов, врожденными пороками сердца и т. п.). Характерна возникающая еще в раннем детстве мышечная слабость с исходом в парезы. В ряде случаев наблюдаются врожденная гидроцефалия и олигофрения.
Диагностика краниовертебральных аномалий
Наряду с клиническим обследованием важное значение в диагностике имеет выполнение рентгенографии черепа и рентгенографии шейного отдела позвоночника. С целью визуализации мягкотканных структур краниовертебрального перехода назначают МРТ головного мозга и МРТ позвоночника в шейном отделе. Исследование выполняется в режимах Т1 и Т2, в сагитальной и аксиальной проекциях. По показаниям проводят МРТ сосудов головного мозга. При невозможности МРТ-обследования, а также для более точной визуализации костных образований краниовертебральной зоны, выполняют КТ позвоночника и КТ головного мозга.
Дополнительно проводят консультацию офтальмолога с офтальмоскопией (осмотром глазного дна), консультацию отоневролога с аудиометрией, непрямой отолитометрией. При необходимости исследуют стволовые вызванные потенциалы. Наличие синдрома позвоночной артерии является показанием к сосудистым исследованиям — РЭГ с функциональными пробами, УЗДГ экстракраниальных сосудов. Для выявления наследственной патологии проводится консультация генетика и генеалогический анализ.
Лечение краниовертебральных аномалий
Пациенты с аномалиями краниовертебрального перехода должны соблюдать ряд предосторожностей, чтобы не спровоцировать и не усугубить клинические проявления аномалии. Не желательны резкие наклоны и повороты головы, стойки на голове, кувырки, занятия травматичным спортом и форсированные нагрузки. Наблюдение субклинических форм КВА и базисная терапия при умеренных проявлениях осуществляется неврологом. Традиционно основу базисного лечения составляют ноотропные, нейротрофические и вазоактивные фармпрепараты, хотя их эффективность при краниовертебральных аномалиях не доказана.
При выраженных клинических проявлениях решается вопрос о возможности нейрохирургической коррекции порока. Показаниями к хирургическому лечению являются симптомы компрессии ствола, мозжечка или спинного мозга, нарушение церебрального кровообращения. При базилярной импрессии и аномалии Киари проводится краниовертебральная декомпрессия, при аномалии Киммерли — резекция дополнительной дужки атланта, при ассимиляции атланта — ламинэктомия для декомпрессии спинного мозга и стабилизация позвоночника при помощи спондилодеза, при синдроме Клиппеля-Фейля — операция цервикализации.
Невринома слухового нерва - симптомы и лечение
Что такое невринома слухового нерва? Причины возникновения, диагностику и методы лечения разберем в статье доктора Касаткина Дениса Сергеевича, нейрохирурга со стажем в 11 лет.
Над статьей доктора Касаткина Дениса Сергеевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
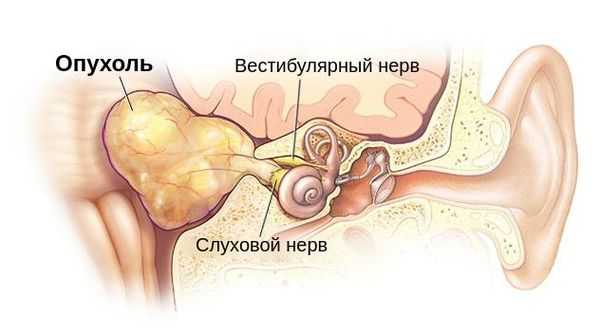
Данная опухоль составляет 82 % всех опухолей мостомозжечкового угла, 7 % всех внутричерепных опухолей и до трети опухолей задней черепной ямки. В год невриному обнаруживают примерно у одного человека на 100 тысяч населения. В 97 % случаев опухоль локализуется только с одной стороны. У остальных пациентов — поражение двустороннее [1] .
Невриномы слухового нерва возникают в 40-50 лет. Более часто они встречаются у женщин, чем у мужчин: примерно 3:2 [1] .
Впервые невриному описал Голландский анатом E. Sandifort в 1777 году, как "небольшое патологическое образование, прилежащее к слуховому нерву". Оно было выявлено у пациента, страдавшего глухотой. Позднее, в 1822 году J. Wishart, хирург из Шотландии, при вскрытии больного описал случай двусторонней опухоли вестибулокохлеарных нервов у пациента, страдавшего тугоухостью на оба уха, приступами головной боли и параличом лицевого нерва.
Наибольший вклад в изучение проблемы лечения вестибулярных шванном сделал американский нейрохирург H.Cushing. Он снизил летальность c 80 % до 10 %. Позднее его коллега из Швейцарии M.G. Yasargil внедрил технику работы с операционным микроскопом, разработал микронейрохирургические инструменты. Это позволило более безопасно и радикально удалять опухоли, сохраняя при этом ствол головного мозга, смежные черепно-мозговые нервы и сосудистую структуру [2] .
Причиной появления невриномы, чаще двусторонней, может быть нейрофиброматоз II типа — распространённая наследственная болезнь, которая предрасполагает к возникновению опухоли, а также наследственная генетическая мутация в 22-ой хромосоме.
Риск развития невриномы увеличивают:
- действие ионизирующего излучения;
- гормональный фон;
- агрессивные факторы внешней среды — жизнь в местности, загрязнённой промышленными отходами, продуктами сгорания авиационного топлива и пр.;
- неправильное питание [4][11] .
К примеру, беременность или облучение прямыми солнечными лучами могут ускорить рост опухоли и спровоцировать появление первых симптомов болезни.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
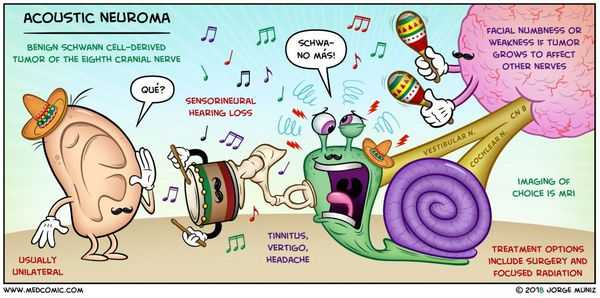
Симптомы невриномы слухового нерва
Первые признаки заболевания:
- Расстройства слуха — шум или звон в ухе, волнообразное, постепенно нарастающее, иногда острое снижение слуха [13] . Чаще эти симптомы связаны с поворотом головы головокружением, иногда со спонтанным нистагмом — непроизвольным ритмичным движением глаз из стороны в сторону.
- Поражение лицевого нерва — негрубая слабость мимических мышц на стороне опухоли, усиленное слезотечение [14] , изменение вкусовых ощущений на передней 2/3 поверхности языка из-за воздействия на барабанную струну, которая отходит от лицевого нерва.
- Поражение тройничного нерва свидетельствует о большом размере опухоли. Первый признак такого нарушения — угнетение роговичного рефлекса (нарушение смыкания век при прикосновении к роговице). В дальнейшем развивается покалывание языка [14] , гипестезия на лице (потеря чувствительности) или тригеминальная невралгия — мучительные стреляющие боли в половине лица.
В дальнейшем могут появиться симптомы поражения черепных нервов каудальной группы:
- языкоглоточного нерва — нарушение вкусового восприятия на задней трети языка, снижение чувствительности слизистой верхней части глотки, дисфагия (нарушение глотания пищи);
- блуждающего нерва — асимметрия мягкого нёба, дисфония (голос становится хриплым) [14] ;
- добавочного нерва — слабость и гипотрофия трапециевидной и грудино-ключично-сосцевидной мышц;
- подъязычного нерва — атрофия мышц языка на стороне опухоли.
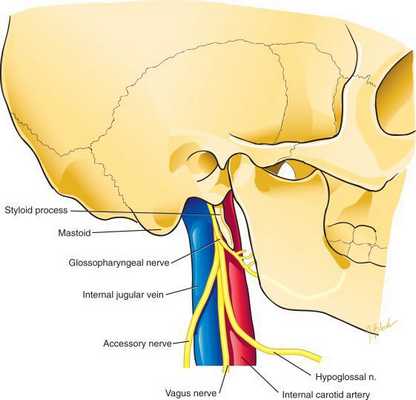
Появление тех или иных симптомов зависит от размеров опухоли и стадия её развития. Дальнейший рост невриномы ведёт к компрессии (сдавлению) 4-го желудочка и ствола головного мозга, появляются симптомы, связанные с увеличением внутричерепного давления. Например, пациент с большой опухолью может жаловаться на слабость в конечностях, асимметрию лица, тошноту, рвоту головокружение, глухоту на одно ухо.
Ниже в таблице представлена частота встречаемости неврологических симптомов невриномы слухового нерва [4] .
Патогенез невриномы слухового нерва
Увеличиваться опухоль может в двух направлениях: в сторону слухового прохода и в сторону мостомозжечкового угла. От направления роста зависит, какие органы и нервы будет сдавливать опухоль при дальнейшем увеличении: мозжечок, лицевой, тройничный или каудальная группа черепных нервов [16] .
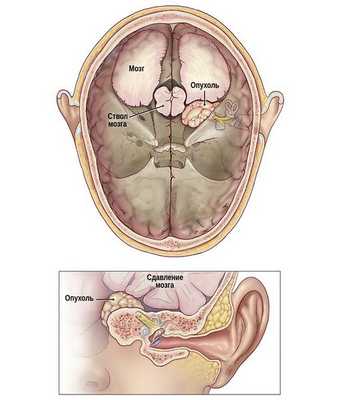
Рис. Схематичное изображение роста невриномы слухового нерва из внутреннего слухового прохода в заднюю черепную ямку со сдавление ствола головного мозга.
Макроскопически опухоль представляет собой бугристую серую сферу неправильной формы. Она не прорастает в ткань мозга и часто в своей структуре имеет вкраплённые кисты, заполненные жидкостью. Обычно растёт медленно — по 2-5 мм в год — и даёт о себе знать, когда достигает больших размеров.
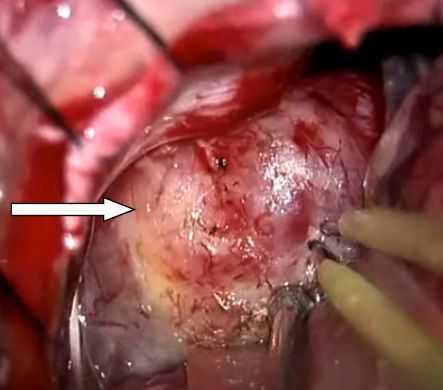
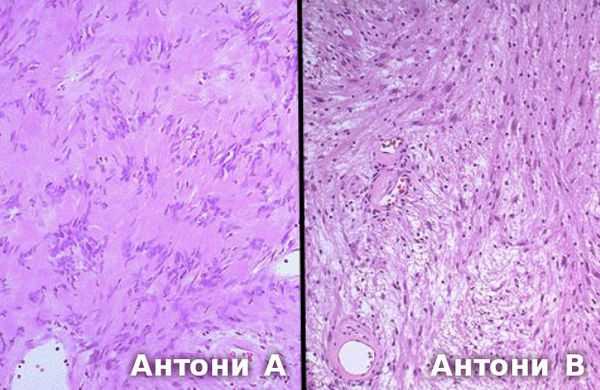
По данным патоморфологических исследований выделяют два основных типа опухоли:
- Антони А — клетки опухоли формируют группы с вытянутыми ядрами;
- Антони В — различные узоры звездообразных клеток и их длинных отростков [5] . Обычно этот тип встречается при больших невриномах. Считается, что они возникает в результате ишемии [14] .
Симптомы и жалобы при вестибулярной шванноме обусловлены четырьмя основным процессами:
- компрессия сосудов головного мозга, которая ведёт к инсульту;
- поражение черепных нервов;
- сдавление и смещение ствола головного мозга;
- сдавление 4-го желудочка [3] .
Классификация и стадии развития невриномы слухового нерва
Все классификации и стадии невриномы слухового нерва учитывают размер опухоли и её положение относительно ствола головного мозга [6] . Активно во врачебной практике используются классификации W. Koos и M. Samii. Они позволяют определить тактику лечения.
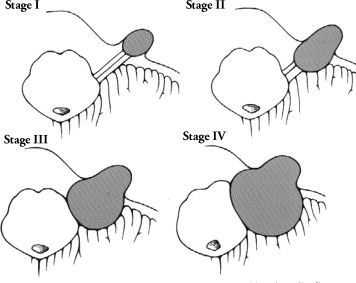
Стадии роста невриномы по W. Koos:
- I стадия — опухоль до 10 мм, не выходит за пределы внутреннего слухового прохода;
- II стадия — опухоль до 20 мм, расширяет внутренний слуховой проход и выходит в мостомозжечковый угол;
- III стадия — опухоль до 30 мм, достигает ствола головного мозга, но не сдавливает его;
- IV стадия — опухоль больше 30 мм, сдавливает ствол головного мозга [15][17] .
Классификация невриномы слухового нерва по M. Samii:
- Т1 — опухоль, расположенная во внутреннем слуховом проходе;
- Т2 — опухоль, растущая из внутреннего слухового прохода;
- Т3а — опухоль, заполняющая цистерну мостомозжечкового угла;
- Т3b — опухоль, достигающая ствола головного мозга;
- Т4а — опухоль, сдавливающая ствол;
- Т4b — опухоль, грубо деформирующая ствол мозга и 4-й желудочек.
Также можно выделить четыре стадии клинического течения болезни:
- отиатрическая стадия — шум или глухота на одно ухо;
- отоневрологическая стадия — присоединяются поражения тройничного и лицевого нервов на стороне опухоли;
- гипертензионно-гидроцефальная стадия — на этой стадии болезни пациент отмечает головные боли, появляется тошнота, рвота;
- бульбарная стадия — добавляется дизартрия, дисфагия, дисфония.
Осложнения невриномы слухового нерва
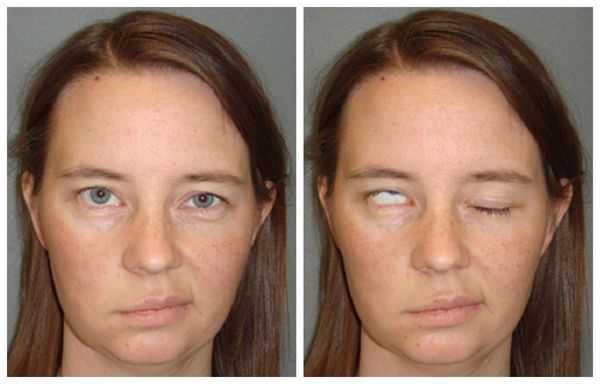
Наиболее распространённым осложнением невриномы является односторонняя нейросенсорная тугоухость: с ростом опухоли человек полностью теряет слух. Также часто страдает лицевой нерв, из-за чего развивается односторонний паралич мимической мускулатуры.
Чем больше размер опухоли, тем выше риск поражения каудальной группы черепных нервов. Это может привести к такому опасному для жизни осложнению, как бульбарный синдром — паралич мышц, которые иннервированы каудальной группой нервов (языкоглоточного, блуждающего и др.). Он может привести к тому, что человек не сможет самостоятельно питаться через рот.
Когда опухоль начинает сдавливать ствол головного мозга, развиваются симптомы поражения пирамидного тракта — нарушается походка, возникает слабость в конечностях, параличи и парезы. А при сдавливании водопровода головного мозга может развиваться гидроцефалия. Если на этой стадии болезни не выполнить хирургическое лечение, дальнейшее компрессия ствола головного мозга приводит к смерти пациента из-за поражения дыхательного цента и ретикулярной формации — всей оси ствола головного мозга [7] .
Невриномы слухового нерва не перерождаются в рак, однако учитывая, что локализация опухоли очень сложная для радикального удаления, она может снова появляться или продолжать расти даже после радиохирургического лечения.
Диагностика невриномы слухового нерва
Диагностика невриномы слухового нерва должна включать в себя неврологическое обследование, исследование слуха, а также лучевые методы исследования.
Ранняя диагностика невриномы основана на точной оценке слуха — аудиограмме. Если заболевание есть, то исследование показывает ассиметричную нейросенсорную потерю слуха, при этом одновременно наблюдается диспропорциональное снижение разборчивости речи.
Так как вестибулярные шванномы постепенно приводят к вестибулярным нарушениям со стороны поражённого уха, пациенты редко жалуются на головокружения и чаще испытывают ощущение шаткости при походке. Уловить эти нарушения может самый чувствительный аудиометрический тест — аудиометрия по слуховым вызванным потенциалам (КСВП). С его помощью исследуют ответную реакцию ствола головного мозга на звуковой раздражитель. При обнаружении отклонений прибегают к визуальным методам исследования.
Оптимальными способами визуальной диагностики являются компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) головного мозга. Эти исследования принято проводить с контрастным усилением, так как оно позволяет обнаружить даже небольшие новообразования [14] . Иногда опухоль обнаруживается случайно — при проведении КТ или МРТ головного мозга по другому поводу [13] . По результатам этих исследований можно поставить точный диагноз, выявить локализацию опухоли, её размеры, структуру, отношение к окружающим тканям задней черепной ямки, спланировать тактику хирургического или радиологического лечения [12] .
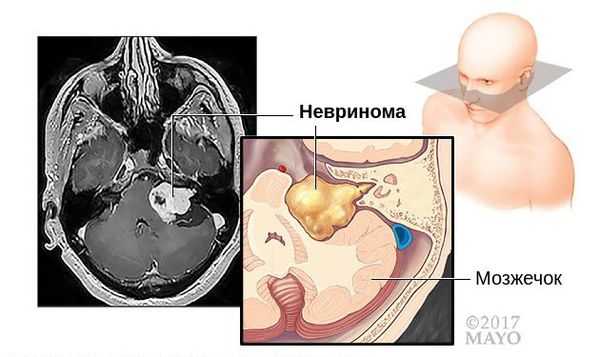
Дифференциальная диагностика невриномы проводится с заболеваниями, которые могут привести к односторонней нейросенсорной потере слуха:
- менингиомой задней черепной ямки;
- холестеатомой пирамиды височной кости;
- внутричерепными метастазами;
- арахноидальной кисты и других опухолей этой локализации.
Лечение невриномы слухового нерва
Алгоритм лечения невриномы зависит от её стадии, симптомов, общего состояния здоровья и возраста пациента. Если опухоль небольшая и не беспокоит больного, то врачи придерживаются выжидательной тактики, так как долгое время они могут не расти или вовсе регрессировать (редко) [17] . При этом необходимо минимум раз в год проходить МРТ, чтобы наблюдать за течением болезни. В других случаях избавиться от невриномы можно либо с помощью хирургического удаления, либо посредством облучения.
Показания к операции:
- молодой возраст больного;
- быстрый рост опухоли или продолженный рост опухоли после её облучения;
- прогрессирующая неврологическая симптоматика — возникновение симптомов сдавления ствола головного мозга, гидроцефалии, бульбарного синдрома [2][6] .
Цель оперативного лечения — радикальное (полное) удаление опухоли с сохранением жизненно важных структур. Может проводиться из различных доступов: через вскрытый сосцевидный отросток (выполняется чаще всего), за ухом и над ухом. Если операция прошла успешно, пациент находится в клинике под наблюдением ещё 5-7 дней. Швы с операционной раны снимают на 10-15 сутки. Существенных ограничений по образу жизни после восстановительного периода нет. Спустя некоторое время после операции рекомендуется пройти курс лучевой терапии, чтобы предотвратить продолженный рост остатков клеток опухоли.
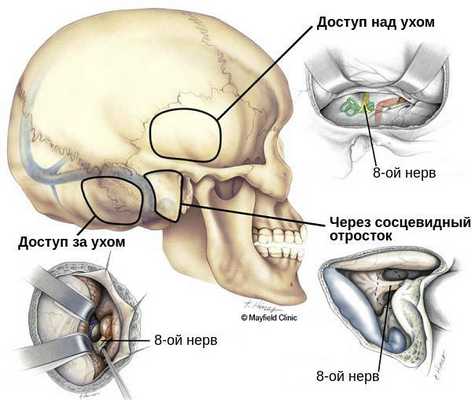
Если имеются противопоказания к традиционному хирургическому вмешательству, следует рассматривать методы лучевой терапии:
- стереотаксическую радиохирургию — удаление опухоли гамма-ножом (альтернатива стандартному оперативному лечению);
- фракционную стереотаксическую радиохирургию (FSRS) — радиотерапию [17] .
Цель лучевой терапии — приостановить дальнейший рост опухоли. Она показана:
- пожилым пациентам;
- людям с наличием сопутствующих заболеваний;
- после частичного удаления опухоли для облучения её остатков.
Максимальная доза лучевой терапии — не более 34 Гр, минимальная — 12 Гр [17] . В итоге такого лечения опухоль чаще всего уменьшается, но иногда она не меняется в размерах и продолжает расти. Поэтому радиотерапию рекомендуют как дополнительный метод лечения после традиционного хирургического лечения.
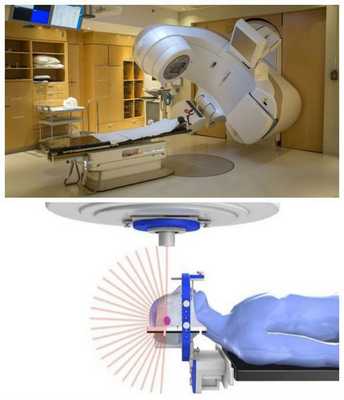
Правильный выбор метода лечения позволяет снизить показатель летальности при невриномах слухового нерва до 1 % [3] [5] [11] . Основными причинами повторного появления опухоли являются нерадикальность операции и отсутствие лучевой терапии в послеоперационном периоде.
Прогноз. Профилактика
Прогноз при невриноме слухового нерва благоприятный, особенно если удаётся выявить опухоль на ранних стадиях. Практически у всех пациентов невриному можно удалить полностью. В таких случаях рецидивы практически не встречаются, а отдалённые осложнения (например, гидроцефалия) развиваются редко.
Наиболее частой и сложной проблемой, с которой сталкиваются пациенты после лечения невриномы, является паралич лицевого нерва. Так как он развивается более чем у 50 % пациентов, разработан целый комплекс методов, которые позволяют восстановить работоспособность мышц лица. Операция на лицевом нерве после удаления вестибулярной шванномы создаёт условия для того, чтобы восстановить нейромышечную проводимость, миодинамическое равновесие и функциональную целостность зон лица. Причём раннее и поэтапное хирургическое лечение лицевого нерва позволяет избежать мышечной атрофии и ускорить выздоровление пациентов с грубой и стойкой асимметрией лица [11] .
Невриномы слухового нерва чаще развиваются спорадически, т. е. случайно в результате трансформации шванновских клеток в слуховом нерве. Поэтому методов первичной профилактики (вакцины) не существует. Однако если среди родственников были люди с нейрофиброматозом II типа или опухолью слухового нерва, человеку нужно быть настороженным в отношении невриномы слухового нерва и периодически выполнять МРТ головного мозга, особенно если появились жалобы на прогрессирующее снижение слуха.
Читайте также:
