Дерматофилиаз глаз. Диагностика и лечение
Добавил пользователь Алексей Ф. Обновлено: 22.01.2026
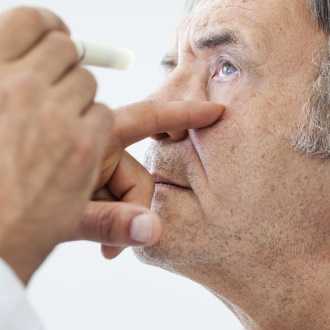
Дирофиляриоз глаз - это редкая гельминтозная инфекция, для которой характерно хроническое течение и медленное развитие. В офтальмологии может встречаться поражение конъюнктивы, век и тканей орбиты.
О заболевании
Дирофиляриоз редко встречается. Как правило, эндемичным регионом является юг. Однако и на других территориях возможны спорадические случаи.
После заражения может пройти несколько лет до тех пор, как появятся клинические симптомы заболевания. В одних случаях они ограничены только зрительными жалобами, в других - появляются видимые изменения.
Человек заражается при укусе комара, в ротовой полости которого содержатся дирофилярии. Комары заражаются, кусая кошек и собак, в теле которых могут находиться дирофиляриозные личинки.
Диагностика заболевания основывается на клинической симптоматике, в т.ч. на обнаружении подвижного образования под кожей, а также на данных объективного исследования глазного яблока. Подтвердить причинную роль дирофилярий помогают лабораторные анализы.
Радикальным методом лечения является хирургическое вмешательство, когда удаляется свернутый в клубок червь. Иногда могут назначаться противогельминтные препараты.
Виды дирофиляриоза
С учетом локализации гельминтов офтальмологи выделяют следующие виды дирофиляриоза:
- дирофиляриозное поражение конъюнктивальной оболочки;
- дирофиляриозное поражение орбитальной области;
- дирофиляриозное поражение век.
Симптомы дирофиляриоза
Симптомы дирофиляриоза в первую очередь определяются токсико-аллергической реакцией тканей в ответ на присутствие этого гельминта. Для дирофиляриоза возможны следующие глазные симптомы:
- отечность и гиперемия век;
- выпячивание глазного яблока;
- спастическое сокращение круговой мышцы век;
- повышенное образование слезы;
- зудящие ощущения;
- боль в глазном яблоке в покое и при ощупывании.
Симптомы не являются специфичными для заболевания. Поэтому при их появлении стоит обратиться к офтальмологу. Врач проведет объективный осмотр и составит план дополнительной диагностики, которая направлена на установление окончательного диагноза.
Признаки дирофиляриоза помимо глазных симптомов включают в себя формирование гранулемы под кожей, ощущение инородного тела в глазу, возможно выявление шевеления в патологическом очаге. Конъюнктива обычно гиперемирована. Дирофиллярии также могут мигрировать под кожей и под слизистыми оболочками. Поэтому человек замечает, что сначала гранулема находилась в одной области, а через некоторое время эта зона не вызывает подозрения, при этом патологический очаг появляется в другом месте.
Причины
Возбудителем дирофиляриоза век является гельминт рода Дирофилярия. В России обычно встречается только тип Dirofilaria repens. Крайне редко могут играть роль такие нематоды, как Dirofilaria immitis, Dirofilaria tennis. В последнее время отмечается рост случаев заболевания. Данный факт ученые связывают с тем, что увеличивается популяция бездомных собак, которые активно перемещаются в разных регионах. В связи с этим каждый человек, который отмечает у себя появление глазных симптомов, должен как можно раньше посетить офтальмолога. Чем раньше будет выявлено заболевание, тем меньшие размеры окажутся у гельминта, и тем быстрее наступит выздоровление.
Дефинитивные облигатные хозяева для гельминта - дикие и домашние представители семейств псовых и кошачьих. Промежуточный хозяин, который и служит переносчиком - это комары различных родов (Aedes, Culex, Anopheles). Окончательный хозяин заражается трансмиссивным путем, то есть при непосредственном проникновении возбудителя в кровоток.
После заражения личинки сначала локализуются подкожно-жировой клетчатке, откуда, превратившись в неполовозрелых особей, перемещаются в легкие и сердце. А через 5-6 месяцев они превращаются в половозрелых особей, которые в организме окончательного хозяина живут 2,5-7 лет и рождают личинок микрофилярий в кровь зараженного животного. Микрофилярии близки по величине к размерам эритроцита и могут циркулировать в организме дефинитивного хозяина до 3 лет. В тело комара возбудители попадают после кровососания, мигрируя в кишечник, где личинки растут и дважды линяют. В последующем ставшими заразными они располагаются в ротовом аппарате комара, поэтому при укусе он заражает окончательного хозяина. Таким образом цикл развития замыкается. В организме насекомого паразит развивается примерно 16 суток. Развитие возбудителя в организме кровососущего насекомого возможно при температуре среды более 14ºС. Стоит помнить, что в квартирных условиях при наличии инвазированных собак, кошек возможно круглогодичное заражение комарами рода Culex, которые обитают в подвалах и способны проникать в квартиры через систему вентиляции.
Человек для дирофилярий является «незапланированной жертвой», при этом цикл развития самого паразита прерывается. Заражение, как правило, происходит на природе: это пребывание на даче, занятие охотой, участие в туристических походах. Пик инвазии приходится на лето, начинаясь в конце мая и заканчивая в сентябре. В этот период наиболее высока вероятность подвергнуться укусам промежуточных хозяев. Стоит учитывать, что в организме человека могут прижиться лишь определенные формы возбудителя. Обычно это 1 неоплодотворенная самка, которая проникает под конъюнктиву или в ткани орбиты. Реже червь может находится в стекловидном теле. Вокруг гельминта образуется капсула с тонкими стенками. Личинок микрофилярий в организме человека не образуется, человек является биологическим тупиком в цикле развития нематоды.
Псевдоэксфолиативный синдром
Псевдоэксфолиативный синдром - это увеопатия, характеризующаяся отложением амилоидоподобного вещества на структурах переднего сегмента глазного яблока. Клиническая картина представлена зрительной дисфункцией, появлением «помутнений» и «радужных кругов» перед глазами, затуманиванием зрения. Диагностика базируется на проведении ультразвуковой биомикроскопии, классической биомикроскопии с использованием щелевой лампы, скополаминовой пробы, УЗИ, визометрии, тонометрии, периметрии, гониоскопии. Консервативная терапия основывается на применении антиоксидантов, антигипоксантов, гипотензивных средств, витаминов группы В, А, Е.
Общие сведения
Псевдоэксфолиативный синдром впервые был описан финским ученым Дж. Линдбергом в 1917 году. Наблюдается взаимосвязь между развитием болезни и возрастом пациента. В 50-59 лет вероятность возникновения патологии составляет 1-2,5%, в 60-69 лет - 30%, после 70 лет - 42%. Согласно статистическим данным, заболевание диагностируется у 30% россиян старше 50 лет. Риск развития глаукомы у пациентов с псевдоэксфолиативным синдромом равен 64,6%. Патология чаще встречается среди представителей женского пола, однако тяжелее протекает у мужчин. Распространенность наиболее высока в серверных регионах.
Причины псевдоэксфолиативного синдрома
Этиология заболевания до конца не изучена. Продолжительное время ученые связывали развитие патологии с изменениями строения эпителия хрусталика, однако диагностика псевдоэксфолиативного синдрома после интракапсулярной экстракции катаракты позволила опровергнуть эту теорию. На сегодняшний день ведущая роль в развитии болезни отводится действию следующих факторов:
- Ультрафиолетовоеизлучение. Воздействие ультрафиолета индуцирует свободно-радикальное окисление и деструкцию клеточной мембраны. Это влечет за собой атрофию с типичными признаками эксфолиации.
- Травматическое повреждение. Травмы глазного яблока приводят к локальным изменениям, которые у генетически скомпрометированных лиц являются пусковым фактором пигментной дисперсии.
- Внутриорбитальные инфекции. Многие авторы полагают, что поражение глаз обусловлено повышенной проницаемостью гематоофтальмического барьера (ГОБ). Способностью проникать через ГОБ наделена токсоплазма, вирус опоясывающего герпеса и краснухи.
- Нарушения иммунного статуса. В пользу этой этиологической теории псевдоэксфолиативного синдрома свидетельствует обнаружение в слезной жидкости повышенной концентрации интерлейкинов 6, 10, иммуноглобулина класса А и лактоферрина.
- Генетическаяпредрасположенность. У некоторых пациентов можно установить нарушение экспрессии генов в ядре и митохондриях. Встречаемость ПЭС среди родственников гораздо выше, чем в популяции. Прослеживается аутосомно-доминантный тип наследования.
Ученые полагают, что развитию болезни способствует курение и аутоиммунные патологии. Удается проследить взаимосвязь между возникновением ПЭС и артериальной гипертензией, атеросклерозом, аневризмой аорты в анамнезе. Некоторые исследователи полагают, что данные изменения - это следствие системной васкулопатии, поэтому пациенты с ПЭС часто страдают кардиоваскулярными заболеваниями.
Патогенез
Ключевая роль в механизме развития заболевания отводится образованию и депонированию аномального экстрацеллюлярного микрофибриллярного белка на поверхности передней капсулы хрусталика и радужки, цилиарном теле, цинновых связках, по краю зрачкового отверстия. Реже визуализируются патологические отложения в области передней камеры. Установлено, что белок относится к амилоидоподобной субстанции, за его синтез отвечает пигментный эпителий и меланоциты радужки. Согласно современным представлениям, патогенез ПЭС связан с нарушением эпителио-мезенхимальных взаимоотношений в структурах глазного яблока. Проникновение белковых структур в толщу его оболочек ведет к их дистрофическому перерождению.
Псевдоэксфолиативный синдром принято рассматривать как системное нарушение метаболизма соединительной ткани. Подтверждением этой теории является обнаружение специфических отложений в паренхиматозных органах (печень, почки, сердце, головной мозг) и кожных покровах. Учеными было обнаружено 14 антигенов главного комплекса гистосовместимости (HLA) при наследуемой форме патологии. Прогрессирование заболевания ведет к атрофии пигментной каймы, что проявляется выраженной дисперсией пигмента. Пигментоциты удается обнаружить в УПК и на радужной оболочке. Из-за поражения дренажной сети нарушается отток водянистой влаги с последующим повышением внутриглазного давления.
Классификация
В офтальмологии различают генетически детерминированный и иммуноопосредованный вариант развития. Вне зависимости от патогенеза болезнь всегда возникает в преклонном возрасте. По выраженности дистрофических изменений выделяют следующие степени псевдоэксфолиативного синдрома:
- I - проявляется легкой атрофией радужки. Патологический процесс не распространяется за пределы корня оболочки. Кайма зрачка имеет неравномерную структуру. В области хрусталика определяется маловыраженное наслоение амилоида.
- II - атрофия стромы радужной оболочки умеренная. На поверхности радужки и в зоне УПК выявляются выраженные псевдоэксфолиативные и пигментные отложения.
- III - атрофические изменения резко выражены. Пигментная кайма имеет вид «целлофановой пленки», что обусловлено дисперсией пигмента. Поражение связочного аппарата вызывает подвывих, реже - вывих хрусталика.
Клиническая классификация базируется на результатах ультразвуковой биомикроскопии. Различают следующие стадии патологического процесса:
- I - признаки поражения соответствуют псевдоэксфолиативному синдрому. Удается визуализировать точечные включения в передних отделах глаз.
- II - к вышеописанным изменениям присоединяются начальные признаки повреждения цинновой связки в виде чередования зон истончения с утолщением. Длина волокон разная.
- III - аномальные включения становятся более плотными, провоцируют разрушение связочного аппарата.
- IV - включения объединяются в большие конгломераты, которые приводят к увеличению продольной оси глазного яблока за счет удлинения переднего сегмента.
Симптомы псевдоэксфолиативного синдрома
Для заболевания характерно длительное бессимптомное течение. Вначале поражается один глаз (зачастую левый). Вовлечение второго глазного яблока, как правило, наблюдается спустя 5-10 лет после развития первых симптомов. Жалобы обычно возникают уже после массивного отложения амилоида. Пациенты отмечают появление «помутнений» перед глазами. При взгляде на источник света появляются специфические «радужные круги». Снижение остроты зрения обусловлено поражением хрусталика, повышением ВГД и атрофией сфинктера радужки. Нарушается аккомодационная способность, в дальнейшем расстройства аккомодации сопровождаются затуманиванием зрения, нарушением рефракции. Болевой синдром появляется только при повреждении связочного аппарата.
Заболевание очень медленно прогрессирует. Пациенты часто игнорируют клинические проявления. Помимо жалоб со стороны глаз при отложении белка во внутренних органах возникают симптомы их поражения. При депонировании амилоида в печени отмечается чувство тяжести в правом подреберье, реже - желтушность кожных покровов. Боль в пояснице по типу почечной колики, нарушения мочеиспускания являются типичными признаками скопления белковых масс в паренхиме почек. При распространении патологического процесса в толщу миокарда наблюдается ощущение сдавливания за грудиной, покалывание в области сердца. Доказано, что ПЭС широко распространена среди больных сенильной деменцией, когнитивными расстройствами, хронической ишемией головного мозга, болезнью Альцгеймера.
Осложнения
Отложение белка в толще хрусталиковых масс провоцирует развитие вторичной катаракты ядерного типа, которая зачастую сопровождается слабостью связочного аппарата. Это приводит к тому, что более чем у половины больных катарактой возникает сублюксация, реже - люксация хрусталика. В большинстве случаев патология осложняется офтальмогипертензией. Поражение трабекулярной сети ведет к возникновению псевдоэксфолиативной открытоугольной глаукомы, а с прогрессированием заболевания - к глаукомной оптической нейропатии или слепоте. Поражение мейбомиевых желез становится причиной ксерофтальмии.
Диагностика
Постановка диагноза на доклинической стадии затруднена. Выявить первые признаки можно только при помощи ультразвуковой биомикроскопии. Специфические методы диагностики включают:
- Биомикроскопию глаза. Позволяет визуализировать скопления белого или сероватого оттенка, напоминающи е хлопья на поверхности оболочек переднего отдела органа зрения. Хаотичные скопления пигмента могут формировать веретено Крукенберга. Псевдоэксфолиации по структуре похожи на воспалительные преципитаты.
- Гониоскопию. В передней камере определяются множественные включения, которые на поздних стадиях формируют крупные конгломераты. При нарушении проницаемости гематоофтальмического барьера в водянистой влаге обнаруживается взвесь крови. Объем камеры не изменен.
- Бесконтактную тонометрию. Характерно повышение внутриглазного давления, которое при вторичной глаукоме тяжело поддается снижению медикаментозным путем. При поражении дренажной системы дополнительно проводится электронная тонография.
- УЗИ глаза. При использовании ультразвуковой диагностики можно обнаружить разрыв цинновой связки с возникновением сферофакии. Из-за массивных отложений белка нарушается соотношение размеров переднего и заднего сегментов. Методика также применяется с целью обследования заднего сегмента глаз при снижении прозрачности оптических сред.
- Ультразвуковую биомикроскопию. Дает возможность выявить мелкоточечные включения слабой акустической плотности на оболочках глаза, разницу длины и лизис отдельных волокон цинновой связки.
- Скопаламиновую пробу. При 1 степени при проведении пробы зрачковое отверстие расширяется до 5 мм, при 2 - до 3,5-4 мм. При 3 степени патологии реакция зрачка отсутствует.
- Визометрию. Зрительная дисфункция наблюдается при помутнении оптических сред или вторичной глаукоме. При тяжелом течении острота зрения снижается вплоть до светоощущения.
- Периметрию. Определяется концентрическое сужение поля зрения. В ряде случаев удается диагностировать выпадение отдельных участков из зрительных полей, скотомы.
Пациентам с данной патологией в анамнезе показана консультация невропатолога, ревматолога, кардиолога, гастроэнтеролога, отоларинголога. Необходимость проведения комплексного обследования вызвана системным поражением фиброзной ткани. Часто выявление первых симптомов поражения глаза позволяет диагностировать отложения амилоида в других паренхиматозных органах.
Лечение псевдоэксфолиативного синдрома
Этиотропная терапия псевдоэксфолиативного синдрома не разработана. Цель консервативного лечения - предупредить развитие тяжелых осложнений. На ранних стадиях показано применение:
- Антиоксидантов. Используются лекарственные средства, в состав которых входит супероксиддисмутаза. СОД относится к классу металлопротеидов. Антиоксиданты вызывают разрушение активных форм кислорода, которые оказывают повреждающее влияние на ткани глаза.
- Антигипоксантов. С целью улучшения метаболизма и стимуляции процесса тканевого дыхания применяется цитохром С. Инстилляции препарата способствуют ускорению эпителизации и репарации повреждений структур передних сегментов глаз.
- Гипотензивныхсредств. Показаны при повышении внутриглазного давления, признаках офтальмогипертензии и начальных стадиях развития псевдоэксфолиативной глаукомы.
- Витаминотерапии. Доказана эффективность применения метилэтилпиридинола (структурный аналог витамина В6), который обладает фибринолитическим и антиоксидантным действием. В окислительно-восстановительных процессах также участвует витамин А (ретинола ацетат) и Е (токоферола ацетат).
При длительном течении патологии целью лечения является устранение или снижение выраженности вторичных осложнений. Медикаментозная терапия псевдоэксфолиативной глаукомы зачастую не оказывает должного эффекта. Возникает необходимость в лазерном или хирургическом вмешательстве. Наиболее целесообразно проведение ранней лазерной трабекулопластики, однако спустя 3-4 года возникают рецидивы повышения ВГД. При выборе метода удаления сублюксированного хрусталика следует отдавать предпочтение факоэмульсификации. Методикой резерва остается экстракапсулярная экстракция.
Прогноз и профилактика
Исход заболевания зависит от степени тяжести, характера поражения структур переднего отдела глаз и типа осложнений. При своевременной диагностике и лечении осложнений прогноз в отношении зрительных функций благоприятный. Возникновение вторичной глаукомы ассоциировано с резистентностью к консервативной терапии и риском необратимой потери зрения. Специфическая профилактика не разработана. Даже при ранних симптомах псевдоэксфолиативного синдрома необходима постановка на диспансерный учет у офтальмолога из-за высокой вероятности развития глаукомы. Показан регулярный контроль внутриглазного давления. Больные должны проходить комплексное офтальмологическое обследование не реже, чем два раза в год.
Дерматит век
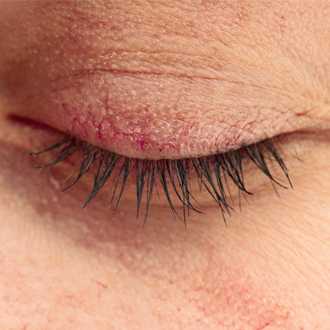
Дерматит век представляет собой воспалительное поражение кожи.
Дерматит век может быть вызван различными факторами. Чаше всего встречаются аллергические формы, которые обусловлены повышенной чувствительностью кожи к веществам уходовой или декоративной косметики. Реже дерматит развивается в ответ на избыточную инсоляцию или как проявление себореи, или инфекционного процесса.
Симптомы дерматита век обычно включают в себя:
- неприятное ощущение зуда и жжения;
- различные высыпания - папулы, пузырьки, корки;
- покраснение и отечность воспаленной зоны.
Для установления диагноза обычно проводится визуальный осмотр кожи и биомикроскопия. Однако, чтобы выявить причины дерматита век, офтальмолог может назначить лабораторные исследования. В одних случаях достаточно общеклинического анализа крови, в других - требуется аллергоскрининг. В сомнительных ситуациях может быть показана биопсия с гистологическим исследованием для исключения злокачественного процесса.
Лечение дерматита глаз направлено на купирование воспалительного процесса. Для достижения этой задачи используются нестероидные средства или кортикостероиды, которые блокируют определенные реакции воспаления. Одновременно с патогенетической целью проводится и этиотропная терапия, направленная на устранение причин заболевания. Так, при инфекционном дерматите используются антибиотики, при атопическом (аллергическом) - антигистаминные средства в сочетании с элиминацией аллергена и т.д.
Дерматит век может быть:
- изолированным, когда в патологический процесс вовлекается только кожа верхнего и/или нижнего века;
- сочетанным, когда поражается не только кожа век, но и кожные покровы другой локализации, особенно часто это периоральная зона (кожа вокруг рта вместе с носогубным треугольником).
По этиологии выделяют следующие варианты заболевания:
- аллергический (атопический) - связан с индивидуальной реакцией гиперчувствительности организма к определенным веществам (аллергенам);
- контактный - обусловлен попаданием агрессивных веществ на кожу века, при этом они запускают воспалительные реакции;
- инфекционный - в роли причинного агента выступают микроорганизмы (в этой группе выделяют бактериальный, вирусный, грибковый дерматит);
- себорейный - обусловлен нарушением нейроэндокринной регуляции и повышенным образованием кожного сала, часто встречается у молодых людей.
Симптомы дерматита век
Как выглядит дерматит век, во многом зависит от природы патологического агента.
- При герпесвирусном заболевании сначала появляется зуд и жжение, кожа может несколько краснеть. Через некоторое время на этом месте появляются пузырьки, заполненные прозрачным содержимым. Вскоре они вскрываются и подсыхают. Корочки отпадают через несколько дней, не оставляя после себя следа. Первичный эпизод герпетической инфекции может протекать с повышением температуры тела, при этом высыпания часто локализуются не только на веках, но и в периоральной зоне. , связанный с вирусом опоясывающего герпеса, протекает, как и герпетический. Однако высыпания характеризуются выраженным болевым синдромом. проявляется выраженной отечностью и покраснением кожи век, при этом часто отмечается интенсивный зуд. На воспаленной коже появляются мелкие папулы (прыщики). Кожа век имеет особое строение, поэтому воспалительный отек всегда диффузный и ярко выраженный, из-за чего пациенту тяжело открыть глаза (глазные щели становятся узкими). Аллергические реакции замедленного типа часто сопровождаются развитием хронического воспаления, для которого характерно шелушение и утолщение кожного покрова.
- Себорейный дерматит век характеризуется повышенной сальностью кожного покрова и зудом. На коже появляется мелкопластинчатое шелушение. Ресницы склеиваются кожным салом, вследствие чего усиленно выпадают. Патологический процесс из пальпебральной зоны быстро распространяется на скулы, лобную область, носовые крылья и волосистую часть головы.
Причины дерматита век
Причинными факторами дерматита век могут быть следующие:
- вирусы - вирус простого и опоясывающего герпеса, вирус кори, ветряной оспы, скарлатины;
- бактерии - стафилококки и стрептококки (обычно присоединяются вторично);
- аллергены - некоторые лекарственные препараты, растительная пыльца, шерсть домашних животных, пылевые клещи, косметические средства;
- физическая энергия - слишком низкие температуры, продолжительное ультрафиолетовое облучение;
- химически агрессивные вещества - средства бытовой химии, кислотные и щелочные растворы, ядовитые вещества;
- повышенная активность сальных желез, к которой предрасполагает гормональный дисбаланс, вегетативная дисфункция, заболевания пищеварительной системы.
В случае себорейного дерматита сальные железы вырабатывают много кожного сала, которое является питательной средой для Propionobacterium acnes. Эти микроорганизмы расщепляют триглицериды до жирных кислот, некоторые из которых обладают раздражающим действием, что приводит к развитию дерматита.
Получить консультацию
Если у Вас наблюдаются подобные симптомы, советуем записаться на прием к врачу. Своевременная консультация предупредит негативные последствия для вашего здоровья.
Узнать подробности о заболевании, цены на лечение и записаться на консультацию к специалисту Вы можете по телефону:
Эндотелиальная дистрофия роговицы ( Дистрофия Фукса )
Эндотелиальная дистрофия роговицы - это заболевание органа зрения, причиной которого является отмирание клеток заднего эпителия роговой оболочки. Клинически проявляется снижением остроты зрения в утреннее время, фотофобией, гиперемией, повышенным слезотечением, болевым синдромом. Диагностика эндотелиальной дистрофии роговицы включает в себя проведение наружного осмотра, конфокальной микроскопии, биомикроскопии, пахиметрии, визометрии. Симптоматическая терапия основывается на инстилляции гипертонических солевых растворов. Хирургическая тактика - проведение сквозной или послойной кератопластики.
МКБ-10
Эндотелиальная дистрофия роговицы, или дистрофия Фукса - это патологическое состояние в офтальмологии, характеризующееся нарушением трофики с последующей дегенерацией роговой оболочки. Первое описание первичной эндотелиальной дистрофии роговицы было представлено австрийским ученым Э. Фуксом в начале ХХ века. Исследователь считал, что патология развивается вследствие нарушения регионального кровоснабжения или иннервации, гормонального дисбаланса.
Заболевание может быть первичным или вторичным, ранним или поздним. При раннем варианте эндотелиальную дистрофию роговицы можно диагностировать у детей до 3 лет. Клиника позднего варианта наблюдается у пациентов в возрасте старше 45 лет. Ранние дистрофии с одинаковой частотой встречаются среди мужчин и женщин. Поздняя форма заболевания более распространена среди лиц женского пола.
Первичная эндотелиальная дистрофия роговицы - это генетически детерминированное заболевание. Установлен аутосомно-доминантный тип наследования с неполной или высокой пенетрантностью. При ранней форме возникает мутация гена COL8A2, при поздней - SLC4A11 или ZEB1. В то же время, у 50% пациентов болезнь развивается спорадически.
Реже триггером выступает дисфункция митохондрий эндотелиоцитов, что ведет к их недостаточности. Патологический процесс локализируется во внутреннем слое роговой оболочки, эндотелиоциты которого в последующем не могут делиться и регенерировать. Этиологической роли факторов внешней среды и системных патологий в развитии данного заболевания не установлено.
Наиболее распространённая причина возникновение вторичной эндотелиальной дистрофии роговицы - травматическое повреждение органа зрения. Ятрогенный фактор реализуется при проведении оперативного вмешательства. Хроническое течение кератита при отсутствии своевременного лечения способствует дегенерации роговой оболочки, что обусловлено повреждением эндотелия. При данной патологии воспалительный процесс является не этиологическим фактором, а лишь предпосылкой к развитию эндотелиальной дистрофии роговицы у генетически скомпрометированных лиц.
Компенсаторная гиперфункция эндотелиоцитов при прогрессировании заболевания не может обеспечить выведение избытка жидкости и поддержание прозрачности роговицы. Это связано с пропотеванием водянистой влаги передней камеры глаза через дефекты в эндотелии в строму роговой оболочки. Выраженная отечность приводит к эндотелиальной дистрофии роговицы. При распространении отека на наружный слой возникает буллезная кератопатия. Проведение оперативных вмешательств на роговой оболочке в связи с выраженным истончением эндотелия часто осложняется отеком, что усугубляет деструктивные процессы.
Симптомы дистрофии роговицы
С клинической точки зрения выделяют первичную и вторичную формы дистрофии Фукса. Первичное поражение роговой оболочки является врождённым. Первые проявления ранней дистрофии обнаруживаются при рождении или в раннем детском возрасте, но этот тип заболевания встречается крайне редко. Поздний вариант первичной эндотелиальной дистрофии Фукса чаще развивается у лиц после 45 лет. Для данного типа патологии характерно бинокулярное, но асимметричное течение. Вторичная дистрофия - это приобретённое заболевание, при котором наблюдается монокулярное поражение.
В зависимости от степени тяжести патологии клиника эндотелиальной дистрофии роговицы может характеризоваться латентным течением или проявлениями буллезной кератопатии. Симптомы заболевания медленно прогрессируют, поэтому с момента появления первых признаков до формирования развернутой клинической картины может пройти около 20 лет.
Первая стадия
На первой стадии эндотелиальной дистрофии роговицы морфологические изменения затрагивают только центральные отделы роговой оболочки. При этом появляются специфические коллагеновые образования (гутты) каплевидной, бородавчатой и грибовидной формы. Жалобы отсутствуют. Единственным симптомом заболевания является незначительное снижение остроты зрения в утреннее время.
Вторая стадия
На второй стадии количество эндотелиоцитов уменьшается, развивается отек роговицы, появляются одиночные буллы. Ощущение инородного тела сменяется снижением чувствительности роговой оболочки из-за дегенерации нервных окончаний. Специфические симптомы этой стадии эндотелиальной дистрофии роговицы представлены фотофобией, гиперемией глаз, снижением остроты зрения в утреннее время с последующим восстановлением к вечеру. Это связано с тем, что из-за сомкнутых глаз в период сна должным образом не осуществляется испарение влаги с роговой оболочки, что приводит к депонированию жидкости. Днем испарение влаги способствует уменьшению отечности и возобновлению зрительных функций.
Длительное течение эндотелиальной дистрофии роговицы становится причиной медленно прогрессирующего снижения остроты зрения. При распространении патологического процесса на эпителиальный слой и появлении буллезных изменений пациенты предъявляют жалобы на ощущение инородного тела и повышенную слезоточивость. Болевой синдром, сопровождающийся сильным дискомфортом в области глазницы, развивается при разрыве булл у больных с буллезной кератопатией.
Третья стадия
На третьей стадии вдоль эпителия базальной мембраны синтезируется фиброзная ткань с последующим формированием паннуса. Общее состояние при этом несколько улучшается, но прогрессирование эндотелиальной дистрофии роговицы в дальнейшем приводит к появлению эпителиальных эрозий, язв микробного генеза и васкуляризации центральной части роговой оболочки.
Диагностика эндотелиальной дистрофии роговицы основывается на результатах наружного осмотра, специальных офтальмологических исследований и генодиагностики. При наружном осмотре выявляется помутнение роговицы, возможна конъюнктивальная инъекция сосудов. Решающие данные получают с помощью:
- Конфокальной микроскопии роговицы. Является золотым стандартом в диагностике данной патологии. Помимо детального изображения эндотелия, измеряется плотность клеток и их средний диаметр на единицу площади. Степень снижения размера и количества клеточных элементов при эндотелиальной дистрофии роговицы зависит от тяжести заболевания. Также выявляются специфические образования (гутты) в виде капель темного цвета с яркой центральной частью и околоклеточной локализацией. В начале развития диметр гутты меньше эндотелиоцита, в последующем они сливаются и имеют вид крупных пятен.
- Биомикроскопии. При проведении биомикроскопии со щелевой лампой визуализируются локальные зоны дегенерации эндотелиального слоя, отечность. При распространении отека на наружный слой определяются специфические буллы на поверхности роговой оболочки, что указывает на развитие буллезной кератопатии.
- Пахиметрии. Методом пахиметрии определяют толщину роговой оболочки. Дегенеративные процессы при эндотелиальной дистрофии роговицы приводят к ее истончению (менее 0,49 мм), но при появлении отека ее толщина может превышать референсные значения (0,56 мм).
- Визометрии. При помощи визометрии измеряется степень снижения остроты зрения. Для получения достоверного результата и косвенного определения степени выраженности отека пациентам с эндотелиальной дистрофией роговицы рекомендовано проводить исследования в утреннее и вечернее время.
Лечение эндотелиальной дистрофии роговицы
Консервативная тактика
Симптоматическая терапия эндотелиальной дистрофии роговицы включает в себя проведение инстилляций гипертонических солевых растворов с целью уменьшения отечности. Выведение с роговой оболочки избыточной жидкости улучшает остроту зрения. С целью купирования болевого синдрома показан пероральный прием анальгетиков или их инстилляция. Для коррекции остроты зрения можно использовать только мягкие контактные линзы или очки. Также в лечении эндотелиальной дистрофии роговицы применяется роговичный кросс-линкинг, в основе которого лежит фотополимеризация волокон стромы при помощи совместного воздействия фотосенсибилизирующего препарата и ультрафиолетового излучения.
Хирургическое лечение
Тяжелое течение эндотелиальной дистрофии роговицы, сопровождающееся выраженным снижением остроты зрения, сильным истончением роговицы по данным пахиметрии и низкой плотностью клеток на единицу площади по результатам конфокальной микроскопии, является показанием к проведению кератопластики. Сквозной вариант хирургического вмешательства показан при тотальном дистрофическом процессе. Послойная кератопластика рекомендована пациентам в случае повреждения одного или нескольких слоев роговой оболочки. При этом зачастую выполняется трансплантация десцеметовой мембраны совместно с эндотелием.
Прогноз при ранней диагностике и лечении для жизни и трудоспособности благоприятный. Отсутствие терапии может привести к полной утрате зрения и инвалидизации пациента. Специфических мер по профилактике эндотелиальной дистрофии роговицы не разработано, поскольку заболевание генетически детерминированное. Неспецифические превентивные меры сводятся к предупреждению травматических повреждений у генетически скомпрометированных лиц, скринингу у новорожденных, своевременной диагностике и лечению офтальмологической патологии. Всем пациентам с установленным диагнозом эндотелиальная дистрофия роговицы необходимо 2 раза в год проходить обследование у офтальмолога.
Дирофиляриоз глаз
Дирофиляриоз глаз - заболевание органа зрения, вызванное паразитами рода Dirofilaria. Сопровождается формированием гранулем или узелков, содержащих гельминтов, в подкожной клетчатке век или структурах глазного яблока. Клиника зависит от места локализации возбудителя. Общие проявления, характерные для всех форм: боль, зуд, ощущение шевеления в глазу. Диагностика основывается на данных анамнеза, осмотра, лабораторных (ОАК, ИФА, ПЦР), инструментальных и паразитологических методов исследований. Хирургическое лечение сводится к удалению гранулем. Параллельно с противогельминтной терапией показан прием НПВС, глюкокортикоидов и антигистаминных средств.
Дирофиляриоз глаз - это гельминтоз, который развивается при инвазии личинки нитевидной нематоды в структуры глазного яблока и характеризуется преимущественно хроническим течением. Первым дирофиляриоз описал португалец Лузитано Амато в 1566 году после выделения дирофилярий из глаза трехлетнего ребенка. Детальным изучением патологии начали заниматься после 1930 года в гельминтологической школе СССР. Согласно статистическим данным, европейцы более подвержены риску заражения, чем афроамериканцы. Заболевание обычно диагностируют у людей средней возрастной категории. Dirofilaria immitis в 2 раза чаще выявляют у представителей мужского пола, Dirofilaria repens, напротив, более склонна поражать женщин, что приводит к их большему инфицированию в популяции из-за широкой распространенности возбудителя. Эпидемиологически значимыми очагами инфекции являются Шри-Ланка, территории Южной и Восточной Европы, Малой Азии. В странах постсоветского пространства часто встречаются подкожные формы заболевания.
Причины дирофиляриоза глаз
Дирофиляриоз глаз развивается при заражении паразитами рода Dirofilaria, относящимися к классу круглых червей. Обычно поражение вызывают D. repens и D. immitis. Средняя длина самки D. repens составляет 145 мм, ширина - 0,4 мм. Продольный размер самца около 55 мм, поперечный - 0,4. Тело самки D. immitis достигает 300 мм, самца - 110 мм. Человек выступает в роле конечного (тупикового) хозяина червей, большинство паразитов погибает в человеческом организме, не достигнув половой зрелости. В литературе описан всего один случай попадания микрофилярий в кровеносное русло.
Инфицирование человека реализуется трансмиссивным путем при укусе комара, пораженного личиночной стадией дирофилярий. Источниками заражения для москитов являются бродячие собаки, редко - кошки. Заражение человека обычно происходит во время выполнения работ в саду и на огороде, при отдыхе возле водоема или во время путешествий. Риск инфицирования возрастает с мая по сентябрь при пребывании в местах, где находится большое количество переносчиков дирофиляриоза.
Симптомы дирофиляриоза глаз
Возбудители дирофиляриоза чаще всего локализируются в подкожной клетчатке век и конъюнктиве, в редких случаях - в структурах глазного яблока (передняя камера, склера). Дирофилярии могут распространяться в окружающие ткани (клетчатку глазницы, брови). При укусе москита формируется ограниченная зона воспаления, которая со временем приобретает плотную консистенцию. Уплотнение заполняется серозным или гнойным содержимым, макрофагами, лейкоцитами и нейтрофилами, внутри уплотнения находится паразит. Снаружи гранулемы образуется фиброзная капсула.
Поражение век сопровождается отеком, снижением подвижности, выраженным зудом и слезотечением. Пациенты предъявляют жалобы на боль при касаниях и в покое. Позже развиваются гиперемия, прогрессирующий птоз и блефароспазм. Уплотнения под кожей век могут увеличиваться в размере и менять форму. Больные обнаруживают гранулемы при самостоятельном осмотре, нанесении макияжа и т. п. Внешне проявления заболевания напоминают ангионевротический отек.
При расположении возбудителей под конъюнктивой или в глазном яблоке специфическими симптомами являются ощущение инородного тела, выпячивание глаза, патологическое шевеление под веком, в глазнице или структурах глазного яблока. При внутриконъюнктивальном расположении паразиты заметны невооруженным глазом, напоминают закрученные нитки или узелки. Их внезапное исчезновение в сочетании с изменением симптоматики говорит о проникновение в глазное яблоко. Происходит присоединение клинической картины конъюнктивита. Движения червей провоцируют жжение, выраженную боль и зуд. Слизистая оболочка глаз становится отечной, гиперемированной. При дирофиляриозе век или конъюнктивы острота зрения не снижается. Возможно незначительное повышение внутриглазного давления.
Проникая в жидкость передней камеры глаза, гельминт становится более подвижным. Со временем вокруг него образуется гранулема. Расширение патологического новообразования приводит к экзофтальму и диплопии. Расположение червей внутри глазного яблока является причиной снижения остроты зрения и ощущения «патологических движений червей», которых часто принимают за зрительные галлюцинации. Вне зависимости от места расположения дирофилярий пациенты предъявляют неспецифические жалобы на общую слабость, раздражительность, бессонницу, головную боль и головокружение.
В зависимости от локализации возбудителя на фоне основного заболевания могут развиваться воспалительные процессы (блефарит, конъюнктивит, кератит, эндофтальмит и др.). Наиболее опасное осложнение дирофиляриоза - отслоение сетчатки. Хроническое течение заболевания приводит к сенсибилизации организма, распад гранулемы при гибели гельминта или нагноении может стать причиной выраженной интоксикации и возникновения аллергической реакции. Гиперчувствительность проявляется в виде папулезных высыпаний на кожных покровах и отеках слизистых оболочек.
Диагностика дирофиляриоза глаз
Диагностика дирофиляриоза основывается на данных анамнеза, результатах лабораторных и инструментальных методов исследования. Анамнестические сведения указывают на пребывание в эндемическом регионе в период высокой активности москитов (с мая по сентябрь). При объективном осмотре век и конъюнктивы глаза часто удается визуализировать возбудителя в виде извитых ниток, расположенных подкожно или в толще слизистой оболочки. Гельминт может сохранять подвижность. При пальпации боль усиливается. Специфическая диагностика заключается в проведении иммуноферментного анализа (ИФА) и полимеразной цепной реакции (ПЦР). Подтвердить диагноз методом ИФА можно при нарастании титра IgM более чем в 4 раза, что говорит об остром или IgG - хроническом течении. ПЦР позволяет выявить ДНК возбудителя, что позволяет идентифицировать вид дирофилярий.
В общем анализе крови возможно незначительное повышение эозинофилов. В комплекс паразитологического исследования входит измерение продольного и поперечного размера и оценка зрелости половых органов дирофилярий. При отсутствии микрофиляриемии у пациента необходимо детально изучить половую систему самки на предмет выявления в ней микрофилярий. Микроскопическая диагностика позволяет обнаружить специфическую гранулему, внутри которой расположен гельминт. Особенностью гистологических срезов дирофилярий является наличие небольших «шипов» на кутикуле гельминта. Диагностика заболевания часто затруднена, идентифицировать возбудителя удается только после его извлечения из глаза.
Оптическая когерентная томография проводится для диагностики дирофиляриоза при расположении гельминтов внутри структур глазного яблока. При внутренней локализации также показано проведение ультразвукового исследования в режиме В-сканирования. Гониоскопия информативна только при расположении дирофилярий в передней камере глаза, данным методом удается выявить подвижных паразитов нитевидной формы. При осмотре у офтальмолога обязательно проведение визометрии и тонометрии, которые позволяют измерить показатели остроты зрения и внутриглазного давления. Значения ВГД и остроты зрения зависят от места расположения червей. При наружной локализации показатели находятся в пределах нормы, при внутреннем расположении паразитов острота зрения снижена, ВДГ повышено. Дифференцировать дирофиляриоз следует с поражением глаз при лоаозе, описторхозе и аскаридозе.
Лечение дирофиляриоза глаз
Лечение дирофиляриоза должно быть комбинированным. В хоре оперативного вмешательства проводится удаление гранулем и других патологических образований, в которых содержится гельминт. Накануне операции рекомендовано применение дитразина с целью снижения подвижности червей. В послеоперационном периоде назначают дезинфицирующие и противовоспалительные средства в каплях и мазях.
Медикаментозная терапия сводится к приему противогельминтных лекарственных средств. Употребление противогельминтных препаратов и распад паразитов в организме могут спровоцировать развитие аллергических реакций и интоксикации. Поэтому симптоматическое лечение включает в себя прием нестероидных противовоспалительных средств, глюкокортикоидов и антигистаминных препаратов.
Прогноз и профилактика дирофиляриоза глаз
Профилактика дирофиляриоза глаз заключается в обработке инсектицидами очагов размножения комаров и деларвации водоемов. При проживании в эндемическом регионе рекомендовано использовать репелленты с пролонгированным эффектом в виде спрея, лосьона или пудры. В случае необходимости следует носить защитную одежду и очки для глаз. Нужно своевременно обследовать домашних животных, проводить дегельминтизацию. Специфических мер по профилактике в офтальмологии не разработано.
Прогноз для жизни и трудоспособности при дирофиляриозе глаз благоприятный. Своевременная диагностика и лечение обеспечивают полное выздоровления без сопутствующего снижения остроты зрения и развития других осложнений (отслойки сетчатки, повышения ВГД).
Читайте также:
- Формы местных лекарств для лечения болезней кожи
- Когнитивные нарушения в медицинских учреждениях. Показатели распространенности деменции в Англии
- Показания для применения лицевых имплантатов в пластической хирургии лица
- УЗИ при патологии плодного яйца и его содержимого
- Синдром Вестфаля-Бернхарда (Westphal-Bernhard)
