Дифференциация болезни Крона. Эндоскопическая картина болезни Крона
Добавил пользователь Евгений Кузнецов Обновлено: 21.01.2026
Преднизолон 40-60 мг/сут,следующие недели: 60,40
15, 10 мг, затем 10 мг через день (3 мес)
Если нет улучшения
Азатиоприн 2 мг/кг/сут или 6-меркаптурин 1,5 мг/кг/сут или циклоспорин
Безусловно, изучение компонентов пиши в качестве возможной причины колита чрезвычайно интересно. Вместе с тем, эти работы не должны ограничиваться изучением роли углеводов или пищевых волокон, необходимо изучать все составляющие питания человека, включая консерванты, специи и т. д. Вероятно, с появлением монокомпонентных элементных диет появится реальная возможность проведения таких исследований.
В последние годы наибольший прогресс достигнут в изучении иммуногенетической теории происхождения болезни Крона и язвенного колита. Вирусной или бактериальной причиной можно объяснить только острое начало заболевания, а объяснение хронического течения болезни следует искать в иммунологических нарушениях.
Причем, возможные этиологические факторы, такие как вирусы, бактерии, пища, токсины и т. п„ рассматриваются как потенциальные участники патогенеза. Как триггеры они способны вызывать начало цепной реакции (схема 1).
Установлено, что имеется генетическая предрасположенность к болезни Крона и язвенному колиту, обнаруживаемая на уровне иммунной системы, слизистой оболочки кишечника. Недостаточность иммунной регуляции приводит к неконтролируемым ответам на различные внешние агенты, что в свою очередь обусловливает местное повреждение тканей и развитие локального воспаления. В дальнейшем включаются эндогенные факторы, в частности нейроэндокринная система.
Схема 1. Предполагаемая схема патогенеза ВЗТК.
Аутоиммунные заболевания, к которым относят болезнь Крона, характеризуются такими нарушениями в иммунном ответе, как неспособность закончить острое воспаление, в результате чего оно переходит в хроническое.
Сегодня известно, что способность иммунной системы регулировать воспаление генетически детерминирована.
Недавно были обнаружены связи между системой гистосовместимости HLA, язвенным колитом и болезнью Крона. Изучение в больших группах хорошо подобранных пациентов показало, что локус DR2 HLA имел высокую связь с язвенным колитом и не был связан с болезнью Крона. Напротив, болезнь Крона характеризовалась связью с гаплотипом DR1 и DRw5. Генетические отличия прослеживаются и в связи язвенного колита и болезни Крона с ANCA (антинейрофильными цитоплазматическими антителами). В ряде наблюдений было продемонстрировано, что особые формы ANCA (р-АМСА) связаны с язвенным колитом и не связаны с болезнью Крона. В противовес ANCA в слизистой больных болезнью Крона обнаружены клоны В-клеток (V 134 и V III a), не встречающиеся при язвенном колите.
Схема 2. Патогеническая модель болезни Крона.
Причем эти клетки выявляются только в активной фазе болезни Крона. Таким образом, язвенный колит и болезнь Крона имеют генетические отличия.
Иммунологические исследования свидетельствуют, что главную роль в инициации и усилении воспаления играет активация Т-клеток.
Доказано, что при болезни Крона повышено число активированных Т-лимфоцитов, особенно тех, которые выполняют цитотоксическую роль и выделяют цитокины (NK-клетки). В 1988 г. Мак Дональд обнаружил, что Т-клетки в момент максимальной продукции способны вызвать ворсинчатую атрофию и гиперплазию клеток крипт, т.е. изменения, предшествующие образованию афтозных язв. Можно предположить, что повреждение эпителиальных клеток в глубине слизистой - очень раннее изменение, характерное для болезни Крона, и задолго предшествует трансмуральному воспалению. Подтверждением патогенетической роли активации Т-лимфоцитов является тот факт, что если пациенты с болезнью Крона заболевают СПИДом, то у них наступает ремиссия гранулематозного колита.
Рисунок 1. Потенциальные точки действия иммуномодулирующих препаратов при неспецифических колитах. Бернштейн и Шанахан
Важным звеном иммунопатогенеза является снижение лимфоцитами продукции интерферона, а это спосбствует недостаточной активации макрофагов для переработки антигена. Возможен и другой механизм неконтролируемого поступления антигена, обусловленного дефектом антигениндуцированной клеточной супрессии, В норме эпителиальные клетки кишечника активируют антигенонеспецифические Т-супрессоры. При болезни Крона эпителиальные клетки стимулируют Т-хелперы.
Увеличение местной реактивности может привести к системным реакциям на нормальные антигены кишечного содержимого. Имеются примеры гуморальных реакций на бактериальные и пищевые антигены при болезни Крона. Недавно было показано, что у больных болезнью Крона наблюдается специфическая серологическая реакция к пивным дрожжам, что может быть связано с дефецитом Т-супрессоров к этому антигену. Любопытно, что макромолекулы, находящиеся в просвете кишки, перестают действовать при ее "отключении" и рецедив болезни Крона не развивается в отделах кишки, расположенных дистальнее сформированной стомы.
Наконец, большое участие в воспалении принимает эндотелий сосудов: изменение проницаемости и диффузия белков в очаг поражения, секреция эндотелиальных цитокинов, отложение комплемента в эндотелии сосудов. Сосуды оказываются интимно вовлечены в гранулемы. Окклюзия артерий в минимально измененных участках слизистой указывает на то, что эндотелий может играть раннюю первичную роль в патогенезе болезни Крона. Последовательность основных звеньев патогенеза представлена на схеме 2.
Современные данные показывают, что концепция одного общего пути патогенеза является наивной, поскольку одномоментно происходит множество перекрещивающихся реакций взаимодействия факторов повреждения и восстановления. Большинство факторов поражения (естественные киллеры, лимфокины, цитотоксические Тлимфоциты, макрофаги, нейтрофилы) опосредуют свое действие через растворимые медиаторы плазмы, клетки слизистой кишечника и содержимое кишки. К этим факторам относятся антитела, пептиды комплемента, эйкосаноиды, кинины, цитокины, эндотоксин, антагонисты рецепторов, оксиданты и антиоксиданты, биогенные аминыи др. Исследования медиаторов необходимо для лучшего понимания патогенеза и создания новой базы для патогенетической терапии.
Диагностика
Диагностика болезни Крона базируется на комплексе характерных клинических, рентгеноэндоскопических и гистологических признаков. К сожалению, мы не имеем специфического маркера воспаления, а генетические маркеры еще не покинули научных лабораторий и не прошли клинической апробации. Макроскопическими признаками болезни Крона являются очаговость и прерывистость воспаления, линейные язвы, афты, изменения слизистой по типу булыжной мостовой, дискретные язвы на фоне малоизмененной слизистой, кишечные свищи, сриктуры кишки и перианальные осложнения, микроскопические афтозные язвы, трансмуральное воспаление, язвы, трещины, эпителиодные гранулемы.
Вместе с тем результаты иммунологических исследований позволили установить гистологические признаки ранних изменений при развитии болезни Крона.
1. Скопления макрофагов и лимфоцитов (микрогранулемы), обнаруживаемые в участках малоизмененной слизистой или вблизи некротизированного эпителия. Возможно, эти изменения являются предшественниками афтозных язв. Нейтрофильной инфильтрации нет, она появляется только при наличии изъязвлений.
2. Можно наблюдать окклюзию фибрином артериол в минимально измененных участках слизистой, где нет поражения эпителия.
3. Увеличена глубина крипт и снижена высота ворсинок в непораженной тощей кишке, что косвенно свидетельствует об активации Т-лимфоцитов.
4. Отмечается диффузное увеличение плотности tgM-клеток на всем протяжении желудочно-кишечного тракта и уменьшение lgAпродуцирующих клеток. Наиболее значимыми для диагностики ранних стадий болезни Крона следует считать реакцию актививрованных Т-лимфоцитов и изменение сосудов.
Современные концепции лекарственной терапии.
Проблема проведения патогенетической терапии заключается в том, что иммунные реакции не имеют клинического выражения, а клинико-эндоскопическая симптоматика обусловлена развернутым воспалением. Гистологические изменения также обнаруживают не переклинические маркеры болезни, а поврежденные воспалением ткани. Именно эти процессы ответственны за клинические проявления и большинство терапевтических средств направлено на их ликвидацию.
Специфические мишени для терапевтического воздействия.
Если признать, что болезнь Крона вызывается факторами, содержащимися в просвете кишки (антигены?), их идентификация может привести к проведению специфической терапии. Пока антимикобактериальная терапия, к сожалению, безуспешна, хотя остаются сомнения в адекватном подборе препаратов и вопрос нельзя считать закрытым. Удаление пивных дрожжей из диеты снижало активность болезни, но имеются сведения о том, что, напротив, добавление дрожжей к диете приносило облегчение симптомов. Снижение неспецифической стимуляции достигалось назначением, элементных диет при болезни Крона тонкой кишки, однако этот эффект мог быть обусловлен удалением продуктов жира и других активных молекул.
Из антибиотиков только метронидазол оказался эффективным при лечении болезни Крона, что было доказано контролируемыми исследованиями.
Безусловно, наибольшие надежды сегдня связывают с проведением иммуномодулирующей терапии, особенно препаратами, которые подавляют Т-клеточные иммунные реакции (см. рисунок).
К сожалению, результаты такой терапии пока малоутешительны и связано это, как уже указывалось, с тем, что клинические проявления болезни Крона часто отражают действие вторичных факторов, таких как мезенхимальные реакции: иммуносупрессия не может влиять на отек и фиброз кишечной стенки. Возможно, регуляця Т-клеток в слизистой имеет свои особенности и может быть менее чувствительной к лекарствам, действующим на системном уровне, или их доставка в кишку оказывается недостаточной. Макрофаги могут быть слабо активированы и не справляться с функцией обезвреживания патологических молекул. После воздействия интерфероном эффективность имуностимуляции повышается.
Взаимодействие лейкоцитов и эндотелия сосудов может регулироваться противоспалительными и иммуносупрессивными средствами. Более специфическая терапия может быть направлена против молекул, вызывающих адгезию нейтрофилов, чтобы предупредить миграцию их во внесосудистое пространство. Гепарин может оказаться эффективным для снижения прилипания нейтрофилов к эндотерию и своим антикоагулянтным действием предупреждать окклюзию сосудов.
В заключение хотелось бы отметить, что для понимания этиологии, патогенеза и терапии болезни Крона необходимо расширить наши исследования и включить в сферу внимания внутриполостные факторы, эпителий, нервную ткань и мезенхиму, а также сосуды.
Изучение лечения не следует фокусировать только на иммунологических и воспалительных эффекторных механизмах. Больше внимания должны получить многокомпонентные лекарственные схемы, например комбинация месалазина и бутирата, циклоспорина и кортикостероидов и т. п.
Дифференциация болезни Крона. Эндоскопическая картина болезни Крона
Болезнь Крона — хроническое прогрессирующее воспалительное заболевание, характеризующееся трансмуральным гранулематозным воспалением различных отделов ЖКТ (любого его отдела), сочетающееся со многими внекишечными проявлениями [1]. Распространенность и заболеваемость составляют 10—15 и 5—10 случаев на 100 000 населения соответственно [2].
Болезнь Крона встречается примерно одинаково часто среди мужчин и женщин [1]. Период манифестации заболевания чаще приходится на возраст 15—35 лет [3]. Наибольшее распространение болезни наблюдается преимущественно в развитых странах и представляет актуальную проблему [4].
Своевременная диагностика болезни Крона очень сложна, иногда правильный диагноз устанавливается спустя 3—5 лет от начала заболевания [5]. Стенозирующее течение болезни Крона встречается у 28,8% больных [6]. По результатам исследований Е.В. Ивановой и соавт. (2011), стриктуры были выявлены в 53,3% случаев.
Как известно, чаще всего при болезни Крона вовлекается илеоцекальный переход [7]. Дифференциальная диагностика включает заболевания, для которых характерны язвенные поражения тонкой кишки: туберкулез, иерсиниоз, сальмонеллез, шигеллез, кампилобактериоз, а также энтеропатию, вызванную лекарственными препаратами, лучевую энтеропатию, новообразования. Подобное разнообразие клинических вариантов не позволяет с легкостью поставить диагноз, лишь на основе эндоскопической картины.
Сложна дифференциальная диагностика между болезнью Крона и туберкулезом, так как между ними имеется патогенетическое сходство — подобный механизм формирования гранулем [7]. В обоих случаях чаще болеют молодые люди, наиболее часто вовлекается илеоцекальный переход [7], воспаление носит трансмуральный гранулематозный характер, но при туберкулезе гранулемы могут иметь казеоз, а при болезни Крона казеоз отсутствует. Наблюдаются похожие проявления: абдоминальные боли, диарея, потеря веса, отсутствие аппетита, формирование инфильтратов в брюшной полости, непроходимость, перфорации [2].

О сложности диагностики свидетельствует тот факт, что до сих пор не существует единственного диагностического метода, единого «золотого стандарта» диагностики болезни Крона. На Международной конференции по капсульной эндоскопии (ICCE, 2006/2007) [8] приняты критерии, по совокупности которых можно заподозрить болезнь Крона (см. таблицу). Основные критерии, позволяющие заподозрить болезнь Крона
Диагноз болезни Крона можно заподозрить при наличии у пациента хотя бы одного признака из раздела, А (клинические проявления заболевания) и одного признака из любого другого раздела (внекишечные проявления заболевания).
Согласно рекомендациям Российской группы по изучению воспалительных заболеваний кишечника (2009 г.) [9], диагноз болезни Крона должен быть подтвержден эндоскопическим и морфологическим и/или рентгенологическим методом [1].
Такой специфический признак, как неказеозные гранулемы, выявляется очень редко [10]. По литературным данным [3, 11], гранулемы находят приблизительно в 10—20% случаев биопсий, по некоторым источникам — несколько чаще (36%) [1].
Таким образом, болезнь Крона остается актуальной проблемой в силу своей относительной редкости, наличия тяжелых осложнений и объективной трудности в диагностике.
Приводим клинический случай.
Цель — обратить внимание на сложность диагностики и необходимость комплекса исследований для выявления болезни Крона.
Материал и методы
Исследование проводилось на материале больной Ч., 34 года, которая обратилась в консультативную поликлинику ГБУЗ ООКБ к врачу-гастроэнтерологу с жалобами на периодические схваткообразные боли в правой половине живота, периодическую задержку стула и газов, ухудшение аппетита и снижение веса примерно на 5—7 кг в течение последних трех месяцев. Примесей слизи и крови в кале не было. Каких-либо заболеваний ранее больная не отмечала, медикаментов не принимала, пищевой и лекарственной аллергии не имела. Туберкулез отрицает.
При обследовании использовались методы: клинические, рентгенологические (КТ, ирригография, обзорная рентгенография брюшной полости, пассаж бария по кишечнику), эндоскопический — колоноскопия.
Результаты
В лабораторных анализах выявлена СОЭ до 25, лейкоцитоз до 10 тыс. Кожные покровы чистые, бледные, регионарные лимфоузлы не увеличены, язык влажный, обложенный белым налетом. Температура тела нормальная. При пальпации живота в правой подвздошной области определялось болезненное опухолевидное образование до 8—10 см в диаметре. Симптомов «плеска» и «падающей капли», а также симптомов раздражения брюшины не было. На обзорной рентгенограмме грудной клетки патологии не выявлено. Микроскопия кала без особенностей.
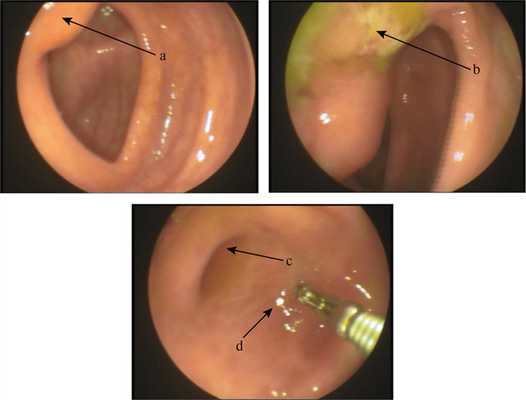
Колоноскопия. При осмотре перианальной области изменений не отмечено. Геморроидальные узлы не увеличены. При пальцевом исследовании прямой кишки болей и патологических образований не выявлено. Тонус сфинктера сохранен. Толстая кишка осмотрена, включая купол слепой кишки. При осмотре со стороны восходящей ободочной кишки особенностей области баугиниевой заслонки не замечено, она имела уплощенную форму (рис. 1). Рис. 1. Больная Ч., 34 года. Колоноскопия. Эндофото. Изменения илеоцекальной области. а — баугиниева заслонка; b — язва; с — устье аппендикулярного отростка; d — купол слепой кишки. Слепая кишка отклонена медиально и деформирована, из-за чего ее форму определить затруднительно. По этой же причине не удалось провести фронтальный осмотр баугиниевой заслонки, но на участке нижней губы баугиниевой заслонки, обращенном к отверстию, выявлена язва (см. рис. 1) средней глубины, неправильной формы, с невыраженным воспалительным валом, ровным дном и налетом серого фибрина. Размеры язвы не определены из-за деформации этой области. Отмечалась повышенная плотность стенки этой области при инструментальной пальпации, перистальтика отсутствовала. Проведение колоноскопа диаметром 1,2 см через отверстие баугиниевой заслонки оказалось невозможным из-за его сужения. Произведен забор фрагментов слизистой оболочки с краев и дна язвы для гистологического и цитологического исследования. Область купола слепой кишки и устья аппендикулярного отростка — без особенностей (см. рис. 1).
Заключение гистологического исследования биоптатов со слизистой оболочки краев и дна язвы баугиниевой заслонки: очаговое склерозирование стромы с преимущественно лимфоидно-клеточной инфильтрацией.
Заключение цитологического исследования: слизистая толстой кишки с умеренной воспалительной инфильтрацией. Опухолевой ткани не найдено.
При обследовании верхних отделов ЖКТ выявлен хронический гастрит, ассоциированный с Helicobacter pylori.
Выполнена компьютерная томография, при которой на задней поверхности слепой кишки обнаружено образование 49×43 мм с довольно четкими контурами, плотностью до 45 едН. Образование несколько компримирует кишку, прилежит к поясничной мышце. Заключение К.Т.: образование брюшной полости? аппендикулярный инфильтрат?
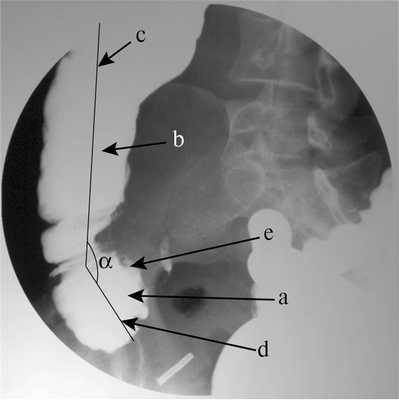
При ирригоскопии выявлена деформация слепой кишки и «изъеденность» ее медиального контура (рис. 2). Рис. 2. Больная Ч., 34 года. Ирригограмма илеоцекального перехода и восходящей ободочной кишки. а — слепая кишка; b — восходящая ободочная кишка; с — ось восходящей ободочной кишки; d — ось слепой кишки; e — изъеденность медиального контура слепой кишки; α — угол между осями восходящей ободочной и слепой кишки. Слепая кишка отклонена медиально, образуя угол 39° по отношению к восходящей ободочной кишке.
Больной была выполнена обзорная рентгенограмма брюшной полости, при которой свободного газа, а также чаш Клойбера не выявлено. Кроме этого, после перорального приема сернокислого бария проводился контроль пассажа бария по кишечнику, при этом отмечалось замедленное прохождение его в толстую кишку до 10—12 ч. В результате комплекса исследований больной были определены показания к операции в связи с частичной кишечной непроходимостью, среди возможных причин которой не исключались болезнь Крона, аппендикулярный инфильтрат, туберкулез, новообразование илеоцекальной области.
Выполнена лапаротомия, правосторонняя гемиколэктомия с формированием илеотрансверзоанастомоза бок в бок.
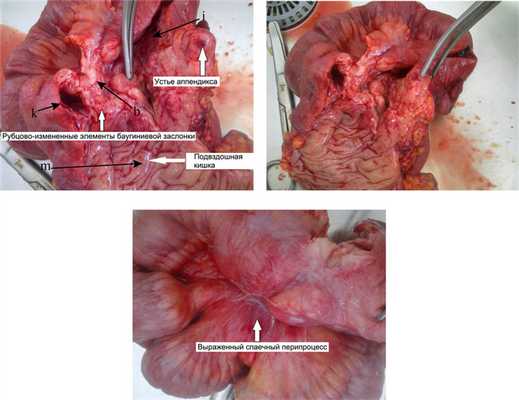
Макропрепарат илеоцекальной области представлял собой конгломерат (рис. 3), Рис. 3. Больная Ч., 34 года. Макропрепараты илеоцекального перехода после правосторонней гемиколэктомии. Фото. b — язва; k — просвет восходящей ободочной кишки; i — просвет слепой кишки; m — просвет подвздошной кишки. состоящий из спаянных между собой петель восходящей ободочной, слепой и подвздошной кишок. При рассечении этого участка определялась значительная плотность ткани, деформация стенки, элементы баугиниевой заслонки не дифференцировались, в районе предполагаемой нижней губы баугиниевой заслонки — глубокая язва, неправильной формы, с плотными краями.
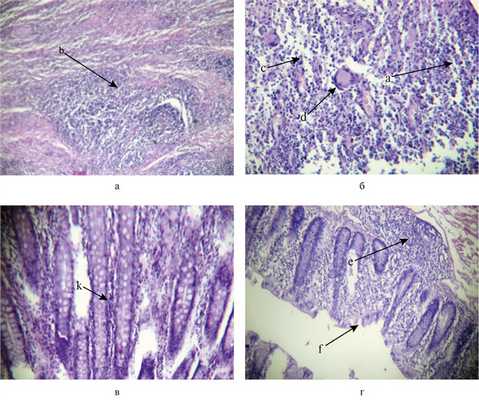
Заключение послеоперационного гистологического исследования удаленного макропрепарата илеоцекального перехода (рис. 4): Рис. 4. Больная Ч., 34 года. Микропрепараты илеоцекального перехода. а — лимфоидно-клеточная инфильтрация; b — лимфоидная гиперплазия; с — склерозирование стенки; d — клетки Пирогова—Лангханса; е — крипт-абсцесс; f — язва; k — бокаловидные клетки. Окраска гематоксилином и эозином; ув. 40 (а, б), ув. 100 (в, г). склерозирование всех слоев стенки с выраженной лимфоцитарной инфильтрацией и очаговой лимфоидной гиперплазией. Определяются гигантские клетки Пирогова—Лангханса, крипт-абсцессы, глубокая язва. Количество бокаловидных клеток сохранено. Данная картина соответствует болезни Крона.
Дифференциальная диагностика болезни Крона должна включать заболевания, для которых характерны язвенные поражения: энтеропатию, вызванную лекарственными препаратами, лучевой нагрузкой, а также язвенный колит, туберкулез, иерсиниоз, сальмонеллез, шигеллез, кампилобактериоз. Но больная лекарственных препаратов не принимала, лучевому воздействию не подвергалась, инфекции были исключены по результатам лабораторных исследований. Против язвенного колита свидетельствует отсутствие изменений в прямой кишке. Нельзя было исключить опухоль илеоцекального перехода, так как пальпаторно определялось объемное образование в правой подвздошной области, выявлено снижение Hb в крови, имелись соответствующие клинические признаки. Можно подумать о туберкулезе кишечника, так как распространенность его в России составляет 78,7 случая на 100 000 населения, а в некоторых регионах — до 395,8 случаев [2]. Кроме того, имеется патогенетическое и клиническое сходство этих заболеваний. R-графия легких в 50% случаев при туберкулезе может соответствовать норме [2]. В биоптатах, полученных при колоноскопии, такой специфический признак, как гранулема (при туберкулезе — казеозная, при болезни Крона — неказеозная), а также бактерии туберкулеза, встречаются нечасто [1]. Но перфорация язвы как осложнениe болезни Крона и формирование инфильтрата с частичной кишечной непроходимостью стоят на первом месте. Поэтому больная была прооперирована в связи с частичной кишечной непроходимостью, причиной которой могли быть болезнь Крона, туберкулез, опухоль илеоцекального перехода, аппендикулярный инфильтрат. Результаты послеоперационного морфологического исследования илеоцекального перехода, трансмуральные поражения стенки кишки, склерозирование, лимфоидная инфильтрация, гигантские клетки Пирогова—Лангханса, язвы, сохранение бокаловидных клеток, послеоперационное лечение утвердили подозрения в болезни Крона илеоцекального перехода, осложненной перфорацией язвы и формированием инфильтрата с частичной кишечной непроходимостью.
Заключение
Диагностика болезни Крона илеоцекального перехода и ее осложнений обусловлена объективными трудностями, требует комплекса методов, основывается на критериях, включая клинические проявления, а также лабораторные, рентгенологические, эндоскопические, иногда оперативные данные. Важным в диагностике является морфологическое подтверждение (трансмуральное поражение, эрозии, глубокие язвы, наличие клеток Пирогова—Лангханса, гранулем, сохранение бокаловидных клеток).
Авторы заявляют об отсутствии конфликта интересов.
Сведения об авторах
Фатеев Иван Николаевич — д.м.н., доцент, профессор кафедры оперативной хирургии и клинической анатомии;
УЗИ — ультразвуковое исследование
ФКП — фекальный кальпротектин
ЯК — язвенный колит
ANCA — антинейтрофильные эндоплазматические антитела
ASCA — антитела к Saccharomyces cerevisiae
α-ФНО — α-фактор некроза опухоли

В 1932 г. Беррилл Бернард Крон (рис. 1) Рисунок 1. Беррилл Бернард Крон (1884—1983). описал и представил американской Медицинской ассоциации 14 больных под рубрикой «Терминальный илеит: новый клинический синдром». В том же году он в соавторстве с коллегами Леоном Гинзбергом и Гордоном Оппенгеймером опубликовал статью «Региональный илеит: патологическая и клиническая сущность». В этих работах был впервые описан терминальный илеит, получивший в дальнейшем имя Б. Крона. Клинические и патологические проявления болезни соответствовали современным представлениям. В последствии оказалось, что болезнь Крона (БК) может локализоваться во всех отделах желудочно-кишечного тракта (ЖКТ). Она характеризуется разнообразными кишечными и внекишечными проявлениями, которые зависят от глубины, протяженности пораженного органа и особенностей иммунных (системных) осложнений.
Распространенность. Заболеваемость БК имеет тенденцию к повышению. Это особенно заметно в странах с высокоразвитой индустрией. В конце прошлого века заболеваемость находилась в пределах от 0,7 до 14,6 на 100 000 населения в год, а в настоящее время в США и Европе достигает 67,1—149 на 100 000 [1]. Результаты эпидемиологических наблюдений дают основания полагать, что в регионах Москвы, Санкт-Петербурга и других крупных городов Российской Федерации заболеваемость воспалительными заболеваниями кишечника — ВЗК (язвенным колитом и БК) сопоставима с заболеваемостью в США и Европе.
Этиология и патогенез. Этиология БК неизвестна, но со времени ее описания и до сих пор актуален вопрос об участии микрофлоры. Так, вновь обсуждается роль одной из разновидностей микобактерии паратуберкулеза (Mycobacterium avium subspecies paratuberculosis), которая вызывает похожую болезнь у рогатого скота [2]. Ген NOD2, ответственный за генетическую восприимчивость БК, подавляет способность макрофагов поглощать эти микроорганизмы, подавляет ответ врожденной и адаптивной иммунной системы на внутриклеточную инвазию микобактерий паратуберкулеза. У лиц, генетически предрасположенных к инфекциям Mycobacterium avium subsp., повышен риск развития БК. Макрофаги, пораженные микобактериями, усиленно экспрессируют α-фактор некроза опухоли (α-ФНО) [3].
В предрасположенности к БК имеют значение и генетически детерминированные дефекты барьерной функции кишечного эпителия, облегчающие проникновение бактериальных антигенов. Ген, ответственный за восприимчивость к БК, с помощью внутриклеточного белка NOD2/CARD15 реагирует на присутствие бактериальных антигенов. Бактериальные антигены вызывают иммунный ответ T-лимфоцитов CD4+. Активируются цитокины α-ФНО, интерферон-γ, интерлейкин-4, 13, 23, 27 и 3, инициирующие воспалительный процесс [4].
Определенное значение в патогенезе БК придают факторам окружающей среды. Рост заболеваемости БК в индустриальных странах мира уже давно и не без оснований связывают с загрязнением окружающей среды, воды и воздуха, ранним переводом грудных детей на искусственное вскармливание, увеличенным потреблением углеводов, животного и молочного белка, увеличенным соотношением ω-6 и ω-3 полиненасыщенных жирных кислот в пище. Люди, употребляющие преимущественно белки растительного происхождения, реже болеют БК. Риск развития БК увеличивают курение и гормональная контрацепция, а также чрезмерно тщательное соблюдение личной гигиены, снижающее активность Т-хелперов 2-го типа, обеспечивающих защиту от инфекций и увеличивающее риск развития ВЗК.
Классификация. Европейским обществом по изучению ВЗК (ECCO) рекомендована Венская классификация БК (1998) с Монреальской модификацией (2005). Выделены варианты БК в зависимости от возраста больного (А), локализации процесса (L) и фенотипа заболевания (B). Время установления окончательного диагноза: A1 — 16 лет или младше; А2 — 17 — 40 лет; А3 — старше 40 лет. У большинства БК устанавливают в возрасте 17—40 лет (А2). Локализация воспалительного процесса: L1 — терминальный илеит; L2 — колит; L3 — илеоколит; L4 — верхний отдел ЖКТ проксимальнее терминального отдела. БК в форме илеита (L1) возникает примерно у 45%, в форме илеоколита (L3) — у 19%, в форме колита (L2) — у 32% и в верхнем отделе ЖКТ (L4) — у 4% [5].
Фенотип (форма) заболевания: В1 — воспалительная (люминальная) форма; B2 — cтенозирующая форма; B3 — пенетрирующая, или свищевая (экстралюминальная), форма (возникновение межкишечных и иных свищей, абсцессов и инфильтратов в брюшной полости), В3p — перианальная форма. Кроме того, с перианальным поражением может сочетаться каждый из фенотипов БК.
Степень тяжести (активность) БК оценивают в баллах. Индекс активности болезни Крона (ИАБК) менее 150 баллов — ремиссия, 150—220 баллов — легкая, 220—450 баллов — умеренная, более 450 баллов — высокая активность. Новейшие исследования показывают, что клинические критерии ремиссии совпадают с эндоскопическими лишь у 1 /5 больных [6]. У остальных больных при колоноскопии (КФС) и илеоскопии наблюдаются признаки воспаления. Поэтому для оценки надежности ремиссии и принятия решения об изменении лечебной тактики уже используют высокочувствительные биомаркеры воспаления — C-реактивный белок (СРБ), фекальный кальпротектин (ФКП) и лактоферритин (ЛФ). Эндоскопический контроль ремиссии оценивают с помощью конфокального лазерного эндомикроскопа. Он дает возможность получить увеличенное изображение слизистой оболочки (СО) и ее сканограмму на глубине до 250 мкм.
Патоморфология. Для БК в отличие от язвенного колита (ЯК), характерно поражение всех слоев кишечной стенки. Особенностью является также мозаичность поражения с формированием четких границ с неповрежденными сегментами кишки. При гистологическом исследовании биоптатов СО пораженной кишки воспаление характеризуется очаговой инфильтрацией нейтрофилами поверхностного эпителия с развитием абсцессов в криптах. В собственной пластинке и более глубоких отделах стенка кишки инфильтрирована лимфоидными клетками. Инфильтрация стенки кишки лимфоидными клетками настолько массивная, что делает рельеф кишки неровным, получившим название «булыжная мостовая». В инфильтрате образуются гранулемы вокруг гигантских клеток Лангханса макрофагального происхождения — характерный признак гранулематозного воспаления. В отличие от туберкулезных и других инфекционных гранулем в них отсутствуют очаги казеозного некроза. Гранулематозное воспаление при БК возникает в подслизистой основе, постепенно распространяется как в сторону СО, так и серозной оболочки кишки, вызывает сужение просвета и/или пенетрацию кишки с образованием свищей. Гранулемы обнаруживают, как правило, только в операционном материале, так как биоптаты, получаемые во время внутрипросветной эндоскопии, ограничиваются только СО. При БК тонкой кишки в биоптатах также можно видеть признаки хронического повреждения СО, укорочение ворсинок, метаплазию эпителия, в частности клеток Панета, являющихся регуляторами кишечной микробиоты.
Клиническая картина. Клинические проявления БК зависят от фенотипа и локализации БК.
Воспалительная (люминальная) форма долгое время ограничивается преимущественно подслизистой основой кишки. Длительное время протекает с неопределенными болями в животе и внекишечными манифестациями (эпизоды немотивированной лихорадки, боли в суставах, узловатая эритема и др.). Заболевание может оставаться неустановленным много лет. Если БК начинается в детстве, то больной отстает в физическом развитии. Первыми клиническими проявлениями болезни служат лихорадка, увеличенная СОЭ, лейкоцитоз и другие симптомы воспалительного заболевания. По мере распространения воспаления на СО, мышечную и серозную оболочки появляются хроническая диарея, кишечные кровотечения, приступообразные боли, свидетельствующие об изъязвлении и сужении пораженного сегмента кишки. Появляются симптомы мальабсорбции: анемия, гипопротеинемия, отеки и снижение массы тела. Иногда развивается картина непроходимости кишечника. Поражение пищевода, желудка и двенадцатиперстной кишки создает картину язвенной болезни, отличающейся множественностью язвенно-эрозивных поражений, резистентных к стандартной терапии. При локализации в аноректальной области образуются незаживающие трещины прямой кишки и парапроктиты.
Стенозирующая форма характеризуется симптомами непроходимости кишечника. В клинической картине преобладают приступообразные боли, чаще в правой подвздошной области, сопровождающиеся рвотой, вздутием живота, громким урчанием, переливанием с задержкой стула и газов. Появляется видимая на глаз перистальтика с периодически поднимающимися «валами». При пальпации живота иногда удается обнаружить инфильтрат в брюшной полости. Диагноз подтверждается при рентгенологическом исследовании или во время лапаротомии. СО приобретает неровный рельеф. Рубцовые изменения стенки приводят к сужению просвета кишки, развитию частичной и даже полной непроходимости кишечника.
Свищевая (экстралюминальная) форма отличается тяжелым течением, трансмуральным поражением стенки кишки с формированием межкишечных сращений, абсцессов и межпетлевых слепых и наружных кишечных свищей.
Внекишечные проявления. Внекишечные или системные проявления встречаются у большинства пациентов с БК. Аутоиммунные системные реакции и генетические нарушения возникают приблизительно у 25% больных.
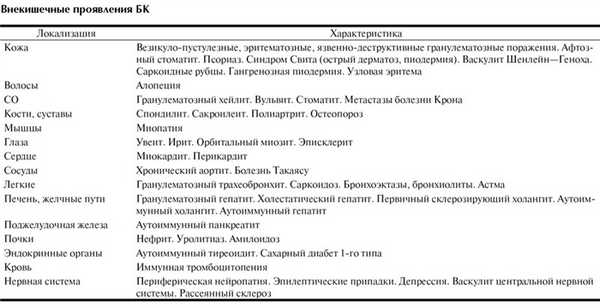
К аутоиммунным относятся артриты, васкулиты, аутоиммунный гепатит, эписклерит, афтозный стоматит, узловая эритема, гангренозная пиодермия. Генетически детерминированные нарушения, связанные с HLA-B27, вызывают анкилозирующий спондилит и сакроилеит, увеит, первичный склерозирующий холангит. Внекишечные проявления, обусловленные мальабсорбцией (остеопороз, мочекаменная и желчнокаменная болезни, анемия, нарушения свертывания крови, тромбозы и др.), энтеропатией с потерей белка и/или амилоидозом (гипопротеинемия, гипоальбуминемия, отеки) появляются у большинства больных еюнитом и илеитом Крона. Внекишечные манифестации и аутоиммунные нарушения, возникающие при БК, в разное время описаны в литературе (см. таблицу).
Особенности течения. БК представляет собой рецидивирующее или непрерывно текущее заболевание, дающее спонтанную (без лечения) ремиссию у 30% больных.
У 50% из них продолжительность ремиссии может достигать 2 лет и более. Фенотипы БК не являются постоянными. При несвоевременном распознавании болезни и запоздалом начале ее лечения (через 3 года от времени появления первых симптомов или позднее) осложнения развиваются практически у всех больных. С течением времени стенка кишки подвергается фиброзу и изначально воспалительный тип трансформируется в стенозирующий или пенетрирующий. У некоторых больных сужение и свищи обнаруживают уже при первом обращении к врачу. У других воспалительный тип может продолжаться на протяжении десятилетий без сужений и свищей. J. Cosnes и соавт. [7] провели ретроспективное исследование эволюции БК у 2002 больных на протяжении 20 лет. У 84% из них была воспалительная (В1), у 4% — стенозирующая (В2) и у 12% — свищевая (В3) форма заболевания. В последующие годы у 60% больных с воспалительной формой БК наблюдалась тенденция к развитию стенозов и свищей. Из них у 79% течение болезни осложнилось свищами, а у 21% — стенозом. В целом через 20 лет воспалительная форма осталась лишь у 12% больных, свищи появились у 70%, стеноз — у 15%. Таким образом, у 60% больных возникает необходимость в хирургическом лечении, причем почти 50% из них нуждаются в повторной операции.
Методы диагностики. Визуализация пораженного участка ЖКТ осуществляется с помощью эндоскопического, рентгенологического и ультразвукового методов. Каждый из них имеет преимущества и недостатки и дополняют друг друга. Глубокая эндоскопия тонкой кишки и капсульная эндоскопия обладают очень высокой чувствительностью и специфичностью в обнаружении воспалительных проявлений СО кишечника. Более глубокие слои кишечной стенки доступны оценке при изображении кишки в поперечном сечении, позволяющем обнаружить стриктуры, свищи и абсцессы. Поэтому при БК одинаково важную роль играют как осмотр поверхности кишки, позволяющий увидеть афты, изменение рельефа и диаметра просвета кишки, доступные эндоскопическому методу, так и оценка толщины всей стенки кишки с помощью ультразвукового исследования (УЗИ), компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ), особенно с использованием контрастных растворов, введенных внутривенно.
Позитронно-эмиссионная томография (ПЭТ) с использованием меченной фтором-18 ФДГ (2-фтор-2-дезокси-D-глюкозы) является функциональным методом визуализации, который чувствителен к метаболизму глюкозы. ФДГ накапливается в местах активного воспалительного процесса в связи с гиперэкспрессией лейкоцитов в зоне переносчиков глюкозы и увеличением метаболической активности. С помощью ПЭТ можно определить воспаленные участки кишки и, что особенно важно, объективно оценить степень активности БК и определить конечную точку ремиссии, необходимую для оценки качества лечения. ПЭТ позволяет различить воспалительные и фиброзные стриктуры, т.е. связать результаты с адекватностью проводимой терапии, а также осуществить скрининг рака [8].
Предложены также серологические тесты, облегчающие диагностику и прогноз БК. Исследуют уровень антител к Saccharomyces cerevisiae (ASCA) и антинейтрофильных эндоплазматических антител (ANCA) [9]. Появление ASCA, а также антител к ламинарибиозиду [Glc(β1,3)Glb(β); ALCA], хитобиозиду (GlcNAc(β1,4) GlcNAc(β); ACCA], маннобиозиду [Man(α1,3)Man(α); AMCA], ламинарину [Glc(β1,3))3n(Glc(β1,6); anti-L] и хитину [(GlcNAc (β1,4)n; anti-C] характерно для БК, а уровень их повышения отражает тяжесть течения БК и прогноз [10].
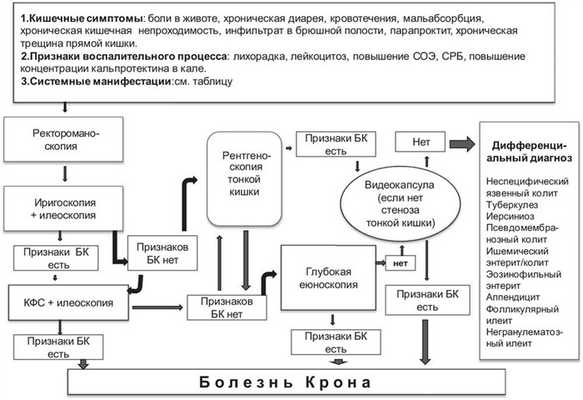
На рис. 2 Рисунок 2. Алгоритм диагностики БК. представлен алгоритм диагностики БК с применением рентгенологических и эндоскопических методов.
БК следует предполагать в следующих случаях:
а) имеются клинические симптомы (приступообразная боль в животе с задержкой стула и газов, вздутием живота и локализующаяся в правой подвздошной области, хроническая диарея (необязательно с кровью), пальпируемый инфильтрат (необязательно), парапроктит или хроническая трещина прямой кишки; б) наличие признаков воспалительного процесса (лихорадка, лейкоцитоз, повышенный уровень СРБ, ФКП и ЛФ); в) определяются внекишечные манифестации и системные (аутоиммунные) нарушения (см. таблицу).
Исследование следует начинать с проктологического осмотра и ректороманоскопии. Затем независимо от результатов нужно выполнить рентгенологическое исследование с тугим заполнением контрастной взвесью толстой кишки и дистального отдела подвздошной кишки. Третий этап — КФС с илеоскопией. С помощью этих исследований устанавливают колит Крона (L2) и илеоколит (L3).
Четвертый этап предназначен для диагностики БК тонкой кишки (L1), пищевода и желудка (L4) и также является обязательным вне зависимости от результатов предыдущих этапов. Больному выполняют рентгенологическое исследование тонкой кишки и при возможности — глубокую антеградную энтероскопию и видеокапсульную энтероскопию (в отсутствие признаков стеноза при эндоскопии). Исследование с помощью видеокапсулы позволяет визуализировать минимально выраженные повреждения СО тонкой кишки.
Дифференциальный диагноз. В основе решения диагностической концепции БК лежит сложный дифференциально-диагностический поиск, в ходе которого должны быть обсуждены многие болезни, сопровождающиеся эрозивно-язвенными поражениями тонкой и толстой кишки, указанными ниже.
Болезнь Крона

- Запись опубликована: 09.10.2020
- Reading time: 4 минут чтения
Болезнь Крона - хроническое воспалительное заболевание кишечника неизвестной этиологии. Воспаление может поражать весь желудочно-кишечный тракт: ротовую полость, пищевод, желудок, двенадцатиперстную кишку, тощую кишку, и чаще всего поражения расположены в подвздошной кишке, а также могут присутствовать по всей толстой и прямой кишке.
Патология встречается у людей разных возрастных групп, но чаще всего поражает молодых пациентов в возрасте от 20 до 30 лет и между 5 и 7 десятилетиями. Благодаря соответствующему лечению больные могут достичь длительного периода ремиссии, в течение которого симптомы не проявляются. Однако предсказать, когда болезнь будет прогрессировать, невозможно.
Что такое болезнь Крона
Болезнь Крона - хроническое кишечное заболевание, характеризующееся воспалением, которое поражает не только поверхностные, но и глубокие слои стенки кишечника. Хотя воспалительные поражения или язвы могут возникать в любом месте кишечника от рта до заднего прохода, обычно поражаются задняя часть тонкой кишки и начало толстой кишки. Кроме того, характерно сегментарное поражение - когда воспаление охватывает не весь кишечник, а лишь некоторые его части.
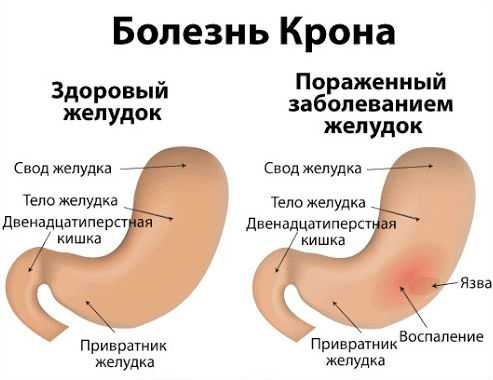
Что такое болезнь Крона
Кто болеет болезнью Крона?
Патология доминирует, прежде всего, в высокоразвитых городских агломерациях Западной и Северной Европы. Примерно у 20% пациентов это генетически обусловленное заболевание, связанное с наличием гена NOD2/CARD15, расположенного на хромосоме 16 (IBD1), что увеличивает вероятность заболеваемости примерно в 20-40 раз.
Также было доказано, что у курильщиков сигарет вероятность развития этого заболевания в два раза выше, и его течение в этих случаях намного тяжелее.
В чем причина болезни Крона
Факторы, ответственные за воспалительные заболевания кишечника, в т. ч. язвенный колит и болезнь Крона, до сих пор полностью не изучены. Считается, что следует учитывать несколько компонентов, способных повлиять на развитие болезни. К ним относятся семейные, генетические, экологические, бактериальные, иммунологические и психологические факторы.
Считается, что начало болезни Крона может быть связано с определенными нарушениями иммунной системы организма.
Несмотря на многочисленные попытки выделить генетический маркер, полезный для идентификации людей, предрасположенных к развитию болезни Крона, не удалось обнаружить ни одного причинного фактора, который оказал бы фундаментальное влияние на развитие болезни.
Симптомы болезни Крона
Из-за протяженности и мультифокальности болезненного процесса клиническая картина при БК зависит от анатомической локализации поражений.
У пациентов с изменениями тонкого кишечника наблюдаются:
В случае локализации высыпаний в толстом кишечнике преобладают боли в животе, метеоризм, диарея с примесью слизи, крови, анемия и общая слабость наряду с похуданием. В остальных случаях первыми симптомами заболевания могут быть свищи, трещины и перианальные абсцессы.
Наиболее частые симптомы болезни Крона:
- боль в правом бедре;
- понос;
- повышенная температура тела;
- потеря веса;
- метеоризм;
- анальная боль;
- перианальные свищи и абсцессы;
- изменения кожи;
- боли в суставах.
Течение болезни
Болезнь Крона может повредить любую часть пищеварительного тракта, но наиболее частые участки поражения - подвздошная кишка и аппендикс. Течение этого заболевания может быть хроническим и рецидивирующим. Обострения обычно чередуются с ремиссиями (временным выздоровлением).
От легкой до умеренной формы заболевания проявляются легкие клинические симптомы. Умеренно-тяжелая форма заболевания протекает с лихорадкой, анемией, похуданием, тошнотой, рвотой.
Тяжелая форма заболевания - сильный жар, боли в животе, рвота, кишечная непроходимость , резкое похудание.
Кишечная непроходимость
Диагностика
Анализы крови могут показывать снижение гемоглобина из-за недостатка железа, фолиевой кислоты или витамина B12, увеличение количества лейкоцитов и изменения скорости оседания эритроцитов.
Поражения кишечника выявляют при рентгенологическом и эндоскопическом исследованиях. Во время эндоскопического исследования (колоноскопия, гастроскопия) для микроскопического исследования берется участок слизистой оболочки (биопсия). Также для определения наличия бактерий, вызывающих воспаление кишечника, проводится посев фекалий.
Как лечится болезнь Крона?
Учитывая сложность воспалительного процесса, степень поражения и отсутствие четкого причинного фактора заболевания, идеальное лекарство для модификации лечения болезни Крона еще не разработано. В настоящее время можно выделить два метода лечения: консервативный и оперативный. Цели лечения - контролировать воспаление в кишечнике, восстанавливать нутритивный статус и предотвращать рецидивы (продление времени ремиссии).
Комплексное консервативное лечение включает: правильное питание, восполнение дефицита, противовоспалительное, иммунодепрессивное, биологическое и симптоматическое лечение. В настоящее время в консервативном лечении используются 5 групп препаратов для поддержания ремиссии заболевания:
- 5-аминосалицилаты - сульфасалазин и 5-аминосалициновая кислота (5-АСК, месалазин);
- глюкокортикостероиды;
- метронидазол, ципрофлоксацин;
- азатиоприн (AZA) и его метаболиты, 6-меркаптопурин (6-MP) и 6-тиогуанин (6-TG);
- биологические препараты (инфликсимаб).
Подсчитано, что примерно 75% пациентов с болезнью Крона в какой-то момент жизни потребуют хирургического вмешательств а.
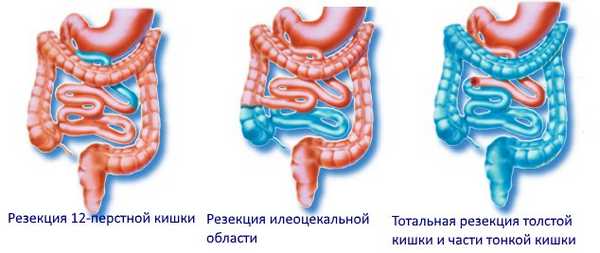
Хирургическое лечение осложнений болезни Крона
Показания к хирургическому лечению включают:
- устойчивость к консервативному лечению со значительным прогрессированием заболевания;
- кишечная непроходимость;
- внутрибрюшинный абсцесс;
- свищ;
- перфорация желудочно-кишечного тракта;
- желудочно-кишечное кровотечение;
- перианальные изменения;
- дисплазия и трансформация опухоли.
В этих случаях операция служит только для облегчения симптомов, но не излечивает само заболевание. Основным принципом хирургического лечения является щадящее удаление воспалительных поражений кишечника, создание новых широких кишечных анастомозов, иссечение перианальных свищей и дренирование абсцесса.
Осложнения
Осложнения могут возникнуть при болезни Крона даже при лечении. Например, часто сужается просвет кишечника, что может привести к кишечной непроходимости.
Также болезнь Крона характеризуется глубокими язвами, которые проникают через всю стенку кишечника в соседние органы - мочевой пузырь, влагалище, кожа, другие кишечники, образуя проток - свищ, который часто загнаивается. Свищи обычно возникают между кишечником и кожей вокруг заднего прохода, а также между тонкой и прямой кишкой. Менее часто возникают кровотечения из кишечника.
При болезни Крона воспаление тонкой кишки приводит к ухудшению всасывания некоторых питательных веществ или их потере с диареей, что приводит к нехватке белка, витаминов, микроэлементов (цинка, магния, кальция, железа), нарушению развития и роста в детстве. Поскольку витамин B12 плохо усваивается, начинается анемия.
Болезнь Крона также может вызывать поражение других органов: воспаление глаз, суставов, поражения кожи, заболевания печени (обычно первичный склерозирующий холангит с поражением желчных протоков), почек и желчных камней.
Затяжная болезнь Крона увеличивает риск рака кишечника, но это осложнение встречается реже, чем при язвенном колите.
Профилактика
Меры по предотвращению болезни Крона неизвестны.
Специальной диеты, помогающей предотвратить усугубление болезни, нет, но у некоторых пациентов симптомы ухудшаются от молока, алкоголя, пряных специй и т. д. Желательно избегать таких продуктов, а во время обострений есть меньше продуктов с высоким содержанием клетчатки. Важно потреблять достаточное количество недостающих витаминов и микроэлементов.
Следует знать, что даже после исчезновения симптомов болезни нужно регулярно принимать лекарства, так как болезнь может вернуться в любой момент.
Поражаться может слизистая оболочка на любых участках ЖКТ от ротовой полости до прямой кишки, но наиболее часто воспаление локализуется в подвздошной кишке и начальном отделе толстой кишки. Развиться болезнь Крона может у любого человека вне зависимости от возраста и пола.
- Иммунологические факторы. У пациентов обнаруживается патологическая реакция иммунитета на кишечную флору, пищу, поступающую в кишечник, другие субстанции. Иммунная система отмечает эти факторы как чужеродные и насыщает стенку кишечника лейкоцитами, в результате чего возникает воспалительная реакция, эрозия и язвенное поражение слизистой.
- Генетические факторы. Очень часто болезнь выявляется близнецов и у родных братьев. Примерно в 17 % случаев больные имеют кровных родственников также страдающих этим заболеванием.
- Инфекционные факторы. Роль этих факторов не подтверждена полностью, но существует предположение о вирусной или бактериальной природе возникновения болезни.
- Образ жизни. Курение, злоупотребление алкоголем, лекарственными средствами, экологические факторы также могут способствовать развитию болезни Крона.
Симптомы болезни Крона
Наличие болезни Крона можно заподозрить при постоянных или ночных поносах, боли в животе, кишечной непроходимости, похудании, ночной потливости. Диарея часто сопровождается болями при дефекации. Позывы к дефекации могут быть до 6 и более раз в сутки. Часто больные жалуются на вздутие живота и рвоту.
При болезни Крона слизистая толстой кишки воспалена, покрыта поверхностными изъязвлениями, что вызывает боль в животе, примеси крови и слизи в кале.
Наблюдаются общее недомогание, потеря аппетита и снижение массы тела, сухость во рту, постоянная жажда.
К внекишечным проявлениям болезни Крона относятся кожные проявления, поражения суставов, воспалительные заболевания глаз, заболевания печени и желчевыводящих путей, васкулит (воспаление сосудов), нарушения гемостаза и тромбоэмболические осложнения, заболевания крови, остеопороз (разрежение костной ткани).
Болезнь Крона протекает длительное время. В развитии этой болезни также наблюдаются периоды обострения и ремиссии. В период обострения симптомы болезни могут быть выраженными, однако в период ремиссии могут полностью отсутствовать.
Клинические проявления при болезни Крона очень схожи с симптомами неспецифического язвенного колита, поэтому необходимо различать одно заболевание от другого.
| Признаки | Болезнь Крона | Язвенный колит |
| Симптомы | Боли в животе, чаще в левой нижней области. Кровавая диарея не характерна | Диарея с примесью крови, слизи и иногда гноя |
| Локализация патологического процесса | Может локализоваться в любом отделе ЖКТ | В пределах толстой кишки и всегда в прямой кишке |
| Распространенность патологического процесса | Очаговый характер | Диффузный характер |
| Эндоскопическая картина | Типа «булыжной мостовой», язвы щелевидной формы на фоне малоизмененной слизистой оболочки. Чаще всего в процесс вовлекается дистальный отдел подвздошной кишки | Зернистость, утрата сосудистого рисунка, наличие эрозий, участков изъязвлений, псевдополипов |
| Гистологическая картина | Трансмуральное (захватывающее все слои кишки) воспаление | Воспаление в пределах слизистой оболочки, микроабсцессы, атрофия |

Диагностика болезни Крона
- Анализ анамнеза заболевания и жалоб - как давно появились боли в животе, существует ли сезонность обострений, с чем пациент связывает возникновение этих симптомов.
- Анализ анамнеза жизни - были ли у пациента кишечные инфекции, отравления, операции на кишечнике, другие заболевания желудочно-кишечного тракта.
- Анализ семейного анамнеза - наличие у родственников заболеваний желудочно-кишечного тракта (гастрита, язвенной болезни желудка и двенадцатиперстной кишки, желчнокаменной болезни).
- Осмотр пациента - при пальпации живота определяется его болезненность, чаще в нижних отделах живота, под пупком (чуть справа).
- . Диагностика возможной анемии, наличия воспаления, заболеваний печени, поджелудочной железы, почек, содержания основных электролитов крови - калия, кальция, магния, натрия, хлора. . Проводится для контроля за мочевыделительной системой.
- Анализ кала на скрытую кровь. Проводится при подозрении на развитие кровотечения из желудочно-кишечного тракта. . Позволяет обнаружить непереваренные фрагменты пищи, большое количество непереваренного жира, грубые пищевые волокна.
- Ультразвуковое исследование (УЗИ) органов брюшной полости. Проводится для оценки состояния желчного пузыря, желчевыводящих путей, поджелудочной железы, почек, кишечника.
- Эзофагогастродуоденоскопия (ЭГДС) .
- Колоноскопия. Позволяет выявить характерные изменения кишечника при болезни Крона. Обследование сопровождается биопсией.
- Хромоэндоскопия с применением специальных красителей. Метод очень схож с колоноскопией. Отличием является окрашивание слизистой специальными веществами, которые реагируют с поврежденной стенкой кишечника, подтверждая тем самым наличие воспалительного процесса при болезни Крона.
- Видеокапсульная эндоскопия. Метод позволяет визуально оценить слизистую оболочку кишечника
- Ирригоскопия. Рентгенологическое исследование толстой кишки, которое позволяет выявить поражения толстой кишки. Ирригоскопию проводят при наличии кишечного стеноза (сужения просвета), когда невозможно провести колоноскопию.
- Компьютерная томография органов брюшной полости. Это исследование обеспечивает более точное изображение, чем обычные рентгеновские снимки. Оно позволяет увидеть весь кишечник, а также ткани вокруг петель кишечника, которые недоступны для осмотра при других исследованиях. . Этот метод позволяет оценить работу кишечника, определить нарушения моторики.
Лечение болезни Крона
Лечение при болезни Крона определяется степенью активности заболевания. В период обострения пациенту необходимо обеспечить полный физический и психический покой.
При небольшой активности болезни врач может назначить кишечные противовоспалительные лекарственные препараты, производные салициловой кислоты.
- Гормональные препараты. Снижают активность воспаления в организме.
- Иммунодепрессанты. Подавляют иммунную систему, участвующую в процессе развития болезни.
- Антибактериальные препараты.
Всем больным назначают витаминные комплексы, богатые витаминами А, Е, К, D, а также В12 и фолиевой кислотой, так как из-за повреждения кишечника эти вещества не поступают в организм с пищей.
Читайте также:
- Интоксикация как причина зуда заднего прохода. Наследственный зуд заднего прохода.
- Цереброваскулярная болезнь: транзиторные ишемические атаки, клиническая анатомия окклюзии сосудов головного мозга
- Наследственные болезни
- Понос после операции в гинекологии
- Диагностика плазмоцитомы и множественной миеломы на КТ, МРТ органов грудной клетки
