Диффузное расширение общего ствола легочной артерии и незаращение овального окна. Болезнь Лютембахера
Добавил пользователь Дмитрий К. Обновлено: 21.01.2026
МКБ-10
Общие сведения
Дефект межжелудочковой перегородки (ДМЖП) - отверстие в перегородке, разделяющей полости левого и правого желудочка, наличие которого приводит к патологическому шунтированию крови. В кардиологии дефект межжелудочковой перегородки - наиболее часто встречающийся врожденный порок сердца (9-25% от всех ВПС). Частота критических состояний при дефекте межжелудочковой перегородки составляет около 21%. С одинаковой частотой порок обнаруживается у новорожденных мальчиков и девочек.
Дефект межжелудочковой перегородки может быть единственной внутрисердечной аномалией (изолированный ДМЖП) или входить в структуру сложных пороков (тетрады Фалло, общего артериального ствола, транспозиции магистральных сосудов, атрезии трехстворчатого клапана и др.). В ряде случаев межжелудочковая перегородка может отсутствовать полностью - такое состояние характеризуется как единственный желудочек сердца.

Причины дефекта межжелудочковой перегородки
Чаще всего дефект межжелудочковой перегородки является следствием нарушения эмбрионального развития и формируется у плода при нарушениях закладки органов. Поэтому дефекту межжелудочковой перегородки часто сопутствуют другие сердечные пороки: открытый артериальный проток (20%), дефект межпредсердной перегородки (20%), коарктация аорты (12%), стеноз устья аорты (5%), аортальная недостаточность (2,5—4,5%), недостаточность митрального клапана (2%), реже - аномальный дренаж легочных вен, стеноз легочной артерии и др.
В 25-50% случаев дефект межжелудочковой перегородки сочетается с пороками развития внесердечной локализации - болезнью Дауна, аномалиями развития почек, расщелиной твердого неба и заячьей губой.
Непосредственными факторами, вызывающими нарушение эмбриогенеза, выступают вредные воздействия на плод в I триместре гестации: заболевания беременной (вирусные инфекции, эндокринные нарушения), алкогольная и лекарственная интоксикации, ионизирующая радиация, патологическое течение беременности (выраженные токсикозы, угроза самопроизвольного прерывания беременности и пр.). Имеются данные о наследственной этиологии дефекта межжелудочковой перегородки. Приобретенные дефекты межжелудочковой перегородки могут являться осложнением инфаркта миокарда.
Особенности гемодинамики при дефекте межжелудочковой перегородки
Межжелудочковая перегородка образует внутренние стенки обоих желудочков и составляет примерно 1/3 площади каждого из них. Межжелудочковая перегородка представлена мембранозным и мышечным компонентами. В свою очередь, мышечный отдел состоит из 3-х частей - приточной, трабекулярной и отточной (инфундибулярной).
После рождения и установления кровотока в большом и малом кругах кровообращения из-за дефекта межжелудочковой перегородки возникает лево-правый сброс крови, объем которого зависит от размеров отверстия. При небольшом объеме шунтируемой крови давление в правом желудочке и легочных артериях остается нормальным либо незначительно повышается. Однако при большом поступлении крови через дефект в малый круг кровообращения и ее возврате в левые отделы сердца, развивается объемная и систолическая перегрузка желудочков.
Значительное повышение давления в малом круге кровообращения при больших дефектах межжелудочковой перегородки способствует возникновению легочной гипертензии. Повышение легочно-сосудистого сопротивления взывает развитие сброса крови из правого желудочка в левый (обратного или перекрестного шунтирования), что приводит к артериальной гипоксемии (синдром Эйзенменгера).
Многолетняя практика кардиохиругов показывает, что наилучших результатов закрытия дефекта межжелудочковой перегородки можно добиться при сбросе крови слева направо. Поэтому при планировании операции тщательно учитываются гемодинамические параметры (давление, сопротивление и объем сброса).
Классификация дефекта межжелудочковой перегородки
Размер дефекта межжелудочковой перегородки оценивается, исходя из его абсолютной величины и сопоставления с диаметром аортального отверстия: маленький дефект составляет 1-3 мм (болезнь Толочинова-Роже), средний - равен примерно 1/2 диаметра аортального отверстия, большой - равен или превышает его диаметр.
С учетом анатомического расположения дефекта выделяют:
- перимембранозные дефекты межжелудочковой перегородки - 75% (приточные, трабекулярные, инфундибулярные) расположены в верхней части перегородки под аортальным клапаном, могут закрываться самопроизвольно;
- мышечные дефекты межжелудочковой перегородки - 10% (приточные, трабекулярные) - расположены в мышечном отделе перегородки, на значительном удалении от клапанной и проводящей систем;
- надгребневые дефекты межжелудочковой перегородки - 5% - расположены выше наджелудочкового гребня (мышечного пучка, отделяющего полость правого желудочка от его выносящего тракта), самопроизвольно не закрываются.
Симптомы дефекта межжелудочковой перегородки
Клинические проявления больших и малых изолированных дефектов межжелудочковой перегородки различны. Малые дефекты межжелудочковой перегородки (болезнь Толочинова—Роже) имеют диаметр менее 1 см и встречаются в 25-40% от числа всех ДМЖП. Проявляются нерезко выраженной утомляемостью и одышкой при нагрузке. Физическое развитие детей, как правило, не нарушено. Иногда у них определяется слабо выраженное куполообразное выпячивание грудной клетки в области сердца - «сердечный горб». Характерным клиническим признаком малых дефектов межжелудочковой перегородки служит аускультативно выявляемое наличие грубого систолического шума над областью сердца, который фиксируется уже на первой неделе жизни.
Большие дефекты межжелудочковой перегородки, имеющие размеры более 1/2 диаметра устья аорты или более 1 см, проявляются симптоматически уже в первые 3 месяца жизни новорожденных, приводя в 25-30% случаев к развитию критического состояния. При больших дефектах межжелудочковой перегородки отмечается гипотрофия, одышка при физической нагрузке или в покое, повышенная утомляемость. Характерны затруднения при кормлении: прерывистое сосание, частые отрывы от груди, одышка и бледность, потливость, пероральный цианоз. В анамнезе у большинства детей с дефектом межжелудочковой перегородки - частые респираторные инфекции, затяжные и рецидивирующие бронхиты и пневмонии.
В возрасте 3-4-лет, по мере нарастания сердечной недостаточности, у таких детей появляются жалобы на сердцебиение и боли в области сердца, склонность к носовым кровотечениям и обморокам. Транзиторный цианоз сменяется постоянным пероральным и акроцианозом; беспокоит постоянная одышка в покое, ортопноэ, кашель (синдром Эйзенменгера). На наличие хронической гипоксии указывают деформация фаланг пальцев и ногтей («барабанные палочки», «часовые стекла»).
При обследовании выявляется «сердечный горб», развитый в меньшей или большей степени; тахикардия, расширение границ сердечной тупости, грубый интенсивный пансистолический шум; гепатомегалия и спленомегалия. В нижних отделах легких выслушиваются застойные хрипы.
Диагностика дефекта межжелудочковой перегородки
К методам инструментальной диагностики дефекта межжелудочковой перегородки относятся ЭКГ, ФКГ, рентгенография грудной клетки, ЭхоКС, катетеризация камер сердца, ангиокардиография, вентрикулография.
Электрокардиограмма при дефекте межжелудочковой перегородки отражает перегрузку желудочков, наличие и степень выраженности легочной гипертензии. У взрослых больных могут регистрироваться аритмии (экстрасистолия, мерцание предсердий), нарушения проводимости (блокада правой ножки пучка Гиса, синдром WPW). Фонокардиография фиксирует высокочастотный систолический шум с максимумом в III-IV межреберье слева от грудины.
Эхокардиография позволяет выявить дефект межжелудочковой перегородки или заподозрить его по характерным нарушениям гемодинамики. Рентгенография органов грудной клетки при больших дефектах межжелудочковой перегородки обнаруживает усиление легочного рисунка, усиленную пульсацию корней легких, увеличение размеров сердца. Зондирование правых полостей сердца выявляет повышение давления в легочной артерии и правом желудочке, возможность проведения катетера в аорту, повышенную оксигенацию венозной крови в правом желудочке. Аортография проводится для исключения сопутствующих ВПС.
Дифференциальная диагностика дефекта межжелудочковой перегородки проводится с открытым атриовентрикулярным каналом, общим артериальным стволом, дефектом аортолегочной перегородки, изолированным стенозом легочной артерии, стенозом аорты, врожденной митральной недостаточностью, тромбоэмболией.
Лечение дефекта межжелудочковой перегородки
Асимптомное течение дефекта межелудочковой перегородки при его небольших размерах позволяет воздержаться от хирургического вмешательства и осуществлять динамическое наблюдение за ребенком. В ряде случаев возможно спонтанное закрытие дефекта межжелудочковой перегородки к 1-4 годам жизни или в более позднем возрасте. В остальных случаях показано хирургическое закрытие дефекта межжелудочковой перегородки, как правило, после достижения ребенком 3-х лет.
При развитии сердечной недостаточности и легочной гипертензии проводится консервативное лечение с помощью сердечных гликозидов, мочегонных препаратов, ингибиторов ангиотензинпревращающего фермента, кардиотрофиков, антиоксидантов.
Кардиохирургическое лечение дефекта межжелудочковой перегородки может быть радикальным и паллиативным. К радикальным операциям относятся ушивание малых дефектов межжелудочковой перегородки П-образными швами; пластика больших дефектов синтетической (тефлон, дакрон и др.) заплатой или биологической (консервированный ксеноперикард, аутоперикард) тканью; рентгенэндоваскулярная окклюзия дефекта межжелудочковой перегородки.
У грудных детей с выраженной гипотрофией, большим лево-правым шунтированием крови и множественными дефектами предпочтение отдается паллиативной операции, направленной на создание искусственного стеноза легочной артерии с помощью манжетки. Данный этап позволяет подготовить ребенка к радикальной операции по устранению дефекта межжелудочковой перегородки в более старшем возрасте.
Течение беременности при дефекте межжелудочковой перегородки
Женщины с небольшим дефектом межжелудочковой перегородки, как правило, в состоянии нормально выносить и родить ребенка. Однако, при больших размерах дефекта, аритмии, сердечной недостаточности или легочной гипертензии риск осложнений во время беременности значительно повышается. Наличие синдрома Эйзенменгера является показанием для искусственного прерывания беременности. У женщин с дефектом межжелудочковой перегородки имеется повышенная вероятность рождения ребенка с аналогичным или другим врожденным пороком сердца.
Перед планированием беременности пациентке с пороком сердца (оперированным или нет) необходимо проконсультироваться с акушером-гинекологом, кардиологом, генетиком. Ведение беременности у категории женщин с дефектом межжелудочковой перегородки требует повышенного внимания.
Прогноз при дефекте межжелудочковой перегородки
Естественное течение дефекта межжелудочковой перегородки в целом не позволяет надеяться на благоприятный прогноз. Продолжительность жизни при данном пороке зависит от величины дефекта и составляет в среднем около 25 лет. При больших и средних дефектах 50-80% детей умирают в возрасте до 6 мес. или 1 года от сердечной недостаточности, застойной пневмонии, бактериального эндокардита, нарушений ритма сердца, тромбоэмболических осложнений.
В редких случаях ДМЖП не оказывает существенного влияния на продолжительность и качество жизни. Спонтанное закрытие дефекта межжелудочковой перегородки наблюдается в 25-40% случаев, преимущественно при его малом размере. Однако даже в этом случае больные должны находиться под наблюдением кардиолога в связи с возможными осложнениями со стороны проводящей системы сердца и высоким риском возникновения инфекционного эндокардита.
Дефект перегородки между аортой и легочной артерией (Q21.4)
Порок чаще встречается в изолированном виде, в более редких случаях сочетается с другими врожденными пороками сердца (дефект межжелудочковой перегородки, вторичный дефект межпредсердной перегородки, перерыв дуги аорты, коарктация аорты, стеноз легочной артерии и др.).

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Типы дефекта аортолегочной перегородки (Meisner и соавторы):
1. Дефект находится на 10-20 мм выше полулунных клапанов легочной артерии, ветви которой располагаются нормально, дистальнее дефекта (наиболее частый вариант).
2. Дефект очень большой и доходит до дуги аорты, ветви легочной артерии отходят от вершины дефекта.
3. Дефект средних размеров, оба сосуда разделены ближе к бифуркации легочной артерии.
4. Аортолегочная перегородка отсутствует, ветви легочной артерии отходят от задней стенки общего сосуда (встречается очень редко).
Этиология и патогенез
Эпидемиология
Факторы и группы риска
Факторы риска, влияющие на формирование врожденных пороков сердца у плода
Семейные факторы риска:
- наличие детей с врожденными пороками сердца (ВПС);
- наличие ВПС у отца или ближайших родственников;
- наследственные заболевания в семье.
Клиническая картина
Клинические критерии диагностики
одышка по типу тахипноэ, отставание в физическом развитии, частые респираторные заболевания, сердечная недостаточность
Cимптомы, течение
Диагностика
2. Рентгенологическая картина достаточно характерна. Сердце, как правило, имеет большие размеры в результате увеличения обоих желудочков и гипертрофии левого предсердия. Расширена сосудистая тень, образованная аортой и значительно расширенной легочной артерией.
В начальном периоде заболевания легочный рисунок усилен. В дальнейшем, по мере развития легочной гипертензии, он меняется.
При резко выраженной легочной гипертензии отмечается характерная ствол и его магистральные ветви резко расширены, а по периферии легочных полей виден прозрачный легочный рисунок (легочный рисунок обеднен).
5. Ангиография. Хорошо выполненная аортография позволяет установить расположение дефекта, его размеры. В случае недостаточности аортального клапана наблюдается регургитация Регургитация - перемещение содержимого полого органа в направлении, противоположном физиологическому в результате сокращения его мышц.
контрастированной крови в левый желудочек.
6. Фонокардиография: регистрируется систолический шум различной интенсивности с пиком в первой половине или в середине систолы, иногда ему сопутствует диастолический шум с максимумом во II-III межреберье.
При значительном лево-правом сбросе на верхушке определяется мезодиастолический шум (относительный стеноз митрального клапана). II тон над легочной артерией усилен, слабо расщеплен или единый (при высокой легочной гипертензии).
При дефекте аортолегочной перегородки наблюдается расщепление II тона, в отличие от общего артериального ствола, при котором II тон всегда единый.
Лабораторная диагностика
Лабораторные исследования проводятся в предоперационном периоде с анализом газового и электролитного составов крови. Если ребенок длительно получал диуретики и сердечные гликозиды, необходимо исключить гипокалиемию.
Дифференциальный диагноз
Осуществляется дифференциальная диагностика дефекта аортолегочной перегородки с дефектом межжелудочковой перегородки, открытым артериальным протоком, общим артериальным стволом.
Лечение
Медицинская коррекция дефекта аортолегочной перегородки осуществляется в течение нескольких дней или недель, чтобы позволить избирательно запланировать метод хирургического вмешательства.
Хирургическая операция необходима для предотвращения развития легочной сосудистой обструктивной болезни, поскольку аортолегочное окно не закрывается спонтанно. Для обеспечения симптоматической пользы, перед хирургической коррекцией обычно назначаются дигоксин и мочегонные средства.
Прогноз
Профилактика
Профилактика возникновения врожденных пороков сердца (ВПС) очень сложна и в большинстве случаев сводится к медико-генетическому консультированию и разъяснительной работе среди людей, относящихся к группе повышенного риска заболевания. К примеру, в случае, когда 3 человека, состоящие в прямом родстве, имеют ВПС, вероятность появления следующего случая составляет 65-100% и беременность не рекомендуется. Нежелателен брак между двумя людьми с ВПС. Помимо этого необходимо тщательное наблюдение и исследование женщин, имевших контакт с вирусом краснухи или имеющих сопутствующую патологию, которая может привести к развитию ВПС.
Профилактика неблагоприятного развития ВПС:
- своевременное выявление порока;
- обеспечение надлежащего ухода за ребенком с ВПС;
- определение оптимального метода коррекции порока (чаще всего, это хирургическая коррекция).
Обеспечение необходимого ухода является важной составляющей в лечении ВПС и профилактике неблагоприятного развития, так как около половины случаев смерти детей до 1-го года во многом обуславливаются недостаточно адекватным и грамотным уходом за больным ребенком.
Специальное лечение ВПС, (в том числе, кардиохирургическое) должно проводиться в наиболее оптимальные сроки, а не немедленно по выявлению порока, и не в самые ранние сроки. Исключение составляют только критические случаи угрозы жизни ребенка. Оптимальные сроки зависят от естественного развития соответствующего порока и от возможностей кардиохирургического отделения.
Профилактика осложнений ВПС определяется характером осложнений.
Грозным осложнением ВПС является инфекционный эндокардит Инфекционный эндокардит - это инфекционное полипозно-язвенное воспаление эндокарда, сопровождающееся образованием вегетаций на клапанах или подклапанных структурах, их деструкцией, нарушением функции и формированием недостаточности клапана
Подробно , который может осложнить любой вид порока и может появиться уже в дошкольном возрасте.
Рекомендуется ограничить назначение антибиотикопрофилактики инфекционного эндокардита группам пациентов с наибольшей вероятностью развития инфекционного эндокардита:
1. Пациенты после протезирования клапана сердца.
2. Инфекционный эндoкардит в анамнезе.
3. Пациенты со следующими врожденными пороками:
- "синие" пороки, без предшествующей хирургической коррекции или с остаточными дефектами, паллиативными шунтами или кондуитами;
- пороки после хирургической коррекции с применением искусственных материалов до 6 месяцев (до тех пор, пока не произошла эндотелизация);
- если после операции на сердце или чрескожной коррекции есть остаточный дефект в месте имплантации искусственного материала или устройства.
Дефект аортолегочной перегородки
Дефект аортолегочной перегородки (аортолегочное окно, аортопульмональный септальный дефект, аортолегочный свищ или фенестрация) обусловлен наличием отверстия, посредством которого аорта и ствол легочной артерии сообщаются между собой. Дефект аортолегочной перегородки - редкая аномалия, составляющая в кардиологии 0,2−0,3% случаев всех врожденных пороков сердца.
Причины дефекта аортолегочной перегородки
Аотролегочное окно является следствием нарушения эмбриогенеза, в результате которого не формируется полноценная аортолегочная перегородка. Разделение эмбрионального артериального ствола на аорту и легочный ствол происходит между 6-7 неделями внутриутробного развития плода. Нарушение этого процесса приводит к возникновению дефекта аортолегочной перегородки.
Причины развития дефекта аортолегочной перегородки аналогичны таковым при формировании других врожденных пороков сердца. Факторами, нарушающими формирование сердца плода на ранних этапах внутриутробного развития, могут выступать инфекции беременной (краснуха, ветряная оспа, герпес, грипп, сифилис и др.), прием алкоголя и токсичных лекарственных препаратов, соматические заболевания матери (сахарный диабет), патологическое течение беременности (угроза самопроизвольного прерывания, сильные токсикозы), наследственность, ионизирующее излучение и пр.
Особенности гемодинамики при дефекте аортолегочной перегородки
При дефекте аортолегочной перегородки кровь под большим давлением поступает из восходящей аорты в легочную артерию. Выраженный артериовенозный (лево-правый) сброс рано приводит к развитию легочной гипертензии, которая присутствует у большинства больных с дефектом аортолегочной перегородки. Когда сопротивление в малом и большом круге кровообращения выравнивается, возникает перекрестный, а затем и веноартериальный (право-левый) сброс крови, что сопровождается развитием цианоза.
Классификация дефекта аортолегочной перегородки
С учетом критериев локализации, формы отверстия и его отношения к легочным артериям различают следующие анатомические типы дефекта аортолегочной перегородки (В. И. Бураковский и соавт., НЦССХ им. А. Н. Бакулева):
I тип - дефект имеет форму протока с хорошо выраженными полюсами; расположен в середине аортолегочной перегородки в удалении от синусов Вальсальвы. Левая и правая легочные артерии отходят дистальнее аортолегочного дефекта.
II тип - дефект имеет форму окна; расположен в проксимальной (нижней) части аортолегочной перегородки над синусами Вальсальвы. Аортолегочная перегородка частично сформирвоана в своей дистальной части; ветви легочной артерии отходят нормально, дистальнее дефекта.
III тип - дефект имеет форму окна; расположен в дистальной (верхней) части аортолегочной перегородки в удалении от синусов Вальсальвы. Аортолегочная перегородка частично сформирвоана в своей проксимальной части. Ветви легочной артерии отходят в зоне вершины дефекта.
IV тип - дефект имеет форму окна; расположен в дистальной (верхней) части аортолегочной перегородки, на уровне отхождения правой ветви легочного ствола. При данном типе дефекта аортолегочной перегородки аорта сообщается как с правой легочной артерией, так и с общим легочным стволом.
V тип - полное отсутствие аортолегочной перегородки, однако клапаны аорты и легочной артерии сформированы и разобщены. Легочные артерии отходят от общего магистрального сосуда, берущего начало от основания сердца.
Симптомы дефекта аортолегочной перегородки
У детей первых месяцев жизни ранним симптомом дефекта аортолегочной перегородки служит одышка по типу тахипноэ. Характерно отставание в физическом развитии, быстрая утомляемость, частые ОРВИ, повторные пневмонии.
На стадии преимущественного артериовенозного сброса кожные покровы физиологической окраски или несколько бледные. Небольшой цианоз может появляться при крике, плаче, явлениях сердечной и дыхательной недостаточности. При развитии перекрестного и веноартериального сброса крови цианоз кожи и видимых слизистых становится выраженным и постоянным. У 70% пациентов с дефектом аортолегочной перегородки обнаруживается деформация грудной клетки по типу «сердечного горба», формирование которого связано с увеличением правого желудочка, работающего в режиме гиперфункции.
При дефекте аортолегочной перегородки небольшого диаметра и у детей длительное время сохраняется удовлетворительное состояние. При больших дефектах рано развивается легочная гипертензия. Продолжительность жизни больных с дефектом аортолегочной перегородки зависит от размеров отверстия и составляет от нескольких месяцев до 30-40 лет (в среднем - 14 лет).
Диагностика дефекта аортолегочной перегородки
При осмотре пациентов с дефектом аортолегочной перегородки отмечается отставание в массе и росте, выпячивание грудной клетки в виде сердечного горба. Перкуторно выявляется расширение границ сердечной тупости в обе стороны; при аускультации выслушивается систолический шум с диастолическим компонентом, изменение сердечных тонов; пальпаторно определяется систолическое дрожание во II-III межреберье.
С помощью фонокардиографии зафиксируется аускультативная картина, изложенная выше. Электрокардиография выявляет признаки перегрузки правых отделов сердца, гипертрофию обоих желудочков, отклонение ЭОС вправо. Рентгенологическая картина при дефекте аортолегочной перегородки типична: увеличение тени сердца, расширение тени аорты и легочной артерии, усиление легочного рисунка в ранний период заболевания и его обеднение при развитии легочной гипертензии. С помощью эхокардиографии обнаруживается дефект в аортолегочной перегородке, устанавливается расположение окна, его размеры, исключаются сопутствующие пороки сердца.
Путем зондирования полостей сердца определяется выраженность легочной гипертензии, величина сброса крови, исследуется степень насыщения крови кислородом в легочной артерии. Диагностическим признаком дефекта аортолегочной перегородки является возможность проведения катетера из легочной артерии через отверстие в начальные отделы восходящей аорты. При выполнении аортографии видно попадание контрастного вещества из восходящей аорты в ствол легочной артерии. Дифференциальная диагностика при дефекте аортолегочной перегородки проводится с ДМЖП, общим артериальным стволом, открытым артериальным протоком.
Лечение дефекта аортолегочной перегородки
Поскольку спонтанное закрытие дефекта аортолегочной перегородки невозможно, единственным способом лечения врожденного порока сердца является кардиохирургическая операция. При большом дефекте аортолегочной перегородки операция выполняется в ранние сроки - до 1 года.
Закрытие аортолегочного окна производится путем ушивания или пластики дефекта с помощью заплаты доступами через просвет аорты или легочной артерии, либо с обеих сторон. Операция выполняется в условиях ИК, гипотермии и фармакохолодовой кардиоплегии.
При дефекте аортолегочной перегородки I типа производится перевязка протока. Невозможность выполнения радикальной операции при легочной гипертензии диктует необходимость выполнения двухэтапного вмешательства: 1 - сужение легочного ствола или легочной артерии; 2 - снятие суживающей манжетки и радикальная операция.
Интраоперационная летальность составляет 3%; послеоперационная достигает 15-20%.
Прогноз при дефекте аортолегочной перегородки
Большие размеры дефекта аортолегочной перегородки обусловливают злокачественное течение порока: 25-30% пациентов погибают в течение первого полугода жизни. Причинами смерти пациентов с дефектом аортолегочной перегородки обычно служат сердечная недостаточность, разрыв аневризмы легочной артерии в полость перикарда, тампонада сердца (гемоперикард), тромбоэмболии, бактериальный эндокардит.
У выживших больных отсутствие хирургического лечения приводит к развитию необратимых изменений в легких, делающих невозможным хирургическое лечение в более поздние сроки. В литературе встречаются единичные указания на больных с дефектом аортолегочной перегородки, доживших до 35−40 лет.
Аномальный дренаж легочных вен
Аномальный дренаж легочных вен - это врожденная патология сердца, морфологическую основу которой составляет аномальное впадение легочных вен в правое предсердие либо входящие в него полые вены. Аномальный дренаж легочных вен проявляется утомляемостью, отставанием в физическом развитии, болями в сердце, одышкой, повторными пневмониями. Для диагностики аномального дренажа легочных вен проводится рентгенография, ЭКГ, УЗИ сердца, зондирование сердца, ангиопульмонография, атрио- и вентрикулография, МРТ. Варианты хирургической коррекции аномального дренажа легочных вен различаются в зависимости от типа порока.



Аномальный дренаж легочных вен - врожденный порок сердца, при котором имеет место впадение устьев всех или отдельных легочных вен в правое предсердие, венечный синус или полые вены. Аномальный дренаж легочных вен составляет 1,5-3% всех ВПС в кардиохирургии с преобладанием у лиц мужского пола.
Чаще всего аномальный дренаж легочных вен сочетается с дефектом межпредсердной перегородки (ДМПП) и открытым овальным окном; в 20% случаев - с общим артериальным стволом, ДМЖП, транспозицией магистральных сосудов, тетрадой Фалло, стенозом легочной артерии, гипоплазией левых отделов сердца, единственным желудочком сердца, декстрокардией. Из экстракардиальной патологии у пациентов с аномальным дренажом легочных вен встречаются дивертикулы кишечника, пупочные грыжи, поликистоз почек, гидронефроз, подковообразная почка, а также различные пороки развития костной и эндокринной систем.

Причины
Общие причины, формирующие аномальный дренаж легочных вен, не отличаются от таковых при других ВПС. Непосредственное разобщение легочных вен с левым предсердием может быть связано с двумя факторами:
- отсутствием их соединения;
- ранней атрезией общей легочной вены.
В первом случае под воздействием неблагоприятных условий левопредсердный вырост не связывается должным образом с венозными сплетениями зачатка легкого, что приводит к формированию аномального венозного дренажа. При ранней атрезии имеет место первоначальное соединение общей легочной вены и легочного сосудистого ложа, однако в дальнейшем происходит облитерация их просвета, поэтому венозный легочный возврат начинает осуществляться через другие доступные коллатеральные пути.
Патогенез
В антенатальном периоде порок обычно не имеет гемодинамических проявлений, поскольку внутрисердечное кровообращение у плода подразумевает поступление крови из правого предсердия в левое (через открытое овальное окно) и в боталлов проток. После рождения выраженность гемодинамических нарушений определяют форма (полная или частичная), вариант аномального дренажа легочных вен, а также сочетание порока с другими дефектами сердца.
При частичной форме аномального дренажа легочных вен гемодинамические нарушения аналогичны таковым при межпредсердных дефектах. Определяющая роль среди них принадлежит патологическому артерио-венозному сбросу крови, приводящему к увеличению объема крови в легочном круге кровообращения.

При впадении устьев всех легочных вен в венозную систему большого круга кровообращения или правое предсердие говорят о полном (тотальном) аномальном дренаже легочных вен. Если в правое предсердие или большой круг дренируется одна или несколько легочных вен, такая форма порока называется частичной. Чаще всего (в 97% случаев) аномально дренируются вены, отходящие от правого легкого.
На основании уровня впадения легочных вен аномальный дренаж классифицируется на 4 анатомических типа (варианта).
- I вариант - супракардиальный (надсердечный). Легочные вены общим коллектором или по-отдельности дренируются в верхнюю полую вену или ее ветви (непарную вену, левую безымянную либо добавочную верхнюю полую вену).
- II вариант - интракардиальный (сердечный). Аномальный дренаж легочных вен происходит в правое предсердие или венечный синус.
- III вариант - субкардиальный, инфракардиальный (подсердечный). Легочные вены впадают в нижнюю полую или воротную вену (редко - в лимфатический проток).
- IV вариант - смешанный. Аномальный дренаж легочных вен в венозную систему осуществляется на различных уровнях в разных сочетаниях.
Симптомы
В основе клинических проявлений аномального дренажа легочных вен лежат анатомо-гемодинамические особенности: уровень общелегочного сопротивления, степень обструкции венозного возврата, размеры межпредсердной коммуникации, функционирование миокарда правого желудочка. При отсутствии дефекта в межпредсердной перегородке или его чрезвычайно маленьком размере порок несовместим с жизнью - в этом случае спасти ребенка позволяет только экстренная эндоваскулярная баллонная атриосептостомия по Рашкинду.
У детей с аномальным дренажом легочных вен отмечаются частые повторные пневмонии и ОРВИ, малая прибавка в массе, одышка, легкий цианоз, кашель, быстрая утомляемость, отставание в физическом развитии, боли в сердце, тахикардия. При выраженной легочной гипертензии уже в раннем детстве развиваются выраженный цианоз, сердечный горб и сердечная недостаточность.
Аускультативная картина аномального дренажа легочных вен напоминает ДМПП и характеризуется негрубым систолическим шумом в проекции легочной артерии, расщеплением II тона. После консультации кардиохирурга проводится:
- Электрокардиография. Данные ЭКГ свидетельствуют о перегрузке правых отделов, неполной блокаде правой ножки пучка Гиса; ЭОС отклонена вправо. Фонокардиография соответствует всем признакам ДМПП.
- Рентген. При анализе результатов рентгенографии грудной клетки обращает внимание расширение границ сердца вправо, выбухание дуги легочной артерии, усиление легочного рисунка. Достоверным признаком аномального дренажа легочных вен в нижнюю полую вену является симптом «турецкой сабли».Правая атриография, вентрикулография, ангиопульмонография, флебография ВПВ позволяют проследить движение контраста через малый круг кровообращения в правое предсердие или полые вены.
- УЗИ сердца. По данным ЭхоКГ устья легочных вен в левом предсердии не обнаруживаются; выявляется дилатация правого желудочка, уменьшенные размеры левых отделов сердца и другие косвенные признаки аномального дренажа легочных вен. Старшим детям и взрослым проводится чреспищеводная ЭхоКГ.
- Инвазивная диагностика. При зондировании полостей сердца катетер из правого предсердия или полой вены проводится в легочную вену. На данном этапе диагностики возможно установить локализацию впадения и количество аномально дренирующихся легочных вен.
У пациентов с аномальным дренажом легочных вен в дифференциально-диагностическом плане необходимо исключить атрезию митрального или аортального клапана, митральный стеноз, изолированный ДМПП, трехпредсердное сердце, стеноз легочных вен, транспозицию магистральных сосудов, лимфангиоэктазию.

Лечение аномального дренажа легочных вен
Естественное течение тотального аномального дренажа легочных вен неблагоприятно: 80% детей погибает в первый год жизни. Пациенты с частичным дренажом легочных вен могут дожить до 20-30 лет. Гибель больных связана с тяжелой сердечной недостаточностью или легочными инфекциями. Результаты хирургической коррекции аномального дренажа легочных вен удовлетворительные, однако среди новорожденных интра- и послеоперационная летальность остается высокой.
2. Сравнительный анализ отдаленных результатов коррекции частичного аномального дренажа правых верхних легочных вен в верхнюю полую вену/ Связов Е.А.// Сибирский журнал клинической и экспериментальной медицины. - 2017.
3. Восстановление синусового ритма после коррекции частичного аномального дренажа легочных вен/ Сабирова Д.Р.// Казанский медицинский журнал. - 2009.
Открытое овальное окно (отверстие) в сердце: причины, закрытие, прогноз
Согласно статистическим данным распространенность открытого овального окна (ООО) в сердце отличается в разных возрастных категориях. Например, у детей до года это считается вариантом нормы, так как по данным УЗИ овальное отверстие обнаруживается у 40% младенцев. У взрослых данная аномалия встречается в 3,65% популяции. Однако, у людей с множественными пороками сердца зияющее овальное окно регистрируется в 8,9% случаев.
Что такое “овальное окно” в сердце?
Овальное окно представляет собой отверстие с клапанной заслонкой, расположенное в перегородке между правым и левым предсердиями. Самое главное отличие данной аномалии от дефекта в межпредсердной перегородке (ДМПП) заключается в том, что овальное окно снабжено клапаном и локализуется непосредственно в области овальной ямки сердца, в то время как при ДМПП именно отсутствует часть перегородки.
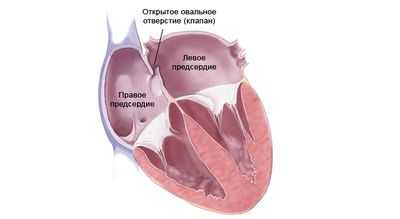
расположение овального окна в сердце
Циркуляция крови у плода и роль овального окна
Кровообращение у плода происходит иначе, чем у взрослого человека. Во время внутриутробного периода у малыша функционируют так называемые “фетальные” (плодовые) структуры в сердечно-сосудистой системе. К ним относятся овальное окно, аортальный и венозный протоки. Все эти структуры необходимы по одной простой причине: плод во время беременности не дышит воздухом, а значит, его легкие не участвуют в процессе насыщения крови кислородом.
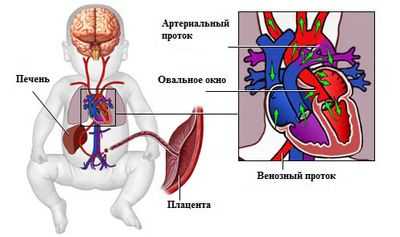
кровообращение и устройство сердца плода
Но обо всем по порядку:
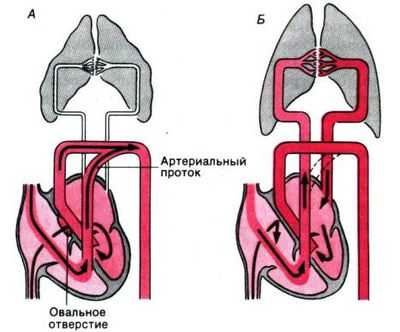
- Итак, обогащенная кислородом кровь поступает в организм плода через пупочные вены, одна из которых впадает в печень, а другая в нижнюю полую вену через так называемый венозный проток. Проще говоря, чистая артериальная кровь попадает только к печени плода, ведь во внутриутробном периоде она осуществляет важную кроветворную функцию (именно по этой причине печень занимает большую часть брюшной полости у малыша).
- Затем два потока смешанной крови от верхней и нижней части туловища впадают в правое предсердие, где благодаря функционирующему овальному окну основная часть крови поступает в левое предсердие.
отличия кровообращение плода (А) и рожденного ребенка в норме (Б)
Оставшаяся кровь попадает в легочную артерию. Но возникает вопрос: зачем? Ведь мы уже знаем, что малый круг кровообращения у плода не осуществляет функцию оксигенации (насыщение кислородом) крови. Именно по этой причине между легочным стволом и дугой аорты есть третья фетальная коммуникация - это аортальный проток. Через него и происходит сброс оставшейся крови из малого круга в большой.
Непосредственно после родов, когда новорожденный делает первый вдох, давление в легочных сосудах возрастает. В результате основная роль овального окна сбрасывать кровь в левую половину сердца нивелируется.
Видео: анатомия овального окна в сердце плода и новорожденного
Овальное окно самостоятельно не закрывается, каковы причины?
Основной причиной такой патологии является генетический фактор. Доказано, что незаращение клапанной заслонки сохраняется у людей с предрасположенностью к соединительнотканной дисплазии, что передается по наследству. Именно по этой причине у данной категории пациентов можно обнаружить и другие признаки снижения прочности и образования коллагена в соединительной ткани (патологическая подвижность суставов, снижение эластичности кожи, пролапс (“провисание”) сердечных клапанов).

Однако, на незаращение овального окна влияют и другие факторы:
- Неблагоприятная экология;
- Прием во время беременности некоторых лекарственных препаратов. Чаще всего данную патологию вызывают нестероидные противовоспалительные средства (НПВС). Доказано, что эти препараты вызывают снижение уровня простагландинов в крови, которые ответственны за закрытие овального окна. При этом прием НПВС опасен в поздние сроки гестации, что является причиной, по которой овальное окно не закрылось;
- Прием алкоголя, а также курение во время беременности;
- Преждевременные роды (у недоношенных детей чаще диагностируется эта патология).
Виды овального окна по степени незаращения
- Если размеры отверстия не превышают 5-7 мм, то обычно в такой ситуации обнаружение овального окна является находкой при эхокардиографии. Традиционно принято считать, что клапанная заслонка защищает от обратного потока крови. Именно поэтому такой вариант является гемодинамически незначимым и проявляется только при высокой физической нагрузке.
- Иногда встречаются случаи, когда овальное окно настолько большое (превышает 7-10 мм), что размеров клапана не хватает, чтоб прикрывать данное отверстие. В таких ситуациях принято говорить о “зияющем” овальном окне, что по клиническим признакам может практически не отличаться от ДМПП. Поэтому в этих ситуациях граница весьма условна. Однако, если рассматривать с точки зрения анатомии, то при ДМПП нет клапанной заслонки.
Как проявляется заболевание?
При небольшом размере овального окна внешние проявления могут отсутствовать. Поэтому о серьезности незаращения может судить лечащий врач.
Для детей грудного возраста при открытом овальном окне характерно:
цианоз - характерный признак сердечных пороков
Посинение губ, кончика носа, пальцев при плаче, натуживании, кашле (цианоз);
У взрослых с патологией также может появиться синюшность губ при:
- Физических нагрузках, которые чреваты увеличением давления в легочных сосудах (длительная задержка дыхания, плавание, ныряние);
- Тяжелом физическом труде (занятия тяжелой атлетикой, акробатической гимнастикой);
- При заболеваниях легких (бронхиальная астма, муковисцидоз, эмфизема легких, ателектаз легкого, пневмония, при надсадном кашле);
- При наличии других пороков сердца.

При выраженном овальном отверстии (более 7-10 мм) внешние проявления заболевания следующие:
- Частые обмороки;
- Появление синюшности кожи даже при умеренных физических нагрузках;
- Слабость;
- Головокружения;
- Отставание ребенка в физическом развитии.
Методы диагностики
Эхокардиография является “золотым” стандартом и самым информативным методом диагностики данной патологии. Обычно выявляются следующие признаки:
- В отличие от ДМПП при открытом овальном окне выявляется не отсутствие части перегородки, а видно лишь ее клиновидное истончение.
- Благодаря цветовой допплерографии можно увидеть “завихрения” потока крови в области овального окна, а также незначительный сброс крови из правого предсердия в левое.
- При небольшом размере овального отверстия нет признаков увеличения стенки предсердий, как это характерно для ДМПП.
Максимально информативным является ультразвуковое исследование сердца, проводимое не через грудную клетку, а так называемая чреспищеводная эхокардиокардиография. При данном исследовании ультразвуковой датчик вводится в пищевод, в результате чего все структуры сердца видны гораздо лучше. Это объясняется анатомической близостью пищевода и сердечной мышцы. Особенно актуально применение этого метода при ожирении пациента, когда визуализация анатомических структур затруднена.
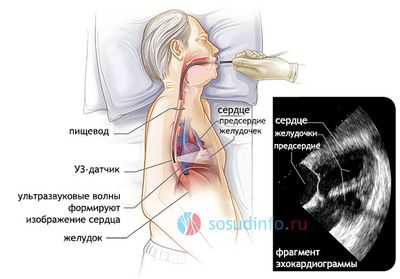
чреспещиводная ЭхоКГ - наиболее информативный метод выявления ООО
Помимо УЗИ сердца могут быть использованы и другие методы диагностики:
- На электрокардиограмме могут выявляться признаки блокады ножек пучка Гиса, а также нарушение проводимости в предсердиях.
- При большом овальном отверстии возможны изменения на рентгенограмме органов грудной клетки (незначительное увеличение предсердий).
Чем опасна патология?
- Людям из группы риска следует избегать тяжелых физических нагрузок, а также выбора таких профессий, как аквалангист, водолаз, дайвер. Доказано, что при наличии этой патологии вероятность развития кессонной болезни в 5 раз, чем среди здорового населения.
- Кроме того, у данной категории лиц возможно развитие такого феномена, как парадоксальная эмболия. Данное явление возможно у людей со склонностью к тромбообразованию в сосудах нижних конечностей. Тромб, оторвавшийся от стенки сосуда, может через овальное отверстие попасть в большой круг кровообращения. В результате возможна закупорка сосудов мозга, сердца, почек и других органов. Если размеры тромба велики, то это может стать причиной смерти.
- Важно помнить, у людей с открытым овальным окном выше вероятность развития такого заболевания, как септический эндокардит. Связано это с тем, что на стенках клапанной заслонки могут образовываться микротромбы.
Методы лечения и профилактики осложнений
При благоприятном течении патологии и при небольшом размере овального окна по данным УЗИ сердца специфического лечения не требуется. Однако, данная категория людей должна состоять на учете у кардиолога и 1 раз в год проходить обследование сердца.
- Учитывая вероятность развития тромбоэмболии, пациентам из группы риска необходимо также исследовать вены нижних конечностей (с оценкой проходимости вен, наличие или отсутствие тромбов в просвете сосудов).
- При проведении любых оперативных вмешательств у пациентов с открытым овальным окном необходимо проводить профилактику тромбоэмболии, а именно: эластическое бинтование нижних конечностей (ношение компрессионного трикотажа), а также прием антикоагулянтов за несколько часов до операции. (О наличии дефекта нужно знать и предупреждать лечащего врача).
- Важно соблюдать режим труда и отдыха, а также дозировать физические нагрузки.
- Санаторно-курортное лечение (положительно влияет электрофорез с сульфатом магния).
При наличии тромбов в нижних конечностях эти пациенты нуждаются в постоянном контроле свертывающей системы крови (особенно важны такие показатели, как международное нормализованное отношение, активированное частичное тромбиновое время, протромбиновый индекс). Также в такой ситуации обязательно наблюдение у гематолога и флеболога.

Иногда у пациентов с открытым овальным окном наблюдаются признаки нарушения проводимости сердца по данным ЭКГ, а также нестабильное артериальное давление. В таких ситуациях можно принимать препараты, улучшающие метаболические процессы в ткани сердечной мускулатуры:
- Лекарственные средства, содержащие магний (“Магне-В6”, “Магнерот”);
- Препараты, улучшающие проводимость нервного импульса (“Панангин”, “Карнитин”, витамины группы В);
- Препараты, активирующие биоэнергетические процессы в сердце (“Коэнзим”).
Хирургическое лечение
Оперативное вмешательство может потребоваться при большом диаметре овального окна с током крови в левое предсердие.
В настоящий момент широкое распространение получила эндоваскулярная хирургия.
Суть вмешательства заключается в том, что через бедренную вену устанавливается тонкий катетер, который через сосудистую сеть проводится до правого предсердия. Контроль за движением катетера осуществляется с помощью рентген-аппарата, а также ультразвуковым датчиком, установленным через пищевод. При достижении области овального окна через катетер проводят так называемые окклюдеры (или графты), которые представляют собой “заплатку”, закрывающую зияющее отверстие. Единственным недостатком метода является то, что окклюдеры могут вызвать местную воспалительную реакцию в ткани сердца.
эндоваскулярное закрытие овального окна в сердце
В связи с этим в последнее время используют рассасывающийся пластырь BioStar. Он проводится через катетер и раскрывается по типу “зонтика” в полости предсердия. Особенностью пластыря является способность вызвать регенерацию тканей. После прикрепления этого пластыря в области отверстия в перегородке, он рассасывается в течение 30 дней, а овальное окно замещается собственными тканями организма. Данная методика высокоэффективна и уже получила широкое распространение.
Прогноз заболевания
При овальном окне менее 5 мм прогноз, как правило, благоприятный. Однако, как уже было сказано выше, большой диаметр овального отверстия подлежит хирургической коррекции.
Беременность и роды у женщин с пороком

При беременности значительно увеличивается нагрузка на сердце. Происходит это по нескольким причинам:
- Возрастает объем циркулирующей крови, к концу беременности он превышает исходный уровень на 40%;
- Растущая матка начинает занимать большую часть брюшной полости и ближе к родам сильно давит на диафрагму. В результате у женщины появляется одышка.
- Во время вынашивания ребенка появляется так называемый “третий круг кровообращения” - плацентарно-маточный.
Все эти факторы способствуют тому, что сердце начинает чаще биться, а также повышается давление в легочной артерии. В связи с этим у женщин с этой аномалией в сердце возможны неблагоприятные осложнения. Поэтому беременные с данной патологией подлежат наблюдению кардиолога.
Берут ли молодых людей с открытым овальным окном в армию?
Несмотря на то, что в большинстве случаев данная аномалия сердца протекает без каких-либо клинических симптомов, молодые люди с открытым овальным окном относятся к категории В с ограничением годности к службе в армии. Связано это прежде всего с тем, что при высоких физических нагрузках велика вероятность развития осложнений.
Выводы
В связи с развитием дополнительных методов исследования выявление такой аномалии, как открытое овальное окно значительно увеличилось.
В большинстве случаев эту патологию обнаруживают как случайную находку при исследовании. Однако, пациенты обязательно должны быть информированы о наличии у них открытого овального окна, также им необходимо знать об определенных ограничениях в физическом труде, а также в выборе профессии.
Особого внимания заслуживает наличие овального отверстия больших размеров, которое по сути является аналогом дефекта межпредсердной перегородки. В данной ситуации пациентам рекомендована хирургическая коррекция.
Читайте также:
- Влияние инсулина на обмен углеводов. Обмен глюкозы под действием инсулина
- Рентгенотерапия бронхэктатической болезни. Виды операций при бронхоэктазиях
- Гемопоэтические факторы роста. Эритропоэтин
- Высокий заднебоковой инфаркт. Глубокий перегородочный инфаркт на ЭКГ
- Советская хирургия туберкулеза легких. Перевязка легочной артерии при туберкулезе легкого
