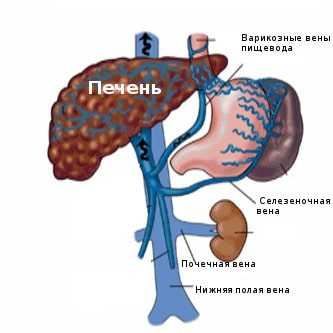
Доступ и ход операции спленоренального шунтирования при портальной гипертензии
Добавил пользователь Владимир З. Обновлено: 28.01.2026
Больница Центросоюза Российской Федерации, Москва, кафедра эндоскопической хирургии ФДПО ФГБОУ ВО «МГМСУ им. А.И. Евдокимова» Минздрава России, Москва, Россия
Кафедра эндоскопической хирургии факультета последипломного образования Московского государственного медико-стоматологического университета
кафедра эндоскопической хирургии ФПДО МГМСУ
Современные представления о хирургических методах лечения больных с варикозно-расширенными венами пищевода и желудка
Журнал: Эндоскопическая хирургия. 2016;22(5): 43‑48
На сегодняшний день кровотечение из варикозно-расширенных вен пищевода и желудка у больных циррозом печени — главная причина летального исхода и самое грозное осложнение портальной гипертензии. В связи с этим необходимость своевременного лечения и проведение профилактики данного заболевания являются основным показанием к хирургическому вмешательству.
Варикозное расширение вен пищевода и желудка встречается у 90% больных циррозом печени, в 35% случаев оно осложняется кровотечениями. В механизме развития варикозной трансформации вен пищевода и желудка важную роль играет затруднение оттока крови по воротной вене, в результате чего формируются 4 основные группы портокавальных анастомозов: 1) гастроэзофагеальные; 2) забрюшинные; 3) между левой ветвью воротной вены и сосудами передней брюшной стенки; 4) между прямокишечным сплетением и нижней полой веной. Но для клиницистов наиболее важен гастроэзофагеальный коллатеральный путь, предопределяющий основное направление хирургического лечения портальной гипертензии [1].
Важно помнить, что хирургические методы лечения портальной гипертензии имеют паллиативный характер, они не направлены на лечение основного заболевания. Их цель — профилактика и ликвидация одного из серьезных симптомов портальной гипертензии — кровотечения из варикозно-расширенных вен пищевода и желудка. Единственный радикальный метод лечения портальной гипертензии у больных циррозом печени на сегодняшний день — трансплантация печени.
Существует 3 подхода к предупреждению кровотечений из варикозно-расширенных вен пищевода и желудка [1].
Вторым подходом в предупреждении кровотечений из варикозно-расширенных вен пищевода и желудка является декомпрессия портальной системы с помощью формирования сосудистых портокавальных анастомозов (дистальный спленоренальный анастомоз, проксимальный спленоренальный анастомоз, Н-спленоренальный анастомоз), а также эндоваскулярный способ формирования шунта — операция TIPS (Transjugular intrahepatic portosystemic shunt, трансъюгулярное внутрипеченочное портосистемное шунтирование) [1].
Существуют 3 вида открытых сосудистых операций по формированию портокавальных шунтов: 1) тотальное шунтирование; 2) парциальное шунтирование; 3) селективное шунтирование [4].
При тотальном шунтировании формируется портокавальный анастомоз большого диаметра (15—25 мм) между нижней полой и воротной, селезеночной или верхней брыжеечными венами. Наиболее распространенная операция при этом — проксимальный спленоренальный анастомоз (анастомоз между селезеночной и левой почечной веной конец в бок) в сочетании со спленэктомией. Одним из условий для формирования шунта является длина селезеночной вены не менее 4—6 см. При выполнении данной операции могут быть получены удовлетворительные результаты, однако летальность составляет 10—35%, энцефалопатия развивается у 3,5—28% больных, возможно развитие послеоперационного панкреатита, а рецидивы кровотечений возникают у 10—27% в связи с тромбозом анастомоза и неполной декомпрессией бассейна воротной вены [2, 5].
При селективном шунтировании происходит избирательная декомпрессия селезеночного и гастроэзофагеального бассейнов. При данном типе шунтирования формируется дистальный спленоренальный анастомоз (операция W. Warren). В литературе имеются работы с описанием данной операции, выполненной лапароскопическим доступом [6]. Селезеночную вену мобилизуют по всему периметру с целью сохранения разобщенности желудочно-селезеночного и брыжеечного бассейнов, однако это чревато повреждением поджелудочной железы и развитием послеоперационного панкреатита, который приводит к тромбозу анастомоза и рецидиву кровотечения из варикозных вен. Сохранение воротного кровотока позволяет снизить частоту развития острой печеночной недостаточности и энцефалопатии в раннем послеоперационном периоде. Поэтому данная операция характеризуется более высокой эффективностью и меньшим процентом осложнений, чем при тотальном шунтировании [5, 7].
При парциальном портокавальном шунтировании формируют анастомоз бок в бок или Н-типа малого диаметра (8—15 мм), выполняемые с использованием любого сосуда портальной системы, кроме воротной вены. При данном типе операции формируется Н-спленоренальный анастомоз, который считается лучшим из всех парциальных портокавальных анастомозов, так как именно в этом случае происходит декомпрессия портальной системы (на 25% интраоперационно снижается давление в портальной вене), а также сохраняется редуцированный кровоток для поддержания функции печени [5, 8].
Операция TIPS впервые разработана J. Rosch в 1969 г. в эксперименте на животных [9]. Впервые в клинической практике операцию TIPS в современном виде выполнил G. Richter в 1998 г. [10]. Данная операция заключается в малоинвазивном способе снижения портального давления путем создания внутрипеченочного соустья между крупными печеночными венами и ветвями воротной вены при помощи чрескожной имплантации металлического стента. Основные показания для данного вмешательства — безуспешность консервативного и эндоскопического методов лечения кровотечений из варикозно-расширенных вен пищевода и желудка, асцит, рефрактерный к диуретической терапии, синдром Budd—Chiari. Одним из серьезных осложнений данной операции являются стенозирование и тромбоз шунта, приводящие к рецидивам кровотечений [11, 12].
Третий подход в профилактике кровотечений из варикозно-расширенных вен пищевода и желудка заключается в разобщении портокавальных связей с помощью хирургических операций, в том числе и малоинвазивных, в целях уменьшения притока крови к варикозно-расширенным венам кардиоэзофагеальной области. К этим операциям относятся деваскуляризация пищевода и желудка, транссекция пищевода и желудка, прошивание варикозных узлов желудка и нижней трети пищевода, резекция пищевода и желудка. К малоинвазивным вмешательствам относятся эндоскопическое склерозирование и лигирование варикозно-расширенных вен пищевода и желудка, эндоваскулярные операции (редукция селезеночного кровотока, редукция печеночного кровотока, эмболизация кардиальных вен желудка, операция BRTO (Balloon-occluded Retrograde Transvenous Obliteration) — ретроградная окклюзия варикозных вен желудка и пищевода) [1].
Впервые оперативное вмешательство по поводу деваскуляризации желудка и нижней трети пищевода в сочетании со спленэктомией выполнил С. Henschen в 1938 г. Классической операцией данного типа является операция M. Hassab (1967), которая заключается в обширной деваскуляризации желудка и нижнего отдела пищевода, включая наддиафрагмальные вены, в сочетании со спленэктомией [2]. Y. Ni и соавт. [13] сравнили широко использующуюся методику деваскуляризации пищевода желудка в сочетании со спленэктомией и без таковой. Для исследования были отобраны 55 пациентов с синдромом портальной гипертензии: 27 из них выполнена деваскуляризация желудка и нижней трети пищевода без спленэктомии (группа А) и 28 пациентам выполнялась данная операция в сочетании со спленэктомией (группа В). Таким образом, портальное давление было снижено на 20% в послеоперационном периоде в обеих группах. Частота возникновения тромбоза в портальной вене в группе, А была значительно ниже, чем в группе В (р=0,032). Частота развития рецидивов кровотечения из вен пищевода и желудка в период послеоперационного наблюдения 1 и 3 года в группе, А составляла 0 и 4,5%, в группе В — 0 и 8,7% соответственно (р=0,631). Таким образом, было доказано, что частота осложнений и возникновение тромбоза в воротной вене у пациентов, оперированных без спленэктомии, ниже, чем у пациентов, оперированных в сочетании со спленэктомией. Однако в настоящее время данная операция чаще всего сочетается с эндоскопическим лигированием варикозно-расширенных вен пищевода, а также без спленэктомии [14].
Операцию транссекции пищевода и желудка впервые предложил N. Tanner (1949), который выполнил транссекцию желудка в поперечном направлении, тем самым разъединив систему воротной вены и верхней полой вены с целью ликвидации кровотечения из варикозно-расширенных вен пищевода и желудка у больных с портальной гипертензией. Суть операции заключается в мобилизации нижнего отдела пищевода и кардии желудка, перевязке левой желудочной артерии и вены через торакоабдоминальный доступ в седьмом и восьмом межреберье слева. Желудок пересекают на 5 см ниже кардии и вновь сшивают. Однако анализ отдаленных результатов операции показал ее неэффективность в связи с рецидивами кровотечений вследствие реваскуляризации в зоне транссекции. В научной литературе описаны работы, в которых данная операция выполнялась лапароскопическим доступом [15, 16]. В 1973 г. М. Sugiura и S. Futagawa разработали комбинированную операцию азигопортального разобщения, которая представляла собой трансторакальную транссекцию пищевода, спленэктомию, деваскуляризацию абдоминального отдела пищевода и верхнего отдела желудка, селективную проксимальную ваготомию и пилоропластику. Спленэктомию, пилоропластику, деваскуляризацию желудка, селективную проксимальную ваготомию выполняют из абдоминального доступа, обширную параэзофагеальную деваскуляризацию до уровня нижних легочных вен и транссекцию пищевода до уровня пищеводного отверстия диафрагмы — из торакального доступа. Данная операция в последнее время претерпела различные модификации (А.А. Шалимов, В.И. Оноприев, О.С. Васнев), в том числе с использованием лапароскопической техники, и аппаратной транссекции пищевода с помощью EEA-stapler, и получила широкое распространение в мире.
Методику прошивания варикозно-расширенных вен пищевода впервые предложил Берем в 1949 г. в случаях экстренного оперативного вмешательства при кровотечениях из вен пищевода. Он прошивал расширенные вены пищевода отдельными узловыми швами и вводил в просвет вен между наложенными лигатурами раствор глюкозы с целью тромбообразования в них. Крайль в 1950 г. прошивал варикозно-расширенные вены пищевода непрерывным кетгутовым швом. Позднее эта операция получила название «операция Берема—Крайля», при этом какие-либо вмешательства на варикозно-расширенных венах желудка не производились. Результаты данной операции показали, что кровотечения могут повторяться как в ближайшем, так и в отдаленном послеоперационном периоде, причем чаще всего (в 40—70% случаев) источником кровотечения являлся разрыв варикозных узлов кардиального отдела желудка. Кроме того, основной причиной смерти при операции Берема—Крайля были несостоятельность швов пищевода с последующим развитием медиастинита и эмпиемы плевры, а также декомпенсация функции печени, приводившие к летальному исходу в 30—70% случаев [1]. В 1967 г. М.Д. Пациора предложила прошивать варикозные узлы желудка и нижней трети пищевода через трансабдоминальную гастротомию в проксимальном отделе желудка в косопоперечном направлении [4, 17]. Суть данной операции заключается в прошивании всех варикозных узлов в кардиальном отделе желудка, а затем прошивании варикозных узлов нижней трети пищевода, в результате чего значительно снижается приток крови к венам пищевода. Данная операция менее травматична, чем операция Берема—Крайля, с низкой частотой летальности, рецидивов кровотечения и осложнений (7,6—15,4%). Однако с развитием малоинвазивных оперативных вмешательств (эндоскопическое лигирование) значимость выполнения полостной операции на варикозно-расширенных венах пищевода снизилась [18—20].
Говоря о пищеводно-желудочных резекциях, следует отметить, что эти операции являются операциями резерва для тех больных, кто ранее многократно был оперирован по поводу рецидива кровотечений из вен пищевода и желудка. Одна из таких операций — частичная эзофагогастрэктомия с инвагинацией пищеводно-желудочного анастомоза по способу К.Н. Цацаниди. Также применяются различные модификации данной операции с интерпозицией сегмента толстой или тонкой кишки. Однако данная операция применяется лишь в исключительных случаях ввиду большого количества осложнений (30—40%), таких как агастральная астения тяжелой формы и рецидивы кровотечения из эрозий культи желудка в послеоперационном периоде [18, 21].
На сегодняшний день малоинвазивные вмешательства — более перспективные методы остановки и профилактики кровотечений из варикозно-расширенных венах пищевода и желудка. Эндоскопическое склерозирование вен пищевода впервые выполнили С. Crafoord и Р. Frenckner в 1939 г. При этой методике интравазально либо паравазально с помощью иглы, проведенной через инструментальный канал эндоскопа, вводят склерозанты (производные жирных кислот — натрия морруат, синтетические вещества — этоксисклерол, тромбовар, а также этиловый спирт, фенол, гистоакрил) в целях образования рубцовой ткани и тромбоза сосудов данной области. Эффективность методики составляет 70—90% [19, 22, 23]. Однако данная операция характеризуется большим количеством осложнений, таких как изъязвления слизистой оболочки пищевода (14%), стриктуры пищевода, плевральные осложнения (9%), субфебрильная температура (6,4%), некроз слизистой пищевода и его перфорация (6,25%), перикардиты (0,4%) [2]. Наиболее частое (65%) и серьезное осложнение — стойкая дисфагия пищевода на фоне выраженных рубцовых стриктур, возникновение которых зависит от количества инъекций и введенного склерозанта [24]. В связи с этим многие клиницисты в последнее время отдают предпочтение эндоскопическому лигированию варикозно-расширенных вен пищевода. Впервые эндоскопическое лигирование варикозно-расширенных вен пищевода выполнил G. Stiegmann в 1986 г., применив латексные кольца. Данную операцию выполняют с помощью многозарядного лигатора фирмы «Wilson-Cook» при лигировании вен пищевода или нейлоновой петли фирмы «Olympus» — при необходимости лигирования вен желудка. Эндоскоп с фиксированным на конце колпачком проводится к выбранному варикозному узлу. Лигирование начинают с кардиоэзофагеального перехода чуть выше зубчатой линии в шахматном порядке по спирали. После аспирации варикозного узла в цилиндр более чем на половину его высоты сбрасывают лигирующее кольцо. Через 6—7 сут начинается отторжение некротизированных узлов, на месте которых образуются поверхностные язвы. Язвы заживают в течение 3 нед, на их месте образуются рубцы без стенозирования просвета пищевода. Наиболее частыми осложнениями данной операции являются аллергическая реакция на латекс, боли при глотании в первые дни, кровотечения из поверхностных язв на фоне отторжения некротизированных узлов. Эта методика позволяет остановить продолжающееся кровотечение в 78—95% случаев, однако рецидив кровотечения отмечается у 28—35% пациентов [25]. Методика эндоскопического лигирования варикозно-расширенных вен пищевода и желудка оказалась более эффективной операцией при кровотечениях из вен пищевода, а также как способ профилактики, чем эндоскопическое склерозирование варикозных вен, так как при лигировании вен отмечалось снижение количества рецидивов кровотечения на 20% и снижение летальности на 15% [26—28].
Осложнения после обширных хирургических вмешательств предписывают отказаться от формирования прямых портокавальных анастомозов в пользу эндоваскулярных методов лечения. Одной из первых эндоваскулярных операций стала чрескожная чреспеченочная эмболизация кардиальных вен желудка, впервые разработанная А. Lunderquist в 1974 г. Данная операция заключается в эмболизации левой желудочной вены и коротких вен желудка посредством металлических спиралей «Гиантурко» и других эмболизирующих средств [29]. В 1986 г. В.А. Черкасов рекомендовал выполнять одномоментно эмболизацию селезеночной артерии и кардиальных вен желудка (левая желудочная вена, короткие вены желудка) [30]. Данная манипуляция эффективна при кровотечениях из варикозно-расширенных вен желудка, а недостаток заключается в быстрой реканализации тромбированных коллатералей, в результате чего возможны рецидивы кровотечения.
Эндоваскулярная эмболизация селезеночной артерии впервые успешно выполнена F. Madson в 1973 г., однако анализ данной методики выявил большое количество осложнений, таких как абсцесс селезенки, бактериальный перитонит, тромбоз воротной вены [31]. В связи с этим Spigos и соавт. в 1979 г. предложили частичную эмболизацию селезеночной артерии, которая применяется по сей день [32]. Одним из основных показаний к данной операции является панцитопения, вызванная тем, что после эмболизации ветвей селезеночной артерии возникают участки инфарктов и некрозов, которые уменьшают депонирование лейкоцитов и тромбоцитов в селезенке, что соответственно приводит к их увеличению в периферической крови.
Операцию BRTO (Balloon-occluded Retrograde Transvenous Obliteration, баллон-ассистированная ретроградная трансвенозная окклюзия) впервые выполнили H. Kanagawa и F. Chikamori независимо друг от друга в 1996 г. [33, 34]. Суть операции заключается в эндоваскулярном перекрытии из антеградного трансфеморального доступа просвета спленоренального шунта окклюзионным баллон-катетером и введении жидкого склерозанта в варикозные узлы желудка [2]. В последние годы выработаны модификации данной операции: катетеризация через бедренную, левую почечную вены и естественный гастроренальный анастомоз — эмболизация варикозных вен желудка [35, 36]; катетеризация через притоки левого брахиоцефального венозного ствола или непарной вены левой перикардио-диафрагмальной вены [36]. Положительные результаты данной операции отмечены в 84—100% случаев. Осложнения встречаются в 5% случаев, среди них — тромбоз воротной вены, легочная эмболия и почечная недостаточность; рецидив кровотечения регистрируется с частотой до 9%; средний уровень выживаемости составляет 90, 75, 68 и 55% через 1, 2, 3 года и 7 лет соответственно [35, 36].
С учетом вышесказанного проблема портальной гипертензии и ее осложнений остается одной из самых сложных областей абдоминальной патологии, несмотря на большое количество существующих видов оперативных вмешательств. Однако все эти операции не радикальны. Все открытые хирургические оперативные вмешательства (деваскуляризирующие операции и операции с формированием портокавальных анастомозов) слишком травматичны, не всегда переносятся больными и не решают проблемы высокого портального давления радикально, в связи с чем остается высоким риск рецидива кровотечения. Эндоваскулярные методы лечения (в частности, операции TIPS, BRTO), а также эндоскопические малоинвазивные вмешательства высокоэффективны, поскольку результаты именно этих операций в последние годы дают надежную гарантию профилактики кровотечения из варикозно-расширенных вен пищевода и желудка.
Сплено-ренальный анастомоз
Термин «спленоренальный шунт» обозначает анастомоз (соединение двух полых органов) между селезеночной и почечной венами, применяемый в основном для лечения портальной гипертензии.
Пока ещё мало используются возможности селезеночной артерии как источника артериального кровоснабжения других внутрибрюшных внутренних органов. Эта большая артерия продемонстрировала адекватную замену для печеночной, верхней брыжеечной или левой почечных артерий.
Сплено-ренальный аностомоз (спленоренальное шунтирование) — сосудистая реконструктивная операция. Показания к ней ограничены. Обычно в качестве «донора» для кровоснабжения почки через почечную артерию используют аорту. Однако в некоторых случаях сделать это не возможно. И тогда применяется сплено-ренальный анстомоз.
Данная процедура выполняется только с левой почечной артерией. В качестве доступа используется лапаротомия или левостроннюю торакофренолюмботомию (разновидность хирургического доступа).
Показания и противопоказания к методу лечения
Потенциальные показания к сплено-ренальному артериальному анастомозу:
1) портальная гипертензия;
2) тромбоз аорты;
3) обструкция почечной артерии;
4) повреждение почек;
5) аневризма почечной артерии;
6) аномальная почечная артерия.
Противопоказанием к процедуре является патология в системе чревного ствола, асцит и тромбоз селезеночной вены.
Подготовка к лечению
Перед проведением процедуры проводиться лечение для нормализации функционального состояния печени.
Как проходит метод лечения
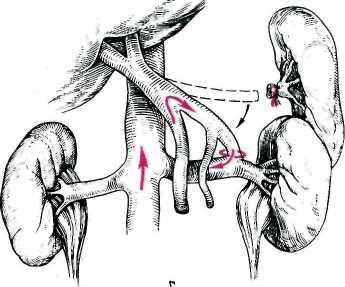
Пациент лежит на правом боку.
Операция проходит в несколько этапов:
1/ Создается доступ к селезенке и левой почке, это достигается с помощью специальных (торакоабдоминального или абдоминодиафрагмального) разрезов.
2/ Мобилизация селезенки (селезенка отделяется от желудка и ободочной кишки). Это нужно для того, чтобы обнажить её сосудистую ножку.
3/ Удаление селезенки.
4/ Выделение селезеночной вены и перевязывание её притоков. Процедура требует осторожности, чтобы не травмировать стенку сосуда. Для сплено-ренального аностомоза необходимо выделить не менее 5 сантиметров вены.
5/ Выделение почечной вены.
6/ Наложение аностомоза. Конец селезеночной вены сшивают с почечной.
Операция длится около 3-х часов.
Возможные осложнения при лечении
Наиболее опасным осложнением анастомоза является тромбоз портальной системы. Очень редко развивается энцефалопатия и послеоперационный панкреатит.
Прогноз после метода лечения
Несомненным плюсом операции является то, что не требуется выделение аорты и использование пластического материала.
После операции снижается риск кровотечения и асцита. Это наиболее эффективный метод лечения варикоза вен пищевода.
Трансъюгулярное внутрипеченочное портосистемное шунтирование (TIPS)
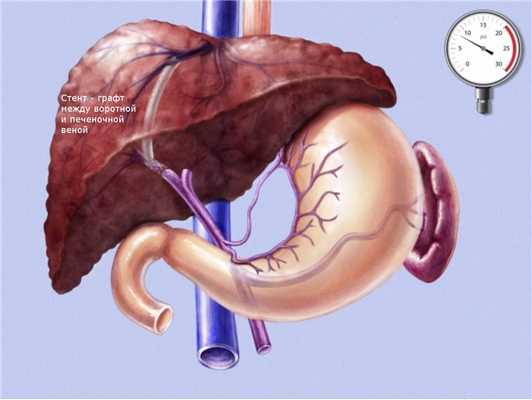
Трансюгулярное внутрипеченочное портосистемное стентирование (TIPS) представляет собой эндоваскулярную операцию по созданию искусственного канала в печени, который обеспечивает отток крови из воротной вены в нижнюю полую вену, минуя пораженную печеночную ткань.
Операция эффективно останавливает кровотечения из варикозных вен пищевода и уменьшает асцит, за счет снижения давления в воротной вене, которое всегда повышено при циррозе печени.
Операция проводится в рентгеноперационной под контролем ангиографии. Во время вмшетельства используются контрастные вещества и ультразвуковое сканирование печени. Средняя продолжительность вмешательства около 2 часов.
Подготовка и обследование для TIPS
Для определения вида портальной гипертензии необходимо выполнить визуализацию структуры печени, проходимость вен воротной системы и определить степень портальной гипертензии и ее риски.
Необходимые методы диагностики:
- УЗИ внутренних органов живота (печени, селезенки, поджелудочной железы) - дают возможность оценить степень поражения печени, выявить опухоли печени и поджелудочной железы, увеличение селезенки.
- УЗИ воротной вены позволяет получить общую информацию о размере и проходимости воротной вены.
- МРТ внутренних органов и вен брюшной полости - в сосудистом режиме позволяет оценить проходимость воротной вены
- Компьютерная томография с ангиографией аорты и венозной фазы - позволяет получить общую оценку воротной системы и варикозных вен в брюшной полости
- Прямая портография (чрезпеченочное введение катетера и контрастирование воротной системы) - заключительный метод диагностики перед вмешательством.
Анестезиологическая поддержка
- За неделю до операции мы переводим пациентов на диету с ограничением белковых продуктов. Это делается для того, чтобы избежать развития энцефалопатии в раннем послеоперационном периоде.
- Накануне вмешательства даются слабительные препараты и ставится очистительная клизма, дается легкий ужин.
- Операция проводится под местной анестезией мест проколов. Анестезиолог присутствует в операционной, для контроля за жизненно-важными функциями организма.
- Пациенту устанавливается мочевой катетер и монитор для измерения артериального давления и снятия ЭКГ.
Как проходит операция
Трансюгулярное внутрипеченочное портосистемное шунтирование проводится под рентгеноскопическим контролем с использованием ультразвукового сканирования для контроля доступов к сосудам.
Доступ к печеночной вене осуществляется через внутреннюю яремную вену на шее. Для облегчения доступа используется ультразвуковой контроль. После пункции устанавливается проводник и интродьюсер. Проводник с катетером проводятся в нижнюю полую и печеночную вену. После установки катетера в печеночной вене измеряется давление прямым методом, чтобы рассчитать в последующем градиент.
Для поиска ветви воротной вены может использоваться УЗИ навигация, либо проводится пункция печени под УЗИ контролем и проводится контрастное исследование портальной системы с использованием функции roadmap.
После определения целевой воротной вены через катетер в печеночной вене проводится пункция специальной иглой. Проведя последнюю в воротную вену через нее устанавливают проводник и проводят катетер. Проводится контрастирование воротной системы через яремный катетер и замеряется давление в воротной системе.
Через паренхиму печени по проводнику проводится баллон, который затем раздувается создавая канал в печеночной ткани. После извлечения баллона по проводнику проводится специальный стент-графт, представляющий собой трубчатую металлическую сетку покрытую внутри специальным герметичным пластиком.
Таким образом, мы соединяем прямым шунтом воротную и печеночную вену, что способствует снижению давления в воротной системе и предупреждает рецидивы кровотечения.
После измерения давления в воротной системе все инструменты удаляются, а пациент помещается в палату наблюдения.
Возможные осложнения
В руках опытного хирурга частота опасных осложнений составляет менее 1%. Очень редко может развиться внутрибрюшное кровотечение или абсцесс печени.
Чаще встречаются осложнения, связанные с успехом процедуры. Прямой поток крови из кишечника может привести к увеличению поступления в системный кровоток азотистых шлаков и развитие энцефалопатии. Проявления энцефалопатии (тремор, бессоница, спутанность сознания) наблюдаются у 25% прооперированных пациентов, однако у большинства пациентов эти симптомы проходят в течение недели после операции. Для предупреждения энцефалопатии необходимо уменьшить потребление белковой пищи.
Недостаточность кровоснабжения печени - ишемический гепатит является более редким осложнением, так как при портальной гипертензии основное кровообращение печень получает за счет печеночной артерии. Однако в некоторых случаях, создание шунта может вызвать ишемическое повреждение печени с острой печеночной недостаточностью, что может потребовать срочного закрытия шунта.
Редким, но серьезным осложнением является развитие инфекционного процесса в зоне вмешательства, то есть нагноения стент-графта. Для предупреждения подобного осложнения в послеоперационном периоде применяются сильные антибиотики.
Прогноз после TIPS
Важно понимать, что портокавальные анастомозы не лечат цирроз печени, но устраняют опасные для жизни осложнения. Пациенты с функционирующим шунтом имеют меньший риск умереть от желудочно-кишечного кровотечения, однако сохраняется риски связанные с печеночной недостаточности.
В целом TIPS позволяет избежать преждевременного неблагоприятного исхода связанного с кровотечениеми и часто применяется как предварительное вмешательство перед пересадкой печени.
Наблюдение после операции
Контроль за функцией шунта осуществляется как с помощью прямых методов визуализации, так и косвенных.
Из косвенных признаков важным является уменьшение диаметра вен в подслизистом слое перехода из пищевода в желудок. Это позволяет иметь уверенность, что рецидива кровотечения не будет. ЭГДС мы рекомендуем выполнять через неделю и через месяц после вмешательства, а затем раз в 6 месяцев.
При ультразвуковом сканировании отмечается кровоток по шунту и определяется его скорость. Оценивается диаметр воротной вены и размеры селезенки. Так же можно отметить уменьшение асцита. УЗИ рекомендуем выполнять каждые 3 месяца у нашего специалиста.
Через год после вмешательства мы рекомендуем выполнить МСКТ ангиографию брюшной полости с оценкой венозной фазы. При этом хорошо выявляется функционирующий стент.
Метод TIPS в Инновационном сосудистом центре
Сосудистые хирурги Инновационного сосудистого центра с 2004 года занимались проблемой лечения осложнений портальной гипертензии, выполняя открытые портокавальные вмешательства. С 2011 года в нашей клинике появилась возможность выполнять эндоваскулярные операции взамен более опасных открытых вмешательств.
Для операций TIPS мы берем пациентов с печеночной формой портальной гипертензии и осложненной тяжелым варикозным расширением вен пищевода, либо уже после состоявшегося пищеводного кровотечения. После обследования мы принимаем решение о виде оперативного вмешательства.
Портальная гипертензия
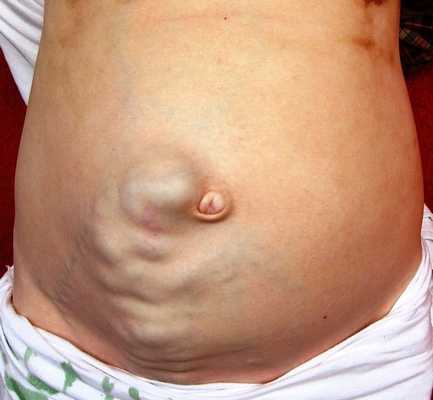
Портальная гипертензия - повышение давления в венах брюшной полости вследствие нарушения венозного оттока через венозную систему печени. Следствием портальной гипертензии является варикозное расширение вен органов брюшной полости с истончением их стенок, что может привести к тяжелым кровотечениям, угрожающим жизни пациента.
Чаще всего портальная гипертензия развивается у больных с циррозом печени и является одним из факторов, приводящим к летальному исходу при данном заболевании. Для портальной гипертензии характерно расширение вен передней брюшной стенки, геморроидальных вен и вен пищевода. Печеночная недостаточность при циррозе печени приводит к недостаточной выработке белков свертывания крови, поэтому у этих пациентов повышенная кровоточивость. Этим обусловлена высокая летальность от кровотечений при портальной гипертензии. Даже при современном состоянии медицины летальность при кровотечении из варикозно расширенных вен составляет более 50%.
Лечение портальной гипертензии в Инновационном сосудистом центре
В Инновационном сосудистом центре для лечения портальной гипертензии применяются как классические операции по созданию сплено-ренальных анастомозов, так и экстренные эндоваскулярные операции трансъягулярного портокавального шунтирования (TIPS).
Эндоваскулярные операции выполняются на ангиографическом комплексе с дополнительным использованием визуализации воротной вены с помощью УЗИ навигации. Такие вмешательства проводятся под местной анестезией с внутривенной седацией.
Операции сплено-ренального анастомоза выполняются у сохранных пациентов, перенесших кровотечение из варикозно-расширенных вен пищевода. Такие вмешательства мы выполняем под наркозом через доступ в левой боковой стенке живота с переходом на грудную клетку. Подобные вмешательства позволяют избежать смертельно-опасных осложнений портальной гипертензии.
![При циррозе печени кровь скапливается в венах желудка, которые расширяются]()
Причины и факторы риска
Портальная гипертензия возникает, когда что-то препятствует кровотоку через печень, повышая давление внутри воротной вены. Эта обструкция (закупорка) может быть внутрипеченочной, подпеченочной (внепеченочной) или надпеченочной.
Внутрипеченочные причины портальной гипертензии
Основной причиной возникновения гипертензии является цирроз (в 70% случаев). Есть много причин возникновения цирроза, наиболее распространенной из них является злоупотребление алкоголем. Цирроз печени может вызвать обширный фиброз (рубцевание). Интенсивное рубцевание препятствует прохождению жидкостей через печень. Фиброз окружает сосуды в печени, что затрудняет кровообращение.
В качестве причины портальной гипертензии выступает большое количество болезней:
- Вирусный гепатит,
- Аутоиммунный гепатит,
- Фиброз печени,
- Опухолевый процесс в печени,
- Болезнь Вильсона, врожденное нарушение метаболизма меди,
- Гемохроматоз, избыточное накопление железа,
- Муковисцидоз, системное наследственное заболевание,
- Холангит, воспаление желчных протоков, связанное с инфекцией,
- Атрезия желчных путей, слабо образованные желчные протоки,
- Инфекции,
- Некоторые метаболические заболевания.
Подпеченочные причины портальной гипертензии
- Тромбоз воротной и селезёночной вены,
- Врожденные аномалии воротной вены, в частности атрезия,
- Сдавление воротной вены опухолью,
- Гематологические заболевания.
Надпеченочные причины портальной гипертензии
Эти причины вызваны обструкцией кровотока из печени в сердце и могут включать:
- Тромбоз печеночной вены, синдром Бадда-Киари,
- Травматический тромбоз нижней полой вены,
- Слипчивый перикардит, воспаление околосердечной сумки, характеризующееся увеличением проницаемости и расширением кровеносных сосудов.
Международные данные по распространенности портальной гипертензии неизвестны, хотя известно что 80% пациентов страдают от портальной гипертензии из-за внутрипеченочных причин, то есть цирроза печени.
Течение заболевания
Течение заболевания можно разбить на 4 стадии:
I стадия — начальная
Заболевание уже появилось, но ещё не может диагностироваться. Протекает бессимптомно, либо пациенты ощущают тяжесть в правом подреберье и легкое недомогание.
II стадия — умеренная
Появляются выраженные клинические симптомы заболевания. Боли в верхней половине живота, метеоризм, расстройства пищеварения (отрыжка, изжога, тяжесть в животе и т.д.), спленомегалия и гепатомегалия (увеличение печени).
III стадия — выраженная
Присутствуют все признаки и симптомы портальной гипертензии в резко выраженной форме.
IV стадия — стадия осложнений
Развивается напряженный асцит, плохо поддающийся терапии, повторяющиеся кровотечения, а также возможные осложнения.
Осложнения
Основные осложнения: желудочно-кишечные кровотечения, асцит и печеночная энцефалопатия (печеночная недостаточность, комплекс психических, нервных и мышечных нарушений).
Спленомегалия часто вызывает анемию, низкие показатели лейкоцитов и низкие показатели тромбоцитов.
Общими осложнениями, связанными с портальной гипертензией, являются аспирационная пневмония, сепсис, почечная недостаточность, кардиомиопатия, аритмии и гипотония.
Портальная гипертензия является опасным заболеванием, поскольку может вызвать кровотечение. Во многих случаях эпизоды кровотечения считаются неотложными медицинскими ситуациями, потому что смертность от варикозных кровотечений составляет около 50%. Варикоз пищевода очень распространен у людей с прогрессирующим циррозом, и считается, что у каждого из трех человек с варикозом развивается кровотечение.
Прогноз
Портальная гипертензия является осложнением основного заболевания печени. Это заболевание часто можно контролировать, а выживаемость зависит от сохранения функций печени. Чем хуже печень выполняет свои функции, тем хуже прогноз.
Более высокие показатели смертности и заболеваемости у пациентов с тяжелым и стойким желудочно-кишечным кровотечением. Смертность пациентов с диагнозом варикозного расширения вен пищевода составляет 30%.
Пациенты, которые имели хотя бы один эпизод кровотечения из-за варикоза пищевода, имеют 80% шансов повторного кровотечения в течение 1 года. У пациентов с варикозом пищевода осложнения иммунных, сердечно-сосудистых и легочных систем способствуют примерно 20-45% смертей.
Преимущества лечения в клинике
Диагностика
Когда кровь не может легко протекать через печень, она пытается обойти портальную систему, используя венозную систему, чтобы вернуться к сердцу. Возникают осложнения, связанные со снижением кровотока через печень и повышенным давлением внутри вен, что приводит к расширению вен. Варикоз может возникать в пищеводе, желудке и прямой кишке.
Когда кровь пытается найти другой путь к сердцу, открываются новые кровеносные сосуды. Среди них те, которые проходят вдоль стенки верхней части желудка и нижнего конца пищевода. Эти вены могут кровоточить. Кровотечение может быть мягким, в этом случае анемия является наиболее распространенным симптомом; либо серьезным, сопровождающееся кровавой рвотой или меленой (черным, смолистым стулом, который появляется из-за кровотечения из верхних отделов желудочно-кишечного тракта). Варикоз пищевода и желудка может привести к кровотечениям, угрожающим жизни.
Брюшная водянка — избыточное скопление жидкости внутри брюшины, обусловленное сочетанием факторов, включая повышенное давление в портальной системе, застой крови и уменьшение уровня белка в крови. Асцит может достигать огромных размеров, сдавливая диафрагму и мешая нормальному дыханию.
Обратимое расстройство нервной и психической деятельности при заболеваниях печени. Проявляется спутанностью сознания, раздражительностью и сонливостью из-за накопления токсических веществ из-за неспособность печени адекватно фильтровать их.
Увеличение селезенки основной симптом при внепеченочной гипертензии, часто сопровождается анемией и тромбоцитопенией (низким уровнем тромбоцитов в кровотоке).
Снижение количества лейкоцитов в крови увеличивает риск инфицирования. Спонтанный бактериальный перитонит наиболее частое инфекционное заболевание, сопровождающее цирроз и печеночную гипертензию. Сопровождается ознобом, лихорадкой и болью в животе.
Портальная гипертензия является опасным осложнением многих заболеваний печени и несет значительные риски для жизни. Диагностика данного заболевания основана на клинических данных, результатах ультразвуковых и эндоскопических исследований желудка.
Лабораторные исследования позволяют оценить функцию печени и почек, что влияет на прогноз заболевания. С целью подготовки к возможному вмешательству при портальной гипертензии используются методы визуализации сосудов воротной системы. Нами используются методы компьютерной томографии и магнито-резонансной диагностики вен брюшной полости.
В клинике применяются следующие диагностические методы:
Лечение
Лечение портальной гипертензии представляет собой сложную задачу. Сложность связана с тем, что развивающаяся печеночная недостаточность обуславливает плохую переносимость тяжелых сосудистых вмешательств. Однако в нашей клинике отработали технологии лечения портальной гипертензии с низким риском для жизни пациента.
Операции по поводу кровотечений из вен портальной системы
При кровотечениях из варикозно-расширенных вен пищевода нередко применяются методы прямого хирургического гемостаза - прошивание кровоточащих вен после рассечения желудка. Такие операции, выполняемые на фоне кровотечения, часто заканчиваются неблагоприятно для пациента. Летальность после таких операций составляет не менее 40%. Иногда общие хирурги дополняют эту операцию спленэктомией, исходя из соображений уменьшения притока крови из-за перевязки селезеночной артерии.
Специальный двухкомпонентный зонд позволяет плотно сжать верхний отдел желудка и нижний отдел пищевода, придавив расширенные вены. Наряду с другими мероприятиями (переливанием плазмы, крови и гемостатических препаратов) позволяет остановить тяжелое желудочно-кишечное кровотечение. Остановка кровотечения не устраняет его причины, поэтому неизбежен рецидив. Но использование этого зонда позволяет отложить вмешательство на портальной системе на более спокойный период и провести его в плановом порядке. Держать зонд в раздутом состоянии рекомендуется не более 6 часов, после чего распускать его на час. Общая продолжительность использования не должна превышать более 2 суток.
- Эмболизация вен пищевода и селезеночной артерии
Эндоваскулярная технология остановки кровотечения из варикозно-расширенных вен пищевода. Редко выполняется как самостоятельное вмешательство, так как требует чреспеченочного доступа, однако применяется совместно с созданием транспеченочного портокавального анастомоза (TIPS). В просвет варикозно-расширенных вен вводятся спирали и микроэмболы, которые блокируют кровоток в кровоточащих сосудах и способствуют остановке кровотечения.
Современный высокотехнологичный метод лечения портальной гипертензии, применяемый в экстренном порядке или как подготовка к пересадке печени. Смысл вмешательства заключается в создании искусственного соустья между ветвями воротной вены в толще печени и печеночной веной из системы нижней полой. В результате улучшается отток из воротной системы и снижается давления в варикозно-расширенных венах пищевода. Кровотечение быстро останавливается.
Трансъюгулярное внутрипечёночное портосистемное шунтирование (ТИПС)
Операция ТИПС - малотравматичный способ снижения портальной гипертензии путём чрезкожной имплантации металлического стента, соединяющего просвет воротной и печёночной вен. Благодаря этой операции, у больных останавливается кровотечение из варикозных вен пищевода и уменьшает асцит. Выполняется под местной анестезией без общего наркоза. Среднее время операции - 1 час.
Содержание статьи:
Допустимые показания к операции ТИПС
Показания и противопоказания к операции ТИПС были сформулированы несколькими группами экспертов, включая Американскую ассоциацию по изучению заболеваний печени (AASLD)
- острое кровотечение из варикозных вен пищевода (желудка), не купируемое комплексом медикаментозных и эндоскопических мероприятий;
- профилактика повторного кровотечения из варикозных вен пищевода после эндоскопического лигирования;
- асцит, рефрактерный к диуретической терапии;
- рефрактерный печёночный гидроторакс;
- кровотечение из варикозных вен тонкой или толстой кишки;
- профилактика повторного кровотечения из вен желудка или эктопических вен (включая толстокишечной и аноректальной зон);
- сидром Budd-Chiari;
- профилактика повторного кровотечения при портальной гастропатии при неудаче лечения бета-блокаторами.
Абсолютные противопоказания к операции ТИПС
- тяжёлая печёночно-клеточная недостаточность (Child-Pugh класс С ≥ 12 баллов);
- изолированный варикоз вен желудка с окклюзией селезёночной вены;
- множественный поликистоз правой доли печени;
- тяжёлая правожелудочковая недостаточность;
- тяжёлая лёгочная гипертензия (≥ 45 мм рт. ст.);
- не разрешаемая желтуха;
- кома;
- нестабильная гемодинамика, наличие более 20 баллов по шкале APACHE II, особенно для пациентов с циррозом печени класса С;
- неконтролируемая системная инфекция или сепсис;
- креатинин сыворотки ≥ 180 ммоль/л (при проведении ТИПС по поводу асцита, резистентного к диуретической терапии).
Как подготовиться к операции ТИПС?
Перед операцией необходимо сдать следующие анализы и результаты исследований:
- УЗИ внутренних органов живота
- УЗИ воротной вены
- МРТ внутренних органов и вен брюшной полости
- Компьютерная томография с ангиографией аорты и венозной фазы
- Прямая портография
Перед операцией внутривенно назначаются антибиотики, предпочтительно из третьей генерации цефалоспоринов.
В отдельных случаях переливается кровь до достижения эритроцитов не менее 20 000/см MHO не должно превышать 2,0.
За неделю до операции пациент должен соблюдать диету - ограничить потребление белковых продуктов. Алкоголь категорически противопоказан. Накануне операции чистится организм - пациенту даются слабительные препараты, ставится клизма.
Как проходит операция ТИПС?
Техника операции ТИПС подразумевает выполнение ряда методологических приёмов.
Пациента привозят в операционную и делают местную анестезию. У больного с выраженным асцитом предварительно выполняется лапароцентез для нормальной позиции печени в брюшной полости.
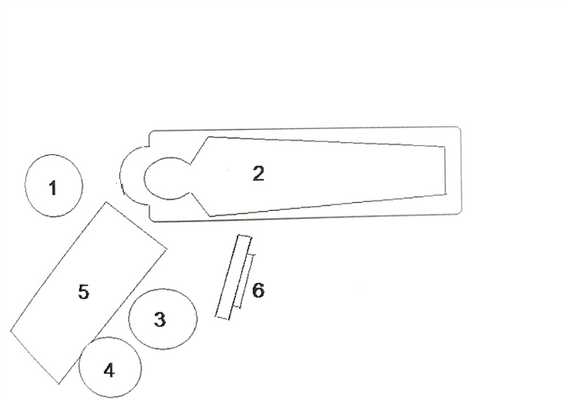
Схема расположения медицинского персонала при проведении операции ТИПС / Рисунок В. Н. Шиповского
1 - оператор;
2 - пациент;
3 - ассистент;
4 - операционная сестра;
5 - операционный столик;
6 - экран монитора.
Затем под контролем «рентгена» (флюороскопии) выполняется безболезненный прокол тонкой иглой на шее (пункция ярёмной вены) и установка специальной полимерной трубочки (интродьюсера). Измеряется давление прямым методом, чтобы рассчитать в последующем градиент.
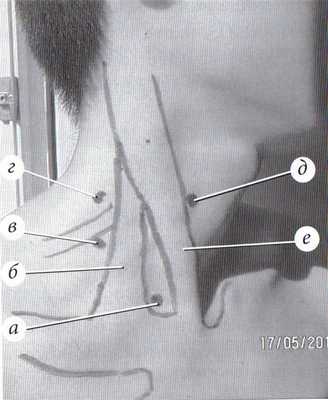
Доступы для пункции внутренней ярёмной вены
а - надключичный;
б - r. lateralis m. sterno-cleido-mastoideus;
в - центральный;
г - задний;
д - передний;
е - r. medialis m. sterno-cleido-mastoideus
Операция проводится без традиционного разреза на коже, а путем катетеризации вены на шее. Для облегчения поиска вены, используется ультразвуковой аппарат.
Как любое хирургическое вмешательство операция ТИПС может сопровождаться осложнениями самого различного характера. Однако сразу следует отметить, что порядок этих осложнений намного меньше, чем при традиционных открытых полостных порто-кавальных операциях. Самое частое возможное осложнение после операции ТИПС- тромбоз (закрытие его просвета сгустком крови) установленного в печени стента. Частота тромбоза стента колеблется от 5% до 30% в зависимости от модели металлического стента. Реже всего происходит закрытие т.н. стент-графтов (стентов с полимерной оболочкой). В случае тромбоза выполняется операция по восстановлению просвета стента опять без разреза через прокол на шеи. Ещё одно осложнение - усиление печёночной энцефалопатии (сонливость, тремор рук, бессонница, слабость, расстройства памяти и проч.), которая в настоящее время успешно лечится в том числе и современными медикаментозными средствами.
Прогноз после операции ТИПС
Во-первых, основные показания к операции ТИПС (кровотечения из вен пищевода или желудка, асцит) являются жизненно необходимыми и выполняются для сохранения жизни пациентов. Во-вторых, до недавнего времени операция ТИПС считалась «мостиком» к трансплантации печени. Однако с использованием современного поколения металлических стентов, устанавливаемых в печени, выявилось, что результаты операции ТИПС имеют хороший результат в долгосрочном периоде (10-15 лет) и поэтому могут считаться самостоятельным методом лечения. Не повторяются кровотечения из вен пищевода и желудка, исчезает жидкость из брюшной полости, накапливается вес пациента, улучшается общее самочувствие. Конечно цирроз печени остаётся, операция не может влиять на него. И это требует особой диеты, продолжения его медикаментозного лечения и специального наблюдения.
Читайте также: