Формирование потенциала действия и потоки ионов
Добавил пользователь Дмитрий К. Обновлено: 22.01.2026
Мембрана всех живых клеток поляризована. Внутренняя сторона мембраны несет отрицательный заряд по сравнению с межклеточным пространством (рис. 1). Величина заряда, который несет мембрана называется мембранным потенциалом (МП). В невозбудимых тканях МП низкий, и составляет около -40 мВ. В возбудимых тканях он высокий, около -60 - -100 мВ и называется потенциалом покоя (ПП).
Потенциал покоя, как и любой мембранный потенциал формируется за счет избирательной проницаемости клеточной мембраны. Как известно, плазмолемма состоит из липидного бислоя, через который движение заряженных молекул затруднено. Белки, встроенные в мембрану, могут избирательно изменять проницаемость мембраны для различных ионов, в зависимости от приходящих стимулов. При этом, для формирования потенциала покоя ведущую роль играют ионы калия, кроме них важны ионы натрия и хлора.
Рис. 1. Концентрации и распределение ионов с внутренней и внешней стороны мембраны.
Большинство ионов распределяются неравномерно с внутренней и внешней стороны клетки (рис. 1). Внутри клетки концентрация ионов калия выше, а натрия и хлора - ниже, чем снаружи. В состоянии покоя мембрана проницаема для ионов калия и практически непроницаема для ионов натрия и хлора. Несмотря на то, что калий может свободно выходить из клетки, его концентрации остаются неизменными благодаря отрицательному заряду на внутренней стороне мембраны. Таким образом, на калий действуют две силы, находящиеся в равновесии: осмотические (градиент концентрации К + ) и электрические (заряд мембраны), благодаря чему число входящих в клетку ионов калия равно выходящим. Движение калия осуществляется через калиевые каналы утечки, открытые в состоянии покоя. Величину заряда мембраны, при которой ионы калия находятся в равновесии можно вычислить по уравнению Нернста:
где Ек — равновесный потенциал для К + ; R — газовая постоянная; Т — абсолютная температура; F — число Фарадея; n — валентность К + (+1), [К + н] — [К + вн] — наружная и внутренняя концентрации К + .
Если подставить в уравнение значения из таблицы на рис. 43, то мы получим величину равновесного потенциала, равную примерно -95 мВ. Это значение вписывается в диапазон мембранного потенциала возбудимых клеток. Отличия ПП разных клеток (даже возбудимых) могут возникать по трем причинам:
- отличия внутриклеточной и внеклеточной концентраций ионов калия в разных тканях (в таблице приведены данные по среднестатистическому нейрону);
- натрий-калиевая АТФаза может вносить свой вклад в значение заряда, так как она выводит из клетки 3 Na + в обмен на 2 К + ;
- несмотря на минимальную проницаемость мембраны для натрия и хлора, эти ионы все-таки могут попадать в клетки, хоть и от 10 до 100 раз хуже, по сравнению с калием.
Чтобы учесть проникновение других ионов в клетку существует уравнение Нернста-Гольдмана:
, где Еm — мембранный потенциал; R — газовая постоянная; Т — абсолютная температура; F — число Фарадея; РK , PNa и РCl — константы проницаемости мембраны для К + Na + и Сl, соответственно; [К + н], [K + вн], [Na + н], [Na + вн], [Сl — н] и [Сl — вн ]- концентрации K + , Na + и Сl снаружи (н) и внутри (вн) клетки.
Такое уравнение позволяет установить более точную величину ПП. Обычно, мембрана оказывается на несколько мВ менее поляризована, по сравнению с равновесным потенциалом для К + .
Потенциал действия (ПД) может возникать в возбудимых клетках. Если на нерв или мышцу нанести раздражение выше порога возбуждения, то ПП нерва или мышцы быстро уменьшится и на короткий промежуток времени (миллисекунда) произойдет кратковременная перезарядка мембраны: ее внутренняя сторона станет заряженной положительно относительно наружной, после чего восстановится ПП. Это кратковременное изменение ПП, происходящее при возбуждении клетки называется потенциалом действия.
Возникновение ПД возможно благодаря тому, что в отличие от ионов калия, ионы натрия далеки от равновесия. Если подставить в уравнение Нернста натрий вместо калия, то мы получим равновесный потенциал, равный примерно +60 мВ. Во время ПД, происходит кратковременное увеличение проницаемости для Na + . При этом, натрий начнет проникать в клетку под действием двух сил: по градиенту концентрации и по заряду мембраны, стремясь подстроить заряд мембраны под свой равновесный потенциал. Движение натрия осуществляется по потенциал-зависимым натриевым каналам, которые открываются в ответ на смещение мембранного потенциала, после чего сами инактивируются.
Рис. 2. Потенциал действия нервного волокна (А) и изменение проводимости мембраны для ионов натрия и калия (Б).
На записи ПД выглядит как кратковременный пик (рис. 44), имеющий несколько фаз.
- Деполяризация (фаза нарастания) (рис. 44) - увеличение проницаемости для натрия из-за открытия натриевых каналов. Натрий стремится к своему равновесному потенциалу, но не достигает его, так как канал успевает инактивироваться.
- Реполяризация - возвращение заряда к величине потенциала покоя. Помимо калиевых каналов утечки здесь подключаются потенциал-зависимые калиевые каналы (активируются от деполяризации). В это время калий выходит из клетки, возвращаясь к своему равновесному потенциалу.
- Гиперполяризация (не всегда) - возникает в случаях, если равновесный потенциал по калию превышает по модулю ПП. Возвращение к ПП происходит после возвращения к равновесному потенциалу по К + .
Во время ПД происходит изменение полярности заряда мембраны. Фаза ПД, при которой заряд мембраны положителен, называется овершутом (рис. 2).
Благодаря Н-воротам инактивация канала происходит раньше, чем потенциал на мембране достигнет равновесной величины по натрию. После прекращения поступления натрия в клетку, происходит реполяризация за счет выходящих из клетки ионов калия. При этом к каналам утечки в этом случае подключаются еще и потениал-активируемые калиевые каналы. Во время реполяризации, в быстром натриевом канале быстро закрываются М-ворота. Н-ворота открываются гораздо медленнее и остаются закрытыми еще некоторое время после возвращения заряда к потенциалу покоя. Этот период принято называть периодом рефрактерности.
Рис. 3. Работа потенциал-управляемого натриевого канала.
Концентрации ионов внутри клетки восстанавливает натрий-калиевая АТФаза, которая с затратой энергии в виде АТФ откачивает из клетки 3 иона натрия и закачивает 2 иона калия.
По немиелинизированному волокну или по мембране мышцы потенциал действия распространяется непрерывно. Возникший потенциал действия за счет электрического поля способен деполяризовать мембрану соседнего участка до порогового значения, в результате чего на соседнем участке возникает деполяризация. Главную роль в возникновении потенциала на новом участке мембраны предыдущий участок. При этом на каждом участки сразу после ПД наступает период рефрактерности, за счет которое ПД распространяется однонаправленно. При прочих равных условиях распространение потенциала действия по немиелинизированному аксону происходит тем быстрее, чем больше диаметр волокна. У млекопитающих скорость составляет 1-4 м/с. Поскольку у беспозвоночных животных отсутствует миелин, в гигантских аксонах кальмара скорость ПД может достигать 100 м/c.
По миелинизированному волокну потенциал действия распространяется скачкообразно (сальтаторное проведение). Для миелинизированных волокон характерна концентрация потенциалзависимых ионных каналов только в областях перехватов Ранвье; здесь их плотность в 100 раз больше, чем в мембранах немиелинизированных волокон. В области миелиновых муфт потенциалзависимых каналов почти нет. Потенциал действия, возникший в одном перехвате Ранвье, за счет электрического поля деполяризует мембрану соседних перехватов до порогового значения, что приводит к возникновению в них новых потенциалов действия, то есть возбуждение переходит скачкообразно, от одного перехвата к другому. В случае повреждения одного перехвата Ранвье потенциал действия возбуждает 2-й, 3-й, 4-й и даже 5-й, поскольку электроизоляция, создаваемая миелиновыми муфтами, уменьшает рассеивание электрического поля. Сальтаторное проведение увеличивает скорость проведения ПД 15-20 раз до 120 м/с.
Работа нейронов
Нервная система состоит из нейронов и глиальных клеток. Однако, главную роль в проведении и передаче нервных импульсов играют нейроны. Они получают информацию от множества клеток по дендритам, анализируют ее и передают или не передают на следующий нейрон.
Передача нервного импульса с одной клетки на другую осуществляется с помощью синапсов. Различают два основных типа синапсов: электрические и химические (рис. 4). Задача любого синапса - передать информацию с пресинаптической мембраны (мембрана аксона) на постсинаптическую (мембрана дендрита, другого аксона, мышцы или другого органа-мишени). Большинство синапсов нервной системы образуется между окончанием аксонов и дендритами, которые в области синапса образуют дендритные шипики.
Преимущество электрического синапса состоит в том, что сигнал с одной клетки на другую переходит без задержки. Кроме того, такие синапсы не утомляются. Для этого пре- и постсинаптические мембраны соединены поперечными мостиками, через которые ионы из одной клетки могут перемещаться в другую. Однако, существенным минусом такой системы является отсутствие однонаправленной передачи ПД. То есть, он может передаваться как с пресинаптической мембраны на постсинаптическую, так и наоборот. Поэтому, такая конструкция встречается достаточно редко и в основном - в нервной системе беспозвоночных.
Рис. 4. Схема строения химического и электрического синапсов.
Химический синапс весьма распространен в природе. О устроен сложнее, так как необходима система преобразования электрического импульса в химический сигнал, затем, вновь в электрический импульс. Все это приводит к возникновению синаптической задержки, которая может составить 0,2-0,4 мс. Кроме того, может произойти истощение запасов химического вещества, что приведет к утомлению синапса. Однако, такой синапс обеспечивает однонаправленность передачи ПД, что является его главным преимуществом.
Рис. 5. Схема работы (а) и электронная микрофотография (б) химического синапса.
В состоянии покоя окончание аксона, или пресинаптическое окончание, содержит мембранные пузырьки (везикулы) с нейромедиатором. Поверхность везикул заряжена отрицательно, чтобы предотвратить связывание с мембраной, и покрыта специальными белками, и принимающими участие в высвобождении везикул. В каждом пузырьке находится одинаковое количество химического вещества, которое называется квантом нейромедиатора. Нейромедиаторы весьма разнообразны по химическому строению, однако, большинство из них производятся прямо в окончании. Поэтому, в нем могут находиться системы, для синтеза химического посредника, а также аппарат Гольджи и митохондрии.
Постсинаптическая мембрана содержит рецепторы к нейромедиатору. Рецепторы могут быть в виде как ионных каналов, открывающихся при контакте со своим лигандом (ионотропные), так и мембранными белками, запускающими внутриклеточный каскад реакций (метаботропные). Один нейромедиатор может иметь несколько как ионотропных, так и метаботропных рецепторов. При этом, часть из них может быть возбуждающими, а часть - тормозными. Таким образом, реакцию клетки на нейромедиатор будет определять тип рецептора на ее мембране, и разные клетки могут совершенно по-разному реагировать на одно и то же химическое вещество.
Между пре- и постсинаптической мембраной располагается синаптическая щель, шириной 10-15 нм.
При приходе ПД на пресинаптическое окончание, на нем открываются потенциал-активируемые кальциевые каналы и ионы кальция входят в клетку. Кальций связывается с белками на поверхности везикул, что приводит к их транспортировке к пресинаптической мембране с последующим слиянием мембран. После такого взаимодействия нейромедиатор оказывается в синаптической щели (рис. 5) и может связаться со своим рецептором.
Ионотропные рецепторы - это лиганд-активируемые ионные каналы. Это значит, что канал открывается только в присутствии определенного химического вещества. Для разных нейромедиаторов это могут быть натриевые, кальциевые или хлорные каналы. Ток натрия и кальция вызывает деполяризацию мембраны, поэтому такие рецепторы называют возбуждающими. Хлорный ток приводит к гиперполяризации, что затрудняет генерацию ПД. Следовательно, такие рецепторы называют тормозными.
Метаботропные рецепторы к нейромедиаторам относят к классу рецепторов, ассоцированных с G-белками (GPCR). Эти белки запускают разнообразные внутриклеточные каскады реакций, приводящих в конечном итоге либо к дальнейшей передачи возбуждения, либо к торможению.
После передачи сигнала необходимо быстро удалить нейромедиатор из синаптической щели. Для этого в щели присутствуют либо ферменты расщепляющие, нейромедиатор, либо на пресинаптическом окончании или соседних глиальных клетках могут располагаться транспортеры, закачивающие медиатор в клетки. В последнем случае он может использоваться повторно.
Каждый нейрон получает импульсы от 100 до 100 000 синапсов. Одиночная деполяризация на одном дендрите не приведет к дальнейшей передаче сигнала. На нейрон могут приходит одновременно множество как возбуждающих, так и тормозных стимулов. Все они суммируются на соме нейрона. Такая суммация называется пространственной. Далее, может возникнуть или не возникнуть (в зависимости от пришедших сигналов) ПД в области аксонного холмика. Аксонный холмик - это область аксона, примыкающая к соме и обладающая минимальным порогом ПД. Далее импульс распространяется по аксону, конец которого может сильно ветвиться и образовывать синапсы со множеством клеток. Помимо пространственной, существует временная суммация. Она происходит в случае, поступления часто повторяющихся импульсов от одного дендрита.
Помимо классических синапсов между аксонами и дендритами или их шипиками, существуют также синапсы, модулирующие передачу в других синапсах (рис. 6). К ним относят аксо-аксональные синапсы. Такие синапсы способны усиливать или тормозить синаптическую передачу. То есть, если на окончание аксона, образующего аксо-шипиковый синапс, пришел ПД, а в это время по аксо-аксональному синапсу на него пришел тормозный сигнал, высвобождения нейромедиатора в аксо-шипиковом синапсе не произойдет. Аксо-дендритные синапсы могут изменять проведение мембраной ПД на пути от шипика к соме клетки. Также существуют аксо-соматические синапсы, которые могут влиять на суммацию сигнала в области сомы нейрона.
Таким образом, существует огромное многообразие различных синапсов, отличающихся по составу нейромедиаторов, рецепторов и их местоположению. Все это обеспечивает разнообразие реакций и пластичность нервной системы.
Формирования потенциал покоя и потенциала действия. Критический уровень деполяризации. Рефрактерный период.
Как же принимает участие мембрана в возникновении биоэлектрических потенциалов, какую роль играют каналы и насосы? В основе всего лежит разность концентраций ионов Na+, K+, Cl-, Ca++ в клетке и окружающей среде
| ИОН | Микромоль на | Литр | |
| Цитоплазма | Кровь | Морская вода | |
| Калий | 360 | 10.0 | 10.0 |
| Натрий | 69 | 425 | 460 |
| Хлор | 157 | 500 | 560 |
| Кальций | 0.4 | 10.0 | 10.0 |
Мембрана в состоянии покоя ПОЛЯРИЗОВАНА. Это значит, что есть разность потенциала между внутренней и наружной поверхностями мембраны. Первая причина поляризации мембраны -это выход КАЛИЯ из клетки в состоянии покоя по концентрационному градиенту: калия в клетке в 10-20 раз больше, чем в окружающей среде. Среда в клетке остается суммарно нейтральной, так как положительный заряд калия компенсируется отрицательными зарядами таких аминокислот, как АСПАРАГИНОВАЯ, ПИРОВИНОГРАДНАЯ, УКСУСНАЯ.
Вторая причина - свободная проницаемость каналов для калия в состоянии покоя.
Для изучения механизмов формирования потенциала покоя и потенциала действия широко использовали крупные нервные клетки ганглиев пиявок, виноградной улитки, гигантские аксоны кальмара. Для выполнения экспериментальной работы необходим микроэлектрод, который вводят в клетку через мембрану. При этом мембрана плотно охватывает кончик микроэлектрода и нет утечки калия из клетки. Необходим также измерительный прибор. Если два электрода прикасаются к поверхностной части мембраны, между ними нет разности потенциалов - на экране прибора регистрируется 0. Как только кончик одного микроэлектрода входит в клетку, касаясь внутренней поверхности мембраны, происходит на экране скачек и регистрируется разность потенциалов - т.е. ПОТЕНЦИАЛ ПОКОЯ. (РИС,) Его величина различна у разных объектов.
| Гигантский аксон кальмара | 50-70 мВ |
| Мышечное волокно сердца лягушки | 61-82 мВ |
| Водоросль нителла | 100-125 мВ |
Исходя из концентрации ионов калия в клетке и окружающей среде по формуле НЕРНСТА можно рассчитать величину потенциала покоя для каждого объекта. НО - мембрана незначительно проницаема в покое и для ионов натрия и хлора. Эти потоки меняют величину мембранного потенциала и он рассчитывается по формуле ГОЛЬДМАНА. Но по концентрационному градиенту калий выходит до момента формирования равновесного потенциала по калию Ек. Происходит уравновешивание двух процессов - выхода калия из клетки под воздействием сил диффузии и электростатической силы, которая возникает в результате скопления на наружной поверхности мембраны ионов калия .Это и есть потенциал покоя.
При раздражении мембраны, резко снижается проницаемость для ионов калия и возрастает для ионов натрия. Если раздражающий стимул достигает порога - (или критического уровня деполяризации) - натрий лавинообразно входит в клетку и происходит перезарядка мембраны - ДЕПОЛЯРИЗАЦИЯ. До критического уровня деполяризации каналы для натрия открываются, но только их малая часть, поэтому ПД не возникает. Если потенциал на мембране достиг критического уровня деполяризации (КУД), возникает ПД и теперь мембрана изнутри заряжена положительно, а снаружи - отрицательно. Таким образом - возникновение деполяризации, т.е. возбуждения или потенциала действия (ПД), определяется потоком ионов натрия внутрь клетки по ионным каналам. На пике ПД натриевые каналы инактивируются, открываются калиевые каналы и наступает реполяризация, т.е. восстановление исходной поляризации мембраны- потенциала покоя. Этот процесс обеспечивается потоком ионов калия внутрь волокна. Таким образом, натриевые каналы могут быть в трех состояниях: закрыты, но их можно открыть раздражением мембраны (электрическим, механическим, температурным):открыты; инактивированы, когда срабатывают инактивационные ворота и каналы невозможно открыть никаким раздражением. В этот момент клетка или волокно находятся в состоянии абсолютной рефрактерности (невозбудимости). Удлинение рефрактерного периода приводит к снижению частоты, которую может воспроизводить данное возбудимое образование. Самый длительный рефрактерный период в волокнах сердечной мышцы, что препятствует возникновению экстрасистолии при появлении патологического очага возбуждения в сердце.
21. Строение и функции ионных каналов. Блокатора ионных каналов. Роль натрий-калиевого насоса клетки в поддержании ПП, Na+K+АТФ-аза.
Но как же тогда происходит движение ионов через мембрану? Эту задачу решают белки, встроенный в мембрану, т.е. в билипидный слой. Белки могут быть частично погружены в билипидный слой с внеклеточной стороны или изнутри клетки. Если белок находится на поверхности мембраны, то на них находятся короткие разветвленные цепочки полисахаридов, образующие ГЛИКОКАЛИКС, с помощью которого клетки опознают друг друга. (РИС.) Некоторые белки насквозь пронизывают мембрану - билипидный слой, они называются ТРАНСМЕМБРАННЫЕ и именно они образуют ИОННЫЕ КАНАЛЫ. Основные ионы, участвующие в генерации электрических сигналов -K+, Na+, Ca++, Cl- - движутся через соответствующие каналы. Для каждого иона есть свой канал и они имеют разное строение. Ионы могут проходить через канал ПАССИВНО по градиенту концентрации (от большей к меньшей) и по ЭЛЕКТРИЧЕСКОМУ ПОТЕНЦИАЛУ НА МЕМБРАНЕ КАНАЛА.
Трансмембранные или интегративные белки асимметрично распределены в бислое и многократно его пересекают. ПО строению - это ЗИГЗАГООБРАЗНЫЕ БЕЛКИ, которые образуют ДОМЕНЫ. Например, в натриевом канале 4 домена (РИС.). Каждый домен имеет 6 трансмембранных участков -S1-S6. Между участками S5-S6 располагается пора для входа натрия. В самом начале канала находится широкое устье, которое сужается до размеров иона селективным фильтром. Далее идет водная пора и система «ворот», которые могут открывать и закрывать канал. Кроме селективного фильтра имеется сенсоры напряжения с определенным зарядом. Следовательно натриевые каналы потенциалзависимые, т.е. вход натрия регулируется зарядом на мембране. Количество каналов на единицу площади мембраны, и изменение состояния мембраны при прекращении работы того или иного канала изучалось с применением различных ядов. Например, если обработать нервное волокно тетраэтиламмонием, перестают работать калиевые каналы, а при действии тетродотоксина ( из рыбы фугу), перестают работать натриевые каналы и можно подсчитать их число на мембране. Еще один тип трансмембранных белков - НАСОСЫ - переносчики веществ через мембрану против концентрационного градиента. Эти белки-насосы необходимы для переноса метаболитов - глюкозы, аминокислот и ионов для поддержания исходной разности их концентраций в клетке и окружающей среде.
Задача мембраны сомы нейрона - формировать возбуждение - ПД, а задача аксона - передача ПД к следующему нейрону или к органу-эффектору. ПД распространяется по мембране немиелинизированного волокна, как огонь по Бикфордову шнуру: участок возбужденный обеспечивает возбуждение соседнего участка мембраны. Происходит постепенное перемещение петли тока, которая возникает между + и - на мембране. Скорость распространения ПД зависит от величины диаметра и физиологического состояния волокна.
Ионные механизмы потенциала действия
За счет чего же возникает потенциал действия, какие механизмы лежат в его основе? Приоритет в ответах на эти вопросы принадлежит двум выдающимся ученым - А. Ходжкину и Э. Хаксли, проводившим исследования в 30-40-х годах прошлого века. Их достижения в детальном объяснении столь сложных биофизических молекулярных процессов трудно переоценить. Все последующие исследования по регистрации одиночных каналов возбудимых тканей лишь дополнили сформированные ими представления о молекулярных механизмах возбуждения .
Рис. 19. Роль ионов натрия и калия в возникновении потенциала действия
Эти ученые работали на гигантском аксоне кальмара, очень удобном объекте, поскольку его диаметр более миллиметра. Крупные размеры позволяли менять внутриклеточный ионный состав аксоплазмы и вводить внутрь аксона один или несколько электродов для отведения потенциала действия и раздражения аксона. Были проведены исследования по влиянию изменений вне- и внутриклеточной концентрации ионов и природных токсинов, блокирующих различные ионные каналы, на форму потенциала действия (рис.19). Оказалось, что при снижении концентрации ионов натрия в окружающей среде потенциал действия уменьшается по амплитуде; следовательно, потенциал действия зависит от концентрации внеклеточного натрия (рис. 19А). При исследовании эффекта тетродотоксина, специфического блокатора натриевых каналов, был получен эффект, аналогичный снижению внеклеточной концентрации ионов натрия - потенциал действия уменьшался, а при высоких концентрациях токсина - не возникал (рис. 19Б). Было сделано заключение, что потенциал действия связан с открытием потенциал- активируемых натриевых каналов и поступлением ионов натрия в цитоплазму.
Далее была проверена роль ионов калия. Для этого использовали тетраэтиламмоний - вещество, специфически блокирующее калиевые каналы. Оказалось, что на амплитуду потенциала действия тетраэтиламмоний влияет слабо, а вот длительность потенциала действия резко увеличивалась (рис. 19В). Был сделан вывод, что ионы калия, выходящие из клетки через потенциал-активируемые калиевые каналы, также имеют значение в формировании потенциала действия, участвуя в фазе реполяризации.
Переворот в анализе ионных токов, участвующих в формировании потенциала действия был произведен при использовании метода фиксации потенциала на мембране, разработанном Коулом, Ходжкиным и Хаксли. Дело в том, что при изучении ионных токов, текущих через мембрану возбудимой клетки, исследователь сталкивается с очень сложной проблемой. Протекание тока через мембрану, за счет перераспределения зарядов приводит к изменению мембранного потенциала, а изменение потенциала сказывается на величине протекающих токов. Поэтому разобраться в этой системе только при регистрации мембранного потенциала очень трудно. Для регистрации токов необходимо фиксировать мембранный потенциал клетки на одном и том же уровне. Принцип метода фиксации потенциала на мембране заключается в следующем (рис. 20А). Мембранный потенциал клетки искусственно смещается до определенного уровня, а специальный усилитель обратной связи не дает мембранному потенциалу изменяться (поддерживает его на заданном
(А) Метод фиксации мембранного потенциала (подробнее в тексте). (Б) Мембранный потенциал быстро смещается с -65 до -9 мВ и поддерживается на этом уровне. При этом регистрируется сначала короткий входящий, а затем длительный выходящий токи. (В) Эффекты тетродотоксина и тетраэтиламмония на ионные токи. Видно, что поздний ток обусловлен выходящим калиевым током, а ранний - входящим натриевым.
уровне) при прохождении ионных токов через мембрану. Ток, поддерживающий мембранный потенциал на постоянном уровне, является отражением ионных токов, протекающих через мембрану.
На рис. 20 Б показан эксперимент, когда мембранный потенциал аксона кальмара искусственно сдвигается на 56 мВ и поддерживается на этом уровне. В этом случае вначале регистрируется входящий ионный ток, который затем сменяется длительным выходящим током. При использовании блокаторовионных каналов оказалось, что быстрый входящий ток блокируется тетродотоксином, а поздний ток исчезает при действии тетраэтиламмония (рис. 20В). На основе этих изящных экспериментов были сделаны следующие выводы: входящий ток переносится ионами натрия, а выходящий - ионами калия; натриевый ток быстро нарастает и быстро заканчивается, а калиевый ток - медленно нарастает и не изменяется в процессе деполяризации. Было предположено, что различная динамика этих токов связана с быстрой инактивацией натриевых каналов и отсутствием инактивации у калиевых каналов.
На основе этих экспериментов Ходжкин и Хаксли создали систему дифференциальных уравнений, которая позволила описать трансмембранные ионные токи и рассчитать их динамику во время потенциала действия. Расчеты по эмпирически полученным формулам, отражающим зависимости натриевой и калиевой проводимостей от потенциала и времени, с удивительной точностью повторили форму реального потенциала действия. На рис. 21 представлена рассчитанная динамика натриевых и калиевых ионных токов, а также мембранного потенциала при развитии потенциала действия. Видно, что фаза деполяризации потенциала действия обусловлена быстрым нарастанием натриевого тока и массивным поступлением положительно зараженных ионов натрия в цитоплазму, что сдвигает мембранный потенциал в направлении потенциала равновесия для натрия (ЕNa). Именно этим объясняется тот факт, что на пике потенциала действия происходит кратковременная смена знака потенциала на внутренней стороне мембраны (овершут). Вспомним, что при открытии потенциал-активируемых натриевых каналов вход натрия обеспечивается движущей силой для натрия (Vm-ЕNa). Однако пик потенциала действия никогда не достигает натриевого равновесного потенциала (около +50 мВ), поскольку быстро наступающая инактивация натриевых каналов прекращает поступление ионов натрия. Наступление фазы реполяризации потенциала действия обусловлена, с одной стороны, прекращением поступления ионов натрия внутрь, а с другой - более медленным нарастанием калиевого тока, выводящего положительно заряженные ионы калия из клетки. Выход калия заканчивается вместе с окончанием потенциала действия.
Рис 21. Кинетика ионных токов при формировании потенциала действия
Реконструкция потенциала действия и кинетики ионных токов, лежащих в его основе, при помощи системы дифференциальных уравнений модели Ходжкина - Хаксли. Видно, что фаза деполяризации потенциала действия формируется за счет быстроразвивающегося натриевого входящего тока, который затем быстро инактивируется. Фаза реполяризации обеспечивается медленно нарастающим калиевым выходящим током.
Мембранный потенциал при этом быстро возвращается к исходному уровню и приближается к калиевому равновесному потенциалу (ЕК). Отсюда сколько положительных зарядов с ионами натрия входит в клетку во время деполяризации, столько положительных зарядов с ионами калия выходит из клетки. Если бы инактивация натриевых каналов была единственным механизмом фазы реполяризации потенциала действия, то возврат мембранного потенциала к уровню потенциала покоя в большинстве клеток происходил бы гораздо медленнее. Следовые потенциалы, наблюдаемые иногда в конце потенциала действия, связаны с небольшими остаточными проводимостями мембраны для натрия и калия. Так, следовая деполяризация обеспечивается входом ионов натрия, а следовая гиперполяризация - выходом калия.
Естественно, вход ионов натрия и выход ионов калия во время потенциала действия приводят к изменению концентраций этих ионов в цитоплазме (концентрация ионов калия уменьшается, а ионов натрия - возрастает). Расчеты показали, что величина этих изменений зависит от размеров клетки и составляет от тысячных до десятых долей процента. В тоже время увеличение внутриклеточной концентрации ионов натрия увеличивает активность натрий-калиевого обменного насоса, так что внутриклеточные концентрации ионов быстро возвращаются к изначальному уровню.
Общая схема процессов, лежащих в основе формирования потенциала действия, представлена на рис. 22. Мы уже говорили, что натриевые и калиевые каналы, участвующие в формировании потенциала действия, являются потенциал-зависимыми, то есть вероятность открытия этих ионных каналов увеличивается с уменьшением мембранного потенциала. Однако влияние деполяризации на натриевую и калиевую проводимость при развитии потенциала действия имеет некоторые особенности. Воздействие деполяризации на натриевую проводимость носит регенеративный характер. Сначала пороговая небольшая деполяризация увеличивает количество открытых натриевых каналов, а затем положительно заряженные ионы натрия, входящие в клетку, производят дальнейшую деполяризацию мембраны, что
Рис. 22. Схема последовательности событий при возникновении потенциала действия
ведет к открытию большего количества каналов и влечет за собой вход еще большего числа ионов натрия, и так далее. Такой самоусиливающийся процесс называется положительной обратной связью (рис. 22). Потенциал-зависимость калиевых каналов, наоборот, характеризуется наличием отрицательной обратной связи. При деполяризации количество открытых калиевых каналов возрастает, и ионы калия выходят из клетки по направлению электрохимического градиента. Однако, выход калия не усиливает деполяризацию, а ведет к реполяризации и уменьшению калиевого тока (рис. 22).
С инактивацией натриевых каналов связана очень важная характеристика возбудимых тканей - рефрактерность (рис. 23). Дело в том, что, закрывшись посредством инактивации, натриевые каналы восстанавливают свою способность активироваться только через некоторое время (миллисекунда и более). Отсюда во время потенциала действия клетка теряет способность возбуждаться, то есть генерировать повторный потенциал действия на любое по силе раздражение. Эта невозбудимость клетки длится в течение всей фазы
Рис. 23. Рефрактерность
Во время потенциала действия происходит изменение возбудимости клетки. Во время фазы деполяризации и части фазы реполяризации потенциала действия возбудимая клетка теряет способность повторно генерировать потенциал действия (абсолютная рефрактерность). Позже возбудимость восстанавливается, но для возникновения повторного потенциала действия необходимо более сильное раздражение (относительная рефрактерность).
деполяризации потенциала действия, части фазы реполяризации и носит название абсолютной рефрактерности. Постепенно натриевые каналы выходят из состояния инактивации, и возбудимость нервной клетки медленно восстанавливается. Но для того, чтобы возбудить клетку в этот период, необходима большая, чем в норме сила раздражения. Этот период времени носит название относительной рефрактерности.
МЕХАНИЗМ ВОЗНИКНОВЕНИЯ МЕМБРАННОГО ПОТЕНЦИАЛА ПОКОЯ
Каждая клетка в состоянии покоя характеризуется наличием трансмембранной разности потенциалов (потенциала покоя). Обычно разность зарядов между внутренней и внешней поверхностями мембран составляет от -80 до -100 мВ и может быть измерена с помощью наружного и внутриклеточного микроэлектродов (рис. 2.10). Разность потенциалов между наружной и внутренней сторонами мембраны клетки в состоянии ее покоя называют мембранным потенциалом (потенциалом покоя).
Создание потенциала покоя обеспечивается двумя основными процессами — неравномерным распределением неорганических ионов между внутри- и внеклеточным пространством и неодинаковой проницаемостью для них клеточной мембраны. Анализ химического состав вне- и внутриклеточной жидкости свидетельствует о крайне неравномерном распределении ионов (табл. 2.1).
В состоянии покоя внутри клетки много анионов органических кислот и ионов К + , концентрация которых в 30 раз больше, чем снаружи; ионов Na + , наоборот, снаружи клетки в 10 раз больше, чем внутри; С1 _ также больше снаружи.
В покое мембрана нервных клеток наиболее проницаема для К + , менее — для СГ и очень мало проницаема для Na + . Проницаемость мембраны нервного волокна для Na + B покое в 100 раз меньше, чем для К + . Для многих анионов органических кислот мембрана в покое совсем непроницаема.
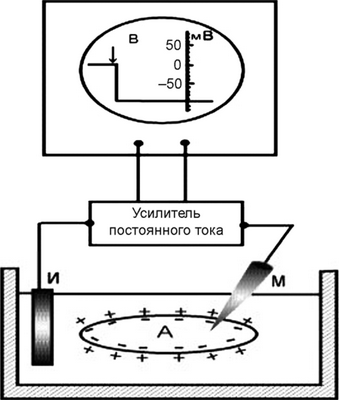
Рис. 2.10. Измерение потенциала покоя мышечного волокна (А) с помощью внутриклеточного микроэлектрода:
М — микроэлектрод; И — индифферентный электрод
Луч на экране осциллографа (В) показывает, что до прокола мембраны микроэлектродом разность потенциалов между М и И была равна нулю. В момент прокола (показан стрелкой) обнаружена разность потенциалов, указывающая, что внутренняя сторона мембраны заряжена отрицательно по отношению к ее наружной поверхности (по Б.И. Ходорову)
Внутри- и внеклеточные концентрации ионов мышечной клетки теплокровного животного, ммоль/л (по Дж. Дудел)
Внутриклеточная концентрация
Внеклеточная концентрация
А" (анионы органических соединений)
В силу градиента концентраций К + выходит на наружную поверхность клетки, вынося свой положительный заряд. Высокомолекулярные анионы не могут следовать за К + из-за непроницаемости для них мембраны. Ион Na + также не может возместить ушедшие ионы калия, ибо проницаемость мембраны для него значительно меньше. СГ по градиенту концентраций может перемещаться только внутрь клетки, увеличивая тем самым отрицательный заряд внутренней поверхности мембраны. Вследствие такого перемещения ионов возникает поляризация мембраны, когда наружная ее поверхность заряжается положительно, а внутренняя — отрицательно.
Электрическое поле, которое создается на мембране, активно вмешивается в распределение ионов между внутренним и наружным содержимым клетки. По мере возрастания положительного заряда на наружной поверхности клетки иону К + как положительно заряженному становится все труднее перемещаться изнутри наружу. Он движется как бы в гору. Чем больше величина положительного заряда на наружной поверхности, тем меньшее количество ионов К + может выходить на поверхность клетки. При определенной величине потенциала на мембране количество ионов К + , пересекающих мембрану в том и другом направлении, оказывается равным, т.е. концентрационный градиент калия уравновешивается имеющимся на мембране потенциалом. Потенциал, при котором диффузионный поток ионов становится равным потоку одноименных ионов, идущих в обратном направлении, называют потенциалом равновесия для данного иона. Для ионов К + потенциал равновесия равен —90 мВ. В миелинизированных нервных волокнах величина потенциала равновесия для ионов С1 _ близка к значению мембранного потенциала покоя (—70 мВ). Поэтому, несмотря на то что концентрация ионов СГ снаружи волокна больше, чем внутри его, не отмечается их одностороннего тока в соответствии с градиентом концентраций. В этом случае разность концентраций сбалансирована потенциалом, имеющимся на мембране.
Ион Na + по градиенту концентраций должен был бы входить внутрь клетки (его потенциал равновесия составляет +60 мВ), и наличие отрицательного заряда внутри клетки не должно было бы препятствовать этому потоку. В этом случае входящий Na + нейтрализовал бы отрицательные заряды внутри клетки. Однако этого в действительности не происходит, так как мембрана в покое малопроницаема для Na + .
Важнейшим механизмом, поддерживающим низкую внутриклеточную концентрацию ионов Na + и высокую концентрацию ионов К + , является натрий-калиевый насос (активный транспорт). Известно, что в клеточной мембране имеется система переносчиков, каждый из которых связывается с тремя находящимися внутри клетки ионами Na + и выводит их наружу. С наружной стороны переносчик связывается с двумя находящимися вне клетки ионами К + , которые переносятся в цитоплазму. Энергообеспечение работы систем переносчиков обеспечивается АТФ. Функционирование насоса по такой системе приводит к следующим результатам:
- • поддерживается высокая концентрация ионов К + внутри клетки, что обеспечивает постоянство величины потенциала покоя. Вследствие того что за один цикл обмена ионов из клетки выводится на один положительный ион больше, чем вводится, активный транспорт играет роль в создании потенциала покоя. В этом случае говорят об электрогенном насосе, поскольку он сам создает небольшой, но постоянный ток положительных зарядов из клетки, а потому вносит прямой вклад в формирование отрицательного потенциала внутри нее. Однако величина вклада электрогенного насоса в общее значение потенциала покоя обычно невелика и составляет несколько милливольт;
- • поддерживается низкая концентрация ионов Na + внутри клетки, что, с одной стороны, обеспечивает работу механизма генерации потенциала действия, с другой — обеспечивает сохранение нормальных осмолярности и объема клетки;
- • поддерживая стабильный концентрационный градиент Na + , на- трий-калиевый насос способствует сопряженному К + , № + -транс- порту аминокислот и сахаров через клеточную мембрану.
Таким образом, возникновение трансмембранной разности потенциалов (потенциала покоя) обусловлено высокой проводимостью клеточной мембраны в состоянии покоя для ионов К + , СГ, ионной асимметрией концентраций ионов К + и ионов СГ, работой систем активного транспорта (Na + /K. + —АТФаза), которые создают и поддерживают ионную асимметрию.
МЕХАНИЗМ ВОЗНИКНОВЕНИЯ ПОТЕНЦИАЛА ДЕЙСТВИЯ
Потенциалом действия называют быстрое изменение мембранного потенциала, возникающее при возбуждении нервных, мышечных и некоторых железистых клеток. В основе его возникновения лежат изменения ионной проницаемости мембраны. В развитии потенциала действия выделяют четыре последовательных периода: 1) локальный ответ; 2) деполяризация; 3) реполяризация и 4) следовые потенциалы (рис. 2.11).
Локальный ответ представляет собой активную местную деполяризацию, возникающую вследствие увеличения натриевой проницаемости клеточной мембраны. Уменьшение мембранного потенциала называется деполяризацией. Однако при подпороговом стимуле начальное повышение натриевой проницаемости недостаточно велико, чтобы вызвать быструю деполяризацию мембраны. Локальный ответ возникает не только при подпороговом, но и при надпороговом раз-
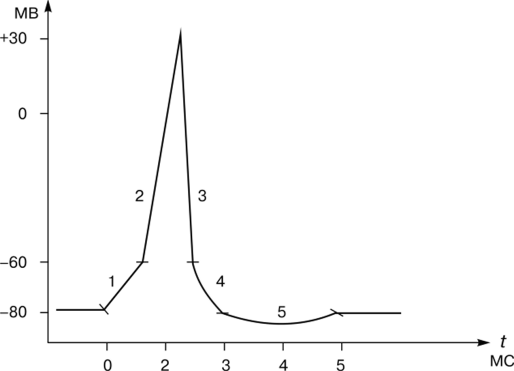
Рис. 2.11. Потенциал действия:
1 — локальный ответ; 2 — фаза деполяризации; 3 — фаза реполяризации; 4 — отрицательный следовой потенциал; 5 — положительный (гиперполяризационный) следовой потенциал
дражении и является составным компонентом потенциала действия. Таким образом, локальный ответ является первоначальной и универсальной формой реагирования ткани на различные по силе раздражения. Биологический смысл локального ответа состоит в том, что если раздражитель по силе мал, то ткань реагирует на него с минимальной тратой энергии, не включая механизмы специфической деятельности. В том же случае, когда раздражение надпороговое, локальный ответ переходит в потенциал действия. Период от начала раздражения до начала фазы деполяризации, когда локальный ответ, нарастая, снижает мембранный потенциал до критического уровня (КУД), называется латентным или скрытым периодом, продолжительность которого зависит от силы раздражения (рис. 2.12).
Фаза деполяризации характеризуется быстрым уменьшением мембранного потенциала и даже перезарядкой мембраны: внутренняя ее часть на некоторое время становится заряженной положительно, а внешняя — отрицательно. Изменение знака заряда на мембране называют извращением — реверсией потенциала. В отличие от локального ответа скорость и величина деполяризации не зависят от силы раздражителя. Продолжительность фазы деполяризации в нервном волокне лягушки составляет около 0,2—0,5 мс.
Продолжительность фазы реполяризации составляет 0,5—0,8 мс. Восстановление исходной величины поляризации мембраны называют реполяризацией. В течение этого времени мембранный потен-
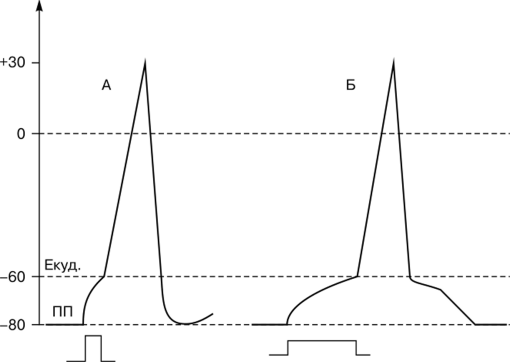
Рис. 2.12. Потенциалы действия, возникающие в ответ на пороговое раздражение коротким (А) и длительным (Б) стимулами Раздражающие стимулы, при воздействии которых получены ответы А и Б: ПП — потенциал покоя; Екуд. — критический уровень деполяризации мембраны (по А.Л. Каталымову)
циал постепенно восстанавливается и достигает 75—85% потенциала покоя. В литературе второй и третий периоды часто называют пиком потенциала действия.
Колебания мембранного потенциала, следующие за пиком потенциала действия, называют следовыми потенциалами. Различают два вида следовых потенциалов — следовую деполяризацию и следовую гиперполяризацию, которые соответствуют четвертой и пятой фазам потенциала действия. Следовая деполяризация (отрицательный следовой потенциал) является продолжением фазы реполяризации и характеризуется более медленным (по сравнению с фазой реполяризации) восстановлением потенциала покоя. Следовая деполяризация переходит в следовую гиперполяризацию (положительный следовой потенциал), представляющую собой временное увеличение мембранного потенциала выше исходного уровня. Увеличение мембранного потенциала называется гиперполяризацией. В миелинизирован- ных нервных волокнах следовые потенциалы имеют более сложный характер: следовая деполяризация может переходить в следовую гиперполяризацию, затем иногда возникает новая деполяризация, лишь после этого происходит полное восстановление потенциала покоя.
Ионный механизм возникновения потенциала действия. Основу потенциала действия составляют последовательно развивающиеся во времени изменения ионной проницаемости клеточной мембраны.
При действии на клетку раздражителя проницаемость мембраны для ионов Na + резко повышается за счет активации (открывания) натриевых каналов.
При этом ионы Na + по концентрационному градиенту интенсивно перемещаются из вне во внутриклеточное пространство. Вхождению ионов Na + в клетку способствует и электростатическое взаимодействие. В итоге проницаемость мембраны для Na + становится в 20 раз больше проницаемости для ионов К + .
Сначала деполяризация идет сравнительно медленно. Когда мембранный потенциал уменьшается на 10—40 мВ, скорость деполяризации резко увеличивается и кривая потенциала действия круто поднимается верх. Уровень мембранного потенциала, при котором резко увеличивается скорость деполяризации мембраны, благодаря тому что поток ионов Na + внутрь клетки оказывается большим, чем поток ионов К + наружу, называют критическим уровнем деполяризации.
Поскольку поток Na + в клетку начинает превышать калиевый ток из клетки, происходит постепенное снижение потенциала покоя, приводящее к реверсии — изменению знака мембранного потенциала. При этом внутренняя поверхность мембраны становится электроположительной по отношению к ее внешней электроотрицательной поверхности. Указанные изменения мембранного потенциала соответствуют восходящей фазе потенциала действия (фазе деполяризации).
Мембрана характеризуется повышенной проницаемостью для ионов Na + лишь очень короткое время (0,2—0,5 мс). После этого проницаемость мембраны для ионов Na + вновь понижается, а для К + — возрастает. В результате поток Na + внутрь клетки резко ослабляется, а ток К + из клетки усиливается.
В течение потенциала действия в клетку поступает значительное количество Na + , а ионы К + покидают клетку. Восстановление клеточного ионного баланса осуществляется благодаря работе натрий- калиевого насоса, активность которого возрастает при повышении внутренней концентрации ионов Na + и увеличении внешней концентрации ионов К + . Благодаря работе ионного насоса и изменению проницаемости мембраны для Na + и К + их концентрация во внутри- и внеклеточном пространстве постепенно восстанавливается.
Итогом этих процессов и является реполяризация мембраны: внутреннее содержимое клетки вновь приобретает отрицательный заряд по отношению к внешней поверхности мембраны.
Следовой отрицательный потенциал регистрируется в период, когда № + -каналы инактивированы и реполяризация, связанная с выходом ионов К + из клетки, происходит медленнее, чем во время нисходящей части пика потенциала действия. Это длительное сохранение отрицательности наружной поверхности возбужденного участка по отношению к невозбужденному называют следовой деполяризацией. Следовая деполяризация означает, что в этот период наружная поверхность возбудимого образования имеет меньший положительный заряд, чем в состоянии покоя.
Следовой положительный потенциал соответствует периоду увеличения мембранного потенциала покоя, т.е. гиперполяризации мембраны. Во время следового положительного потенциала наружная поверхность клетки более положительно заряжена, чем в состоянии покоя. Следовой положительный потенциал часто называют следовой гиперполяризацией. Она объясняется длительным сохранением повышенной проницаемости для ионов К + . Вследствие этого на мембране устанавливается потенциал, равный потенциалу равновесия (для К + — 90 мВ).
Изменения возбудимости в процессе развития возбуждения. Воздействуя раздражителями разной силы в различные фазы потенциала действия, можно проследить, как изменяется возбудимость в ходе возбуждения. На рис. 2.13' видно, что период локального ответа характеризуется повышенной возбудимостью (мембранный потенциал приближается к критическому уровню деполяризации); во время фазы деполяризации мембрана утрачивает возбудимость (клетка становится рефрактерной), которая постепенно восстанавливается в ходе реполяризации.
Выделяют период абсолютной рефрактерности, который в нервных клетках продолжается около 1 мс и характеризуется их полной невоз- будимостью. Период абсолютной рефрактерности возникает в результате практически полной инактивации (непроницаемости) натриевых каналов и повышения калиевой проводимости мембраны. Даже в состоянии покоя активированы не все каналы мембраны, 40% из них находятся в состоянии инактивации. При деполяризации количество инактивированных каналов увеличивается и вершина пика потенциала действия соответствует инактивации всех натриевых каналов.
По мере реполяризации мембраны происходит реактивация натриевых каналов. Это период относительной рефрактерности: потенциал действия может возникнуть только при действии более сильных (надпороговых) раздражителей.
В период отрицательного следового потенциала фаза относительной рефрактерности сменяется фазой повышенной (супернормальной) возбудимости. В этот период порог раздражения снижен по сравнению с исходным значением, поскольку мембранный потенциал ближе к критической величине, чем в состоянии покоя (рис. 2.14) [1] [2] .
Фаза следовой гиперполяризации, обусловленная остаточным выходом калия из клетки, напротив, характеризуется снижением
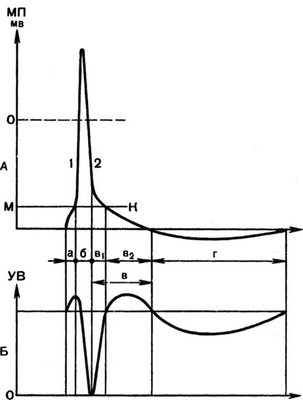
Рис. 2.13. Изменение возбудимости в процессе потенциала действия:
А — компоненты волны возбуждения: 1 —деполяризация; 2 — реполяризация; МП — мембранный потенциал; мВ — микровольт; МК — критический уровень деполяризации: а — длительность порогового потенциала; б — длительность потенциала действия; в — следовая отрицательность; г — следовая положительность; Б — изменения возбудимости в разные фазы волны возбуждения; УВ — уровень возбудимости в покое: а — повышение возбудимости в период порогового потенциала; б — падение возбудимости до нуля во время протекания потенциала действия (абсолютная рефрактерность); в, — возвращение возбудимости к исходному уровню во время следовой отрицательности (относительная рефрактерность); в2 — повышение возбудимости в период конца следовой отрицательности (экзальтация'или супернормальность); в — весь период следовой отрицательности; г — падение возбудимости в период гиперполяризации (субнормальность)
возбудимости. Поскольку мембранный потенциал больше, чем в состоянии покоя, требуется более сильный раздражитель для его «смещения» до уровня критической деполяризации.
Таким образом, в динамике возбудительного процесса изменяется способность клетки реагировать на раздражители, т.е. возбудимость.
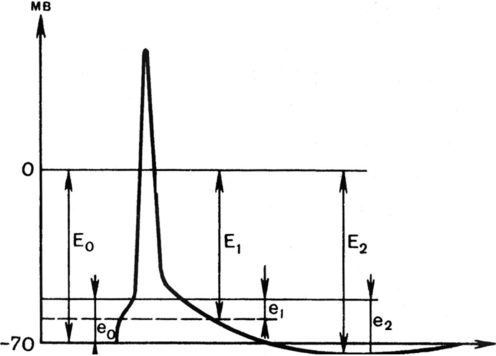
Рис. 2.14. Величина мембранного и порогового потенциалов в разные фазы развития возбуждения
Величина мембранного потенциала: Е0 — в покое; — в фазе экзальтации; Е2 — в фазе гиперполяризации. Величина порогового потенциала: е0 — в покое; е, — в фазе экзальтации; е2 — в фазе гиперполяризации
Это имеет большое значение, поскольку в момент наибольшего возбуждения (пика потенциала действия) клетка становится абсолютно невозбудимой, что защищает ее от гибели и повреждений.
Читайте также:
- Физиологические изменения молочной железы в норме
- Агаммаглобулинемия, сцепленная с Х-хромосомой
- Влияние гипофиза на жировой обмен. Атеросклероз при нарушениях углеводного обмена
- Пример гипотиреоза при пороке сердца. Синдром Шершевского-Тернера при пороке сердца
- Схема лечения паралича Белла (идиопатического паралича лицевого нерва)
