Гемодинамические параметры. Влияние тонуса сосудов на сердечный выброс
Добавил пользователь Владимир З. Обновлено: 21.01.2026
крови из аретрий повышение АД; или- понижение тонуса артериол увеличение оттока крови из артерий понижение АД. Благодарѐ влиѐния на величину оттока крови из артерий, артериолы играят роль «кранов» и обуславливаят
регулѐция местного кровотока.
Венулы имеят меньшее сопротивление по сравнения с артериолами, около 4 % от общего сопротивлениѐ сосудов (артериолы - 50%)
Сосудодвиг нервы. Гладкие мышцы сосудов имеят базальный тонус - то есть способны поддерживатьминимальнуя сократимость без нервных и гуморальных влиѐний, а также находѐтсѐ под влиѐнием постоѐнной тонической
импульсации от симпатических нервов.
Симпатические нервы обуславливаят вазоконстрикция, парасимпатические - вазодилѐтация. Плеганглионарные волокна обоих отделов ВНС вырабатываят ацетилхолин, который взаимодействует с Н-холинорецепторами.
Постганглионарное волокно симпатического отдела ВНС вырабатывает норадреналин, который взаимодействует с бета- адренорецепторами (при этом вызывает вазодилѐтация) и с альфа-адренорецепторами (вызывает
вазоконстрикция повыш АД). Постганглионарное волокно парасимпатического отдела ВНС выделѐет ацетилхолин как и преганглионарное, но в этом случае ацетилхолин взаимодействует с М-холинорецепторами. Вазодилѐтациѐ играет огромнуя роль в сосудах скелетных мышц, что предотвращает спазм сосудов.
Понятие о сердечно-сосудистом центре. Прессорный и депрессорный рефлексы (собственные и сопряженные)
Сосудодвигательный центр - обеспечивает определеннуя степень сужениѐ артериального русла. Находитсѐ в
продолговатом мозге (более точно - на дне IV желудочка) и находитсѐ в состоѐнии постоѐнной тонической активности. Устранение его влиѐниѐ влечет за собой расширение сосудов и падение АД. Состоит из двух отделов - прессорного (сужение сосудов повышение АД) и депресорного (расширение сосудов пониж АД), находѐщихсѐ в постоѐнных
реципрокных отношениѐх. Влиѐниѐ, идущие от сосудосуживаящего центра, приходѐт к нервным центрам симпат отдела ВНС - боковым рогам грудных сегментов спинного мозга, которые регулируят тонус сосудов отдельных участков тела.
Собственные сосудистые рефлексы - вызываятсѐ сигналами от самих сосудов. Рецепторы сосредоточены в области дуги аорты и месте разветвлениѐ общей сонной артерии - названы сосудистыми рефлексогенными зонами (они ѐвлѐятсѐ
барорецепторами). От рецепторов дуги аорты идут центростремительные волокна нерва-депрессора, которые повышаят тонус ѐдер блуждаящего нерва и тормозѐт тонус сосудосуживаящего центра расширение сосудов и пониж АД, а также замедлѐетсѐ сердечный ритм. От рецепторов каротидного синуса идет нерв Геринга, который понижает тонус сосудосуж
центра и повыш тонус ѐдер блужд нервов расширение сосудов и пониж АД. Это были описаны депрессорные рефлексы.
В тех же областѐх есть и хеморецепторы, повышаящие тонус сосудосуж центра, то есть повышаящие давление - это прессорные рефлексы.
Сопрѐженные сосудистые рефлексы - вызываят приемущественно повышение АД. Их можно вызвать, например, раздражением поверхности тела от ноцирецепторов и терморецепторов (холодовых) повыш АД, оосбенно в бряшной полости или кожных артериол от терморецепторов.
Гемодинамические параметры. Влияние тонуса сосудов на сердечный выброс
Сердце - главный центр кровеносной системы, работающий по типу насоса, благодаря чему в организме движется кровь. В результате физической тренировки размеры и масса сердца увеличиваются в связи с утолщением стенок сердечной мышцы и увеличением его объема, что повышает мощность и работоспособность сердечной мышцы.
При регулярных занятиях физическими упражнениями или спортом: увеличивается количество эритроцитов и количество гемоглобина в них, в результате чего повышается кислородная емкость крови; повышается сопротивляемость организма к простудным и инфекционным заболеваниям, благодаря повышению активности лейкоцитов; ускоряются процессы восстановления после значительной потери крови. У тренированных людей количество эритроцитов (красные кровяные тельца) с 4,5-5 млн. в 1 мм3 крови до 6 млн. Эритроциты - переносчики кислорода, поэтому при увеличении их количества кровь может получить больше кислорода в легких и большее количество его доставить тканям, главным образом мышцам. У тренированных людей увеличивается и количество лимфоцитов - белых кровяных телец. Лимфоциты вырабатывают вещества, которые нейтрализуют различные яды, поступающие в организм или образующиеся в организме. Увеличение количества лимфоцитов - одно из доказательств того, что в результате физических упражнений увеличиваются защитные силы организма, повышается устойчивость организма против инфекции. Люди, систематически занимающиеся физическими упражнениями и спортом, реже болеют, а если заболевают, то в большинстве случаев легче переносят инфекционные болезни [3].
Важным показателем работоспособности сердца является систолический объем крови (СО) - количество крови, выталкиваемое одним желудочком сердца в сосудистое русло при одном сокращении. Показатели систолического объема сердца у тренированного человека гораздо выше и при мышечной работе, и в покое, чем у нетренированных людей.
Другими информативными показателем работоспособности сердца является число сердечных сокращений (ЧСС). В процессе спортивной тренировки ЧСС в покое и во время физической нагрузки со временем становится реже за счет увеличения мощности каждого сердечного сокращения. Объясняется это тем, что сердце нетренированного человека для обеспечения необходимого минутного объема крови (количество крови, выбрасываемое одним желудочком сердца в течение минуты) вынуждено сокращаться с большей частотой, так как у него меньше систолический объем. Сердце тренированного человека более часто пронизано кровеносными сосудами, в таком сердце лучше осуществляется питание мышечной ткани, и работоспособность сердца успевает восстановиться в паузах сердечного цикла. Схематично сердечный цикл можно разделить на 3 фазы: систола предсердий (0,1 с), систола желудочков (0,3 с) и общая пауза (0,4 с). Даже если условно принять, что эти части равны по времени, то пауза отдыха у нетренированного человека при ЧСС 80 уд./мин будет равна 0,25 с, а у тренированного при ЧСС 60 уд./мин пауза отдыха увеличивается до 0,33 с. Значит, сердце тренированного человека в каждом цикле своей работы имеет большее времени для отдыха и восстановления [1].
Кровяное давление - давление крови внутри кровеносных сосудов на их стенки. Измеряют кровяное давление в плечевой артерии, поэтому его называют артериальное давление (АД), которое является весьма информативным показателем состояния сердечно-сосудистой системы и всего организма. Различают максимальное (систолическое) АД, которое создается при систоле (сокращении) левого желудочка сердца, и минимальное (диастолиеское) АД, которое отмечается в момент его диастолы (расслабления). Пульсовое давление (пульсовая амплитуда) разница между максимальным и минимальным АД. Давление измеряется в миллиметрах ртутного столба (мм рт. ст.). В норме для студенческого возраста в покое максимальное АД находится в пределах 100-130; минимальное - 65-85, пульсовое давление - 40-45 мм рт. ст.
Пульсовое давление при физической работе увеличивается, его уменьшение является неблагоприятным показателем (наблюдается у нетренированных людей). Снижение давления может быть следствием ослабления деятельности сердца или чрезмерного сужения периферических кровеносных сосудов.
При интенсивной физической работе у тренированных людей максимальное АД повышается до 200 мм рт. ст. и более, может долго держаться, но во время отдыха после физической работы максимальное и минимальное АД быстро приходит в норму. У нетренированных людей максимальное АД сначала повышается до 200 мм рт. ст., затем снижается в результате утомления сердечной мышцы, а после физической нагрузки максимальное и минимальное АД долго остаются повышенными.
Кровь в организме человека выполняет следующие функции: транспортная, регуляторная, защитная, теплообмен. Полный круговорот крови по сосудистой системе осуществляется за 21-22 секунды, при физической работе - 8 секунд и меньше, что ведет к повышению снабжения тканей тела питательными веществами и кислородом.
Физическая работа способствует общему расширению кровеносных сосудов, нормализации тонуса их мышечных стенок, улучшению питания и повышению обмена веществ в стенках кровеносных сосудов. При работе окружающих сосуды мышц происходит массаж стенок сосудов. Кровеносные сосуды, проходящие через мышцы, массируются за счет гидродинамической волны от учащения пульса и за счет ускоренного тока крови. Все это способствует сохранению эластичности стенок кровеносных сосудов и нормальному функционированию сердечно-сосудистой системы без патологических отклонений.
Напряженная умственная работа, малоподвижный образ жизни, особенно при высоких нервно-эмоциональных напряжениях, вредные привычки вызывают повышение тонуса и ухудшение питания стенок артерий, потерю их эластичности, что может привести к стойкому повышению в них кровяного давления, и, в конечном итоге, к гипертонической болезни. Потеря эластичности кровеносных сосудов, а значит, повышение их хрупкости и сопутствующее этому повышение кровяного давления могут привести к разрыву кровеносных сосудов. Если разрыв происходит в жизненно важных органах, то наступает тяжелое заболевание или скоропостижная смерть.
Таким образом, мы видим, что физическая культура и спорт благоприятно влияют не только на мускулатуру, но и на другие органы, в частности на кровеносную систему, улучшая и совершенствуя их работу. Чтобы быть здоровым, крепким, выносливым и разносторонне развитым человеком, необходимо активизировать кровообращение с помощью физических упражнений. Особенно полезное влияние на кровеносную систему оказывают занятия циклическими видами упражнений: бег, плавание, бег на лыжах, на коньках, езда на велосипеде [2].
Чурсин В.В. Клиническая физиология кровообращения (методические материалы к лекциям и практическим занятиям)
Чурсин В.В. Клиническая физиология кровобращения. Методические материалы к практическим и семинарским занятиям, - 2011. - 44 с.
Содержит информацию о физиологии кровообращения, нарушениях кровообращения и их вариантах. Также представлена информация о методах клинической и инструментальной диагностики нарушений кровообращения.
Данные материалы являются переработанным вариантом предыдущих изданий (1999г., 2003г.), первым автором которых являлся В.Ф.Туркин - доцент кафедры анестезиологии и реаниматологии АГИУВ.
Предназначается для врачей всех специальностей, курсантов ФПК и студентов медвузов.
Введение
Академик В.В.Парин (1965г.) дает такое пояснение: «Клиническая физиология исходит из положения, что в организме при болезни многие возникающие реакции являются приспособительными. Под влиянием чрезвычайных раздражителей приспособительные реакции резко изменяются и, приобретая опасное для организма значение, становятся реакциями патологическими. Переход приспособительных реакций в патологические является узловым звеном в патогенезе заболеваний. А его детальное изучение является одной из главных задач клинической физиологии кровообращения».
Исходя из этого пояснения, можно отметить, что значение клинической физиологии любой системы предполагает:
Более образно это можно представить в следующем виде (рисунок 1).
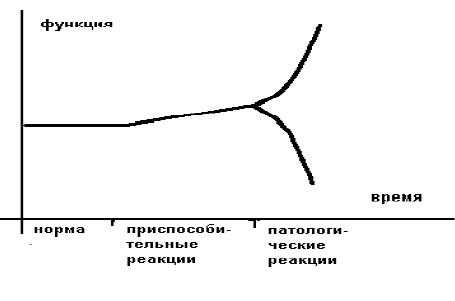
Приспособительные реакции обеспечивают компенсацию, а патологические реакции обуславливают декомпенсацию страдающего органа или страдающей системы. В общем виде отличием (границей) между нормой и приспособлением является изменение свойств приспосабливающего органа или приспосабливающейся системы.
Границей между приспособлением и патологией является резкое изменение ("излом") приспособительной реакции по направлению и величине.
Различают срочные приспособительные реакции и долговременные. Врачам интенсивной терапии чаще приходится иметь дело с острыми расстройствами, поэтому необходимы знания срочных приспособительных реакций и их переход в патологические.
Кровообращение - определение, классификация
Кровообращение - это непрерывное движение (обращение) крови по замкнутой системе, именуемой сердечно-сосудистой.
- 2 - аорта и крупные артерии, имеют много эластических волокон, представляются как буферные сосуды, благодаря им резко пульсирующий кровопоток превращается в более плавный;
- 3 - прекапиллярные сосуды, это мелкие артерии, артериолы, метартериолы, прекапиллярные жомы (сфинктеры), имеют много мышечных волокон, которые могут существенно изменить свой диаметр (просвет), они определяют не только величину сосудистого сопротивления в малом и большом кругах кровообращения (поэтому и называются резистивными сосудами), но и распределение кровопотока;
- 4 - капилляры, это обменные сосуды, при обычном состоянии открыто 20-35% капилляров, они образуют обменную поверхность в 250-350 кв.м., при физической нагрузке максимальное количество открытых капилляров может достигать 50-60%;
- 5 - сосуды - шунты или артериоло-венулярные анастомозы, обеспечивают сброс крови из артериального резервуара в венозный, минуя капилляры, имеют значение в сохранении тепла в организме;
- 7 - вены, крупные вены, они обладают большой растяжимостью и малой эластичностью, в них содержится большая часть крови (поэтому и называются емкостными сосудами), они определяют "венозный возврат" крови к желудочкам сердца, их заполнение и (в определенной мере) ударный объём (УО).
Объем циркулирующей крови (ОЦК)
Вопрос объема имеет важное значение. Прежде всего потому, что определяет наполнение камер сердца и таким образом влияет на величину УО.
По классическому представлению ОЦК составляет у мужчин 77 и у женщин 65 мл/кг массы тела 10%. В среднем берётся 70 мл/кг.
Необходимо чётко представлять, что ОЦК является «жидким слепком сосудистой системы» - сосуды не бывают полупустыми. Ёмкость сосудистой системы может изменяться в достаточно больших пределах, в зависимости от тонуса артериол, количества функционирующих капилляров, степени сдавления вен окружающими тканями («наполненность» интерстиция и тонус мышц) и степенью растянутости свободно расположенных вен брюшной полости и грудной клетки. Разница в ОЦК, определяемая изменением состояния вен, предположительно составляет примерно 500-700 мл у взрослого человека (А.Д.Ташенов, В.В.Чурсин, 2009г.). Мнение, что венозная система может вместить, кроме ОЦК, еще 7-10 литров жидкости, можно считать ошибочным, так как излишняя жидкость достаточно быстро перемещается в интерстиций. Депо ОЦК в организме является интерстициальное пространство, резервная-мобильная емкость которого составляет примерно ещё 1 литр. При патологии интерстиций способен принять около 5-7 литров жидкости без формирования внешне видимых отеков (А.Д.Ташенов, В.В.Чурсин, 2009г.).
Особенностью интерстициальных отеков при некорректной инфузионной терапии является то, что жидкость при быстром поступлении в организм прежде всего уходит в наиболее «мягкие» ткани - мозг, легкие и кишечник.
Последствием этого является наиболее наблюдаемые недостаточности - церебральная, дыхательная и кишечная.
Физиологи на сегодняшний день считают, что практически у среднего человека номинальной величиной ОЦК принимается 5 литров или 5000 см 3 . В ОЦК различают две составных части: объем заполнения (U) и объем растяжения (V) сосудистой системы. U составляет 3300 см., V составляет 1700 см 3 . Последний, объем растяжения имеет непосредственное отношение к давлению крови и скорости объемного потока крови в сосудах.
Избыточная, особенно быстрая, инфузия растворов ведет к увеличению объема, прежде всего в сосудах легких, чем в других органах. При быстрой инфузии, особенно крупномолекулярных растворов (декстраны, ГЭК, СЗП, альбумин) жидкость не успевает переместиться в интерстиций, и при этом жидкость депонируется в первую очередь в легочных венах. Имеются сведения о том, что легочные вены могут дополнительно вместить еще примерно 53% общего легочного объема крови. При дальнейшей избыточной инфузии в действие вступает рефлекс Китаева. При этом рефлексе импульсы с рецепторов перерастянутых легочных вен, возбуждающе действуя на мускулатуру легочных артериол, суживают их, предотвращая таким образом переполнение легочных венозных сосудов.
Из-за спазма легочных артериол при дальнейшей избыточной инфузии наступает объемная перегрузка правых отделов сердца, в первую очередь правого желудочка. При его чрезмерной перегрузке в действие вступает рефлекс Ярошевича. Импульсы с рецепторов легочных артерий, возбуждающе действуя на мускулатуру в устьях полых вен, суживают их, предотвращая таким образом переполнение правых отделов сердца.
Здесь граница, за которой далее приспособление может перейти в патологию. В случае продолжения избыточной инфузии - вследствие избыточного давления в правом предсердии и его перерастяжения возникают следующие условия.
Во-первых ухудшается отток в правое предсердие значительной части крови из коронарных вен. Затруднение оттока по коронарным венам приводит к затруднению притока крови по коронарным артериям и доставки кислорода к миокарду (боль в области сердца).
Во-вторых, может возникнуть рефлекс Бейнбриджа (подробнее - раздел регуляции кровообращения), он вызывает тахикардию, которая всегда увеличивает потребность миокарда в кислороде.
У лиц со скрытой коронарной недостаточностью (что почти никогда не выявляется у больных перед операцией из-за недостаточного обследования) и у лиц с явной ишемической болезнью сердца (ИБС) все это может обусловить возникновение острой коронарной недостаточности вплоть до возникновения острого инфаркта миокарда (ОИМ) с дальнейшим развитием острой сердечной лево-желудочковой недостаточности (ОСЛН).
Если компенсаторные возможности коронарного кровообращения не скомпрометированы и не реализуется рефлекс Бейнбриджа, то дальнейшая объемная перегрузка приводит к растяжению полых вен. При этом с рецепторов, расположенных в устьях полых вен, импульсация поступает к центрам осморегуляции в гипоталамусе (супраоптическое ядро). Уменьшается секреция вазопрессина, приводящая к полиурии (выделению мочи более 2000 мл/сут), что отмечается утром дежурным врачом (и, как правило, безотчётливо) - больной спасает себя. Хорошо, если у больного регуляция водного баланса не нарушена и почки функционируют, в противном случае больной будет «утоплен» с благими намерениями.
Не затрагивая вопросов о «хроническом» уменьшении ОЦК, когда это обусловлено хроническим уменьшением потребления жидкости, коснемся вопроса уменьшения ОЦК, обусловленного именно острой кровопотерей, с чем чаще всего имеют дело врачи анестезиологи-реаниматологи.
По современным представлениям отмечаются следующие приспособительные изменения функции сердечно-сосудистой системы.
Когда ОЦК снижается на 10-20%, то такая кровопотеря представляется компенсируемой. При этом первой приспособительной реакцией является уменьшение емкости венозных сосудов за счёт сдавления их окружающими тканями. Вены из округлых становятся сплющенными или почти полностью спадаются, и таким образом емкость сосудов приспосабливается к изменившемуся объему циркулирующей крови. Венозный приток крови к сердцу и его УО поддерживаются на прежнем уровне. Компенсаторную реакцию организма можно сравнить с ситуацией, когда содержимое неполной 3-х литровой банки переливают в 2-х литровую и она оказывается полной.
Компенсаторным механизмом является и перемещение жидкости из интерстиция за счёт уменьшения венозного давления и увеличения скорости кровотока (укорочения времени изгнания даже без развития тахикардии) - жидкость как бы засасывается из интерстиция. Этот компенсаторный механизм можно наблюдать у доноров при донации, когда экстракция 500 мл крови не приводит к каким-либо изменениям кровообращения.
С уменьшением ОЦК до 25-30% (а это уже потеря растягивающей части ОЦК - V) кровопотеря представляется не компенсируемой за счёт критического уменьшения ёмкости венозной системы. Начинает уменьшаться венозный приток к сердцу и страдает УО. При этом развивается приспособительная (компенсаторная) тахикардия. Благодаря ей поддерживается достаточный уровень сердечного выброса (СВ за минуту = МСВ) за счёт уменьшенного УО и более частых сердечных сокращений. Одновременно с тахикардией развивается сужение периферических артериальных сосудов - централизация кровообращения. При этом ёмкость сосудистой системы значительно уменьшается, подстраиваясь под уменьшенный ОЦК. При сниженном УО и суженных периферических артериальных сосудах поддерживается достаточный уровень среднего артериального давления (АДср) в сосудах, направляющих кровь к жизненно важным органам (мозг, сердце и лёгкие). Именно от величины АДср зависит степень перфузии того или иного органа. Таким образом, развивается приспособительная централизация кровообращения за счет уменьшения кровоснабжения периферических тканей (кожа, скелетные мышцы и т.д.). Эти ткани могут переживать ишемию (I фазу нарушения микроциркуляции) и кислородную недостаточность в течение более продолжительного времени.
Эта реакция аналогична процессу воспаления, при котором организм, образуя грануляционный вал и отторгая омертвевшее, жертвует частью во имя сохранения целого.
Когда ОЦК снижается более чем на 30-40% и восполнение кровопотери задерживается, то такая кровопотеря переходит в разряд некомпенсированной и может стать необратимой. При этом несмотря на тахикардию, СВ уменьшается и снижается АДср. Из-за недостаточного транспорта кислорода в организме усиливается метаболический ацидоз. Недоокисленные продукты метаболизма парализуют прекапиллярные сфинктеры, но периферический кровоток не восстанавливается из-за сохраняющегося спазма посткапиллярных сфинктеров.
Развивается II фаза нарушений микроциркуляции - застойной гипоксии. При этом за счёт ацидоза повышается проницаемость капилляров - плазматическая жидкость уходит в интерстиций, а форменные элементы начинают сладжироваться, образуя микротромбы - развивается ДВС-синдром. К моменту, когда на фоне нарастающего ацидоза парализуются и посткапиллярные сфинктеры (III фаза нарушений микроциркуляции) капиллярное русло уже необратимо блокировано микротромбами.
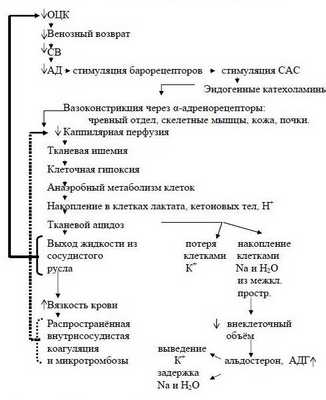
Наступает несостоятельность тканевой перфузии. Во всех случаях затянувшегося синдрома малого СВ присоединяется преренальная анурия. Всё это клиническая форма шока с классической триадой: синдром сниженного СВ, метаболический ацидоз, преренальная анурия. При этом во многих органах, как отмечает профессор Г.А.Рябов, "наступают необратимые изменения и даже последующее восполнение кровопотери и восстановление ОЦК не всегда предотвращает смертельный исход из-за осложнений, связанных с необратимыми изменениями в некоторых органах" - развивается полиорганная недостаточность (ПОН) или мультиорганная дисфункция (МОД).
Последовательность в нарушениях гомеостаза при кровопотере схематически представлена на рисунке 2 (Р.Н.Лебедева и сотр., 1979 г.).
Таким образом, при абсолютном снижении ОЦК практически любого происхождения границей перехода приспособления в декомпенсацию является увеличение частоты сердечных сокращений (ЧСС) с одновременным снижением СВ и АДср.
Данное положение не применимо к случаям, когда имеется относительное уменьшение ОЦК за счет патологической вазодилятации.
Следует учитывать и то, что очень часто острая кровопотеря сопровождается болью и это вносит разлад в последовательность компенсаторных механизмов - раньше чем нужно и в большем количестве выбрасываются эндогенные катехоламины. Централизация развивается быстрее и времени на спасение больного остается меньше.
Гемодинамика обеспечивается регулярной систолической функцией сердца, определение состоятельности которой, в первую очередь, возможно при ультразвуковом исследовании (эхокардиографии). Весьма точную оценку систолической функции левого желудочка (ЛЖ) можно провести биплановым методом дисков (метод Симпсона) в 4-камерной и 2-камерной позициях [1, 2].
Кроме того, при допплеровской эхокардиографии возможно определение скоростных характеристик кровотока в выносящем тракте ЛЖ с расчетом интеграла линейной скорости кровотока (VTI, сумма всех значений линейной скорости в момент изгнания крови в аорту) [2].
В последние годы доступен эхокардиографический метод оценки локальной и глобальной функции ЛЖ путем определения подвижных точек (speckle tracking). Данный метод представляет собой оценку степени утолщения каждого сегмента миокарда в систолу (деформация миокарда ЛЖ). Как правило, указывается положительное значение показателя глобальной деформации миокарда, т.е. его модуль. В норме модуль глобальной деформации миокарда (Global Longitudinal strain — GLS) более 19. Значение GLS 15,9—19 рассматривается как умеренное снижение, а GLS ниже 15,9 — признак выраженной систолической дисфункции ЛЖ. При определении систолической функции ЛЖ с помощью метода speckle tracking отмечалось меньше ошибок по сравнению со стандартными методами расчета фракции выброса [1—6].
К другим методам оценки систолической функции ЛЖ можно отнести рентгенконтрастную вентрикулографию, позитронно-эмиссионную томографию, мультиспиральную компьютерную томографию, магнито-резонансную томографию (МРТ). Все эти методы имеют высокую точность в определении фракции выброса ЛЖ, оценке жизнеспособности миокарда и выявлении зон ишемии. «Золотым стандартом» в определении массы миокарда, сократимости сердца и оценке объемов камер является МРТ сердца. Указанные способы диагностики могут использоваться самостоятельно или совместно с трансторакальной эхокардиографией, повышают точность диагностики и в меньшей степени являются субъективными. Однако применение этих методов ограничено наличием ионизирующего излучения, необходимостью применения радиофармпрепаратов, высокой стоимостью оборудования, труднодоступностью и низкой пропускной способностью. В связи с этим указанные методики не могут быть использованы в качестве скрининговых [6—7].
Регулярное определение систолической функции сердца необходимо при любой кардиальной патологии, особенно у пациентов с сердечной недостаточностью или ишемической болезнью сердца. Кроме того, выявление изменений систолической функции миокарда крайне важно на фоне подбора и контроля лечения, реабилитации пациентов или при физической активности.
Известно, что характеристики пульсовой волны зависят от систолической функции миокарда, клапанной патологии, а также от состояния сосудистой стенки. Регистрируя пульсовую волну у пациента, мы имеем возможность определить состояние и динамику систолической функции сердца.
Графически зарегистрировать пульс возможно с помощью методов сфигмографии или фотоплетизмографии с помощью механических или оптических датчиков.
В графике пульсовой волны выделяют восходящий участок — анакроту, инцизуру, дикротический подъем и катакроту (нисходящий участок кривой пульсовой волны). Растяжение стенки сосуда, возникающее вследствие повышения систолического давления, отражается на пульсовой волне в виде участка подъема — анакроты. Этот участок отображает временной интервал от начала периода изгнания крови из желудочков до достижения максимального давления в сосуде. В конце изгнания крови до закрытия полулунных клапанов происходит снижение давления в аорте, на кривой пульсовой волны регистрируется инцизура. Затем полулунные клапаны закрываются, кровь отражается от закрытых клапанов, и возникает повторная волна повышения давления (дикротический подъем или зубец). Время от момента снижения давления в артерии до минимального и восстановление исходного диаметра артерии отображается спадом пульсовой волны — катакрота [8].
Форма пульсовой волны индивидуальна и может помочь в оценке состояния сердечно-сосудистой системы. Она зависит от частоты пульса, состояния сосудистой стенки, диаметра сосудов и многих других показателей. По данным сфигмограммы можно определить продолжительность сердечного цикла, частоту и ритм сердечных сокращений. Продолжительность анакротического подъема и инцизуры отражает длительность периода изгнания крови, а также помогает определить скорость изгнания, состояние аорты и полулунных клапанов. По наклону анакроты можно рассчитать скорость пульса. Также, анализируя пульсовую волну, можно выявить начало диастолы желудочков (это соответствует возникновению инцизуры) и фазы изометрического расслабления желудочков (отражается появлением дикротического подъема) [9].
При наличии повышенного периферического сопротивления кривая пульсовой волны расценивается как pulsus tardus. Отмечается пологий, неровный подъем и «позднее систолическое выпячивание» (вершина кривой смещена к окончанию систолы). Такая форма кривой пульсовой волны может наблюдаться при развитии атеросклероза стенок сосудов, гипертонической болезни, а также у пациентов с аортальным стенозом.
При сниженном периферическом сопротивлении и высоком систолическом выбросе, что отмечается, например, у пациентов с недостаточностью аортального клапана, пульсовая волна имеет форму pulsus celer. При этом регистрируются крутой подъем, резкое снижение пульсовой волны и маловыраженная инцизура.
Необходимо также отметить, что при сниженной эластичности сосудистой стенки инцизура располагается ближе к вершине кривой. При вазодилатации она, напротив, расположена в пределах нижней половины сфигмограммы. К патологическим признакам кривой пульса относятся наличие у вершины добавочных волн (симптом «петушиного гребня»), регистрация более пологой катакроты по сравнению с анакротой, наличие на восходящей части «ступеньки», маловыраженный дикротический зубец, увеличенная продолжительность анакротической фазы. Различные исследования показали, что патологические признаки пульсовой волны соотносятся с различными заболеваниями. Так, например, отсутствие дикротического подъема на кривой сфигмограммы наблюдается при гипертонической болезни и атеросклерозе [10, 11].
Скорость распространения пульсовой волны (СРПВ) помогает оценить функционирование сосудистой системы, тонус сосудов, влияние лекарственных средств на сосудистую стенку. СРПВ изменчива и зависит от множества факторов, таких как строение сосуда, его диаметр, жесткость стенки, возраст, уровень АД, ЧСС и ряда других [12].
Как показало Роттердамское исследование, СРПВ является прогностическим фактором ИБС и инсульта. При увеличении СРПВ отмечалось достоверное повышение риска сердечно-сосудистых событий [13].
Измерение СРПВ является методом исследования упруговязких свойств сосудистой системы. Данные свойства зависят от морфологии стенки сосуда, возраста и других индивидуальных особенностей пациента. По мнению ряда авторов, СРПВ увеличивается с возрастом. Кроме того, СРПВ различается для артерий эластического и мышечного типа. Считается, что СРПВ у здоровых людей колеблется в пределах 500—700 см/с для сосудов эластического типа и 500—800 см/с для сосудов мышечного типа. Для оценки СРПВ датчики пульса устанавливают на лучевую, сонную и бедренную артерии и одновременно проводится запись сфигмограмм. В дальнейшем производится расчет СРПВ с использованием длины артерии между датчиками пульса по специальным формулам [11].
Измерение СПРВ считается «золотым стандартом» для оценки жесткости сосуда, потому что на данный момент имеется большая доказательная база, подтверждающая этот аспект. Кроме того, оценка СРПВ является доступным методом в техническом плане. СРПВ — важный биомаркер сосудистого повреждения, который может помочь в определении общего сердечно-сосудистого риска [15].
Определение СРПВ проводят, используя метод фотоплетизмографии. В основе плетизмографии лежит принцип изменения объема ткани в зависимости от кровенаполнения. Плетизмография применяется для получения данных минутного объема кровообращения. Объем ткани является постоянным, а объем крови, заполняющей ткань, меняется с каждой фазой сердечного цикла. Запись кривой плетизмографии (плетизмограммы) проводится специальными приборами — плетизмографами. Различают водяные, электро- и фотоплетизмографы. Такое устройство имеет специальный датчик и плетизмографический рецептор. При фотоплетизмографии регистрируется оптическая плотность ткани. На участок ткани, который исследуется, воздействует инфракрасный свет, который затем поступает в фотопреобразователь. Интенсивность сигнала зависит от объема крови в данном участке ткани. Сигнал, получаемый в результате фотопреобразования, называется фотоплетизмограммой [15,16].
Параметры пульсовой волны в оценке систолической функции сердца
В ряде работ рассматривали отношение скорости пульсовой волны к глобальной продольной деформации при гипертонической болезни. Отношение скорости пульсовой волны к глобальной продольной деформации (PWV/GLS) было ниже у гипертоников (n=299), чем в контрольной группе (-0,61±0,21 против -0.45±0,11 м/с, р<0,001). Низкие значения PWV/GLS были ассоциированы с толщиной интимы в сонной артерии более 0,9 мм, увеличением массы миокарда ЛЖ и объема левого предсердия (р<0,02). При этом не было значимой связи между показателем эластичности артерии и ЛЖ с толщиной интимы в сонной артерии и резервом коронарного кровотока [17].
Как известно, артериальная жесткость увеличивает нагрузку давлением на ЛЖ, что приводит к гипертрофии ЛЖ и субэндокардиальной ишемии. Кроме того, нейрогормоны стимулируют фиброз миокарда и дисфункцию ЛЖ. Корейские исследователи проводили работы по изучению взаимосвязи артериальной жесткости и механической функции ЛЖ у пациентов с гипертонической болезнью (n=195). Группе пациентов с гипертонией измерялась СРПВ, оценивался показатель GLS с помощью методики speckle traking, а также определялся альдостерон плазмы для оценки нейрогормональной активации. Было выявлено, что у пациентов с артериальной гипертензией GLS ЛЖ и левого предсердия коррелировал с изменением скорости распространения пульсовой волны (β=0,223, p=0,031 и β= −0,311, p=0,002 соответственно). Авторы отметили, что двухмерная слой-специфическая эхокардиография с использованием speckle tracking достоверно обнаруживала механическую дисфункцию ЛЖ и обеспечивала патофизиологическое понимание механических адаптаций ЛЖ при гипертонии [18].
Также разрабатывался метод Modelflow для оценки сердечного выброса по форме пульсовой волны при постоянной записи аппаратом Beat-by-beat, используя трехэлементную модель входного импеданса аорты (характерный импеданс аорты, податливость артерий и системное сосудистое сопротивление). У группы здоровых молодых людей (n=16) во время выполнения физических упражнений с помощью метода Modelflow рассчитывался сердечный выброс. В качестве контрольного метода была использована эхокардиография. Расчетный сердечный выброс, оцененный по методу Modelflow, значительно коррелировал с одновременной оценкой с помощью эхокардиографии. Коэффициенты корреляции варьировали от 0,91 до 0,98 (p<0,001). Несмотря на то, что метод Modelflow несколько переоценил сердечный выброс, ошибки между двумя оценками существенно не отличались. Эти результаты показывали, что метод Modelflow может обеспечить оценку относительного изменения сердечного выброса во время физических нагрузок у здоровых молодых людей [19].
Современные технологии по регистрации пульсовой волны и ЭКГ
Одним из новых приборов для регистрации пульсовой волны является CardioQVARK (Москва, Россия). Это устройство выполнено в виде чехла для телефона, который подключается к смартфону и представляет собой персональный электрокардиограф (см. рисунок).
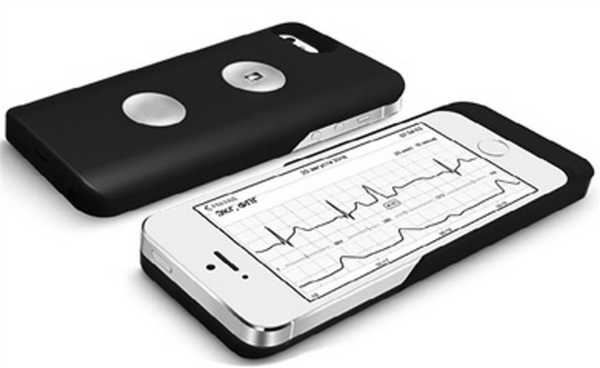
Персональный электрокардиограф CardioQVARK.
CardioQVARK — персональный электрокардиограф, подключаемый к смартфону с установленным программным обеспечением. Система позволяет записывать сигнал ЭКГ с пальцев рук (I стандартное отведение ЭКГ), а также с отведений II, III, aVR, aVL, aVF, V5 с помощью подключаемых электродов. Кроме того, датчики CardioQVARK непрерывно регистрируют фотоплетизмографическое изображение пульсовой волны, синхронизированное с циклами ЭКГ. Представляется возможность регистрации сердечного ритма, оценки динамики ЭКГ в указанных отведениях и определения параметров пульсовой волны.
Крайне интересным представляется расчет времени между деполяризацией миокарда (зубец R) и пиком пульсовой волны. Такой показатель потенциально может ассоциироваться с эффективностью ответа миокарда на возбуждение и временем, необходимым для достижения пульсовой волной дистального капиллярного русла (на пальцах рук). Нами начато исследование для анализа роли различных параметров пульсовой волны в совокупности с записью ЭКГ в оценке гемодинамических показателей.
На основании проведенных исследований следует отметить высокую точность системы CardioQVARK в определении эпизодов фибрилляции предсердий (чувствительность 98%, специфичность 91%), анализе длительности интервала QT (точность в сравнении с 12-канальной ЭКГ — 99%), выявлении патологической волны Т (чувствительность 90%, специфичность 75%), а также при регистрации нарушений атриовентрикулярной проводимости (чувствительность 79%, специфичность 99%). Такие данные обосновывают целесообразность дальнейших исследований с применением системы CardioQVARK [20—23].
Заключение
Параметры пульсовой волны зависят как от состояния сосудов, так и от систолической функции ЛЖ, патологии клапанного аппарата и иной структурной патологии сердца. Оценка систолической функции ЛЖ с помощью параметров пульсовой волны позволила бы улучшить скрининг сердечно-сосудистых заболеваний и повысить доступность обследования. На нашей кафедре начата работа по сравнению параметров пульсовой волны с одновременной записью ЭКГ с комплексными показателями систолической функции ЛЖ при эхокардиографии.
Часть II. Физиология сосудистого русла
1. Краткая характеристика основных гемодинамических показателей
Гемодинамика представляет собой раздел физиологии, изучающий закономерности движения крови в сосудистой системе. Она является составной частью гидродинамики - раздела физики, исследующего законы движения жидкости по трубам.
Ключевыми гемодинамическими параметрами, во многом характеризующими интенсивность сердечной деятельности и функциональное состояние сосудистого русла являются следующие:
минутный объем кровотока (или минутный объем сердца, подробно рассмотрен в части I) - количество крови, выбрасываемое одним из желудочков сердца за 1 минуту; этот же объем протекает через суммарное поперечное сечение любого участка большого или малого круга кровообращения за 1 минуту. Минутный объем, с одной стороны, определяется как произведение систолического объема на частоту сердечных сокращений (т.е. на количество таких систол, произведенных за минуту). С другой стороны, минутный объем кровотока можно определить, исходя из основного уравнения гидродинамики (1)
где Q - количество жидкости, протекающее через поперечное сечение трубки в единицу времени,
Р1 и Р2 - давление в начале и в конце трубки, соответственно разница между этим давлениями (т.н. градиент давления по ходу трубки) является той силой, которая способствует продвижению жидкости в трубке
R - сопротивление движению жидкости, представляет собой силу, препятствующую продвижению жидкости
Если применить данное уравнение к большому кругу кровообращения, то Р1 и Р2 - это будет соответственно давление в устье аорты и в области синусов полых вен (мест впадения полых вен в сердце), Q - минутный объем кровотока, а R - суммарное периферическое сопротивление движению крови. Поскольку давление в области синусов полых вен почти равно нулю, то основное уравнение гидродинамики для сердечно-сосудистой системы (в частности, для большого круга кровообращения) будет выглядеть следующим образом:
где АД - артериальное давление в аорте
R - суммарное периферическое сопротивление движению крови в большом круге кровообращения
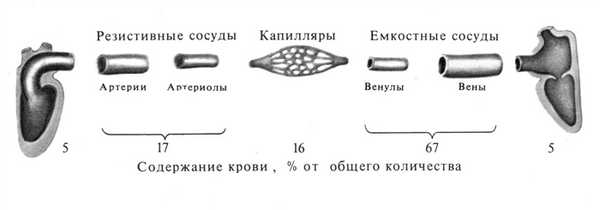
М О - минутный объем кровотока в большом круге кровообращения (т.е. то количество крови, которое выбрасывается левым желудочком за 1 минуту, оно же пересекает любое суммарное поперечное сечение большого круга кровообращения за 1 минуту)
Рис. 15. Распределение минутного объема крови в различных отделах большого круга кровообращения
периферическое сосудистое сопротивление - это суммарное сопротивление, создаваемое сосудистым руслом (большого или малого круга кровообращения) движению крови. Сопротивление, создаваемое каждым в отдельности сосудом (подобно сопротивлению, создаваемому какой-то трубкой) можно рассчитать по формуле Пуазейля (3):
где R - сопротивление движению крови
l - длина сосуда
- вязкость крови, протекающей по сосуду
r - радиус сосуда.
Из данного уравнения следует, что сопротивление движению крови будет тем больше, чем меньше внутренний диаметр сосуда и чем больше его длина и вязкость крови, протекающей по нему.
При движении крови вдоль сосуда в центре потока движутся в основном форменные элементы (осевой ток), а вдоль стенки сосуда - плазма (пристеночный ток). Следовательно, вязкость крови, составляющей осевой ток, будет гораздо выше, чем таковая пристеночного тока. Вместе с тем в большинстве сосудов (за исключением капилляров) выражены и осевой и пристеночный токи, в связи с чем суммарная вязкость крови от сосуда к сосуду не изменяется. И только в капиллярах, отличающихся самым малым диаметром (5-7 мкм) резко сокращается доля осевого тока, что обуславливает уменьшение вязкости крови, заполняющей капилляры.
Самыми узкими сосудами в сосудистом русле являются капилляры. Именно поэтому сопротивление, создаваемое каждым в отдельности капилляром, больше такового создаваемого каждым в отдельности каким-либо другим более крупным сосудом (артериолой, венулой или мелкой артерией).
Вместе с тем суммарное сопротивление, создаваемое какими-то участками сосудистого русла, зависит не только от диаметра просвета сосудов, образующих этот участок, но и от способа их соединения. Известно, что при последовательном подключении трубок суммарное сопротивление движению, создаваемое ими, определяется как сумма сопротивлений каждой в отдельности трубки:
где Rпоследовательное - суммарное периферическое сопротивление, создаваемое группой последовательно соединенных трубок,
R1, R2, R3 и т.д. - соответственно сопротивления движению, создаваемые каждой в отдельности трубкой.
В случае параллельного соединения трубок суммарное сопротивление, создаваемое ими, определяется следующим образом:
Rпараллельное= и т.д. (5)
где Rпараллельное - суммарное периферическое сопротивление, создаваемое группой параллельно соединенных трубок,
Следовательно, суммарное сопротивление движению, создаваемое определенной группой трубок, будет выше при последовательном их соединении и меньше в случае параллельного их соединения.
кровяное давление - это суммарный запас энергии, которым обладает движущаяся кровь в определенном участке сосудистого русла. Этот суммарный запас энергии сообщается крови в результате работы сердца. Различают артериальное, капиллярное и венозное давление. В связи с тем, что кровь при своем движении преодолевает силы сопротивления движению (прежде всего трение о стенку сосуда), кровяное давление по ходу сосудистого русла снижается. Так, максимальным оно является в сосудах, выносящих кровь из сердца (в аорте и легочном стволе), а минимальным (близким, но неравным нулю) - в сосудах, возвращающих кровь в сердце (в полых и легочных венах). Таким образом, чем дальше удалилась кровь от сердца как насоса (т.е. чем больший путь она прошла по сосудистому руслу), тем меньшим запасом суммарной энергии она обладает (т.е. тем ниже кровяное давление в данном участке сосудистого русла).
В начальной части сосудистого русла (в крупных, средних и даже некоторых мелких артериях) кровяное давление зависит от фазы сердечного цикла: в момент систолы, когда желудочками изгоняются порции крови, оно возрастает, а в момент диастолы - напротив, понижается. В мелких же артериях, артериолах, капиллярах, венулах и венах кровяное давление не зависит от фаз сердечного цикла, оно уменьшается по ходу сосудистого русла, но в каждом данном его участке является постоянным, не зависящим от фазы сердечного цикла. Превращению пульсирующего кровотока в постоянный способствуют крупные артерии (сосуды эластического типа) и отчасти средние артерии (сосуды смешанного типа - мышечно-эластического). Благодаря своей эластичности стенки этих артерий в момент систолы желудочков растягиваются, принимая определенное количество крови (при этом давление в них повышается до уровня максимального или систолического), тогда как в момент диастолы - сжимаются, проталкивая принятую из желудочка порцию крови далее (при этом давление в начальном отделе сосудистого русла понижается до уровня минимального или диастолического). Таким образом пульсирующий кровоток постепенно по ходу сосудистого русла преобразуется в постоянный, а пульсовые колебания артериального давления - гаснут. Постоянное, не зависящее от фаз сердечного цикла, давление в артериолах, капиллярах и венулах, составляющих микроциркуляторное русло (и особенно в капиллярах), является основным залогом нормального осуществления транскапиллярного обмена - того, ради чего существует система кровообращения вообще.
В связи с тем, что давление в артериальной части сосудистого русла колеблется в динамике сердечного цикла, различают следующие его разновидности:
максимальное или систолическое давление - это давление в начальном отделе сосудистого русла в момент систолы желудочков, оно во многом характеризует насосную функцию сердца (величину систолического выброса) и растяжимость крупных и средних артерий. Различают боковое и конечное систолическое давление. Боковое давление - это давление крови, передаваемое на стенки сосудов. Конечное давление - это суммарный запас потенциальной и кинетической энергии, которым обладает движущаяся кровь на определенном участке сосудистого русла; оно на 10-20 мм.рт.ст. выше бокового. Разность между конечным и боковым систолическим давлением называется ударным давлением, которое во многом отражает интенсивность сердечной деятельности и состояние стенок сосудов. В норме величина систолического давления в плечевой артерии у здоровых молодых людей составляет 110-125 мм.рт.ст., а в легочном стволе - 25мм.рт.ст.
минимальное или диастолическое давление - это давление в начальном отделе сосудистого русла в момент диастолы желудочков, во многом зависит от периферического сосудистого сопротивления. В норме его величина в плечевой артерии у здоровых молодых людей составляет 60-80 мм.рт.ст., а в легочном стволе - 10 мм.рт.ст.
среднее артериальное давление - это давление, отражающее энергию движущейся крови, так как если бы она вытекала из сердца не порциями, а непрерывной струей (т.е. без пульсовых колебаний). Иными словами, среднее артериальное давление является равнодействующей артериального давления в разные фазы сердечного цикла и отражает энергию непрерывного движения крови. В связи с тем, что продолжительность понижения диастолического давления больше, чем повышения систолического, среднее артериальное давление ближе к величине диастолического давления и может быть рассчитано по следующей формуле:
АДсреднее= 0,42 АДсистолическое + 0,58 АДдиастолическое (6)
пульсовое артериальное давление является амплитудой колебаний давления в начальном отделе сосудистого русла, обусловленных периодической насосной деятельностью сердца. Пульсовое артериальное давление определяется как разность между систолическим и диастолическим артериальным давлением и во многом характеризует насосную функцию сердца (зависит от величины систолического выброса)
АДпульсовое = АДсистолическое - АДдиастолическое (7)
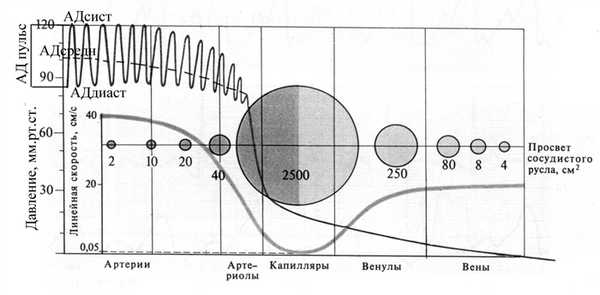
П ульсовые колебания артериального давления в крупных сосудах (т.н. волны первого порядка, самые частые) обусловлены ритмичной периодической работой сердца. Наряду с этими пульсовыми волнами на кривой артериального давления, как правило, наблюдаются еще и дыхательные волны (или волны второго порядка) - небольшие колебания артериального давления, совпадающие с дыхательными движениями (при вдохе артериальное давление несколько понижается, а при выдохе - наоборот, повышается). Наконец, в некоторых случаях на кривой артериального давления могут появляться волны третьего порядка - самые медленные повышения и понижения артериального давления, каждое из которых охватывает несколько волн второго порядка; эти волны являются следствием периодического изменения тонуса сосудодвигательного центра, вызванного, как правило, недостаточным кровоснабжением мозга кислородом или отравлением его некоторыми ядами.
Читайте также:
