Изменения кровообращения у новорожденного. Закрытие артериального протока
Добавил пользователь Владимир З. Обновлено: 01.02.2026
МКБ-10

Общие сведения
Открытый артериальный (Боталлов) проток - незаращение добавочного сосуда, соединяющего аорту и легочную артерию, который продолжает функционировать после истечения срока его облитерации. Артериальный проток (dustus arteriosus) является необходимой анатомической структурой в системе эмбрионального кровообращения. Однако после рождения, в связи с появлением легочного дыхания, необходимость в артериальном протоке исчезает, он перестает функционировать и постепенно закрывается. В норме функционирование протока прекращается в первые 15-20 часов после рождения, полное анатомическое закрытие продолжается от 2 до 8 недель.
В кардиологии открытый артериальный проток составляет 9,8% среди всех врожденных пороков сердца и в 2 раза чаще диагностируется у женщин. Открытый артериальный проток встречается как в изолированной форме, так и в сочетании с другими аномалиями сердца и сосудов (5-10%):
- стенозом устья аорты;
- стенозом и атрезией легочных артерий;
- открытым атриовентирикулярным каналом;
- ДМЖП, ДМПП и др.
При пороках сердца с дуктус-зависимым кровообращением (транспозиции магистральных артерий, крайней форме тетрады Фалло, перерыве дуги аорты, критическом легочном или аортальном стенозе, синдроме гипоплазии левого желудочка) открытый артериальный проток является жизненно необходимой сопутствующей коммуникацией.

Причины
Открытый артериальный проток обычно встречается у недоношенных детей и крайне редко у детей, рожденных в срок. У недоношенных новорожденных с массой менее 1750 г частота открытого артериального протока составляет 30-40 %, у детей, чья масса при рождении не превышает 1000г, - 80%. Нередко у таких детей обнаруживаются врожденные аномалии развития ЖКТ и мочеполовой системы. Незаращение фетальной коммуникации у недоношенных в постнатальном периоде связано с синдромом дыхательных расстройств, асфиксией в родах, стойким метаболическим ацидозом, длительной оксигенотерапией высокими концентрациями кислорода, избыточной инфузионной терапией.
У доношенных детей открытый артериальный проток намного чаще встречается в высокогорных районах. В некоторых случаях его незаращение вызвано патологией самого протока. Довольно часто открытый артериальный проток является наследуемой сердечной аномалией. Артериальный проток может оставаться открытым у детей, чьи матери перенесли краснуху в I триместре беременности.
Таким образом, факторами риска открытого артериального протока являются преждевременные роды и недоношенность, семейный анамнез, наличие других ВПС, инфекционные и соматические заболевания беременной.
Особенности гемодинамики при открытом артериальном протоке
Открытый артериальный проток расположен в верхнем этаже переднего средостения; он берет начало от дуги аорты на уровне левой подключичной артерии и впадает в легочный ствол в месте его бифуркации и частично в левую легочную артерию; иногда встречается правосторонний или двусторонний артериальный проток. Боталлов проток может иметь цилиндрическую, конусовидную, окончатую, аневризматическую форму; его длина составляет 3-25 мм, ширина - 3-15 мм.
Артериальный проток и открытое овальное окно - необходимые физиологические компоненты фетального кровообращения. У плода кровь из правого желудочка поступает в легочную артерию, а оттуда (поскольку легкие не функционируют) через артериальный проток - в нисходящую аорту. Сразу после рождения, с первым самостоятельным вдохом новорожденного, легочное сопротивление падает, а давление в аорте поднимается, приводя к развитию сброса крови из аорты в легочную артерию. Включение легочного дыхания способствует спазму протока за счет сокращения его гладкомышечной стенки. Функциональное закрытие артериального протока у доношенных детей происходит в течение 15-20 ч после рождения. Однако полная анатомическая облитерация Боталлова протока наступает к 2-8 неделе внеутробной жизни.
Об открытом артериальном протоке говорят в том случае, если его функционирование не прекращается спустя 2 недели после рождения. Открытый артериальный проток относится к порокам бледного типа, поскольку при нем происходит сброс оксигенированной крови из аорты в легочную артерию. Артерио-венозный сброс обусловливает поступление дополнительных объемов крови в легкие, переполнение легочного сосудистого русла и развитие легочной гипертензии. Повышенная объемная нагрузка на левые отделы сердца приводит к их гипертрофии и дилатации.
Классификация открытого артериального протока
С учетом уровня давления в легочной артерии выделяют 4 степени порока:
- Давление в ЛА в систолу не превышает 40% от артериального;
- Умеренная легочная гипертензия; давление в ЛА составляет 40-75% от артериального;
- Выраженная легочная гипертензия; давление в ЛА более 75% от артериального; лево-правый сброс крови сохраняется;
- Тяжелая степень легочной гипертензии; давление в ЛА равняется или превышает системное, что приводит к возникновению право-левого сброса крови.
В естественном течении открытого артериального протока прослеживаются 3 стадии:
- I - стадия первичной адаптации (первые 2-3 года жизни ребенка). Характеризуется клинической манифестацией открытого артериального протока; нередко сопровождается развитием критических состояний, которые в 20% случаев заканчиваются летальным исходом без своевременной кардиохирургической помощи.
- II - стадия относительной компенсации (от 2-3 лет до 20 лет). Характеризуется развитием и длительным существованием гиперволемии малого круга, относительного стеноза левого атрио-вентрикулярного отверстия, систолической перегрузки правого желудочка.
- III - стадия склеротических изменений легочных сосудов. Дальнейшее естественное течение открытого артериального протока сопровождается перестройкой легочных капилляров и артериол с развитием в них необратимых склеротических изменений. На этой стадии клинические проявления открытого артериального протока постепенно вытесняются симптомами легочной гипертензии.
Симптомы открытого артериального протока
Клиническое течение открытого артериального протока варьирует от бессимптомного до крайне тяжелого. Открытый артериальный проток малого диаметра, не приводящий к нарушению гемодинамики, может длительное время оставаться нераспознанным. И, напротив, наличие широкого артериального протока обусловливает бурное развитие симптоматики уже в первые дни и месяцы жизни ребенка.
Первыми признаками порока могут служить постоянная бледность кожных покровов, преходящий цианоз при сосании, крике, натуживании; дефицит массы тела, отставание в моторном развитии. Дети с открытым артериальным протоком склонны к частым заболеваниям бронхитами, пневмониями. При физической активности развивается одышка, утомляемость, тахикардия, неритмичность сердцебиения.
Прогрессирование порока и ухудшение самочувствия может происходить в пубертатный период, после родов, в связи со значительными физическими перегрузками. При этом цианоз становится постоянным, что свидетельствует о развитии веноартериального сброса и нарастании сердечной недостаточности.
Осложнениями открытого артериального протока могут служить бактериальный эндокардит, аневризма протока и ее разрыв. Средняя продолжительность жизни при естественном течении протока составляет 25 лет. Спонтанная облитерация и закрытие открытого артериального протока происходит крайне редко.
Диагностика открытого артериального протока
При осмотре пациента с открытым артериальным протоком нередко выявляется деформация грудной клетки (сердечный горб), усиленная пульсация в проекции верхушки сердца. Основным аускультативным признаком открытого артериального протока служит грубый систоло-диастолический шум с «машинным» компонентом во II межреберье слева.
Обязательный минимум исследований при открытом артериальном протоке включает рентгенографию грудной клетки, ЭКГ, фонокардиографию, УЗИ сердца. Рентгенологически выявляется кардиомегалия за счет увеличения размеров левого желудочка, выбухание дуги легочной артерии, усиление легочного рисунка, пульсация корней легких. ЭКГ-признаки открытого артериального протока включают указания на гипертрофию и перегрузку левого желудочка; при легочной гипертензии - на гипертрофию и перегрузку правого желудочка. С помощью ЭхоКГ определяются косвенные признаки порока, производится непосредственная визуализация открытого артериального протока, измеряются его размеры.
К проведению аортографии, зондирования правых отделов сердца, МСКТ и МРТ сердца прибегают при высокой легочной гипертензии и сочетании открытого артериального порока с другими аномалиями сердца. Дифференциальную диагностику открытого артериального протока следует проводить с дефектом аортолегочной перегородки, общим артериальным стволом, аневризмой синуса Вальсальвы, аортальной недостаточностью и артериовенозным свищом.
Лечение открытого артериального протока
У недоношенных детей применяется консервативное ведение открытого артериального протока. Оно предполагает введение ингибиторов синтеза простагландина (индометацина) с целью стимуляции самостоятельной облитерации протока. При отсутствии эффекта от 3-кратного повторения медикаментозного курса у детей старше 3-х недель показано хирургическое закрытие протока.
В детской кардиохирургии при открытом артериальном протоке используются открытые и эндоваскулярные операции. Открытые вмешательства могут включать перевязку открытого артериального протока, его клипирование сосудистыми клипсами, пересечение протока с ушиванием легочного и аортального концов. Альтернативными методами закрытия открытого артериального протока являются его клипирование в процессе торакоскопии и катетерная эндоваскулярная окклюзия (эмболизация) специальными спиралями.
Прогноз и профилактика открытого артериального протока
Открытый артериальный проток даже небольших размеров сопряжен с повышенным риском преждевременной смерти, поскольку ведет к снижению компенсаторных резервов миокарда и легочных сосудов, присоединением серьезных осложнений. Больные, перенесшие хирургическое закрытие протока, имеют лучшие показатели гемодинамики и большую продолжительность жизни. Послеоперационная летальность низка.
Для уменьшения вероятности рождения ребенка с открытым артериальным протоком необходимо исключить все возможные риск-факторы: курение, алкоголь, прием лекарственных препаратов, стрессы, контакты с инфекционными больными и пр. При наличии ВПС у близких родственников на этапе планирования беременности необходима консультация генетика.
Врожденные пороки сердца
Врожденные пороки сердца - группа заболеваний, объединенных наличием анатомических дефектов сердца, его клапанного аппарата или сосудов, возникших во внутриутробном периоде, приводящих к изменению внутрисердечной и системной гемодинамики. Проявления врожденного порока сердца зависят от его вида; к наиболее характерным симптомам относятся бледность или синюшность кожных покровов, шумы в сердце, отставание в физическом развитии, признаки дыхательной и сердечной недостаточности. При подозрении на врожденный порок сердца выполняется ЭКГ, ФКГ, рентгенография, ЭхоКГ, катетеризация сердца и аортография, кардиография, МРТ сердца и т. д. Чаще всего при врожденных пороках сердца прибегают к кардиохирургической операции - оперативной коррекции выявленной аномалии.

Врожденные пороки сердца - весьма обширная и разнородная группа заболеваний сердца и крупных сосудов, сопровождающихся изменением кровотока, перегрузкой и недостаточностью сердца. Частота встречаемости врожденных пороков сердца высока и, по оценке различных авторов, колеблется от 0,8 до 1,2% среди всех новорожденных. Врожденные пороки сердца составляют 10-30% всех врожденных аномалий. В группу врожденных пороков сердца входят как относительно легкие нарушения развития сердца и сосудов, так и тяжелые формы патологии сердца, несовместимые с жизнью.
Многие виды врожденных пороков сердца встречаются не только изолированно, но и в различных сочетаниях друг с другом, что значительно утяжеляет структуру дефекта. Примерно в трети случаев аномалии сердца сочетаются с внесердечными врожденными пороками ЦНС, опорно-двигательного аппарата, ЖКТ, мочеполовой системы и пр.
К наиболее частым вариантам врожденных пороков сердца, встречающимся в кардиологии, относятся дефекты межжелудочковой перегородки (ДМЖП - 20%), дефекты межпредсердной перегородки (ДМПП), стеноз аорты, коарктация аорты, открытый артериальный проток (ОАП), транспозиция крупных магистральных сосудов (ТКС), стеноз легочной артерии (10-15% каждый).

Причины врожденных пороков сердца
Этиология врожденных пороков сердца может быть обусловлена хромосомными нарушениями (5%), генной мутацией (2-3%), влиянием факторов среды (1-2%), полигенно-мультифакториальной предрасположенностью (90%).
Различного рода хромосомные аберрации приводят к количественным и структурным изменениям хромосом. При хромосомных перестройках отмечаются множественные полисистемные аномалии развития, включая врожденные пороки сердца. В случае трисомии аутосом наиболее частыми пороками сердца оказываются дефекты межпредсердной или межжелудочковой перегородок, а также их сочетание; при аномалиях половых хромосом врожденные пороки сердца встречаются реже и представлены, главным образом, коарктацией аорты или дефектом межжелудочковой перегородки.
Врожденные пороки сердца, обусловленные мутациями единичных генов, также в большинстве случаев сочетаются с аномалиями других внутренних органов. В этих случаях сердечные пороки являются частью аутосомно-доминантных (синдромы Марфана, Холта-Орама, Крузона, Нунана и др.), аутосомно-рецессивных синдромов (синдром Картагенера, Карпентера, Робертса, Гурлер и др.) или синдромов, сцепленных с Х-хромосомой (синдромы Гольтца, Аазе, Гунтера и др.).
Среди повреждающих факторов внешней среды к развитию врожденных пороков сердца приводят вирусные заболевания беременной, ионизирующая радиация, некоторые лекарственные препараты, пагубные привычки матери, производственные вредности. Критическим периодом неблагоприятного воздействия на плод являются первые 3 месяца беременности, когда происходит фетальный органогенез.
Внутриутробное поражение плода вирусом краснухи наиболее часто вызывает триаду аномалий - глаукому или катаракту, глухоту, врожденные пороки сердца (тетраду Фалло, транспозицию магистральных сосудов, открытый артериальный проток, общий артериальный ствол, клапанные пороки, стеноз легочной артерии, ДМЖП и др.). Также обычно имеют место микроцефалия, нарушение развития костей черепа и скелета, отставание в умственном и физическом развитии.
В структуру эмбриофетального алкогольного синдрома обычно входят дефекты межжелудочковой и межпредсердной перегородки, открытый артериальный проток. Доказано, что тератогенное действие на сердечно-сосудистую систему плода оказывает прием амфетаминов, приводящий к транспозиции магистральных сосудов и ДМЖП; противосудорожных средств, обусловливающих развитие стеноза аорты и легочной артерии, коарктации аорты, открытого артериального протока, тетрады Фалло, гипоплазии левых отделов сердца; препаратов лития, приводящих к атрезии трехстворчатого клапана, аномалии Эбштейна, ДМПП; прогестагенов, вызывающих тетраду Фалло, другие сложные врожденные пороки сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Кроме непосредственных причин, выделяют факторы риска формирования аномалий сердца у плода. К ним относят возраст беременной младше 15-17 лет и старше 40 лет, токсикозы I триместра, угрозу самопроизвольного прерывания беременности, эндокринные нарушения у матери, случаи мертворождения в анамнезе, наличие в семье других детей и близких родственников с врожденными пороками сердца.
Классификация врожденных пороков сердца
Существует несколько вариантов классификаций врожденных пороков сердца, в основу которых положен принцип изменения гемодинамики. С учетом влияния порока на легочный кровоток выделяют:
- врожденные пороки сердца с неизмененным (либо незначительно измененным) кровотоком в малом круге кровообращения: атрезия аортального клапана, стеноз аорты, недостаточность легочного клапана, митральные пороки (недостаточность и стеноз клапана), коарктация аорты взрослого типа, трехпредсердное сердце и др.
- врожденные пороки сердца с увеличенным кровотоком в легких: не приводящие к развитию раннего цианоза (открытый артериальный проток, ДМПП, ДМЖП, аортолегочный свищ, коарктация аорты детского типа, синдром Лютамбаше), приводящие к развитию цианоза (атрезия трехстворчатого клапана с большим ДМЖП, открытый артериальный проток с легочной гипертензией)
- врожденные пороки сердца с обедненным кровотоком в легких: не приводящие к развитию цианоза (изолированный стеноз легочной артерии), приводящие к развитию цианоза (сложные пороки сердца - болезнь Фалло, гипоплазия правого желудочка, аномалия Эбштейна)
- комбинированные врожденные пороки сердца, при которых нарушаются анатомические взаимоотношения между крупными сосудами и различными отделами сердца: транспозиция магистральных артерий, общий артериальный ствол, аномалия Тауссиг-Бинга, отхождение аорты и легочного ствола из одного желудочка и пр.
В практической кардиологии используется деление врожденных пороков сердца на 3 группы: пороки «синего» (цианотического) типа с веноартериальным шунтом (триада Фалло, тетрада Фалло, транспозиция магистральных сосудов, атрезия трехстворчатого клапана); пороки «бледного» типа с артериовенозным сбросом (септальные дефекты, открытый артериальный проток); пороки с препятствием на пути выброса крови из желудочков (стенозы аорты и легочной артерии, коарктация аорты).
Нарушения гемодинамики при врожденных пороках сердца
В результате выше названных причин у развивающего плода может нарушаться правильное формирование структур сердца, что выражается в неполном или несвоевременном закрытии перепонок между желудочками и предсердиями, неправильном образовании клапанов, недостаточном повороте первичной сердечной трубки и недоразвитии желудочков, аномальном расположении сосудов и т. д. После рождения у части детей остаются открытыми артериальный проток и овальное окно, которые во внутриутробном периоде функционируют в физиологическом порядке.
При врожденных пороках сердца бледного типа с артериовенозным сбросом вследствие гиперволемии развивается гипертензия малого круга кровообращения; при пороках синего типа с веноартериальным шунтом у больных имеет место гипоксемия.
Около 50% детей с большим сбросом крови в малый круг кровообращения погибают без кардиохирургической помощи на первом году жизни от явлений сердечной недостаточности. У детей, перешагнувших этот критический рубеж, сброс крови в малый круг уменьшается, самочувствие стабилизируется, однако постепенно прогрессируют склеротические процессы в сосудах легких, обусловливая легочную гипертензию.
При цианотических врожденных пороках сердца венозный сброс крови или ее смешение приводит к перегрузке большого и гиповолемии малого круга кровообращения, вызывая снижение насыщения крови кислородом (гипоксемию) и появление синюшности кожи и слизистых. Для улучшения вентиляции и перфузии органов развивается коллатеральная сеть кровообращения, поэтому, несмотря на выраженные нарушения гемодинамики, состояние больного может длительное время оставаться удовлетворительным. По мере истощения компенсаторных механизмов, вследствие длительной гиперфункции миокарда, развиваются тяжелые необратимые дистрофические изменения в сердечной мышце. При цианотических врожденных пороках сердца оперативное вмешательство показано уже в раннем детском возрасте.
Симптомы врожденных пороков сердца
Клинические проявления и течение врожденных пороков сердца определяется видом аномалии, характером нарушений гемодинамики и сроками развития декомпенсации кровообращения.
У новорожденных с цианотическими врожденными пороками сердца отмечается цианоз (синюшность) кожных покровов и слизистых оболочек. Синюшность усиливается при малейшем напряжении: сосании, плаче ребенка. Белые пороки сердца проявляются побледнением кожи, похолоданием конечностей.
Дети с врожденными пороками сердца обычно беспокойные, отказываются от груди, быстро устают в процессе кормления. У них появляется потливость, тахикардия, аритмии, одышка, набухание и пульсация сосудов шеи. При хроническом нарушении кровообращения дети отстают в прибавлении веса, росте и физическом развитии. При врожденных пороках сердца обычно сразу поле рождения выслушиваются сердечные шумы. В дальнейшем обнаруживаются признаки сердечной недостаточности (отеки, кардиомегалия, кардиогенная гипотрофия, гепатомегалия и др.).
Осложнениями врожденных пороков сердца могут стать бактериальный эндокардит, полицитемия, тромбозы периферических сосудов и тромбоэмболии сосудов головного мозга, застойные пневмонии, синкопальные состояния, одышечно-цианотические приступы, стенокардитический синдром или инфаркт миокарда.
Диагностика врожденных пороков сердца
Выявление врожденных пороков сердца осуществляется путем комплексного обследования. При осмотре ребенка отмечают окраску кожных покровов: наличие или отсутствие цианоза, его характер (периферический, генерализованный). При аускультации сердца нередко выявляется изменение (ослабление, усиление или расщепление) сердечных тонов, наличие шумов и пр. Физикальное обследование при подозрении на врожденный порок сердца дополняется инструментальной диагностикой - электрокардиографией (ЭКГ), фонокардиографией (ФКГ), рентгенографией органов грудной клетки, эхокардиографией (ЭхоКГ).
ЭКГ позволяет выявить гипертрофию различных отделов сердца, патологическое отклонение ЭОС, наличие аритмий и нарушений проводимости, что в совокупности с данными других методов клинического обследования позволяет судить о тяжести врожденного порока сердца. С помощью суточного холтеровского ЭКГ-мониторирования обнаруживаются скрытые нарушения ритма и проводимости. Посредством ФКГ более тщательно и детально оценивается характер, длительность и локализация сердечных тонов и шумов. Данные рентгенографии органов грудной клетки дополняют предыдущие методы за счет оценки состояния малого круга кровообращения, расположения, формы и размеров сердца, изменений со стороны других органов (легких, плевры, позвоночника). При проведении ЭхоКГ визуализируются анатомические дефекты перегородок и клапанов сердца, расположение магистральных сосудов, оценивается сократительная способность миокарда.
При сложных врожденных пороках сердца, а также сопутствующей легочной гипертензии, с целью точной анатомической и гемодинамической диагностики, возникает необходимость в выполнении зондирования полостей сердца и ангиокардиографии.
Лечение врожденных пороков сердца
Наиболее сложной проблемой в детской кардиологии является хирургическое лечение врожденных пороков сердца у детей первого года жизни. Большинство операций в раннем детском возрасте выполняется по поводу цианотических врожденных пороков сердца. При отсутствии у новорожденного признаков сердечной недостаточности, умеренной выраженности цианоза операция может быть отложена. Наблюдение за детьми с врожденными пороками сердца осуществляют кардиолог и кардиохирург.
Специфическое лечение в каждом конкретном случае зависит от разновидности и степени тяжести врожденного порока сердца. Операции при врожденных дефектах перегородок сердца (ДМЖП, ДМПП) могут включать пластику или ушивание перегородки, рентгенэндоваскулярную окклюзию дефекта. При наличии выраженной гипоксемии детям с врожденными пороками сердца первым этапом выполняется паллиативное вмешательство, предполагающее наложение различного рода межсистемных анастомозов. Подобная тактика улучшает оксигенацию крови, уменьшает риск осложнений, позволяет провести радикальную коррекцию в более благоприятных условиях. При аортальных пороках выполняется резекция или баллонная дилатация коарктации аорты, пластика аортального стеноза и др. При ОАП производится его перевязка. Лечение стеноза легочной артерии заключается в проведении открытой или эндоваскулярной вальвулопластики и т. д.
Анатомически сложные врожденные пороки сердца, при которых радикальная операция не представляется возможной, требуют выполнения гемодинамической коррекции, т. е. разделения артериального и венозного потоков крови без устранения анатомического дефекта. В этих случаях могут проводиться операции Фонтена, Сеннинга, Мастарда и др. Серьезные пороки, не поддающиеся оперативному лечению, требуют проведения пересадки сердца.
Консервативное лечение врожденных пороков сердца может включать в себя симптоматическую терапию одышечно-цианотических приступов, острой левожелудочковой недостаточности (сердечной астмы, отека легких), хронической сердечной недостаточности, ишемии миокарда, аритмий.
Прогноз и профилактика врожденных пороков сердца
В структуре смертности новорожденных врожденные пороки сердца занимают первое место. Без оказания квалифицированной кардиохирургической помощи в течение первого года жизни погибает 50-75% детей. В периоде компенсации (2-3 года) смертность снижается до 5%. Ранее выявление и коррекция врожденного порока сердца позволяет существенно улучшить прогноз.
Профилактика врожденных пороков сердца требует тщательного планирования беременности, исключения воздействия неблагоприятных факторов на плод, проведения медико-генетического консультирования и разъяснительной работы среди женщин групп риска по рождению детей с сердечной патологией, решения вопроса о пренатальной диагностике порока (УЗИ, биопсия хориона, амниоцентез) и показаниях к прерыванию беременности. Ведение беременности у женщин с врожденными пороками сердца требует повышенного внимания со стороны акушера-гинеколога и кардиолога.
Открытое овальное окно
Открытое овальное окно - неполное закрытие овального отверстия в межпредсердной перегородке, в норме функционирующего в эмбриональный период и зарастающего в первый год жизни ребенка. Открытое овальное окно может проявляться цианозом носогубного треугольника, замедлением физического развития, одышкой и тахикардией, внезапными обмороками, головной болью, частыми ОРВИ и бронхолегочными заболеваниями. Диагностика открытого овального окна включает ЭКГ (в покое и после физической нагрузки), обычную и доплер-ЭхоКГ, рентгенографию, зондирование полостей сердца. При открытом овальном окне может применяться антикоагулянтная терапия, при необходимости - оперативное лечение (эндоваскулярная окклюзия дефекта).

У здоровых доношенных детей при нормальных условиях развития открытое овальное окно обычно закрывается и перестает действовать уже в первые 12 месяцев после рождения. Но его закрытие происходит у каждого индивидуально: в среднем, к возрасту 1 года овальное окно остается открытым у 40-50% детей. Наличие открытого овального окна после 1-2 лет жизни ребенка относят к малым аномалиям развития сердца (МАРС - синдрому). У пациентов зрелого возраста открытое овальное окно выявляется примерно в 25-30% случаев. Достаточно высокая распространенность открытого овального окна определяет актуальность этой проблемы в современной кардиологии.

Причины открытого овального окна
Все дети рождаются с открытым овальным окном сердца. После первого самостоятельного вдоха у новорожденного включается и начинает полноценно функционировать легочный круг кровообращения, и необходимость в открытом овальном окне отпадает. Повышение давления крови в левом предсердии по сравнению с правым приводит к прикрытию клапана овального окна. В большинстве случаев клапан закрывается плотно и полностью зарастает соединительной тканью - открытое овальное окно исчезает. Иногда отверстие закрывается частично или не зарастает вообще и при определенных условиях (при надсадном кашле, плаче, крике, напряжении передней брюшной стенки) происходит сброс крови из правой предсердной камеры в левую (функционирующее овальное окно).
Причины неполного закрытия овального окна не всегда бывают ясны. Считается, что к открытому овальному окну могут привести наследственная предрасположенность, недоношенность ребенка, врожденные пороки сердца, соединительнотканная дисплазия, воздействие неблагоприятных факторов внешней среды, курение и употребление алкоголя женщиной во время беременности. В силу генетических особенностей диаметр клапана может быть меньше диаметра овального отверстия, что будет препятствовать его полному закрытию.
Открытое овальное окно может сопутствовать врожденным порокам митрального или трикуспидального клапанов, открытому артериальному протоку.
Факторами риска открытия клапана овального окна могут быть значительные физические нагрузки у спортсменов, занимающихся тяжелой атлетикой, борьбой, атлетической гимнастикой. Особенно актуальна проблема открытого овального окна у водолазов и дайверов, погружающихся на значительную глубину и имеющих в 5 раз более высокий риск развития кессонной болезни. У пациентов с тромбофлебитом нижних конечностей или малого таза с эпизодами ТЭЛА в анамнезе сокращение сосудистого русла легких может вызывать повышение давления в правых отделах сердца и возникновение функционирующего открытого овального окна.
Особенности гемодинамики при открытом овальном окне
Клиническое значение открытого овального окна неоднозначно. Открытое овальное окно может не вызывать гемодинамических нарушений и не оказывать негативного воздействия на здоровье пациента за счет небольшого размера и наличия клапана, препятствующего шунту крови слева направо. Большинство людей с открытым овальным окном не подозревают об этой аномалии и ведут обычный образ жизни.
Наличие открытого овального окна у больных первичной легочной гипертензией считается прогностически благоприятным в плане продолжительности жизни. Однако превышение давления в правом предсердии по сравнению с левым при открытом овальном окне приводит к периодическому возникновению право-левого шунта, пропускающего определенный объем крови и приводящего к гипоксемии, преходящим нарушениям мозгового кровообращения (ТИА), развитию угрожающих жизни осложнений: парадоксальной эмболии, ишемического инсульта, инфаркта миокарда, инфаркта почки.
Симптомы открытого овального окна
Открытое овальное окно не имеет специфических внешних проявлений, в большинстве случаев протекает латентно, иногда может сопровождаться скудной симптоматикой. Косвенными признаками открытого овального окна могут являться: резкая бледность или цианоз кожи в области губ и носогубного треугольника при физическом напряжении (плаче, крике, кашле, натуживании, купании ребенка); склонность к частым простудным и воспалительным бронхолегочным заболеваниям; замедление физического развития ребенка (плохой аппетит, недостаточная прибавка в весе), низкая выносливость при физических нагрузках, сочетающаяся с симптомами дыхательной недостаточности (одышкой и тахикардией); внезапные обмороки и симптомы нарушения мозгового кровообращения (особенно у пациентов молодого возраста, при варикозной болезни вен, тромбофлебите нижних конечностей и малого таза).
Пациентов с открытым овальным окном могут беспокоить частые головные боли, мигрень, синдром постуральной гипоксемии - развитие одышки и снижение насыщения артериальной крови кислородом в положении стоя с улучшением состояния при переходе в горизонтальное положение. Осложнения открытого овального окна возникают редко. Для парадоксальной эмболии мозговых сосудов, отягощающей данную аномалию, характерно внезапное развитие неврологической симптоматики и достаточно молодой возраст больного.
Диагностика открытого овального окна
Изучение анамнеза и физикальный осмотр пациента часто не позволяют сразу определить наличие открытого овального окна, а могут лишь допустить возможность данной аномалии межпредсердной перегородки (цианоз кожи, обмороки, частые ОРВИ, отставание развития ребенка). Аускультация помогает выявить присутствие сердечных шумов как результат патологического шунта крови из камеры с более высоким давлением в камеру с низким давлением.
Для установления точного диагноза открытого овального окна используются инструментальные исследования и методы визуализации: ЭКГ (в покое и после физической нагрузки), обычная и доплер- ЭхоКГ, рентгенография грудной клетки, зондирование полостей сердца.
При открытом овальном окне на электрокардиограмме появляются изменения, свидетельствующие о повышении нагрузки на правые отделы сердца, особенно на правое предсердие. У лиц старшего возраста с открытым овальным окном могут выявляться рентгенологические признаки увеличения правых камер сердца и повышение объема крови в сосудистом русле легких.
У новорожденных и у детей раннего возраста применяют трансторакальную двухмерную эхокардиографию, позволяющую визуально определить наличие открытого овального окна и его диаметр, получить графическое изображение движений створок клапана во времени, исключить дефект межпредсердной перегородки. Доплер-ЭхоКГ в графическом и цветовом режиме помогает уточнить наличие и размер открытого овального окна, выявить турбулентный поток крови в области овального отверстия, его скорость и примерный объем шунта.
У детей старшего возраста, подростков и взрослых для диагностики открытого овального окна используют более информативную чреспищеводную ЭхоКГ, дополненную пробой с пузырьковым контрастированием и пробой с натуживанием (пробой Вальсальвы). Пузырьковое контрастирование улучшает визуализацию открытого овального окна, позволяет определить его точные размеры, дать оценку патологического шунта крови.
Наиболее информативным, но более агрессивным методом диагностики открытого овального окна является зондирование сердца, которое проводят непосредственно перед оперативным лечением в специализированном кардиохирургическом стационаре.
Обследование на наличие открытого овального окна необходимо пройти пациентам с варикозной болезнью, тромбофлебитом, нарушением мозгового кровообращения, хроническими заболеваниями легких, входящим в группу риска развития парадоксальной эмболии.
Лечение открытого овального окна
При бессимптомном течении открытое овальное окно может считаться вариантом нормы. Пациентам с открытым овальным окном при наличии эпизода транзиторной ишемической атаки или инсульта в анамнезе для профилактики тромбоэмболических осложнений назначается системная терапия антикоагулянтами и дезагрегантами (варфарином, ацетилсалициловой к-той). Методом контроля антикоагулянтной терапии является международное нормализованное отношение (МНО), которое при открытом овальном окне должно находиться в диапазоне 2-3.
Необходимость устранения открытого овального окна определяется объемом шунтированной крови и его влиянием на работу сердечно-сосудистой системы. При небольшом сбросе крови, отсутствии сопутствующей патологии и осложнений операция не требуется.
При выраженном патологическом сбросе крови из правого предсердия в левое выполняют малотравматичную рентгенэндоваскулярную окклюзию открытого овального окна. Операцию проводят под рентгенологическим и эхокардиоскопическим контролем с помощью специального окклюдера, который, раскрываясь, полностью закупоривает отверстие.
Прогноз открытого овального окна
Пациентам с открытым овальным окном рекомендуется регулярное наблюдение у врача-кардиолога и ЭхоКГ контроль. Выполненная эндоваскулярная окклюзия открытого овального окна позволяет пациентам вернуться к обычному ритму жизни без ограничений. В первые 6 месяцев после оперативного лечения открытого овального окна рекомендован прием антибиотиков для профилактики развития бактериального эндокардита. Наибольший эффект от эндоваскулярного закрытия открытого овального окна отмечается у больных с платипноэ, имевших выраженный сброс крови справа налево.
Открытое овальное окно - лечение в Москве

Комментарии к статье
В сентябре 2019 закрыли ООО 2, 7 см в клинике Ю Корее. Сделали нагрузочную пробу, при выдохе и напряжении пресса с кашлем отчетливо видел сам в монитор фонтаны подкрашенной крови. До этого всего в 2015 был инсульт в 45 лет Потерял часть полей зрения, узнал об инсульте через десть дней проверяя причину потери зрения. Инсульт перенес без потери сознания но сильно упало давление и закружилась голова, скорую вызывать постеснялся, но понял что что то произошло. Через 5 лет лечил простатит, и возможно (скорей всего) врач слишком перебрал с курсами антибиотиков Было три курса 3 недели Таваник через 20 дней т/к лучше не стало 14 дней Вильпрофен - Джозасимин + 8 дней Метронадзол После 20 дней Юнидокс Солютаб (Доксициклин). Антибиотики макролиды как известно часто вызывают аритмию удлиняя интервал QT (азитромицин, кларитромицин, Джозасимин! Рокситромицин, ципрофлоксацин, Эритромицин,! Левофлоксацин, моксифлоксацин) На третьем курсе у меня ритм стал срываться, через месяц начались параксизмы. Установили ЭКС, стали сбивать сотагексал (соталол) с беталок (метопролол) Только хуже. Через два месяца сделал РЧА в клинике Мешалкина, Ритм стал синусовый, но давольно высокий. Сразу после РЧА вырос в покое днем с 60 до 85 потом за пол года снизился, но то ли из-за почек то ли из-за Овального Окна давление было с малой разницей ДД и СД 100/75 стоя падало до 80/60 (ООО обнаружили в Мешалкина, но значения не придали, написали 3 мм и все) Поехал спустя год в Ю Корею обследовать почки, если возможно закрыть Окклюдером ушко левого предсердия. Профессор отказался это делать, но спросил нет ли у меня ООО. Узнав что есть, отравил на обследование с пробой Я все увидел сам, тут же через пару дней он поставил мне окклюдер 2, 7 мм, сказал через три дня можешь жить обыкновенной жизнью. Я спросил а спортом можно, подумав ответил, спортом через месяц. Так как раз в 2015 году инсульт произошел на фоне начала мной значительных усилий на тренировках, похожих на тест (я приступил тогда к тренировкам бег на лыжах только с помощью рук, где в подьем очень сильно напрягается пресс при одновременном отталкивании руками, и при этом естественно сильный вдох и резкий выдох) Прошел год, в груди зашит не нужный ЭКС (это сказал доктор в Мешалкина и в Корее) В Корее по моей просьбе мне переставили включение ЭКС с 50 уд на 40 уд, т/к ни голова у меня не кружится, (а раньше при резком вставании с кровати бывало, так произошел инсульт) Возобновил спорт, меньше конечно чем раньше, но не мало для обыкновенного человека. 2 часа на ЧСС от 110уд/мин до 165уд/мин со средним 125 уд/мин это обыкновенное занятие без усталости. Хотел все же чтобы уменьшить дозу антикоагулянтов установить окклюдер в ушко левого предсердия, но в Мешалкина ответили что после установки окклюдера на ООО мне теперь нельзя, и нельзя делать если что вдруг сорвется РЧА. Это конечно меня расстроило, но будем надеятся на лучшее. Дозу апиксабана все же я уменьшил, т/к по ночам от обычной дозы в слюне кровь.
Открытый артериальный проток у детей
Открытый артериальный проток у детей (ОАП) является небольшим добавочным сосудом-шунтом, который соединяет просвет аорты и легочной артерии. Его присутствие у младенца расценивается как порок развития. В медицинской литературе можно встретить и другое название данной аномалии - «открытый Боталлов проток». В норме у новорожденного он закрывается через 15-20 часов после появления на свет и полностью зарастает за 2 недели. У недоношенных детей его закрытие иногда длится до 2 месяцев. ОАП может наблюдаться как самостоятельно, так и в комбинации с другими врожденными аномалиями - транспозицией магистральных артерий, стенозом устья аорты или ее коарктацией, дефектом перегородок между предсердиями, желудочками.

В большинстве случаев для устранения открытого артериального протока у детей проводится операция
Истинные причины того, почему артериальный проток не закрывается, ученые пока не смогли выяснить. Наблюдения показывают, что врожденная аномалия чаще развивается под волиянием следующих факторов:
- недоношенность или малый вес при рождении - менее 2500 г;
- присутствие других врожденных аномалий развития сердца, сосудов и других органов;
- гипоксия или асфиксия при родах;
- хромосомные аномалии;
- влияние на организм будущей матери неблагоприятных факторов: вирусные заболевания, злоупотребление алкоголем и наркотическими средствами, лечение тератогенными лекарствами, осложнения сахарного диабета и пр.;
- длительная оксигенация ребенка после рождения;
- продолжительный метаболический ацидоз;
- неоправданно избыточные внутривенные вливания.
По наблюдениям специалистов, в 2 раза чаще открытым артериальный проток остается именно у девочек, а его распространенность среди других врожденных пороков приближается к 9,8%.
Гемодинамика при ОАП сердца
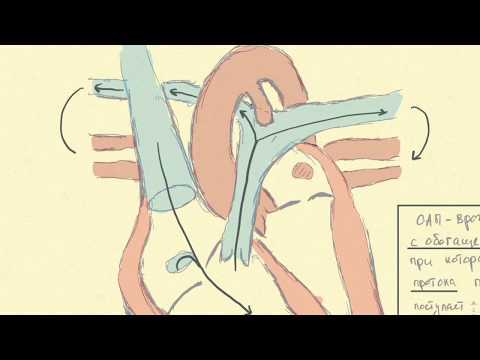
Понять, что такое ОАП, поможет знание процесса изменения гемодинамики на фоне порока. При незаращении добавочного сосуда после родов кровь в аорте из-за более высокого давления вливается через присутствующий шунт в просвет легочной артерии. Это приводит к переполнению правого желудочка. Нарушение распределения крови в камерах сердца провоцирует возрастание нагрузки на правые отделы возрастание давления в сосудах легких - легочную гипертензию.
До рождения малыша просвет добавочного протока и овальное окно являются необходимыми функциональными структурами, которые создают адекватное кровообращение в условиях отсутствия вентиляции воздуха через легкие и отключенности малого круга. Благодаря их наличию плод получает кислород, поступающий из сосудов матери.
Сразу после рождения и первого вдоха давление в просвете аорты возрастает, и этот процесс вызывает спазмирование гладкой мускулатуры и спадание Боталлового протока. Далее просвет добавочного сосуда зарастает соединительной тканью, что и приводит к полному закрытию ОАП.
Если заращение ОАП не наступает, то гемодинамика нарушается, у ребенка возникает легочная гипертензия. Степень ее выраженности определяется формой и размером этого шунта между аортой и легочной артерией, так как именно эти параметры определяют объем поступающей в правый желудочек крови. В некоторых случаях, при определенных сопутствующих сердечных аномалиях, ОАП, наоборот, способствует нормализации кровообращения.
При длинном и извитом добавочном шунте, который ответвляется от аортальной стенки под острым углом, серьезных изменений в кровообращении не происходит. Со временем может наблюдаться закрытие ОАП.
Классификация
В своем развитии ОАП проходит три стадии:
- первичной адаптации - присутствует до 2-3 лет, сопровождается появлением первых клинических признаков порока и иногда приводит к критическим состояниям. В сложных случаях эти опасные эпизоды могут становиться причиной смерти ребенка;
- относительной компенсации - наблюдается в более старшем возрасте и сохраняется вплоть до 20 лет, у ребенка выявляют симптомы недостаточности кровообращения в сосудах малого круга и повышенной нагрузки на правый желудочек;
- склерозирования - характеризуется выраженными изменениями легочных сосудов, в стенке которых откладывается соединительная ткань, что провоцирует легочную гипертензию.
В зависимости от показателей разницы артериального давления в малом и большом кругах кровообращения, специалисты выделяют 4 степени тяжести порока:
- I (легкая) - легочное не превышает 40% от системного;
- II (умеренная) - составляет 40-75%;
- III (выраженная) - достигает 75% и более;
- IV (тяжелая) - наблюдается выравнивание показателей или повышение системного АД.
Руководствуясь данными об изменении давления в легочной артерии, специалисты оценивают тяжесть врожденного порока. По анализу результатов они принимают решение о дате корректирующей операции по устранению ОАП и других сердечных аномалий, нуждающихся в устранении.
Симптомы
ОАП у детей может протекать как без явных симптомов, так и с признаками легочной гипертензии различной степени тяжести. В сложных случаях дебют порока возникает уже в первые сутки или месяцы жизни малыша. В дальнейшем примерно у 20% детей, уже при явной манифестации болезни, могут возникать опасные для жизни явления, вызванные сердечной недостаточностью.
Нарушения кровообращения при ОАП сопровождаются следующими проявлениями:
- снижение выносливости к физическим нагрузкам;
- периодическая синюшность при плаче, натуживании, крике и пр.;
- эпизодическая одышка;
- тахикардия;
- бледность;
- потливость;
- медленная прибавка веса.
При прогрессировании патологии к вышеописанным симптомам присоединяются другие:
- более продолжительный или постоянный цианоз;
- гипотрофия;
- кашель;
- сердечные аритмии;
- осиплость голоса;
- отставание в интеллектуальном развитии;
- склонность к частым воспалительным процессам бронхов и легких.
Признаки прогрессирования ОАП обычно возникают на фоне интенсивной физической активности или после начала подросткового периода и первых родов. Они указывают на возникновение недостаточности в работе сердца и показывают, чем опасен этот врожденный порок.
В редких случаях ОАП закрывается самостоятельно и состояние стабилизируется.
При физикальном обследовании ребенка с артериальным протоком обнаруживаются:
- сердечный горб;
- визуально заметная пульсация в области грудной клетки;
- грубый «машинный» шум во втором межреберье слева.
ОАП может приводить к следующим последствиям:
- бактериальный эндокардит;
- инфаркт миокарда;
- разрыв появившейся в стенках протока аневризмы.
Все вышеописанные осложнения способны стать причиной смерти ребенка. В среднем, при отсутствии адекватного лечения ОАП, больные живут не более 25 лет.

Только после диагностики можно сказать, чем опасен ОАП в конкретном случае
Диагностика
Для своевременного выявления открытого артериального протока у детей проводятся следующие исследования:
- ЭКГ;
- фонокардиография;
- Эхо-КГ с допплерографией.
Эти методики обследования позволяют обнаружить порок и частично оценивают степень его выраженности.
Для более детальной диагностики и выявления показаний к проведению того или иного метода хирургической коррекции, должны выполняться следующие исследования:
- МРТ и МСКТ сердца;
- аортография;
- зондирование камер правой половины сердца.
Их обычно назначают при значительной легочной гипертензии, когда есть показания к операции.
Полученные данные позволяют не только оценить степень тяжести ОАП, но и дифференцировать его от другой патологии, например, артериовенозного свища, недостаточности аортального клапана, аневризмы синуса Вальсальвы, дефекта аорто-легочной перегородки или общего артериального ствола.
Лечение
Особенно пристального внимания требует ведение ОАП у недоношенного ребенка!

У недоношенных детей операция по устранению ОАП может проводиться после стабилизации состояния
В тяжелых случаях или при неэффективности трех проведенных курсов консервативного лечения маленьким пациентам старше 3-х недель показана операция. Другим малышам вмешательство может проводиться после 1 года. Большинство специалистов считают, что оптимальным возрастом для кардиокоррекции является возраст до 3-х лет.
Для закрытия ОАП, в том числе у новорожденных, могут использоваться различные кардиологические операции, выполняющиеся открытым или внутрисосудистым доступом:
- катетерная эндоваскулярная эмболизация спиралями;
- клипирование добавочного протока при торакоскопии;
- перевязка патологического соустья;
- пересечение ОАП с ушиванием аортального и легочного конца.
Многие родители задают специалистам вопрос: «Чем опасно вмешательство по коррекции ОАП?» В большинстве случаев операции по ликвидации открытого артериального порока хорошо переносятся и сопровождаются низким риском осложнений.
Видео
* Представленная информация не может быть использована для самостоятельной постановки диагноза, определения лечения и не заменяет обращение к врачу!
Оптимизм - магнит счастья. Будьте позитивной, и в вашей жизни станет больше хороших вещей и приятных людей
Коарктация аорты у детей: причины порока сердца, симптомы и лечение
Коарктация аорты у детей может быть выражена в разной степени, но этот врожденный порок сердца, сопровождающийся сужением просвета сосуда, всегда является поводом для постоянного наблюдения у детского кардиолога. Уменьшение просвета наиболее крупной магистральной артерии обычно происходит в нисходящей части ее дуги, реже симптомы возникают в грудном и брюшном отделах. Экстренная операция выполняется при выраженном стенозе аорты, который способен приводить к развитию опасных для жизни малыша последствий.

Почему возникает и как развивается?
Точные причины коарктации аорты ученым пока неизвестны. Формирование данного порока начинается еще во время внутриутробного развития и провоцируется следующими факторами:
- перенесенные во время беременности бактериальные или вирусные инфекции;
- вредные привычки: алкоголизм, наркомания или никотиновая зависимость;
- негативное влияние экологической обстановки;
- работа на вредных предприятиях или контакт с токсическими веществами;
- синдром Шерешевского-Тернера;
- прием тератогенных лекарств.
На организм будущего ребенка может влиять как один из вышеперечисленных факторов, так и их комбинация.
По наблюдениям специалистов, коарктация в 4-5 раз чаще обнаруживается у мальчиков, а ее общая доля среди всех врожденных аномалий сердца достигает 7-15%. Порок в 80% случаев комбинируется со следующими аномалиями:
- открытый Боталлов проток;
- дефект межжелудочковой перегородки;
- двухстворчатый аортальный клапан (в норме у него три створки);
- сужение устья легочной артерии;
- стеноз отверстия аортального или митрального клапанов.
Присутствие сочетанных пороков усугубляет состояние ребенка коарктации и приводит к нарастанию симптомов коарктации.
Классификация и стадии развития
В зависимости от протяженности сужения сосуда, специалисты выделяют две разновидности коарктаций:
- инфантильные - сегмент стеноза наблюдается на значительном участке аортальных стенок и сопровождается открытым артериальным протоком;
- взрослые - стенозу подвергается небольшой участок аорты, но артериальный проток закрыт.
Выраженность стенозирования при этом пороке бывает различной, и от этого фактора зависит тяжесть течения коарктации. Сужение определяется по результатам визуализирующих и инвазивных диагностических методик, эти данные являются важным критерием для оценки целесообразности проведения кардиохирургического вмешательства.
Коарктация аорты у детей в своем прогрессировании проходит три этапа:
- стадия скрытой артериальной гипертензии. АД в сосудах верхней половины туловища повышается только после плача, кормления, переодевания или физической активности;
- стадия транзиторных нарушений. На ребрах малыша возникают узуры. Эти неровности становятся результатом возникающих извитости и расширения реберных артерий. При измерении АД выявляется артериальная гипертензия, которая наблюдается и после физических нагрузок, и в состоянии покоя;
- стадия склерозирования аорты. Из-за постоянного повышенного давления стенки артерии растягиваются, уплотняются и подвергаются разрастанию соединительной ткани. Процессы склерозирования сосуда приводят к прогрессированию нарушений кровообращения в камерах сердца и гипертрофии левого желудочка.
Стадия склерозирования плавно переходит в осложнения. Особенно высок риск у новорожденных. Стабильно прогрессирующие нарушения кровообращения приводят к ухудшению снабжения всех систем и органов.
Как и тетрада Фалло, коарктация может протекать скрыто или почти компенсироваться у новорожденных, но с возрастом она всегда приводит к тяжелым и опасным для жизни последствиям, поэтому всегда нуждается в современном и правильном лечении. Даже после проведения кардиохирургической коррекции, заключающейся в выполнении двух операций, стеноз аорты может рецидивировать в будущем. Дети с такой аномалией должны состоять на диспансерном учете всю жизнь для профилактики осложнений.

Операция при коарктации аорты проводится после детального обследования ребенка.
Характер и степень проявлений при коарктации аорты у детей определяется выраженностью стенозирования сосуда и присутствием другой патологии сердечно-сосудистой системы. При небольшом стенозе обогащенная кислородом кровь, выходящая из камеры левого желудочка, продолжает в достаточном объеме поступать в ткани и органы, поэтому проявления порока остаются скрытыми или малозаметными. У этих детей возникновение симптомов может происходить в более старшем или уже подростковом возрасте. Если же степень сужения магистральной артерии значительная, то проявления становятся заметными сразу же после рождения малыша или до годовалого возраста.
Родителей и специалистов, наблюдающих за маленьким ребенком, должны насторожить следующие проявления:
- беспокойство и капризность;
- бледность кожи;
- потливость;
- быстрая утомляемость при сосании соски или груди;
- появление одышки после переодевания, кормления, плача или других активных действий;
- носовые кровотечения;
- синюшность кожи на стопах;
- непропорциональность между развитием верхней и нижней частей туловища;
- замедленное физическое развитие;
- склонность к воспалительным заболеваниям верхних дыхательных путей.
После проведения врачебного осмотра могут выявляться следующие симптомы коарктации:
- ослабленная пульсация сосудов на ногах;
- прощупываемые на поверхности реберных костей неровности (узуры);
- разные показатели АД при измерении на руках и ногах;
- шумы при прослушивании сердца.
По мере взросления все вышеописанные признаки становятся более выраженными. В итоге, если лечение так и не было проведено, они могут быть причиной развития опасных осложнений, которые способны привести к летальному исходу.
Если симптомы коарктации аорты выражены в максимальной степени, то у ребенка развивается так называемый циркуляторный шок, который проявляется признаками почечной недостаточности и метаболического ацидоза, сопровождающихся нарастающей одышкой, цианозом и бледностью, тахикардией и приглушенность тонов сердца. Также у маленького пациента снижается АД и развивается брадиаритмия.
Если коарктация аорты при рождении была минимально выражена, то к более старшему возрасту или пубертатному периоду у ребенка появляются такие признаки:
- чувство слабости и снижение толерантности к нагрузкам;
- учащенное сердцебиение;
- боли и периодическое ощущение пульсации в голове;
- покраснение лица из-за приливов крови;
- звон в ушах;
- кардиалгии во время нагрузок;
- нарастающая при активности одышка;
- снижение слуха и зрения;
- боли в икроножных мышцах после ходьбы;
- носовые кровотечения;
- ухудшение способностей к запоминанию и решению интеллектуальных задач;
- долгое заживление ожогов или травм на ногах.
Все вышеописанные симптомы прогрессируют и нарастают по мере постоянного ухудшения кровоснабжения органов и систем, а отсутствие правильного лечения лишь усугубляет заболевание. Нарушенная внутрисчердечная гемодинамика при коартации аорты у детей может способствовать развитию септического эндокардита, который иногда осложняется тромбоэбмолиями и инфарктом органов.
При осмотре специалист выявляет:
- разные характеристики пульса и АД на нижних и верхних конечностях;
- пульсацию артерий на груди и животе - заметную визуально, усиливающуюся при наклоне туловища вперед или нагрузке ;
- усиленный сердечный толчок;
- шумы при прослушивании крупных сосудов в области между лопатками и на груди;
- расширение границ левого желудочка;
- при прослушивании сердца: определение так называемого «кошачьего мурлыканья» между II и III ребром, акцент второго тона над аортой, систолический шум во II-III (иногда IV) межреберье.
Выраженность вышеописанных изменений зависит от степени коарктации, наличия сочетанных аномалий сердца или магистральных сосудов.
К каким осложнениям приводит?
Коарктация аорты у детей при тяжелом течении и при отсутствии адекватной кардиохирургической коррекции может вызывать следующие опасные последствия:
- артериальная гипертензия;
- острые нарушения кровообращения (инсульты, инфаркты других органов);
- сердечная астма;
- отек легкого;
- бактериальный или септический эндокардит;
- эндомиокардит;
- эндоаортит;
- аневризмы на стенках самой аорты и ее ответвлений;
- тромбоэмболии;
- почечная недостаточность;
- кальцинирование стенок аорты;
- сердечная недостаточность.
Результатом всех вышеперечисленных осложнений может стать гибель ребенка.

У новорожденных результаты диагностики могут указывать на необходимость срочной операции
Для выявления коарктации аорты и других врожденных пороков у новорожденных клинические рекомендации предлагают провести следующие исследования:
- рентгенография органов грудной клетки;
- ЭХО-КГ;
- электро- и фонокардиография;
- магнитно-резонансная томография сердца;
- аортография с контрастом;
- зондирование сердца.
Анализ полученных данных позволяет формировать дальнейшую стратегию по наблюдению и лечению пациента. Результаты обследования у новорожденных могут указывать на необходимость срочного вмешательства хирургов - только такое лечение спасает малыша. Руководствуясь диагностической информацией, кардиохирурги могут выбирать тактику дальнейшей коррекции, необходимой для сохранения жизни ребенка.

Без проведения операции последствия коарктации аорты могут быть опасными для жизни
Коарктация аорты всегда нуждается в проведении кардиохирургической операции. Только иногда, при совсем незначительном сужении, ребенку могут рекомендовать диспансерное наблюдение.
Хирургическое лечение обычно проводится в два этапа, а дата первой паллиативной операции определяется тяжестью клинического случая - иногда она выполняется сразу после рождения малыша, а при возможности откладывается до достижения им 3-5 (иногда 10) лет. До выполнения кардиохирургической коррекции ребенку назначаются устраняющая или облегчающая симптомы терапия, соблюдение постельного режима с существенным ограничением любых физических нагрузок и диета, ограничивающая потребление жиров.
В качестве хирургического лечения до достижения трех лет ребенку обычно проводится одна из облегчающих состояние операций:
- легочная вальвулотомия;
- инфундибулярная резекция по Броку;
- легочно-подключичный шунт по Блейлоку;
- аорто-легочный шунт по Поттс-Смиту;
- аорто-легочное шунтирование с протезированием.
В послеоперационном периоде ребенку показано соблюдение режима, предписанного врачом. Для стабилизации состояния назначаются лекарственные средства.
Через 2-6 месяцев выполняется вторая, заключительная операция, цель которой - полное устранение существующего дефекта. Это вмешательство проводится в условиях искусственного кровообращения и с соблюдением принципов защиты миокарда от гипоксии. Операция начинается с охлаждения находящегося в аппарате перфузата до 21,6 °C. После этого выполняется пережатие аорты и вскрытие полости правого желудочка. Далее применяется одна из выбранных для кардиокоррекции стеноза методик. После завершения этого этапа дефект межжелудочковой перегородки закрывается заплатой, а при помощи другого лоскута увеличивают ширину выходного отверстия правого желудочка.
После второй операции ребенку назначается курс реабилитации, а в дальнейшем он должен соблюдать данные при выписке рекомендации. Диспансерное наблюдение таким детям показано до конца жизни. В тяжелых случаях комиссией врачей рассматривается возможность присвоения группы инвалидности.
Коарктация аорты является врожденной аномалией развития сердечно-сосудистой системы и сопровождается сужением отдельного сосудистого сегмента. Степень тяжести зависит от ряда факторов и определяется в ходе всесторонней кардиологической диагностики. После завершения обследования большинству детей проводится хирургическое лечение.

Читайте в следующей статье: потница у новорожденных
Читайте также:
