Менопаузальный индекс. Осложнения климакса - остеопороз, рак матки и молочных желез
Добавил пользователь Алексей Ф. Обновлено: 28.01.2026
В последние годы продолжительность жизни женщин стремительно увеличивается. В настоящее время средний возраст наступления менопаузы — 49± 0,5 лет, следовательно, примерно 1/3 своей жизни каждая женщина проводит в состоянии гипоэстрогении. В ряде случаев
В последние годы продолжительность жизни женщин стремительно увеличивается. В настоящее время средний возраст наступления менопаузы — 49± 0,5 лет, следовательно, примерно 1/3 своей жизни каждая женщина проводит в состоянии гипоэстрогении. В ряде случаев климактерий приобретает черты и признаки патологического процесса. Женщины, страдающие от патологических проявлений климактерия, обращаются за помощью к различным специалистам — невропатологу, кардиологу, эндокринологу, психиатру и др. В России только 1-2% женщин получают современную терапию. По статистическим данным, препараты из группы заместительной гормональной терапии (ЗГТ) применяют лишь 20 млн из 470 млн.
Как следует из таблицы 1, менее половины женщин в различных странах мира получают адекватную терапию. Крайне редко пациенткам с патологическим климактерием назначают индивидуальное комплексное лечение. Более 80% практикующих врачей плохо ориентируются в вопросах лечения патологического климактерия. В настоящее время в распоряжении врачей есть большой арсенал средств, позволяющих корригировать осложнения гипоэстрогенного состояния. Однако от правильного выбора тактики, времени начала, длительности терапии и ряда других факторов зависит состояние здоровья женщин. Учитывая все вышеизложенное, мы решили проанализировать показания и противопоказания к проведению патогенетической терапии препаратами группы ЗГТ и изложить принципы лечения патологических проявлений климактерия у женщин.
Проявления патологического климактерия у женщин, развивающиеся на фоне изменений гормонального статуса, носят полиморфный характер и относятся к различным областям практической медицины — терапии, кардиологии, урологии, неврологии, травматологии и др.
Гормональными маркерами, или критериями, климактерия являются:
- снижение уровня эстрадиола;
- высокий уровень ФСГ;
- индекс ЛГ/ФСГ < 1;
- индекс эстрадиол/эстрон < 1;
- относительная гиперандрогения;
- увеличение уровня ЛГ;
- увеличение соотношения андроген/эстроген ≤ 1;
- снижение уровня ингибина.
В течение длительного времени было принято считать, что основными органами-мишенями для половых гормонов являются матка и молочные железы, т. е. так называемые репродуктивные мишени. Однако благодаря успехам фундаментальной науки были выявлены новые типы рецепторов. Так, помимо репродуктивных органов-мишеней у человека имеются и нерепродуктивные.
Органы-мишени и локализация рецепторов к половым гормонам
- половые органы;
- гипоталамус;
- гипофиз;
- молочные железы.
- мозг;
- сердечно-сосудистая система;
- костно-мышечная система;
- уретра и мочевой пузырь;
- кожа и волосы;
- толстый кишечник;
- печень и др.
К числу наиболее значимых и оказывающих влияние на качество жизни женщины осложнений и проявлений гипоэстрогенного состояния относятся: климактерический синдром, урогенитальные изменения, дистрофические процессы в коже и ее придатках, атеросклероз и его осложнения, обменно-метаболические нарушения, остеопороз, болезнь Альцгеймера и др.
Время манифестации и степень выраженности основных симптомов и патологических состояний подвержены значительным индивидуальным колебаниям. Однако, несмотря на это, в последовательности их проявлений просматриваются определенные закономерности, представленные в таблице 2.
В настоящее время наиболее эффективным методом терапии климактерических расстройств является ЗГТ эстрогенсодержащими препаратами. Весь спектр лечебно-профилактических мероприятий можно разделить на два типа:
- немедикаментозное воздействие — диетотерапия, ЛФК, физиотерапия, рефлексотерапия, психотерапия, аутотренинг и фитотерапия;
- медикаментозная терапия — патогенетическая и симптоматическая.
Немедикаментозная профилактика и коррекция осложнений патологического климактерия у женщин
В профилактике и лечении осложнений климактерия важную роль играют правильное питание и изменение образа жизни:
- ночной сон не менее 8 ч;
- прогулки на свежем воздухе не менее 1-1,5 ч;
- комплекс общеукрепляющих упражнений и закаливание;
- отказ от вредных привычек — курения и употребления алкоголя.
Диетотерапия
Комплекс диетологических рекомендаций направлен на профилактику поздних обменно-метаболических нарушений, к которым относятся атеросклероз и его осложнения, остеопороз и ожирение. Диетологические рекомендации включают:
- соблюдение режима питания, дробное 5-6-разовое питание;
- последний прием пищи не позже 18 ч;
- дневной каллораж принимаемой пищи не > 2000-2200 ккал (однако при изменении уровня и интенсивности физической нагрузки данный показатель необходимо корректировать); ограничение потребления или полный отказ от легкоусвояемых углеводов;
- диета с низким содержанием жиров животного происхождения;
- употребление в пищу продуктов с высоким содержанием кальция (для женщин до 50 лет — 1000 мг/сут; для женщин в периоде постменопаузы — 1500 мг/сут; для женщин постменопаузального возраста, получающих ЗГТ эстрогенами, — 1000 мг/сут);
- ежедневный прием «естественных витаминов» и продуктов, богатых клетчаткой.
Психотерапия
С целью профилактики осложнений и лечения климактерия у женщин применяют психотерапию и обучение пациенток основам аутотренинга. Данные мероприятия помогают сформировать у женщин оптимистическое отношение к переходному периоду — климактерию и осознать обратимый характер большинства наблюдающихся у них явлений.
Физиотерапия
Помимо вышеперечисленного, следует отметить позитивные возможности физиотерапевтической коррекции многих осложнений климактерия у женщин. Арсенал современных физиотерапевтических средств достаточно широк. Наиболее часто применяемые физиотерапевтические средства, относящиеся к группе «естественных», можно разделить на следующие категории:
- климатотерапия — оптимальным является пребывание женщины в «своем» климатическом поясе;
- аэротерапия — лечение воздухом, наиболее доступна ходьба на свежем воздухе, при отсутствии противопоказаний возможно увеличение интенсивности нагрузки до бега. Также возможно проведение свето-воздушных ванн (оптимальная температура воздуха — не ниже 18°С и скорость ветра — не более 5 м/с);
- гелиотерапия, или инсоляция, — перед назначением данного вида терапии необходимо исключить следующие патологии: заболевания сердечно-сосудистой системы, тиреотоксикоз, объемные новообразования и др. Целесообразно начинать с пребывания на солнце в течение 5-7 мин и доводить продолжительность процедур до 45 мин — в утреннее время, до 10 или после 17 ч.
Ко второй группе физиотерапевтических мероприятий относятся физические и химические воздействия. Более подробно хотелось бы остановиться лишь на некоторых из них.
- При преобладании вегетативной симптоматики при патологическом развитии климактерия у женщин рекомендуется:
- ручной массаж;
- электрофорез эуфиллина на область «воротника»;
- гальванизация шейно-лицевой зоны и др.
- При преобладании жалоб психоэмоционального характера целесообразны следующие мероприятия:
- эндоназальная гальванизация;
- циркулярный душ;
- электросон и др.
- При склонности к артериальной гипертензии показаны следующие процедуры:
- электросон;
- гальванизация или электрофорез брома;
- гальванический анодный воротник или электрофорез магния;
- электрофорез с β-адреноблокирующими препаратами и др.
Лечебная физкультура
Немаловажную роль играет применение комплексов или отдельных упражнений, которые можно использовать во все периоды климактерия и сениума:
- ходьба, особенно в сочетании с аэротерапией;
- бег (при отсутствии противопоказаний);
- комплекс дыхательных упражнений;
- упражнения, направленные на расслабление, как общее, так и отдельных мышц;
- комплекс тренировки мышц малого таза и детрузора;
- упражнения, направленные на укрепление мышечного корсета и профилактику остеопороза и др.
Медикаментозная коррекция и профилактика патологических проявлений патологического климактерия у женщин
Принимая во внимание патогенетические особенности и механизмы развития основных осложнений климактерия, т. е. гипоэстрогении, у женщин медикаментозную терапию можно разделить на патогенетическую и симптоматическую. К первой категории относится заместительная гормональная терапия. В настоящее время на Российском рынке имеется обширный набор препаратов данной группы, различающихся по способу введения, основному действующему веществу, дозировке, химической структуре и другим параметрам.
Для ЗГТ используют различные препараты эстрогенов, в состав которых входят натуральные или синтетические эстрогены. Для терапии проявлений климактерия, как правило, применяются натуральные эстрогены и их агонисты. В таблице 3 представлены некоторые типы эстрогенов, применяемых для ЗГТ.
Основной целью применения ЗГТ является замена при помощи фармакологических средств гормональной функции яичников у женщин, испытывающих дефицит половых гормонов. Важно достичь таких уровней гормонов в крови, при которых обеспечивались бы улучшение настоящего состояния, профилактика поздних обменно-метаболических нарушений, и при этом отрицательное воздействие на органы-мишени — эндометрий и молочные железы — было бы наименьшим.
Показаниями для начала проведения ЗГТ у женщин являются ранняя манифестация менопаузы (до 40 лет), отягощенный анамнез (особенно по сердечно-сосудистым патологиям, остеопорозу, болезни Альцгеймера), первичный или вторичный гипогонадизм у женщин, состояние после овариоэктомии, урогенитальные расстройства, ранние вазомоторные симптомы климактерического синдрома, мигрень, ожирение и др.
Абсолютные и относительные противопоказания для назначения препаратов ЗГТ
Абсолютные противопоказания для ЗГТ: беременность, кровотечения из половых путей неясной этиологии, острый гепатит, острый тромбоз глубоких вен, острые тромбоэмболические заболевания, некоторые опухоли половых органов и молочных желез, менингиома.
Относительные противопоказания к ЗГТ: миома матки, эндометриоз, мигрень, венозный тромбоз или эмболия в анамнезе, семейная гипертриглицеридемия, желчнокаменная болезнь, эпилепсия, отягощенный семейный анамнез по раку молочных желез, рак яичников.
Противопоказания для использования эстрогенов: рак молочной железы в анамнезе, рак эндометрия, патологии, сопровождающиеся дисфункцией печени, порфирия, эстрогензависимые опухоли, декомпенсация сахарного диабета.
Перед назначением препаратов ЗГТ пациентке должен быть проведен тщательный мониторинг состояния. К обязательным обследованиям относятся:
- контроль уровня АД;
- определение уровней — гликемии, липопротеидов, ФСГ, Е2 в сыворотке крови, ТТГ, Т3 и Т4, показателей свертывающей системы крови;
- гинекологический осмотр;
- УЗИ репродуктивных органов малого таза с определением толщины эндометрия;
- пальпация молочных желез и мамографическое исследование.
В ряде случае также необходимо провести:
- ЭКГ-исследование;
- консультацию эндокринолога, невропатолога, кардиолога, флеболога и др.
В настоящее время на отечественном фармацевтическом рынке представлены различные по составу, пути введения и дозе действующего вещества препараты, применяемые для ЗГТ. На рисунке представлены основные пути введения препаратов, используемых для ЗГТ.
Принимая во внимание физиологические особенности женского организма, применять препараты группы ЗГТ в различные периоды климактерия следует по-разному; так, при решении вопроса о выборе типа препарата и режима терапии необходимо определить состояние матки (при ее отсутствии важно выяснить причины проведения гистерэктомии) и фазу климактерия. В периоды пре- и ранней менопаузы препараты данной группы восстанавливают менструальный цикл, что помимо всего прочего благоприятно влияет на состояние женщины; наиболее физиологичным считается использование трехфазных препаратов. В периоды «позднего климактерия», в отличие от пременопаузы, когда оправдана стимуляция секреторной гормональной функции яичников, основополагающим должно быть условие сохранение возрастного гомеостаза.
Следует также определить доминирующие проявления патологического климактерия — вегетативные, кардиальные, урогенитальные или др.
В настоящее время существуют следующие основные режимы применения ЗГТ:
- монотерапия эстрогенами (прогинова, дивигель, овестин, эстрофем, премарин, климара и др.) или прогестагенами (дюфастон, МПА и др.);
- комбинированная терапия (эстрогены и прогестогены) в циклическом режиме (дивина, климен, климонорм, трисеквенс, климодиен и др.);
- монофазная комбинированная терапия (эстрогены и прогестогены) в непрерывном режиме (клиогест и др.);
- применение других препаратов (ливиал, гинодиан-депо и др.).
В настоящее время в нашей стране все более активно используются препараты для трансдермального введения активного вещества, ЗГТ. В практике существуют два способа парентерального применения эстрогенсодержащих препаратов через неповрежденную кожу: нанесение гипоалкогольного геля либо использование трансдермального пластыря или наклейки с контролируемым высвобождением эстрадиола. Однако трансдермальные формы — это монокомпонентные лекарственные препараты. При применении данных препаратов у женщин с интактной маткой необходимо применение прогестогенов. В настоящее время и ученые, и клиницисты пришли к выводу, что продолжительность применения ЗГТ должна составлять в среднем 5-7 лет, так как это оптимальный срок не только и не столько для достижения положительного результата (купирования уже имеющих место патологических проявлений климактерия) терапии, но и для профилактики более серьезных осложнений патологического климактерия.
При использовании препаратов ЗГТ необходимо обязательно контролировать уровни эстрадиола и ФСГ через 3 мес, а в дальнейшем — каждые 6 мес; УЗИ органов малого таза и мамографическое исследование следует проводить ежегодно; анализ показателей свертывающей системы производится каждые 6 мес и др.
Суммарный положительный эффект от применения ЗГТ: уменьшение вегетативно-эмоциональных проявлений климактерия (отмечается у 90-95% пациенток), снижение патологических урогенитальных проявлений (у 85% женщин), снижение риска переломов шейки бедра на 50% и позвонков на 60-70%, снижение частоты инфаркта миокарда (у 35-50% пациенток), снижение частоты случаев болезни Альцгеймера на 30-60%.
Учитывая несомненные достоинства терапии ЗГТ, необходимо также иметь в виду ее отрицательные стороны. К достоинствам ЗГТ относятся: патогенетически обусловленное воздействие, быстрый регресс симптоматики, удобство в использовании, лечебное и профилактическое действие, комплексное межсистемное воздействие. Среди недостатков ЗГТ: большой список противопоказаний, комплексное межсистемное воздействие, необходимость постепенного снижения дозы эстрогенного компонента препарата при отмене приема, высокая цена, негативный настрой к применению ЗГТ у врачей и пациенток.
В связи с этим закономерно встает вопрос о необходимости применения альтернативных методов коррекции осложнений патологического климактерия.
Препараты для симптоматической терапии можно рассматривать как средства альтернативной терапии патологических проявлений климактерия. В первую очередь к ним следует отнести фитоэстрогены. Это природные вещества, входящие в состав растений и обладающие эстрогенным или антиэстрогенным действием. В настоящее время выделяют три основных класса фитоэстрогенов:
- изофлавины (генистеин, дайдзеин);
- лигнаны (энтеролактон, энтеродиол);
- куместаны (куместралы).
Данные вещества входят в состав ряда фармакологических препаратов, в том числе гомеопатических.
Учитывая основную симптоматику, по направленности воздействия препараты можно разделить на следующие группы:
- препараты для коррекции основных проявлений климактерического синдрома — гомеопатические препараты климакт-хель, климактоплан, ременс и др.;
- седативные препараты — ново-пассит, белласпон, грандоксин и др.;
- гипотензивные средства — конкор, небилет, моэксиприл и др.;
- гиполипидемические препараты — зокор и др.;
- препараты урологической направленности действия — дриптан и др.;
- лекарственные средства для коррекции костно-метаболических нарушений — миакальцик, фосомакс, альфа Д3-Тева;
- общеукрепляющие средства и препараты для проведения витаминотерапии и др.
Подводя итоги, следует еще раз подчеркнуть, что больные с патологическими проявлениями климактерия могут обращаться с жалобами к самым различным специалистам — кардиологу, невропатологу, эндокринологу и др. Поэтому врачи всех специальностей должны хорошо знать клинику и современные методы коррекции проявлений патологического климактерия у женщин. Это, несомненно, будет способствовать повышению качества жизни женщины, а также снизит частоту заболеваемости и смертности от таких социально-значимых патологий, как инфаркт миокарда, болезнь Альцгеймера, остеопороз и др.
Е. В. Доскина, кандидат медицинских наук
РМАПО, Москва
Рак эндометрия (рак тела матки) - симптомы и лечение
Что такое рак эндометрия (рак тела матки)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Ильина Антона Алексеевича, онколога-гинеколога со стажем в 13 лет.
Над статьей доктора Ильина Антона Алексеевича работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Маргарита Тихонова
Определение болезни. Причины заболевания
Рак эндометрия (endometrial cancer) — это злокачественная опухоль, которая развивается из клеток внутреннего слоя матки. Основным симптомом, который появляется уже на начальной стадии болезни, являются кровянистые выделения из половых путей.
Рак эндометрия ещё называют раком тела матки и аденокарциномой эндометрия.
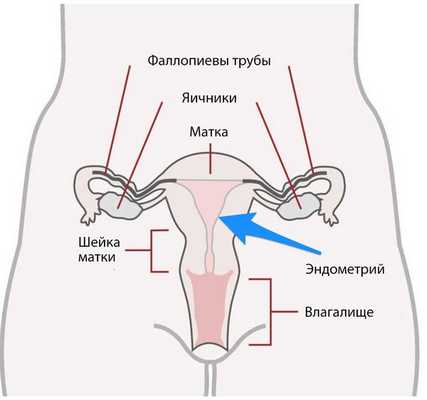
Распространённость
Рак эндометрия — это самая частая злокачественная опухоль женских половых органов. Но если болезнь выявлена своевременно и проведено адекватное лечение, большинство пациенток выздоравливает [1] .
В основном раком эндометрия заболевают женщины в постменопаузе: более 90 % случаев диагностируются после 50 лет. Чаще всего болезнь встречается среди пациенток в возрасте 65-69 лет — заболеваемость среди них составляет 98,1 на 100 тыс. женщин. Средний возраст на момент начала болезни — 63 года. До 49 лет рак эндометрия встречается относительно редко: в 4-5 % от всех случаев [11] .
Факторы риска
Около 5 % случаев рака эндометрия имеют наследственный характер. Злокачественная опухоль эндометрия может развиться при наследственном неполипозном колоректальном раке (синдроме Линча) [12] . Болезнь возникает из-за поломки генов MLH1, MSH2, MSH6 или PMS2. При таких мутациях риск развития рака эндометрия и колоректального рака составляет 24-51 %, рака яичников — 11-15 % [13] .
Помимо генетической предрасположенности, на заболеваемость влияют следующие факторы:
- лишний вес (риск развития рака эндометрия повышается в 1,32 раза); (в 2,54 раза); (в 2,1 раза);
- раннее начало и позднее прекращение менструаций: до 10-12 и после 55 лет (в 2,1 раза); (в 2,9 раза);
- приём Тамоксифена — гормонального препарата для лечения рака молочной железы (в 2,5 раза);
- монотерапия эстрогенами более пяти лет (в 10-30 раз); ;
- лучевая терапия на органы малого таза.
Ожирение является одним из основных факторов риска. Жировая ткань преобразует в эстрогены другие гормоны — андрогены. Если уровень эстрогенов значительно повышен, то риск развития опухолей эндометрия также увеличивается. Получается, чем больше жировой ткани, тем выше вероятность заболеть раком эндометрия.
Тамоксифен — это препарат, который используется при лечении рака груди. В ткани молочной железы он действует как антиэстроген, но в матке механизм действия иной, аналогичный гормону эстрогену. При лечении Тамоксифеном рекомендуется ежегодно наблюдаться у гинеколога.
При синдроме поликистозных яичников значительно повышается уровень андрогенов и эстрогена, а также снижается уровень прогестерона. Изменение соотношения эстрогена и прогестерона является одной из основных причин развития рака эндометрия.
Предшествующая лучевая терапия. Радиация используется для лечения некоторых типов опухолей. При облучении сложно, а иногда невозможно не затронуть смежные органы. Радиация повреждает ДНК здоровых тканей и может приводить к развитию рака в прежде здоровых органах.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы рака эндометрия
Эффективных программ скрининга рака эндометрия пока не существует. Единственный способ обнаружить заболевание на ранней стадии — это ежегодно посещать гинеколога. Также к доктору нужно обратиться, если болит низ живота или появились кровянистые выделения из половых путей между менструациями или в постменопаузе. Кровянистые выделения при раке эндометрия встречаются у 90 % пациенток. Чаще всего выделения слабые или умеренные, их характер зависит от распространения опухоли.
Признаком злокачественной опухоли также может быть изменение характера выделений, даже без примеси крови [2] . Боль, потеря веса и тяжесть в животе появляются уже на поздних стадиях болезни.
Патогенез рака эндометрия
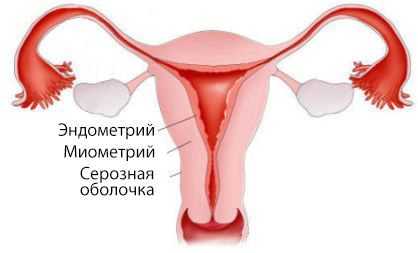
Матка состоит из двух частей: тела и шейки. В теле матки выделяют три слоя:
- наружный — серозная оболочка;
- средний — миометрий, или мышечный слой;
- внутренний — эндометрий, который частично отторгается вместе с кровью при каждой менструации.
Аденокарцинома развивается непосредственно из эндометрия.
В 1963 году была предложена и обоснована теория о двух основных типах аденокарциномы матки. Первый вариант наблюдается у 60-70 % пациенток и протекает с нарушениями углеводного и жирового обмена на фоне избыточного количества эстрогенов [14] [15] . Женщины с этим типом рака страдают маточными кровотечениями, бесплодием, ожирением и сахарным диабетом. У них поздно наступает менопауза и развиваются гиперпластические процессы в эндометрии (качественно-количественное изменение его клеток).
Второй патогенетический вариант болезни встречается у 30-40 % пациенток. У них описанные выше нарушения выражены слабо или отсутствуют [14] [15] . Изменения в эндометрии носят атрофичный характер, развиваются полипы, атипическая гиперплазия и рак.
Отнести заболевание к первому типу можно в следующих случаях:
- присутствует более половины перечисленных признаков;
- симптомы гиперэстрогении (болезненные менструации и маточные кровотечения вне их) сочетаются с обменными нарушениями, например с ожирением и сахарным диабетом.
Согласно другому разделению, к первому типу рака эндометрия относят эндометриоидный рак, ко второму — неэндометриоидный (серозный или светлоклеточный). Они встречаются в 80-90 % и 10-20 % случаев соответственно [3] . Такое разделение связано с различиями в молекулярном профиле опухолей, методах лечения и прогнозе.
Чаще всего раковые опухоли образуются из-за повреждения гена-супрессора PTEN, который подавляет развитие и рост раковых клеток. Данная аномалия встречается у 83 % пациенток с раком эндометрия [4] .
Болезнь также может развиваться при поломке в системе репарации (т. е. исправления) ошибок спаривания нуклеотидов. Эта система отвечает за важный этап нормального деления здоровых клеток. Рак эндометрия первого типа, как правило, связан с мутациями в генах KRAS и CTNNB. Второй тип часто протекает на фоне хромосомной нестабильности, генетических расстройств и мутации в гене р53.
Классификация и стадии развития рака эндометрия
В онкологии существуют две системы TNM, т. е. стадирования рака — FIGO (International Federation of Gynecology and Obstetrics) и AJCC (American Joint Committee on Cancer). Обе системы используют следующие ключевые параметры для описания рака и установки стадии:
- размер опухоли (Tumor);
- наличие или отсутствие опухоли в лимфатических узлах (Node);
- наличие или отсутствие метастазов опухоли (Metastasis) [5] .
Исходя из этих признаков, выделяют четыре основные стадии. Чем меньше стадия, тем лучше прогноз. Рак обычно стадируется дважды. Первый раз — до лечения, такое стадирование называется клиническим. Второй раз — после операции, такое стадирование называется патологоанатомическим и считается более точным и окончательным. Со временем опухоль может расти или распространяться на органы, в которых её раньше не было, а также повторно развиваться после полного излечения. В этом случае стадия, установленная однажды, меняться не будет.
Стадии рака эндометрия по системе TNM
Более схематично стадии рака эндометрия отражены на рисунке:
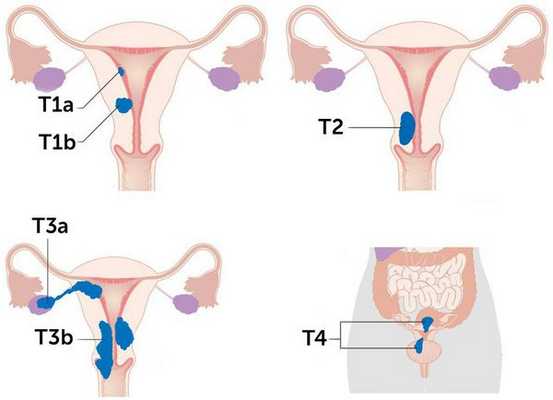
Согласно международной гистологической классификации рака тела матки, выделяют несколько видов опухолей:
- Злокачественные эпителиальные опухоли. В эту группу входят различные виды рака, среди которых эндометриальная аденокарцинома, серозный и светлоклеточный рак.
- Злокачественные смешанные эпителиальные и мезенхимальные опухоли — аденосаркома и карциносаркома.
- Мезенхимальные опухоли — леймиосаркома, эпителиоидная и миксоидная леймиосаркома, эндометриальная стромальная саркома низкой и высокой степени злокачественности.
Лучший прогноз имеет эндометриоидная форма, худший — серозная и светлоклеточная, но основным прогностическим критерием является стадия заболевания. Например, выживаемость с IV стадией эндометриоидного рака ниже, чем с I стадией светлоклеточного.
Рак тела матки также классифицируется на основании вида клеток, из которых он развился. Чтобы установить разновидность рака и его дифференцировку, исследуются удалённые органы или их части. Тип опухоли устанавливает эксперт-патолог, работающий с тканями под микроскопом.
Дифференцировка — это схожесть раковой клетки со здоровой. Она отражает, насколько быстро опухоль может расти и распространяться. Описаны три степени дифференцировки: G1, G2, G3, где G3 — самая неблагоприятная с быстрым ростом опухоли. Сейчас чаще выделяют только два класса: низкой злокачественности (low grade) и высокой (high grade). Low grade включает G1 и G2, a high grade — G3.
Осложнения рака эндометрия
Без специализированного лечения рак эндометрия неизбежно прогрессирует: боль и кровотечение из половых путей усиливаются, мочевой пузырь и прямая кишка сдавливаются, их функции нарушаются. У пациенток учащается мочеиспускание и стул либо, наоборот, возникают запоры.
Если опухоль проросла в мочевой пузырь и кишку, в моче и кале может появиться кровь. Очаги опухоли могут также образоваться в других органах и тканях: печени, лёгких и брюшной полости. При метастазах в лёгких появляется кашель, боль в грудной клетке и одышка; метастазы в печени проявляются болью в правом подреберье [6] .
Диагностика рака эндометрия
В отличие от рака шейки матки для рака эндометрия не существует программ скрининга. Диагноз устанавливается после комплексного обследования, которое включает:
- осмотр на гинекологическом кресле;
- подтверждение наличия опухолевых клеток;
- магнитно-резонансную томографию (МРТ) с контрастированием;
- ультразвуковое исследование (УЗИ);
- компьютерную томографию (КТ).
Осмотр на гинекологическом кресле позволяет оценить, где расположена и насколько распространилась опухоль, а также выявить, поражены ли смежные органы малого таза.
Подтверждение наличия опухолевых клеток, или верификация, — это необходимый компонент обследования. Получить клетки можно двумя способами:
- Пайпель-биопсия — процедура, при которой эндометрий забирается из полости матки с помощью тонкого зонда. Не требует общего наркоза и специальных условий.
- Гистерорезектоскопия — операция, при которой перед забором эндометрия врач может осмотреть полость матки. Гистероскопия предпочтительна при безоперационном лечении, проводится под наркозом и редко занимает более 15 минут. Точность гистероскопии выше, чем пайпель-биопсии, и составляет около 72 % [7] .
Ультразвуковое исследование может быть выполнено через брюшную стенку и интравагинально, т. е. через влагалище. Интравагинальное УЗИ позволяет лучше оценить состояние эндометрия, аномальное утолщение которого может косвенно указывать на онкологическое заболевание. Данная процедура является относительно простой и не требует специальной подготовки, поэтому часто назначается пациенткам на первом этапе диагностики. Правильно интерпретировать результаты УЗИ может только врач-онкогинеколог.
Магнитно-резонансная томография с контрастированием является более точным методом диагностики по сравнению с УЗИ. МРТ назначается при планировании лечения и позволяет определиться с объёмом операции.
Компьютерную томографию (КТ) с контрастированием применяют, чтобы определить, есть ли метастазы в органах грудной клетки и брюшной полости.
Специфических онкомаркеров для диагностики рака эндометрия не существует. Один из немногих маркеров с относительной чувствительностью — Са-125, но такой анализ не входит в стандартное обследование. Этот онкомаркер выявляется при лимфоме, раке яичников, поджелудочной и молочной железы. Также его уровень может повышаться при беременности, различных воспалительных заболеваниях или доброкачественных образованиях, например кистах яичников и миоме матки.
Лечение рака эндометрия
Основной метод лечения рака эндометрия — это операция, при которой удаляются тело и шейка матки с придатками.
Операция может проводиться через три вида доступа:
- лапаротомный (разрез передней брюшной стенки);
- лапароскопический (через проколы 5-10 мм);
- влагалищный.
Чаще всего применяется лапароскопия, так как после неё пациентки быстрее всего восстанавливаются.
Необходимость лимфодиссекции (удаления лимфатических узлов) зависит от наличия факторов риска метастазирования опухоли, результатов морфологического заключения и данных инструментальной диагностики. При удалении лимфатических узлов важно оценить, есть ли в них опухолевые клетки, что имеет решающее значение при планировании лечения после операции.
Чем больше объём операции, тем выше риски послеоперационных осложнений. При удалении лимфоузлов примерно в половине случаев образуются лимфокисты — отграниченные скопления лимфатической жидкости в малом тазу [8] . Чтобы минимизировать риски их развития и избежать лимфодиссекции, в некоторых клиниках используется технология определения сигнальных лимфоузлов (СЛУ). Во время процедуры в шейку матки вводится краситель, который по лимфатическим сосудам попадает в лимфоузлы. Затем хирург находит лимфоузлы, в которых накопился краситель, и удаляет узел, расположенный ближе всего к матке. Далее, непосредственно во время операции, проводится гистологическое исследование, позволяющее подтвердить или исключить наличие метастазов в СЛУ и избежать их полного удаления.
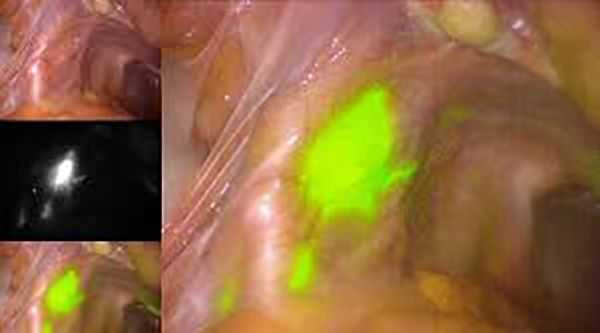
Если женщина планирует беременность, то в некоторых случаях допустимо безоперационное лечение. Оно возможно при эндометриоидном типе рака, стадии IA и высокой дифференцировке. Лечение проводится гормональными препаратами, которые блокируют работу яичников и оказывают терапевтический эффект на опухоль. Применяются два основных препарата: Мегестрола ацетат и Медроксипрогестерон.
Продолжительность гормонального лечения, как правило, составляет 6-12 месяцев. Затем при хорошем эффекте врач может разрешить беременность. После родов зачастую рекомендуется удалить матку, так как опухоль часто развивается повторно.
Лучевая терапия или химиотерапия на первом этапе менее эффективны, чем хирургическое лечение. Они назначаются, если нельзя провести операцию, например при тяжёлых хронических заболеваниях, распространённости опухоли и лечении рецидивов.
Чтобы предотвратить повторное появление опухоли, после операции могут проводиться дистанционное облучение малого таза и брахитерапия (контактная лучевая терапия, при которой источник излучения вводится внутрь поражённого органа).
Метод подбирается врачом в зависимости от типа и стадии рака, состояния лимфатических узлов. Например, при неэндометриоидном раке после операции назначается химиотерапия в сочетании с брахитерапией, а при эндометриальном раке I стадии может быть достаточно брахитерапии или наблюдения.
Прогноз. Профилактика
Без лечения рак эндометрия неизбежно прогрессирует и со временем приводит к гибели пациентки.
Для оценки прогнозов в онкологии используется термин «пятилетняя выживаемость», который сравнивает пациентов с конкретной стадией болезни с людьми из общей популяции. Например, если пятилетняя выживаемость при первой стадии болезни достигает 95 %, то такие пациенты по сравнению со здоровыми людьми с вероятностью 95 % проживут пять лет.
При своевременном выявлении и лечении рак эндометрия имеет самые благоприятные прогнозы среди всех злокачественных опухолей женских половых органов:
- для I стадии пятилетняя выживаемость составляет 85-95 %;
- для II — 65-70 %;
- для III — 29 % [9] .
Стадия болезни является самым значимым фактором при определении прогноза, но далеко не единственным. Онкологи оценивают гистологический тип опухоли, её дифференцировку, размеры, расположение в матке, прорастание или метастазирование в другие органы и лимфатические узлы. Точный прогноз врач сможет дать только после всестороннего анализа этих параметров.
Современный подход к лечению женщин с патологическим климактерием
«Медицинский совет»; Урология и гинекология; №3-4; 2010; стр. 15-20.
М.А.Геворкян, д.м.н., профессор, И.Б.Манухин, д.м.н., профессор, К.З.Фаталиева, Е.И. Манухина, к.м.н., МГМСУ, Москва
В течение многих лет внимание не только гинекологов, но и урологов, кардиологов и врачей других специальностей привлекает проблема качества жизни у женщин в возрасте климактерия [1—3]. Это связано с системными осложнениями дефицита эстрогенов, происходящего в результате постепенного прекращения гормональной функции яичников, проявляющимися симптомами климактерического синдрома, урогенитальными расстройствами и остеопорозом.
Рецепторы к эстрадиолу выявлены практически во всех органах и тканях женского организма. Биологические эффекты эстрогенов в ЦНС играют важную роль в ментальных и когнитивных функциях, определяющих качество жизни женщины, ее трудоспособность. Период пре- и постменопаузы занимает практически треть жизни социально-активного возраста женщины. В связи с этим, течение климактерия (климактерический синдром, урогенитальные нарушения, остеопороз) резко ухудшают состояние здоровья и качество жизни. Следует отметить, что средняя продолжительность жизни женщин увеличилась, в частности в Европе она составляет 80 лет.
Для определения того или иного периода климактерия используют различные термины, что обусловлено возрастными изменениями функции яичников. Мы считаем, что целесообразно пользоваться классификацией, предложенной Международным обществом по менопаузе (рис. 1).
Рисунок 1. Периоды климактерия
Менопауза (естественная) — это последнее менструальное кровотечение, обусловленное гормональной функцией яичников. Возраст менопаузы оценивается ретроспективно через 12 месяцев аменореи и соответствует примерно 50—51 годам жизни женщины.
Хирургическая менопауза — это выключение менструальной функции, произошедшее в результате оперативного вмешательства: гистерэктомия с придатками или без придатков, овариоэктомия (аднексэктомия) без гистерэктомии. Последний вид хирургического вмешательства проводится крайне редко у женщин, которые впоследствии могут реализовать генеративную функцию в программе вспомогательных репродуктивных технологий.
Менопаузальный переход, или больше принятый в России термин пременопауза, — это вариабельный по длительности период, предшествующий менопаузе и характеризующийся нарушением менструального цикла. Международное общество по менопаузе рекомендует пользоваться термином «менопаузальный переход», поскольку многие зарубежные исследователи подразумевают под пременопаузой период жизни женщины от первой до последней менструации.
Вегетативно-сосудистые, нервно-психические и обменно-трофические симптомы возникают у 70—80% женщин в период снижения гормональной функции яичников и чаще проявляются в перименопаузе из-за дефицита эстрогенов.
Перименопауза — это период, характеризующийся эндокринологическими и клиническими проявлениями дефицита эстрогенов. Ее длительность составляет примерно 1,5—2 года до и после менопаузы (последней менструации).
Через 1,5—2 года после последней менструации начинается постменопауза, которая продолжается в течение всей дальнейшей жизни.
Климактерий включает все вышеперечисленные периоды жизни женщины и характеризуется постепенным снижением и полным выключением генеративной, менструальной и гормональной функции яичников. Он является длительным периодом перехода от репродукции к старости.
Для климактерического синдрома (КС) характерны вегетативно-сосудистые, нервно-психические и обменно-трофические симптомы, которые возникают у 70—80% женщин на фоне снижения гормональной функции яичников и чаще проявляются в перименопаузе из-за дефицита эстрогенов. Частота, характер и тяжесть климактерических нарушений во многом зависит от внешних факторов (режима труда и отдыха, питания, вредных привычек и др.), сопутствующих экстрагенитальных заболеваний, отягощающих течение КС. При оценке тяжести течения КС используют модифицированный менопаузальный индекс (ММИ): по сумме баллов выделяют 3 степени: 12—34 баллов, 35—58 баллов, более 58 баллов. По количеству приливов в сутки 3 степени: легкая до 10 приливов в сутки, средняя — 10—20 приливов и тяжелая — более 20 приливов. При этом необходимо учитывать наличие приливов в ночное время, нарушение трудоспособности, превалирование нейропсихических симптомов.
Примерно у 40% пациенток с экстрагенитальными заболеваниями отмечаются осложненные формы КС.
Наибольшая частота урогенитальных нарушений и остеопороза, положительно коррелирующая с длительностью постменопаузы, отмечается в постменопаузе. Однако в ходе последних исследований показано, что урогенитальная атрофия наблюдается уже в перименопаузе, на что необходимо обращать внимание практикующим врачам. Это важно в аспекте времени начала терапии, поскольку длительно существующие урогенитальные нарушения трудно поддаются лечению даже препаратами эстрогенов в результате инволютивных процессов рецепторного аппарата.
К сожалению, даже в настоящее время практикующие врачи продолжают лечить атрофический постменопаузальный кольпит антибиотиками, руководствуясь принципами терапии урогенитальной инфекции. Но данная терапия не является патогенетической, поскольку она не устраняет причину — дефицит эстрогенов.
Для лечения климактерических нарушений с 40-х годов XX в. успешно применяют гормональные препараты, содержащие аналоги натуральных половых стероидов [4]. К сожалению, не только пациентки, но и многие практикующие врачи испытывают страх перед гормонотерапией [5]. Женщины считают, что при проведении гормонотерапии прибавят в весе. Но результаты многочисленных исследований свидетельствуют об обратном (обзор Cochrane по результатам 22 исследований). Показано, что своевременно начатая ЗГТ оказывает профилактическое действие на перераспределение жировой ткани и формирование висцерального ожирения. На консенсусе российских кардиологов и гинекологов было отмечено, что с помощью ЗГТ поддаются профилактике или коррекции метаболические нарушения в пери— и ранней постменопаузе, которые только формируются или продолжительность и глубина которых еще не велики [6].
В последние годы, после представления результатов эпидемиологических рандомизированных исследований (РЕРI, HERS, WHI, MWS и др.: влияние ЗГТ на заболевания сердца и сосудов, на риск рака молочной железы), многочисленные экспертные советы Международных ассоциаций по менопаузе были посвящены критическому анализу этих работ. В результате, на Международном конгрессе по менопаузе (Мадрид, 2008) были выдвинуты следующие основные положения, которые рекомендовано соблюдать практикующим врачам при назначении ЗГТ [7, 8]:
Перед назначением гормонотерапии очень важно грамотно проконсультировать пациентку. В России, по данным проведенного опроса (Горячая линия, 2007 г.), 60% женщин получают информацию о ЗГТ из СМИ, тогда как в Европе тот же процент женщин — от врачей. Как можно определить приемлемость проведения гормонотерапии? В первую очередь по использованию гормональных препаратов врачами гинекологами. По предварительным данным Сметник В.П., среди гинекологов России гормональную контрацепцию используют примерно 30— 60%, а ЗГТ — 10—30%. Таким образом, очевидно, что именно этот небольшой процент практикующих врачей рекомендуют ЗГТ для лечения КС. Врач должен информировать женщину о том, что риски ЗГТ напрямую связаны с личным и семейным анамнезом, имеющимися заболеваниями, возрастом, длительностью постменопаузы. Польза и риск от применения ЗГТ постепенно изменяются с возрастом женщины и обусловлены физиологией старения, а не приемом ЗГТ.
ГОРМОНАЛЬНАЯ ТЕРАПИЯ КЛИМАКТЕРИЧЕСКИХ НАРУШЕНИЙ
Существуют следующие виды системной ЗГТ: эстроген — заместительная терапия; комбинации эстрогенов с прогестагенами; SERM (ралоксифен) — селективные модуляторы эстрогеновых рецепторов; тиболон (ливиал) — тканеселективный регулятор эстрогенной активности (STEAR), c 2009 г. согласно реестру Center for Drug Statistic Methodology отнесен к новой группе «Другие эстрогены» для лечения КС.
Показаниями к назначению ЗГТ являются:
Дополнительным преимуществом при назначении ЗГТ при симптомах КС является благоприятное влияние на костную ткань. Доказано, что ЗГТ в стандартных дозах (2 мг/сут эстрогена) снижает риск переломов; низкодозированная терапия — 1 мг/сут — обладает такой же эффективностью и может применяться длительное время при наличии метаболически инертного прогестагена, в частности дроспиренона (анжелик). ЗГТ может быть первой фазой длительной программы лечения, точнее, профилактики остеопороза (с назначением в последующем бисфосфонатов, селективных модуляторов эстрогеновых рецепторов и др.). Прогрессивное снижение МПКТ происходит в первые 5 лет постменопаузы. В связи с этим очень важно своевременно назначать ЗГТ при симптомах КС, что оказывает протективное действие на костную массу. У женщин из группы риска по остеопорозу без проявлений климактерического синдрома ЗГТ целесообразно назначать после подтверждения снижения МПКТ по результатам остео-денситометрии. Женщинам этой группы необходимо применять ЗГТ как минимум до среднего возраста наступления менопаузы (51 год). Затем вопрос о продолжении приема ЗГТ решается индивидуально с учетом приверженности пациентки к гормональной терапии. Назначение только препаратов кальция не показано, так как всасывание кальция происходит только при действии эстрогенов или бисфосфонатов.
ЗГТ, при отсутствии симптомов климактерического синдрома, не назначается только с целью профилактики сердечно-сосудистых заболеваний или ухудшения памяти и деменции (болезнь Альцгеймера).
Препаратами выбора при терапии только урогенитальных нарушений являются местные средства, не обладающие системным эстрогенным действием.
При необходимости купирования менопаузальных расстройств у женщин в постменопаузе особенно показана комбинация эстрадиола с прогестагеном дроспиреноном, учитывая высокую частоту артериальной гипертензии и ее значимость в качестве фактора риска ССЗ, наряду с другими проявлениями метаболического синдрома.
Противопоказания к назначению ЗГТ являются:
Обследование женщин перед назначением ЗГТ включает:
Для выявления риска тромбозов используют опросник:
1. Были ли у Вас или кого-либо из членов вашей семьи инсульты и/или инфаркты в молодом возрасте?
2. Проходили ли Вы или кто-нибудь из Вашей семьи тестирование на наследственную (генетическую) предрасположенность к тромбообразованию?
3. Было ли у Вас в анамнезе привычное невынашивание беременности и/или преждевременные роды с мертворождением?
4. Страдаете ли варикозным расширением вен?
5. Были ли у Вас тромбозы или тромбоэмболии (тромбоз глубоких вен голени, ТЭЛА)?
6. Повышалось ли у Вас артериальное давление во время беременности (гестоз)?
7. Был ли у Вас период неподвижности более 24 часов за последние 2 недели (болезнь, травма)?
8. Больны ли Вы раком или страдали раком раньше?
9. Предстоит ли Вам в ближайшее время плановая хирургическая операция?
ВЫБОР СХЕМЫ ТЕРАПИИ
При наличии матки проводят комбинированную терапию эстроген+гестагенами:
При отсутствии матки в течение 3-х лет проводят монотерапию эстрогеном (климар, эстрожель, диви-гель, прогинова).
При выборе препарата для ЗГТ также необходимо учитывать наличие сопутствующих гинекологических и соматических заболеваний. У женщин с миомой матки и/или аденомиозом, наличием в анамнезе менометроррагий, частых выскабливаний препарат первого выбора для терапии КС в перименопаузе является климонорм. Прогестагенный компонент (левоноргестрел) является производным норстероидов, что надежно защищает эндометрий и не способствует росту миомы. Оптимальным видом ЗГТ для таких женщин является введение левоноргестрел-рилизинговой внутриматочной системы мирена в комбинации с трансдермальными (или пероральными) эстрогенами. После купирования симптомов КС мирена служит для профилактики полипов эндометрия, которые часто рецидивируют в постменопаузе.
У женщин в перименопаузе с метаболическим синдромом (МС), сахарным диабетом (СД), ожирением и артериальной гипертензией (АГ), другой экстрагенитальной патологией, а также для профилактики метаболических нарушений применяется комбинация эстрадиола с прогестагеном — дроспиреноном, положительно влияющим на метаболизм во время климакса. Клинические данные, полученные в последнее время при использовании новых прогестагенов, свидетельствуют о том, что положительные эффекты ЗГТ могут быть более весомыми, чем просто купирование менопаузальных проявлений. Дроспиренон (ДРСП) — прогестаген, являющийся производным 17-αспиронолактона и антагонистом альдостероновых рецепторов, характеризуется достаточно выраженной антиминералокортикоидной активностью, превышающей таковую спиронолактона в 8 раз, а также умеренным антиандрогенным влиянием, при этом у него отсутствуют нежелательные андрогенные и глюкокортикоидные свойства. По своим фармакологическим характеристикам ДРСП максимально близок к эндогенному прогестерону. Применение комбинации 1 мг эстрадиола и 2 мг ДРСП (анжелик) способствует снижению веса до 1,5 раз уже в течение первого года терапии [9]. Назначение анжелика у пациенток в постменопаузе с уже развившимся МС не влияет на толерантность к глюкозе и не способствует развитию инсулинорезистентности (Порывкина О.Н. и соавт.). Кроме того, убедительно продемонстрированы достаточно выраженные антигипертензивные эффекты анжелика у пациенток с АГ I и II стадии, в том числе при наличии СД 2 типа, при этом ДРСП не оказывает влияния на уровень АД у женщин с нормальными показателями [10, 11]. Это представляется крайне важным, принимая во внимание высокую частоту АГ и ее значимость в качестве важнейшего компонента МС.
При патологии гепатобилиарного тракта и/или непереносимости пероральных форм рекомендуется ежедневно трансдермально вводить эстрогены и на II фазу (условного цикла) 10 дней каждого месяца интравагинально — утрожестан 200 мг/с или мирена в сочетании с климарой или другими эстрогенами.
В перименопаузе на фоне циклического режима ЗГТ иногда наблюдаются прорывные кровотечения, что побуждает врача госпитализировать женщину для выскабливания по поводу гиперплазии эндометрия. Это можно объяснить тем, что гормональная функция яичников еще сохранена, а под влиянием эндогенного и экзогенного (ЗГТ) эстрадиола в эндометрии происходят пролиферативные процессы, что клинически проявляется менометроррагиями. В данном случае необходимо отменить препараты ЗГТ и через 7 дней после прекращения кровянистых выделений провести УЗИ. При нормальных данных эхографии гормонотерапию можно продолжить, а при наличии больших фолликулов в яичниках нужно сделать перерыв до возобновления симптомов КС.
Длительность гормонотерапии при лечении симптомов КС составляет 2—3 года. В последнее время все больше женщин хотят продолжить прием препаратов для ЗГТ после купирования симптомов КС с целью улучшения качества жизни. При этом если возраст женщины соответствует менопаузе (50—51 лет) или при приеме циклических препаратов нет менструальной реакции, рекомендуется перейти на непрерывный режим ЗГТ.
Принципы ЗГТ в постменопаузе:
Продолжительность ЗГТ зависит от показаний, по которым она назначается:
Перед началом терапии, а затем ежегодно пациентки должны проходить обследование.По заключению экспертов Международного общества по менопаузе, нет четких данных, что длительное использование ЗГТ улучшает или ухудшает показатель польза-риск, нет необходимости лимитировать длительность использования ЗГТ при том, если польза-риск обсуждаются с пациенткой ежегодно [7, 8].
Таким образом, проблема ранних и отдаленных последствий дефицита эстрогенов в климактерии является актуальной не только в медицинском, но и в социальном аспекте. На современном этапе ее можно успешно решить благодаря созданию безопасных и эффективных гормональных препаратов.
ЛИТЕРАТУРА
1. Манухин И.Б., Тумилович Л.Г., Геворкян М.А. Гинекологическая эндокринология. Клинические лекции. Москва, 2009. ГЕОТАРМЕДИА.
2. Тумилович Л.Г., Геворкян М.А. Справочник гинеколога-эндокринолога. Москва, 2009. Практическая медицина.
3. Сметник В.П. Медицина климактерия. Москва, 2006. Литера.
4. Подзолкова Н.М., Подзолков А.В. Ренессанс тиболона. Значение доказательной медицины в оценке эффективности, безопасности и приемлемости заместительной гормональной терапии. // Проблемы репродукции. — 2009. — № 6. — С. 71—76.
5. Юренева С.В. и соавт. Заместительная гормонотерапия: дискредитация и реабилитация // Проблемы репродукции. 2009. — №2. — С. 73—78.
6. Чазова И.Е, Сметник В.П. и соавт. Ведение женщин с сердечнососудистым риском в пери— и постменопаузе: консенсус российских кардиологов и гинекологов. // Проблемы репродукции. — 2008. — №5. — С. 79—87.
7. Updated practical recommendation for HRT in peri-and postmenopause. // Climacteri. — 2008. — V.11. — P. 108—123.
8. NAMS position statement // Menopause. — 2008.
9. Archer D.F., Thorneycroft I.H., Foegh M., et al. Long-term safety of drospirenone-estradiol for hormone therapy: a randomized, double-blind, multicenter trial. // Menopause. — 2005. — V. 12. — P.716— 727
10. White W.B., Pitt B., Preston R.A., Hanes V. Effect of a New Hormone therapy, DRSP and 17β-E2 in Postmenopausal Women with Hypertension. // Hypertension. — 2006. — V. 48. — P. 1—8.
11. Preston R.A., Alonso A., Darlene P., et al. Additive effect of Drospirenone/17-β-Estradiol in hypertensive postmenopausal women receiving Enalapril. // American Journal of Hypertension. — 2005. V. 18. — P. 797—804.
Читайте также:
- Гистологический диагноз рака. Стадия развития злокачественной опухоли
- Распределение жевательной нагрузки на мостовидные протезы. Критерии выбора
- Зона просветления костей рук. Рентгенологические признаки перегрузки кости
- Лучевая диагностика внутренней и наружной резорбции зуба
- Диагностика риска развития миодистрофии Дюшенна. Методы
