КТ, ангиография при тромбозе верхней брыжеечной артерии (ВБА)
Добавил пользователь Евгений Кузнецов Обновлено: 21.01.2026
Ангиография чревного ствола и брыжеечных артерий представляет собой рентгенологическое исследование сосудов брюшной полости после внутриартериального введения контрастного вещества. Как правило, катетер проводят через бедренную артерию в аорту, а затем под рентгеноскопическим контролем устанавливают в чревном стволе либо в верхней или нижней брыжеечной артерии. Введение контрастного вещества в одну или несколько артерий позволяет визуализировать сосудистую сеть брюшной полости. При суперселективной ангиографии контрастное вещество вводят в ветвь брыжеечной артерии, при этом можно подробно исследовать особенности кровоснабжения определенного участка ЖКТ. Серия последовательных рентгеновских снимков позволяет оценить состояние сосудистого русла на всем его протяжении, включая артерии, капилляры и вены. Ангиографию чревного ствола и брыжеечных артерий выполняют при невозможности эндоскопическим путем установить источник желудочно-кишечного кровотечения, а также с целью уточнения характера опухоли в случае, если исследования с барием, УЗИ, радиоизотопное исследование или КТ оказались недостаточно информативными.
Кроме того, показаниями к проведению ангиографии являются цирроз печени и портальная гипертензия (особенно если планируется наложение портокавального анастомоза), повреждения сосудов (в том числе сосудов печени и селезенки) при травмах живота, а также необходимость в уточнении патологических изменений сосудистого русла. Ангиография позволяет визуализировать нижнюю полую вену даже при обратном кровотоке по воротной вене, поэтому данный метод используется чаще, чем спленопортография. К осложнениям, связанным с проведением ангиографии, относятся кровотечение, венозный тромбоз, образование тромбов в полости сердца, аритмии и тромбо- или атероэмболия при отрыве атеросклеротической бляшки.
- Установить источник желудочно-кишечного кровотечения.
- Дифференцировать доброкачественную опухоль от злокачественной.
- Определить выраженность цирроза печени и портальной гипертензии.
- Определить характер повреждений сосудистого русла при травмах живота.
- Выявить патологические изменения сосудов.
Подготовка
- Следует объяснить пациенту, что исследование позволяет оценить состояние сосудов брюшной полости после введения контрастного вещества.
- Пациент должен воздержаться от приема пищи в течение 8 ч до исследования.
- Следует объяснить пациенту, что при исследовании ему внутривенно вводят седативные препараты, а место введения сосудистого катетера обезболивают, при этом он может почувствовать укол, а при пальпации бедренной артерии - также давление, но болезненных ощущений при пункции бедренной артерии благодаря местному обезболиванию почти не бывает.
- Пациента предупреждают, что при введении контрастного вещества он может почувствовать кратковременное жжение.
- Пациента предупреждают также, что в процессе исследования (при выполнении снимков) он может слышать громкие щелкающие звуки.
- Во время исследования пациент должен лежать неподвижно (для этого при необходимости его фиксируют к рентгеновскому столу), так как в противном случае снимки получатся нечеткими.
- Необходимо предупредить пациента, что пребывание в неподвижном состоянии на жестком рентгеновском столе впоследствии может привести к непродолжительному ощущению скованности.
- Следует сообщить пациенту, кто и где будет выполнять исследование и сколько оно продлится (обычно от 30 мин до 3 ч в зависимости от числа исследуемых сосудов).
- Необходимо проследить, чтобы пациент или его родные дали письменное согласие на исследование.
- Следует выяснить, нет ли у пациента повышенной чувствительности к йоду, контрастным веществам и морепродуктам.
- Необходимо удостовериться в наличии результатов анализа крови (уровень гемоглобина и гематокрит, время свертывания, АЧТВ, ПВ, количество тромбоцитов).
- Следует предупредить пациента о необходимости переодеться в больничную одежду, снять с себя украшения и другие рентгеноконтрастные предметы, которые могут быть видны на рентгеновских снимках.
- Перед исследованием пациента просят помочиться, определяют исходные физиологические показатели.
- При необходимости следует назначить седативные препараты.
Процедура и последующий уход
- После укладывания пациента на рентгеновском столе катетеризируют вену для проведения инфузионной терапии и восполнения ОЦК. Подключают пульсоксиметр и аппараты для контроля сердечной деятельности и АД.
- Делают обзорный снимок брюшной полости, определяют ЧСС.
- Место пункции артерии промывают водой с мылом, выбривают, обрабатывают раствором повидон-йода и изолируют стерильным бельем.
- Вводят местный анестетик и пальпируют бедренную артерию. Осторожно вводят иглу до появления в шприце крови.
- Через иглу в аорту вводят проводник, после чего иглу извлекают.
- По проводнику вводят катетер, проводник извлекают и вводят контрастное вещество для определения места расположения катетера. После этого под рентгеноскопическим контролем в выбранную для исследования артерию вновь устанавливают проводник.
- После установки проводника катетер продвигают по ходу артерии. Проводник извлекают и вводят контрастное вещество для определения места расположения катетера.
- К катетеру присоединяют инжектор. После введения контрастного вещества быстро выполняют серию рентгеновских снимков.
- После контрастирования одной или нескольких главных артерий можно приступить к проведению суперселективной ангиографии. Под рентгеноскопическим контролем катетер продвигают в выбранную для исследования ветвь главной артерии, вновь вводят контрастное вещество и быстро выполняют серию снимков. При необходимости можно последовательно катетеризировать и исследовать несколько ветвей главных артерий.
- При выявлении окклюзии выполняют баллонную ангиопластику.
- После завершения исследования катетер извлекают. Пункционный канал придавливают в течение 15 мин.
- Следует периодически осматривать место пункции в связи с возможностью кровотечения и образования гематомы, а также ощупывать пульс на периферических артериях.
- После исследования не разрешается вставать с постели в течение 4-6 ч и сгибать ногу на стороне исследования. Угол наклона кровати не должен превышать 30°. Чтобы воспользоваться подкладным судном, пациент может перевернуться на бок или прибегнуть к посторонней помощи.
- Следует периодически определять основные физиологические показатели до их стабилизации. При осмотре нижних конечностей важно определить пульсацию периферических артерий (подколенная артерия и тыльная артерия стопы) и обратить внимание на цвет и температуру кожи.
- При развитии кровотечения необходимо придавить место пункции; для рассасывания гематомы назначают согревающие компрессы.
- После исследования пациент может вернуться к обычной для него диете. Если во время исследования инфузионная терапия не проводилась, пациенту рекомендуют обильное питье, чтобы ускорить выведение контрастного вещества.
Меры предосторожности
У больных с коагулопатией ангиографию чревного ствола и брыжеечных артерий следует выполнять с осторожностью.
Предостережение. В большинстве случаев побочные реакции, связанные с введением контрастного вещества, развиваются в течение получаса. Необходимо тщательное наблюдение за состоянием пациента для своевременного выявления гиперемии лица, крапивницы, признаков отека гортания и шока.
Исследование противопоказано при беременности из-за повышенного риска тератогенного эффекта.
Нормальная картина
В норме на снимках прослеживаются 3 фазы перфузии: артериальная, капиллярная и венозная. Артерии постепенно сужаются и разветвляются по направлению к периферии. Контрастное вещество равномерно заполняет синусоиды. Воротная вена появляется на снимках спустя 10-20 с после введения контрастного вещества, это время, необходимое для протекания контрастного вещества через сосуды селезенки в селезеночную вену, через капилляры кишечника в верхнюю брыжеечную вену и по ним в воротную вену.
Отклонение от нормы
При желудочно-кишечном кровотечении наблюдается вытекание контрастного вещества из поврежденных сосудов. Причиной кровотечения из верхних отделов ЖКТ могут быть синдром Мэллори-Вейса, язва желудка или двенадцатиперстной кишки, геморрагический гастрит, а также эрозии слизистой оболочки желудка в области грыжи пищеводного отверстия диафрагмы. Пищеводное кровотечение редко удается диагностировать при ангиографии чревного ствола и брыжеечных артерий, поскольку контрастное вещество обычно не поступает в вены пищевода. Кровотечение из нижних отделов ЖКТ может возникать из дивертикула, при раке или ангиодисплазии. При опухолях органов брюшной полости, таких как карциноид, аденома, лейомиома, ангиома и аденокарцинома, отмечаются различные нарушения кровоснабжения. Если опухоль располагается в непосредственной близости от артерий и вен, она может искажать рисунок сосудистой сети, а на поздних стадиях и вовсе замещать ее. Сосуды, кровоснабжающие опухоль, определяются на снимках как зоны патологической васкуляризации. Участки некроза представляют собой скопления контрастного вещества. Контрастное вещество может задерживаться в капиллярах опухоли, что отражается на снимках в виде пятен, соответствующих зоне ее расположения. В зависимости от размера и локализации опухоль может приводить к образованию артериовенозных шунтов. Поскольку при различных опухолях перечисленные признаки встречаются с разной частотой, их сочетание позволяет провести дифференциальную диагностику между доброкачественными и злокачественными новообразованиями. На ранней стадии цирроза печени изменения воротной вены почти отсутствуют, а печеночная артерия и ее ветви имеют нормальный вид. По мере прогрессирования заболевания венозный отток затрудняется, печеночная артерия и ее ветви становятся расширенными и извитыми, появляются венозные коллатерали. На поздних стадиях цирроза печени наблюдается обратный ток крови в воротной вене, однако она визуализируется на рентгеновских снимках, иногда с признаками тромбоза.
Травмы живота нередко приводят к разрыву селезенки, реже повреждается печень. При разрыве селезенки обычно наблюдаются смещение артерий, проходящих внутри нее, и вытекание контрастного вещества из сосудистого русла в паренхиму. Если разрыв не сопровождается образованием субкапсулярной гематомы, селезенка сохраняет нормальные размеры. При образовании субкапсулярной гематомы селезенка увеличивается и смещает селезеночную артерию и вену. На снимке гематома имеет вид крупного бессосудистого образования, которое растягивает артерии, проходящие внутри селезенки, внедряясь между паренхимой и капсулой.
Аналогичные изменения наблюдаются при повреждении печени. Наблюдается смещение печеночной артерии и внепеченочных ветвей. При образовании внутрипеченочной или субкапсулярной гематомы отмечаются смещение и растяжение артерий, проходящих внутри печени. Повреждение сосудов печени может повлечь за собой формирование артериовенозной фистулы между системой печеночной артерии и воротной вены. Ангиография позволяет выявлять различные поражения, сопровождающиеся изменением диаметра и хода артерий. Образование атеросклеротических бляшек или атером (отложений липидов под интимой) приводит к сужению просвета артерий или их окклюзии, что сопровождается образованием коллатералей. К другим изменениям, которые могут выявляться на ангиограммах, относятся аневризмы, тромбоз и эмболия.
Факторы, влияющие на результат исследования
- Движения пациента во время исследования.
- Остатки бария в кишечнике после предшествующего рентгеноконтрастного исследования ЖКТ, наличие газа или каловых масс в кишечнике.
- Атеросклеротические изменения катетеризируемой артерии (невозможность провести катетер).
"Ангиография чревного ствола и брыжеечных артерий" и другие статьи по рентгенологическим исследованиям
Верхней мезентериальной (брыжеечной) артерии синдром
Синдром верхней мезентериальной (брыжеечной) артерии является редкой патологией, обусловленной частичным сдавлением нижней горизонтальной части двенадцатиперстной кишки верхней мезентериальной артерией.
Синонимы
- синдром Уилки (Wilkie)
- синдром верхней брыжеечной артерии
Эпидемиология
Встречается редко, но распознается легко. В англоязычной литературе описано около 400 случаев. Чаще встречается у женщин, обычно начинается в детском и подростковом возрасте.
Анатомия
Верхняя брыжеечная артерия берет свое начало на уровне I-го поясничного позвонка и отходит от аорты под острым углом. Горизонтальная (нижняя) часть двенадцатиперстной кишки (pars horizontalis /inferior/), пересекает аорто-мезентериальный угол на уровне III-го поясничного позвонка, ниже ДПК проходит левая почечная вена. В норме аорто-мезентериальный угол составляет 38-65°, а расстояние между сосудами находится в пределах 13-34 мм.
Патология
Анатомические причины развития синдрома включают выраженный поясничный лордоз, аномально высокое прикрепление дуоденоеюнального изгиба связки Трейца, аномально низкое отхождение ВБА или уменьшение количества жировой клетчатки в аорто-мезентериальном углу.
Диагностика
Диагностика синдрома верхней брыжеечной артерии основывается на сочетании клинической картины и данных визуализации указывающих на обструкцию. Диагностические критерии синдрома ВБА включают снижение угла до 6 - 16° и уменьшение расстояния до 5-11 мм.
КТ/МРТ
КТ и МР ангиография позволяют визуализировать сдавление верхней брыжеечной артерией двенадцатиперстной кишки путем измерения угла отхождения и расстояние между ВБА и аортой:
- в норме угол между ВБА и аортой колеблется в диапазоне 38-65°, а дистанция между сосудами составляет 13-34 мм
- при синдроме верхней брыжеечной артерии оба значения снижены и колеблются в пределах 6°-16° и 5-11 мм.
Литература
Bavelloni A, Piazzi M, Raffini M, Faenza I, Blalock WL. Prohibitin 2: At a communications crossroads. (2015) IUBMB life. 67 (4): 239-54. doi:10.1002/iub.1366 - Pubmed
Острая окклюзия мезентериальных сосудов
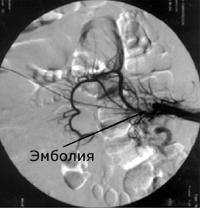
Острая окклюзия мезентериальных сосудов - острое нарушение кровообращения в брыжеечных сосудах, приводящее к ишемии кишечника. Заболевание проявляется резкой, нестерпимой болью в животе, рвотой и поносом с примесью крови, шоковым состоянием. Диагноз острой окклюзии мезентериальных сосудов определяют на основании клинической картины, данных селективной ангиографии, рентгенографии брюшной полости, лапароскопии. Острая окклюзия мезентериальных сосудов требует экстренного оперативного вмешательства (эмбол- или тромбэндартериоэктомии, резекции пораженных отделов кишечника), профилактики перитонита и повторных окклюзий.
Общие сведения
Острая окклюзия мезентериальных сосудов - неотложная патология в гастроэнтерологии, возникающая вследствие тромбоза или эмболии сосудов брыжейки. Острая окклюзия мезентериальных сосудов проявляется резким нарушением кровообращения в сосудистых участках проксимальнее и дистальнее места обструкции, сопровождается выраженным ангиоспазмом и дополнительным тромбообразованием, в результате чего возникает острое нарушение питания и ишемическое поражение стенки кишечника. В дальнейшем начинают развиваться необратимые деструктивные изменения, формируется анемический и геморрагический инфаркт (некроз) кишечника. Острая окклюзия мезентериальных сосудов характеризуется крайне тяжелым течением и высокой летальностью.
Локализация и протяженность ишемического поражения кишечника при острой окклюзии мезентериальных сосудов зависит от вида и уровня обструкции, наличия коллатеральных путей компенсации кровотока. В 90% случаев наблюдается окклюзия основного ствола или одной из ветвей верхней брыжеечной артерии, в большей степени обеспечивающей кровоснабжение пищеварительного тракта. Нижняя брыжеечная артерия имеет хорошие коллатеральные связи, поэтому при ее окклюзии редко возникают серьезные нарушения мезентериального кровообращения. Окклюзия брыжеечных вен встречается реже; возможно также смешанное поражение брыжеечных артерий и вен, при котором острой окклюзии одного из сосудов предшествует хроническая обструкция другого.
Острая окклюзия мезентериальных сосудов встречается преимущественно у лиц мужского пола в возрасте старше 50-60 лет.
Причины острой окклюзии мезентериальных сосудов
Острая окклюзия мезентериальных сосудов развивается как осложнение различных сердечно-сосудистых заболеваний (атеросклероза, пороков сердца, системных аллергических васкулитов, ревматизма, гипертонической болезни, аневризмы брюшной аорты, аритмии), предшествующих операций на сердце и аорте, злокачественных опухолей, травм.
Непосредственной причиной острой окклюзии мезентериальных сосудов являются тромбоз и эмболия. При тромбозе просвет сосудов брыжейки перекрывается тромбом, образовавшимся вследствие изменения сосудистых стенок на фоне повышенной свертываемости крови и замедленного кровотока (патогенетическая триада Вихрова). При эмболии наблюдается обструкция брыжеечных сосудов частицей тканью опухоли, инородным телом или пузырьком воздуха, мигрировавшими от первичного источника поражения с током крови.
Острая окклюзия мезентериальных сосудов может протекать с компенсацией, субкомпенсацией и декомпенсацией мезентериального кровотока. При компенсации мезентериального кровотока (спонтанно или под воздействием консервативной терапии) все функции кишечника восстанавливаются полностью. Субкомпенсация мезентериального кровотока ввиду недостаточного кровоснабжения может приводить к ряду заболеваний кишечника: брюшной жабе, язвенным энтеритам и колитам и др. Декомпенсация мезентериального кровообращения вызывает распространенный гнойный перитонит и развитие тяжелого абдоминального сепсиса.
Симптомы острой окклюзии мезентериальных сосудов
Развернутой клинической картине острой окклюзии мезентериальных сосудов могут предшествовать предвестники заболевания, сходные с предынфарктным состоянием, - так называемая «брюшная жаба».
В большинстве случаев острая окклюзия мезентериальных сосудов имеет внезапное начало и на стадии ишемии (первые 6-12 часов) характеризуется невыносимыми, схваткообразными болями в животе. Пациент испытывает беспокойство, не находит себе места, принимает вынужденную позу с приведенными к животу ногами. Возникают тошнота и рвота с примесью желчи и крови, позднее рвота с каловым запахом, неоднократный жидкий стул с примесью крови («ишемическое опорожнение кишечника»).
Наблюдается резкая бледность кожных покровов, цианоз, шоковое состояние, повышение артериального давления на 60-80 единиц (симптом Блинова), брадикардия. Для острой окклюзии мезентериальных сосудов характерно несоответствие между тяжестью состояния больного и данными его осмотра: в первые часы живот остается мягким, брюшная стенка участвует в дыхании, отмечается незначительная болезненность без симптомов раздражения брюшины.
В стадии инфаркта (через 6-12 часов от начала острой окклюзии мезентериальных сосудов) болевые ощущения немного уменьшаются, но нарастает локальная (в зоне поражения кишки) болезненность при пальпации, между пупком и лобком может прощупываться тестовидная припухлость (симптом Мондора), ухудшается состояние больного. Эвакуаторная функция кишечника сохраняется, артериальное давление нормализуется, пульс учащается.
Диагностика
Распознавание острой окклюзии мезентериальных сосудов опирается на анализ клинической картины заболевания: острый болевой абдоминальный синдром, поражение сердца и сосудов в анамнезе. Важное диагностическое значение имеет исследование коагулограммы, определение количества тромбоцитов, холестерина крови.
При обзорной рентгенографии брюшной полости определяется пневматизация кишечника, наличие горизонтальных уровней жидкости в брюшной полости. Специфическим методом диагностики острой окклюзии мезентериальных сосудов является селективная мезентерикография, которая уже на ранней стадии заболевания может выявить отсутствие кровотока в стволе и ветвях брыжеечной артерии. При наличии технической возможности выполняется магнитно-резонансная ангиография мезентериальных сосудов.
Диагностическая лапароскопия позволяет обнаружить изменения кишечника и брюшной полости, наличие признаков анемического и геморрагического инфаркта кишки. Острую окклюзию мезентериальных сосудов дифференцируют от прободной язвы желудка и двенадцатиперстной кишки, острого аппендицита, кишечной непроходимости, острого панкреатита и острого холецистита.
Лечение острой окклюзии мезентериальных сосудов
При острой окклюзии мезентериальных сосудов показано экстренное хирургическое вмешательство, целью которого служит ревизия кишечника с оценкой его жизнеспособности, ревизия основных брыжеечных сосудов, устранение причины сосудистой непроходимости и восстановление мезентериального кровотока, резекция некротизированных отделов кишечника, профилактика перитонита.
Реваскуляризация кишечника выполняется путем непрямой эмбол- или тромбэндартериоэктомии, в трудных случаях проводится реконструктивное обходное шунтирование с использованием сосудистых протезов (протезирование верхней брыжеечной артерии).
При некрозе кишечника реваскуляризация дополняется частичной или обширной резекцией пораженных участков кишечника и активным назоинтестинальным дренированием для лечения послеоперационного пареза кишечника. Через 24-48 часов возможно выполнение релапаротомии с целью контроля состояния брюшной полости или наложения отсроченного анастомоза.
Пред- и послеоперационное ведение больного с острой окклюзией мезентериальных сосудов включает назначение антитромботических препаратов для профилактики повторной эмболии и ретромбоза; мероприятия интенсивной терапии с целью восстановления ОЦК, устранения интоксикации, улучшения кровотока и тканевого метаболизма, стабилизации сердечной деятельности. Проводится антибактериальная терапия, дренирование и санация брюшной полости для предупреждения гангрены и перитонита.
Прогноз и профилактика
Восстановление кровотока в брыжеечных артериях в течение первых 4-6 часов («золотой период») может предотвратить инфаркт кишечника и восстановить его функции. Как правило, оперативное вмешательство приходится на II и III стадии острой окклюзии мезентериальных сосудов, поэтому летальность после операции достигает 80-90%. Прогноз ухудшает наличие основного заболевания, приведшего к острому нарушению мезентериального кровообращения.
Профилактика острой окклюзии мезентериальных сосудов заключается в своевременном устранении потенциального источника тромбоэмболии, т. е. первичного заболевания (атеросклероза, мерцательной аритмии, ревматического порока сердца, аневризм и др.).
Тромбоз воротной вены ( Пилетромбоз )
Тромбоз воротной вены - это полная или частичная окклюзия ствола воротной вены и ее ветвей тромботическими массами. Патология проявляется абдоминальным синдромом, рвотой, диареей, признаками портальной гипертензии (асцит, спленомегалия, расширение венозных коллатералей), осложняется кровотечением из верхних отделов пищеварительного тракта, инфарктом кишечника и другими состояниями. Основу диагностики составляют методы визуализации - УЗДС, МР- и КТ-ангиография, венография пораженных участков. Лечебная тактика предполагает антикоагулянтную терапию, тромболизис, хирургическую коррекцию.
МКБ-10
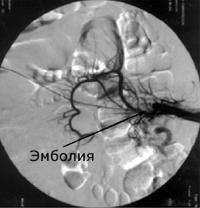
Тромбоз воротной вены (пилетромбоз) считается достаточно редким явлением, риск возникновения которого не превышает 1% в общей популяции. Его распространенность среди пациентов с циррозом печени варьируется от 0,6 до 26%, что, по-видимому, связано с различием в критериях выборки и диагностических методах. Заболевание называют причиной 5-10% случаев портальной гипертензии у жителей развитых стран и до 40% - в азиатском регионе (из-за более высокой частоты инфекционной патологии). Распространенность первичного тромбоза у взрослых и детей одинакова. Гендерных отличий в развитии болезни не выявлено, кроме цирротической обструкции, чаще диагностируемой у мужчин.

Причины
Заболевание имеет мультифакторную природу. Тромбоз развивается под влиянием системных и локальных нарушений, участвующих в повреждении сосудистой стенки, усилении коагуляции, замедлении венозного кровотока. Среди наиболее значимых причин отмечают следующие:
- Цирроз печени. Является основным этиологическим фактором, составляя 24-32% случаев тромботической окклюзии. Вероятность тромбоза повышается на поздних стадиях болезни, при необходимости трансплантации органа. Переход цирроза в гепатоцеллюлярную карциному увеличивает частоту внепеченочных пилетромбозов.
- Новообразования. Злокачественные новообразования печеночного или панкреатического происхождения являются причиной 21-24% случаев тромбоза. Развитие патологии опосредовано компрессией или прямой опухолевой инвазией, сопутствующей гиперкоагуляцией, гормональными сдвигами.
- Тромбофилии. Системные нарушения вызваны врожденными дефектами коагуляции - генетическими мутациями (фактора V Лейдена, протромбина, ингибитора активатора плазминогена), дефицитом протеинов C и S, антитромбиновой недостаточностью. К приобретенным факторам относят хроническую миелопролиферативную патологию, антифосфолипидный синдром, пароксизмальную ночную гемоглобинурию.
- Воспалительные заболевания. Патологический процесс может возникать на фоне абдоминальной воспалительной патологии (панкреатита, холецистита, гепатита), инфекционных заболеваний (малярии, брюшного тифа, амебиаза). У детей и новорожденных половина случаев тромбоза приходится на долю омфалита, пупочного сепсиса, аппендицита.
- Травмы и оперативные вмешательства. Воротная вена подвергается повреждению при травмах живота и хирургических вмешательствах на органах брюшной полости (спленэктомии, холецистэктомии, трансплантациии печени). Патология возникает после портосистемного шунтирования, тонкоигольной аспирационной биопсии печени, склеротерапии вен пищевода.
К другим факторам риска тромбоза воротной вены относят беременность, прием пероральных контрацептивов, гиперхолестеринемию. Отмечена роль внутрибрюшной аденопатии, синдрома системного воспалительного ответа. В детском возрасте окклюзия возникает при врожденных аномалиях сосудистой системы (дефектах межжелудочковой и межпредсердной перегородок, деформации полой вены) и желчевыводящих путей. Причина 10-30% тромботических стенозов остается невыясненной.
Патогенез
Исходя из современных представлений, пилетромбоз является результатом системных коагулопатий (наследственных, приобретенных) и действия локальных факторов. Повреждение стенки сосуда опухолью, инвазивными процедурами или травмами характеризуется выработкой цитокинов, активацией тромбоксана A2 и тромбина, усилением адгезии и агрегации тромбоцитов. Венозный застой при наружной компрессии сопровождается гипоксией эндотелия, накоплением активированных факторов свертывания. Все это запускает формирование пристеночного кровяного сгустка с дальнейшим его увеличением.
Сосудистая окклюзия сопровождается портальной гипертензией, что ведет к изменению системной и внутриорганной гемодинамики. Печень теряет около 2/3 своего кровоснабжения, но это компенсируется дилатацией печеночной артерии и быстрым развитием сети коллатералей. Вокруг тромбированной вены формируется кавернома, а сама она превращается в фиброзный тяж. Новообразованные сосуды расположены в пределах желчных протоков и пузыря, поджелудочной железы, антрального отдела желудка, двенадцатиперстной кишки.
Патогенез тромбоза при печеночном циррозе до конца не ясен. Важное значение отводят портальной гипертензии с замедлением кровотока по воротной вене, периферическому лимфангииту, перипортальному фиброзу. Системное шунтирование крови провоцирует гемосидероз, гепатоциты в зонах гипоперфузии подвергаются апоптозу. В тонком и толстом кишечнике выше уровня окклюзии определяются застойные явления, в желудке - гастропатия. Брыжеечная ишемия может привести к переходу тромботического процесса на мезентериальные сегменты.
Классификация
Формальной классификации тромбоза воротной вены не существует. Согласно клиническим рекомендациям по портальной гипертензии, при постановке диагноза учитывают участок тромбоза и его проявления, наличие и характер основного заболевания, степень окклюзии (частичную, полную), вовлеченность внепеченочных сегментов. В зависимости от локализации тромба различают несколько форм патологии:
- Стволовая (трункулярная). Участок окклюзии расположен в стволе воротной вены, дистальнее слияния селезеночной и верхней мезентериальной. Возникает первично или путем распространения из корешкового сегмента.
- Радикулярная (корешковая). Характеризуется поражением корешковых ветвей - селезеночной вены и брыжеечных сосудов.
- Терминальная. Пилетромбоз распространяется на внутрипеченочные разветвления и капилляры, сопровождаясь мелкими или развитыми коллатералями.
Представленная классификация позволяет оценить последствия тромботической обструкции и трудоспособность пациента. При поражении сначала интерстициальных сосудов, а затем крупных стволов констатируют восходящий (первичный) процесс. Мезентериальный тромбоз, возникающий из-за обструкции воротной или селезеночной вен, называют нисходящим (вторичным). В клинической флебологии также различают острую, подострую и хроническую стадии, последовательно сменяющие друг друга.
Симптомы
Клиническая картина тромбоза воротной вены определяется происхождением, степенью, протяженностью, локализацией, темпами нарастания окклюзии, выраженностью коллатералей. Частичное тромбирование протекает бессимптомно, выявляясь лишь при инструментальной диагностике, полной обструкции (90-100% просвета) присуще бурное развитие за несколько суток. Подострая форма прогрессирует на протяжении 4-6 недель, а хронический процесс характеризуется медленным нарастанием симптоматики (от нескольких месяцев до года).
Стволовой тромбоз
Острый стволовой пилетромбоз проявляется резкими болями в правом подреберье и эпигастрии, сочетающимися с метеоризмом, частой рвотой, диареей (нередко с примесью крови). Быстро нарастают признаки портальной гипертензии - расширение подкожных, пищеводных, геморроидальных вен, асцит. Зачастую выявляют желтуху, недостаточность печеночной функции. Общее состояние пациентов быстро становится тяжелым, что в основном обусловлено рецидивирующими кровотечениями из желудочно-кишечного тракта.
Радикулярный тромбоз
Радикулярный тромбоз на уровне селезеночного сегмента начинается остро, с боли в левом подреберье, кровавой рвоты и дегтеобразного стула. Увеличение селезенки и субфебрильная лихорадка сочетаются с обычными размерами печени. В подостром периоде постепенно нарастают спленомегалия, асцит, расширяется венозная сеть на животе. Терминальная форма патологии выявляется только при распространенном поражении - у таких пациентов обычно определяют увеличенную селезенку, широкие подкожные коллатерали.
Хронический тромбоз
Хронический пилетромбоз не имеет специфических проявлений. Отсутствие аппетита и общая слабость - иногда единственные симптомы болезни. У большинства пациентов выявляют подкожные анастомозы, умеренный асцит. В 20-40% случаев патология манифестирует кровотечением из варикозных расширений пищевода. Вялотекущие варианты тромбоза воротной вены характеризуются нерезким болевым синдромом, субфебрилитетом, чувствительностью печении при пальпации. Отмечаются спленомегалия с признаками гиперспленизма, тяжестью в подреберье, исхуданием.
Осложнения
Наиболее опасное следствие острой окклюзии мезентериальных сосудов - инфаркт кишечника с развитием перитонита и полиорганной недостаточности (характерно для 5% случаев). Большинство осложнений длительного пилетромбоза обусловлено портальной гипертензией. Расширение пищеводных вен у многих пациентов сопровождается кровотечением, риск которого в 100 раз выше при циррозе печени. Выраженное портосистемное шунтирование приводит к печеночной энцефалопатии, вторичным изменениям в желчевыводящих путях (портальной билиопатии, холангиопатии). При сохраняющихся факторах риска тромбозы могут рецидивировать, осложняться эмболизацией.
Отсутствие специфических признаков тромбоза, необходимость определения предпосылок, уровня, степени и последствий поражения создают потребность в комплексном обследовании пациента. Основой диагностической программы выступают методы инструментальной визуализации:
- УЗАС воротной вены. Обладая высокой специфичностью (60-100%), признано методом выбора при первичной диагностике. УЗДС определяет неоднородный очаг повышенной эхогенности с нечеткими контурами, частично или полностью перекрывающий сосудистый просвет. Допплеровское картирование дает возможность выявить отсутствие кровотока в вене и ее притоках, наличие портосистемных шунтов, каверноматозную трансформацию.
- КТ и МР-ангиография сосудов.КТ с контрастированием дает точную информацию о состоянии венозных стенок, протяженности тромбированных участков, наличии перивисцеральных коллатералей, варикозных вен в забрюшинном пространстве. Магнитно-резонансную ангиографию используют для выяснения состоятельности портального кровотока, оценки просвета шунтов - ее результаты более надежны, чем УЗДС.
- Портальная венография. Используется в случаях, когда неинвазивными методами подтвердить или исключить тромботическое поражение не удается. Контрастная венография выявляет не только стенозы, но и дефекты наполнения от сдавления извне. Однако при установленной проходимости сосуда в ней нет необходимости.
Проводя диагностику пилетромбоза, врачи-флебологи обращают внимание на показатели коагулограммы (увеличение фибриногена, протромбинового индекса, замедление времени свертывания крови), низкий уровень антитромбина. Выявить варикозно-расширенные вены пищевода позволяет ФГДС, исключить цирроз удается благодаря эластографии и биопсии печени. Дифференциальная диагностика осуществляется с печеночным шистосомозом, тромбозом нижней полой вены, сдавливающим перикардитом, рестриктивной кардиомиопатией.
Лечение тромбоза воротной вены
Задачами лечебной коррекции являются восстановление проходимости сосуда, предотвращение прогрессирования патологии, устранение осложнений венозной гипертензии. Исходя из остроты процесса, возраста пациента, этиологических и прочих факторов, применяют комбинацию консервативных и радикальных методов:
- Антикоагулянтная терапия. Является лучшим способом для реканализации венозного просвета, но единого мнения о ее применении нет. Длительность лечения антикоагулянтами (низкомолекулярными гепаринами, пероральными средствами) у лиц с острым пилетромбозом составляет от 3 до 6 месяцев, а при хроническом решается в индивидуальном порядке.
- Введение тромболитиков.Регионарный тромболизис (введение стрептокиназы, альтеплазы, тенектеплазы) транспеченочным или трансъюгулярным доступом позволяет обеспечить реканализацию, избежав побочных эффектов антикоагулянтной терапии. При острой тотальной или субтотальной окклюзии может выполняться системный тромболизис.
- Хирургические методы. При неэффективности консервативных мероприятий операцией выбора является дистальное спленоренальное шунтирование. В условиях нарушенной проходимости селезеночного участка накладывают мезентерикопортальный или мезентерикокавальный анастомоз с применением сосудистых протезов.
Варикозные расширения пищевода лечат с помощью лигирования, эндоскопической склеротерапии. В ургентных ситуациях при кровотечении могут производить операции азигопортального разобщения (гастротомию с прошиванием нижней трети пищевода, деваскуляризацию желудка). Тяжелый гиперспленизм требует спленэктомии.
В целом прогноз при заболевании относительно благоприятный. Сгустки могут подвергаться асептическому аутолизу, организации, васкуляризации. Десятилетняя выживаемость для взрослых достигает 60%, а общий уровень смертности составляет менее 10%. При наличии цирроза и злокачественных новообразований прогноз ухудшается. Иногда тромбы превращаются в эмболы, становятся источником сепсиса. Но своевременное и интенсивное лечение приводит к реканализации сосуда, что сопровождается полным клиническим выздоровлением. Профилактика рецидивов проводится путем назначения антикоагулянтов.
1. Тромбоз воротной вены в практике гастроэнтеролога/ Подлесских М.Н., Цодиков Г.В., Волчкова Е.В. и др.// Фарматека. — 2010. — № 2.
2. Тромбоз воротной вены: современный взгляд на вопросы этиопатогенеза, профилактики и лечения / Бакулин И.Г., Шаликиани Н.В.// Эффективная фармакотерапия. Гастроэнтерология. - 2014- №2 (43).
3. Тромбоз воротной и селезеночных вен - предпеченочная портальная гипертензия/ Онучина Е.В.// Сибирский медицинский журнал. - 2005.
4. Тромбоз воротной вены у пациента с острым панкреатитом и хроническим алиментарно-токсическим гепатитом/ Карнута Г.Г. , Зиновьева С.Ю., Юркова Т.Е., Костюкевич О.И.// Русский медицинский журнал. - 2016. - №17.
Синдром верхней брыжеечной артерии ( Артериомезентериальная компрессия двенадцатиперстной кишки , Синдром Уилки )
Синдром верхней брыжеечной артерии (СВБА) — это разновидность дуоденальной непроходимости, вызванной сдавлением 12-перстной кишки между верхней брыжеечной артерией и абдоминальным отделом аорты. Болезнь проявляется болями в животе после еды, тошнотой, рвотой, ощущением переполнения желудка. Для диагностики применяют инструментальные методики: рентгенографию ЖКТ с пероральным контрастированием, ЭФГДС, УЗИ и комбинированную компьютерную томографию. Лечение в основном консервативное: назначается щадящая диета и лекарственные средства (прокинетики, спазмолитики, ферменты). При декомпенсированном варианте синдрома показано хирургическое вмешательство.


В медицинской литературе у СВБА есть несколько синонимов: артериомезентериальная или сосудистая компрессия двенадцатиперстной кишки, синдром Уилки. Заболевание встречается редко. Истинная распространенность неизвестна, что связано со сложностями диагностического поиска. Частота синдрома верхней брыжеечной артерии, по данным рентгенографии пассажа бария, составляет 0,013-0,3%. У женщин болезнь выявляется в 2 раза чаще. В 75% случаев сосудистая компрессия наблюдается у детей старше 10 лет, подростков и молодых людей до 30 лет.
Основным этиологическим фактором синдрома являются индивидуальные особенности анатомии гастродуоденальной зоны. Характерен угол около 20-25° (по сравнению с 30-60° в норме) между брюшной аортой и верхней брыжеечной артерией, из-за чего пространство между двумя сосудами сокращается до 10 мм и менее. Также отмечается высокое расположение связки Трейца, которая подтягивает горизонтальную часть 12-перстной кишки (ДПК) к вершине аортомезентериального угла.
Способствующие факторы
Дуоденальная компрессия происходит только при наличии провоцирующих факторов. Распространенные причины синдрома:
- резкое снижение веса, которое сопровождается сокращением объема висцерального жира − при этом расстояние между аортой и брыжеечной артерией уменьшается;
- поясничный лордоз, сколиоз;
- слабость мышц живота;
- строгий постельный режим после травм и операций.
Наиболее подвержены развитию синдрома верхней брыжеечной артерии подростки, у которых происходит быстрый скачкообразный рост без компенсаторного увеличения веса.
Хроническая дуоденальная непроходимость, связанная со сдавлением кишечника верхней брыжеечной артерией, развивается в 3 этапа. Для стадии компенсации характерно неполное перекрытие просвета органа и повышение внутрипросветного давления, что способствует прохождению пищи в нижележащие отделы ЖКТ. В этот период появляются стойкие нарушения трофики и микроциркуляции кишечной стенки, снижается поступление желчи и ферментов поджелудочной железы.
На этапе субкомпенсации дуоденальная перистальтика снижается. Обычно происходит обратный заброс содержимого в желудок, панкреатический проток или желчевыводящие ходы. Наиболее тяжело протекает стадия декомпенсации, которая проявляется дуоденостазом. Характерно патологическое расширение желудка и начальных отделов кишечника наряду с тотальной обструкцией артерией горизонтального участка двенадцатиперстной кишки.
Симптомы СВБА
В большинстве ситуаций синдром верхней брыжеечной артерии имеет хроническое течение, а его симптоматика нарастает постепенно. Острое начало заболевания возможно у больных с травмами позвоночника, ортопедическими проблемами или ожогами — состояниями, которые требуют длительной иммобилизации. Острый вариант синдрома манифестирует сильнейшими болевыми ощущениями в полости живота и кишечной непроходимостью.
Основной признак хронического сдавления ДПК верхней брыжеечной артерией — боли в эпигастрии, которые возникают спустя 20-40 минут после еды (постпрандиальный болевой синдром). Иногда боли появляются сразу после приема пищи. Болезненность достаточно ощутима, что вынуждает пациентов есть небольшими порциями или вовсе голодать. Для уменьшения дискомфорта человек принимает вынужденное положение: лежа на левом боку или на животе, стоя в коленно-локтевой позе.
Боли сопровождаются тошнотой и рвотой, чувством переполненного желудка. В рвотных массах содержится частично переваренная пища с включениями желчи. После рвоты больные чувствуют облегчение. Зачастую беспокоит горькая отрыжка, изжога. Характерно чувство раннего насыщения. Для декомпенсированной стадии характерно резкое похудение вплоть до истощения. При хроническом течении синдрома развивается апатия, снижается физическая и умственная трудоспособность.
При хроническом нарушении дуоденальной проходимости присоединяется желудочная патология. У 50% пациентов определяются гиперхлоргидрия и гиперацидный гастрит, который в 25-45% случаев переходит в язвенную болезнь. В субкомпенсированной стадии наблюдается дисфункция пилорического сфинктера, в результате чего формируется дуодено-гастральный рефлюкс. Повреждение желудочной стенки желчными кислотами проявляется в виде рефлюкс-гастрита.
Декомпенсированная стадия компрессии ДПК верхней мезентериальной артерией осложняется хроническим дуоденитом. Воспалительный процесс вызван свободным перемещением инфицированного желудочного содержимого в двенадцатиперстную кишку и обратно. В запущенных случаях синдрома снижается тонус сфинктера Одди, и застойное дуоденальное содержимое попадает в протоки. Как следствие, развивается хронический холецистопанкреатит, усугубляющий состояние больных.
На основании физикального обследования врачу-гастроэнтерологу трудно заподозрить артериомезентериальную компрессию ввиду отсутствия патогномоничных симптомов. Предположить сосудистый характер непроходимости можно у людей с астеничным телосложением, истощенных соматических или онкологических пациентов. Постановка диагноза синдрома верхней брыжеечной артерии основывается на применении ряда методов инструментальной диагностики:
- Рентгенологическое исследование.Рентгенография с контрастным веществом выявляет застой бария в сдавленной артерией горизонтальной части двенадцатиперстной кишки и замедленное опорожнение желудка (до 4-6 часов). Также визуализируется расширенная верхняя часть ДПК и стойкий дуоденогастральный рефлюкс. Еще один типичный признак — снижение перистальтики.
- ЭФГДС. При СВБА обнаруживают расширение желудка, а также начального отдела двенадцатиперстной кишки с патологическим сужением ее дистального отдела. При эндоскопическом исследовании визуализируется гиперемированная и отечная слизистая гастродуоденальной зоны. На декомпенсацию процесса указывает зияние сфинктера привратника.
- УЗИ гастродуоденальной зоны. Ультразвуковое исследование необходимо для наблюдения за сократительной функцией желудка и ДПК в режиме реального времени. Допплерография выполняется, чтобы оценить состояние брюшного отдела аорты, брыжеечных артерий, измерить сосудистый угол.
- КТ брюшной полости. Контрастирование пищеварительного канала с одновременной ангиографией абдоминальной части аорты назначается для верификации диагноза в сомнительных случаях. Исследование проводится для оценки стадии патологического процесса, измерения дуоденального просвета, величины угла, который образуют аорта и верхняя брыжеечная артерия.

Лечение синдрома верхней брыжеечной артерии
Консервативная терапия
В компенсированной и субкомпенсированной стадиях сосудистой компрессии проводится диетотерапия и медикаментозное лечение. Основные задачи консервативных мероприятий — усиление питания и уменьшение степени дуоденальной непроходимости. Лечебная диета предполагает прием жидкой, полужидкой и протертой пищи малыми порциями. Для коррекции состояния применяется ряд препаратов:
- Прокинетики. Лекарства стимулируют перистальтику ЖКТ, способствуя более быстрому продвижению химуса по пищеварительному каналу. Прокинетики нормализуют тонус мышечных сфинктеров, предотвращают дуоденальный рефлюкс.
- Спазмолитики. Назначаются короткими курсами перед приемом прокинетиков для снижения внутриполостного давления в 12-перстной кишке, которая сдавлена мезентериальной артерией. Препараты быстро устраняют боли и дискомфорт в эпигастральной зоне.
- Ферментные препараты. Для улучшения пищеварительной функции используют средства заместительной терапии с панкреатическими ферментами. Лекарства способствуют нормализации стула, уменьшают вздутие живота и диспепсические симптомы.
- Антибактериальные средства. Чтобы уменьшить риск гастродуоденитов, при дуоденальном рефлюксе рекомендуют кишечные антисептики, которые не оказывают системного действия. С целью подавления бактериальной инфекции показаны фторхинолоны, макролиды.
Хирургическое лечение
Критериями отбора больных для проведения оперативного вмешательства являются прогрессирующая потеря массы тела, выраженный дуоденостаз, развитие осложнений СВБА. Наиболее часто проводят дуоденоеюностомию, которая позволяет полностью устранить симптомы у 90% пациентов. В современной абдоминальной хирургии используют лапароскопическую операцию по разделению связки Трейца и уменьшению дуоденальной компрессии.
Сочетание медикаментозного лечения со специальной диетой показывает хорошие отдаленные результаты у пациентов с начальными стадиями синдрома. С учетом современных хирургических методов лечения прогноз благоприятен даже при декомпенсации заболевания. Меры профилактики включают своевременную коррекцию искривлений позвоночного столба, соблюдение рациональной диеты с адекватной калорийностью.
1. Синдром верхней брыжеечной артерии. Клинический случай в педиатрической практике/ Н.М. Тихон, М.П. Волкова, А.В. Хмеленко, А.И. Гринь // Вестник Витебского государственного медицинского университета. — 2016.
2. Синдром верхней мезентериальной артерии/ М.Б. Щербинина, В.Н. Гладун, С.И. Кожан, А.В. Семашко, С.И. Фещенко// Современная гастроэнтерология. — 2012.
3. Синдрома верхней мезентериальной артерии (синдром Уилки): клиническое наблюдение/ А.К. Графов, М.А. Халилов, Н.Н. Шевердин, А.Г. Алексеев // Российский вестник детской хирургии, анестезиологии и реаниматологии. — 2015.
4. Хроническая дуоденальная непроходимость. Т.Д. Звягинцева, И.И. Шаргород// Восточноевропейский журнал внутренней и семейной медицины. - №2 — 2016.
Читайте также:
