КТ, МРТ печени при болезни Вильсона-Коновалова
Добавил пользователь Алексей Ф. Обновлено: 22.01.2026
Болезнь Вильсона-Коновалова (синонимы гепатолентикулярная дегенерация, гепатоцеребральная дистрофия) - тяжелое прогрессирующее наследственное заболевание, передающееся по аутосомно-рецессивному типу, в основе которого лежит нарушение экскреции меди из организма, приводящее к избыточному накоплению этого микроэлемента в тканях и сочетанному поражению паренхиматозных органов (прежде всего печени) и головного мозга (преимущественно подкорковых ядер).
NB! Причиной возникновения БВК являются мутации гена ATP7B, который локализован на 13 хромосоме в локусе 13q14.3 и кодирует медь транспортирующую АТФ-азу Р-типа - ATP7B.
Код(ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| E83.0 | Нарушение обмена меди (Болезнь Вильсона-Коновалова) |
Дата разработки/пересмотра протокола: 2017 год.
Сокращения, используемые в протоколе:
| анти-LC | антитела к цитозольному антигену печени |
| анти-LKM | антитела к микросомам печени и почек |
| анти-LP | антитела к белкам печени и поджелудочной железы |
| анти-SLA | антитела к растворимым печеночным антигенам |
| БВК | болезнь Вильсона-Коновалова |
| БХАК | биохимический анализ крови |
| ГГТП | Гамма-глютамилтранспептидаза |
| ГЛД | гепатолентикулярная дегенерация |
| КТ | компьютерная томография |
| МРТ | магниторезонансная томография |
| ОАК | общий анализ крови |
| ОАМ | общий анализ мочи |
| СОЭ | скорость оседания эритроцитов |
| СРБ | С-реактивный протеин |
| УЗИ | ультразвуковое исследование |
| ЩФ | Щелочная фосфотаза |
| ЭКГ | электрокардиограмма |
| ЭНМГ | электронейромиография |
| ЭРХПГ | Эндоскопическая ретроградная холангиопанкреатография |
| ЭЭГ | электроэнцефалография |
| ANA | антинуклеарные антитела |
| IgG | иммуноглобулин G |
| АNCА | антитела к цитоплазме нейтрофилов |
| АМА | антимитохондриальные антитела |
Пользователи протокола: врачи общей практики, педиатры, детские гастроэнтерологи, детские неврологи.
Категория пациентов: дети.
Шкала уровня доказательности:
| A | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| B | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| C | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая клиническая практика. |

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Клиническая картина гепатолентикулярной дегенерации характеризуется большим полиморфизмом в отношении как неврологических, так и соматических проявлений. Этот полиморфизм отражен в различных классификациях заболевания.
Формы болезни Вильсона [3]:
· Бессимптомная форма;
· Печеночная форма;
· Церебральная форма;
· Смешанная форма.
В зависимости от вовлечения в патологический процесс печени и центральной нервной системы и характера экстрапирамидной симптоматики, распознают 5 форм гепато-церебральной дистрофии [11]:
· Брюшная (абдоминальная) форма - манифестирует в возрасте от 5 до 17 лет и характеризуется различными вариантами поражения печени, нередко принимающими злокачественное «галопирующее» течение, приводящее к смерти раньше появления симптомов со стороны нервной системы. Её продолжительность от нескольких месяцев до 3-5 лет.
· Ригидно-аритмогиперкинетическая, или ранняя форма отличается быстрым течением; начинается также в детском возрасте. В клинической картине преобладают мышечная ригидность, приводящая к контрактурам, бедность и замедленность движений, хореоатетоидные или торсионные насильственные движения. Характерны дизартрия и дисфагия, судорожный смех и плач, аффективные расстройства и умеренное снижение интеллекта. Заболевание длится 2-3 года, заканчивается летально.
· Дрожательно-ригидная форма встречается чаще других; начинается в юношеском возраста, протекает медленнее, порой с ремиссиями и внезапными ухудшениями, сопровождающимися субфебрильной температурой; характеризуется одновременным развитием тяжѐлой ригидности и дрожания, дрожание очень ритмичное (2-8 дрожаний в секунду), резко усиливается при статическом напряжении мышц, движениях и волнении, в покое и во сне исчезает. Иногда обнаруживаются атетоидные хореоформные насильственные движения; наблюдаются также дисфагия и дизартрия. Средняя продолжительность жизни около шести лет.
· Дрожательная форма начинается в возрасте 20-30 лет, протекает довольно медленно (10-15 лет и больше); дрожание резко преобладает, ригидность появляется лишь в конце болезни, а порой наблюдается гипотония мышц; отмечается амимия, медленная монотонная речь, тяжѐлые изменения психики, часты аффективные вспышки. Наблюдаются эпилептиформные припадки.
· Экстрапирамидно-корковая форма встречается реже других форм. Типичные для гепатоцеребральной дистрофии нарушения в дальнейшем осложняются апоплектиформно развивающимися пирамидными парезами, эпилептиформными припадками и тяжѐлым слабоумием (обнаруживаются обширные размягчения в коре больших полушарий). Длится 6-8 лет, заканчивается летально.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ [1-6,10,19,20]: на БВ должны обследоваться дети в возрасте от 2 до 18 лет, имеющих необъяснимое повышение сывороточных аминотрансфераз, проявления фульминантной печеночной недостаточности, хронического гепатита, цирроза печени, неврологические нарушения неустановленной этиологии, Кумбс-негативную гемолитическую анемию, отягощенный семейный анамнез по БВ. Диагностика БВ базируется на комбинации клинических симптомов, данных лабораторного обследования и молекулярно-генетического тестирования.
Диагностические критерии 4
Жалобы:
· боли в животе различной локализации;
· изменение цвета кожи;
· носовые кровотечения;
· тремор и непроизвольные движения;
· слюнотечение, дизартрия, нарушение глотания;
· мигренеподобные головные боли;
· бессонница;
· депрессия;
· невротическое поведение;
· изменения личности;
· психоз.
Клинические признаки болезни отражены в таблице 1.
Таблица 1 - Клинические признаки болезни Вильсона.
| Проявления болезни Вильсона-Коновалова | Симптомы |
| Поражение печени | Бессимптомная гепатомегалия |
| Изолированная спленомегалия | |
| Стеатогепатит | |
| Острый (фульминантный) гепатит | |
| Аутоиммуноподобный гепатит | |
| Цирроз печени | |
| Поражение ЦНС | Двигательные нарушения (тремор, непроизвольные движения) |
| Слюнотечение, дизартрия | |
| Ригидная дистония | |
| Псевдобульбарный синдром | |
| Вегетососудистая дистония | |
| Мигренеподобные головные боли | |
| Бессоница | |
| Дистонические атаки | |
| Психиатрические симптомы | Депрессия |
| Невротическое поведение | |
| Изменения личности | |
| Психоз | |
| Другие системы | Офтальмология: кольца Кайзера-Флейшера, «медная» катаракта |
| Гемолитическая анемия | |
| Патология почек: аминоацидурия, нефролитиаз | |
| Патология скелета: ранний остеопороз, артрит | |
| Поражение сердца: кардиомиопатия, нарушения ритма | |
| Панкреатит, желчекаменная болезнь | |
| Гипопаратиреодизм, гигантизм |
Физикальное обследование 5:
необходимо оценить наличие:
· смуглого («медный») цвета кожи;
· желтушности склер;
· незначительной или умеренной гепатомегалии;
· спленомегалии;
· неврологических нарушений и психических расстройств в виде непроизвольных движений в мышцах торса и конечностей;
· мигренеподобной головной боли;
· скованности в мышцах;
· эмоциональной лабильности;
· агрессивности.
Лабораторные исследования 6:
· общий анализ крови: лейкопения, нормохромная анемия, тромбоцитопения, ретикулоцитоз, ускоренная СОЭ.
· общий анализ мочи: при поражении почек можно обнаружить микрогематурию, незначительную протеинурию, гиперкальциурию.
· суточная экскреция мочи: гиперкупренилурия, признаки развившейся тубулопатии с признаками: глюкозурией, аминоацидурией, фосфатурией, уратурией, протеинурией.
· биохимический анализ крови: снижение церулоплазмина и общей меди, увеличение уровней свободной меди (таблица 1), аминотрасфераз (в 1,5-50 раз); билирубин повышен более чем в 2 раза, преимущественно за счет прямой фракции; уровень щелочной фосфатазы обычно повышен; может быть повышена активность гаммаглютамилтранспептидазы (ГГТП); гипоальбуминемия.
· коагулограмма: снижение протромбинового индекса, гипофибриногенемия, снижение тромбинового времени.
· пеницилламиновый тест: необходимо исследовать мочу, собранную сразу после приема 500 мг пеницилламина и через 12 часов. У пациентов с болезнью Вильсона-Коновалова суточная экскреция меди будет повышаться до более 1500 мкг/дл/сут (норма
Показатели лабораторных исследований представлены в таблице 2.
Таблица 2 - Лабораторные показатели при гепатолентикулярной дегенерации [6].
| Показатель | Норма | ГЛД |
| Церулоплазмин, мг/дл | 17-40 | < 17 |
| Общая медь в сыворотке крови, мкмоль/л | 12-32 | < 12 |
| Свободная медь в сыворотке крови, мкг/дл | 5-12 | > 50 |
| Суточная экскреция меди с мочой, мкг/сут | < 50 | > 100-1000 |
| Суточная экскреция меди с мочой в пробе с Д-пеницилламином, мкг/сут | 600-800 | 1000-3000 |
| Количественное содержание меди в печени, мкг/г | 15-55 | > 250 |
Инструментальные исследования 5:
· УЗИ печени и селезенки: позволяют выявить увеличение печени и реже селезенки, признаки портальной гипертензии и цирроза печени [5].
· ЭКГ - при поражении сердца можно выявить признаки гипертрофии левого или обоих желудочков, депрессию сегмента ST, инверсию зубца Т, различные виды нарушений ритма.
· ЭхоКГ - в ходе этого исследования можно выявить кардиомиопатию, гидроперикард.
· Электроэнцефалография - проводится пациентам с тяжелыми нарушениями со стороны ЦНС с эпилептическими приступами, регистрируется эпилептическая активность.
· Эзофагогастродуоденоскопия: на наличие варикозно расширенных вен пищевода и желудка.
· МРТ головного мозга: более информативно в диагностике, чем КТ головного мозга. Характерны билатеральные очаги пониженной плотности 3-15 мм в диаметре в области базальных ганглиев (хвостатое ядро, скорлупа и бледный шар), в таламусе, в области зубчатых ядер и коры мозжечка - симптом «морды гигантской панды» [19]. По мере прогрессирования процесса выявляются признаки диффузного атрофического процесса головного мозга с равномерным расширением субарахноидальных пространств и желудочковой системы [20]. Изменения МР-сигнала от структур головного мозга могут отсутствовать у 7-17% детей со смешанной формой болезни Вильсона при наличии неврологической симптоматики в виде тремора, дизартрии и изменения мышечного тонуса по экстрапирамидному типу 5.
· Пункционная биопсия печени: 1. для морфологического исследования биоптата печени, где выявляются дистрофические изменения клеток, некрозы, слабую воспалительную инфильтрацию и фиброз различной степени выраженности; 2. Определения концентрации меди в препарате печени - при ГЛД медь находится на уровне 1 000 мкг на 1 г сухого вещества печени. На доклинической стадии уровень печеночной меди не всегда превышает 250 мкг/г, у гетерозиготных носителей может быть в пределах 150-200 мкг/г. Нормальный уровень печеночной меди исключает ГЛД, тогда как повышенный подтверждает диагноз при наличии соответствующих клинических данных 5.
· Гистологическое исследование биоптата печени: морфологические изменения печени при болезни Вильсона не являются патогномоничными и включают в себя на ранних стадиях заболевания признаки жировой инфильтрации гепатоцитов (крупнокапельной и мелкокапельной), гликогеновой дегенерации ядер и фокальный гепатоцеллюлярный некроз, а также преобладание минимальной и низкой степени активности воспалительного процесса, нередко в сочетании с выраженными фибротическими изменениями. Могут быть изменения по типу аутоиммунного гепатита, вирусного, алкогольного и лекарственного поражения печени. По мере прогрессирования повреждений паренхимы, формируется фиброз и, впоследствии, цирроз печени. Обычно встречается гистологическая картина крупноузлового цирроза печени в исходе болезни Вильсона, однако, встречаются случаи и мелкоузлового цирроза.
Показания для консультации специалистов 3:
· консультация офтальмолога - для выявления колец Кайзера-Флейшера, также на наличие катаракты у детей, с целью исключения других болезней накопления;
· консультация невропатолога - оценка неврологического статуса, нервно-психического статуса;
· консультация психиатра - диагностика психиатрических состояний;
· консультация психотерапевта - коррекция психологических проблем;
· консультация гастроэнтеролога - коррекция нарушений желудочно-кишечного тракта;
· консультация гематолога - при наличии симптомов гемолитической анемии, коагулопатии;
· консультация нефролога - при наличии патологии в анализах мочи;
· консультация сурдолога - определение остроты слуха;
· консультация физиотерапевта - определение методов физиотерапевтического лечения;
· консультация хирурга - при риске пищеводно-желудочных кровотечений, для выявления показаний к проведению трансплантации печени у детей с признаками цирроза печени (ЦП), печеночно-клеточной декомпенсацией;
· консультация инфекциониста - при наличии сопутствующего вирусного гепатита;
· консультация отоларинголога - при инфекциях верхних дыхательных путей.
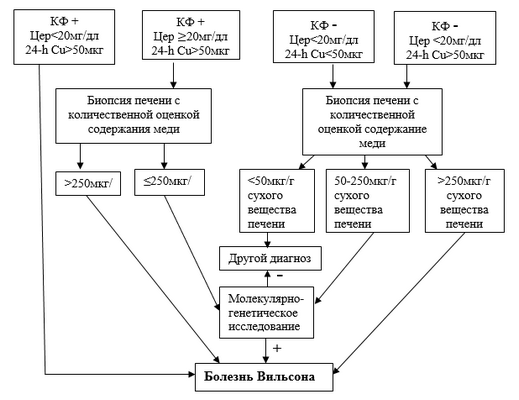
Диагностический алгоритм:
Рисунок 1- Алгоритм диагностики болезни Вильсона [3]. КФ - кольца Кайзера-Флейшера; Цер - церулоплазмин; 24-h Cu - суточная экскреция меди с мочой.
Ни один лабораторный тест (за исключением полного секвенирования патологического гена АТР7В) не обладает 100% чувствительностью и не обеспечивает 100% специфичность, таблица 3.
Таблица 3 - Тесты для диагностики болезни Вильсона.
| Тест | Характерные находки | Ложноотрицательный результат | Ложноположительный результат |
| Сывороточный церулоплазмин | Уменьшение на 50% относительно нормы | Нормальный уровень у пациентов с выраженным воспалением в печени. Завышение результата при иммунологических методах исследования. Беременность, прием эстрогенов. | Низкий уровень при: -мальабсорбции; -ацерулоплазминемии; -гетерозиготы |
| Суточная экскреция меди с мочой | >0,64мкмоль/24часа | Норма: -неправильный сбор мочи; -дети без вовлечения печени | Повышение: -гепатоцеллюлярный некроз; -холестаз; -контаминация |
| Свободная медь сыворотки | >1,6мкмоль/л | Норма при завышении уровня церулоплазмина иммунологическими методами | |
| Печеночная медь | >4мкмоль/г сухого вещества | В зависимости от места взятия материала: -активная болезнь печени; -узелки регенерации | Синдромы холестаза |
| Кольцо Кайзера-Флейшнера (при использовании щелевой лампы) | Наличие кольца | Отсутствует: -у 50% пациентов с печеночной формой; -у большинства асимптоматических сибсов | Первичный биллиарный цирроз |
Диагноз болезни Вильсона ставится на основании совокупности клинических данных, результатов лабораторного исследования и молекулярно-генетического анализа (таблица 4).
Таблица 4 - Лейпцигские балльные критерии диагностики болезни Вильсона [11]
Родственники по прямой линии вновь выявленного больного с болезнью Вильсона должны проходить скрининг на наличие у них болезни Вильсона-Коновалова.
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований 17
Таблица 5- Дифференциальный диагноз болезни Вильсона-Коновалова.
Цирроз печени - симптомы и лечение
Что такое цирроз печени? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Цирроз печени (ЦП) — это хроническое дегенеративное заболевание печени, связанное с диффузным патологическим процессом, при котором нормальные клетки печени повреждаются, а затем замещаются рубцовой тканью, образуя избыточный фиброз и структурно-анатомические регенераторные узлы.

Этиология
По этиологическим характеристикам можно выделить:
- распространённые формы ЦП;
- редкие формы ЦП.
К распространённым относят вирусные (В, С, D), алкогольные и метаболические формы цирроза печени.
Редкими формами ЦП являются:
- аутоиммунные, лекарственные, токсические, первичные и вторичные билиарные циррозы;
- генетически обусловленные патологии — гемохроматоз (нарушение обмена железа), болезнь Вильсона — Коновалова, дефицит белка альфа-1-антитрипсина, гликогеноз IV типа (недостаток ферментов), галактоземия, наследственная тирозинемия и непереносимость фруктозы;
- нарушение венозного оттока из печени — венокклюзионные формы ЦП (болезнь Бадда — Киари);
- тяжёлая правожелудочковая сердечная недостаточность;
- флебопортальные циррозы (типа Банти).
Пути заражения
Заразиться циррозом печени нельзя. Однако, если он вызван вирусным гепатитом, то возбудитель может передаться через кровь, при половых контактах и от матери к ребёнку.
Основную роль в возникновении и развитии вирусного ЦП играют симптомные, малосимптомные и бессимптомные формы острого вирусного гепатита В, С, а также одновременное заболевание гепатитами В и D с последующим переходом в активный хронический вирусный гепатит. У большинства больных интервал между острым гепатитом С и клинически выраженными проявлениями ЦП превышает 30 лет. Только у мужчин, употребляющих более 50 г спирта в день, выраженные формы ЦП возникают через 13-15 лет.
Наиболее частыми причинами смерти больных ЦП является:
- большая печёночная недостаточность;
- кровотечение из варикозно расширенных вен пищевода;
- первичный рак печени;
- иммунопротективная недостаточность, влекущая за собой активизацию инфекционных (микробных) процессов, в первую очередь спонтанного бактериального перитонита и пневмонии, а также возникновение оксидативного стресса.
У больных в терминальной (заключительной) фазе заболеваний печени в основном наблюдаются декомпенсированные формы цирроза печени: асцит, варикозное расширение вен пищевода и желудка, энцефалопатия и желтуха.
Особенности цирроза печени у детей
Заболевание у детей встречается крайне редко и обычно связано:
- с аутоиммунным поражением печени;
- кардиогенными заболеваниями — лёгочной гипертензией и хронической сердечной недостаточностью;
- болезнью Бадда — Киари;
- врождёнными болезнями накопления — наследственным гемохроматозом, лизосомальными болезнями накопления, болезнью Вильсона — Коновалова;
- флебопортальным циррозом (типа Банти).
Прогноз у таких детей неблагоприятный, чаще всего они погибают, так как не успевают попасть к гепатологу и выяснить диагноз. Также они обычно страдают от множества сопутствующих болезней, в том числе от основного заболевания, ставшего причиной цирроза.
Проявления заболевания у детей и взрослых схожи. Единственный эффективный метод лечения цирроза у детей — это пересадка печени. Поэтому крайне важно вовремя диагностировать заболевание и встать в очередь на пересадку печени.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы цирроза печени
Цирроз печени в течение длительного времени может протекать латентно, т. е. бессимптомно.
Клиническая картина ЦП зависит от его формы и течения, активности основного заболевания, а также наличия или отсутствия печёночно-клеточной недостаточности, синдрома портальной гипертензии, холестаза и внепечёночных проявлений.
Основные общие симптомы, которые чаще всего встречаются при ЦП:
- повышенная утомляемость;
- похудение;
- нарушения сознания и поведения;
- ухудшение аппетита и чувство дискомфорта в животе;
- пожелтение кожи, белковых оболочек глаз и слизистой;
- осветление или обесцвечивание кала;
- потемнение мочи;
- болевые ощущения в животе;
- отёки;
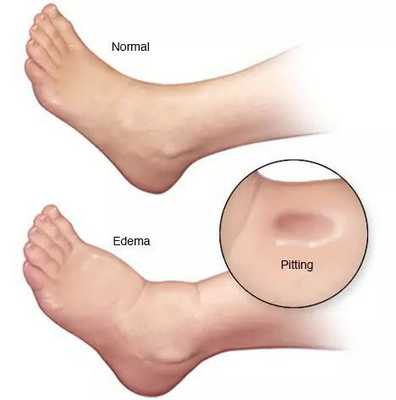
- асцит (скопление жидкости в брюшной полости);
- кровотечения из носа, желудочно-кишечного тракта, дёсен или геморроидальных узлов, а также подкожные кровоизлияния;
- часто возникающие бактериальные инфекции (например, органов дыхания);
- снижение полового влечения;
- кожный зуд.
Симптомы распространённых форм ЦП
При высокоактивном ЦП, кроме общей утомляемости, осветления стула и потемнения мочи, может возникать тупая боль в правом подреберье и вздутие живота.
Во время осмотра часто выявляют:
- субиктеричность (желтушность) склер;
- расширение вен брюшной стенки, напоминающее голову медузы;
- венозный шум при выслушивании в эпигастральной области живота (шум Крювелье — Баумгартена);
- серо-коричневатый цвет шеи;
- гинекомастию (увеличение грудных желёз);
- гипогонадизм (у мужчин);
- контрактуру Дюпюитрена (укорочение сухожилий ладоней).
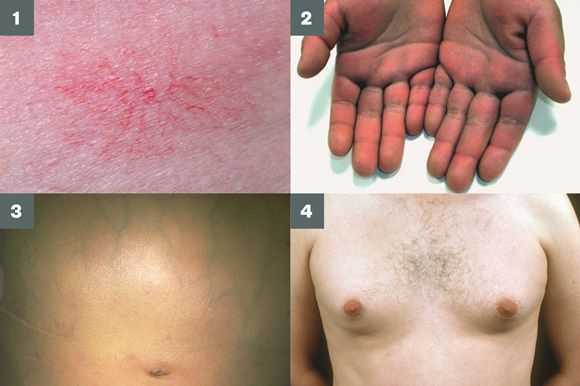
Три последних признака цирроза печени зачастую наблюдаются при алкогольных ЦП.
В области грудной клетки в 50-80% случаев наблюдаются телеангиэктазии кожи (расширения мелких сосудов), чаще при алкогольных ЦП. Пальпаторно печень отчётлива уплотнена, имеет неровный нижний край. Размеры печени различны — от значительного увеличения до уменьшения.
Часто при пальпации выявляется умеренно увеличенная селезёнка, причём её край может выступать из-под рёберной дуги на 1-3 см.
При развитии ЦП появляются симптомы белково-энергетической недостаточности, асцит, отёки, а также печёночный запах при тяжёлой печёночной недостаточности.
Симптомы при малоактивных и начальных стадиях ЦП
Данные формы ЦП зачастую протекают бессимптомно и выявляются в ходе периодических медицинских осмотров, диспансеризации, а также как случайная находка при обследовании пациента со смежной патологией или внепечёночными проявлениями.
При малоактивном ЦП, как правило, не возникают жалобы, связанные с печенью. Во время активного расспроса можно выявить весеннее снижение работоспособности, частые болезни, после которых возможны кровоточивость дёсен и потемнение мочи. Такие пациенты хуже, чем раньше, переносят длительные физические и нервно-психические нагрузки.
Желтухи и выраженного увеличения билирубина, за исключением периода интеркурентного острого гепатита, нет. Неяркая телеангиоэктазия кожи (сосудистые звёздочки) в области грудной клетки наблюдаются у 40-60% людей с ЦП.
Телеангиоэктазии кожи, плотная печень с фестончатым краем и умеренно увеличенная селезёнка — ценная клинико-диагностическая триада, которая с вероятностью 80-90% свидетельствует о ЦП или далеко зашедшем активном хроническом гепатите.
Патогенез цирроза печени
В основе патофизиологии цирроза лежит повреждение и некроз паренхимы (основной ткани) печени с деструкцией и гибелью гепатоцитов (клеток печени), а также системное поражение интерстициальной ткани.
При всех формах ЦП нарушается иммунологическое равновесие организма, преобладающими становятся аутоиммунные процессы: иммунная система человека принимает собственные клетки печени за чужеродные и повреждает их. В конечном итоге, это приводит к разрушению гепатоцитов и структуры печени в целом. Однако при этом каждая форма ЦП имеет свои патогенетические особенности:
- при вирусных гепатитах повреждающим агентом является сама вирусная частица, которая, размножаясь в клетке, разрушает её, вызывая цитолиз;
- при алкогольном ЦП прямое токсическое воздействие на мембраны гепатоцитов оказывает ацетальдегид с развитием алкогольной жировой болезни печени и алкогольного стеатогепатита;
- при метаболическом ЦП ведущую роль в патогенезе играет ожирение и сахарный диабет через стадию неалкогольного стеатогепатита с инсулинорезистентностью и последующей запрограммированной гибелью клеток печени.
В основе патогенеза более редких причин цирроза печени лежат ещё более частные механизмы развития повреждения и разрушения гепатоцитов и структуры печени:
- нарушение обмена и накопления железа при гемохроматозе;
- накопление меди при болезни Вильсона — Коновалова;
- окклюзия в системе воротной вены при гепатопортальном склерозе.
Цирроз формируется на протяжении многих лет. С течением времени происходят изменения генетического аппарата клеток печени, в результате чего появляются новые патологические клетки. Этот процесс в печени является иммуновоспалительным, он поддерживается чужеродными агентами, в роли которых могут выступать разные субстраты:
- вирус гепатита В;
- алкогольный гиалин;
- денатурированные белки;
- некоторые лекарственные средства;
- медьбелковые и железобелковые комплексы (ферритин).
В итоге повреждения паренхимы печени развивается гепатоцеллюлярная (печёночно-клеточная) недостаточность за счёт диффузного фиброза и трансформации ткани печени в анормальные узлы-регенераты. [3] [4] [5]
Классификация и стадии развития цирроза печени
В 1974 году на съезде гепатологов в Акапулько (Мексика) была принята единая морфологическая классификация, которую позже уточнили и несколько доработали эксперты ВОЗ. В настоящее время она является общепринятой.
Болезнь Вильсона ( Болезнь Вестфаля-Вильсона-Коновалова , Болезнь Вильсона-Коновалова , Гепатолентикулярная дистрофия , Гепатоцеребральная дистрофия , Лентикулярная прогрессирующая дегенерация )
Болезнь Вильсона — наследственное заболевание, передающееся по аутосомно-рецессивному типу. Возникает в условиях мутаций в гене АТР7В, кодирующем белок медьтраснпортирующей АТФазы печени. Характерный признак болезни Вильсона — накопление меди в различных органах и тканях, в большей степени в печени и базальных ганглиях. Болезнь Вильсона может протекать в брюшной, ригидно-аритмогиперкинетической, дрожательной или экстрапирамидно-корковой форме. Диагностика болезни Вильсона включает офтальмологическое обследование, биохимические анализы мочи и крови, МРТ или КТ головного мозга. Основу патогенетической терапии составляют тиоловые препараты, которые могут приниматься в течении нескольких лет и даже пожизненно.
МКБ-10
Общие сведения
Болезнь Вильсона — наследственное заболевание, передающееся по аутосомно-рецессивному типу. Возникает в условиях мутаций в гене АТР7В, кодирующем белок медьтраснпортирующей АТФ-азы печени. Характерный признак болезни Вильсона — накопление меди в различных органах и тканях, в большей степени в печени и базальных ганглиях. Первооткрыватель заболевания — А.К. Вильсон, описавший заболевание в 1912 году, в отечественной медицине — Н.А. Коновалов. Патогенез болезни Вильсона был выявлен в 1993 году. Понятию «болезнь Вильсона» соответствуют также: болезнь Вильсона-Коновалова, болезнь Вестфаля-Вильсона-Коновалова, дистрофия гепатоцеребральная, дистрофия гепатолентикулярная, дегенерация лентикулярная прогрессирующая.
Причины
Ген АТР7В картирован на длинном плече хромосомы 13 (13q14.3-q21.1). Организм человека содержит около 50-100 мг меди. Суточная потребность меди для человека — 1-2 мг. 95% абсорбированной в кишечнике меди, транспортируется в форме комплекса с церулоплазмином (один из глобулинов сыворотки, синтезируемых печенью) и только 5% в форме комплекса с альбумином. Кроме того, ион меди входит в состав важнейших метаболических ферментов (лизилоксидаза, супероксиддисмутаза, цитохром-С-оксидаза и др.). При болезни Вильсона происходит нарушение двух процессов обмена меди в печени — биосинтез главного медьсвязывающего белка (церулоплазмина) и выведение меди с желчью, следствием чего становится повышение уровня несвязанной меди в крови. Концентрация меди в различных органах (чаще всего в печени, почках, роговице и головном мозге) увеличивается, что приводит к их токсическому поражению.
Согласно классификации Н.В. Коновалова различают пять форм болезни Вильсона:
- брюшная
- ригидно-аритмогиперкинетическая
- дрожательно-ригидная
- дрожательная
- экстрапирамидно-корковая
Симптомы
Для болезни Вильсона характерен клинический полиморфизм. Первые проявления заболевания могут появиться в детстве, юношестве, в зрелом возрасте и гораздо реже в зрелом возрасте. В 40-50% случаев Болезнь Вильсона манифестирует с поражения печени, в остальных — с психических и неврологических расстройств. С вовлечением в патологический процесс нервной системы обнаруживается кольцо Кайзера-Флейшера.
Брюшная форма развивается преимущественно до 40 лет. Характерный признак — тяжелое поражение печени по типу цирроза печени, хронического гепатита, фульминантного гепатита.
Ригидно-аритмогиперкинетическая форма манифестирует в детском возрасте. Начальные проявления — мышечная ригидность, амимия, смазанность речи, трудности при выполнении мелких движений, умеренное снижение интеллекта. Для этой формы заболевания характерно прогрессирующее течение, с наличием эпизодов обострения и ремиссии.
Дрожательная форма возникает в возрасте от 10 до 30 лет. Преобладающим симптомом является тремор. Кроме того, могут наблюдаться брадикинезия, брадилалия, тяжелый психоорганический синдром, эпилептические приступы.
Экстрапирамидно-корковая форма встречается весьма редко. Ее начало схоже с началом какой-либо из вышеперечисленных форм. Для нее характерны эпилептические припадки, экстрапирамидные и пирамидные нарушения и выраженный интеллектуальный дефицит.
Офтальмологическое исследование с помощью щелевой лампы выявляет кольцо Кайзера-Флейшера. Биохимические исследования мочи обнаруживают повышенную экскрецию меди в суточной моче, а также снижение концентрации церулоплазмина в крови. С помощью визуализационных методов (КТ и МРТ головного мозга) обнаруживают атрофию полушарий большого мозга и мозжечка, а также базальных ядер.
При диагностике болезни Вильсона неврологу необходимо дифференцировать ее от паркинсонизма, гепатоцеребрального синдрома, болезни Геллервордена-Шпатца. Основным дифференциально-диагностическим признаком этих заболеваний является отсутствие характерных для болезни Вильсона кольца Кайзера-Флейшера и расстройств обмена меди. Для подтверждения болезни Вильсона проводится генодиагностика.
Лечение болезни Вильсона
Основой патогенетического лечения является назначение тиоловых препаратов, в первую очередь — D-пеницилламина либо унитиола. Главное преимущество купренила — низкая токсичность и возможность длительного приема при отсутствии побочных эффектов. Его назначают по 0,15 г (1 капсула) в сутки (только после еды), в дальнейшем, в течение 2,5-3 месяцев дозу увеличивают до 6-10 капсул/сутки (оптимальная доза). Лечение D-пеницилламином проводится годами и даже пожизненно с небольшими перерывами (на 2-3 недели) в случае появления побочных эффектов (тромбоцитопения, лейкопения, обострения язвенной болезни желудка и т. д.).
Унитиол назначают в случае непереносимости (плохой переносимости) D-пеницилламина. Длительность одного курса лечения — 1 месяц, после чего лечение приостанавливают на 2,5-3 месяца. В большинстве случаев наступает улучшение общего состояния пациента, а также регресс неврологических симптомов (скованности, гиперкинезов). В случае доминирования гиперкинезов рекомендовано назначение небольших курсов нейролептиков, при ригидности — леводопы, карбидопы, тригексифенидила.
В случае тяжелого течения болезни Вильсона, при неэффективности консервативного лечения за рубежом прибегают к трансплантации печени. При положительном исходе операции состояние пациента улучшается, восстанавливается обмен меди в организме. В дальнейшем лечение пациента составляет иммуносупрессивная терапия. В России на сегодня постепенно внедряется в клиническую практику метод биогемоперфузии с изолированными живыми клетками селезенки и печени (т. н. аппарат «вспомогательная печень). Немедикаментозное лечение состоит в назначении диеты (стол №5) в целях исключения продуктов богатых медью (кофе, шоколад, бобовые, орехи и т. д.).
Прогноз и профилактика
В случае своевременного диагностирования болезни Вильсона и проведения адекватной медьснижающей терапии возможна нормализация общего состояние пациента и обмена меди в организме. Постоянный прием тиоловых препаратов по схеме, назначенной врачом-специалистом, позволяет поддерживать профессиональную и социальную активность пациента.
Для предотвращения рецидивов болезни Вильсона рекомендовано проведение лабораторных исследований крови и мочи пациента несколько раз в год. Необходим контроль следующих показателей: концентрация меди, церулоплазмина и цинка. Кроме того, рекомендовано проведение биохимического анализа крови, общего анализа крови, а также регулярные консультации у терапевта и невролога.
МРТ при болезни Вильсона-Коновалова
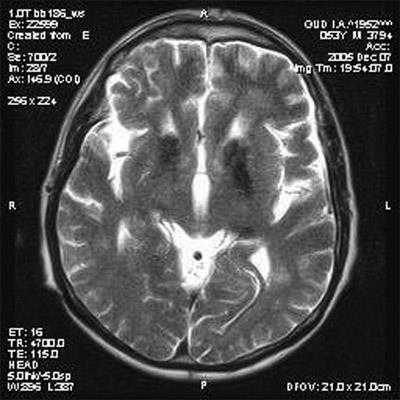
Болезнь Вильсона-Коновалова — наследственное заболевание, при котором происходит накопление меди в различных органах и тканях, но чаще всего поражаются печень и головной мозг.
Диагностика болезни Вильсона-Коновалова носит комплексный характер: лечащий врач, как правило, назначает офтальмологическое обследование, биохимические анализы мочи и крови, а также МРТ головного мозга.
Особенности болезни Вильсона-Коновалова
Формы данного заболевания классифицируются с учетом локализации патологического процесса или по преобладающим симптомам.
- брюшная (при поражении печени);
- ригидно-аритмогиперкинетическая (при выраженном напряжении в мышцах);
- дрожательная (в случае, если у пациента развился тремор);
- экстрапирамидно-корковая (этой форме характерны эпилептические припадки и синдром пирамидной недостаточности*);
- абдоминальная (при гепатопатии, вильсоновском гепатите, циррозе печени).
Клиническая картина болезни Вильсона-Коновалова многообразна: типичного набора симптомов заболевания нет, но обычно у пациентов наблюдается ригидность мышц и кольцо Кайзера Флейшера*. Остальные проявления заболевания зависят от его формы. Со временем в головном мозге пациента развиваются характерные для этой болезни структурные изменения, хорошо выявляемые на МРТ.
Проявления указанной патологии на МРТ выявляются благодаря повышению МР-сигнала в режиме Т2 и снижении в режиме Т1 от подкорковой области (ограды, скорлупы, хвостатых ядер, латеральных бледных шаров, наружной капсулы), среднего мозга, зубчатых ядер мозжечка и червя.
Первыми, как правило, поражаются скорлупа и хвостатые ядра. В мосту мозга распознаются поражение его срединных и дорзальных отделов с сохранностью пирамидных трактов и аналогичным изменением МР-сигнала от этих структур.
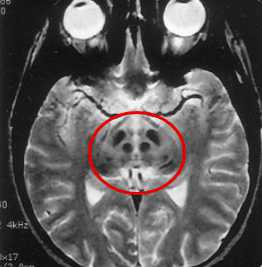
Последовательная эволюция изменений сигнала от дорзальной части моста напоминает «морду детеныша панды» с «глазами», которые формируются патологическим сигналом от центральных покрышечных проводящих путей.
Поражение среднего мозга носит диффузный характер, однако преобладает поражение белого вещества с сохранностью ядерных структур, в том числе наиболее крупных красных шаров. На поздних стадиях болезни выявляются атрофические изменения в подкорковых структурах.
Высокое качество визуализации структурных изменений в головном мозге, которое обеспечивает МР-томография, очень важна для правильной постановки диагноза. Таким образом, проявления болезни на МРТ считаются патогномоничными (т.е. безусловно характерными), что позволяет дифференцировать болезнь Вильсона-Коновалова от других неврологических патологий.
Узнайте,Опытные врачи

Врач высшей категории

Пашкова Анна Александровна
Кандидат медицинских наук



Александров Тимофей Александрович

Томограф экспертного класса
- Напряженность магнитного
поля — 1,5 Тл (высокопольный) - Высокое качество изображения
- Тонкие срезы
- Все виды МРТ-исследований
Как проходит процедура МРТ-исследования
Запись исследования на ваш выбор*| на диск | на пленку | на флешку |
Частые вопросы о МРТ-исследованиях

Артефакты (от лат. artefactum) - это погрешности, допущенные человеком, в процессе исследования. Артефакты значительно ухудшают качество изображения. Существует обширная группа физиологических (другими словами, относящихся к поведению человека) артефактов: двигательные, дыхательные, артефакты от глотания, моргания, случайных неуправляемых движений (тремор, гипертонус). Все артефакты, связанные с человеческим фактором, легко преодолеваются, если человек в процессе исследования полностью расслаблен, дышит ровно и свободно, без глубоких глотательных движений и частых морганий. Однако в медицинской практике нередки случаи использования легкого наркоза.
Магнитно-резонансная томография не имеет возрастных ограничений, поэтому ее можно проводить детям с самого рождения. Но ввиду того, что во время процедуры МРТ необходимо соблюдать неподвижность, обследование маленьких детей проводится в условиях анестезиологического пособия (поверхностного наркоза). В нашем центре исследование под наркозом не осуществляется, поэтому мы обследуем детей исключительно с семилетнего возраста.
Все противопоказания к проведению МРТ можно разделить на абсолютные и относительные.
Абсолютными противопоказаниями к проведению МРТ являются следующие особенности пациента: наличие у него кардиостимулятора (водителя ритма сердца) и других вживляемых электронных устройств, присутствие ферримагнитных (железосодержащих) и электрических протезов стремечка (после реконструктивных операций на среднем ухе), гемостатических клипс после операций на сосудах головного мозга, брюшной полости или легких, металлических осколков в области глазницы, крупных осколков, дроби или пуль вблизи сосудисто-нервных пучков и жизненно важных органов, а также беременность до трех месяцев.
К относительным противопоказаниям относятся: клаустрофобия (боязнь замкнутого пространства), наличие в теле пациента массивных не ферримагнитных металлических конструкций и протезов, наличие ВМС (внутриматочной спирали). Кроме того, все пациенты с магнитосовместимыми (не ферримагнитными) металлическими конструкциями могут обследоваться только по прошествии месяца после проведенного оперативного вмешательства.
Направление врача - необязательное условие посещения центра МРТ. Нам важна Ваша забота о своем здоровье, согласие на проведение обследования, а также отсутствие противопоказаний для проведения МРТ.
Любому человеку знакома головная боль, но если она повторяется подозрительно часто, безусловно, это нельзя оставить без внимания. Мы рекомендуем пациенту с сильными головными болями пройти МРТ головного мозга и его сосудов. В отдельных случаях этого может быть недостаточно, потому как не всегда причина головных болей связана именно с патологией головного мозга. Головные боли могут быть следствием шейного остеохондроза, поэтому наши специалисты дополнительно советуют пройти МРТ шейного отдела позвоночника и сосудов шеи.
Средняя продолжительность одного исследования в нашем центре составляет от 10 до 20 минут, однако, все зависит от выявленных изменений: иногда для уточнения заболевания врач-рентгенолог может расширить протокол исследования и прибегнуть к использованию контрастного усиления. В таких случаях время исследования увеличивается.
Магнитно-резонансная томография - это полностью безвредный и безопасный метод лучевой диагностики. В основе получения изображения МРТ отсутствует ионизирующие излучение, свойственное методу компьютерной томографии (КТ). Но существуют противопоказания, с которыми необходимо ознакомиться, перед тем как записаться на обследование.
Абсолютным противопоказанием к МРТ является беременность до трех месяцев. При подозрении на ургентные (угрожающие жизни) заболевания женщины решение о проведении МРТ в ранние сроки беременности принимает врач-гинеколог.
В нашем центре можно пройти МРТ во время беременности во втором и третьем триместре - для этого необходимо предоставить направление от лечащего врача, назначившего МРТ, а также справку от акушера-гинеколога о том, что проведение магнитно-резонансной томографии разрешено.
Нарушения обмена меди (болезнь Вильсона) у детей
Болезнь Вильсона (БВ) (синонимы: болезнь Вильсона-Коновалова, гепатолентикулярная дегенерация, гепатоцеребральная дистрофия) — редкое тяжёлое наследственное мультисистемное заболевание, проявляющееся преимущественно печёночными, неврологическими и психиатрическими нарушениями вследствие чрезмерного отложения меди в органах и тканях [1]. Это заболевание относится к числу трудно диагностируемых в связи с длительным латентным течением и полиморфизмом клинической симптоматики. БВ может клинически манифестировать как в детском и подростковом, так и в более старшем возрасте. При отсутствии медь-элиминирующей терапии это заболевание является фатальным.
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем. связанных со здоровьем (МКБ-10)
Клиническая картина БВ характеризуется большим полиморфизмом в отношении как неврологических, так и соматических проявлений. Это нашло своё отражение в различных классификациях заболевания [26, 27]. В настоящее время чаще всего используется классификация БВ, в основе которой лежит клинико-патоморфологический принцип [28]. Выделяют следующие формы БВ.
- Бессимптомная форма (около 10% случаев): клинических проявлений нет, диагноз установлен до проявления симптомов,
- Абдоминальная (печёночная) форма (около 40 % случаев): раннее начало, преимущественно с острой печёночной недостаточности или признаков хронической печёночной недостаточности; фульминантная печёночная недостаточность, цирроз печени.
- Церебральная (неврологическая) форма (около 40-50 % случаев): характерны разнообразные экстрапирамидные нарушения (тремор конечностей и головы, дистония, мозжечковая атаксия, паркинсонизм, нарушение почерка, дизартрия, мышечная ригидность, хорея, атетоз), психические нарушения (депрессия, раздражительность, расторможенность поведения, психотические эпизоды),
- Смешанная форма: сочетание неврологических и печёночных проявлений.
Этиология и патогенез
БВ развивается при наличии у человека патогенных вариантов в компаунд-гетерозиготном (чаще) или гомозиготном (реже) состоянии в гене ATP7B, который располагается на длинном плече 13 хромосомы (13q14.3-q21.1) и состоит из 21 экзона и 20 интронов (общая геномная длина гена составляет около 80 тысяч пар оснований).
Ген АТР7В кодирует одноимённый медь-транспортирующий белок из группы АТФаз Р-типа, который располагается в транс-Гольджи аппарате, обеспечивает транспорт меди через мембраны органелл гепатоцитов, способствуя выведению её с жёлчью, а также включению в молекулу апоцерулоплазмина (церулоплазмин без меди) с образованием голоцерулоплазмина (церулоплазмин с 6 молекулами меди). Наиболее высокая экспрессия гена ATP7B наблюдается в печени, однако он также экспрессируется в почках, плаценте, молочных железах, головном мозге и лёгких.
Тип наследования БВ аутосомно-рецессивный. К настоящему времени в гене АТР7В описано более 700 патогенных вариантов [88], большая часть из которых являются миссенс, однако нонсенс, инсерции/делеции и мутации сайтов сплайсинга также встречаются [13, 14] Наиболее распространённым патогенным вариантом в гене АТР7В среди европеоидной расы является Н1069Q. Около 50-80% пациентов с БВ, проживающих в странах Центральной, Восточной и Северной Европы являются носителями по крайней мере одного аллеля с таким вариантом. По данным ряда исследователей, в России среди пациентов с подтверждённым диагнозом БВ доля больных с вариантом Н1069Q в гетерозиготном состоянии составляет 50 %, а доля пациентов с этим вариантом в гомозиготном состоянии — 26,3 % [17]. В настоящее время чётких корреляций между патогенными вариантами и фенотипами БВ неизвестно.
Медь по своему общему содержанию в теле человека занимает третье место среди переходных металлов, незаменимых для организма. Она выступает в роли кофактора и (или) структурного компонента для нескольких ферментов, участвует во многих физиологических процессах, включая энергетический обмен, антиоксидантную защиту и обмен железа. Физиологическая потребность в меди для взрослых составляет около 1,0 мг/сут, для детей в зависимости от возрастной группы — от 0,5 до 1,0 мг/сут [18]. В организм медь поступает в основном с пищей. Наиболее богаты медью печень, моллюски, крабы, креветки, устрицы, лобстеры, соевые бобы, шоколад, орехи, злаки. Среднее потребление меди у человека составляет 1,5-2,5 мг/сут. Верхний допустимый уровень потребления составляет 5 мг/сут. Всасыванию в проксимальных отделах тонкой кишки подвергается от 20 % (при потреблении более 5 мг/сут) до 50 % (при потреблении менее 1 мг/сут) меди, остальное экскретируется с фекальными массами. В крови всосавшаяся медь связывается с альбумином и транскупреином и
Снижение функции медь-транспортирующей АТФазы в результате патогенных вариантов в гене АТР7В в компаунд-гетерозиготном или гомозиготном состоянии приводит к нарушению гепатобилиарной экскреции меди и нарушению её встраивания в церулоплазмин. Поскольку период полужизни апоцерулоплазмина значительно короче такового у церулоплазмина, нагруженного медью (5 ч против 5,5 сут), при БВ, как правило, в крови наблюдется снижение содержания церулоплазмина. Вместе с тем примерно у трети пациентов с БВ уровень церулоплазмина в крови может быть в пределах нормальных значений. Необходимо отметить, что использование метода определения медь-зависимой оксидазной активности позволяет точнее определить содержания апоцерулоплазмина, в то время как иммунологические тесты могут завышать получаемые значения, т.к. не способны дифференцировать апо- и голоцерулоплазмин.
Основным следствием дефицита медь-транспортирующей АТФазы является накопление меди в различных органах и тканях: первоначально — в печени, а по мере прогрессирования заболевания и при отсутствии лечения, когда способность печени аккумулировать медь исчерпывается, — в головном мозге, роговице глаз и почках. Это обусловливает полиморфизм клинических появлений БВ. Накопление меди в паренхиматозных органах сопровождается снижением содержания общей меди в сыворотке, т.к. в норме около 90 % общей меди составляет медь, связанная с церулоплазмином.
Несмотря на важнейшую роль меди во многих физиологических процессах, её избыток является губительным для организма. Патогенные эффекты избытка меди в клетке опосредованы образованием свободных радикалов с развитием перекисного окисления липидов, повреждением белков, нуклеиновых кислот, митохондрий в сочетании с истощением антиоксидантных систем. Медь может также ингибировать функции многих белков, напрямую связываясь с их тиоловыми и аминогруппами. Кроме того, избыток меди активирует проапоптотические механизмы. Всё это в конечном счёте приводит к разрушению перегруженных медью клеток, преимущественно гепатоцитов. Лизис таких гепатоцитов обусловливает повышение содержания свободной меди в сыворотке и, следовательно, компенсаторному повышению её суточной экскреции с мочой и накоплению в других органах-мишенях [19]. Помимо этого, избыток свободной меди в сыворотке может приводить к гемолитическим кризам [4].
Эпидемиология
Болезнь Вильсона является редким (орфанным) заболеванием, хотя показатели распространённости варьируют в зависимости от исследования. По данным ряда исследований, её распространённость составляет около 1 случая на 7 000-10 000 населения, в то время как частота гетерозиготного носительства патогенных вариантов в АТР7В составляет около 1:40 [20, 21].
Наиболее часто указывается распространённость 1:30,000 [21, 22, 23, 24,140]. Более поздние исследования из Китая [141] и Франции [142] свидетельствуют о более низкой распространенности 1: 56,000 и 1:66,000, соответственно.
Клиническая картина
Cимптомы, течение
Клиническая картина БВ характеризуется многообразием симптомов и манифестирует в возрасте от 3 до 74 лет (средний возраст 13,2 года), однако до 5-летнего возраста развёрнутая симптоматика развивается редко [29,30,31].
Развёрнутая клиническая картина БВ обусловлена избыточным накоплением меди в различных органах и тканях и преимущественно проявляется симптомами поражения печени, центральной нервной системы, глаз, реже почек, костей, сердца, желёз внутренней секреции.
Неврологическая симптоматика БВ манифестирует позже, чем поражение печени, в большинстве случаев на втором-третьем десятилетии жизни, но может проявляться и в детском возрасте до 10 лет [32, 33]. Наиболее часто клиническая картина включает в себя дистонию (до 69 %), атаксию (до 30 %), постурально-кинетический и интенционный тремор (до 90 %), паркинсонизм (до 62 %), сопровождающиеся на более поздних стадиях слюнотечением, дизартрией и дисфагией; реже наблюдаются хорея (16 %), атетоз (14 %), эпилепсия (6 %) и др. [3,32,89].
Дистония при БВ может затрагивать разные части тела. По мере прогрессирования болезни в случае отсутствия лечения фокальная или сегментарная форма дистонии может переходить в генерализованную [89]. Паркинсонизм при БВ характеризуется брадикинезией, ригидностью и постуральной неустойчивостью, при этом эти явления нередко имеют симметричный характер [90]. Тремор является одним из частых неврологических проявлений БВ. Тремор может быть постуральным, интенционным, отмечаться в покое или иметь все перечисленные условия возникновения (тремор Холмса) [32]. Мозжечковая атаксия наблюдается почти у 30 % пациентов с БВ [91]. Дизартрия является наиболее частым неврологическим симптомом БВ. Основываясь на преобладающей характеристике нарушения речи, можно выделить несколько типов дизартрии при БВ, включая гипокинетическую, псевдобульбарную (спастическую), гиперкинетическую (дистоническую), атактическую и смешанную [34]. Дисфагия, определяемая как затруднение в любой фазе глотания, встречается примерно у 18% пациентов с ВД и у 50% пациентов с неврологическими симптомами [34, 90]. Может быть затронута любая фаза акта глотания, включая пероральный приём, приготовление/жевание, пероральный транзит и само глотание. Дисфагия может возникнуть из-за нарушения мышечного тонуса (например, при орофациальной дистонии), нарушения координации акта глотания, медлительности и слабости мышц. Слюнотечение относится к наиболее заметным и частым симптомам БВ и наблюдается примерно у 70 % пациентов с неврологическими проявлениями заболевания. Очень часто это является следствием дисфагии и (или) неспособности удерживать слюну во рту из-за орофациальной дистонии [34].
У детей ранние неврологические признаки болезни выражаются в поведенческих нарушениях, отставании в учёбе, проблемах при выполнении заданий, требующих сочетанной координации работы рук и глаз, ухудшении мелкой моторики, изменяется почерк.
Психиатрические проявления. Наряду с поведенческими нарушениями психиатрические проявления включают расторможенное поведение, депрессию, тревожность, психотические симптомы. У детей снижается успеваемость в школе, появляется лабильное настроение, неадекватное, агрессивное поведение. У большинства пациентов с неврологической и (или) психиатрической симптоматикой БВ развивается цирроз печени, длительно протекающий бессимптомно [4,31,34].
Симптомы поражения печени при БВ весьма вариабельны. У детей поражение печени развивается раньше, чем неврологическая симптоматика. Клинический дебют БВ может быть в виде фульминантного гепатита (чаще у детей и подростков), проявляющегося коагулопатией, энцефалопатией, Кумбс-негативной гемолитической анемией, печёночной и почечной недостаточностью [3,4,31]. Иногда клинические симптомы крайне напоминают картину острого вирусного гепатита. Этот вариант заболевания без проведения трансплантации печени приводит к практически 100 %-й летальности, поэтому таких пациентов необходимо незамедлительно включать в лист ожидания трансплантации печени.
Клиническая картина хронического гепатита при БВ мало отличима от поражения печени другого генеза и без патогенетической терапии приводит к формированию цирроза, что диктует необходимость исключения БВ у всех пациентов как с острым, так и с хроническим поражением печёночной паренхимы с наличием или без признаков цирроза. Характерной чертой хронического гепатита при БВ является умеренное повышение биохимических маркеров цитолиза, холестаза и уровня билирубина с высоким уровнем структурных изменений печёночной паренхимы при морфологическом исследовании биоптатов печени. БВ может клинически протекать по типу аутоиммунного гепатита с повышением сывороточных иммуноглобулинов и неспецифических аутоантител, в связи с чем у пациентов с аутоиммунным гепатитом при неэффективности кортикостероидной терапии следует также исключать БВ [31].
Поражение органа зрения. Патогномоничным симптомом БВ являются кольца Кайзера-Флейшера — отложение меди в десцеметовой мембране роговицы. У детей с бессимптомным и лёгким печёночным течением БВ они обьино не визуализируются [39]. Кольца Кайзера-Флейшера выявляются у 95 % пациентов с неврологическими симптомами и примерно у половины больных без неврологических нарушений [3]. Для их достоверного определения необходимо проводить осмотр при помощи щелевой лампы [40,92]. Следует учесть, что кольца Кайзера-Флейшера не всегда специфичны для БВ, и могут формироваться у пациентов с хроническими холестатическими заболеваниями или при холестазе новорождённых [41,42]. К другим возможным офтальмологическим проявлениям БВ относится передняя субкапсулярная катаракта (так называемая «медная катаракта») — она тоже выявляется при осмотре при помощи щелевой лампы.
Кумбс-негативная гемолитическая анемия у пациентов с БВ может протекать как единичный острый эпизод или иметь хронический характер. В ряде случаев это может быть единственным симптомом дебюта БВ. Пациенты, у которых в анамнезе отмечалась желтуха до установления диагноза БВ, скорее всего, перенесли ранее нераспознанный гемолиз.
Во время беременности у пациенток с БВ возможно развитие острого гепатита и гемолиза, что требует дифференциальной диагностики с HELLP-синдромом.
- дисфункция почечных канальцев: урикозурия, глюкозурия, аминоацидурия, протеинурия, почечный тубулярный ацидоз [35,36];
Читайте также:
- Польза изюма и его вред. Как выбирать?
- Факторы выделяющиеся при разрушении клеток. Воспаление. Признаки воспаления. Классические признаки острого воспаления по Цельсу. Гистамин.
- Случайное введение ветеринарных препаратов
- Естественные антитела легких. Секреторный IgA легких
- Синдром Гланцманна-Риникера (Glanzmann-Riniker)
