Естественные антитела легких. Секреторный IgA легких
Добавил пользователь Владимир З. Обновлено: 28.01.2026
Высокоспецифичный тест диагностики и мониторирования H. pyloi - ассоциированного гастрита и язвенной болезни желудка и 12-перстной кишки.
Метод Вестерн-блота для определения антител к H. Pylori, в отличие от обычного ИФА, даёт дифференцированные сведения о наличии антител к целому спектру антигенов возбудителя. Это достигается электрофоретическим разделением белков экстракта H. Pylori. В результате выявляется порядка 15 антигенов (полный антиген), что значительно повышает информативность исследования.
Использующиеся в анализе антигены разделяют на три категории:
- 1 категория - перекрёстнореагирующие и неопределённые антигены;
- 2 категория - уреаза В (антиген с м.в. 66 кДа);
- 3 категория - видоспецифичные и высокоспецифичные антигены.
Данная диагностическая система прямо отличает специфические антигены от неспецифических. Поэтому вестерн-блот метод гарантирует высокую специфичность исследования.
Клинические изоляты H. Pylori можно разделить на 2 типа. Штаммы H. pylori I типа могут экспрессировать специфический вакуолизирующий цитотоксин (VacA) и цитотоксин-ассоциированный белок (CagA). Штаммы, не способные синтезировать этот белок, относят к типу II. Инфекции, вызванные агентом I типа, оказываются более патогенными, клинические симптомы включают гастрит и образование язв, возможны отдалённые последствия в виде злокачественной лимфомы и аденокарциномы желудка. Указанные белки входят в состав специфических антигенов, используемых для тестирования антител к H. Pylori методом иммуноблота, что также даёт дополнительную информацию для специалистов.
Состав используемых для выявления антител к H. Pylori специфических антигенов:
| АНТИГЕН | СПЕЦИФИЧНОСТЬ |
| CagA p120 | белок, ассоциированный с цитотоксином А, высокоспецифичен |
| VacA p95 | вакуолизирующий цитотоксин А, высокоспецифичен |
| p75 | неспецифичен |
| FSH p57 | белок жгутиковых, неспецифичен, обуславливает перекрёстную реактивность с другими бактериями, содержащими уреазу |
| Ure B p66 | тяжёлая субъединица уреазы, обуславливает перекрёстную реактивность с другими бактериями, содержащими уреазу |
| гомолог HSP p57 | гомолог белка теплового шока, неспецифичен |
| флагеллин p54 | неспецифичен, обуславливает перекрёстную реактивность с другими бактериями, содержащими флагеллин |
| p50 | неспецифичен |
| p41 | неспецифичен |
| p33 | предположительно специфичен |
| CMP p30 | Белок наружной мембраны, видоспецифичен |
| UreA p29 | лёгкая субъединица уреазы, высокоспецифичен |
| p26 | высокоспецифичен |
| CMP p19 | белок наружной мембраны, видоспецифичен |
| p17 | предположительно специфичен |
Антитела класса IgA появляются спустя некоторое время после контакта с H. Pylori. Этот тип антител (секреторные антитела), характерен больше для слизистых оболочек, где они образуются локально и обеспечивают местную защиту. IgA не всегда обнаруживаются в крови. Положительные результаты по IgA к H. Pylori хорошо коррелируют с активностью гастрита, считается, что повышенный титр IgA может выполнять роль маркёра хронической инфекции.
Специальная подготовка не требуется. Рекомендуется взятие крови не ранее чем через 4 часа после последнего приема пищи. С общими рекомендациями для подготовки к исследованиям можно ознакомиться здесь >>.
Что такое иммуноглобулины и зачем они нужны
зложена на разныеЧеловеческий иммунитет - это сложная многоступенчатая система защиты организма от вредоносного воздействия извне (вирусов, бактерий, аллергенов, грибков). Не существует одного органа, который бы отвечал за иммунную защиту. Эта функция возложена на разные органы иммунной системы: начиная с лимфатических узлов до кишечника и заканчивая белковыми веществами - иммуноглобулинами.
Общая характеристика иммуноглобулинов
Иммуноглобулины (Ig), или антитела, представляют собой гликопротеины, имеющие в своем составе центры специфического нековалентного связывания антигена, основанного на принципе комплементарности. Существуют растворимые формы иммуноглобулинов, которые и называют антителами, и мембранные формы иммуноглобулинов, составляющие основу В-клеточных рецепторов на поверхности В-лимфоцитов. Иммуноглобулины содержатся в крови и в некоторых секреторных жидкостях и вырабатываются как ответ на контакт с антигенами, например, бактериями или вирусами. Иногда иммуноглобулины продуцируются после контакта с собственными тканями организма, называемыми аутоантигенами.
Дефицит или избыток антител может быть признаком различных патологий, поэтому определение их количества в крови является важной частью при диагностике многих заболеваний. Кроме того, современные достижения в биомедицине позволяют использовать синтетические антитела в лечении некоторых заболеваний.
Структура антител
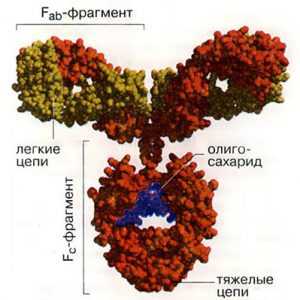
Иммуноглобулины - это симметричные Y-образные молекулы, состоящие из двух тяжелых длинных (Н) и двух коротких легких (L). цепей, которые соединены друг с другом либо дисульфидными (SS), либо водородными связями. Каждая молекула иммуноглобулина содержит не менее двух идентичных Н-цепей. Тяжелые цепи иммуноглобулинов разных классов состоят из четырех или пяти доменов и обозначаются буквами греческого алфавита соответственно латинской аббревиатуре класса. Принадлежность антитела к конкретному классу и подклассу называют изотипом, который обозначается по типу тяжелой цепи.
Легкие цепи построены из двух доменов. В их составе обязательно находится два вида доменов - вариабельный (V - variable) и константный (С-coпstaпt). Иммуноглобулины, продуцируемые разными клонами плазматических клеток, имеют разные по аминокислотной последовательности вариабельные домены. Константные домены сходны или очень близки для каждого изотипа иммуноглобулина. Вариабельные домены являются N-концевыми. В составе легкой цепи N-концевой домен является вариабельным (VL), С-концевой домен - константным (CL). Тяжелые цепи имеют один вариабельный (N-концевой) домен (Vн) и несколько константных доменов. Легкие и тяжелые цепи иммуноглобулинов гликозилированы.
Иными словами, каждое антитело подходит к антигену по принципу ключа и замка, а при соединении образуют иммунные комплексы. Но также антитела способны проявлять гибкость чужеродных агентов, благодаря чему с легкостью адаптироваться к различным антигенам. Однако эта способность иммуноглобулинов иногда провоцирует у человека перекрестные аллергические реакции - когда иммунитет человека с аллергией не может различать аллергены. Например, человек с аллергией на цветочную пыльцу вследствие “ошибки” иммуноглобулинов может также реагировать на сырые фрукты и овощи.
Разновидности иммуноглобулинов
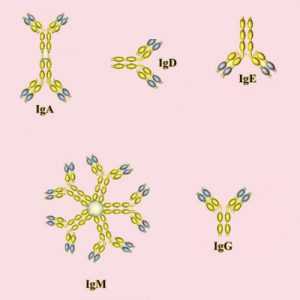
В человеческом организме иммуноглобулины представлены в двух формах:
- растворимые (продуцируются плазматическими клетками);
- связанные с наружной мембраной B-лимфоцитов, они же - рецепторные антитела.
Кроме того, существуют разные классы и подклассы (изотопы) иммуноглобулинов. Они различаются по своим биологическим особенностям, структуре и нацеленности на «мишени». На основе различий в структуре тяжелых цепей было выделено несколько классов антител. Каждый из них отличается функциями и ответными реакциями.
Кроме основных классов иммуноглобулинов существует несколько подклассов. Разница между ними основана на незначительных отличиях в типе тяжелых цепей каждого класса. В человеческом организме встречаются 4 подкласса антител. Нумерация соответствует порядку уменьшения их концентрации в сыворотке. Так, антитела IgG и IgA дополнительно группируют на подклассы IgG1, IgG2, IgG3, IgG4, а также IgA1 и IgA2.
Большинство антител (IgG, IgD, IgE) в организме представлены в форме мономера (одной молекулы). Исключение составляет антитела класса А, которые также встречается в форме димера, и IgМ, образующий форму снежинки (пентамер).
Характеристика разных классов иммуноглобулинов
Класс IgA
Около 15% антител, содержащихся в организме здорового человека, это иммуноглобулины класса IgA, которые разделяются на два подкласса IgA - IgA1 и IgA2. Они различаются молекулярной массой тяжелых цепей и концентрацией в сыворотке, где IgA представлен в основном как мономер, с молекулярной массой 160 кДа. В секреторных жидкостях иммуноглобулины присутствуют в виде димера, образованных двумя мономерами, их содержание составляет 10-15% от общего количества сывороточных иммуноглобулинов. Димерные иммуноглобулины присутствуют в большинстве секреторных жидкостей, включая слизистые оболочки дыхательных и мочеполовых путей, ЖКТ, а также слюну, слезы, молозиво и молоко у женщин. Поскольку IgA присутствует на слизистых оболочках пищеварительной системы, где он может подвергаться воздействию ферментов, в его составе есть специальный компонент, который защищает молекулу от преждевременного разрушения.
Иммуноглобулины класса A, как правило, не являются специфическими с точки зрения «подстраивания» под специфический антиген. Обычно антитела из этой группы присутствуют в уязвимых местах организма или на участках, где микробы могут легко проникнуть внутрь. Иммуноглобулины класса A обеспечивают местный гуморальный иммунитет. Это связано с их свойствами предотвращать проникновение патогенов через эпителиальные поверхности, благодаря присутствию IgA в секрете слизистых оболочек (слюна, слезы) он защищает организм от некоторых локальных инфекций.
Основная функция иммуноглобулинов этого класса состоит не в разрушении антигенов, а в предотвращении проникновения инфекционных агентов в систему кровообращения. Сами по себе IgA не способны самостоятельно разрушать бактерии, поэтому они всегда работают вместе с лизоцимами - ферментами, которые также присутствуют в секреторных жидкостях и могут разрушать бактерии.
Нарушения концентрации иммуноглобулинов класса IgA в организме способствуют его восприимчивости к инфекционным заболеваниям дыхательных путей и мочеполовой системы, в том числе нефропатии. Лица, с недостаточностью IgA, более склонны к аутоиммунным расстройствам, таким как ревматоидный артрит, волчанка, аллергия и астма.
К снижению содержания IgA могут привести разные заболевания, среди которых - гонорея. Бактерии, вызывающие гонорею, продуцируют фермент, который расщепляет IgA на две части: Fc и Fab фрагменты. Что интересно, Fab все еще может находить опасные для организма бактерии, но без взаимодействия с Fc он не способен противостоять им.
Класс IgD
Иммуноглобулины класса D в организме человека представлены в очень маленьком количестве и составляют примерно 0,2% от всех антител. Известно, что IgD прикрепляется к поверхности некоторых В-лимфоцитов как рецептор В-клеток. Тем не менее его функции в человеческом организме на сегодня до конца еще не изучены. Предполагается, что именно IgD является причиной аллергии на пенициллин, а также он может участвовать в запуске аутоиммунных реакций.
Класс IgE
Иммуноглобулин IgE в норме составляет не более 0.1% от общего количества сывороточных иммуноглобулинов. Более 90% синтезируемого плазматическими клетками IgE секретируется в слизистых экзосекретах желудочно-кишечного тракта. Биологическая функция заключается в защите от внеклеточных паразитов, хотя она полностью не выяснена, и резкое увеличение количества IgE является патогенетическим признаком при аллергических реакциях.
Иммуноглобулины этой группы связываются с поверхностью базофилов и тучных клеток. Дальше к ним присоединяется антиген, что в свою очередь ведет к выбросу в кровоток вазоактивных аминов и развитию IgE-зависимой аллергической реакции по следующему механизму.
Различные антигены, такие как пыльца, ядовитые вещества, споры грибов, пылевые клещи или перхоть домашних животных связываются с IgE и запускают высвобождение гепарина, гистамина, протеолитических ферментов, лейкотриенов и цитокинов. Это ведет к расширению сосудов и повышению их проницаемости, что способствует проникновению чужеродных агентов в капилляры, а затем и в ближайшие ткани, вследствие чего развиваются характерные для аллергической реакции симптомы. Однако, большинство типичных аллергических реакций в виде чихания, кашля, слезотечения и повышенного выделения слизи способствует выведению из организма оставшихся аллергенов.
Исследования показали, что такие расстройства, как астма, ринит, экзема, крапивница и дерматит вызывают повышение уровня IgE. Антитела Е-типа также активно продуцируются в ответ на присутствие в организме гельминтов, персистирующих инфекций (герпесвирусы, атипичные микроорганизмы) и некоторых членистоногих (например, вшей). Кроме того, IgE играет косвенную роль в иммунном ответе, стимулируя другие иммунные компоненты. Также он может защищать поверхности слизистых оболочек, вызывая, в случае опасности, воспалительные реакции.
Патологически низкий уровень антител класса IgE может возникать на фоне редкого генетического заболевания, сопровождающегося нарушением координации мышц (атаксия телеангиэктазия).
Класс IgG
Иммуноглобулины класса G являются доминирующими в человеческом организме. На их долю приходится 75% всех антител. Частично это связано с длительным периодом полураспада: от 7 до 23 дней (зависимо от подкласса). Кроме того, они могут сохраняться в крови в течение нескольких десятков лет после контакта с антигеном.
Существуют 4 подкласса IgG:
- IgG1 составляет от 60 до 65% от общего количества иммуноглобулина этого класса. Его дефицит обычно является признаком гипогаммаглобулинемии (дефицит плазматических клеток).
- IgG2 - второй по распространенности изотоп, составляет 20-25% от общего количества IgG. «Взрослые» концентрации антитела обычно появляются к 6-7-летнему возрасту. Дефицит IgG2 связывают с рецидивирующими инфекциями дыхательных путей.
- IgG3 занимает от 5 до 10% от общего IgG. Играет основную роль в иммунных реакциях против белковых или полипептидных антигенов.
- IgG4 составляет до 4% в общей доле IgG. Раньше IgG4 связывали только с пищевой аллергией, но недавние исследования показали, что повышение IgG4 в сыворотке отмечается у пациентов, страдающих склерозирующим панкреатитом, холангитом и интерстициальной пневмонией. Тем не менее точная роль IgG4 до сих пор неизвестна.
IgG играет ключевую роль в гуморальном иммунном ответе. Это основной иммуноглобулин, содержащийся в крови, а также в лимфатической, спинномозговой и брюшной жидкостях. Способность оставаться в организме в течение длительного времени делает его наиболее полезным антителом для пассивной иммунизации. Это единственное антитело, способное проникать через плаценту матери и попадать в кровообращение плода, обеспечивая послеродовую защиту новорожденного в течение первых месяцев его жизни.
Главные функции IgG:
- усиление фагоцитоза в макрофагах и нейтрофилах;
- нейтрализация токсинов;
- инактивация вирусов;
- уничтожение бактерий.
Класс IgM
IgM - это самый важный представитель семейства человеческих иммуноглобулинов, хотя он и отличается весьма коротким периодом полураспада - около 5 дней.
Иммуноглобулины класса IgM в общей доле сывороточных антител в человеческом организме составляют примерно 10-13%. Они участвуют в первичных иммунных реакциях и обладает выраженной антибактериальной активностью, способностью связывать комплемент, не проникают через плацентарный барьер. Первыми синтезируются в ответ на антигенную стимуляцию организма. Наиболее ранние антитела относятся к иммуноглобулинам класса М, что нередко используется в диагностике инфекционных заболеваний. Они же первыми появляются в процессе онтогенеза и филогенеза.
Повышение уровня IgM можно расценивать как признак недавно перенесенной инфекции или присутствия в организме антигена. На мембране В-лимфоцитов присутствует мономерная форма IgM, выполняющая функцию основной составляющей В-клеточного рецептора.
Роль иммуноглобулинов в организме
Антитела являются частью гуморального иммунного ответа и действуют очень специфично, так как всегда направлены против определенного антигена.
Задача любого антитела в организме человека - участвовать в иммунных реакциях. Иммуноглобулины обладают способностью образовывать иммунные комплексы с молекулами антигена, активировать систему комплемента (комплекс белков, содержащихся в крови, необходимых для защиты организма от чужеродных агентов) и вызывать воспаления. Все эти действия направлены на нейтрализацию антигена и безопасное удаление его из организма.
Вследствие различных структурных свойств разные классы антител могут выполнять специализированные функции:
- нейтрализовать паразитов (IgE);
- нейтрализовать микроорганизмы (IgM, IgG);
- защищать от повторных заболеваний, таких как эпидемический паротит (IgG);
- защищать слизистые оболочки (IgA);
- участвовать в синтезе лимфоцитов (IgD);
- защищать плод (IgG) и новорожденного малыша (IgA).
Антитела и иммунологическая память
Иммунный ответ делится на первичный и вторичный. Первичный ответ проявляется во время первого контакта с антигеном, после чего организм сначала вырабатывает иммуноглобулины класса IgM, которые затем замещаются более специфическими и стабильными антителами IgG.
Вторичный иммунный ответ возникает при повторном контакте с тем же антигеном. Он интенсивнее первичного, концентрация антител достигает более высоких уровней, чем в первый раз.
Такой эффект обусловлен иммунологической памятью, которая опосредована В-имфоцитами. Это долгоживущие клетки которые вступают в контакт с антигеном, начинают очень интенсивно делиться и продуцировать специфические антитела.
Как определяется количество антител
Антитела составляют от 12% до 18% сывороточных белков. Количества отдельных белковых фракций, в лабораторных условиях определяется на основании протеинограмм.
Тест на антитела методом иммуноферментного анализа (ИФА), как правило, проводится с венозной кровью (позволяет определить количество иммуноглобулинов класса IgM, IgG, IgE, IgA). Кроме того, определить количество антитела класса IgA можно путем биохимического исследования слюны или кала человека - методом полимеразной цепной реакции (ПЦР). В отдельных ситуациях тест может быть проведен с использованием другого материала, например спинномозговой жидкости.
Если в крови пациента диагностировано критическое повышение некоторых иммуноглобулинов, говорят о гипергаммаглобулинемии. Как правило, у таких пациентов чрезмерно повышаются антитела класса IgM, при этом остальные остаются в дефиците.
На фоне патологического повышения некоторых антител могут развиваться разные заболевания, в том числе:
- острые и хронические воспаления;
- паразитарные, бактериальные, вирусные или грибковые заболевания;
- аутоиммунные болезни;
- цирроз печени;
- саркоидоз; .
Патологически низкое количество антител в сыворотке может возникать на фоне:
- врожденных генетически расстройств;
- приема некоторых противомалярийных, цитостатических, глюкокортикоидных препаратов;
- недоедания;
- инфекции, в том числе ВИЧ;
- онкологических заболеваний;
- нефротического синдрома;
- обширных ожогов;
- тяжелой диареи.
Иммуноглобулины и вакцинация
Антитела играют ключевую роль в развитии иммунитета после вакцинации. В результате контакта с антигеном, содержащимся в вакцине, иммунная система вырабатывает антитела. Сначала менее стойкий и специфический IgM, а затем более стойкий IgG. Например, во время вакцинации против вируса гепатита В, вакцину вводят трижды с определенным интервалом между прививками. Это позволяет создать стойкий иммунитет к болезни. Эффективность такой вакцинации определяется изменением в организме количества антител IgG.
Антитела в медицине
Благодаря развитию биохимии, молекулярной биологии и медицины, в наше время стало возможным синтезировать иммуноглобулины в лабораторных условиях (как правило, антитела класса IgG). Такие антитела называются моноклональными, так как они происходят из клона одной клетки и работают против определенного антигена.
Сегодня моноклональные иммуноглобулины используют для лечения разных заболеваний. Впервые эта методика была применена в 1981 году для лечения лимфомы. А уже в 1984 году изобретатели моноклональных антигенов - немецкий биолог Георг Келер и британский иммунолог Сезар Мильштейн - получили Нобелевскую премию.
В современной медицине моноклональные антитела применяют для:
- уничтожения раковых клеток;
- ингибирования отдельных клеток иммунной системы после трансплантации органов (позволяет предотвратить отторжение пересаженного органа);
- подавления иммунных реакций при аутоиммунных заболеваниях.
Иммунный ответ на каждый отдельный антиген включает продукцию множества молекул антител, синтезируемых разными плазматическими клетками, и имеющих разное строение активного центра и изотип. Вследствие различий в строении активных центров образующиеся антитела имеют различную специфичность и аффинность.
Специальность: врач педиатр, инфекционист, аллерголог-иммунолог .
Секреторные иммуноглобулины А - «главная скрипка» мукозального иммунитета
В полости рта и ротоглотке наибольшее протективное значение имеют sIgA слюны, а в носовых ходах и носоглотке - sIgA назального секрета 2 .
Доминирующим изотипом иммуноглобулинов (Ig) на поверхности слизистых оболочек дыхательных путей и ротоглотки является секреторный IgA (sIgA), который по праву называют «главной скрипкой» мукозального адаптивного иммунитета.
Доминирование секреторного иммуноглобулина А среди других антител в слизистой оболочке дыхательных путей и ротоглотки
В полости рта и ротоглотке наибольшее протективное значение имеют sIgA слюны, а в носовых ходах и носоглотке - sIgA назального секрета. Помогают этим антителам в нейтрализации вирусов и бактерий секреторные IgM (sIgM), но их защитное значение существенно ниже 2 .
Помимо sIgA и sIgM, в верхних отделах дыхательных путей и ротоглотке обнаруживаются в небольших количествах и все другие известные изотипы Ig. Появление IgG и мономерного («сывороточного») IgA в слюне и назальном секрете обусловлено транссудацией этих молекул из плазмы крови. При патологических (например, воспалительных) процессах увеличивается транссудация IgG, мономерного IgA и более крупных полимерных молекул IgM. В секретах слизистых оболочек дыхательных путей выявляют еще и IgD, который тоже участвует в противоинфекционном ответе 3 .
ОСОБЕННОСТИ ВЫРАБОТКИ СЕКРЕТОРНЫХ ИММУНОГЛОБУЛИНОВ А И М
Вначале плазматические клетки слизистых оболочек синтезируют димерный IgA, в котором два мономера IgA соединены между собой J-цепью. После этого димерный IgA захватывается рецептором к полимерным иммуноглобулинам на базальной поверхности эпителиальных клеток и подвергаются транспорту к апикальной поверхности эпителиоцитов. Здесь происходит распад транспортирующего рецептора, в результате которого внеклеточная часть этого рецептора (так называемый «секреторный компонент») остается связанной с димерным IgA, который высвобождается в окружающую среду (слюну, слизь, другие биологические жидкости). Именно такой димерный IgA, связанный с секреторным компонентом, называют sIgA 2 .
Как уже упоминалось, существуют еще и секреторный IgM (sIgM). Выработка sIgM напоминает таковую sIgA. Все начинается с синтеза плазматическими клетками в слизистой оболочке пентамерного IgM, который захватывается рецептором к полимерным иммуноглобулинам на базальной поверхности эпителиальных клеток и подвергаются трансэпителиальному транспорту. На апикальной поверхности эпителиоцитов пентамерный IgM вместе с секреторным компонентом высвобождается во внешнюю среду, превращаясь в sIgM 3 .
Секреторные компоненты в составе sIgA и sIgM стабилизируют соответственно димерную или пентамерную структуру этих Ig и обеспечивают их длительное функционирование в биологических жидкостях 3 .
ГДЕ ПРОИСХОДИТ ИНДУКЦИЯ ВЫРАБОТКИ СЕКРЕТОРНОГО ИММУНОГЛОБУЛИНА А В СЛЮНЕ И НАЗАЛЬНОМ СЕКРЕТЕ?
Появление sIgA в слюне и назальном секрете происходит как следствие первичного контакта с антигенами патогенов в разных индуктивных зонах в верхних отделах респираторного и пищеварительного трактов. Главными индуктивными зонами при этом являются небные и носоглоточные миндалины, а также протоки слюнных (особенно малых, поднижечелюстных и подъязычных) желез, открытые для прямого воздействия антигенов. К индуктивным зонам относятся и другие участки слизистой оболочки полости рта, глотки, верхних и нижних дыхательных путей.
Все перечисленные индуктивные зоны доступны для стимулирующего действия топических бактериальных лизатов ИРС®19 и Имудон® 1 .
Еще одной индуктивной зоной, антигенная стимуляция которой может привести к выработке антител в слюне и дыхательных путях, является лимфоидная ткань, ассоциированная с кишечником (Gut-Associated Lymphoid Tissue - GALT). Эта зона также доступна для действия топических бактериальных лизатов, компоненты которых неминуемо попадают в желудочно-кишечный тракт в результате проглатывания 1 .
Важно то, что топические бактериальные лизаты ИРС®19 и Имудон® при курсовом применении не только индуцируют начальные этапы созревания В-лимфоцитов, получивших антигенную информацию, но и способствуют выработке эндогенного интерферона, а также обеспечивают сигналы хемотаксиса, привлекающие созревающие антитело-продуцирующие клетки из системной циркуляции в верхние отделы респираторного тракта и ротоглотку. В результате ИРС®19 и Имудон® существенно увеличивают выработку sIgA в зонах их введения в организм пациента 1 .
При раннем назначении топических бактериальных лизатов адаптивные антибактериальные механизмы (локальная продукция sIgA) включаются как раз тогда (4-5-е сутки), когда наиболее высок риск развития вторичной бактериальной инфекции 1 .
Таким образом, ИРС®19 и Имудон® не только предотвращают развитие вторичных бактериальных осложнений вирусной инфекции, но и неспецифически усиливают противовирусную и антибактериальную защиту уже в первые часы терапевтического применения. Препараты обладают целым рядом фармакологических свойств, которые принципиально отличают их от иммуностимуляторов с системным действием, связанных со сложными маршрутами миграции иммунокомпетентных клеток. ИРС®19 и Имудон® действуют нацелено на стимуляцию противоинфекционной защиты в месте их первичного введения в организм т.е. во входных воротах для болезнетворных вирусов и бактерий и арене ключевых патогенетических событий 1 .
Подробнее
Материал разработан при поддержке компании Abbott в целях повышения осведомлённости пациентов о состоянии здоровья. информация в материале не заменяет консультацию специалиста здравоохранения. Обратитесь к лечащему врачу.
Иммуноглобулины класса A (IgA)
Сывороточный IgA синтезируется В-лимфоцитами (плазмоцитами); является фракцией гамма-глобулинов и cоставляет 10 - 15% всех классов растворимых иммуноглобулинов. Мономерная молекула состоит из двух тяжёлых и двух лёгких цепей. В сыворотке 90% IgA представлено мономерными молекулами. IgA большей частью присутствует не в сыворотке, а на поверхности слизистых оболочек, содержится в молоке, молозиве, слюне, в слёзном, бронхиальном и желудочно-кишечном секрете, желчи, моче.
Период полувыведения антител этого класса составляет 4 - 5 суток. Секреторный компонент делает IgA резистентным к перевариванию протеолитическими ферментами, в связи с чем он может функционировать на различных слизистых поверхностях, богатых этими ферментами.
Основной функцией сывороточного IgA является нейтрализация вирусов. Его главная роль - защита дыхательных, мочеполовых путей и желудочно-кишечного тракта от инфекции. Секреторные антитела обладают выраженным антиадсорбционным действием: они препятствуют прикреплению бактерий к поверхности эпителиальных клеток, предотвращают адгезию, без которой бактериальное повреждение клетки становится невозможным. Вместе с неспецифическими факторами они обеспечивают защиту слизистых оболочек от микробов и вирусов. IgA не проходит через плацентарный барьер, уровень его у новорожденных около 1% от концентрации у взрослых (к году жизни этот показатель составляет всего 20% от уровня взрослых). Поэтому новорожденным в первые дни жизни секреторные IgA поступают с молозивом матери, защищая их дыхательные пути и желудочно-кишечный тракт до тех пор, пока не сформируются механизмы его синтеза в собственном организме. Возраст 3 мес. многими авторами определяется как критический период; этот период особенно важен для диагностики врождённой или транзиторной недостаточности местного иммунитета. Уровня, характерного для взрослого человека, достигает примерно к 5-летнему возрасту.
Накануне исследования необходимо исключить повышенные психоэмоциональные и физические нагрузки (спортивные тренировки), приём алкоголя.
- Рецидивирующие бактериальные респираторные инфекции (синуситы, пневмонии), а также отиты и менингиты, бронхиальная астма.
- Хроническая диарея, синдром мальабсорбции.
- Анафилактические посттранфузионные реакции.
- Синдром Луи-Бара (атаксия - телеангиэктазия).
- Опухолевые заболевания лимфоидной системы (миелома, лейкозы, лимфомы, ретикулосаркомы).
- Диффузные заболевания соединительной ткани (ревматоидный артрит, системная красная волчанка, дерматомиозит).
- Хронический гепатит, цирроз печени.
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Свободные легкие цепи иммуноглобулинов каппа и лямбда сыворотки с расчетом индекса каппа/лямбда (Serum immunoglobu-lin free light chains (FLC, sFLC) kappa and lambda, kappa/ lambda ratio)
Синонимы: Анализ крови на легкие цепи иммуноглобулинов; Свободные κ и λ цепи иммуноглобулинов в крови; Свободные легкие цепи иммуноглобулинов в крови.
Краткое описание исследования «Свободные легкие цепи иммуноглобулинов каппа и лямбда сыворотки с расчетом индекса каппа/лямбда»
Иммуноглобулины (антитела) продуцируются лимфоцитами и плазматическими клетками. Структурная единица любого иммуноглобулина включает две идентичные тяжелые и две идентичные легкие цепи белка. Различают два типа легких цепей: каппа и лямбда. Индивидуальный В-лимфоцит может продуцировать либо каппа, либо лямбда легкие цепи (но не оба типа одновременно).
При синтезе антител легкие цепи продуцируются в избытке и присутствуют в сыворотке не только в составе полных молекул иммуноглобулинов, но и в виде свободных легких цепей. Концентрация их в сыворотке зависит от баланса продукции ивыведения.
Выводятся свободные легкие цепи из крови почками: проходят через клубочковый фильтр, после чего, в отсутствие гиперпродукции и при сохранной функции проксимальных отделов почек, практически полностью реабсорбируются и подвергаются метаболизму в проксимальных канальцах.
С какой целью определяют Свободные легкие цепи иммуноглобулинов каппа и лямбда сыворотки с расчетом индекса каппа/лямбда
Оценку уровня свободных легких цепей в сыворотке крови используют в целях диагностики и контроля течения миелом, первичного амилоидоза и других видов патологий, сопровождающихся моноклональной пролиферацией плазматических клеток.
Что может повлиять на результаты исследования «Свободные легкие цепи иммуноглобулинов каппа и лямбда сыворотки с расчетом индекса каппа/лямбда»
Миеломная трансформация плазматических клеток сопровождается избыточной пролиферацией лимфоцитов одного клона, синтезирующих однородный (моноклональный) иммуноглобулин или его фрагменты. В результате повышается концентрация вовлеченного типа легкой цепи и меняется соотношение каппа/лямбда в сыворотке, что позволяет использовать этот феномен для диагностики плазмоклеточных заболеваний. Среди пациентов с множественной миеломой разных типов изменение индекса каппа/лямбда свободных легких цепей в сыворотке отмечается в 60-70% случаев заболевания.
При заболеваниях, сопровождающихся поликлональным повышением продукции иммуноглобулинов (инфекции, воспаление), а также при нарушении функции почек можно наблюдать повышение уровня легких цепей в сыворотке (вплоть до 30-40-кратного прироста), однако соотношение каппа/лямбда цепей остается прежним или меняется незначительно.
Свободные легкие цепи имеют короткий период полувыведения из крови (для цепей типа каппа - 2-4 часа, лямбда - 3-6 часов), поэтому снижение их уровня в сыворотке при серийном определении можно использовать в качестве раннего маркера ответа на терапию. Примерно у 20% пациентов с множественной миеломой секретируемый моноклональный белок представлен только легкими цепями иммуноглобулинов.
Исследование концентрации свободных легких цепей в сыворотке ценно не только для диагностики, но и для контроля терапии этой патологии, в том числе у пациентов с почечной недостаточностью.
Моноклональная продукция свободных легких цепей является преобладающей причиной поражений почек, ассоциированных с множественной миеломой и родственными видами моноклональных гаммапатий. Одним из проявлений может стать острое поражение почек, связанное с агрегацией свободных легких цепей и белка Тамма-Хорсфалла и формированием цилиндров в дистальных канальцах (миеломная почка). Оценку уровня свободных легких цепей в сыворотке можно использовать в целях ранней диагностики этого состояния.
Правила подготовки к анализу крови «Свободные легкие цепи иммуноглобулинов каппа и лямбда сыворотки с расчетом индекса каппа/лямбда»
В каких случаях выполняют тест «Свободные легкие цепи иммуноглобулинов каппа и лямбда сыворотки с расчетом индекса каппа/лямбда»:
- первичный скрининг при подозрении на моноклональную гаммапатию, в дополнение к электрофорезу сыворотки и электрофорезу с иммунофиксацией (тест можно применять вместо электрофореза с иммунофиксацией 24-часовой мочи при различных клинических целях первичного скрининга, кроме диагностики AL-амилоидоза);
- обследование в целях прогноза, оценки рисков, мониторинга пациентов с диагностированной множественной миеломой, солитарной плазмоцитомой, тлеющей/вялотекущей миеломой, несекретирующей миеломой, моноклональной гаммапатией неопределенного значения, AL-амилоидозом;
- скрининг для выявления нефротоксичного уровня свободных легких цепей в целях ранней диагностики миеломной почки.
Трактовка результатов исследования «Свободные легкие цепи иммуноглобулинов каппа и лямбда сыворотки с расчетом индекса каппа/лямбда»
Полученные результаты следует интерпретировать в комплексе с клиническими данными и результатами других тестов, в том числе рутинного электрофореза сыворотки и электрофореза с иммунофиксацией.
Если показатели концентрации каппа и лямбда свободных легких цепей иммуноглобулинов и каппа/лямбда индекса не выходят за пределы референсных значений, при электрофорезе белков сыворотки парапротеинов не выявлено, то наличие моноклональной гаммапатии маловероятно.
Аномальный каппа/лямбда индекс в комплексе с повышением уровня каппа или лямбда легких свободных цепей свидетельствует о вероятности моноклональной гаммапатии и требует дальнейших исследований, хотя небольшие отклонения следует интерпретировать с осторожностью. Пограничные отклонения каппа/лямбда индекса можно иногда наблюдать у пациентов с поликлональным повышением уровня свободных легких цепей (в частности, у пациентов с нарушением функции почек или пациентов с гипергаммаглобулинемией, обусловленной, например, инфекциями или воспалительным процессом).
Международная группа по изучению миеломы (International Myeloma Working Group, IMWG) утвердила применение соотношения концентрации разных типов свободных легких цепей в сыворотке в качестве одного из маркеров активной множественной миеломы. Критерием предложено считать 100-кратное преобладание концентрации одного из типов свободных легких цепей, т. е. индекс каппа/лямбда менее 0,01 или более 100 (при условии, что абсолютная концентрация в сыворотке вовлеченного типа свободных легких цепей составляет не менее 100 мкг/мл). Содержание свободных легких цепей второго типа при этом обычно находится в пределах нормы или ниже.
При моноклональной гаммапатии невыясненного значения выраженное нарушение соотношения свободных легких цепей свидетельствует о высоком риске миеломной трансформации. Выраженное изменение каппа/лямбда индекса отмечается также при солитарной и несекретирующей миеломе, первичном амилоидозе с поражением внутренних органов, парапротеинемических полиневритах, парапротеинемиях с поражением почек.
На фоне эффективной терапии миеломы наблюдается нормализация индекса каппа/ лямбда сыворотки (благоприятный прогностический признак), возрастание концентрации моноклональных свободных легких цепей указывает на рецидив заболевания.
У пациентов с миеломной почкой обычно отмечается концентрация свободных легких цепей сыворотки выше 500 мкг/мл (этот уровень связывают с вероятностью цилиндровой нефропатии).
Читайте также:
