КТ, МРТ при лимфатической мальформации головы и шеи
Добавил пользователь Алексей Ф. Обновлено: 28.01.2026
- Стадия I: Поражение лимфатических узлов одной группы или одного экстранодального органа.
- Стадия II: Поражение лимфатических узлов 2 и более групп или одного экстранодального органа и более одной группы лимфатических узлов по одну сторону диафрагмы.
- Стадия III: Поражение лимфатических узлов по обе стороны диафрагмы, с поражением или без поражения селезенки или экстранодального органа.
- Стадия IV: Диссеминированное поражение одного и более экстранодального органа с поражением или без поражения лимфатических узлов.
Клинические проявления
Типичные симптомы лимфомы лимфоузлов:
- Множественные, обычно двусторонние безболезненные объемные образования в области шеи
- Потливость по ночам
- Повышение температуры тела
- Потеря веса
- Иногда лимфома имеет симптомы кожного заболевания
- Зуд
Какой метод диагностики лимфомы лимфоузлов выбрать: МРТ, КТ, УЗИ, ангиографию
Методы выбора
Для чего проводят УЗИ шеи при лимфоме лимфоузлов
- Увеличение размеров и количества лимфатических узлов
- Обычно имеют сферическую форму
- Очень низкая эхогенность
- Часто отсутствует эхо-сигнал от ворот
- Четко очерченные края
- При дуплексном УЗИ выявляется значительное повышение васкуляризации с наличием разветвленной сосудистой сети в узлах
- Высокий индекс резистентности внутри лимфатических узлов (ИР <0,8).
Информативна ли МСКТ лимфоузлов с контрастом при лимфоме шеи
- Пораженные лимфатические узлы имеют плотность, идентичную мышцам
- Склонны к образованию конгломератов
- Лимфатические узлы обычно имеют гомогенную плотность
- При лимфоме Ходжкина может быть снижена плотность в центре узлов, что свидетельствует о некрозе
- Минимальное усиление после введения контрастного вещества
- Иногда при неходжкинской лимфоме наблюдается интенсивное усиление
- Кальцинаты обычно не образуются до окончания терапии.
Что покажут снимки МРТ шеи с контрастом при лимфоме лимфоузлов
- Пораженные лимфатические узлы изоинтенсивны по отношению к мышцам на Т1 -взвешенном изображении и гиперинтенсивны - на Т2-взвешенном изображении и в последовательности STIR
- Как и при КТ, обычно наблюдается гомогенное усиление после введения контрастного вещества
- В случае некроза в центре узла при лимфоме Ходжкина выявляется высокая интенсивность сигнала на Т2-взвешенном изображении и очень низкая — на Т1 -взвешенном изображении
- Наблюдается высокая интенсивность сигнала от пораженных узлов на Т2-взвешенном изображении после введения USPIO.
Отличительные признаки лимфомы
- Увеличение количества и размеров лимфатических узлов
- Соотношение продольного размера к поперечному
- Часто двусторонние конгломераты лимфатических узлов
- При лимфоме Ходжкина обычно имеют равномерную плотность и интенсивность сигнала
- При неходжкинских лимфомах в центре некоторых лимфатических узлов наблюдается некроз
- лимфома Ходжкина и неходжкинские лимфомы невозможно отличить друг от друга только на основании данных методов визуализации
- В случае неходжкинских лимфом чаще происходит генерализация процесса, в то время как лимфома Ходжкина носит более локализованный характер.
Что хотел бы знать лечащий врач
- Наличие экстранодального поражения
- Какие группы лимфатических узлов поражены?
- Изменения сосудов и нервов.
Какие патологии имеют симптомы, схожие с лимфомой лимфоузлов
Саркоидоз
- В некоторых случаях наблюдается диффузное увеличение шейных лимфатических узлов
- Обычно сочетается с увеличением лимфатических узлов средостения и корней легких
- В ряде случаев образуются крупные кальцинаты
Метастазы
- Пораженные узлы расположены в зоне лимфооттока от основной опухоли
- В центре крупных лимфатических узлов обычно выявляется зона некроза
Шейный лимфаденит
- Проявления инфекционного заболевания
- Болезненная припухлость лимфатических узлов
- Возможно образование полости в центре узлов
Лечение
- Лимфома имеет лечение, которое зависит от стадии процесса, клеточного типа поражения и возраста пациента
- При неходжкинских лимфомах или лимфоме Ходжкина низкой степени злокачественности в группе благоприятного прогноза обычно достаточно только лучевой терапии
- В группе промежуточного прогноза или при неходжкинских лимфомах высокой степени злокачественности применяют химио- и лучевую терапию
- При лимфоме Ходжкина в группе неблагоприятного прогноза показана комбинированная химиотерапия
- В случае рецидива лимфомы Ходжкина требуется пересадка костного мозга или стволовых клеток.
Врачи каких специальностей диагностируют и лечат лимфому лимфоузлов
- Радиолог (лучевая терапия)
- Гематолог (контроль показателей крови, подбор лечения)
Прогноз лимфомы
- Излечение наступает в 50-90% случаев, в зависимости от группы прогноза
Неходжкинские лимфомы низкой степени злокачественности:
- Медленное прогрессирование
- Обычно наступает генерализованная стадия, которая не поддается лечению
- Продолжительность жизни - 2-10 лет
- При локализованной стадии излечение наступает в 50% случаев.
Неходжкинские лимфомы высокой степени злокачественности:
- Быстрое прогрессирование
- Локализованный процесс в 10-15% случаев, генерализованный - в 85-90% случаев
- В отсутствие лечения - продолжительность жизни небольшая
- При адекватной терапии примерно в 50% случаев наступает излечение.
Лимфома 4 стадии имеет неблагоприятный прогноз, если уровень ЛДГ и микроглобулинапривышен в 1,5 раза.
Возможные осложнения и последствия лимфомы
- Повышен риск развития вторичных опухолей, развивающихся после применения химио- и лучевой терапии.
- Выпадение волос
- Кардиомиопатия
- Увеличение масся тела
- Бесплодие у мужчин
Осложнения лучевой терапии:
- Гипотериоз
- Сухость во рту
- Лучевой пневмонит
- Лучевой колит
- Лучевой цистит
Осложнения вследствие заболевания
- Сдавление рядом прилегающий тканей за счет увеличенных лимфоузлов
- Поражение костного мозга, спинного и головного мозга, печени, костей
- Интоксикация вследствие распада опухолевых клеток
- Инфекционные осложнения
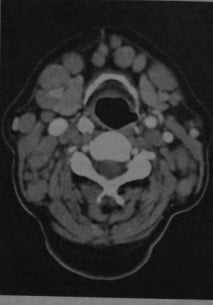
Лимфома шеи у женщины с хроническим лимфолейкозом. КТ с контрастированием: выраженное увеличение размеров и количества шейных лимфатических узлов, особенно в переднем и боковом треугольниках шеи. Плотность лимфатических узлов соответствует окружающим мышцам или выше.
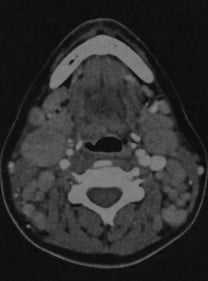
Неходжкинская лимфома. КТ с контрастированием: множественные лимфатические узлы под нижней челюстью и около яремной вены, а также позади грудино-ключично-сосцевидной мышцы. Узлы имеют овальную или округлую форму, повышенную плотность по сравнению с окружающими мышцами, после введения контраста наблюдается гомогенное усиление.
КТ, МРТ при лимфатической мальформации головы и шеи
Лимфатическая мальформация является пороком развития лимфатических сосудов, который начинает формироваться на втором месяце внутриутробного развития. В настоящее время доказано отсутствие признаков опухоли у данного образования. Термин «лимфангиома» рекомендовано оставить для истинных доброкачественных опухолей лимфатических сосудов. Лимфатическая мальформация составляет 6-18% от доброкачественных образований у детей [I] . Пороки развития лимфатических сосудов в области головы и шеи чаще всего определяются при рождении или в первые годы жизни ребёнка (в возрасте до одного года в 60-80% случаев) [2] -->.
В классификации Международного общества по изучению сосудистых мальформаций (ISSVA, 2014 год) лимфатические мальформации отнесены к простым порокам развития сосудов.
Оригинальная классификация лимфатических мальформаций ISSVA и её русский перевод, выполненный врачами нашего отделения.
В челюстно-лицевой области, на шее встречаются кистозные формы лимфатических мальформаций, которые подразделяются на мелкокистозные (при наличии полостей менее 1 см в диаметре), крупнокистозные (при наличии полостей более 1 см в диаметре) и смешанные (при наличии полостей разного диаметра).
Микрофотография и УЗИ мелкокистозной формы лимфатической мальформации (по классификации ISSVA 2014 года). МРТ и УЗИ крупнокистозной формы лимфатической мальформации (по классификации ISSVA 2014 года). МРТ и УЗИ смешанной формы лимфатической мальформации (по классификации ISSVA 2014 года).
Лимфатические мальформации могут быть как ограниченными, так и распространёнными, занимая две и более области. В области языка, верхней губы, лба чаще всего встречается мелкокистозная форма мальформации, в орбитальной, околоушно-жевательной — смешанная форма порока развития лимфатических сосудов, на шее — крупнокистозная лимфатическая мальформация. Обширная лимфатическая мальформация чаще всего локализуется в области дна полости рта, распространяясь на клетчаточные пространства глотки, гортани и средостения.
Лимфатическая мальформация является потенциально опасным образованием для человека. Пороки развития лимфатических сосудов в области головы и шеи, диагностируемые внутриутробно, обычно имеют огромные размеры, тем самым создают угрозу жизни как матери, так и ребёнка. Эти образования могут блокировать ход плода по родовым путям матери, сдавливать и смещать соседние органы и ткани, тем самым приводя к гипоксии и ишемии этих органов. Распространённые образования, локализующиеся в области дна полости рта, могут приводить к нарушению дыхания, в отдельных случаях до полной асфиксии, невозможности самостоятельного приёма пищи. Лимфатическая мальформация в орбитальной области способствует развитию нарушения зрения у пациента.
Наиболее частым осложнением у больных с данной патологией является воспаление лимфатической мальформации, спровоцированное любым воспалительным процессом (ОРВИ, тонзиллит, отит, аденоидит, стоматит, и т.д.). В результате воспаления патологические ткани увеличиваются в объёме, что приводит к увеличению асимметрии лица и шеи, перекрытию дыхательных путей, нарушению приёма пищи, речи. Мелкокистозные образования в полости рта и конъюнктивы глаз могут кровоточить. При локализации патологических тканей в области орбиты возможно развитие выраженного экзофтальма. Всё это приводит к косметическим, функциональным нарушениям, а также состояниям, угрожающим жизни ребёнка. Воспаление лимфатической мальформации требует неотложного лечения, включающего в себя антибактериальную (антибактериальные препараты широкого спектра действия), противовоспалительную (нестероидные противовоспалительные препараты в соответствии с возрастом ребёнка) терапии.
Диагностика
Фиброларингоскопия
(фото гортаноглотки).
Основными методами визуализации лимфатической мальформации являются ультразвуковое исследование (УЗИ) и магнитно-резонансная томография (МРТ). [II] Данные исследования позволяют определить площадь и объём патологических тканей, размеры кист, топографию образования. При лимфатической мальформации распространённого характера, кроме УЗИ и МРТ, необходимо проведение фиброларингоскопии, компьютерной томографии.
Лечение
Ведущим методом лечения лимфатических мальформаций является хирургический. [III] Помимо него применяется склерозирующая терапия растворами доксициклина, блеомицина, пицибанила (ОК-432), этоксисклерола и комбинированная методика, сочетающая хирургию и склерозирование. [IV] Операции проводятся по жизненным, функциональным и косметическим показаниям. К жизненным показаниям относятся нарушения дыхания и приёма пищи, что обычно бывает у детей с обширными формами лимфатических мальформаций. Стоит отметить, что дети данной группы нуждаются в многоэтапных сложных операциях, целью которых является максимально возможное удаление патологических тканей с сохранением функции и эстетики тканей. К функциональным относятся нарушения жевания, звукопроизношения, зрения. Часто к нарушению функции могут приводить рецидивирующие воспалительные процессы в патологических тканях. Косметические показания определяются при наличии асимметрии лица и шеи, увеличении объёма тканей в той или иной области.
Таким образом, лимфатические мальформации в области головы и шеи являются тяжёлым пороком развития лимфатических сосудов, при котором требуется лечение и динамическое наблюдение у специалистов: челюстно-лицевого хирурга, торакального хирурга, оториноларинголога, педиатра, ортодонта.
↑I. В связи с тем, что ранее данные образования относились к опухолям, статистические данные берутся из раздела «новообразования» (прим. авт.).
1. Исаков Ю. Ф. Детская хирургия. / Исаков Ю. Ф., Долецкий С. Я. // Москва, Медицина, 1978. — 502 с.
2. Coffin C. M. Vascular tumors in children and adolescents: a clinicopathologic study of 228 tumors in 222 patients. / Coffin C. M., Dehner L. P. // Pathol. ann. — 1993. — № 23. — Part. 1. — Р. 97-120
1. Возможности лечения детей с обширными лимфатическими и лимфовенозными мальформациями в области головы и шеи. // Материалы VI съезда детских онкологов с международным участием. 2015. — С. 283. (Комелягин Д.Ю., Дергаченко А.В., Дубин С.А., Петухов А.В., Иванов А.В., Владимиров Ф.И., Дергаченко А.В., Стрига Е.В., Вафина Х.Я., Пасечников А.В., Пачес О.А., Слипенко В.Г., Строганов И.А.)
2. Применение доксициклина в лечении детей с лимфатическими и лимфовенозными мальформациями головы и шеи. // Российская стоматология. 2015. — Т. 8, № 1. — С. 112 (Комелягин Д.Ю., Петухов А.В., Романов Д.В., Дубин С.А., Владимиров Ф.И., Дергаченко А.В., Пачес О.А., Топольницкий О.З., Иванов А.В., Вафина Х.Я., Пасечников А.В., Борзаева С.А., Солдатский Ю.Л., Воробьёв В.В.).
1. Комелягин Д.Ю. Возможности лечения детей с обширными лимфатическими и лимфовенозными мальформациями в области головы и шеи. / Комелягин Д.Ю., Петухов А.В., Дубин С.А, Дергаченко А.В., Владимиров Ф.И., Слипенко В.Г., Хаспеков Д.В., Дергаченко А.В., Пачес О.А., Фокин Е.И. // Онкопедиатрия. — 2015. — Том 2, № 3. — С. 285
2. Опыт лечения ребёнка с обширной лимфатической мальформацией в области головы и шеи. // Журнал Федерации специалистов по лечению заболеваний головы и шеи — Голова и шея. 2015. — С. 25 (Комелягин Д.Ю., Дергаченко А.В., Дубин С.А., Петухов А.В., Иванов А.В., Владимиров Ф.И., Дергаченко А.В., Стрига Е.В., Вафина Х.Я., Пасечников А.В., Пачес О.А., Слипенко В.Г., Строганов И.А., Топольницкий О.З., Романов Д.В., Щепин Н.В., Воробьев В.В., Шафранов В.В.)
3. Лечение детей с обширными лимфатическими и лимфовенозными мальформациями в области головы и шеи. // Сборник трудов по материалам VII Международной научно-практической конференции Стоматология славянских государств. 2015. — С. 144-147 (Комелягин Д.Ю., Дергаченко А.В., Петухов А.В., Дубин С.А., Владимиров Ф.И., Хаспеков Д.В., Дергаченко А.В., Пачес О.А., Фокин Е.И., Иванов А.В., Стрига Е.В., Слипенко В.Г., Вафина Х.Я., Строганов И.А.).
4. Treatment experience of child with extensive lymphatic malformations in head and neck. // XXV World Congress of Lymphology. San Francisco, California. — 2015. P. 136-204 (Komelyagin D., Dergachenko A.V., Dubin S., Petuchov A., Vladirov F.I., Dergachenko A.V., Topolniskiy O.Z.).
1. Комелягин Д.Ю. Малоинвазивный метод лечения детей с лимфатическими мальформациями головы и шеи. / Комелягин Д. Ю., Романов Д. В., Петухов А. В., Дубин С. А., Пачес О. А., Вафина Х. Я., Солдатский Ю. Л. // Росс. журнал детской онкологии и гематологии. — М. — 2014. — № 2. — С. 110
3. Komelyagin D.Ju. Indications for puncture method of treatment of children with lymphatic and lymphovenous malformations of head and neck area. / Komelyagin D.Ju., Petukhov A.V., Dubin S.A., Dergachenko A.V., Vladimirov F., Yamatina S.V., Khaspekov D.V., Topilin O.G., Slipenko V.G., Striga E.V., Dergachenko An.V., Topolnitsky O.Z., Ivanov A.V., Pasechnikov A.V., Vafina H.Ya., Strogonov I.A. // 21st International workshop on vascular anomalies. ISSVA 2016, Argentina, Buenos Aires. — 2016. — Р. 101
4. Оценка эффективности применения пропранолола у детей с младенческими гемангиомами в области головы и шеи. // Вестник Российского государственного медицинского университета. Материалы X Международной (XIX Всероссийской) Пироговской научной медицинской конференции студентов и молодых учёных. М. — 2015. С. 786 (Комелягин Д.Ю. в соавт. с Дергаченко А.В., Топольницким О.З., Владимировым Ф.И., Петуховым А.В., Гордеевым Д.Н., Дергаченко Ан.В.).
5. Склерозирующая терапия в лечении детей с лимфатическими мальформациями в области головы и шеи. // Вестник Российского государственного медицинского университета. Материалы X Международной (XIX Всероссийской) Пироговской научной медицинской конференции студентов и молодых учёных. М. — 2015. С. 788 (Комелягин Д.Ю. в соавт. с Дергаченко А.В., Топольницким О.З., Владимировым Ф.И., Петуховым А.В., Гордеевым Д.Н., Дергаченко Ан.В.).
6. Лечение детей с лимфатическими и лимфовенозными мальформациями в области головы, шеи, средостения. // IV междисциплинарный конгресс по заболеваниям органов головы и шеи. М. — 2016. — С. 132-134 (Комелягин Д.Ю., Петухов А.В., Хаспеков Д.В., Топилин О.Г., Дергаченко А.В., Владимиров Ф.И., Яматина С.В., Слипенко В.Г., Стрига Е.В., Дергаченко А.В., Фокин Е.И., Топольницкий О.З., Иванов А.В., Вафина Х.Я., Пасечников А.В., Строганов И.А.).
7. Склерозирующая терапия раствором доксициклина в лечении детей с лимфатическими мальформациями в области головы и шеи. // Материалы V Всероссийской научно-практической конференции с международным участием «Колесовские чтения». М. — 2016. — С. 143-154 (Комелягин Д.Ю., Петухов А.В., Топольницкий О.З., Дубин С.А., Дергаченко А.В., Владимиров Ф.И., Хаспеков Д.В., Топилин О.Г., Яматина С.В., Слипенко В.Г., Стрига Е.В., Дергаченко Ан.В., Иванов А.В., Пасечников А.В., Вафина Х.Я., Строганов И.А.).
8. Doxycycline use in lymphatic and lymphovenous treatment of children with malformations in the head and neck area. // XX International Workshop on Vascular Anomalies (ISSVA). Melbourne, Australia. — 2014. — P. 63 (Komelyagin D., Romanov D., Petuchov A., Dubin S., Dergachenko A., Vladimirov F., Ivanov A.).
9. Doxycycline use in lymphatic and lymphovenous treatment of children with malformations in the head and neck area. // XXV World Congress of Lymphology. San Francisco, California. — 2015. P. 135-198 (Komelyagin D., Dergachenko A.V., Dubin S., Petuchov A., Vladirov F.I., Dergachenko A.V., Topolniskiy O.Z.).
10. Indications for puncture method of treatment of children with lymphatic and lymphovenous malformations of head and neck area. // XXI International Workshop on Vascular Anomalies (ISSVA). Buenos Aires, Argentina. — 2016. — P. 72 (Komelyagin D., Petuchov A., Dubin S., Dergachenko A., Vladimirov F., Yamatina S., Khaspekov D., Topilin O., Slipenko V., Striga E., Dergachenko A., Topolnitsky O., Ivanov A., Pasechnikov A., Vafina K.).
ФГБУ «ЦНИИС и ЧЛХ» Минздрава России, Москва
ФГБУ «Центральный научно-исследовательский институт стоматологии и челюстно-лицевой хирургии» Минздрава России, Москва, Россия
ГБОУ ВПО «Рязанский государственный медицинский университет имени академика И.П. Павлова» Минздрава России, Рязань
Магнитно-резонансная томография лимфатических мальформаций лица и шеи
Журнал: Стоматология. 2016;95(6‑2): 102‑103
Фролов С.С., Надточий А.Г., Федотов И.А., Ломака М.А. Магнитно-резонансная томография лимфатических мальформаций лица и шеи. Стоматология. 2016;95(6‑2):102‑103.
Frolov SS, Nadtochiy AG, Fedotov IA, Lomaka MA. . Stomatologiya. 2016;95(6‑2):102‑103. (In Russ.).
Актуальность. Наиболее распространенным методом диагностики лимфатических мальформаций (ЛМ) лица и шеи является ультразвуковое обследование, обогащенное в последние годы эластографией. Однако для уточнения распространенности и оценки состояния глубоких областей лица нередко используется компьютерная и магнитно-резонансная томография (КТ и МРТ). Вместе с тем магнитно-резонансная (МР) семиотика ЛМ в отечественной литературе освещена явно недостаточно: не отражены особенности визуализации в зависимости от выраженности воспаления, наличия кровоизлияния в полость ЛМ, не разработаны критерии для выявления резидуальных ее элементов. Кроме того, по данным литературы, ЛМ может сочетаться с капиллярной или венозной мальформацией, что требует разработки технологий визуализации данного варианта патологии.
Цель исследования — повышение качества диагностики лимфатических мальформаций путем уточнения МР-семиотики и их различных форм и оптимизации протоколов МР-исследования.
Материал и методы. Проанализированы результаты МР-исследований 11 пациентов с ЛМ лица и шеи в возрастной группе от 5 мес до 16 лет. Обследования проводились на аппаратах различных марок с напряженностью магнитного поля от 1,5 до 3 Т с использованием следующих протоколов: T1 в трех проекциях (аксиальная, коронарная, сагиттальная) с толщиной среза не более 2—3 мм; Т2 в трех проекциях с толщиной среза не более 2—3 мм; T2 в трех проекциях с подавлением сигнала от жировой ткани, с толщиной среза не более 2—3 мм; Т1 с подавлением сигнала от жировой ткани и внутривенным контрастным усилением в 3D-режиме с толщиной среза не более 1,5 мм (начало сканирования после 40 с с момента введения препарата — отсроченная фаза), также проводилась бесконтрастная МР-артериография для исключения связи с артериальным сосудистым руслом. Продолжительность исследования — 70 мин. С учетом возраста пациентов и обязательной седации при выполнении исследования, была осуществлена оптимальная последовательность, которая отвечает на все поставленные вопросы и при этом сокращает время исследования до 30 мин: T1 в аксиальной проекции с толщиной среза не более 2—3 мм, Т2 в аксиальной проекции с толщиной среза не более 2—3 мм, T2 в корональной проекции с подавлением сигнала от жировой ткани, с толщиной среза не более 2—3 мм, Т1 с подавлением сигнала от жировой ткани и внутривенным контрастным усилением, не более 1,5 мм (с отсроченной фазой), бесконтрастная МР-артериография.
Результаты. МРТ позволяет идентифицировать лимфатические мальформации, оценить распространенность патологического процесса (в том числе — выявить вовлечение челюстных костей). Использование отработанного протокола МР-исследования, в котором в каждой из трех стандартных плоскостей сканирования выполняется лишь одна из необходимых импульсных последовательностей, позволяет сократить время сканирования и продолжительность седации до 25—30 мин без ущерба для качества диагностики.
Вывод. Применениеразработаннойметодики МР-диагностики позволяетполучить детальную МР-характеристику различных видов лимфатических мальформаций при минимально затраченном времени, что дает более четкую оценку при планировании тактики лечения, в том числе хирургического.
А.В. Петухов, Д.Ю. Комелягин, О.З. Топольницкий, С.В. Яматина
Детская городская клиническая больница святого Владимира; Московский государственный медико-стоматологический университет им. А.И. Евдокимова; НИИ хирургии детского возраста РНИМУ им. Н.И. Пирогова
Введение. Лимфатическая мальформация (ЛМ) — это порок развития лимфатических сосудов, имеющий различные формы проявления. Порок развития лимфатических сосудов и вен является комбинированным и носит название лимфовенозной мальформации (ЛВМ). В области головы и шеи встречается кистозный тип мальформаций.
Ранее к доброкачественным образованиям из лимфатических сосудов применялся термин «лимфангиома», а к лимфовенозным мальформациям — термин «лимфгемангиома». В настоящее время с помощью иммуногистохимических методов исключены маркеры опухолей в данных образованиях и рекомендовано их называть мальформациями или ангиодисплазиями (P. North, 2010).
Вышеуказанные нозологические единицы представлены в одной из современных классификаций пороков развития сосудов, а именно классификации Международного общества по изучению сосудистых мальформаций (ISSVA, 2014 г.). В данное международное сообщество входят специалисты из всех стран мира, активно занимающиеся изучением сосудистых опухолей и ангиодисплазий.
Основными методами лечения лимфатических мальформаций у детей в области головы и шеи являются следующие: хирургический, склерозирующая терапия и комбинированный (А.П. Малинин, 1974; В.В. Приходченко, 1986).
По мере накопления опыта лечения больных склерозирующей терапией отечественными учеными были выявлены следующие недостатки данного метода лечения: введение в патологические ткани 70 и 96% растворов спирта вызывало выраженный болевой синдром; существовал высокий риск передозировки склерозирующего раствора; раствор хинин-уретана оказался не-удобен для применения из-за быстрой дезактивации раствора, наличия индивидуальной непереносимости к хинину, частого отсутствия необходимых ингредиентов. Также к недостаткам относились длительность лечения и необходимость многократных инъекций склерозирующих растворов для получения полного фиброзирования образования (А.П. Малинин, 1974).
S. Wiegand (2011) провела анализ публикаций по склерозирующей терапии и указала на следующие данные: при крупнокистозной форме мальформаций препарат ОК-432 был эффективен у 96% пациентов в исследовании C. Giguere (2002), а по данным J. Yoo (2009), хороший результат при лечении 55 больных был получен в 76% случаев; P. Burrows (2008), пролечив 41 пациента с лимфатической мальформацией головы и шеи доксициклином, получил хороший результат в 83% случаев; Z. Qin (1998) пролечил 200 пациентов с лимфангиомами препаратом блеомицин и получил хороший результат в 86% случаев.
Несмотря на полученные хорошие результаты лечения, разнообразие применяемых препаратов косвенно говорит об отсутствии идеального препарата. При этом анализ результатов проводился с использованием разных критериев, что приводило к отличающимся численным данным.
По изученным источникам литературы, отсутствие стандартов лечения является причиной разработки новых методик лечения.
Цель исследования — разработать алгоритм склерозирующей терапии для лечения детей с лимфатическими и лимфовенозными мальформациями головы и шеи с применением современных препаратов.
Материал и методы. С 2011 по 2017 г. в отделении челюстно-лицевой хирургии ДГКБ святого Владимира (Москва) проведено лечение 42 детей с лимфатическими и лимфовенозными мальформациями в области головы и шеи методом пункционной склерозирующей терапии. Из них 15 (35,7%) девочек, 27 (64,3%) мальчиков. ЛМ были у 31 (73,8%), ЛВМ — у 11 (26,2%) больных. По возрастным группам пациенты делились следующим образом: с рождения до 1 года включительно было 12 детей, с 1 года до 3 лет — 12 пациентов, с 3 до 7 лет — 13, с 7 до 11 лет — 4, с 12 до 17 лет — 1 ребенок. Общее число детей до 3 лет 24 (57,1%).
Крупнокистозная форма была выявлена у 22 (52,4%) пациентов, смешанная — у 19 (45,2%) больных, мелкокистозная — у 1 (2,4%) ребенка.
Ограниченная форма мальформации, когда патологические ткани занимают не более 2 областей, встретилась у 20 (47,6%) больных. Патологические ткани локализовались в следующих областях: орбитальная — 1 (5%), щечная — 4 (20%); околоушно-жевательная — 3 (15%); дно полости рта — 2 (10%), шея — 10 (50%).
Обширная форма мальформаций (порочные ткани занимают 3 области и более) выявлена у 22 (52,4%) больных. Наиболее часто ЛМ и ЛВМ определялись в областях дна полости рта с распространением на околоушно-жевательную область и шею.
Крупнокистозная форма ЛМ и ЛВМ встречалась в областях шеи и в щечной области, мелкокистозная мальформация располагалась в области языка, подбородка, верхней губы. При локализации патологических тканей в пространствах дна полости рта, орбите, околоушно-жевательной области чаще всего определялась смешанная форма мальформации.
Операции проводились по жизненным, функциональным и косметическим показаниям.
Пациенты готовились к плановой операции по общим правилам, для чего собирались данные по общему и биохимическому анализам крови, общему анализу мочи, ЭКГ.
В алгоритм обследования детей с ЛМ и ЛВМ были включены следующие обследования: ультразвуковое исследование (Toshiba Aplio MX), МРТ (Toshiba Atlas 1,5T), фиброларингоскопия (Olympus Exera II CLV 180), магнитно-резонансная томография (Toshiba Atlas 1,5T). Компьютерная томография (Toshiba Aquilion 16) проводилась при обширных образованиях с подозрением на поражение костей черепа и деформацию последних.
При проведении диагностики образований наибольшую трудность вызывало установление до операции диагноза ЛВМ. В ходе операции данный диагноз ставился после пункции кисты и получения лимфы с кровью. Однако в дальнейшем, при накоплении опыта проведения МРТ, предварительный диагноз лимфовенозная мальформация ставился по данным обследования, проведенного в режиме Т2-взвешенного изображения, когда получали 2 разных сигнала от жидкостей, находящихся в одной кисте и четко разделенных друг от друга. Один сигнал характеризовал наличие в кисте жидкого содержимого (лимфы), а другой — более насыщенной или густой жидкости (крови). Диагноз Л.М. ставился при получении из образования лимфы.
Противопоказаниями для применения доксициклина являлись: гиперчувствительность, порфирия, тяжелая печеночная недостаточность, лейкопения; для блеомицина: гиперчувствительность, выраженная дыхательная недостаточность (фиброз легких, хроническая интерстициальная пневмония, острые легочные инфекции), тяжелая хроническая почечная недостаточность, атаксия-телеангиэктазия (синдром Луи—Бар). Противопоказаний к применению данных препаратов у пролеченных детей выявлено не было.
Склерозирующая терапия проводилась пункционным методом с ультразвуковой навигацией в условиях общей анестезии. Вид анестезии, комбинированный ингаляционный наркоз с интубацией трахеи или использованием ларингеальной маски зависел от локализации и объема патологических тканей. Интубация трахеи проводилась, во-первых, при наличии риска развития отека тканей дна полости рта, глотки и гортани, во-вторых, при локализации патологических тканей в полости рта для удобства проведения операции.
Пункция, аспирация содержимого полостей мальформации и введение в полость склерозирующего препарата проводились с использованием внутривенных катетеров 14G (2,1×45 мм) или 16G (1,8×45 мм), которые фиксировались к кожному покрову узловыми швами. Большой диаметр рабочей части позволил уменьшить риск закупорки входного отверстия катетера взвесью, образующейся в кисте после обработки склерозирующим раствором, а также снизил возможность перекрытия входа в катетер септой многокамерной формы мальформации.
Эвакуируемое содержимое полостей направлялось на цитологическое исследование. В эвакуируемой лимфе выявлены лимфоциты, единичные макрофаги на фоне слущенного эпителия, единичные клетки красной крови. При ЛВМ в пунктате на кровянистом фоне были определены лимфоидные элементы в большом количестве, моноцитарные структуры, клетки красной крови в большом количестве.
Объем склерозирующего раствора, вводимого в полость кисты, соответствовал объему лимфы (ЛМ) или лимфы с примесью крови (ЛВМ), удаленной из образования. Экспозиция препарата составляла 60 мин.
Сразу после операции (в течение 5 сут) проводилась оценка возможной токсической и аллергической реакции, местных воспалительных симптомов, выраженности болевого синдрома.
Введенный в образование раствор пассивно эвакуировался из полости мальформации в специальную емкость в течение 3—5 сут через установленный катетер. Последний удалялся из полости мальформации при отсутствии отделяемого из образования. Обычно это происходило на 3—5-е сутки. В послеоперационном периоде использовались давящие повязки. На 1-е, 3-и сутки после операции проводились контрольные ультразвуковые исследования. Пациент выписывался на 5-е сутки после операции. Клинический и ультразвуковой осмотры проводились через 1, 3, 6, 12 мес после операции и далее каждые 6 мес при отсутствии жалоб. Через 6 мес после операции проводилась контрольная магнитно-резонансная томография. Далее данное исследование проводилось 1 раз в год.
Результаты. Анализ результатов лечения и осложнений у детей с ЛМ и ЛВМ головы и шеи проводился по ряду параметров. Оценивались, во-первых, токсические и аллергические реакции, местные воспалительные симптомы, выраженность болевого синдрома, во-вторых, уменьшение объема образования. Наибольшая длительность наблюдения больных составила 6 лет.
Стоит отметить, что в результате проведенной работы не выявлена зависимость результатов лечения от вида мальформации (ЛМ, ЛВМ).
Одному ребенку с обширной лимфовенозной мальформацией дна полости рта, шеи, языка была проведена склерозирующая терапия крупных кист по жизненным показаниям. В результате лечения общий объем патологических тканей уменьшился незначительно. Послеоперационный период осложнился развитием некроза подкожно-жировой клетчатки и кожи, прилежащих к кистам образования. Однако угрозы жизни удалось избежать. От дальнейшего хирургического удаления патологических тканей отказались родители.
В послеоперационном периоде после применения раствора доксициклина отмечались выраженный болевой синдром у 25 (81%) больных, диспепсические расстройства (тошнота, рвота) у 5 (16%) детей. Болевой синдром купировался применением анальгетиков или нестероидных противовоспалительных препаратов в возрастных дозировках. У всех пациентов тошнота и однократная рвота купировались самостоятельно в течение суток. В ряде случаев в месте введения данного склерозирующего раствора через сутки после операции определялась выраженная инфильтрация мягких тканей.
У пациентов, которым применялся раствор блеомицина, болевого синдрома не было, однако диспепсические расстройства и лихорадка (субфебрильная, фебрильная) присутствовали у большинства больных (9 детей, 82%). Данные симптомы купировались самостоятельно или на фоне инфузионной терапии, приема жаропонижающих средств.
Аллергических реакций на введенные препараты выявлено не было ни у одного пациента.
Предварительные результаты лечения оценивались после однократного введения склерозирующего раствора не ранее чем через 3 мес после операции. Критерием оценки результатов лечения было уменьшение объема образования. Оценка проводилась на основании клинических данных и результатов ультразвукового исследования.
Отличный результат определялся при уменьшении объема образования более чем на 90%, хороший результат — от 50 до 90%, удовлетворительный — от 30 до 50%, неудовлетворительный — менее 30%.
Через 3 мес после применения доксициклина при лимфатической и лимфовенозной мальформации были получены следующие результаты: отличный — 15 (48,4%) детей, хороший — 9 (29%) больных, удовлетворительный — 2 (6,5%) пациента и неудовлетворительный — 5 (16,1%) детей. При крупнокистозной, ограниченной форме ЛМ и ЛВМ отличный результат был получен более чем в 85% случаев. При мелкокистозной форме мальформации результат лечения был неудовлетворительным.
После применения 11 больным раствора блеомицина отличный результат был получен у 1 (9,0%) ребенка, хороший — у 3 (27,3%), удовлетворительный — у 3 (27,3%), неудовлетворительный — у 4 (36,4%) пациентов. С крупнокистозной формой мальформации отличный результат лечения был получен только у 1 (14,3%) больного.
Таким образом, отличный и хороший результаты после применения доксициклина были получены в 77,4%, а при использовании раствора блеомицина — в 36,4% случаев.
При сохранении образования через 3 мес после лечения, но уменьшении его объема проводилось наблюдение до 6 мес после операции. Через 6 мес после операции проводилась контрольная магнитно-резонансная томография, по результатам которой при наличии крупных кист (более 1 см в диаметре) выставлялись показания к повторной операции. Повторные операции проводились также при наличии функциональных и косметических показаний.
После однократного применения доксициклина повторная склерозирующая терапия из 11 детей с хорошими и удовлетворительными результатами была проведена только 2 пациентам в связи с наличием функциональных и косметических показаний. Повторная операция после применения блеомицина проведена 4 больным с улучшением клинического результата лечения.
Детям с обширной смешанной формой ЛМ и ЛВМ с неудовлетворительным результатом склерозирующей терапии (7 (16,6%) детей) было выполнено удаление патологических тканей с последующим достижением хорошего результата лечения.
При наблюдении в динамике (с 2011 по 2017 г.) за больными с отличными и хорошими результатами после проведенной склерозирующей терапии растворами доксициклина и блеомицина показаний к повторной операции не было выявлено ни у одного больного.
Вывод. Склерозирующая терапия растворами доксициклина и блеомицина показана пациентам с крупнокистозной формой лимфатической или лимфовенозной мальформации при наличии функциональных и косметических показаний. При данном типе мальформации был получен в большинстве случаев отличный результат. Наилучший эффект от лечения достигается у детей с ограниченной крупнокистозной формой лимфатической или лимфовенозной мальформации.
При жизнеугрожающих состояниях данный вид лечения не показан из-за длительного ожидания результата лечения. Также склерозирующая терапия не показана при мелкокистозной форме мальформации.
При смешанной форме ЛМ и ЛВМ, когда крупнокистозный компонент преобладает над мелкокистозным компонентом, показано проведение склерозирующей терапии с возможным получением хорошего клинического результата.
Удовлетворительный и неудовлетворительные результаты лечения были связаны с наличием у пациентов смешанной формы лимфатической мальформации, при которой значительно выражена строма образования и основной объем представлен мелкими кистами. Также причинами неудовлетворительного результата являлись мелкокистозная форма лимфатической мальформации и возможное вовлечение в патологический процесс околоушной слюнной железы. Данной группе больных склерозирующая терапия показана как этапное хирургическое лечение с целью уменьшения объема образования перед хирургическим удалением последнего, что в дальнейшем способствовало сокращению времени операции и травматизации тканей, или после операции при появлении новых крупных кист.
Доксициклин значительно более эффективен, чем блеомицин, в пункционной склерозирующей терапии детей с лимфатическими и лимфовенозными мальформациями в области головы и шеи.
В большинстве случаев (28 (66,7%) пациентов) для получения отличного или хорошего клинического результата после склерозирующей терапии было достаточно 1—2 операци.
Клиника хирургии усовершенствования врачей №1 им. П.А. Куприянова Военно-медицинской академии;
клиника флебологии и медицинской косметологии Артмедия;
клиника "Медальп", Санкт-Петербург
ГБОУ ВПО «Первый московский государственный медицинский университет им. И.М. Сеченова» Минздрава России;
Детская городская клиническая больница св. Владимира, Москва, Российская Федерация
Московский государственный медико-стоматологический университет
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова», Минздрава России, Россия
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, Детская городская клиническая больница святого Владимира, Москва, Россия
Кафедра педиатрии Московского государственного стоматологического медицинского университета
БУ «Республиканское бюро судебно-медицинской экспертизы» Министерства здравоохранения Чувашии, Чебоксары, Чувашская Республика, Россия
ГБОУ ВПО «Первый московский государственный медицинский университет им. И.М. Сеченова» Минздрава России;ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, Российская Федерация;
Детская городская клиническая больница св. Владимира, Москва
Детская городская клиническая больница св. Владимира Департамента здравоохранения Москвы, Москва, Россия, 107014
Применение доксициклина в лечении детей с лимфатическими мальформациями в области головы и шеи
Журнал: Российская стоматология. 2016;9(2): 86‑86
Петухов А.В., Комелягин Д.Ю., Топольницкий О.З., Дубин С.А., Дергаченко А.В., Владимиров Ф.И., Хаспеков Д.В., Топилин О.Г., Слипенко В.Г., Стрига Е.В., Дергаченко Ан.В., Яматина С.В., Иванов А.В., Пасечников А.В., Вафина Х.Я., Строгонов И.А. Применение доксициклина в лечении детей с лимфатическими мальформациями в области головы и шеи. Российская стоматология. 2016;9(2):86‑86.
Petukhov AV, Komeljagin DJu, Topol'nitskiĭ OZ, Dubin SA, Dergachenko AV, Vladimirov FI, Haspekov DV, Topilin OG, Slipenko VG, Striga EV, Dergachenko AnV, Jamatina SV, Ivanov AV, Pasechnikov AV, Vafina KhYa, Strogonov IA. . Russian Stomatology. 2016;9(2):86‑86. (In Russ.).
Единый алгоритм лечения детей с пороками развития сосудов головы и шеи до сих пор не выработан. Дети с данными пороками относятся к одной из самых сложных групп пациентов. Во всем мире продолжается научный и клинический поиск наиболее эффективных методов лечения детей с пороками развития сосудов. С XIX века основным методом лечения лимфатических мальформаций (лимфангиом) было хирургическое лечение (Покровский М.О., 1898; Оппель В.А., 1899). В отечественной челюстно-лицевой хирургии данный метод остается основным методом лечения (Фролова А.И., 1983; Приходченко В.В., 1986; Шаргородский А.Г., 1999; Топольницкий О.З., 2011; Комелягин Д.Ю. и соавт., 2015).
Однако ряд авторов отмечают, что многоэтапные операции при пороках развития лимфатических сосудов не дают хорошего результата и чреваты опасностью возникновения длительно незаживающих ран, сопровождающихся лимфореей, повторными воспалительными процессами (Ninh T.N., 1974; Emery P.J., 1984; Alqahtani A., 1999; Kennedy T.L., 2001; Luzzatto C., 2005; Yoshifumi K. и соавт., 2007; Kella N., 2011; Qin Zhou, 2011). Также отмечается, что одномоментная радикальная операция возможна только в тех случаях, когда объем поражения невелик и полное удаление патологического очага не сопряжено с развитием осложнений (Покровский М.О., 1898; Оппель В.А., 1899; Исаков Ю.Ф., 1974; Dowd C.N., 1913; Alqahtani А., 1999; Luzzatto C., 2000; Amen E.A., 2001). В связи с этим продолжается поиск малоинвазивных и эффективных методов лечения лимфатических мальформаций. В зарубежной литературе все чаще публикуются схемы лечения детей с лимфатическими мальформациями (Augustín-Morales, 2008; Deepika Nehra, 2008), где первой линией терапии является склерозирующая терапия растворами доксициклина (Комелягин Д.Ю. и соавт., 2014; Molitch H.I., 1995; Cordes B.M., 2007; Nehra D., 2008; Burrows P.E., 2008; Мustrat R., 2013; Komelyagin D.Ju., 2014), блеомицина (Yura J., 1977; Zhong P.Q., 1998; Bai Y., 2009; Kella N., 2011), пицибанила (Ogita S., 1987; Qin Zhou, 2011). В основе предложенных схем лежат принципы малоинвазивности и эффективности, при этом единого подхода к склерозирующей терапии детей с лимфатическими мальформациями головы и шеи по настоящее время в мире не выработано: не известны показания и противопоказания к склерозирующей терапии; имеются ли возрастные ограничения к применению данного метода лечения; отсутствует единая отработанная методика применения склерозанта; не выработаны четкие критерии, в каких клинических случаях применять тот или иной склерозант; не проработаны вопросы устранения возможных осложнений после склеротерапии. Данные вопросы являются наиболее важными для детской челюстно-лицевой хирургии, так как лимфатические мальформации в 50—75% встречаются в области головы и шеи (Исаков Ю.Ф., 1983; Krainick-Strobel U., 2006; Enjolras O., 2008; Ocete Pérez R.F., 2012) и проявляются в 80—90% в возрасте до 2 лет (Копарзова О.А., 2005; Gross R.E., 1953; Bill A.H., 1965; Dubois J., 1997). В связи с этим вопрос склерозирующей терапии у детей с лимфатическими мальформациями в области головы и шеи остается актуальным.
Материал и методы. С 2011 по 2014 г. в ДГКБ святого Владимира проведено лечение 29 детей с лимфатическими мальформациями в возрасте от 14 дней до 16 лет. Больные по возрастным группам распределились следующим образом: до 1 года — 6 (20,7%) пациентов, от 1 года до 3 лет — 17 (58,6%), от 3 до 6 лет — 3 (10,3%) ребенка, от 7 лет до 12 — 1 (3,5%), от 12 до 16 лет — 2 (6,9%). Наибольшее количество — 23 (79,3%) пациента — были дети до трех лет.
Пороки развития лимфатических сосудов встречались в следующих областях: шея — 13 (44,8%), орбитальная — 2 (6,9%), щечная — 2 (6,9%); дно полости рта — 1 (3,5%); околоушно-жевательная, щечная, область шеи — 5 (17,2%); дно полости рта и язык — 6 (20,7%).
Пациенты были распределены по двум группам. В 1-ю группу вошли 20 (69%) детей, впервые обратившихся для лечения. 2-я группа больных была сформирована из пациентов, которым ранее проводилось то или иное лечение мальформаций в других клиниках. После хирургического вмешательства — 8 (27,6%) детей, после рентгенотерапии — 1 (3,4%). У 13 (45%) из 29 пациентов встречалась смешанная форма лимфатической мальформации, у 16 (55%) детей — крупнокистозная форма. Многокамерная форма лимфатической мальформации встретилась у 21 (72%) ребенка.
Всем детям с лимфатическими мальформациями в области головы и шеи проводился стандартный общеклинический осмотр и инструментальное обследование. В диагностический алгоритм обследования детей с пороками развития лимфатических сосудов входило: ультразвуковое исследование, фиброларингоскопия, магнитно-резонансная томография, компьютерная томография.
Ультразвуковое исследование является базовым методом диагностики сосудистых образований, позволяющим визуализировать структуру образования, подтвердить наличие жидкостного компонента, оценить васкуляризацию данного образования. Данное обследование не позволяет одновременно оценить объем образования и взаимоотношение с окружающими структурами. Магнитно-резонансная томография позволяет воспроизвести полную топографию и характер образования.
Для визуализации и исключения наличия лимфатической мальформации в верхних отделах дыхательных путей всем детям с пороками развития сосудов проводилась фиброларингоскопия. Фиброларингоскопия позволяла осмотреть глотку и гортань до голосовых связок для исключения наличия патологических тканей, а также для оценки степени перекрытия дыхательных путей лимфатической мальформацией.
Компьютерная томография проводилась при наличии деформации костей лицевого скелета у детей с обширной смешанной формой лимфатической мальформации.
Важно проводить дифференциальную диагностику лимфатической мальформации дна полости рта с ретенционной кистой поднижнечелюстной слюнной железы, а также с дермоидной кистой дна полости рта.
Магнитно-резонансная и компьютерная томографии детям до 5 лет проводились в условиях общей анестезии.
Обследования проводились на следующих аппаратах: УЗИ — Toshiba Aplio MX; МРТ — Toshiba Atlas 1,5T; КТ с контрастированием — Toshiba Aquilion 16; фиброларингоскопия — Olympus Exera II CLV 180.
Пункция полостей мальформации проводилась под наркозом, с использованием периферических внутривенных катетеров 14G (2,1×45 мм) или 16G (1,8×45 мм), под обязательным ультразвуковым контролем с применением портативного ультразвукового сканера SonoSite MicroMaxx (линейный датчик 7,5 МГц). Содержимое полостей эвакуировалось, направлялось на цитологическое исследование. В полости мальформации вводился раствор доксициклина из расчета 100 мг на 5 мл физиологического раствора (2% раствор доксициклина), в объеме, соответствующем удаленному из образования. Через 40 мин раствор препарата эвакуировался из полостей мальформации. После проведения манипуляции в течение 2—4 сут применялись давящие повязки. Контрольное ультразвуковое исследование послеоперационных областей проводилось на 3-и, 5-е сутки. Пациент выписывался на 5-е сутки после операции.
Результаты. Результат лечения оценивался через 3 мес после хирургического вмешательства. Критерием оценки результатов лечения было уменьшение объема образования. Оценка проводилась на основании клинических данных, подтвержденных результатами ультразвукового исследования.
Результат считался хорошим при уменьшении объема полостей образования более 50% от первоначального объема. При уменьшении объема лимфатической мальформации от 30 до 50% результат лечения оценивался как удовлетворительный. Неудовлетворительным результат был при уменьшении объема образования менее чем на 30%.
В 1-й группе у 14 (70%) детей результаты оценены как хорошие, у 2 (10%) пациентов как удовлетворительные. У 4 (20%) больных образование уменьшилось менее 30%. Во 2-й группе получены следующие результаты: хороший — у 3 (33,3%) пациентов, удовлетворительный — у 2 (22,2%), неудовлетворительный — у 4 (44,4%).
Всем детям с неудовлетворительными и удовлетворительными результатами в последующем была проведена повторная склерозирующая терапия. При получении неудовлетворительного результата после второго курса детям было проведено удаление патологических тканей.
Хороший результат лечения был получен у детей с макрокистозной формой лимфатической мальформации, при количестве кист не более трех. У детей с хорошим результатом лечение проводилось до отличного результата, критерием которого было уменьшение объема образования более 90%. Отличный результат был получен у 17 (58,6%) детей, что было подтверждено данными УЗИ и МРТ.
Причиной неудовлетворительного результата лечения детей как первой, так и второй групп была смешанная форма лимфатической мальформации. Другой причиной неудовлетворительного результата являлась микрокистозная форма лимфатической мальформации.
Абсолютным противопоказанием к применению 2% раствора доксициклина является аллергическая реакция. Также общими противопоказаниями к применению доксициклина у пациента являются следующие заболевания: порфирии, миастения, тяжелая форма почечной и печеночной недостаточности, лейкопения. У детей с лимфатическими мальформациями головы и шеи данные заболевания в нашей практике не встречались.
Вывод. Склерозирующая терапия 2% раствором доксициклина с ультразвуковой навигацией может проводиться независимо от возраста, является эффективным малоинвазивным способом лечения макрокистозных форм лимфатических мальформаций и должна являться первой линией терапии данной группы детей. При лечении детей с макрокистозной формой лимфатической мальформации, при достижении хорошего результата лечения (уменьшение объема образования более 50%) после однократной терапии склерозантом, показано продолжение лечения до получения отличного результата (уменьшение объема образования более 90%). Детям со смешанной формой лимфатической мальформации, в качестве вспомогательного к хирургическому методу, можно применять склерозирующую терапию при наличии макрокист. При микрокистозной форме склерозирующая терапия не эффективна.
Читайте также:
