Максимальная степень повышения желудочкового давления. Дисфункция левого желудочка при сердечной недостаточности
Добавил пользователь Дмитрий К. Обновлено: 28.01.2026
Нормальная диастолическая функция сердца подразумевает способность левого желудочка принимать в диастолу количество крови, необходимое для поддержания сердечного выброса, заключается в способности ее расслабления после этапа изгнания крови.
Под диастолической дисфункцией (ДД) понимают невозможность левого желудочка принимать кровь под низким давлением и наполняться без компенсаторного повышения давления в левом предсердии вследствие структурной и функциональной перестройки миокарда.
Диастолическая дисфункция левого желудочка является достаточно распространенным явлением. Нарушение диастолических свойств негипертрофированного миокарда, возможно, обусловлено развитием в нем интерстициального фиброза и наблюдается после 45 лет, как вариант возрастной нормы.
Этот тип изменения диастолы характерен для стареющего сердца (даже при отсутствии какого-либо сердечнососудистого заболевания) в связи с закономерно возникающими при нормальном старении нарушениями растяжимости, жесткости и податливости миокарда левого желудочка, обусловленными изменениями, происходящими в тканях (прежде всего увеличением содержания коллагена), пониженной рецепторной функцией, эндотелиальной дисфункцией и пр.
Для эхографической оценки диастолической функции левого желудочка применяют импульсное допплеровское исследование трансмитрального кровотока и тканевое допплеровское исследование диастолического подъема основания левого желудочка.
По данным трансмитрального кровотока исследуют максимальную скорость раннего диастолического наполнения левого желудочка (Е), максимальную скорость наполнения левого желудочка в систолу предсердия (А).
Методом тканевой допплерографии измеряют максимальную скорость диастолических волн, соответствующие раннему (е`) и позднему (а`) наполнению левого желудочка.
Метод тканевой допплерэхокардиографии относится к наиболее информативным способам диагностики диастолических нарушений ЛЖ и позволяет регистрировать раннюю диастолическую дисфункцию левого желудочка у всех больных гипертонической болезнью 1-2 ст.
При гипертонической болезни развитие диастолической дисфункции ассоциировано с увеличением тяжести гипертензии: умеренные нарушения диастолической функции наблюдаются уже при I стадии артериальной гипертензии.
Общепринято определять наличие диастолической дисфункции левого желудочка методом эхокардиографии, при этом используется комбинированная оценка трансмитрального диастолического потока и скорости движения митрального кольца.
Выделяют три типа наполнения левого желудочка: с замедленной релаксацией, псевдонормальный и рестриктивный, которые соответствуют незначительной, умеренной и тяжелой диастолической дисфункции.
Выделяют следующие типы диастолической дисфункции
- нарушение релаксации, псевдонормальный и рестриктивный тип. Первые два могут не сопровождаться симптомами, в то время как последний тип соответствует тяжелой степени ХСН с выраженными симптомами.
Диастолическая дисфункция левого желудочка по 1 типу - релаксационному типу характеризуется нарушением способности миокарда левого желудочка расслабиться для полноценного заполнения кровью.
Рабочей группой Европейского общества кардиологов разработаны ультразвуковые диагностические нормативы определения диастолической дисфункции.
Первый тип соответствует начальному нарушению диастолического наполнения, он характеризуется удлинением изоволюмического расслабления левого желудочка, снижением скорости и объема раннего диастолического наполнения, увеличением кровотока во время систолы предсердий. Другими словами, происходит перераспределение трансмитрального кровотока: большая часть крови поступает в желудочек в систолу предсердий. Заметим, что диастолическое давление в левом желудочке при этом может оставаться на нормальном уровне. Сейчас такой тип диастолической дисфункции принято называть Замедленным расслаблением левого желудочка.
Одной из причин ДДЛЖ является Гипертоническая болезнь - при которой нарушается активное расслабление и податливость, увеличение массы и жесткость миокарда, увеличение массы желудочков за счет утолщения их стенки,
Факторы, приводящие к развитию диастолической дисфункции, ухудшают процесс расслабления, уменьшают эластичность стенок левого желудочка, главным образом, вследствие развития гипертрофии (утолщения) миокарда.
При артериальной гипертонии нарушение релаксации выявляется у 90% больных с гипертрофией левого желудочка и у 25% - без таковой. Значительная диастолическая дисфункция иногда наблюдается у больных с весьма умеренным и локализованным утолщением стенки желудочка и без обструкции.
Диастолическое наполнение левого желудочка в норме и при патологии определяется двумя основными факторами — расслаблением миокарда и податливостью (или жесткостью) камеры желудочка
Нарушение диастолического расслабления миокарда. Уменьшению скорости и полноты активного диастолического расслабления принадлежит ведущая роль в патогенезе диастолической дисфункции
Расслабление миокарда представляет сложный энергозависимый процесс, который, согласно современным представлениям, регулируется следующими основными факторами: 1) нагрузкой на миокард во время его сокращения и 2) расслабления, 3) полнотой разъединения акто-миозиновых мостиков в результате обратного захвата ионов кальция саркоплазматическим ретикулумом и 4) равномерностью распределения нагрузки на миокард и разъединения акто-миозиновых мостиков в пространстве и времени. Нагрузка на миокард во время расслабления, в свою очередь, определяется: 1) конечно-систолическим стеночным напряжением в период быстрого наполнения, 2) стеночным напряжением, 3) наполнением венечных артерий в период изоволюмического расслабления и 4) энергией конечно-систолической деформации желудочка (D. Brutsaert с соавт., 1984).
Для раннего выявления диастолической дисфункции левого желудочка у больных гипертонической болезнью необходимо выполнение эхокардиографическое исследование включая проведение тканевого допплеровского исследования
Исследование функции левого желудочка «в покое» включает как определение его глобальной сократимости, так и оценку диастолического наполнения, характеризуемого по трансмитральному кровотоку. Особо подчеркнем целесообразность оценки диастолической функции, так как убедительно доказано, что диастолическая функция левого желудочка изменяется уже на ранних стадиях артериальной гипертензии тесно связана со степенью его гипертрофии. В связи с этим необходимо определять количественные показатели трансмитрального кровотока и тип нарушения (если он имеется) диастолы - нарушение релаксации, псевдонормальный, рестриктивный. На основании этих данных лечащий врач будет в дальнейшем производить дифференциальную диагностику между нарушением релаксации, диастолической дисфункцией левого желудочка и диастолической недостаточностью.
Нарушения диастолической функции левого желудочка часто выявляются у больных с гипертонической болезнью даже при отсутствии гипертрофии левого желудочка. Метод тканевой допплерэхокардиографии в импульсно-волновом режиме является хорошим дополнением к обычной допплерэхокардиографии трансмитрального потока в ранней диагностике диастолической дисфункции левого желудочка, в отсутствие выраженных изменений его геометрии, так как результаты, полученные с помощью данного метода не зависят от гемодинамических условий.
Хроническая перегрузка сердца давлением сопровождается комплексом структурных изменений, включающих диастолическую дисфункцию (ДД) левого желудочка, увеличение массы его миокарда.
Заведующая функциональной и ультразвуковой диагностикой Чибрикова Лилия Медихатовна и врач функциональной диагностики Лютков Евгений Степанович.
Гипертензивная болезнь сердца, осложненная сердечной недостаточностью
Гипертоническая болезнь (артериальная гипертония, АГ) - стабильное повышение систолического артериального давления до 140 мм.рт.ст. и более и/или диастолического артериального давления до 90 мм.рт.ст. и более (в результате как минимум трех измерений, произведенных в различное время на фоне спокойной обстановки; больной при этом не должен принимать лекарственные средства как повышающие, так и понижающие АД).
Сердечная недостаточность - симптомокомплекс, характеризующийся слабостью, одышкой, задержкой жидкости, который развивается вследствие различных заболеваний сердечно-сосудистой системы, приводящих к:
- неспособности сердца перекачивать кровь со скоростью, необходимой для удовлетворения метаболических потребностей тканей, или же обеспечению этих потребностей только при повышенном давлении наполнения;
- хронической гиперактивации нейрогормональных систем.
1. Достижение компенсации основных симптомов АГ и сердечной недостаточности - снижение АД, уменьшение одышки, сердцебиения, повышение толерантности к физической нагрузке, снижение утомляемости, задержки жидкости в организме.
2. Защита органов-мишеней от поражения (сердце, почки, головной мозг, сосуды, скелетная мускулатура).
Период протекания

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Классификация ВОЗ/МОАГ 1999 г.
Категории нормального АД:
- оптимальное АД < 120 / 80 мм.рт.ст.
- нормальное АД - высокое нормальное АД или предгипертония 130 - 139 / 85-89 мм.рт.ст.
Степени АГ:
- степень 1 - 140-159 / 90-99;
- степень 2 - 160-179/100-109;
- степень 3 - ≥180 / ≥110
- изолированная систолическая гипертензия - ≥140/
Степени риска АГ:
- Группа низкого риска (риск 1). Эта группа включает мужчин и женщин в возрасте моложе 55 лет с АГ 1 степени при отсутствии других факторов риска, поражения органов-мишеней и ассоциированных сердечно-сосудистых заболеваний. Риск развития сердечно-сосудистых осложнений в ближайшие 10 лет (инсульта, инфаркта) составляет менее 15%.
- Группа среднего риска (риск 2). В эту группу входят пациенты с АГ 1 или 2 степени. Основным признаком принадлежности к этой группе является наличие 1-2 других факторов риска при отсутствии поражения органов-мишеней и ассоциированных сердечно-сосудистых заболеваний. Риск развития сердечно-сосудистых осложнений в ближайшие 10 лет (инсульта, инфаркта) составляет 15-20%.
- Группа высокого риска (риск 3). К этой группе относятся пациенты с АГ 1 или 2 степени, имеющие 3 или более других факторов риска или поражение органов-мишеней. В эту же группу входят больные с АГ 3 степени без других факторов риска, без поражения органов-мишеней, без ассоциированных заболеваний и сахарного диабета. Риск развития сердечнососудистых осложнений в этой группе в ближайшие 10 лет колеблется от 20 до30%.
- Группа очень высокого риска (риск 4). К этой группе относятся пациенты с любой степенью АГ, имеющие ассоциированные заболевания, а также пациенты с АГ 3 степени, с наличием других факторов риска и/или поражением органов-мишеней и/или сахарным диабетом даже при отсутствии ассоциированных заболеваний. Риск развития сердечно-сосудистых осложнений в ближайшие 10 лет превышает 30%.
Стратификация риска для оценки прогноза больных АГ
| Другие факторы риска (кроме АГ), поражения органов-мишеней, ассоциированные заболевания | Артериальное давление, мм.рт.ст Степень 1 САД 140-159 ДАД 90-99 | Артериальное давление, мм.рт.ст Степень 2 САД 160-179 ДАД 100-109 | Артериальное давление, мм.рт.ст Степень 3 САД >180 ДАД >110 |
| I. Нет факторов риска поражения органов-мишеней, ассоциированных заболеваний | Низкий риск | Средний риск | Высокий риск |
| II. 1-2 фактора риска | Средний риск | Средний риск | Очень высокий риск |
| III. 3 фактора риска и более и(или) поражение органов мишеней | Высокий риск | Высокий риск | Очень высокий риск |
| IV. Ассоциированные (сопутствующие) клинические состояния и(или) сахарный диабет | Очень высокий риск | Очень высокий риск | Очень высокий риск |
Классификация гипертонического сердца (Frohlich, 1987 г.)
- 1 стадия - отсутствуют клинические признаки гипертонического сердца, но с помощью специальных методов исследования выявляются признаки повышенной нагрузки на миокард, увеличение потребности миокарда в кислороде и напряжения миокарда, ранние признаки нарушения диастолической функции миокарда левого желудочка, в частности, в снижение индекса опорожнения левого предсердия.
- 2 стадия - увеличение левого предсердия (по данным ЭКГ и ЭХОКГ).
- 3 стадия - развитие гипертрофии левого желудочка (по данным ЭКГ, ЭХОКГ, рентгенографии), при этом отсутствуют клинические признаки недостаточности кровообращения.
- 4 стадия - развитие сердечной недостаточности вследствие прогрессирования гипертонической болезни сердца, часто присоединяется ишемическая болезнь сердца.
| Функциональные классы ХСН (могут изменяться на фоне лечения) | Стадии ХСН (меняются на фоне лечения) |
| I ФК | I стадия |
| Ограничения физической активности отсутствуют: привычная физическая активность не сопровождается быстрой утомляемостью, появлением одышки или сердцебиением. Повышенную нагрузку больной переносит, но она может сопровождаться одышкой |
Степени
Описание
Диастолическая дисфункция левого желудочка
Диастолическая дисфункция левого желудочка в сочетании с его
Застойная сердечная недостаточность (выраженная одышка, Rtg -
признаки отека легких, что соответсвует ХСН III-IV ФК) при
нормальной фракции выброса левого желудочка (50% и больше)
Застойная сердечная недостаточность с низкой фракцией выброса
левого желудочка (меньше 50%)
| Факторы риска сердечно-сосудистых заболеваний | Поражение органов-мишеней | Сопутствующие (ассоциированные) клинические состояния |
| 1. Используемые для стратификации риска: - Величина САД и ДАД (степень 1-3) - Возраст: - мужчины >55 лет - женщины > 65лет - Курение - Уровень общего холестерина в крови >6,5 ммоль/л - Сахарный диабет - Семейные случаи раннего развития сердечно-сосудистых заболеваний 2. Другие факторы, неблагоприятно влияющие на прогноз*: - Сниженный уровень холестерина ЛПВП - Повышенный уровень холестерина ЛПНП - Микроальбуминурия (30-300 мг/сут) при сахарном диабете - Нарушение толерантности к глюкозе - Ожирение - Сидячий образ жизни - Повышенный уровень фибриногена в крови - Социально- экономические группы с высоким риском - Географический регион высокого риска | - Гипертрофия левого желудочка (ЭКГ, ЭхоКГ, рентгенография) |
- Протеинурия и/или
небольшое повышение
креатинина плазмы (106 -
177 мкмоль/л)
- Ультразвуковые или
рентгенологические
признаки атеросклеротического
поражения сонных, подвздошных и бедренных
артерий, аорты
Диагностика
Критерии диагностики:
1. Подтверждение наличия АГ и установление ее стабильности (повышении АД выше 140/90 мм.рт.ст. у больных неполучающих регулярную гипотензивную терапию в результате как минимум трех измерений в различной обстановке).
2. Исключение вторичной артериальной гипертонии.
3. Стратификация риска АГ (определение степени повышения АД, определение устранимых и неустранимых факторов риска, поражения органов-мишеней и ассоциированных состояний).
4. Выявление заболеваний, приводящих к развитию сердечной недостаточности на фоне АГ: перенесенный инфаркт миокарда, стенозирующий атеросклероз коронарных артерий, сахарный диабет, тяжелые инфекции, пароксизмальная мерцательная аритмия и трепетание предсердий.
5. Симптомы сердечной недостаточности: одышка, сердцебиение, повышенная утомляемость, задержка жидкости в организме.
6. Клинические и инструментальные проявления гипертрофии левого желудочка: смещение верхушечного толчка влево, смещение кнаружи левой границы сердца, появление IV тона, систолического шума митральной регургитации; ЭКГ-признаки (отклонение оси влево, индекс Соколова-Лайона Sv1+Rv5 - более 35 мм у лиц старше 40 лет, более 45 мм у лиц моложе 40 лет; Корнельского индекса Ravl+Sv3 - более 28 мм у мужчин, более 20 мм у женщин), ЭХОКГ-признаки - Тзслж более 1.2 см, Тмжп более 1,2 см; увеличение индекса массы миокарда ЛЖ (более 134 г/см 2 для мужчин, 110 г/см 2 у женщин); концентрическое ремоделирование ЛЖ, уменьшение трансмитрального кровотока.
7. ЭХОКГ-признаки сердечной недостаточности - укорочение миокарда в средней части левого желудочка, снижение фракции выброса меньше 40%. Рентгенологические признаки застойных явлений в легких.
Перечень основных диагностических мероприятий:
- биохимический анализ крови (глюкоза, белок, белковые фракции, билирубин и его фракции, креатинин, натрий, калий);
Лечение
Тактика лечения
1. Диета калорийная, легкоусвояемая с небольшим содержанием соли (при ХСН 1 ФК - менее 3 г в сутки, при ХСН 2-3 ФК - 1.2-1,8 г /сутки, при тяжелой ХСН 4 ФК - менее 1г/сутки) и ограничением приема жидкости, но не менее 750 мл в сутки.
2. Физическая реабилитация (ходьба или велотренинг). Нагрузка строго дозирована и индивидуальна. Расчет нагрузки: 30-60 мин активных занятий при ЧСС, составляющей 75% максимальной. Применение данного метода повышает толерантность к нагрузкам, аэробную способность организма и переносимость лекарственных средств.
3. Психологическая и социальная реабилитация.
4. Медикаментозная терапия.
4.1 Снижение АД
4.2 Разгрузка сердца: объемная - диуретики.
Диуретики необходимо применять с ИАПФ, использовать вместе с антагонистами альдостерона, назначать ежедневно в минимальных дозах, позволяющих добиться необходимого положительного диуреза (для активной фазы лечения +800 мл).
Гидрохлортиазид. Назначается в дозах по 50-100 мг/сут утром. Максимальная доза 200 мг/сут. Препарат принимается ежедневно или через день. Возможны кратковременные перерывы (3-5 дней).
Фуросемид. Доза устанавливается индивидуально в каждом конкретном случае. В процессе лечения режим дозирования корригируется в зависимости от величины диуретического эффекта и динамики состояния больного. При приеме внутрь средняя начальная доза 40-80 мг/сут, поддерживающая 20-40 мг/сут. При необходимости быстрого улучшения самочувствия препарат вводится в/в или в/м, начальная доза 20-50 мг. При одновременном приеме с ИАПФ препараты калия не назначаются.
4.3 Гемодинамическая - (ИАПФ, блокаторы рецепторов ангиотензина II, антагонисты альдостерона).
ИАПФ - эналаприл (нач. доза 2.5 мг с повышением до 10 мг 2 раза/сутки), периндоприл (нач.доза 2 мг 1 раз/сутки, оптимальная 4 мг/с), лизиноприл (нач. доза 2.5 мг с повышением до 20 мг 1 раза/сутки). Обязательны для всех больных ХСН независимо от этиологии, стадии процесса и характера течения. Неназначение ИАПФ больным с ХСН (при отсутствии абсолютных противопоказаний - аллергические реакции и двусторонний стеноз почечных артерий) не оправдано и ведет к сознательному увеличению риска смерти декомпенсированных пациентов.
Блокаторы рецепторов ангиотензина II. Эпросартан - средство выбора при непереносимости пациентами ИАПФА и при сочетании АГ с диабетической нефропатией назначается в дозе 300-600 мг/сут в зависимости от уровня АД. Антагонисты альдостерона - спиронолактон в дозе при поддерживающей терапии 25-50 мг/сутки. При тяжелой декомпенсации и ухудшении течения ХСН 150/300 мг/сутки однократно утром, либо в два приема, но в первой половине дня .
4.4 Миокардиальная - бета-адреноблокаторы (метопролол). Применяют только дополнительно к ИАПФ. Назначают терапию с 1/8 средней терапевтической дозы (для метопролола 12,5 мг). Дозу повышают медленно (в 2 раза, не чаще чем через 2 недели) до достижения оптимальных суточных доз (для метопролола до 200 мг/сутки).
Кардиотонические средства (сердечные гликозиды) при ХСН уменьшают выраженность симптоматики, заболеваемость (число госпитализаций в связи с обострением ХСН) и не влияют на прогноз. Назначаются в малых дозах (дигоксин до 0,25 мг/сутки) при мерцательной аритмии и трепетании предсердий. При синусовом ритме назначать с осторожностью и в малых дозах.
Перечень дополнительных лекарственных средств:
1. Статины (симвастатин).
Вспомогательные лекарственные средства эффект которых и влияние на прогноз больных не доказаны, но их применение диктуется определенными клиническими ситуациями.
2. Периферические вазодилататоры (нитраты) не являются средствами лечения ХСНА. Назначают только при сопутствующей стенокардии, когда есть уверенность, что именно они избавляют пациента от приступов стенокардии.
3. Нитроглицерин - быстродействующие формы: под язык 0,3-0,6 мг, табл. и капс., повторяют по потребности. Принимают внутрь, не разжевывая, запивая водой, лучше после еды, 1-2 табл. (капс.) 2 раза/сут. (обычно утром и в полдень), в отдельных случаях до 4 раз/сут, но не более 12 табл. в день. Может применяться в виде аэрозоля для сублингвального применения, 1-2 дозы (0,4-0,8 мг) под язык. Нитроглицерин в/в инфузионно 5-200 мкг/мин (титруется с учетом изменения САД, которое должно быть больше 90мм.рт.ст.). Дозу повышают до получения желаемого гемодинамического эффекта или побочных проявлений (головная боль, тошнота). Необходим мониторинг АД.
4. Изосорбида динитрат - внутрь, не разжевывая, запивая водой, лучше после еды. Кратность зависит от длительности действия: таблетки средней продолжительности действия 3-4 раза в день по 1-30 мг на прием; препараты пролонгированного действия 20 мг 2-3 раза в сутки, препараты пролонгированного действия 40 и 60 мг 2 раза в сутки, препараты пролонгированного действия 120 мг 1 раз в сутки. Аэрозоль для сублингвального приема в положении сидя 1-3 дозы (1.25-3.75 мг) п/я. Лекарственные формы для наклеивания на десну 20-40 мг 1-3 раза в сутки. В/в инфузионно 2-10 мг/ч. и более (титруется с учетом изменения САД, которое должно быть больше 90мм.рт.ст.).
5. Блокаторы кальциевых каналов (амлодипин) назначают дополнительно к ИАПФ при клапанной регургитации и легочной гипертензии. Начальная доза составляет 5 мг 1 раз в сутки, средняя поддерживающая доза 10 мг/сут.
6. Антиаритмические средства (амиодарон) применяют при опасных для жизни желудочковых аритмиях. Внутрь в течение 1-й недели 200 мг 3 раза в сутки, в течение 2-й недели 200 мг 2 раза в сутки, далее уменьшение дозы до поддерживающей 100-400 мг в сутки. В/в инфузия: 5-7 мк/кг за 20-120 мин. под контролем ЭКГ и АД, при необходимости продолжение инфузии 1.2-1,8 г/сут. (Предлагается включить данный препарат в список жизненно важных препаратов как препарат выбора для купирования пароксизмальных наджелудочковых и желудочковых тахикардиях, мерцательной аритмии, желудочковой тахикардии и фибрилляции желудочков. Высокоэффективен как средство первичной и вторичной профилактики внезапной аритмической смерти у постинфарктных больных и при ХСНА).
7. Ацетилсалициловая кислота по 75-160 мг 1 раз в сутки.
Перечень основных медикаментов:
1.*Гидрохлортиазид 25 мг, табл.
2. *Фуросемид 40 мг, табл.
3. *Эналаприл 2,5 мг, 10 мг, табл.
4. *Периндоприл 4 мг, табл.
5. *Лизиноприл 2,5 мг, 5 мг, 10 мг, 20 мг табл.
6. *Спиронолактон 25 мг, 50 мг, табл.
7. *Дигоксин 62,5 мкг, 250 мкг, табл.
8. Моэксиприл 7,5 мг, 15 мг, табл.
Перечень дополнительных медикаментов:
1. Эпросартан 300 мг, табл.
2. *Ацетилсалициловая кислота 100 мг, 500 мг табл.
3. Симвастатин 5-80 мг, табл.
4.*Ловастатин 10 мг, 20 мг, 40 мг, табл.
Недостаточность митрального клапана - симптомы и лечение
Что такое недостаточность митрального клапана? Причины возникновения, диагностику и методы лечения разберем в статье доктора Верещагиной Натальи Валентиновны, терапевта со стажем в 29 лет.
Над статьей доктора Верещагиной Натальи Валентиновны работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина
Определение болезни. Причины заболевания
Недостаточность митрального клапана — порок, при котором из-за неполного смыкания створок клапана возникает обратный ток крови (регургитация) из левого желудочка в левое предсердие [8] .
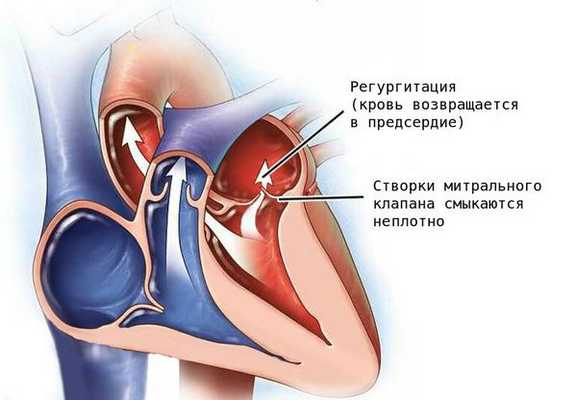
Патология проявляется слабостью, головокружением, ощущением нехватки кислорода и утомлением, так как при заболевании нарушается кровоснабжение головного мозга. Без лечения тяжёлая регургитация митрального клапана может стать причиной сердечной недостаточности и нарушений сердечного ритма (аритмии).
Причины митральной недостаточности:
- ;
- бактериальный эндокардит;
- отложение солей кальция в тканях клапана;
- заболевания соединительной ткани — ревматоидный артрит, системная красная волчанка, склеродермия, синдромы Марфана и Элерса-Данло;
- травматический отрыв створок клапана при тяжёлой физической нагрузке;
- травмы при хирургических операциях на клапане;
- утолщение створок клапана;
- опухоли предсердия;
- лучевая терапия [8] .
Митральная недостаточность находится на первом месте среди всех приобретённых клапанных пороков сердца. Патология редко встречается изолированно, зачастую она сочетается с митральным стенозом и с пороками аортального клапана. Распространённость недостаточности митрального клапана в сочетании с пролапсом митрального клапана среди населения составляет 2-6 % [15] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы недостаточности митрального клапана
Симптомы заболевания:
- общая слабость и головокружение;
- учащённое сердцебиение;
- одышка, возникающая даже при незначительных нагрузках;
- ноющие, давящие и колющие боли в сердце, которые могут отдавать в левое плечо и руку;
- "неудовлетворённость вдохом" — больной делает один вдох за другим, но ощущает нехватку воздуха и впадает в панику;
- частые простудные заболевания;
- кровотечения из носа и дёсен, длительные менструации у женщин;
- ухудшение памяти, панические атаки, тревога, мнительность (это связано с нехваткой снабжения головного мозга кислорода, нарушением обменных процессов и замедлением передачи импульсов между нейронами);
- дрожь в теле;
- частое появление синяков;
- дискомфорт при нахождении в закрытом и душном помещении, возможны обмороки;
Постоянная тревога часто приводит пациента на консультацию к психиатру или неврологу. Очень важно не допустить таких больных в профессиональный спорт, так как чрезмерные нагрузки могут вызвать смерть на тренировках и соревнованиях.
У пациенток с митральной недостаточностью во время беременности возможны перебои в работе сердца, особенно нежелательные при родах, но в основном беременность протекает без осложнений [3] [4] .
Патогенез недостаточности митрального клапана
Сердце человека состоит из четырёх камер: правое и левое предсердия, правый и левый желудочки. Между предсердиями и желудочками расположены входные клапаны — трикуспидальный и митральный. На выходе из желудочков находятся похожие по строению выходные клапаны — лёгочный и аортальный.
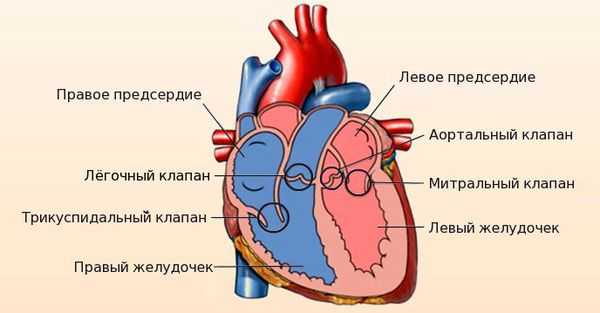
Клапаны имеют створки, которые открываются и закрываются во время сердечных сокращений. Иногда клапаны не открываются или не закрываются должным образом, при этом нарушается ток крови.
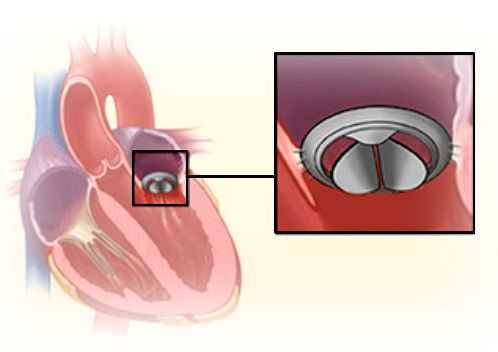
Митральный клапан состоит из двух створок и открывается, позволяя крови течь в левый желудочек. Затем клапан закрывается, чтобы кровь не текла обратно в левое предсердие. При митральной недостаточности этот клапан закрывается неплотно, в результате чего кровь попадает обратно в левое предсердие.
В патогенезе первичной или врождённой недостаточности митрального клапана важную роль играет хронический дефицит ионов магния. Нехватка магния приводит к тому, что фибробласты вырабатывают неполноценные эластин, коллаген и фибронектин, а также к нарушению свойств ферментов, регулирующих обмен коллагена. В результате нарушается строение и функции соединительных тканей сердца [14] .
Вторичная форма митральной недостаточности возникает в результате перенесённых заболеваний и травм. При патологии происходит расширение полости левого желудочка, прогибание створок митрального клапана, дисфункция сосочков мышц и разрыв сухожильных хорд, соединяющих клапаны с сосочковыми мышцами. Иногда причиной развития вторичной недостаточности митрального клапана становится кальциноз клапанного фиброзного кольца. Кальциноз митрального кольца — это хронический дегенеративный процесс, при котором происходит отложение кальция в кольце клапана. Митральное кольцо при кальцификации становится утолщённым и менее гибким. Хотя изначально кальциноз митрального клапана считался возрастным дегенеративным процессом, накапливаются данные о том, что его развитию способствуют атеросклероз и генетически обусловленные нарушения кальций-фосфорного обмена [16] .
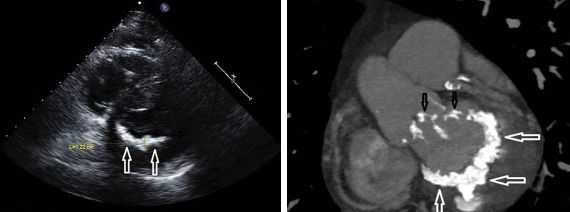
Классификация и стадии развития недостаточности митрального клапана
В течении заболевания выделяют три периода:
- Компенсация дефекта клапана усиленной работой левого предсердия и левого желудочка. Это продолжительный период хорошего самочувствия, но уже на этой стадии начинают появляться первые характерные симптомы: слабость, головокружение, частые простудные заболевания, чувство нехватки воздуха, перебои в работе сердца, одышка.
- Развитие венозной митральной недостаточности. Больные жалуются на одышку и учащённое сердцебиение. При интенсивной физической нагрузке наблюдаются приступы сильной одышки и кровохарканье.
- Одышка уменьшается, но пациент ощущает тяжесть в правом подреберье. Появляются отёки, уменьшается количество мочи, набухают шейные вены. Кровохарканье усиливается, развивается отёк лёгких, возникают нарушения сердечного ритма (мерцательная аритмия и наджелудочковая экстрасистолия) и тромбоэмболические осложнения.
С учётом выраженности обратного тока крови выделяют четыре степени митральной недостаточности: с незначительной митральной регургитацией, с умеренной, выраженной и тяжёлой.
Стадии митральной недостаточности:
- Митральный возврат крови составляет 20-25 %. На этой стадии пациент здоров.
- Митральный возврат крови в пределах 25-50 % от систолического объёма крови. Развивается застой крови в лёгких второй степени. Появляются кашель, одышка, перебои в работе сердца.
- Выраженная недостаточность митрального клапана. Возврат крови в левое предсердие составляет 50-90 %. Возникают кашель, кровохарканье, приступы удушья, увеличивается печень, появляются отёки [8] .
Осложнения недостаточности митрального клапана
Осложнения порока:
- Кровохарканье и отёк лёгких. Проявляется одышкой, затруднённым вдохом, влажным кашлем. В мокроте появляется кровь. Температура тела повышается до субфебрильных ( 37-38 °C ) и фебрильных ( 38-39 °C ) значений. Необходима срочная госпитализация в отделение реанимации.
- Нарушения сердечного ритма в виде мерцательной аритмии и наджелудочковой экстрасистолии. Проявляются перебоями в работе сердца, головокружением, слабостью, обмороками. Требуется госпитализация в отделение кардиологии.
- Тромбоэмболические осложнения (тромбоз левого предсердия, сосудов кишечника, почек, головного мозга). Последствия будут зависеть от локализации тромба. При тромбозе сосудов головного мозга возможен инсульт. Если тромб находится в почках и сосудах кишечника, то пациент испытывает острые боли в животе. Необходима госпитализация в отделение реанимации [8][9] .
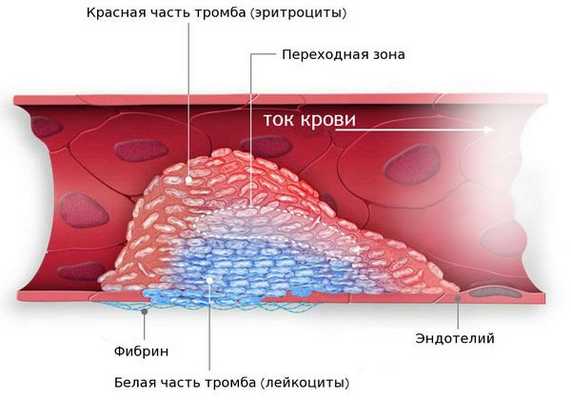
Диагностика недостаточности митрального клапана
При сборе анамнеза кардиолог уточняет:
- ощущает ли пациент нехватку воздуха при вдохе;
- беспокоят ли перебои в работе сердца;
- возникает ли одышка при незначительных физических нагрузках;
- мучает ли тревога, страх смерти, панические атаки.
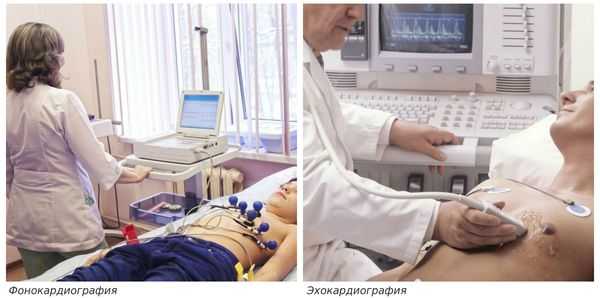
При аускультации ("выслушивании" сердца) выявляется систолический шум у верхушки и над основанием сердца. Важное значение для диагностики митральной недостаточности имеет фонокардиография (ФКГ). ФКГ - это метод исследования работы сердечной мышцы, который основан на регистрации и последующем анализе звуков, возникающих во время работы сердца .
Другой важный инструментальный метод диагностики — эхокардиография (Эхо-КГ) . Эхо-КГ — это безболезненное ультразвуковое исследование, которое позволяет исследовать работу сердца в реальном времени. Эхокардиография покажет уменьшение эластичности клапана, его повреждение, размер отверстия митрального клапана и расстояние между его створками. Также при исследовании можно увидеть разрыв папиллярной мышцы и провисание клапанных створок в полость левого предсердия [4] [8] [9] .
Лечение недостаточности митрального клапана
При обострении заболевания необходим постельный режим. Также следует принимать препараты, содержащие магний и B6 по две таблетки три раза в день (например, "Магнелис").
Обязательно следует проводить лечение и профилактику осложнений. Для предупреждения тромбоэмболии пациентам старше 30-40 лет назначают препарат "Тромбо АСС", препятствующий тромбообразованию .
Если беспокоит частый пульс (более 80 ударов в минуту), то назначаются бета-адреноблокаторы, диуретики, антикоагулянты, нитроглицерин.
Если пациент страдает от приступов тревоги, то в качестве симптоматической терапии можно рекомендовать короткий курс феназепама на ночь.
Если развивается сердечная недостаточность и нарушается сердечный ритм, то проводят лечение бета-адреноблокаторами, диуретиками, ингибиторами ангиотензинпревращающего фермента, антикоагулянтами, блокаторами кальциевых каналов.
При значительной недостаточности митрального клапана показано оперативное лечение.
Основные хирургические методы коррекции митральной недостаточности:
- пластика митрального клапана;
- протезирование с частичным или полным сохранением хордального аппарата;
- протезирование без сохранения хордального аппарата.
Своевременное хирургическое вмешательство позволяет достичь хороших результатов и не допустить развитие осложнений.
Прогноз. Профилактика
При соблюдении рекомендаций врача прогноз благоприятный.
Для профилактики осложнений следует:
- ежегодно проходить осмотр у терапевта и кардиолога и проводить эхокардиографию сердца (Эхо-КГ);
- принимать препараты магния, а для предупреждения тромбоэмболии — антикоагулянты;
- исключить тяжёлые физические нагрузки, переохлаждение и перегрев;
- снизить эмоциональные перегрузки;
- отдыхать в дневные часы;
- при тревожных расстройствах принимать успокоительные препараты, освоить методы аутотренинга и расслабления мышц;
- проходить санаторно-курортное лечение [4] .
При ревматизме и после перенесённой ангины для профилактики недостаточности митрального клапана назначают антибиотик "Бициллин-3". Препарат подавляет развитие стрептококковой и стафилококковой инфекций.
После 40 лет всем пациентам, страдающим недостаточностью митрального клапана, необходимо контролировать уровни фибриногена, РФМК (растворимых фибринмономерных комплексов), D-димера (продукта распада фибрина). Эти анализы нужны для предотвращения тромбоэмболии лёгочной артерии и артерий внутренних органов. При повышении вышеуказанных показателей назначают антикоагулянты.
Если недостаточность митрального клапана обнаружена у ребёнка и его беспокоит слабость, головокружение, расстройство внимания, то рекомендуется временно перейти на домашнее обучение. Таким детям следует избегать чрезмерных физических нагрузок, им разрешена только лечебная физкультура.
Если при проведении Эхо-КГ обнаружено сильное прогибание створок клапана, то необходима консультация у кардиохирурга. Восстановление клапана или его замена могут потребоваться при эндокардите, сердечной недостаточности, нарушениях ритма, сильных болях в грудной клетке, признаках застоя в лёгочной системе (одышке, уменьшении объёма вдоха и ощущении нехватки воздуха).
Правожелудочковая сердечная недостаточность
Правожелудочковая сердечная недостаточность - это сложный клинический синдром, который развивается при дисфункции правого желудочка. Патология возникает остро на фоне ТЭЛА и органического повреждения миокарда, хронические формы зачастую связаны с левожелудочковой недостаточностью. Болезнь проявляется симптомами нарушений гемодинамики в большом круге кровообращения: отеками, увеличением печени, постоянной слабостью. Для диагностики проводится ЭКГ и ЭхоКГ, катетеризация сердца, расширенный биохимический анализ крови. Лечение ПЖСН предполагает прием диуретиков, инотропных препаратов и антикоагулянтов, в тяжелых случаях проводятся кардиохирургические операции.
МКБ-10



Общие сведения
Доля правожелудочковой сердечной недостаточности (ПЖСН) составляет около 15-20% среди всех форм кардиоваскулярной недостаточности. Среди пациентов с кардиологическими проблемами, которые поступают в реанимационное отделение, острая ПЖСН определяется в 3-9% случаев. Истинную частоту патологии сложно оценить из-за ее длительного малосимптомного течения, частого сочетания с поражением левого желудочка. Поэтому усилия современной кардиологии направлены на улучшение процессов диагностики и лечения таких состояний.

Причины
Развитие заболевания связывают с анатомическими особенностями правого желудочка (ПЖ): он имеет тонкие стенки и малую мышечную массу, поэтому плохо справляется с перегрузками. Компенсаторные механизмы работы ПЖ недостаточно развиты, из-за чего под действием неблагоприятных факторов быстро нарушается механика работы сердца. Наиболее распространенные причины правожелудочковой сердечной недостаточности:
- Легочная гипертензия. Патология вызывает повышение сосудистого сопротивления в легочной ткани, на фоне которого развивается компенсаторная гипертрофия миокарда. По мере истощения адаптационных резервов сердца возникает хроническая форма правожелудочковой недостаточности.
- Острое возрастание постнагрузки.Тромбоэмболия легочной артерии является основной причиной острой недостаточности правой половины сердца. ПЖСН возникает у 25-30% пациентов с респираторным дистресс-синдромом, у четверти больных в раннем послеоперационном периоде после трансплантации сердца.
- Поражение миокарда ПЖ. Острая недостаточность сердца проявляется на фоне вирусных или бактериальных миокардитов, инфаркта стенки правого желудочка, посткардиотомического шока. Причиной хронических нарушений кровообращения выступают аритмогенные кардиомиопатии.
- Патологии клапанов. Причиной ПЖСН являются заболевания клапанного аппарата сердца, такие как недостаточность трикуспидального клапана, стеноз клапана легочной артерии. Они сопровождаются перегрузкой ПЖ и постепенным угнетением его сократительной способности.
Патогенез
Острая правожелудочковая недостаточность возникает при резком увеличении постнагрузки на ПЖ, в результате чего снижается ударный объем сердца и незначительно увеличивается систолическое давление. Происходит быстрое расширение полости правого желудочка, вследствие чего наблюдается регургитация крови через трикуспидальный клапан. При этом происходит смещение межжелудочковой перегородки, левый желудочек принимает D-образную форму.
При острой ПЖСН наблюдается повышенное давление в правых отделах сердца и застой в коронарном синусе, из-за чего развивается прогрессирующая ишемия. Увеличенное системное венозное давление приводит к нарушениям кровотока в органах брюшной полости, ухудшению функций печени и почек, застою жидкости. Прогрессирование таких нарушений в сочетании с усугубляющейся дисфункцией левого желудочка угрожает жизни пациента.
Хроническая правожелудочковая сердечная недостаточность (хПЖСН) выступает закономерным результатом постоянной перегрузки левой половины сердца. При длительно существующей левожелудочковой сердечной недостаточности сначала происходит компенсаторная гипертрофия и ремоделирование миокарда ПЖ, затем наблюдается декомпенсация заболевания. На позднем этапе хПЖСН происходит гибель кардиомиоцитов и замещение их фиброзной тканью.

В практической кардиологии используется несколько вариантов систематизации заболевания, что обусловлено его сложным патогенезом и многообразием клинических вариантов. По скорости развития симптоматики выделяют острую и хроническую форму патологии. Для постановки диагноза при хронической ПЖСН используется классификация Василенко-Стражеско, которая включает 3 стадии:
- Iстадия. Признаки нарушения функции правого желудочка возникают только при физической нагрузке. Отсутствует поражение внутренних органов.
- IIстадия. Характеризуется стойкими нарушениями гемодинамики и застойными явлениями в большом и малом кругах кровообращения. При стадии IIA наблюдается изолированная правожелудочковая недостаточность, на стадии IIB вовлекается вся кардиоваскулярная система.
- IIIстадия. На этом этапе имеющиеся расстройства кровообращения вызывают необратимые патологические изменения внутренних органов. Первыми при ПЖСН страдают почки, печень, легкие.
Симптомы правожелудочковой сердечной недостаточности
При острой форме заболевания развиваются признаки синдрома малого сердечного выброса: бледная кожа с мраморным оттенком, холодные конечности, слабый пульс. У больного резко снижается артериальное давление, уменьшается количество выделяемой мочи. На поражение ПЖ указывает расширение яремных вен, увеличение окружности живота вследствие асцита, массивные отеки голеней. При острой декомпенсации хронической ПЖСН возникает анасарка.
При хроническом варианте правожелудочковой недостаточности симптоматика развивается постепенно и отражает основной патологический процесс, негативно влияющий на работу ПЖ. Пациенты испытывают постоянную слабость, ухудшение работоспособности, снижение переносимости физических нагрузок. Возникает распирание и дискомфорт в животе, боли в области сердца, отеки на ногах. Во время активности наблюдается одышка, головокружение.
Поскольку хроническая форма болезни часто сопровождается недостаточностью ЛЖ, характерны симптомы застоя в малом круге. Пациенты жалуются на сильную одышку, приступы удушья и кашля, которые в основном возникают по ночам. Для облегчения самочувствия человек вынужден сидеть, слегка склонившись и опираясь на вытянутые руки. При кашле возможно выделение вязкой слизистой или кровянистой мокроты.
Осложнения
Обследование пациента у врача-кардиолога начинается с физикального осмотра. На вероятную ПЖСН указывает перкуторная гипертрофия правых камер сердца, усиление второго тона над клапаном легочного ствола, шум Грехема-Стилла. Визуально определяется пульсация шейных вен, отеки нижних конечностей, асцит. Для детального изучения функции сердца и подтверждения диагноза назначается:
- ЭКГ. По результатам электрокардиограммы определяется расширение комплексов QRS, увеличение высоты зубца Р, блокада правой ножки пучка Гиса. Характерны наджелудочковые аритмии в виде экстрасистол, эпизодов фибрилляции предсердий.
- ЭхоКГ. При УЗИ сердца обнаруживается гипертрофия стенок и расширение полости правого желудочка, наличие трикуспидальной регургитации, снижение показателя систолической экскурсии трикуспидального кольца (TASPE). Для уточнения данных выполняется трехмерная эхокардиография в режиме реального времени (RT3DE).
- Рентгенодиагностика. При рентгенографии органов грудной клетки определяется увеличение размеров и деформация контуров сердца, повышение прозрачности периферических отделов легких, выпячивание ствола легочной артерии. Для более точной визуализации внутрисердечных структур применяется КТ.
- Катетеризация сердца. Инвазивная диагностика назначается для измерения давления внутри ПЖ, оценки параметров заклинивания легочной артерии. Дополнительно проводится тест на вазореактивность для оценки степени тяжести легочной артериальной гипертензии.
- Анализы крови. Для подтверждения правожелудочковой сердечной недостаточности показано исследование уровня натрийуретических пептидов, кардиоспецифических тропонинов. Характерно повышение печеночных показателей (трансаминаз, билирубина), признаки почечной дисфункции (возрастание мочевины и креатинина).
При выявлении характерного симптомокомплекса и лабораторно-инструментальных данных диагноз ПЖСН не оставляет сомнений. Дифференциальная диагностика требуется на первой стадии болезни, когда выраженные органические признаки отсутствуют. Поскольку недостаточность правых сердечных камер зачастую связана с хроническими патологиями дыхательной системы, пациенту может потребоваться консультация пульмонолога.

Лечение правожелудочковой сердечной недостаточности
Консервативная терапия
Тактика ведения пациента зависит от формы заболевания. При острой сердечной недостаточности необходимо начинать лечебные мероприятия в кратчайшие сроки, чтобы поддержать функцию ПЖ, облегчить субъективные симптомы и предупредить жизнеугрожающие осложнения. Лечение проводится в отделении интенсивной терапии, включает следующие направления:
- Диуретики. В остром периоде всем пациентам назначаются петлевые мочегонные препараты для быстрого устранения перегрузки правого желудочка. При резистентных отеках терапию усиливают тиазидоподобными и калийсберегающими диуретиками.
- Вазопрессоры. Лекарства применяются для стабилизации показателей артериального давления, повышения сердечного выброса, нормализации межжелудочкового взаимодействия.
- Антикоагулянты. Препараты используются при ТЭЛА, тромбозах глубоких вен нижних конечностей и других тромбоэмболических процессах, возникающих на фоне правожелудочковой сердечной недостаточности.
- Оксигенотерапия. При гипоксемии назначается неинвазивная вентиляция легких для пациентов с сохраненной функцией самостоятельного дыхания. В случае критического состояния показано проведение эндотрахеальной интубации.
- Механическая поддержка кровообращения. Методика используется при отсутствии эффекта от фармакотерапии, Она включает экстракорпоральные системы поддержания жизнеобеспечения, имплантацию устройств вспомогательного кровообращения для правого желудочка.
Для коррекции хронического варианта болезни пациентам подбирается индивидуальная схема терапии. Чаще всего используются диуретики, бета-адреноблокаторы, ингибиторы АПФ и блокаторы рецепторов ангиотензина. При развитии хронического легочного сердца назначаются вазодилататоры из группы антагонистов эндотелиновых рецепторов, аналогов простациклина. Пациентам необходимо контролировать водный баланс, ограничить потребление поваренной соли.
Хирургическое лечение
Помощь сосудистых хирургов требуется при острой ПЖСН на фоне ТЭЛА. При отсутствии эффекта от тромболизиза или наличии противопоказаний к его проведению пациентам назначается оперативная легочная эмболэктомия для нормализации кровообращения в малом круге. После стабилизации состояния пациента рассматривается вопрос о проведении аортокоронарного шунтирования, если ПЖСН существует вторично на фоне левожелудочковой недостаточности.
Прогноз и профилактика
Вероятность полного выздоровления при острой ПЖСН зависит от причины ее возникновения и своевременности оказания медицинской помощи. Современные программы лечения хронической сердечно-сосудистой недостаточности увеличивают ожидаемую продолжительность жизни больных на 30-35%. Профилактика заболевания заключается в раннем выявлении и коррекции кардиоваскулярной и пульмонологической патологии.
2. Острая правожелудочковая недостаточность/ А.Е. Баутин, В.В. Островских // Вестник анестезиологии и реаниматологии. - 2018. - №5.
4. Современное ведение пациентов с острой правожелудочковой недостаточностью/ Н.Т. Ватутин, А.С. Смирнова, Г.Г. Тарадин// Практическая ангиология. - 2016. - №3.
Гипертрофическая кардиомиопатия
Гипертрофическая кардиомиопатия - первичное изолированное поражение миокарда, характеризующееся гипертрофией желудочков (чаще левого) при уменьшенном или нормальном объеме их полостей. Клинически гипертрофическая кардиомиопатия проявляется сердечной недостаточностью, болью в грудной клетке, нарушениями ритма, синкопальными состояниями, внезапной смертью. Диагностика гипертрофической кардиомиопатии включает проведение ЭКГ, суточного ЭКГ-мониторирования, ЭхоКГ, рентгенологического исследования, МРТ, ПЭТ сердца. Лечение гипертрофической кардиомиопатии проводится b-адреноблокаторами, блокаторами кальциевых каналов, антикоагулянтами, антиаритмическими препаратами, ингибиторами АПФ; в ряде случаев прибегают к кардиохирургической операции (миотомии, миоэктомии, протезированию митрального клапана, двухкамерной электрокардиостимуляции, имплантации кардиовертер-дефибриллятора).

В кардиологии различают первичные (идиопатические) кардиомиопатии (гипертрофическую, констриктивную, дилатационную, рестриктивную, аритмогенную дисплазию правого желудочка) и специфические вторичные кардиомиопатии (алкогольную, токсическую, метаболическую, климактерическую и ряд других).
Гипертрофическая кардиомиопатия - самостоятельное, не зависящее от других сердечно-сосудистых заболеваний, значительное утолщение миокарда левого (реже правого) желудочка, сопровождающееся уменьшением его полости, нарушением диастолической функции с развитием нарушений сердечного ритма и сердечной недостаточности.
Гипертрофическая кардиомиопатия развивается у 0,2-1,1% населения, чаще мужского пола; средний возраст пациентов составляет от 30 до 50 лет. Коронарный атеросклероз среди больных гипертрофической кардиомиопатией встречается в 15-25 % случаев. Внезапная смерть, вызванная с тяжелыми желудочковыми аритмиями (пароксизмальной желудочковой тахикардией), наступает у 50% пациентов с гипертрофической кардиомиопатией. У 5-9 % больных заболевание осложняется инфекционным эндокардитом, протекающим с поражением митрального или аортального клапана.

Гипертрофическая кардиомиопатия - заболевание с аутосомно-доминантным типом наследования, поэтому обычно носит семейный характер, что не исключает, однако, возникновение спорадических форм.
В основе семейных случаев гипертрофической кардиомиопатии лежат передаваемые по наследству дефекты генов, кодирующих синтез сократительных белков миокарда (гена тяжелой цепи b-миозина, гена сердечного тропонина Т, гена а-тропомиозина, гена, кодирующего сердечную изоформу миозин-связывающего белка). Спонтанные мутации этих же генов, происходящие под воздействием неблагоприятных факторов среды, обусловливают развитие спорадических форм гипертрофической кардиомиопатии.
Гипертрофия миокарда левого желудочка при гипертрофической кардиомиопатии не связана с врожденными и приобретенными пороками сердца, ИБС, гипертонической болезнью и другими заболеваниями, которые обычно приводят к подобным изменениям.
В патогенезе гипертрофической кардиомиопатии ведущая роль принадлежит компенсаторной гипертрофии сердечной мышцы, обусловленной одним из двух возможных патологических механизмов - нарушением диастолической функции миокарда или обструкцией выходного тракта левого желудочка. Диастолическая дисфункция характеризуется поступлением в желудочки недостаточного количества крови в диастолу, что связано с плохой растяжимостью миокарда, и обусловливает быстрый подъем конечного диастолического давления.
При обструкции выходного отдела левого желудочка имеет место утолщение межжелудочковой перегородки и нарушение движения передней створки митрального клапана. В связи с этим в период изгнания возникает перепад давления между полостью левого желудочка и начальным отрезком аорты, что сопровождается повышением конечного диастолического давления в левом желудочке. Возникающая в этих условиях компенсаторная гиперфункция сопровождается гипертрофией, а затем и дилатацией левого предсердия, в случае же декомпенсации развивается легочная гипертензия.
В ряде случаев гипертрофической кардиомиопатии сопутствует ишемия миокарда, обусловленная снижением вазодилататорного резерва коронарных артерий, увеличением потребности гипертрофированного миокарда в кислороде, сдавлением во время систолы интрамуральных артерий, сопутствующим атеросклерозом венечных артерий и т. д.
Макроскопическими признаками гипертрофической кардиомиопатии служит утолщение стенок левого желудочка при нормальных или уменьшенных размерах его полости, гипертрофия межжелудочковой перегородки, дилатация левого предсердия. Микроскопическая картина гипертрофической кардиомиопатии характеризуется беспорядочным расположением кардиомиоцитов, замещением мышечной ткани на фиброзную, аномальным строением интрамуральных венечных артерий.
В соответствии с локализацией гипертрофии выделяют гипертрофическую кардиомиопатию левого и правого желудочков. В свою очередь, гипертрофия левого желудочка может быть асимметричной и симметричной (концентрической). В большинстве случаев выявляется асимметричная гипертрофия межжелудочковой перегородки на всем протяжении или в ее базальных отделах. Реже встречается асимметричной гипертрофия верхушки сердца (апикальная гипертрофическая кардиомиопатия), задней или переднебоковой стенки. На долю симметричной гипертрофии приходится около 30 % случаев.
С учетом наличия градиента систолического давления в полости левого желудочка различают обструктивную и необструктивную гипертрофическую кардиомиопатию. Симметричная гипертрофия левого желудочка, как правило, представляет собой необструктивную форму гипертрофической кардиомиопатии.
Асимметричная гипертрофия может являться как необструктивной, так и обструктивной. Так, синонимом асимметричной гипертрофии межжелудочковой перегородки служит понятие «идиопатический гипертрофический субаортальный стеноз», гипертрофии средней части межжелудочковой перегородки (на уровне папиллярных мышц) - «мезовентрикулярная обструкция». Верхушечная гипертрофия левого желудочка, как правило, представлена необструктивным вариантом.
В зависимости от степени утолщения миокарда выделяют умеренную (15-20 мм), среднюю (21-25 мм) и выраженную (более 25 мм) гипертрофию.
На основании клинико-физиологической классификации выделяют IV стадии гипертрофической кардиомиопатии:
- I - градиент давления в выходном тракте левого желудочка (ВТЛЖ) не более 25 мм рт. ст.; жалобы отсутствуют;
- II - градиент давления в ВТЛЖ возрастает до 36 мм рт. ст.; появляются жалобы при физической нагрузке;
- III - градиент давления в ВТЛЖ увеличивается до 44 мм рт. ст.; появляются стенокардия, одышка;
- IV - градиент давления в ВТЛЖ выше 80 мм рт. ст.; развиваются выраженные нарушения гемодинамики, возможна внезапная сердечная смерть.
Симптомы гипертрофической кардиомиопатии
Длительное время течение гипертрофической кардиомиопатии остается бессимптомным, клиническая манифестация чаще происходит в возрасте 25-40 лет. С учетом преобладающих жалоб выделяют девять клинических форм гипертрофической кардиомиопатии: малосимптомную, вегетодистоническую, кардиалгическую, инфарктоподобную, аритмическую, декомпенсационную, псевдоклапанную, смешанную, молниеносную. Несмотря на то, что каждый клинический вариант характеризуется определенными признаками, всем формам гипертрофической кардиомиопатии присущи общие симптомы.
Необструктивная форма гипертрофической кардиомиопатии, не сопровождающаяся нарушением оттока крови из желудочка, обычно малосимптомна. В этом случае жалобы на одышку, перебои в работе сердца, неритмичный пульс могут отмечаться при выполнении физической нагрузки.
Типичными симптомами обструктивной гипертрофической кардиомиопатии служат приступы ангинозных болей (70%), выраженная одышка (90%), головокружения и обморочные состояния (25-50%), преходящая артериальная гипотензия, нарушения ритма сердца (пароксизмальная тахикардия, фибрилляция предсердий, экстрасистолия). Возможно возникновение приступов сердечной астмы и отека легких. Нередко первым эпизодом проявления гипертрофической кардиомиопатии служит внезапная смерть.
При диагностическом поиске обнаруживается систолический шум, высокий, скорый пульс, смещение верхушечного толчка. Инструментальные методы обследования при гипертрофической кардиомиопатии включают ЭхоКГ, ЭКГ, ФКГ, рентгенографию грудной клетки, холтеровское мониторирование, поликардиографию, ритмокардиографию. С помощью эхокардиографии выявляется гипертрофия МЖП, стенок миокарда желудочка, увеличение размеров левого предсердия, наличие обструкции ВТЛЖ, диастолическая дисфункция левого желудочка.
ЭКГ-признаки гипертрофической кардиомиопатии малоспецифичны и требуют дифференциальной диагностики с очаговыми изменениями миокарда, гипертонической болезнью, ИБС, аортальным стенозом и другими заболеваниями, осложняющимися гипертрофией левого желудочка. Для оценки тяжести гипертрофической кардиомиопатии, прогноза и выработки рекомендаций по лечению используются нагрузочные пробы (велоэргометрия, тредмил-тест).
Суточное мониторирование ЭКГ позволяет документировать пароксизмальные эпизоды желудочковой экстрасистолии и тахикардии, фибрилляции и трепетания предсердий. На фонокардиограмме регистрируется систолический шум различной степени выраженности, сохранность амплитуды I и II тонов. Сфигмография демонстрирует двухвершинную кривую каротидного пульса, характеризующуюся дополнительной волной на подъеме.
При рентгенологическом исследовании изменения контуров сердца (увеличение левых отделов сердца, расширение восходящей части аорты, выбухание ствола и расширение ветвей легочной артерии) обнаруживаются только в развернутой стадии гипертрофической кардиомиопатии. Для получения дополнительных данных за гипертрофическую кардиомиопатию прибегают к проведению зондирования левых отделов сердца, вентрикулографии, коронарографии, сканированию сердца с радиоизотопом таллия, МРТ, ПЭТ сердца. Окончательным подтверждающим методом служит генодиагностика.
Лечение гипертрофической кардиомиопатии
Пациентам с гипертрофической кардиомиопатией (особенно с обструктивной формой) рекомендуется ограничение физических нагрузок, которые могут спровоцировать увеличение градиента давления «левый желудочек-аорта», аритмии сердца и обмороки.
При умеренно выраженных симптомах гипертрофической кардиомиопатии назначают b-адреноблокаторы (пропранолол, атенолол, метопролол) или блокаторы кальциевых каналов (верапамил), уменьшающие ЧСС, удлиняющие диастолу, улучшающие пассивное наполнение левого желудочка и снижающие давление наполнения. В связи с наличием высокого риска развития тромбоэмболий необходим прием антикоагулянтов. При развитии сердечной недостаточности показаны диуретики, ингибиторы АПФ; при нарушениях желудочкового ритма - антиаритмические препараты (амиодарон, дизопирамид).
При обструктивной гипертрофической кардиомиопатии проводится профилактика инфекционного эндокардита, т. к. в результате постоянной травматизации передней створки митрального клапана на ней могут появляться вегетации. Кардиохирургическое лечение гипертрофической кардиомиопатии целесообразно при градиенте давления между левым желудочком и аортой >50 мм рт.ст. В этом случае может выполняться септальная миотомия или миоэктомия, а при структурных изменениях митрального клапана, вызывающих значительную регургитацию, - протезирование митрального клапана.
Для уменьшения обструкции ВТЛЖ показана имплантация двухкамерного электрокардиостимулятора; при наличии желудочковых нарушений ритма - имплантация кардиовертер-дефибриллятора.
Прогноз гипертрофической кардиомиопатии
Течение гипертрофической кардиомиопатии вариабельно. Необструктивная форма гипертрофической кардиомиопатии протекает относительно стабильно, однако при длительном стаже заболевания все же развивается сердечная недостаточность. У 5-10% пациентов возможен самостоятельный регресс гипертрофии; у такого же процента больных отмечается переход гипертрофической кардиомиопатии в дилатационную; еще столько же пациентов сталкивается с осложнением в виде инфекционного эндокардита.
Без лечения летальность при гипертрофической кардиомиопатии составляет 3-8 %, при этом в половине подобных случаев возникает внезапная смерть вследствие фибрилляции желудочков, полной атриовентрикулярной блокады, острого инфаркта миокарда.
Читайте также:
