Нервная система при церамидозе (липогрануломатозе, болезни Фарбера)
Добавил пользователь Владимир З. Обновлено: 21.01.2026
ГБУЗ МО «Московский областной научно-исследовательский институт им. М.Ф. Владимирского», Москва, Россия
Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского
Неврологические проявления при болезни Фабри
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2016;116(9): 98‑105
Болезнь Фабри (болезнь Андерсона—Фабри) — Х-сцепленная рецессивная лизосомальная болезнь накопления, возникающая вследствие недостаточной активности лизосомальной гидролазы (альфа-галактозидазы А), приводящей к прогрессирующей аккумуляции глоботриаозилцерамида (Gb3) в различных клетках, преимущественно эндотелиальных и клетках гладкой мускулатуры сосудов, с поражением органов, включая ЦНС. Болезнь Фабри проявляется прогрессирующей почечной и сердечной недостаточностью, нейропатической болью, инсультами, кожными и желудочно-кишечными симптомами. Клинические проявления начинаются в детстве, но диагностируются у многих пациентов только во взрослом возрасте. Женщины болеют также тяжело, как и мужчины. Возможен летальный исход вследствие раннего инсульта, болезней сердца и почек. Раннее распознавание симптомов, определение уровня активности ферментов, концентрации Gb3 в крови, моче, биопсия кожи, генетическое тестирование (GLA ген) позволяют осуществлять раннюю диагностику и фермент-заместительную терапию. Данная терапия способствует стабилизации или редуцированирю прогрессирования болезни. Раннее начало лечения позволяет предотвратить развитие осложнений.
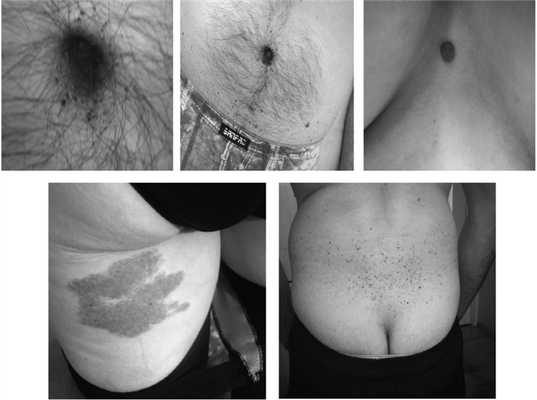
Примеры ангиокератомы у мужчин с «классической» болезнью Фабри.
В 1898 г. немецкий врач Дж. Фабри и английский У. Андерсон независимо друг от друга описали кожные изменения в сочетании с признаками поражения других органов у 2 пациентов мужского пола (мальчика и взрослого мужчины). В дальнейшем заболевание получило название «болезнь Фабри» или «болезнь Андерсона—Фабри» [1]. В 1967 г. Brady и соавт. открыли первичный биохимический дефект, лежащий в основе заболевания — недостаточность α-галактозидазы А, позднее в 1989 г. был секвенирован ген α-галактозидазы А, что дало возможность с помощью генно-инженерных методов синтезировать данный фермент in vitro и создать препараты для фермент-заместительной терапии заболевания. При болезни Фабри происходят мутации в гене GLA, расположенном на Х хромосоме и кодирующем фермент α-галактозидазу А. От больного мужчины мутантная Х-хромосома передается дочерям. Оставаясь, как правило, клинически здоровыми, дочери могут передать поврежденную хромосому и, следовательно, патологический аллель половине своих потомков. Однако женщины-носительницы также могут иметь проявления заболевания и в некоторых случаях столь же тяжелые, как и больные мужчины. Мужчины имеют одну Х-хромосому, следовательно, при наличии у мальчиков мутантной Х-хромосомы всегда развивается болезнь. Около 5% случаев связаны с так называемыми мутацииями de novo из-за чего болезнь Фабри может встречаться у людей, не имеющих отягощенного семейного анамнеза.
В результате мутации в гене α-галактозидазы, А при болезни Фабри имеется уменьшение активности данного фермента в лизосомах, результатом чего является неполное расщепление гликосфинголипидов. В результате этого в лизосомах откладываются нейтральные сфинголипиды и другие соединения. Основной накапливаемый субстрат — глоботриаозилцерамид (Gb3) [2]. Эти вещества накапливаются в гладкомышечных и эндотелиальных клетках сосудов; клетках ЦНС, роговицы, почек, сердечной мышцы. Накопление Gb3 начинается с раннего возраста, происходит поражение различных тканей и органов, повреждение имеет прогрессирующий характер и может быть необратимым. Дисфункция эндотелия и стенок сосудов с последующим воспалением вызывает обструктивные процессы, аналогичные атеросклеротическим поражениям [3]. Накопление Gb3 запускает процесс поражения иммунной системы с явлениями местного и общего воспаления, вызывающего повреждение органов [4].
Гомизиготные больные мужчины без резидуальной активности α-галактозидазы, А имеют выраженные неврологические (боль), кожные (ангиокератомы), почечные (протеинурия, почечная недостаточность), кардиоваскулярные (кардиомиопатия, аритмия), кохлеовестибулярные, цереброваскулярные (инсульты) проявления болезни. У гетерозиготных женщин симптоматика варьирует от слабой до ярко выраженной [1].
Симптомы заболевания можно разделить на ранние и поздние [5]. К ранним относятся акропарестезии; пониженноепотоотделение, приводящее к перегреванию и снижению переносимости жары; ангиокератомы, расстройства ЖКТ;дискомфорт, боль в кистях и стопах, появляющиеся при повышении окружающей температуры или при физических упражнениях [6]. Выделяются два типа болей: нейропатическая (акропарестезии) — постоянное жжение, покалывание, ощущение дискомфорта и кризы Фабри — периодически возникающие, сильные, жгучие, изнуряющие боли, продолжающиеся от нескольких минут до нескольких дней [7].
По мере прогрессирования болезни могут присоединяться следующие симптомы: повышенная утомляемость; желудочно-кишечные расстройства, образование дивертикулов в кишечнике [8—10]; головные боли; шум в ушах, снижение слуха [11, 12]; отеки голеней; боль в груди или сердцебиение.
Поздними осложнениями, определяющими смертность после 30 лет, являются: поражение почек [13, 14]; поражение сердца [15—17]; нарушения мозгового кровообращения [18—21].
В головном мозге отмечаются прогрессирующая многоочаговая окклюзия сосудов малого калибра, которая обусловливает клиническую симптоматику болезни вследствие ишемии и инфарктов в различных органах, изменение формы артерий, эндотелиальная дисфункция, явления тромбоза, церебральная гипоперфузия, кардиальные эмболы, повреждение белого вещества. Поражаются небольшие перфорантные артерии в перивентрикулярной области, области ствола мозга и базальных ганглиев. Для болезни Фабри специфичными являются пульвинарные кальцификаты. Вследствие отложения гликосфинголипидов в эндотелиальных клетках сосудов происходит замедление скорости кровотока [22, 23]. Также имеется неспецифическое поражение белого вещества головного мозга, нарастающее с возрастом, встречающееся одинаково часто у мужчин и женщин [24]. Субарахноидальные кровоизлияния при болезни Фабри встречаются редко [25], также как и асептический менингит [26].
У пациентов с болезнью Фабри в 10 раз чаще чем в популяции встречается обструктивная болезнь легких, характеризующаяся одышкой, хрипами в легких, сухим кашлем [27, 28]. Почечные, кардиоваскулярные, цереброваскулярные осложнения уменьшают на 20 и 10 лет продолжительность жизни у мужчин и женщин, не получающих заместительную терапию, по сравнению с популяцией соответственно [29].
При болезни Фабри преимущественно поражаются тонкие нервные волокна [30—33]. Клинически поражение тонких волокон проявляется в периодической боли и жжении в дистальных отделах конечностей [34], триггером может выступать повышение температуры окружающей среды. Помимо этого, дисфункция тонких миелиновых и безмиелиновых волокон может вызывать симпатические и парасимпатические расстройства. Симпатическая дисфункция объясняет гипогидроз, непереносимость физических упражнений и перегревания [35]. В отличии от нейропатии при других болезнях, при болезни Фабри страдает температурная чувствительность при сохранной вибрационной и тактильной [36]. Нейропатия при болезни Фабри также характеризуется поражением срединного нерва (в рамках туннельного синдрома), дисфункцией температурных афферентных волокон, при которой холодовая чувствительность нарушается больше, чем тепловая [37,38]. Описаны случаи нейропатии зрительного нерва [39—41]. Нейропатия тонких нервных волокон иногда может быть единственным симптомом болезни Фабри в зрелом возрасте [42]. Прямая зависимость между степенью выраженности боли и функционированием тонких безмиелиновых волокон отсутствует. По мере старения пациента и развития болезни боль может уменьшаться, в то время как функционирование волокон будет продолжать ухудшаться [43, 44].
Гетерозиготные пациентки с болезнью Фабри, даже без клинической манифестации заболевания, имеют периферическую нейропатию, подтверждаемую биопсией [45], однако при электронейромиографии патология может не выявляться [26]. Могут наблюдаться нарушения сна, обструктивное апное во время сна и связанные с нейропатической болью синдром «беспокойных ног» [46, 47]. Могут отмечаться кохлеовестибулярные расстройства, дисфункция вегетативной нервной системы [48, 49]. Пациенты имеют замедленные походку и движения рук. Однако у них отсутствуют двигательные экстрапирамидные симптомы, значительные когнитивные нарушения, гипоосмия, ортостатическая недостаточность, расстройства сна на стадии быстрого движения глаз, которые обычно имеются при нейродегенеративных заболеваниях.
Многие пациенты с болезнью Фабри находятся в состоянии постоянного стресса, связанного с болями, соматической патологией и психосоциальной стигматизированностью [50] они более подвержены депрессии, сонливы днем, имеют низкое качество жизни. Иногда отмечается наличие и более выраженной психической патологии, суицидальных попыток [50—52]. Однако выраженные когнитивные нарушения для болезни Фабри не характерны [53].
Сексуальная сфера у мужчин и автономная регуляция сердечно-сосудистой системы при болезни Фабри не страдают [54, 55].
Симптомы начинают проявлятся в детстве, а диагноз часто ставится только в развернутой стадии болезни у взрослых [56, 57]. В среднем проходит примерно 10 лет от начала появления симптомов до постановки диагноза [58]. Очень важно поставить правильный диагноз в детстве, чтобы начать раннюю заместительную терапию [59].
С болезнью Фабри связано одновременное поражение многих органов и систем [60]. Болезнь может мимикрировать под другую патологию, например, рассеянный склероз [61]. При наличии полиорганной патологии, необходимо шире подходить к проблеме и лечить не десяток одновременно протекающих болезней, а сосредоточиться на наследственном заболевании [62—65].
При наличии инсульта в раннем возрасте можно заподозрить болезнь Фабри, особенно при криптогенной этиологии, вертебробазилярной локализации, коморбидной дисфункции почек [66, 67].
Одним из ранних патогномоничных симптомов является мутовчатая кератопатия, легко обнаруживаемая при рутинном осмотре глаза с помощью щелевой лампы [68, 69]. Специфичными офтальмологическими проявлениями болезни Фабри являются патология сосудов конъюнктивы и сетчатки, помутнение роговицы и хрусталика. Как правило, они не вызывают значительного нарушения зрения, однако могут выступать в качестве маркеров болезни. Глаз является наружным органом легко доступным для изучения. Без применения инвазивных технологий. Он может использоваться для мониторирования протекания болезни и контроля за результатами лечения [70].
Дерматологическими проявлениями болезни Фабри являются ангиокератомы (см. рис.), телангиоэктазии, лимфодема, ангидроз или гипогидроз, псевдоакромегалические черты лица [71, 72]. Пациенты часто имеют характерный внешний вид, напоминающий больных с акромегалией — грубые черты лица, утопленный лоб, густые брови, выступающие супраорбитальные дуги и лобные бугры, выступающую нижнюю челюсть, увеличенные губы, широкую переносицу, грушевидный нос.
Снижение слуха отмечается у 90% пациентов. После 44 лет почти ни один больной не имеет нормального слуха [73].
Золотым стандартом диагностики болезни Фабри является определение активности лизосомного фермента α-галактозидазы, А в плазме, лейкоцитах, сыворотке крови, сухих пятнах крови, слезной жидкости, в любом биоптате или культуре клеток кожных фибробластов. У мужчин сниженная активность α-галактозидазы, А является достаточно информативным признаком болезни. Однако у 1/3 женщин с болезнью Фабри, а также у здоровых носителей активность этого фермента может быть нормальной, поэтому надежно исключить или подтвердить диагноз позволяет только генетический тест (секвенирование гена GLA). Также у всех гемизиготных и свыше 90% гетерозиготных носителей имеется в моче повышенный уровень Gb3. Для всех мужчин с пониженной активностью α-галактозидазы, А или атипичными симптомами болезни измерение уровня Gb3 в моче исеквенирование гена GLA являются обязательными [74]. При наличии мутации у пробанда необходимо проведение обследования всех его родственников, потенциально являющихся носителями мутантной X-хромосомы. Для мониторинга состояния пациента может использоваться количественное определение сфинголипидов, так как на фоне успешной патогенетической терапии происходит снижение их содержания в плазме.
Очень информативна диагностика заболевания у новорожденных [75, 76]. Возможна пренатальная диагностика с определением активности лизосомного фермента α-галактозидазы, А и секвенирование гена GLA в ворсинках хориона или культивированных амниотических клетках. Возможна предимплантационная диагностика [77].
Учитывая, что сильная нейропатическая боль, гипогидроз, нарушение холодовой перцепции характерны для болезни Фабри, их инструментальное тестирование может служить для оценки эффективности проводимого лечения [78, 79]. Для оценки степени выраженности и прогрессирования болезни у взрослых пациентов применяются также соответствующие шкалы: Mainz Severity Score Index (MSSI) и Fabry Outcome Survey Mainz Severity Score Index (FOS-MSSI) [80], а также стандартные опросники качества жизни пациентов [81].
Диффузионно-тензорная томография (ДТ МРТ, более чувствительна, по сравнению с рутинной МРТ, для обнаружения изменений в мозговой ткани при болезни Фабри. Она позволяет оценивать динамику болези и эффективность проводимой терапии [82]. С возрастом на МРТ обнаруживается ухудшение состояния нервной ткани [83].
При наличии органной патологии может применяться биопсия [84—86].
При болезни Фабри применяют симптоматическую терапию (обезболивающие препараты, гипотензивные средства, диализ, трансплантацию почек, искусственный водитель ритма, антидепрессанты) [87]. Для профилактики инсультов могут использоваться статины [88]. Для купирования нейропатической боли эффективны карбамазепин, фенитоин, габапентин [89].
Начиная с 2001 г. проводят фермент-заместительную терапию (ФЗТ) рекомбинантными препаратами α-галактозидазы, А [90]. Она позволяет уменьшить нейропатическую боль [91—97], улучшить функционирование различных типов нервных волокон иинтрадермальных рецепторов вибрации [98], также отмечается улучшение функции потооделения, переносимость жары, температурная чувствительность [99, 100]. Наблюдается положительная динамика при лечении синдрома беспокойных ног [101]. Кроме того при проведении заместительной терапии отмечается улучшение функционирования сердца [102—104]. Лечение эффективно при гипертрофии левого желудочка, [105, 106]. Заместительная терапия эффективна при легком и умеренном поражении почек, но неэффективна в тяжелых случаях (при протеинурии >1 г/сутки и грубом снижении уровня клубочковой фильтрации) [107—109]. При раннем начале лечения отмечается улучшение функционирования ЖКТ [110—112].
У пациентов с поздними стадиями болезни Фабри — при выраженном фиброзе и необратимом поражении органов, ФЗТ может быть неэффективна [113, 114], хотя есть данные [115], что ее раннее начало позволяет предотвратить поражение внутренних органов.
У некоторых больных, в ответ на введение данных препаратов, вырабатываются антитела класса IgG, что влияет на безопасность и эффективность лечения. При введении агалзидазы бета антител вырабатывается больше, чем при введении агалзидазы альфа. Антител класса IgE к агалсидазе альфа выявлено не было [122]. Лечение агалсидазой альфа в течении 10 лет предупреждает прогрессирование и уменьшает проявление кардиомиопатии при болезни Фабри, а также снижает накопление GB3 в миокарде [123]. При проведении ФЗТ происходят улучшения в течение заболевания, качестве жизни пациентов, а также снижается смертность. Согласно данным Программы оценки исходов болезни Фабри (FOS), медиана выживаемости у мужчин, получавших агалсидазу альфа в течении 5 лет составила 77,5 года, в сравнении с 60 годами у мужчин в контрольной группе, которые не получали заместительной ферментной терапии [124].
В настоящее время мужчинам с болезнью Фабри заместительная терапия показана сразу после установления диагноза. У мальчиков с бессимптомной болезнью Фабри лечение может быть начато в возрасте 10—13 лет, в то время как при наличии симптомов откладывать заместительную терапию не следует. У женщин показаниями к лечению считают выраженные симптомы или признаки прогрессирующего поражения органов-мишеней, в том числе хроническую нейропатическую боль в кистях и стопах, резистентную к стандартной терапии, персистирующую протеинурию, снижение скорости клубочковой фильтрации
В настоящее время развиваются новые терапевтические направления — лечение белками-шаперонами и генная терапия [126—134]. Также проводятся исследования комбинации сапосина В с модифицированной α-N-ацетил-галактозаминидазой [135]. Также рассматривается возможность использования энзимных активаторов и молекул, модифицирующих активность гена GLA [136].
Диагностика и комплексное лчение пациентов с болезнью Фабри требуют мультидисциплинарного подхода, включающего генетическое тестирование, интерпретацию тестов, генетическое консультирование, долговременное мониторирование симптомов болезни, выработку рекомендаций по лечению, координацию терапии проводимой врачами разных специальностей [137].
Липогранулематоз Фарбера
Липогранулематоз Фарбера - редкое наследственное заболевание. Описано американским педиатром Фарбером (S. Farber). Имеются сведения всего о 30 больных.
Что провоцирует / Причины Липогранулематоза Фарбера:
Липогранулематоз обусловлен отсутствием лизосомного фермента церамидазы, гидролизирующего жирную кислоту, прикрепленную к сфингозиновому стержню гликосфинголипидов. Доказан аутосомно-рецессивный тип наследования.
Патогенез (что происходит?) во время Липогранулематоза Фарбера:
Церамид накапливается в подкожных узлах, почках, где его содержание в 10 раз превышает норму, и печени, где концентрация повышена в 60 раз. При гистологическом исследовании в подкожных узлах определяется окрашиваемый реактивом Шиффа жирорастворимый материал.
Симптомы Липогранулематоза Фарбера:
Тяжесть течения болезни варьирует от легкой степени до тяжелой, характерно быстрое прогрессирование. Болезнь проявляется на третьем - четвертом месяце жизни. Характерными симптомами являются болезненное припухание суставов, в частности межфаланговых, метакарпальных, голеностопных, лучезапястных, коленных, локтевых. По мере прогрессирования развиваются сгибательные контрактуры голеностопных, лучезапястных суставов и суставов кисти. Наблюдается образование подкожных мягких узелков в области пораженных суставов. Подкожные узелки увеличиваются в размерах, локализуются также в местах давления - на затылке, в пояснично-крестцовой области, на конъюнктиве, ушной раковине, в области ноздрей и рта. В ряде случаев возможно их спонтанное исчезновение. Отмечаются охриплость голоса, которая может прогрессировать вплоть до афонии, нарушения глотания и дыхания (обусловлено наличием гранулем в области язычка и гортани), интермиттирующая лихорадка. Дети тяжело и шумно дышат, характерна гипертрофия.
Постоянными симптомами являются задержка психомоторного развития, психические расстройства, поражение периферических нервов. Прогрессирование заболевания сопровождается нарастанием дисфагии, повторными пневмониями, кахексией. Больные погибают обычно до 2-летнего возраста от легочных осложнений.
Диагностика Липогранулематоза Фарбера:
Диагноз подтверждается при выявлении снижения активности церамидазы в лейкоцитах и культивируемых фибробластах, характерных гранулематозных образований и макрофагов с включениями липидов в подкожных узлах, в печени, почках и других тканях. С помощью тонкослойной хроматографии из подкожных узлов можно выделить церамид и определить его количество по содержанию в нем сфингозина.
Дифференциальный диагноз проводится с ревматоидным артритом, гистиоцитозами Х и базируется в основном на данных биохимических исследований.
Лечение Липогранулематоза Фарбера:
Специфическое лечение не разработано. Для облегчения состояния больных применяют кортикостероиды. В связи с дыхательными нарушениями в ряде случаев прибегают к трахеостомии.
К каким докторам следует обращаться если у Вас Липогранулематоз Фарбера:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Липогранулематоза Фарбера, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Липоматоз
Липоматоз - это появление в подкожной клетчатке многочисленных липом, обладающих соединительнотканной капсулой или переходящих в область нормальной жировой ткани без четкой границы.
Что провоцирует / Причины Липоматоза:
Причины липоматоза не выяснены.
Патогенез (что происходит?) во время Липоматоза:
По распространению липоматоз может быть общим и местным (регионарным), по характеру процесса - диффузным, узловатым и диффузно-узловатым.
Развитие липоматоза связывают с локализованным дефектом липолиза (разрушения жировых отложений). Дискутируется роль заболеваний печени, поджелудочной железы, гипофункции щитовидной железы и гипофиза. Часто липоматоз развивается на фоне алкоголизма, диабета, злокачественных опухолей верхних дыхательных путей. Описываются семейные случаи с аутосомно-доминантным наследованием липоматоза. Липоматоз чаще развивается у мужчин. Основные симптомы развиваются медленно. В одних случаях с самого начала наблюдается формирование в подкожной клетчатке болезненных опухолей. В других - им предшествуют общая слабость, нарушения сна, памяти, головные боли и головокружения, неопределенные боли в разных частях тела. Могут наблюдаться ипохондрия, депрессивное состояние. Лишь в дальнейшем появляются опухоли. Липомы могут быть безболезненными, гистологически они соответствуют нормальной жировой ткани. Адипоциты липом проявляют большую устойчивость по отношению к липолитическим факторам, они не уменьшаются даже у исхудавших лиц. Описаны липомы, развивающиеся в пределах внутренних органов.
Симптомы Липоматоза:
Синдром Деркума. Для синдрома Деркума характерно развитие липом, проявляющих спонтанную или компрессионную болезненность. Этот синдром описывают как наследственную (возможно, с аутосомно-доминантным типом передачи) болезненную, часто симметричную гипертрофию жировой ткани на теле и конечностях в сочетании с адинамией, астенией, депрессией, кожным зудом. Болевые ощущения в области жировых скоплений, появляющиеся при пальпации или даже легком прикосновении, отличают синдром Деркума от других видов ожирения. Иногда болезненность определяется в участках жировой ткани, не принимающих формы опухолей. Такого рода болезненность подкожной клетчатки следует дифференцировать с ее поражением воспалительного характера.
Синдром Грама. Синдром Грама является одним из вариантов синдрома Деркума. Его обнаруживают преимущественно у женщин пожилого возраста. Патология характеризуется прогрессирующим ожирением с преимущественным отложением жира в области коленных суставов, деформирующим артрозом коленных суставов, кератодермией, чаще в области конечностей. К частым проявлениям синдрома относится артериальная гипертензия. Тип наследования - предположительно аутосомно-доминантный.
Синдром Маделунга. Синдром Маделунга является разновидностью наследственного множественного липоматоза (диффузная липома шеи, доброкачественный симметричный липоматоз, жирная шея Маделунга, синдром Лонуа-Бансода). Жировые разрастания охватывают переднебоковые и задние поверхности шеи, далее распространяются на подбородок и грудную клетку. Иногда отмечаются множественные симметричные липоматозные узлы на туловище и конечностях. Течение обычно медленное, но иногда наблюдается быстрый рост опухолей. Боль возникает при значительном увеличении количества жировой ткани, когда сдавливаются периферические нервы. Нарушается венозный отток, могут сдавливаться гортань, глотка, что проявляется расстройством дыхания, дисфагией, дизартрией, стенокардией, псевдомиопатией, постепенным нарастанием слабости в мышцах конечностей. Болеют преимущественно мужчины в возрасте 35-40 лет. Лабораторные сдвиги не обнаруживаются. При гистологическом обследовании выявляют скопления жировой ткани нормальной структуры. Тип наследования - аутосомно-доминантный.
Множественный липоматоз Роша-Лери. Множественный липоматоз Роша-Лери диагностируют обычно на четвертом десятилетии жизни. Липомы локализуются чаще в области верхних конечностей и ягодиц, реже - в других частях тела, в том числе в желудочно-кишечном тракте. Хромосомный анализ указывает на связь заболевания с нарушениями в участке 12q 13-14. Медико-генетическое консультирование аналогично таковому при синдроме Деркума. Близок к липоматозу Роша - Лери липоматоз врожденный диффузный, который наследуется по аутосомно-доминантному типу. Местами первоначальных и наиболее многочисленных поражений являются бедра и предплечья, иногда сочетается с гипертрофией мышц конечностей.
Липогранулематоз подкожный гипертонический. Это редкая и малоизученная форма, развивающаяся у тучных женщин, страдающих гипертонической болезнью. Характерно появление плотных, быстро увеличивающихся в размерах узлов на голенях и бедрах, которые могут подвергаться центральному размягчению и распаду.
Другие формы липоматоза. Липоматоз Вернея-Потена - доброкачественные узловые отложения в надключичной области. Липоматоз гипертрофический - происходит разрастание жировой ткани между атрофированными мышечными волокнами. Процесс генерализованный, симметричный. Развитие таких липом придает больному облик Геркулеса. Липоматоз ограниченный симметричный характеризуется появлением липоматозных узлов, до 3-4 см в диаметре и локализующихся в области рук, бедер, живота и поясницы. Возникает обычно в возрасте 35-40 лет, реже - в детском возрасте и в период полового созревания. Некоторыми авторами признается значение наследственного фактора в развитии этой формы. Липоматоз ладонный и липоматоз Пастера отличаются, соответственно, расположением липом на ладонной поверхности кистей и боковых поверхностях грудной клетки. Липоматоз сегментарный характеризуется сегментарным расположением липом. Диффузный липоматоз детского возраста наблюдается исключительно у детей, от ограниченного симметричного липоматоза отличается преимущественным развитием узлов на предплечьях и бедрах, нередко в сочетаниях с мышечной гипертрофией конечности.
Лечение Липоматоза:
Лечение липоматоза оперативное, после операции могут быть рецидивы. При диффузно-узловых формах развитая сосудистая сеть в липоматозных разрастаниях может явиться причиной кровотечений при операции. Лечение синдрома Деркума симптоматическое. При симптомах гипофункции отдельных эндокринных желез применяют соответствующие гормональные препараты. Назначают диету, препятствующую прогрессированию ожирения, а при нервно-психических нарушениях - психофармакологические средства. Хирургическое удаление отдельных узлов неэффективно, так как они обычно рецидивируют вблизи места операции или в других областях тела. Тем не менее оно может быть показано при резкой болезненности узлов, препятствующей функции того или иного сустава или ношению одежды.
К каким докторам следует обращаться если у Вас Липоматоз:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Липоматоза, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Болезнь Деркума ( Адипозалгия , Болезненный липоматоз , Болезненный фибролипоматоз , Нейролипоматоз )
Болезнь Деркума - это нейроэндокринное заболевание, основными клиническими проявлениями которого являются единичные или множественные диффузно-локализованные жировые образования, адинамия, астенизация пациента, депрессия. Рост липом сопровождается компрессионно-ишемическим повреждением кожных ветвей периферических нервов, что проявляется хроническими болями, чувством онемения пальцев, неловкостью движений. Диагноз ставится на основании анамнеза и комплексного обследования. Консервативное лечение предполагает назначение анальгетиков, кортикостероидов, цитостатиков, сеансов гипербарической оксигенации. Крупные липомы удаляются хирургическим путем.
МКБ-10
Общие сведения
Для обозначения патологии используется ряд синонимичных терминов: синдром Деркума, болезненный липоматоз, нейролипоматоз, болезненный фибролипоматоз, липалгия, адипозалгия, болезненное ожирение. Заболевание было описано в 1888 году американским невропатологом и психиатром Френсисом Ксавьером Деркумом. С тех пор исследователи мало продвинулись в понимании механизмов развития заболевания. Диагностируется липалгия у женщин 25-60 лет. В 85% наблюдений первые симптомы появляются у пациенток до наступления менопаузы. Описаны случаи нейролипоматоза у мужчин молодого и среднего возраста. Соотношение заболевших лиц женского и мужского пола составляет 20:1.
Причины
Малое число наблюдений, позднее выявление больных, диагностические ошибки вследствие разнообразия проявлений системных патологических процессов затрудняют проведение систематических исследований по изучению болезни Деркума, причин его развития. В настоящее время существует несколько научных теорий, выделяющих в качестве ведущей причины следующие факторы:
- Наследственная предрасположенность. Предполагается, что болезнь Деркума наследуется по аутосомно-доминантному типу. Исследование выборки ключевых пациентов позволило проследить развитие заболевания по линии «бабушка-мать-дочь». Однако большинство случаев, особенно у мужчин, развивается спорадически, что может свидетельствовать о спонтанно возникающих мутациях или же о вариативности экспрессии генов, ответственных за развитие липалгии.
- Метаболические нарушения. Одним из механизмов развития болезненного ожирения может быть патология обмена липидов на фоне дисбаланса гормонов. Ключевую роль в этом процессе по одной из рабочих гипотез отводят нарушениям в обмене С18 жирных кислот. Поражение щитовидной железы и гипофиза ряд исследователей считает вторичным по отношению к неврологическим нарушениям.
- Аутоиммунные процессы. Системный характер поражения дает основания исследователям предполагать аутоиммунную природу болезни, такую же, как у ревматоидного артрита или системной красной волчанки. Единственное отличие между этими заболеваниями в том, что поражается не соединительная, а преимущественно жировая ткань.
- Неврологические нарушения. Ряд авторов основное значение в генезе синдрома Деркума отводит поражению нервных центров высших отделов ЦНС. Не исключено влияние на обмен липидов синдрома диэнцефальных расстройств, для которого характерен целый комплекс обменных, вегетативных, эндокринных нарушений.
Есть указания на связь липоматоза с аллергическими, инфекционными заболеваниями, состояниями, связанными с гормональной перестройкой организма (беременность, менопауза). Поражение гипоталамуса, как пусковой фактор развития патологии, может быть следствием черепно-мозговой травмы, перенесенного энцефалита. Описаны случаи дебюта болезни Деркума после хирургических операций.
Патогенез
Нарушение гуморальной регуляции обмена липидов при синдроме Деркума является следствием дегенеративно-дистрофических изменений в тканях желез внутренней секреции. Больше прочих страдают надпочечники, щитовидная железа, гипофиз. Кистозное перерождение, склероз, дистрофия паренхимы приводят к снижению выработки гормонов, регулирующих обменные процессы.
Локальные скопления гипертрофированных адипоцитов активно васкуляризуются и дают начало множественным быстрорастущим ангиолипомам. Жировые депозиты сдавливают нервные стволы, развивается нейропатия. Это в сочетании с сопутствующей симпатической дизрегуляцией провоцирует появление локальных болей, которые не купируются обычными анальгетиками. Нарушение циркуляции крови по артериолам и венулам кожи вследствие компрессии часто становится причиной формирования рубцов и диффузных уплотнений.
По мере прогрессирования неврологических и эндокринных нарушений развиваются изменения со стороны органов и тканей. Потеря плотности костной ткани приводит к остеопорозу. Вторичные дистрофические изменения симпатических нервных узлов проявляются нарушениями потоотделения, снижением настроения, мышечной слабостью. Из-за хронического болевого синдрома у больного нарушается процесс засыпания, развиваются тревожные расстройства, депрессия.
Классификация
В клинической дерматологии разработано и применяется несколько классификаций болезни Деркума. Наиболее полной считается классификация, составленная в 2011 году Ханссоном и соавторами на основе наблюдения за 111 пациентами с липалгией. В ее основу положено наличие болезненных липом и преимущественная локализация болей. Согласно этой классификации выделяют 4 формы заболевания:
- Генерализованная диффузная. Болевые ощущения не имеют четкой локализации, не связаны с липомами, охватывают всю жировую ткань. При этом четко очерченных ангиолипом у пациента может не быть.
- Генерализованная узловая.Липомы множественные. Боли в области липом интенсивные, усиливаются при надавливании. Умеренная или незначительная болезненность отмечается в жировой ткани вне мест расположения ангиолипом.
- Локализованная узловая. Болевые ощущения локализуются в области жировых депозитов и в окружающей их ткани.
- Юкста-артикулярная. У пациента выявляются одиночные липомы, которые располагаются преимущественно в области крупных суставов.
Симптомы болезни Деркума
Местные проявления
В большинстве случаев первыми проявлениями нейролипоматоза являются жировые натечники, которые образуются под кожей без видимой причины и могут самопроизвольно исчезать, оставляя после себя уплотнения или наплывы кожи, белые стрии. Липомы могут располагаться на любом участке тела, часто бывают множественными. На одном и том же участке натечники могут формироваться повторно, в том числе и после их хирургического удаления. Одновременно с жировыми депозитами неправильной формы развивается общее ожирение. При отсутствии характерных жировых уплотнений диагностика заболевания затруднена, врачу сложно судить о реальной тяжести состояния пациента.
Болевой синдром
Иногда на первый план в клинической картине выходит болевой синдром. Он может иметь разную степень интенсивности, циклическую вариабельность. Боль описывается как ноющая, жгучая или колющая. Она усиливается при прикосновении и нажатии. Преимущественная локализация болевых ощущений: внутренние поверхности плеч и бедер, живот, ягодицы, область «галифе». Болезненные ощущения могут отмечаться в области лица, кистей рук, аногенитальной области.
Способствует уменьшению боли сухое тепло, прием горячей ванны. Усиление болей отмечается в период менструаций, при смене погоды, в холодное время года. Спровоцировать усиление неприятных ощущений могут инфекционные заболевания, даже такие безобидные, как ОРВИ. Одновременно с болями в области ангиолипом и подкожной жировой клетчатки могут отмечаться оссалгии длинных трубчатых костей конечностей, крупных суставов, головные боли. Свои ощущения в стопах некоторые больные описывают как «хождение по стеклу».
Общие симптомы
На фоне хронических болей у пациента развивается бессонница, тревожное расстройство, отмечается снижение настроения вплоть до депрессии. Астенический синдром проявляется общей слабостью, которая резко усиливается при незначительных нагрузках, снижением работоспособности. У некоторых пациентов помимо жировых натечников образуются скопления жидкости в различных областях тела. Отеки сходят в результате лечения, но могут спонтанно появиться снова.
Дебют заболевания, обострение болезни Деркума может ознаменоваться лихорадкой неясного генеза. Температура тела может подняться до 37,5-39 ° C и держаться на этом уровне в течение нескольких недель. Может присоединиться онемение пальцев, скованность движений в первой половине дня. В тяжелых случаях на фоне ухудшения общего состояния развивается оглушение или летаргия. Прогрессирует заболевание в течение десятилетий, но под воздействием провоцирующих факторов больной может потерять трудоспособность за пару месяцев. Возможны кратковременные периоды ремиссии.
Осложнения
Подкожные ангиолипомы не угрожают жизни больного, чего не скажешь про жировики, расположенные в области легких и сердца. Легочные осложнения являются ведущей причиной смерти у пациентов с адипозалгией. Поражение сердечной мышцы приводит к недостаточности кровообращения, что дополнительно усугубляет состояние больного.
На фоне системного патологического процесса часто развиваются психические нарушения: психоорганический синдром, деменция, психотические явления. Нервно-психические расстройства неуклонно прогрессируют вместе с основным заболеванием. Лечение синдрома Деркума уменьшает выраженность психотических явлений, однако часть пациентов нуждается в помощи психиатра даже в период ремиссии по основному заболеванию.
Диагностика
Специфических тестов для выявления болезни Деркума не разработано. Диагноз липалгии ставится методом исключения других заболеваний со сходной симптоматикой. Дифференциальная диагностика проводится с болезнью Маделунга, ВИЧ-ассоциированной липодистрофией, множественным симметричным липоматозом. Комплекс лабораторных и инструментальных тестов включает:
- Анализы крови и мочи. На усмотрение специалиста больному могут быть даны направления на проведение общего и биохимического анализов мочи, определение уровня гормонов, маркеров воспаления. Перечень обследований у дерматолога, эндокринолога и хирурга может существенно разниться в зависимости от предполагаемых диагнозов, сопутствующей патологии, возможных осложнений.
- Магнитно-резонансная томография. Пациенту может быть назначено МРТ головного мозга для выявления патологических изменений в ЦНС, МРТ грудной клетки при подозрении на наличие липом в области сердца, легких, МРТ мягких тканей для проведения дифференциальной диагностики доброкачественных и злокачественных новообразований.
- Ультразвуковая диагностика. С целью выявления ангиолипом, подтверждения диагноза болезненного фиброматоза, определения показаний для оперативного лечения проводится УЗИ мягких тканей. Повысить информативность исследования позволяют методики эластографии и цветного доплеровского картирования.
Основными диагностическими критериями нейролипоматоза является ожирение и хроническая боль в подкожной клетчатке длительностью более 3 месяцев. Подкожные скопления жира и другие симптомы не являются обязательными и могут присоединиться позже.
Лечение болезни Деркума
Наиболее подходящий метод терапии подбирается с учетом формы основного заболевания, наличия сопутствующей патологии, имеющихся осложнений. На начальных этапах с одинаковым успехом могут быть использованы и консервативные, и хирургические методы лечения, особенно в тех случаях, когда ангиолипомы расцениваются человеком как заметный косметический дефект.
Немедикаментозное лечение
Больному рекомендована диета, направленная на снижение массы тела, физические нагрузки, релаксационные техники для уменьшения физического дискомфорта и психологического напряжения, прием теплых ванн. Цель воздействий - нормализация веса, процесса засыпания. Курсами может выполняться массаж, сеансы акупунктуры, парафино- или озокеритотерапия. В состоянии ремиссии или невыраженного обострения показано санаторно-курортное лечение.
Медикаментозное лечение
Особенностью синдрома Деркума является его низкая чувствительность к большинству лекарственных препаратов. В связи с этим дерматологу приходится менять схемы лечения для подбора наиболее эффективной. В число основных групп лекарственных препаратов для лечения нейролипоматоза входят:
- Анальгетики. Эффект от системного применения нестероидных противовоспалительных препаратов, как правило, неудовлетворительный. Для уменьшения болевых ощущений применяются пластыри с лидокаином, обкалывание липом местными анестетиками. Обработка больших по площади областей может проводиться с помощью спреев или кремов местноанестезирующего действия.
- Цитостатики. Больным могут назначаться метотрексат и инфликсимаб. В научной литературе описаны единичные случаи удовлетворительного результата такого лечения. Ограничивает широкое применение цитостатиков большое количество осложнений и побочных реакций.
- Глюкокортикостероиды. Метилпреднизолон для лечения болезни Деркума вводится местно, поэтому он может применяться только при локализованных формах заболевания. Эффект использования кортикостероидов непредсказуем. Препараты могут снизить уровень болевых ощущений или же наоборот существенно усилить болезненность в тканях.
- Витамины. Длительный прием левокарнитина способствует нормализации жирового обмена и массы тела, повышает эффективность диеты и занятий спортом. Применение препарата в комплексном лечении синдрома Деркума способствует уменьшению болевых ощущений, препятствует образованию липом.
Косметологические процедуры
Эндермология LPG - это разновидность аппаратного массажа, который предполагает воздействие на кожу, подкожную клетчатку и мышцы специальных моторизованных роллеров. По своему воздействию на ткани метод сравним с липосакцией и может быть использован для устранения жировых уплотнений при болезни Деркума. Сведений об устранении болевого синдрома методом LPG-массажа недостаточно для того, чтобы рекомендовать его широкому кругу лиц.
Хирургическое лечение
Оперативное устранение симптомов болезни может проводиться на ранних стадиях в том случае, если анальгезирующие препараты не купируют болевой синдром или есть противопоказания к их применению. Хирургические вмешательства технически несложные, однако требуют подготовки больного, у которого на фоне нарушения работы эндокринной системы могут развиться нежелательные реакции. Хирургическое лечение проводится двумя способами:
- Липосакция. Метод позволяет устранить неэстетичные наплывы жира, скорректировать контуры тела и одновременно уменьшить выраженность болевого синдрома. При помощи канюли врач во время процедуры повреждает нервные волокна, проходящие в подкожной жировой ткани, что разрывает непрерывную цепь патологической нервной импульсации и устраняет боли.
- Хирургическое удаление липом. Во время операции могут быть удалены жировики, имеющие капсулу. Образования без четких границ лучше удалять методом липосакции. Проводится вмешательство под местной анестезией в амбулаторных условиях. Все манипуляции выполняются через небольшие разрезы кожи, чтобы избежать заметного рубцевания.
Экспериментальные методики
Получены удовлетворительные результаты лечения синдрома Деркума методом гипербарической оксигенации. Метод был испробован на добровольцах, страдающих нейролипоматозом. Пневматическое вытеснение жидкости из патологического очага приводит к уменьшению локальных отеков, способствует восстановлению нормального кровообращения, уменьшению кислородного голодания тканей. Это позволяет снизить выраженность болевых ощущений, замедлить прогрессирование системных нарушений болезни.
Прогноз и профилактика
Болезнь Деркума имеет хроническое прогредиентное течение. Ремиссии, как правило, нестойкие. Самопроизвольный регресс отдельных элементов не свидетельствует о выздоровлении. Выраженный болевой синдром, связанная с ним адинамия, нарушение общего состояния пациента приводят к утрате трудоспособности, нарушению социальных контактов. Своевременно поставленный диагноз, хирургическое удаление жировых скоплений, сдавливающих нервные узлы и стволы, предотвращает развитие вторичных дегенеративных изменений в периферической нервной системе. Это улучшает прогноз, повышает эффективность мероприятий, направленных на купирование нейропатической боли.
1. Ультразвуковая диагностика липом мягких тканей с использованием методик цветного допплеровского картирования и эластографии/ Вецмадян Е.А., Труфанов Г.Е., Рязанов В.В., Мостовая О.Т., Новиков К.В., Караиванов Н.С.// Вестник российской военно-медицинской академии. - 2012 - №2.
2. Клинический случай поздней диагностики нейролипоматоза (болезни Деркума)/ Шнайдер Н.А., Киселев И.А., Дмитренко Д.В.// Нервно-мышечные болезни. - 2013 - №2.
4. Review of Dercum’s disease and proposal of diagnostic criteria, diagnostic methods, classification and management/ Emma Hansson, Henry Svensson, Hakan Brorson// Orphanet Journal of Rare Diseases. - 2012.
Нейрофиброматозы
Нейрофиброматозы - наследственные заболевания, характеризующиеся образованием доброкачественных опухолей в коже, мягких тканях, нервной системе и внутренних органах. Выделяют 6 типов нейрофиброматозов, клинически значимы типы I и II. Общие симптомы включают нейрофибромы на коже, опухоли спинномозговых корешков, слуховых и зрительных нервов, пигментные пятна, костные деформации. Диагностика основана на данных осмотра пациентов, выявлении опухолей с помощью МРТ и КТ спинного и головного мозга, внутренних органов. Лечение симптоматическое - проводится резекция опухолей, рентгенотерапия, химиотерапия.
Нейрофибромы - доброкачественные опухоли, развивающиеся из оболочек нервных волокон. Чаще всего располагаются в слоях кожи и подкожной клетчатке, иногда поражают головной мозг, нервные волокна, корешки спинного мозга, мягкие ткани, внутренние органы. Нейрофиброматоз - болезнь, при которой образуются многочисленные нейрофибромы. Распространенность разных типов патологии значительно колеблется: заболеваемость 1 типом составляет 1:2 500, 2 типом - 1:50 000. Другие варианты встречаются еще реже, их точная эпидемиология не определена. Гендерной и расовой предрасположенности не выявлено. Дебют клинических проявлений возможен в любом возрасте, зависит от типа болезни.
Причины нейрофиброматозов
Образование множественных нейрофибром детерминировано генетически. При нейрофиброматозе I существует мутация гена НФ1, расположенного на длинном плече 17 хромосомы. Он относится к генам-супрессорам роста опухолевых тканей, большая часть из которых - нейроэктодермального генеза. При дефекте в гене НФ1 нарушается синтез белков, ответственных за клеточную пролиферацию. Мутации носят характер транслокаций, делеций, инверсий, точковых изменений. Больше 80% из них приводят к синтезу нефункциональных белков или к полному отсутствию белковых молекул. Наследование происходит по аутосомно-доминантному механизму с высокой степенью пенетрации: при наличии мутационного гена у одного из родителей вероятность болезни у ребенка составляет 50%, если оба родителя имеют мутацию, риск повышается до 80-90%. Известны случаи спонтанных мутаций.
Причиной нейрофиброматоза II является мутационное изменение гена НФ2, локализованного на 22 хромосоме. Он кодирует производство белка мерлина (шванномина) - супрессора опухолевого роста. Тип наследования - аутосомно-доминантный с небольшой степенью пенетрации. Передача одного мутантного гена зачастую не проявляется, поскольку второй ген обеспечивает синтез достаточного количества белков. Если он повреждается, синтез нормальных фракций мерлина прекращается, пролиферация клеток усиливается, развивается новообразование. При других типах нейрофиброматозов также существуют мутации в генах, обеспечивающих воспроизведение молекул белков-супрессоров роста опухолей.
Общим патогенетическим механизмом развития нейрофиброматозов является наследственно обусловленная недостаточность какого-либо белка, подавляющего процессы опухолевой пролиферации клеток в тканях нейроэктодермального происхождения. При мутации одного гена производство опухолевых супрессоров прекращается наполовину, равновесие роста и гибели клеток смещается в сторону митотического деления. Нормальный аллельный ген частично компенсирует дефицит белка. Тяжесть нейрофиброматоза определяется тем, насколько дефектный ген влияет на активность белка-супрессора - частично или полностью нарушает функциональность, полностью блокирует производство. Кроме этого, выраженность клинических признаков зависит от сохранности противоопухолевого иммунитета.
Во многих органах и тканях пациентов формируются доброкачественные опухолевые образования, состоящие из соединительной ткани и пигментных клеток. На нервных стволах образуются невриномы; на поверхности кожи - пигментированные области, жировые бляшки, расширенные сосуды; на сетчатке глаз - факоматоз. Изменяется строение костей, они остаются недоразвитыми либо чрезмерно утолщаются, искривляется позвоночный столб.
Симптомы нейрофиброматозов
Заболевания проявляются признаками поражения кожи, нервной системы. Классическим клиническим вариантом является нейрофиброматоз типа I, на долю которого приходится 90% случаев болезни. Характерный симптом - гиперпигментация. У больных при рождении или в раннем детстве появляются кожные пятна, цвет которых варьируется от светло-золотистого до коричневого «кофе с молоком». В отдельных случаях пятна имеют фиолетовый или синий оттенок. На радужке глаза обнаруживаются узелки Лиша (пятна пигмента - гамартомы) небольшого размера, белесоватые или светло-бежевые, заметные только при офтальмологическом осмотре. Являются специфическим признаком нейрофиброматоза 1, образуются по мере взросления: у детей до 4 лет распространенность составляет 22%, с 5 до 9 лет - 41%, с 10 до 19 лет - 85%, после 20 лет - 95%.
В период пубертата и позже формируются кожные и плексиформные нейрофибромы, располагающиеся соответственно подкожно (на мелких нервных волокнах, иннервирующих кожу) и на крупных нервах. Они представляют собой небольшие доброкачественные новообразования. Кожные нейрофибромы воспринимаются как косметический дефект, при определенном расположении травмируются. Плексиформные опухоли, локализующиеся по ходу периферических нервов, выявляются на конъюнктиве, веках, в брюшной полости и средостении. Проявляются хронической болью, онемением, судорогами, параличом. Опухоли ЦНС находятся внутри черепа, представлены глиомами зрительных нервных волокон, астроцитомами, эпендимомами, невриномами слухового нерва, менингиомами и нейрофибромами. Клиническая картина определяется размерами новообразований, вовлеченностью мозговых структур в патологический процесс. В детском возрасте диагностируются расстройства психического развития: снижение когнитивных способностей, гиперактивность, редко - деменция.
При тяжелом нейрофиброматозе деформируется костная система. У больных возникает сколиоз, краевые структурные изменения тел позвонков и их отростков, эрозийные поражения краев межпозвоночных отверстий и задних ребер. Характерна атрофия либо, наоборот, гипертрофия трубчатых костей. Кости часто искривлены, на поверхности обнаруживаются периостальные гребни и наслоения. В полостях костей могут образовываться нейрофибромы. Если в процесс вовлекаются кости черепа, появляется внешняя асимметрия, наиболее выраженная при поражении лицевой части и глазниц. Свод черепа может иметь атрофированные участки, дефекты, узуры, иногда отмечается локальное увеличение костного вещества.
При типе 2 формируются высокодифференцированные опухоли, которые, однако, более агрессивны, чем при заболевании 1 типа. Пигментных пятен нет. Образуются невриномы - подвижные и болезненные неоплазии. Нередко они локализуются на слуховом нерве, вызывая потерю слуха. Нейрофиброматоз 3 типа отличается большим количеством нейрофибром, ускоренным развитием нейролемм и глиом зрительного нерва, приводящих к расстройству зрения. Специфический признак - появление нейрофибром на ладонях. При болезни 4 типа симптомы похожи, сохраняется риск поражения зрительных волокон. Для 5 типа характерны пигментные темные пятна, опухоли больших размеров, провоцирующие асимметрию тела. Течение 6 типа сопровождается лишь пигментными пятнами. При 7 типе выявляются нейрофибромы средних размеров, гиперпигментации нет.
В 10% случаев нейрофибромы трансформируются в злокачественные опухоли. В группе высокого риска находятся пациенты с большим катамнестическим стажем, беременные женщины. У 6% детей нарушается умственное развитие: они имеют проблемы при освоении учебных навыков (чтение, письмо, счет), с трудом запоминают новую информацию, долго адаптируются в незнакомых ситуациях. Больные всех возрастов подвержены депрессии, поскольку испытывают дискомфорт, чувство стыда и неловкости из-за обезображенной внешности. Множественные нейрофибромы провоцируют эндокринные расстройства, эпилептические припадки, гипотонию мышц, стеноз почечной и легочной артерии, легочные кисты, интерстициальную пневмонию, гипертрофию клитора, нарушения развития органов ЖКТ.
Подозрение на нейрофиброматоз возникает при множественных подкожных опухолях, пигментных пятнах, спинальной шванноме, ухудшении слуха и зрения. Обследование проводят дерматовенеролог, невролог, офтальмолог, отоларинголог и генетик. Перед инструментальными и лабораторными процедурами осуществляется сбор семейного и личного анамнеза, клинический опрос и осмотр. В ходе генеалогического анализа выявляется передача заболевания в нескольких поколениях, реже определяется первичная спонтанная мутация. На теле пациентов обнаруживаются нейрофибромы, пигментные области (при определенных типах болезни), искривления позвоночника, деформации костей, нарушения зрения, слуха, координации движений. Производится дифференциальная диагностика различных вариантов нейрофиброматозов, исключается синдром Протея, рассеянный липоматоз, синдром Клиппеля-Треноне-Вебера. Для уточнения диагноза назначаются:
- МРТ, КТ. Визуализационные методы исследований позволяют определить наличие нейрофибром в головном мозге, позвоночнике, внутренних органах. Двусторонние невриномы 7 пары черепных нервов являются диагностическим критерием нейрофиброматоза II типа. Часто выявляются глиомы, шванномы, менингиомы. Для I типа свойственно развитие плексиформных и обычных новообразований, глиом.
- Рентгенография костей скелета. Диагностическая процедура выполняется с целью подтверждения и оценки тяжести сколиоза, костных атрофий и гипертрофий, локальных утолщений и эрозийных поражений костных структур. При большинстве типов болезни наблюдается истончение кортикального слоя, ложные суставы, дисплазии крыльев клиновидной кости, дугообразное искривление большеберцовой и малоберцовой костей, кисты длинных костей.
- Офтальмологическое исследование. Нейрофиброматоз типа 1 сопровождается плексиформной нейрофибромой век, меланоцитарными гамартомами радужки, глиомой оптических нервных волокон, астроцитарной гамартомой сетчатки, утолщением роговичных нервов, конъюнктивальной нейрофибромой, ишемическими поражениями венул сетчатки. Патогномоничный признак - пятна светлого оттенка на глазном дне и радужке (гамартомы). При 2 типе диагностируется задняя субкапсулярная катаракта, помутнение хрусталика.
- Аудиологическое исследование. При опухолевом поражении слуховых нервов и жалобах на нарастающую глухоту (тугоухость) выполняется электрокохлеография и импедансометрия. Результаты указывают на снижение остроты слуха, наличие слуховой нейропатии, определяют причину и локализацию нарушения.
Лечение нейрофиброматозов
В настоящее время терапия данной группы заболеваний заключается в симптоматической помощи больным. Пациенты регулярно проходят обследования, нацеленные на контроль формирования и увеличения опухолей. При наличии нейрофибром, провоцирующих боль, расположенных в местах повышенного риска травмирования, сдавливающих или смещающих жизненно важные органы, проводится их хирургическое удаление. Применяются классические методики резекции неоплазий и участков нервов, криодеструкция, лазерная хирургия. При множественных новообразованиях назначается лучевая терапия, химиотерапия. Больным с поражением опорно-двигательного аппарата показаны реабилитационные мероприятия (физиолечение, ЛФК).
Активно разрабатываются способы этиологического лечения нейрофиброматозов. На стадии клинических испытаний находится терапия ингибиторами RAS (белков-активаторов роста опухолей) у лиц с нейрофиброматозом первого типа. Этап теоретических разработок проходят методы генной инженерии. Усилия ученых-генетиков направлены на создание и внедрение в организм больных нормального НФ1 гена, отвечающего за синтез нейрофибромина, на расшифровку и введение гена ФН2, обеспечивающего транскрипцию белка шванномина. В некоторых медицинских центрах предпринимаются попытки применения патогенетической терапии, в основе которой лежит комплексное использование стабилизаторов мембран тучных клеток, антипролиферативных препаратов и ферментов, корректирующих метаболические процессы.
Нейрофиброматозы являются прогностически благоприятными заболеваниями - малигнизация опухолей происходит редко, в большинстве случаев больные остаются трудоспособными и социально адаптированными. При правильных и регулярных реабилитационных мероприятиях нарушения со стороны костной системы и задержка умственного развития успешно корректируются. Поскольку заболевание является наследственным, профилактика возможна на этапе планирования беременности, парам из групп риска (с отягощенным семейным анамнезом) рекомендуется медико-генетическое консультирование с определением вероятности рождения больного ребенка.
1. Нейрофиброматоз: этиология, патогенез, лечение/ Скаварская Е.А.// Международный журнал педиатрии, акушерства и гинекологии - 2014 - Т.5, №2.
2. Клинико-диагностические аспекты нейрофиброматоза/ Попова А.А.// Университетская медицина Урала - 2016 - №2.
3. Нейрофиброматоз первого типа (болезнь Реклингхаузена)/ Н.А. Шнайдер, А.И. Горелов// Сибирское медицинское обозрение - 2007.
Читайте также:
