Первичная медиастинальная лимфома на рентгенограмме, КТ, ПЭТ
Добавил пользователь Alex Обновлено: 21.01.2026
Первично медиастинальная (тимическая) В-клеточная крупноклеточная лимфома является одним из самых агрессивных видов В-крупноклеточных лимфомы. Чаще всего она начинается в лимфатических узлах средостения (область за грудиной, то есть за центральной плоской костью на груди, к которой присоединяются рёбра). Болезнь быстро распространяется на все тело, и тогда лимфатические узлы увеличиваются группами на шее, подмышками, в паху и в других местах, а также появляются одиночные опухоли во внутренних органах. Увеличенные узлы можно прощупать руками или найти с помощью рентгена и ультразвука (УЗИ). У больного могут появляться такие признаки болезни, которые называются «В-симптомы»: поднимается температура, он быстро худеет и сильно потеет вечером и ночью. Первично медиастинальная В-крупноклеточная лимфома быстро прогрессирует, однако вполне излечима.
Диагноз
Чтобы поставить правильный диагноз, обязательно берут кусочек опухоли или увеличенного лимфатического узла для морфологического и иммуногистохимического исследования . Только после такого сложного комплексного анализа можно быть уверенным в диагнозе и провести эффективное лечение.
Для того чтобы точно узнать, есть ли увеличенные лимфатические узлы и каково их количество в тех частях тела, которые нельзя увидеть при внешнем осмотре, необходимо сделать компьютерную томографию грудной клетки, брюшной полости и малого таза. Стадию болезни устанавливают по системе «Ann-Arbor», которая показывает, какие органы и лимфатические узлы затронуты болезнью.
Лечение
Чтобы вылечить пациента с этим заболеванием, используют разнообразные схемы, применяя лекарство «ритуксимаб». Лечение зависит от особенностей болезни и, главное, от общего состояния здоровья больного. Между курсами химиотерапии, для оценки их эффективности, может потребоваться контрольная компьютерная томография. Если лечение небольшими дозами лекарств не помогает, то проводят более интенсивное лечение, так называемую высокодозную химиотерапию, которую поддерживают собственными стволовыми клетками больного.
Применение современных методов и лекарств позволяет полностью излечить около 85% пациентов.
Лимфома средостения
Лимфома средостения - опухоль злокачественного типа, развивающаяся из медиастинальных лимфатических узлов. В большинстве случаев лимфома средостения проявляется симптомами сдавления органов грудной полости: кашлем, затруднением дыхания и глотания, болями в грудной клетке; часто отмечается кожный зуд, ночная потливость. Лимфома средостения обнаруживается с помощью рентгенографии и КТ, диагноз подтверждается после проведения медиастиноскопии, гистологического и иммуноморфологического исследования фрагмента опухоли. Стандартные схемы лечения лимфом предусматривают проведение лучевой и химиотерапии; в некоторых случаях возможно хирургическое удаление опухоли средостения.
МКБ-10



Общие сведения
Под термином «лимфома средостения» понимаются неходжскинские (ретикулосаркома, лимфосаркома) и ходжкинские (лимфогранулематоз) лимфомы, первично поражающие лимфоузлы средостения. Среди всех опухолей средостения лимфомы составляют немногочисленную группу, тем не менее, частота поражения средостения при лимфогранулематозе составляет до 90%, а при неходжкинских лимфомах - до 50%. Медиастинальные лимфомы преимущественно обнаруживаются у лиц молодого и среднего возраста (20-45 лет).
Чаще всего лимфомы локализуются в передне-верхнем этаже средостения. Длительное индолентное (при лимфогранулематозе) или быстрое агрессивное (при лимфосаркоме) течение затрудняют своевременное выявление злокачественных лимфом. Решение этой проблемы требует интеграции усилий специалистов в области онкологии и торакальной хирургии.

Причины лимфомы средостения
В большинстве случаев непосредственная причина развития лимфомы средостения у конкретного пациента остается невыясненной. Однако гематологии известны факторы, повышающие вероятность возникновения лимфоидных неоплазий в популяции в целом. В группу повышенного риска включены пациенты:
- переболевшие инфекционным мононуклеозом, вирусным гепатитом С
- страдающие аутоиммунной патологией (СКВ, ревматоидным артритом и др.)
- те, чьи ближайшие родственники страдали гемобластозами
- имеющие генетические патологии, характеризующиеся первичным иммунодефицитом - это синдромы Вискотта-Олдрича, Луи-Бар (с-м атаксии-телеангиэктазии), Дункана и др.
- проходящие химиотерапевтическое или лучевое лечение по поводу других онкозаболеваний
- лица, получающие иммуносупрессивную терапию после трансплантации органов.
Среди неблагоприятных экзогенных факторов первостепенное значение придается производственным вредностям, экологическому неблагополучию, избыточной инсоляции, повышенному потреблению животных белков. Влияние употребления алкоголя и табакокурения на развитие лимфом однозначно не подтверждено.
Лимфомы средостения могут иметь первичное (изначально развиваются в медиастинальном пространстве) или вторичное происхождение (являются метастатическими новообразованиями или проявлением генерализованной формы лимфогранулематоза).
Симптомы лимфомы средостения
Ходжкинские лимфомы
Лимфогранулематоз средостения на начальных этапах протекает с минимальной симптоматикой. Нередко увеличение медиастинальных узлов, выявленных с помощью рентгенографии грудной клетки, является единственным признаком заболевания. Начальные клинические проявления обычно включают недомогание, повышенную утомляемость, бессонницу, пониженный аппетит, похудание. Характерны периодические подъемы температуры тела, сухой кашель, потливость по ночам, кожный зуд.
В поздних стадиях ходжкинской лимфомы средостения развивается компрессионный синдром, вызванный сдавлением структур средостения. Клиническим выражением этого синдрома может служить одышка, тахикардия, нарушение глотания, осиплость голоса, одутловатость шеи и лица (синдром верхней полой вены). При осмотре часто определяется увеличение шейных и подмышечных лимфоузлов, выбухание грудной клетки, расширение подкожных вен на груди.
Неходжскинские лимфомы
Чаще бывают представлены ретикулосаркомой, нодулярной или диффузной лимфосаркомой средостения. Они отличаются стремительным инфильтративным ростом и ранним метастазированием в легкие, костный мозг, селезенку, печень, кожу. При лимфосаркоме средостения преобладают признаки компрессионного медиастинального синдрома - затруднение дыхания, удушливый кашель, дисфония, цианоз, сдавление ВПВ.
Примерно у 10% пациентов с лимфомой средостения возникает экссудативный плеврит или хилоторакс, вызванные затруднением венозного или лимфатического оттока либо опухолевой инвазией плевры. В далеко зашедших стадиях опухоль может прорастать перикард, аорту, диафрагму, грудную стенку.
Диагностика
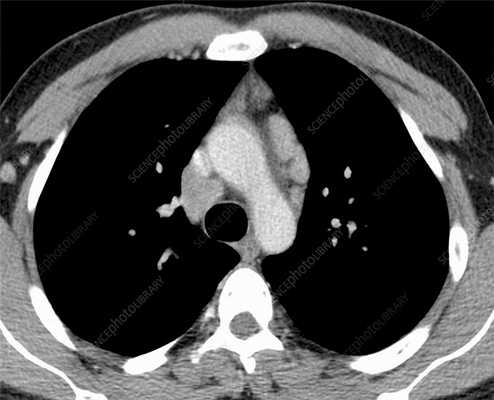
Лимфомы медиастинальной локализации не всегда диагностируются при рентгенологическом обследовании. Компьютерная томография, более детально, чем обзорная рентгенография позволяет рассмотреть конгломерат опухоли, увеличение лимфоузлов средостения, вовлечение паратрахеальных, трахеобронхиальных, прикорневых лимфатических узлов. Диагностическая значимость магнитно-резонансной томографии в верификации лимфом средостения признается не всеми авторами.

КТ ОГК. Объемное образование в средостении (патологически измененный лимфоузел), подтвержденная лимфома.
В дополнение к названным исследованиям используется УЗИ средостения, позволяющее оценить состояние внутригрудных лимфоузлов, недоступных для рентгенологической визуализации. Еще более высокочувствительным методом служит лимфосцинтиграфия с цитратом галлия. Для выявления компрессии трахеи и бронхов проводится бронхоскопия.
Поскольку тактика лечения лимфомы средостения определяется гистологическим и иммуногистохимическим типом опухоли, то обязательным этапом диагностики является биопсия. При увеличении доступных для пальпации лимфоузлов проводят эксцизионную, пункционную или прескаленную биопсию. В остальных случаях прибегают к операционной биопсии с помощью медиастиноскопии, парастернальной медиастинотомии, диагностической торакоскопии.
Дифференцировать лимфому средостения необходимо с другими медиастинальными опухолями, кистой средостения, саркоидозом, туберкулезом ВГЛУ, эхинококкозом, лимфаденитом различной этиологии, метастазами рака легкого, медиастинитом и др.

Лечение лимфомы средостения
Выбор протокола лечения лимфомы средостения зависит, главным образом, от типа и распространенности опухоли. При локальном лимфогранулематозе показана местная лучевая терапия. Иногда при изолированном поражении медиастинальных лимфоузлов прибегают к их хирургическому удалению с последующим лучевым лечением. Алгоритм лечения распространенных стадий лимфогранулематоза предусматривает проведение комбинированной химиолучевой терапии или полихимиотерапии.
Лимфосаркомы средостения также хорошо поддаются лечению с помощью консервативных методов - лучевой и химиотерапии. Многие онкологи и торакальные хирурги в последние годы высказываются за обоснованность хирургического удаления лимфомы средостения. В операбельных случаях операция может быть произведена уже на диагностическом этапе (так называемая тотальная биопсия), однако большинство хирургов признает целесообразность ее выполнения после предварительной противоопухолевой терапии (удаление остаточной опухоли).
Прогноз
Успешность лечения и выживаемость пациентов с лимфомой средостения во многом зависит от иммуноморфологического диагноза. 5-летний безрецидивный порог выживаемости при локальных формах лимфомы Ходжкина преодолевают 90% больных; при IV стадии лимфогранулематоза, даже после полихимиолучевого лечения этот показатель составляет не более 45%. Лимфосаркомы имеют гораздо более неблагоприятный прогноз ввиду быстрой генерализации процесса и частого рецидивирования.
1. Клинические рекомендации по диагностике и лечению лимфопролиферативных заболеваний/ Ассоциация онкологов России (авторский коллектив). - 2014.
2. Неходжкинские лимфомы из периферических T-клеток с преимущественным поражением средостения/ Мазурок Л.А. , Тумян Г. С., и др.// Клиническая онкогематология. - 2008 - Т.1, №3.
3. Дифференциальная диагностика В-клеточных лимфом средостения из крупных клеток: Диссертация/ Артемьева А.С. - 2015.
Первичная медиастинальная лимфома на рентгенограмме, КТ, ПЭТ
Первичная медиастинальная В-крупноклеточная лимфома (ПМВКЛ) - агрессивный вариант В-крупноклеточной лимфомы, клинически проявляющийся медиастинальный синдромом, синдромом верхней полой вены в связи с распространением большого конгломерата лимфоузлов в средостении. Диагностика данного варианта часто затруднена, и, если нет развития характерных клинических признаков, отсутствует периферическая лимфаденопатия, может являться случайной находкой. Несмотря на достижения иммунохимиотерапии в лечении данной патологии, остается большой процент пациентов, рефрактерных к лечению. Оценку динамики процесса проводят спустя 2-3 курса химиотерапии (ХТ) методами спирально-компьютерной томографии. Однако в настоящее время позитронно-эмиссионная томография (ПЭТ-КТ) играет не менее существенную роль как в первоначальной диагностике, стадировании процесса, так и в оценке эффекта от лечения. В зависимости от результатов ПЭТ-КТ существуют понятия «ПЭТ-позитивный ответ/результат», когда результат в баллах шкале Deauville составляет 4-5, «ПЭТ-негативный ответ/результат», когда результат в баллах шкалы Deauville составляет 1-2. Но не всегда ПЭТ-позитивный результат может считаться отсутствием эффекта от терапии. В исследовании обнаружена связь между общей и бессобытийной выживаемостью пациентов с ПМВКЛ и ПЭТ-ответом на проводимую терапию. Также выявлена более низкая выживаемость больных с ПМВКЛ при наличии «bulky disease».

1. Luca Ceriani, Maurizio Martelli, Pier Luigi Zinzani, Andrés J. M. Ferreri, Barbara Botto, Caterina Stelitano, Manuel Gotti, Maria Giuseppina Cabras, Luigi Rigacci, Livio Gargantini, Francesco Merli, Graziella Pinotti, Donato Mannina, Stefano Luminari, Anastasios Stathis, Eleonora Russo, Franco Cavalli, Luca Giovanella, Peter W. M. Johnson, Emanuele Zucca; Utility of baseline 18FDG-PET/CT functional parameters in defining prognosis of primary mediastinal (thymic) large B-cell lymphoma. Blood. 2015. Vol. 126 (8). P. 950-956. DOI: 10.1182/blood-2014-12-616474.
2. Giulino-Roth L., O'Donohue T., Chen Z., Bartlett N.L., LaCasce A., Martin-Doyle W., Barth M.J., Davies K., Blum K.A., Christian B., Casulo C., Smith S.M., Godfrey J., Termuhlen A., Oberley M.J., Alexander S., Weitzman S., Appel B., Mizukawa B., Svoboda J., Afify Z., Pauly M., Dave H., Gardner R., Stephens D.M., Zeitler W.A., Forlenza C., Levine J., Williams M.E., Sima J.L., Bollard C.M., Leonard J.P. Outcomes of adults and children with primary mediastinal B-cell lymphoma treated with dose-adjusted EPOCH-R. Br J. Haematol. 2017. Vol. 179 (5). P. 739-747. DOI: 10.1111/bjh.14951.
3. Salem A.E., Zaki Y.H., El-Hussieny G., ElNoueam K.I., Shaaban A.M., Koppula B.R., Bustoros M., Salama M., Elsayes K.M., Morton K., Covington M.F. An Overview of Selected Rare B-Cell Lymphoproliferative Disorders: Imaging, Histopathologic, and Clinical Features. Cancers (Basel). 2021. Vol. 13 (22). P. 5853. DOI: 10.3390/cancers13225853.
4. Архипова О.Е., Черногубова Е.А., Тарасов В.А., Лихтанская Н.В., Кит О.И., Еремеева А.А., Матишов Д.Г. Уровень онкологических заболеваний как индикатор медико-экологической безопасности территорий (на примере Ростовской области) // Вестник Южного научного центра РАН. 2013. Т. 9. № 3. С. 7-14.
5. Камаева И.А., Лысенко И.Б., Николаева Н.В., Пушкарева Т.Ф., Капуза Е.А., Гайсултанова Я.С., Величко А.В. Применение иммунотерапии для лечения рефратерных форм лимфомы Ходжкина в реальной клинической практике // Южно-Российский онкологический журнал. 2021. № 2 (2). С. 34-41. DOI: 10.37748/2686-9039-2021-2-2-4.
7. Meignan M. Quantitative FDG-PET: a new biomarker in PMBCL. Blood. 2015. Vol. 126 (8). P. 924-926. DOI: 10.1182/blood-2015-07-653386.
8. Schmitz C., Hüttmann A., Müller S.P., Hanoun M., Boellaard R., Brinkmann M., Jöckel K.H., Dührsen U., Rekowski J. Dynamic risk assessment based on positron emission tomography scanning in diffuse large B-cell lymphoma: Post-hoc analysis from the PETAL trial. Eur. J. Cancer. 2020. Vol. 124. P. 25-36. DOI: 10.1016/j.ejca.2019.09.027.
10. Wijetunga N.A., Imber B.S., Caravelli J.F., Mikhaeel N.G., Yahalom J. A picture is worth a thousand words: a history of diagnostic imaging for lymphoma. Br J. Radiol. 2021. Vol. 94 (1127). P. 20210285. DOI: 10.1259/bjr.20210285.
11. Illidge T., Mikhaeel N.G., Specht L., Yahalom J. Lymphoma: advances in imaging and radiotherapy - introductory editorial. Br J. Radiol. 2021. Vol. 94 (1127). P. 20219005. DOI: 10.1259/bjr.20219005.
12. Galimberti S., Genuardi E., Mazziotta F., Iovino L., Morabito F., Grassi S., Ciabatti E., Guerrini F., Petrini M. The Minimal Residual Disease in Non-Hodgkin's Lymphomas: From the Laboratory to the Clinical Practice. Front Oncol. 2019. Vol. 9. P. 528. DOI: 10.3389/fonc.2019.00528.
14. Ceriani L., Milan L., Johnson P.W.M., Martelli M., Presilla S., Giovanella L., Zucca E. Baseline PET features to predict prognosis in primary mediastinal B cell lymphoma: a comparative analysis of different methods for measuring baseline metabolic tumour volume. Eur. J. Nucl. Med. Mol. Imaging. 2019. Vol. 46 (6). P. 1334-1344. DOI: 10.1007/s00259-019-04286-8.
15. Pinnix C.C., Ng A.K., Dabaja B.S., Milgrom S.A., Gunther J.R., Fuller C.D., Smith G.L., Abou Yehia Z., Qiao W., Wogan C.F., Akhtari M., Mawlawi O., Medeiros L.J., Chuang H.H., Martin-Doyle W., Armand P., LaCasce A.S., Oki Y., Fanale M., Westin J., Neelapu S., Nastoupil L. Positron emission tomography-computed tomography predictors of progression after DA-R-EPOCH for PMBCL. Blood Adv. 2018. Vol. 2 (11). P. 1334-1343. DOI: 10.1182/bloodadvances.2018017681.
16. Oliveira M., Lasnon C., Nganoa C., Gac A.C., Damaj G., Aide N. Comprehensive analysis of the influence of G-CSF on the biodistribution of 18F-FDG in lymphoma patients: insights for PET/CT scheduling. EJNMMI Res. 2019. Vol. 9 (1). P. 79. DOI: 10.1186/s13550-019-0546-1.
17. Phillips E.H., Iype R., Wirth A. PET-guided treatment for personalised therapy of Hodgkin lymphoma and aggressive non-Hodgkin lymphoma. Br J. Radiol. 2021. Vol. 94 (1127). P. 20210576. DOI: 10.1259/bjr.20210576.
18. Fakhri B., Ai W. Current and emerging treatment options in primary mediastinal B-cell lymphoma. Ther Adv Hematol. 2021. Vol. 12. 20406207211048959. DOI: 10.1177/20406207211048959.
20. Камаева И.А., Лысенко И.Б., Николаева Н.В., Капуза Е.А., Волошин М.В. Некоторые клинические факторы и терапевтические аспекты, влиящие на выживаемость пациентов с первичной медиастинальной в-крупноклеточной лимфомой // Современные проблемы здравоохранения и медицинской статистики. 2021. № 3. С. 50-66.
Первичная медиастинальная В-крупноклеточная лимфома (ПМВКЛ), не так давно выделенная в самостоятельную нозологию, является подтипом диффузной В-крупноклеточной лимфомы, возникающей из небольшой популяции В-клеток в тимусе [1]. Клинически характеризуется образованием конгломерата лимфоузлов в средостении с распространением на близлежащие ткани и органы. ПМВКЛ наблюдается преимущественно у молодых пациентов, а лечение агрессивными режимами химиотерапии в сочетании с ритуксимабом и лучевой терапией или без нее, по-видимому, дает лучшие результаты, чем при других ДВКЛ, отчасти в результате более молодого возраста пациентов, а 5-летняя выживаемость в недавних исследованиях составляет более чем 90% 4. При прогнозировании риска раннего рецидива принято использовать Международный прогностический индекс, а также индекс, скорректированный по возрасту. Несмотря на агрессивность лечения, остается высокой частота рецидивов ПМВКЛ, а также первично-рефрактерных форм заболевания.
Согласно клиническим рекомендациям, оценку эффективности лечения проводят спустя 2-3 курса ХТ, а также после завершения иммунохимиотерапии. Наиболее информативным методом диагностики в таком случае является позитронно-эмиссионная томография (ПЭТ-КТ), чему посвящены многочисленные современные исследования 6. ПЭТ-КТ - неинвазивный количественный метод визуализации биохимических, физиологических и биологических процессов in vivo. На сегодняшний день это наиболее специфичный и чувствительный метод визуализации. Опухоли имеют ускоренный гликолиз, при этом радиофармпрепарат (РФП) задерживается в тканях с повышенной метаболической активностью по сравнению с нормальными тканями [9].
Цель исследования: проанализировать результаты ПЭТ-контроля у пациентов после проведенного лечения, а также оценить общую и бессобытийную 5-летнюю выживаемость пациентов в зависимости от ПЭТ-ответа.
Материалы и методы исследования. В исследование были включены данные о 32 пациентах с установленным диагнозом первичной медиастинальной В-крупноклеточной лимфомы различных стадий, получающих лечение на базе онкогематологического отделения ФГБУ «НМИЦ онкологии» МЗ РФ в период с 2016 по 2021 гг. Пациенты разделены на группы в зависимости от ПЭТ-ответа, а также от полученной терапии. Статистическая обработка данных осуществлялась с использованием пакета STATISTICA13, метода Каплана-Мейера и логрангового критерия.
Результаты исследования и их обсуждение. ПЭТ-КТ для оценки эффективности иммунохимиотерапии применялась в качестве оценки динамики у всех 32 пациентов. Терапией первой линии во всех случаях стали стандартные CHOP-подобные режимы (R-CHOP, DAR-EPOCH) в сочетании с ритуксимабом (R).
ПЭТ-позитивный результат (4-5 баллов по шкале Deauville) после проведенной терапии 1-й линии наблюдался у 14 человек (43,75%). Среди этих пациентов преобладали больные с IV стадией процесса (85,7%), в основном за счет вовлечения легочной ткани и сосудов. «В-симптомы» наблюдались у 78,5% пациентов. ПЭТ-негативный результат (1-2 балла по шкале Deauville) наблюдался у 12 пациентов (37,5%), всем пациентам была назначена консолидирующая дистанционная лучевая терапия (ДЛТ). У 6 больных (18,75%) ответ расценен как неоднозначный результат (Deauville 3).
Средняя продолжительность жизни больных в группе с высокой метаболической активностью составила 30,8±9,0 месяца, тогда как у пациентов с низкой активностью - 34,5±4,2 месяца (р=0,0003). В группе пациентов, имеющих ПЭТ-позитивный ответ (4-5 баллов по шкале Deauville), 5-летняя общая выживаемость составила 32,1±14,6% (±SE), в то время как 5-летняя общая выживаемость в группе пациентов с низкой метаболической активностью составила 93,9±4,2% (±SE) (р=0,0003) (рис. 1).
В группе больных, имеющих ПЭТ-негативный результат, бессобытийная 50-месячная выживаемость составила 87,7±5,8% (±SE) (рис. 2). Средняя продолжительность бессобытийного периода жизни в группе пациентов, имеющих ПЭТ-позитивный ответ, составила 10,9±3,6 месяца, в группе пациентов с низкой метаболической активностью - 33,3±4,4 месяца (р=0,0000).
В нашем исследовании также обнаружена связь между наличием массивного конгломерата в средостении (bulky disease) и течением заболевания. В среднем объем конгломерата в средостении среди пациентов составил 109,73±60,55 мм (151; 222). В исследовании «bulky disease» обнаружен у 31 пациента (96,8%). ПЭТ-позитивный результат (4-5 баллов по шкале Deauville) в данной группе пациентов наблюдался у 12 больных (38,7%).
Средняя продолжительность жизни больных из группы пациентов, имеющих «bulky disease», составляет 28,5±4,3 месяца; в группе пациентов без «bulky disease» - 42,8±7,7 месяца. (±SE) (р=0,0111). Следует отметить, что 5-летняя общая выживаемость у пациентов без «bulky disease» составила 100% (рис. 3), в то время как у пациентов, имеющих «bulky disease», она составила 60,0±10,6% (±SE) (рис. 4). Медиана бессобытийной выживаемости достигнута только в одной группе пациентов с «bulky disease» и составляет 23,5 месяца. Средняя продолжительность бессобытийного периода жизни в группе без «bulky disease» - 35,8±7,0 месяца (±SE), а в группе c «bulky disease» - 21,8±3,8 месяца. Пятилетняя бессобытийная выживаемость без «bulky disease» - 87,5±8,3% (р=0,0086) (рис. 4), в то время как c «bulky disease» - 40,1±12,0% (±SE).
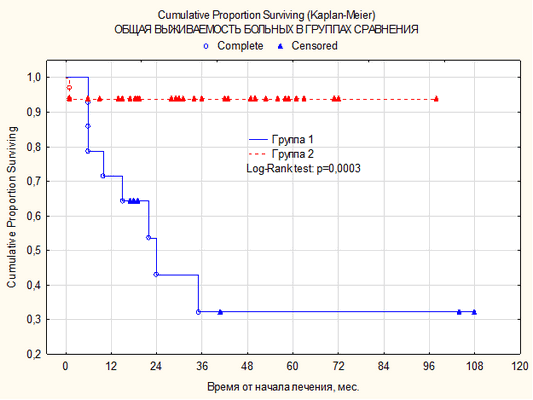
Рис. 1. Кривая общей 5-летней выживаемости по Каплану-Майеру в зависимости от наличия высокой метаболической активности по ПЭТ-КТ (4-5 баллов)
Группа 1 - пациенты, имеющие ПЭТ-позитивный ответ (4-5 баллов по шкале Deauville), обозначены синей линией.
Группа 2 - пациенты, имеющие ПЭТ-негативный ответ (1-3 балла по шкале Deauville), обозначены красной линией.
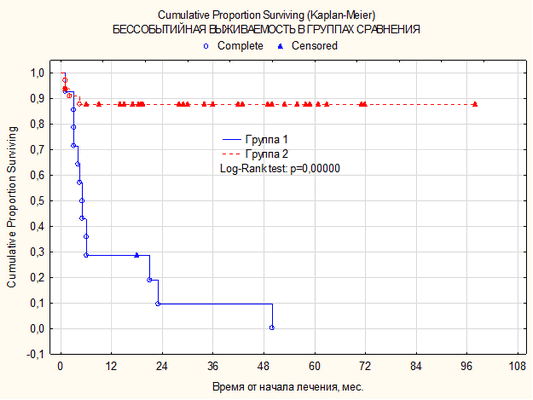
Рис. 2. Кривая бессобытийной выживаемости по Каплану-Майеру в зависимости от наличия высокой метаболической активности по ПЭТ-КТ (4-5 баллов)
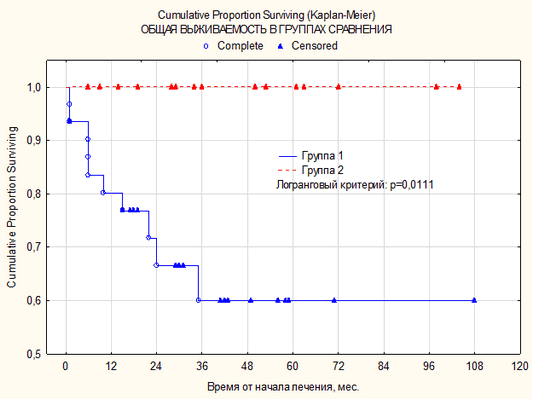
Рис. 3. Кривая общей 5-летней выживаемости по Каплану-Майеру в зависимости от наличия «bulky disease»
Группа 1 - пациенты, имеющие «bulky disease», обозначены синей линией.
Группа 2 - пациенты без «bulky disease», обозначены красной линией.
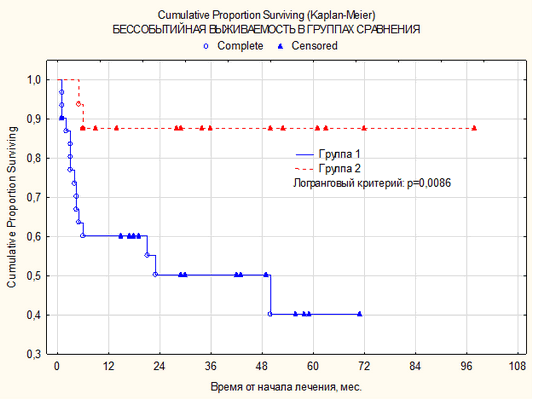
Рис. 4. Кривая бессобытийной выживаемости по Каплану-Майеру в зависимости от наличия «bulky disease»
По данным разных авторов, роль ПЭТ-КТ в диагностике неходжкинских лимфом (НХЛ) разной степени злокачественности противоречива [9, 10]. Имеются исследования о возможности дифференциальной диагностики ПМВКЛ и лимфомы Ходжкина (ЛХ) на основе некоторых лабораторных показателей и данных ПЭТ-КТ [11]. Также отмечается связь между накоплением Ki-67, накоплением РФП и прогнозом [12, 13]. ПЭТ-КТ может использоваться на различных этапах диагностики и лечения пациентов: как на этапе стадирования, так и для оценки проводимого лечения и определения тактики ведения больного. Все пациенты в нашем исследовании проходили контрольное исследование (ПЭТ-КТ) после завершения лечения и получали дальнейшую терапию в зависимости от результата.
Согласно литературным данным (L. Ceriani, L. Milan, PWM Johnson, 2019), сохранение ПЭТ-позитивности остаточного конгломерата может наблюдаться по нескольким причинам, одной из которых является накопление ФДГ остаточной тканью тимуса. В группе пациентов с неоднозначным ответом ориентировались на уровень накопления фармпрепарата в печени, что считается более информативным и прогностически значимым [14].
Стоит отметить отсутствие литературных данных относительно выживаемости пациентов с наличием «bulky disease» при ПМВКЛ. Согласно результатам исследования (H. Takasaki, W. Yamamoto, 2015), наличие «bulky disease» у пациентов с диффузной В-крупноклеточной лимфомой не коррелировало с ухудшением общей и бессобытийной выживаемости таких пациентов. В этом же исследовании оценивался ПЭТ-ответ в зависимости от наличия массивного конгломерата в средостении и без него. Общая выживаемость у пациентов с ПЭТ-позитивным результатом составила 34% против 75% у пациентов с ПЭТ-негативным ответом, бессобытийная выживаемость пациентов с ПЭТ-позитивным результатом и «bulky disease» составила 83% против 36% у пациентов с ПЭТ-негативным результатом (у=95%). Однако в данном исследовании при инвазии окружающих структур считалось, что у пациента - ПМВКЛ, что являлось критерием исключения [19].
Также существуют данные о возможных ложноположительных результатах вследствие остаточной ткани тимуса и применения моноклональных антител (МКА) и гранулоцитарных колониестимулирующих факторов (ГКСФ) в терапии 1-й линии [13]. Поскольку фтордезоксиглюкоза (ФДГ) поглощается инфильтрирующими опухоль лейкоцитами и ГКСФ, он стимулирует продукцию лейкоцитов и изменяет распределение ФДГ.
Выводы. Таким образом, ПЭТ-ответ может считаться фактором, влияющим на выживаемость пациентов с ПМВКЛ. Планирование дальнейшей терапии у пациентов с ПМВКЛ в зависимости от результатов ПЭТ-КТ является в настоящий момент критерием выбора для оценки динамики процесса и успешности проводимого лечения. В нашем исследовании ПЭТ-позитивный ответ (4-5 баллов) после проведенной ХТ 1-й линии коррелировал с более низкой общей и бессобытийной выживаемостью пациентов с ПМВКЛ. Особого внимания заслуживает распространенность ПЭТ-позитивных результатов у пациентов с наличием массивного конгломерата в средостении «bulky disease» (38,7%), так как наличие данного симптома может также служить причиной более низкой выживаемости больных с ПМВКЛ. При ПЭТ-негативном ответе пациентам в нашем исследовании проводилась ДЛТ, которая также улучшила общую выживаемость пациентов с ПМВКЛ [20]. Тактика ведения пациентов с неоднозначным ответом при ПЭТ-контроле требует дальнейшего изучения и обсуждения в каждом конкретном случае.
Ограничения исследования. Настоящее исследование имеет ряд ограничений, которые необходимо учитывать. Работа представляет собой одноцентровое ретроспективное исследование с небольшой выборкой пациентов, что могло повлиять на интерпретацию результатов.
Лимфомы средостения
Целая группа опухолевых новообразований, которые развиваются в медиастинальных лимфоузлах. Течение болезни и симптомы зависят от вида опухоли, часто осложняются нарушением дыхания, сильным кашлем, болями в груди. Схемы лечения подбираются индивидуально, они включают химиотерапию, лучевую терапию, хирургическое вмешательство.

Злокачественная лимфома средостения
Лимфомы - опухоли злокачественного типа, для которых характерно поражение медиастинальных лимфатических узлов. Они занимают небольшой процент среди всех новообразований средостения, чаще локализуются в его верхнем этаже. Главная особенность - агрессивное течение многих видов, затрудненная ранняя диагностика.
Заболевание делится на два основных типа по характеру возникновения:
- ходжскинские - выявляются в 40% случаев, занимают до 10% всех онкологических заболеваний в стране;
- неходжскинские - на группу приходится до 60% всех диагностированных случаев.
Большинство пациентов - люди возраста от 20 до 45 лет. Заболевание характеризует быстрое течение, рост патогенной ткани, что затрудняет диагностику и лечение.


Причины заболевания
Вопрос о причинах появления злокачественных клеток и формирования лимфом средостения остается малоизученным и открытым. В большинстве случаев онкологам не удается выявить, почему возникла опухоль у конкретного пациента. Но гематологи выделяют несколько факторов, повышающих вероятность тяжелого заболевания:
- инфицирование гепатитом С, инфекционным мононуклеозом;
- вирус иммунодефицита человека;
- различные аутоиммунные патологии;
- наличие у близких родственников гемобластоза;
- активные стадии других онкологических болезней, которые подавляют работу иммунной системы;
- прохождение иммуносупрессивной терапии.
Влияние на формирование опухолевого процесса также оказывает неблагоприятная экологическая обстановка, в которой проживает человек. Повышает риск лимфомы постоянное пребывание под солнечными лучами, повышенное содержание в рационе белковой пищи животного происхождения.
Достоверно неизвестно, влияет ли на образование опухолей злоупотребление алкоголем, курение или лишний вес пациента. Среди возможных провоцирующих факторов онкологи не исключают работу во вредных условиях, которая ослабляет иммунитет, повышает вероятность интоксикации организма.
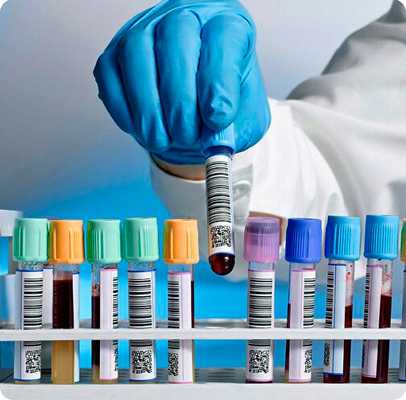
Этиология лимфомы средостения
Характер болезни зависит от вида лимфомы. Патогенез ходжкинских опухолей имеет следующие теории происхождения:
- генетическая предрасположенность, наследственные факторы;
- осложнения после перенесенных инфекционных заболеваний;
- спонтанная мутация лимфоцитов под влиянием внутренних или внешних факторов.
Патогенез неходжкинских лимфом не имеет доказанной теории развития и возникновения, но у большинства пациентов в анамнезе присутствуют следующие особенности:
- у родственников были различные онкологические заболевания, тяжелые патологии органов кроветворения;
- больные ранее перенесли мононуклеоз или цитомегаловирусную инфекцию;
- больные получают специальную терапию после трансплантации внутренних органов.
Большинство онкологов уверены, что лимфома у взрослых - последствия сбоя в работе иммунной системы.

Симптомы
Ежегодно только в России регистрируют до 12 тыс. случаев неходжкинских лимфом, которые занимают более 2,5% от всех онкологических заболеваний. Основная группа пациентов - молодые люди от 16 до 35 лет. Для опухолевого процесса характерно:
- повышение температуры выше субфебрильных показателей;
- сильная потливость во время ночного сна;
- мышечная слабость.
Иногда симптомы лимфомы средостения у взрослых принимают за простуду, грипп и другие респираторные инфекции. Но болезненное состояние продолжается в течение нескольких недель. Пациент теряет вес, не меняя режим питания. На теле увеличиваются лимфатические узлы: при пальпации они плотные на ощупь, но не дают болезненных ощущений.
Характерным симптомом является появление неспецифических болей в шейных, подмышечных и других лимфоузлах при употреблении алкогольных напитков. У пациентов нередко возникают кожная аллергия, сильные высыпания на укусы комаров и других насекомых, которые ранее не отмечалась в анамнезе. Нетипичная реакция также возникает на царапины кошек: они не заживают в течение 2-3 недель, сильно воспаляются, зудят, причиняют дискомфорт.
Для болезни характерно увеличение одного или нескольких лимфатических узлов одновременно. Как правило, они воспаляются на одном участке, провоцируют сдавливание расположенных рядом кровеносных сосудов, нервных окончаний. При разрастании опухоли в средостении появляется ощущение сдавливания в груди. Человек ощущает дискомфорт во время глотания пищи, проблемы с дыханием. При компрессии вены увеличиваются, проступают под кожей на шее и голове.
У пациентов с лимфомой средостения сильно увеличивается селезенка. Она выступает в левом подреберье, становится болезненной на ощупь. Больной жалуется на нарушение сна, снижение аппетита, апатию.
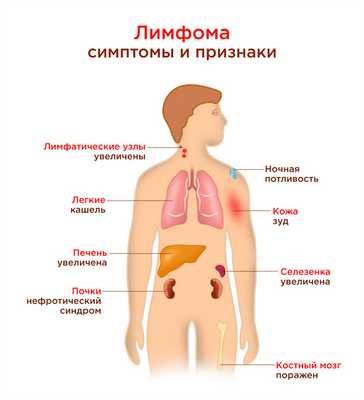
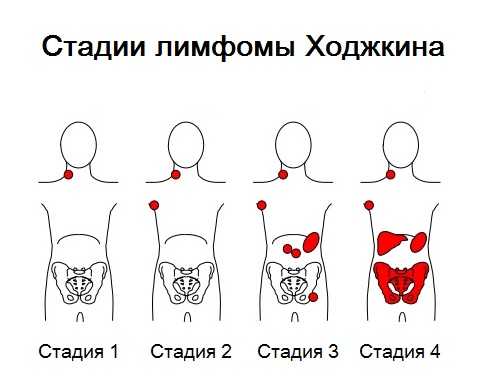
Стадии развития
При классификации и диагностике врачи придерживаются разных модификаций. Тяжесть течения и симптомы зависят от стадии.
Первая стадия
Злокачественные клетки обнаруживаются в узлах на одном участке. Человек ведет привычный образ жизни, не ощущает признаков болезни. Иногда возникает переутомление после интенсивных физических нагрузок или умственной работы.
Вторая стадия
Диагностируют поражение лимфатических узлов в 2 и более зонах, которые расположены по разные стороны от диафрагмы, Злокачественные клетки также обнаруживаются в органах, имеющих экстралимфатические ткани (костный мозг, селезенка, печень). На второй стадии пациент жалуется на утомляемость, сонливость, отказывается от занятий спортом и активного отдыха.
Третья стадия
Наблюдается воспаление и поражение лимфоузлов в разных частях тела, включая паховую шейную зоны. Нередко вовлекается селезенка, которая значительно увеличивается в размере, выпирает в подреберье. Больные жалуются на сильную слабость, с трудом обслуживают себя в быту. Они стараются больше лежать в постели, ухудшаются аппетит и сон, проявляются характерные признаки лимфомы.
Четвертая стадия
Для стадии характерно множественное поражение лимфоузлов иных органов. Опухоли могут достигать в диаметре более 10 см. Присутствуют признаки интоксикации, уровень СОЭ в крови резко повышается. Пациенты соблюдают постельный режим, практически обездвижены, теряют способность к самообслуживанию, избегают любой физической нагрузки.
При диагностике значение имеют количество и удаленность пораженных лимфатических узлов, что также влияет на стадию болезни.
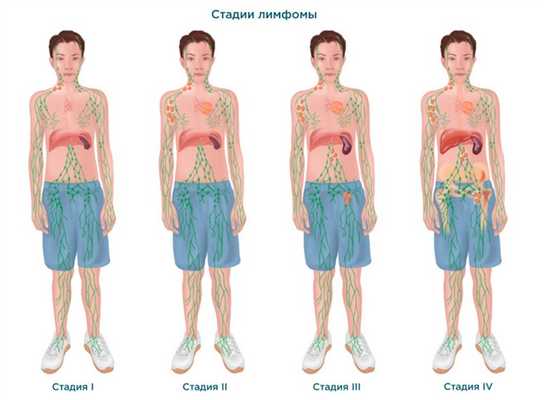
Осложнения
Опухоль активно разрастается, поражает окружающие органы. Она собирает воспалительный экссудат, создавая повышенное давление на кровеносные сосуды. Среди осложнений при лимфоме средостения:
- синдром верхней полой вены;
- компрессия спинного мозга;
- патологические переломы костей, ребер, позвоночника;
- кишечная непроходимость;
- развитие сердечно-легочной недостаточности;
- паралич конечностей;
- энцефалопатия.
У пациентов с неходжкинской лимфомой часто возникают лимфоматоидный менингит, непроходимость. Ослабление иммунитета приводит к частым вирусным инфекциям, которые протекают с тяжелыми осложнениями.
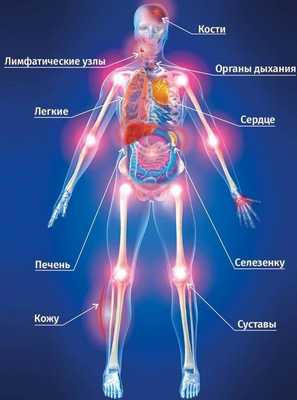
В группу входит несколько видов лимфом средостения, которые можно диагностировать по результатам биопсии, гистологических и цитологических исследований. Расширенная классификация помогает онкологу определиться с тактикой лечения, подобрать эффективную терапию.
Лимфома Ходжкина
В зависимости от типа клеток выделяют две основные подгруппы:
- нодулярный тип лимфоидного преобладания;
- классическая лимфома Ходжкина.
Это моноклональные лимфоидные опухоли B-клеточного генеза, которое состоят из одноядерных и многоядерных клеток. В инфильтрате обнаруживаются нейтрофилы, малые неопухолевые лимфоциты, коллагеновые волокна.
Лимфома Ходжкина встречается возрасте 15−35 лет, второй пиковый период наблюдается после 55 лет. В большинстве случаев поражаются подмышечные, парааортальные и медиастинальные лимфоузлы, селезенка. Костный мозг вовлекается в процесс только в 5% случаев.
Другие варианты классической лимфомы Ходжкина диагностируют в 30% случаев от всех видов ходжкинских лимфом. Они характерны для пациентов с аутоиммунными заболеваниями, ВИЧ. В 70% случаев они встречаются у мужчин. Кроме селезенки и костного мозга, происходит тяжелое поражение печени.
Диагностику проводят в зависимости от гистологического типа клеток. Заболевание часто протекает в виде нодулярной или диффузной лимфосаркомы средостения, ретикулосаркомы. Сопровождается активным ростом патологических клеток, образованием метастазов в печени, органах дыхания, костном мозге.
Диффузная крупноклеточная В-клеточная лимфома
Наиболее распространенный вариант среди неходжкинских лимфом, на который приходится до 30% диагностированных случаев. Чаще развивается в пенсионном возрасте, преобладает у женщин в период менопаузы. Опухоль растет быстро, локализуется в лимфатических узлах, желудочно-кишечном тракте, органах средостения.
Симптомы диффузной В-крупноклеточной лимфомы средостения осложняются при поражении костного мозга. Возникают сильные боли, парез конечностей, снижается подвижность, нарушается иннервация органов малого таза.
Первичная медиастинальная В-крупноклеточная лимфома
Является самостоятельной клинической единицей. На этот вид приходится не более 4% от всех диагностированных неходжкинских лимфом. Ее активное изучение проводится с 1980 года.
- значительное преобладание среди женщин;
- наибольшее количество пациентов - молодые люди до 40 лет;
- большой размер опухоли (более 10-12 см);
- частая манифестация в органы средостения.
Симптомы первичной медиастинальной В-крупноклеточной лимфомы: сильный кашель, одышка при минимальной физической нагрузке, боли в области желудка, синдром верхней полой вены.
Медиастинальная лимфома средостения
Впервые в отдельное заболевание была выделена 2005 году. Сочетает признаки классической лимфомы Ходжкина и первичной медиастинальной В-крупноклеточной опухоли. Характерные особенности патологии:
- чаще диагностируется в возрасте от 20 до 40 лет;
- у 20% пациентов определяется вирус Эпштейн-Барра;
- массивные опухоли разрастаются в переднем средостении, практически не вовлекая лимфоузлы над ключицей.
Медиастинальная лимфома средостения часто поражает печень, селезенку, костный мозг, вызывает серьезные дыхательные патологии, одышку, нарушение кровообращения.
Заболевание практически не изучено. У некоторых пациентов оно протекает в виде классической лимфомы Ходжкина, которая через несколько лет рецидивирует в первичную медиастинальную В-крупноклеточную форму. В инфильтрате присутствуют опухолевые клетки разного типа, что затрудняет исследование биоматериала.
Т-лимфобластная лимфома средостения
Тяжелое заболевание часто встречается среди детей и подростков (до 40% всех лимфом и 15% острых лейкозов). Т-клеточный тип лимфомы занимает до 75% диагностированных случаев, представляет собой незрелую полиферацию лимфоидных клеток. По характеру течения во многом напоминает острый лейкоз.
- лимфоаденопания;
- наличие острого респираторного дистресс-синдрома;
- образование выпотного плеврита;
- перикардит;
- прогрессирование в лейкоз.
Т лимфобластная лимфома средостения (ранее использовалось название «саркома Штейнберга») относится к высокоагрессивным онкологическим заболеваниям. Она быстро прогрессирует, протекает с частыми рецидивами и осложнениями, показывает высокую степень летальности. Опухолевый процесс поражает центральную нервную систему, половые железы, костный мозг.
Главная особенность заболевания - Т лимфома средостения может прогрессировать до лейкозной фазы. Это требует длительной и интенсивной химиотерапии, облучения средостения для местного контроля и снижения риска рецидива.
Лимфому средостения не всегда можно обнаружить на рентгенографии. При подозрении на опухоль пациентам назначают компьютерную томографию: среди онкологов она признается как наиболее эффективный и точный диагностический метод.
На КТ можно обследовать с одновременным измерением формы и объема увеличенных лимфатических узлов. Методика показывает скопление воспалительного экссудата, конгломерат опухоли, количество и расположение пораженных групп лимфоузлов.
Кроме КТ, при лимфоме средостения врачи назначают:
- УЗИ грудной клетки и средостения для выявления новообразований, которые не визуализируются на рентгеновских снимках;
- лимфосцинтиграфию с применением цитрата галлия;
- бронхоскопию.
Для определения типа злокачественной лимфомы средостения рекомендована гистология. Биопсию можно взять из лимфатических узлов в области шеи, подмышечных впадин. В большинстве случаев проводится пункция содержимого.
В сложных и спорных ситуациях врачи назначают операционную биопсию. Это позволяет с высокой точностью исключить саркоидоз, доброкачественные кисты средостения, метастазы при раке легкого.
Лечение
При боли в воспаленных лимфатических узлах не рекомендуется прогревание или холодный компресс: это стимулирует отток воспалительного экссудата, ускоряет распространение опухолевых клеток по лимфатической системе.
Прогноз при лечении лимфомы средостения во многом зависит от типа заболевания, стадии, возраста и особенностей здоровья пациента. Большое значение имеет наличие вторичного поражения селезенки, печени, костного мозга.
При лечении ходжскинских лимфом врачи рекомендуют сочетание лучевой и медикаментозной терапии. При химиотерапии на 1-2-й стадиях заболевания рекомендованы препараты:
- Доксорубицин;
- Винбластин;
- Дакарбазин.
Моно- или полихимиотерапия протекает с минимальными осложнениями, показывает хорошие результаты у 90-95% пациентов. На 3-4-й стадиях лечение ходжскинских лимфом средостения при тяжелых симптомах включает медикаментозную терапию сильнодействующими препаратами: Винкристин, Прокарбазин, Циклофосфамид. Они эффективно подавляют рост патологических клеток, но повышают риск лейкемии.
Лечение лимфомы средостения при слабовыраженных симптомах основано на лучевой терапии, которую усиливает химиотерапия. В сложных ситуациях рекомендована последующая трансплантация стволовых клеток или костного мозга.
Среди экспериментальных методик - использование моноклональных антител. Некоторые медицинские центры в качестве эксперимента проводят генетическое исследование полученного биоматериала, типирование клеток. Они создают вакцину против каждого конкретного вида лимфомы с учетом особенностей гена пациента.
Операция
Операция при лимфоме средостения может проводиться на любой стадии. Многие онкологи уверены в эффективности хирургического лечения при полном удалении опухоли на этапе тотальной биопсии. Ряд специалистов высказывается за операцию после предварительной противоопухолевой химиотерапии, курса лучевой терапии.
Прогноз выживаемости
Прогноз при лечении лимфомы средостения зависит от симптомов, стадии болезни, вида опухоли. При локальных формах ходжкинских новообразований и своевременном лечении выживаемость достигает 90%. На 4-й стадии неходжкинских лимфосарком показатель редко превышает 45%. Это связано с частыми рецидивами, быстрым развитием патологического процесса.

Лимфомы средостения
Клиника лечения заболеваний легких, трахеи, бронхов, плевры, грудной стенки и средостения
Поражение легких при лимфоме
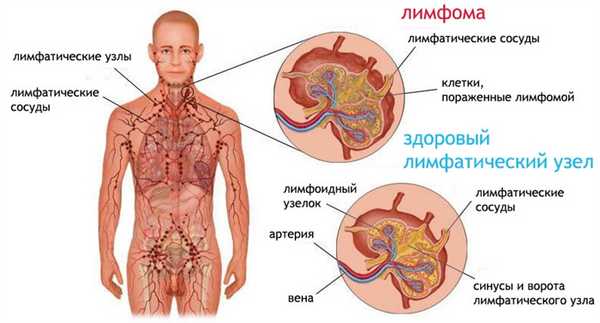
Лимфома (лимфоролиферативный процесс) — это группа онкологических процессов с поражением лимфоцитов (клеток иммунной системы), которые сопровождаются изменениями в лимфатических узлах и сосудах. При этом может происходить метастазирование — миграция злокачественных клеток в соседние органы и ткани с образованием вторичных очагов рака. Увеличенные узлы при лимфоме (> 1 см в поперечнике) — плотные и абсолютно безболезненные, поэтому выявляемость заболевания на ранней стадии сравнительно низкая. В этой статье мы расскажем, какие бывают лимфомы, о симптомах, которые должны насторожить, о визуализации патологических изменений на КТ.
Лимфома легких — что это?
Лимфатическая система легких напоминает ветвистое дерево — ее сосуды пронизывают грудную клетку по всей длине и отвечают за лимфоток. Здесь расположено 13 разновидностей лимфотических узлов, классифицируемых по 5 группам:
1.Надключичные лимфатические узлы;
2.Верхние медиальные лимфатические узлы (паратрахеальные, преваскулярные, превертебральные);
3.Аортальные лимфатические узлы;
4.Нижние медиастинальные лимфатические узлы;
5.Корневые, долевые, (суб)сегментарные лимфатические узлы.
В узлах фильтруется лимфа и происходит созревание лимфоцитов. Лимфомы возникают в лимфатических узлах.
Поскольку лимфатическая система представляет собой обширную сеть сосудов, капилляров и полостей, то злокачественные клетки могут распространиться по всему телу, образовав множественные диссеминированные метастазы.
Диагностика лимфомы легких
Обычно медицинские специалисты отдают предпочтение МРТ, поскольку отсутствует лучевая нагрузка однако в случае с обследованием воздушной ткани легочной паренхимы, которая в норме практически не содержит жидкость, наиболее подробные результаты обследования и детализированное изображение можно получить с помощью КТ легких. Если лимфома выявлена на МРТ, и у врача есть подозрение, что раковые клетки мигрировали в костную ткань, то пациенту будет рекомендовано дополнительное обследование костей. В ходе компьютерной томографии исследуют ткани разной морфологии, попадающие в зону интереса: кости, внутренние органы, сосуды. Для диагностики последних необходимо дополнительное контрастирование.
Симптомы лимфомы лёгких
Основным симптомом, по которому проще всего заподозрить лимфому легких, является увеличение лимфоузлов, локализованных в области ключиц, шеи, средостения, между ребрами. Некоторые узлы спрятаны в самой грудной клетки и не пальпируются. В таком случае лимфома дает о себе знать только тогда, когда увеличивается в размере и начинает давить на соседние органы, что вызывает дискомфорт.
Важно понимать, что увеличение лимфоузлов не является специфическим признаком злокачественной лимфомы. Оно наблюдается после антибактериальной терапии и при любом инфекционно-воспалительном заболевании — педикулезе, ОРВИ, инфекциях ротоглотки и гортани (включая заболевания стоматологического характера), при болезни кошачьих царапин (лимфоузлы увеличиваются в ответ на повреждение кожи или укус, но не сразу, а в течение последующих 3-20 дней).
Обычно лимфоузлы, увеличенные из-за воспалений, при пальпации болят и вызывают дискомфорт. При лимфоме узлы безболезненные.
Некоторые вирусы способны менять нормальную структуру ДНК лимфоцитов таким образом, что клетки превращаются в злокачественные. Так вирус Эпштейна-Барр (ВЭБ) или ВИЧ-инфекции в анамнезе существенно повышает риск развитие лимфом.
К ранним симптомам лимфомы легких относится:
- Усталость, общая слабость;
- Высокая температура (около 38 градусов), лихорадка;
- Гипергидроз (преимущественно в ночное время).
В течение первых четырех недель проявляются и другие симптомы лимфомы лёгких:
- Увеличение лимфоузлов;
- Потеря аппетита и веса;
- Дисфагия (затрудненное глотание);
- Боль и дискомфорт в грудной клетке.
У некоторых пациентов наблюдается кожный зуд. Если лимфома сдавливает органы дыхания или происходит их поражение агрессивными раковыми клетками, возможны затрудненное дыхание, кашель, одышка.
Диагностировать лимфому самостоятельно невозможно, необходимо медицинское исследование внутренних органов и тканей лимфатической системы методом КТ или МРТ.
Лимфома легких — это рак?
Не всегда. Однако к лимфомам относятся преимущественно злокачественные новообразования лимфатической системы, которые формируются из-за бесконтрольного накопления патологически измененных лимфоцитов. Исключением могут быть индолентные лимфомы. Они не требуют лечения, однако наблюдать их тоже важно. Если при этом у пациента проявляется вышеописанная симптоматика (температура, лихорадка, боль в грудной клетке), то обследование и лечение таких лимфом должно проводиться обязательно.
Злокачественные клетки-лимфоциты обладают формой, отличной от «правильных» клеток, и представляют собой фатальный «сбой» в работе организма. У таких клеток возникают совсем другие функции - они производят огромное количество белков и токсинов, при этом не уничтожаются клетками иммунной системы как враждебные.
Лимфомы не всегда являются первичным очагом онкологии. Патологически увеличенный узел или их группа (диссеминированная или локализованная в одном месте) часто бывает следствием метастатических процессов. Это происходит в связи с тем, что лимфатический узел выполняет функцию фильтра и накапливает в себе злокачественные клетки, отделившиеся от первично пораженного органа. В таком случае важно не только выявить лимфому, но и первичный очаг. Увеличение лимфоузлов легких может указывать на рак легких, молочной железы, средостения, желудка, то есть органов, расположенных в непосредственной близости.
Уточнить диагноз относительно доброкачественного или злокачественного новообразования можно по результатам биопсии (гистологического исследования образца ткани). Также пациент сдает клинический и биохимический анализы крови.На КТ легких врачи выявляют новообразование, могут оценить его размер, распространенность увеличенных лимфоузлов, однако сделать точный вывод о разновидности опухоли без анализов не представляется возможным.
Какие бывают лимфомы?
Первично лимфомы принято делить на две большие группы:
- Лимфомы Ходжкина / лимфогранулематоз (болезнь Ходжкина, ходжинские лимфомы),
- Неходжскинские лимфомы (лимфосаркомы, НХЛ).
По данным НМИЦ онкологии им. Н.Н. Блохина, в России заболеваемость неходжкинскими лимфомами в 1,5-3 раза превышает заболеваемость лимфогранулематозом.
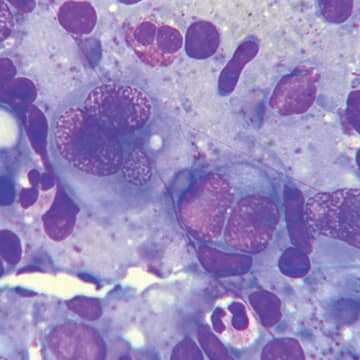
Разница между этими лимфомами становится ясна после морфологического исследования образца ткани (биопсии). При болезни Ходжкина в пораженных лимфоузлах обнаруживаются крупные мутировавшие клетки Березовского — Штернберга — Рида. Ходжкинские лимфомы отличаются более агрессивным течением с ярко выраженной симптоматикой, но они легко поддаются лечению.
Пораженные Ходжкинской болезнью лимфоузлы чаще всего расположены над ключицами, в области шеи, подмышечных впадин, средостения.
Неходжкинские лимфомы помимо B-лимфоцитов, поражают еще и T-лимфоциты. Заболевание обычно протекает без выраженной симптоматики и тяжело лечится. Но сначала необходимо правильно определить разновидность неходжкинской лимфомы — актуальная классификация состоит из 30 наименований, включая:
- хронический лимфолейкоз;
- Т-клеточный лейкоз;
- фолликулярная лимфома;
- диффузная В-крупноклеточная лимфома;
- грибовидный микоз Сезари и др.
4 стадии лимфомы легких
Стадии течения заболевания определяют по распространенности лимфом и объему пораженной ткани:
- 1 стадия: в патологический процесс вовлечен 1 лимфоузел или 1 группа лимфатических узлов;
- 2 стадия: в патологический процесс вовлечены 2 и более групп узлов, расположенных по одну сторону от диафрагмы;
- 3 стадия: поражены лимфоузлы с обеих сторон, в патологический процесс вовлечено несколько групп.
- 4 стадия: помимо тканей лимфатической системы болезнь поражает внутренние органы (легкие, сердце и др.)
При этом симптомы лимфомы могут быть выраженными уже на первой стадии, а могут не ощущаться пациентом практически до четвертой.
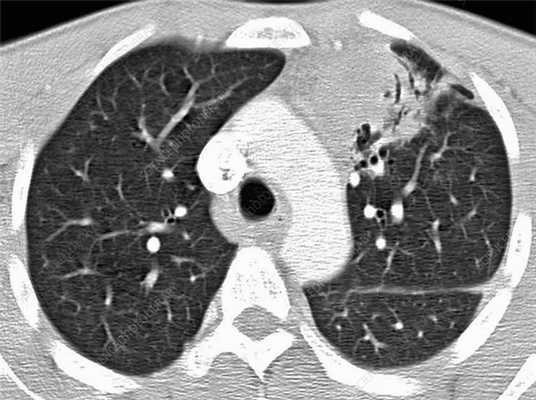
Лимфома легких на КТ
Признаки лимфомы легких особенно выражены на четвертой стадии заболевания, когда болезнь поражает дыхательный орган. На КТ при этом будут видны увеличенные лимфоузлы, формирующие цепочки, конгломераты. При этом у пациента может также наблюдаться отек легких. Однако высокая разрешающая способность КТ позволяет выявить лимфому на ранней, первой стадии.
На КТ лимфомы, как и любые уплотнения, визуализируются сравнительно более светлым цветом. В норме воздушная легочная паренхима практически однородного темного цвета. Иногда таких уплотнений несколько и они диссеминированны. Контуры лимфомы четкие и ровные. Вокруг патологических очагов обнаруживаются участки «матового стекла».
Читайте также:
- Повышение чувствительности цветовой допплерографии. Цветовая допплерография на ранних сроках беременности
- Лечение задержки роста при терминальной почечной недостаточности
- Изменения, происходящие в организме с возрастом
- Синдром Риля (Riehl)
- Локализация висцеральной боли. Пути передачи висцеральной боли
