Поражения почек у больного раком - диагностика, лечение
Добавил пользователь Skiper Обновлено: 21.01.2026
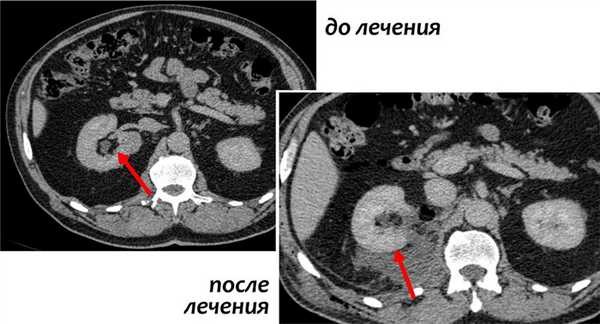
UPD 10.02.2021
Вопрос о том, сколько живут с раком 4 стадии с метастазами или еще более конкретный: «Маме (тете, бабушке…) поставили IV стадию, сколько ей осталось?», регулярно задают врачам-онкологам родственники пациентов. Не услышав однозначного ответа, вопрошающие, как правило, начинают сетовать на врачей.
Почему на вопрос о том сколько живут больные раком IV стадии нет и не может быть четкого ответа? От чего зависит продолжительность жизни пациента с этой самой поздней стадией онкологического заболевания? Этот вопрос мы задали врачу высшей категории, заведующей научным отделом инновационных методов терапевтической онкологии и реабилитации НИИ онкологии им. Н.Н. Петрова, доктору медицинских наук Семиглазовой Татьяне Юрьевне.
На сегодняшний день словосочетание «IV стадия рака» не несет под собой ровным счетом никакой информации, за исключением понимания степени распространенности процесса (наличие отдаленных метастазов).
Клетки рака - это собственные клетки человека над ростом и размножением которых организм потерял контроль.
Эволюция рака насчитывает 4 этапа - 4 стадии, каждую из которых принято обозначать римскими цифрами от I до IV. Обнаружение опухоли на этапе, когда уже появились метастазы в отдаленные лимфоузлы и/или ткани и органы, автоматически определяет стадию процесса как четвертую.
Что влияет на продолжительность жизни пациента с 4 стадией рака?
Прогноз жизни больных злокачественной опухолью IV стадии определяется скоростью распространения опухоли в окружающие ткани и отдаленные органы.
Период удвоения опухоли может занимать от 30 дней до нескольких лет и десятилетий. Есть опухоли, о существовании которых в своем организме человек может никогда и не узнать. Они характеризуются очень медленным ростом и длительно себя клинически никак не проявляют. Это так называемые, латентные, вялотекущие или «добрые» опухоли.
Пример из практики . В 1997 году под руководством профессора Михаила Лазаревича Гершановича мы лечили больную неходжкинской лимфомой IV стадии. Муж больной спрашивал нас о том, сколько осталось жить его молодой жене? После проведенной полихимиотерапии и лучевой терапии на оставшиеся очаги, больная вот уже 20 лет приходит ко мне на прием в полном здравии, а ее сын успешно поступил в Университет.
Есть «злые опухоли», для которых характерен агрессивный потенциал метастазирования. При, казалось бы, маленьких размерах первичного очага отмечается бурная диссеминация процесса — быстрое появление и рост отдаленных метастазов в различных органах, чаще всего в печени, легких, костях, головном мозге… Однако, в большинстве случаев, с помощью современного и своевременного противоопухолевого лечения все же удается взять под контроль симптомы заболевания и замедлить, а то и приостановить, «бег» самой болезни.
В ряде случаев резко усугубляют прогноз жизни больного сопутствующие заболевания (тяжелая форма сахарного диабета, хроническая декомпенсированная сердечная недостаточность, дыхательная или почечная недостаточность, цереброваскулярные и тромбоэмболические заболевания, хронические инфекции и т.д.), которые не дают провести лечение в полном объеме.
Парадоксы возраста
Существует мнение, что пожилым людям сложнее бороться с недугом под названием рак. Ведь большое количество сопутствующих заболеваний ограничивает применение тех или иных видов лечения, в связи с риском развития различных осложнений. С другой стороны — у пожилых людей обменные процессы замедлены, и течение самого заболевания не активное, вялотекущее. При этом важно помнить, что на сегодняшний день пожилой и старческий возраст не является сам по себе противопоказанием к назначению противоопухолевой лекарственной терапии. Большее значение имеет биологический возраст больного, а не тот, что указан в паспорте.
У молодых пациентов напротив — количество сопутствующих заболеваний в разы меньше, а серьезных и вовсе может не быть. Но активные обменные процессы могут отчасти способствовать агрессивному течению опухоли. Так что возраст становится и союзником, и врагом.
Большое значение имеет длительность анамнеза (истории) болезни, а также резервы противоопухолевого лечения.

Все зависит зависят от ряда важных факторов, главным из которых является паспорт опухоли, который определяется результатами гистологического, иммуногистохимического + молекулярно-генетического заключения.
Противоопухолевое лечение при IV стадии рака на сегодняшний день может включать:
- виды лекарственной противоопухолевой терапии:
- (например, антрациклиновые антибиотики - доксорубицин, или антиметаболиты - фторурацил, метотрексат);
- гормонотерапию (например, тамоксифен из группы антиэстрогенов);
- таргетную терапию (это когда противоопухолевый препарат действует на определенную опухолевую мишень как «ключ к замку», например, анти-HER2 препарат трастузумаб);
- иммунотерапию (моноклональные антитела к CTLA-4, PD-1, PD-L1 целенаправленно воздействуют на опухоль через иммунную систему, например, ипилимумаб, пембролизумаб, ниволумаб, пролголимаб, атезолизумаб и дурвалумаб);
- иммуноконъюгаты (химиотерапевтический препарат связан с таргетным препаратом посредством мостика, например, трастузумаб эмтанзин);
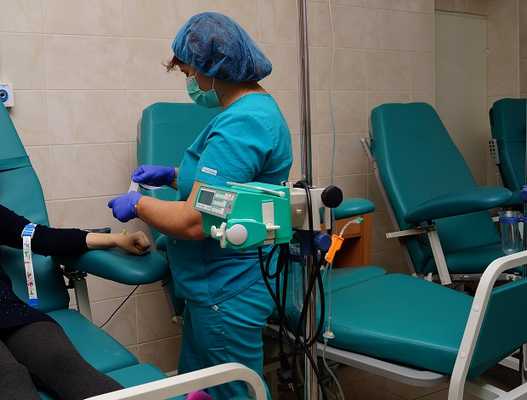
Химиотерапия
Показания к назначению химиотерапии больному IV стадией рака определяются чувствительностью опухоли к цитостатикам.
Поэтому по чувствительности к химиотерапии опухоли подразделяются на 3 основные группы:
- Высоко чувствительные к химиотерапии, которые с ее помощью могут излечиваться (герминогенные опухоли, пузырный занос, лимфома Ходжкина и т.д.).
- Опухоли, которые отвечают на химиотерапию, но с ее помощью до конца не излечиваются (неходжкинские лимфомы, рак молочной железы, мелкоклеточный рак легкого, рак яичников и т.д.).
- Опухоли, которые плохо поддаются химиотерапевтическому лечению, такие как рак желудка, рак печени, рак поджелудочной железы, меланома и т.д..
Иммунотерапия
За последние 20 лет возможности лекарственного противоопухолевого лечения больных IV стадией рака радикально изменились.
Важно помнить, что иммунотерапия - это не панацея от всех болезней. На данный вид терапии отвечает только 20-30% больных иммунокомпетентными опухолями. Вероятность ответа к иммунотерапии при соблюдении определенных показаний в соответствии с регистрационным удостоверением иммуноонкологических препаратов присутствует у больных следующими метастатическими опухолями:
- метастатические опухоли с высоким уровнем микросателлитной нестабильности (MSI-H);
- неоперабельная или метастатическая меланома;
- предлеченная неоперабельная или метастатическая карцинома Меркеля;
- рецидивирующий или метастатический плоскоклеточный рак головы и шеи;
- метастатический немелкоклеточный рак легкого (НМРЛ);
- метастатический мелкоклеточный рак легкого (МРЛ);
- предлеченный местнораспространенный или метастатический рак желудка или пищеводно-желудочного перехода;
- рефрактерная или рецидивирующая метастатическая лимфома Ходжкина;
- предлеченный метастатический рак эндометрия;
- предлеченный метастатический рак шейки матки;
- метастатический почечно-клеточный рак;
- неоперабельная или метастатическая гепатоцеллюлярная карцинома;
- местнораспространенный или метастатический уротелиальный рак;
- метастатический трижды негативный рак молочной железы с PD-L1 экспрессий в первой линии.
Реакция организма пациента на иммунотерапию особая. Поэтому для всех препаратов, относящихся к новому классу ингибиторов точек иммунного ответа, лечение следует начинать под контролем опытных и квалифицированных онкологов.
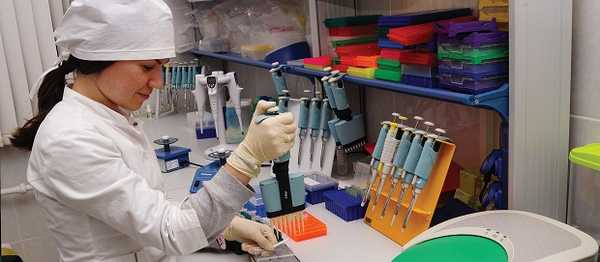
Лаборатория молекулярной онкологии
Участие в клинических исследованиях
Для онкологических больных IV стадией участие в клинических исследованиях крайне важно. Лечение инновационными лекарственными препаратами в рамках клинических испытаний позволяет в ряде случаев эффективно контролировать болезнь долгие годы. По российскому законодательству регистрация любого нового противоопухолевого препарата в России возможна после проведения исследований с участием российских пациентов. На включение нового препарата в действующие клинические рекомендации уходят годы, поскольку важно подтвердить безопасность и эффективность лекарственного средства. Пациент, желающий принять участие в клиническом исследовании после беседы с лечащим врачом-онкологом подписывает информированное согласие в нескольких экземплярах. В рамках клинического испытания больного информируют обо всех диагностических исследованиях и лечебных процедурах, включая введение исследовательского препарата, а также о том, что исследуемый препарат может оказаться неэффективным для пациента, как, впрочем, и препарат, назначенный в соответствии с клиническими рекомендациями. При этом участники клинического исследования обязаны четко соблюдать условия протокола, неукоснительно следуя графику процедур и визитов в исследовательский Центр. Контроль за соблюдением прав пациента осуществляется Министерством Здравоохранения России и этическим комитетом.
Почему опухоль сразу не отвечает на лечение или возобновляется рост метастазов после длительной ремиссии?
Ответ на этот вопрос кроется в биологии самой опухолевой клетки, которая, как все живое на планете, старается как можно быстрее адаптироваться к агрессивной окружающей среде. Например, многократный прием пенициллиновых антибиотиков способствует возникновению резистентности (потере чувствительности) у бактерий, поэтому требуется смена антибиотиков при очередном обострении воспалительного процесса.
Опухолевые клетки - это те же клетки организма, над которыми сам организм по ряду причин потерял контроль. Вместо запрограммированной гибели клетки опухоли приобрели способность бесконтрольного деления, роста и метастазирования. Поэтому после длительного и стойкого регресса (уменьшения) опухоли возобновляется рост опухоли или возникают новые метастазы. Опухоль со временем «умнеет»: с каждой линией нового лечения период до обострения болезни будет все короче и короче. Больные часто не понимают этого и просят вернуться к лечению, которое когда-то было столь эффективно.
Важно относиться с пониманием, когда врачи просят выполнить биопсию новых метастазов, например, в печени или легких. Поскольку новые опухолевые очаги могут отличаться по рецепторному и мутационному статусу, а может возникнуть и новая опухоль. Поэтому больному потребуется назначение нового лечения в зависимости от биологического подтипа или вновь обнаруженных мутаций.
Важно, чтобы проведение, по сути, токсичного лечения было возможно с учетом исчерпанных в ряде случаев резервов организма пациента или сопутствующей патологии. Например, при возникновении вирусных инфекций, в том числе гриппа или новой инфекции COVID-19, противоопухолевое лечение, как правило, приостанавливается, и все силы врачей, и все силы организма будут направлены на борьбу с заболеванием. Сроки возобновления противоопухолевого лечения обсуждаются с лечащим терапевтом и врачом-онкологом индивидуально.
Среди пациентов с 4 стадией онкологического заболевания нужно особо выделить паллиативных пациентов.
Паллиативные пациенты — это те онкологические больные, которые исчерпали все возможности лечения, их организм не может больше бороться с болезнью. Физическое состояние таких пациентов, обусловлено в ряде случаев полиорганной недостаточностью. Исчерпанные возможности противоопухолевого лечения не позволяют продолжать лечение. По картине клинического анализа крови можно увидеть, что резко угнетено кроветворение (к примеру, низкие показатели гемоглобина, тромбоцитов, лейкоцитов). В биохимическом анализе крови, наоборот, могут «зашкаливать», например, показатели креатинина, билирубина и/или трансаминаз и т.д.
Этап, когда паллиативный пациент испытывает сильную слабость, не встает с постели и самостоятельно не передвигается, не ест, у него наблюдается спутанность сознания — называют терминальным. Все возможные виды лечения уже испробованы и перестали работать, возможна лишь симптоматическая помощь (например, купирование болевого синдрома). Причиной гибели онкологических пациентов зачастую является полиорганная недостаточность. Опухоль угнетает функции важных органов и систем организма, опухолевая масса растет и становится несовместимой с жизнью. Тем не менее, пациенты с 4 стадией рака, получающие грамотную паллиативную медицинскую помощь, которая в настоящее время оказывается в полном объеме квалифицированным и специально подготовленным персоналом ХОСПИСов, могут жить достаточно долго и с хорошим качеством жизни. У каждого больного всегда есть шанс дождаться новых видов лечения, к которым рак будет чувствителен. Наука двигается вперед семимильными шагами!
Нельзя забывать также о психологической, социальной и духовной составляющих. Найти свои «духовные якоря» онкологическим пациентам часто помогают медицинские психологи.

Что дает онкологическому больному психологическая помощь?
- Улучшается эмоциональное состояние больных и родственников;
- преодолеваются тревоги, страхи, возникшие сложности в семейных взаимоотношениях;
- укрепляется мотивация к прохождению лечения;
- повышается качество жизни больных и членов их семей;
- приобретаются навыки эффективного общения с медицинским персоналом, коллегами, друзьями и близкими людьми.
Важно помнить, что IV стадия злокачественного процесса сегодня - это хорошо управляемый процесс, который с помощью противоопухолевого лечения успешно переводится в хронический и вялотекущий процесс. Это в свою очередь дает возможность больным доживать до нового и более эффективного лечения. Двадцатилетний опыт работы химиотерапевтом в НИИ онкологии им. Н.Н. Петрова на вопрос: «Cколько живут больные раком 4 стадии?» позволяет ответить: «Долго», но при условии своевременного и современного лечения.


Авторская публикация:
Татьяна Юрьевна Семиглазова
врач высшей категории
доктор медицинских наук
заведующая научным отделом инновационных методов терапевтической онкологии и реабилитации НИИ онкологии им. Н.Н. Петрова
Что вам необходимо сделать
Если вы хотите узнать побольше о бесплатных возможностях ФБГУ НМИЦ онкологии им. Н.Н. Петрова Минздрава России, получить очную или заочную консультацию по диагностике и лечению, записаться на приём, ознакомьтесь с информацией на официальном сайте.
Если вы хотите общаться с нами через социальные сети, обратите внимание на аккаунты в ВКонтакте и Одноклассники.
Почечная недостаточность при раке
Поражения почек при раке довольно распространены. Они многообразны как по своему характеру, так и по механизмам развития. Почечная недостаточность — состояние, при котором почки перестают справляться со своей функцией, и токсичные вещества, образующиеся в организме, скапливаются в крови. Это нарушает работу различных органов, значительно ухудшает самочувствие пациента, а в самых тяжелых случаях может привести к смертельному исходу.
Нарушение работы почек, вне зависимости от того, имелось ли оно ранее или возникло на фоне онкологического заболевания, ухудшает прогноз для онкобольного. Почечная недостаточность ослабляет организм, становится дополнительным фактором риска смертности, делает невозможным активное противоопухолевое лечение. При своевременной диагностике и начале лечения это осложнение можно предотвратить, и в ряде случаев полностью устранить, если оно уже развилось. В федеральной сети клиник «Евроонко» для этого применяются наиболее современные методики.
Причины развития почечной недостаточности при раке
К поражению почек при онкологических заболеваниях может приводить множество факторов. Основной причиной может стать непосредственно первичная злокачественная опухоль или метастатические очаги. Некоторые злокачественные новообразования приводят к обструкции (нарушению проходимости) мочевыводящих путей. В результате нарушается отток мочи, в почечной лоханке повышается давление, и из-за этого развивается поражение органа. Также опухоль может сдавливать сосуды, кровоснабжающие почку.
Целый ряд осложнений связан с противоопухолевой терапией:
- Острый канальцевый некроз — повреждение клеток, из которых состоят почечные канальцы. В норме в этих структурах происходит обратное всасывание воды и некоторых веществ из мочи в кровоток. Острый канальцевый некроз может протекать без симптомов или приводить к почечной недостаточности. Помимо нефротоксичных противоопухолевых препаратов, к этому осложнению у онкологических больных приводит сепсис.
- Нефролитиаз — конкременты (камни) в мочевыводящих путях. Развивается из-за ацидоза (повышения уровня кислотности) в почечных канальцах, поражения почек свободными радикалами, геморрагического цистита (воспаление мочевого пузыря, при котором появляется примесь крови в моче), инфекций мочевыводящих путей на фоне химиотерапии.
- Уратная нефропатия — поражение почек кристаллами мочевой кислоты.
- Лекарственный тубулоинтерстициальный нефрит — поражение почек, которое могут вызывать такие препараты, как цисплатин, некоторые обезболивающие средства, антибиотики.
- Тромботическая микроангиопатия (тромбоз и воспаление мелких сосудов) и мезангиолизис (разрушение соединительной ткани в почечных клубочках). К этим осложнениям могут приводить такие химиопрепараты, как винбластин, циклоспорин, митомицин.
У некоторых пациентов к поражению почек приводит синдром распада опухоли — состояние, при котором во время химиотерапии погибает большое количество опухолевых клеток, и в кровь выделяются токсичные вещества.
Отдельную группу патологий почек у онкологических больных составляют паранеопластические нефропатии. Их причиной является паранеопластический синдром, развивающийся в результате продукции раковыми клетками биологически активных веществ и реакции организма на злокачественную опухоль. Паранеопластические нефропатии — довольно большая группа заболеваний.
У онкологических больных нередко возникают обменные нарушения, например, повышение в крови уровня кальция, фосфатов, снижение уровня калия. Они также способны привести к поражению почек, в том числе острой почечной недостаточности.
Как развивается почечная недостаточность при онкологических заболеваниях?
Почечная недостаточность — это не какое-то одно заболевание. Под данным термином понимают комплекс симптомов, характеризующий нарушение функции почек. Он может возникать при разных заболеваниях, в качестве осложнения рака, противоопухолевой терапии.
Острая почечная недостаточность (острое повреждение почек*) характеризуется внезапным нарушением функции почек в течение нескольких дней или недель. Она развивается в результате ишемии (нарушения притока крови) и непосредственного повреждения ткани органа, например, токсичными веществами, которые образуются в организме при онкологическом заболевании, нефротоксичными лекарственными препаратами. В крови при этом повышается содержание азотистых соединений. Основные симптомы острой почечной недостаточности: тошнота, рвота, потеря аппетита, слабость. Может уменьшиться количество мочи. Быстро возникает нарушение водного, кислотно-щелочного, электролитного баланса. Если не начать вовремя лечение, у больного возникают эпилептические припадки, он впадает в кому.
"Острое повреждение почек" — более современный термин, принятый в 2007 году. Это более широкое понятие, чем «острая почечная недостаточность», оно отражает в том числе многие обратимые поражения почек.
Наиболее частыми причинами острой почечной недостаточности у онкологических больных являются:
- Острый канальцевый некроз на фоне противоопухолевой терапии.
- Синдром распада опухоли.
- Гиперкальциемия. Данное состояние развивается при поражении метастазами костей, разрушении костной ткани и вымывании кальция в кровь.
- Побочные эффекты химиопрепаратов, анальгетиков (НПВС), антибиотиков, рентгеноконтрастных препаратов.
Хроническая почечная недостаточность (хронические болезни почек) развивается в течение длительного времени. Функция почек снижается постепенно. Когда нарушения становятся выраженными, они приводят к таким симптомам, как потеря аппетита, стоматит, тошнота, рвота, металлический или кислый привкус во рту, апатия, частые мочеиспускания по ночам, снижение ясности ума, зуд, постоянное чувство усталости, судороги, отеки, истощение, поражение периферических нервов (нейропатия).
У некоторых пациентов хроническая почечная недостаточность развивается на фоне злокачественной опухоли, а у некоторых возникает первой и сама становится фактором повышенного риска развития ряда онкозаболеваний. Некоторые факторы риска, например, воздействие токсинов, являются общими для хронических болезней почек и злокачественных опухолей. Так или иначе, поражение почек ухудшает течение онкологического заболевания, а рак ухудшает течение хронической почечной недостаточности.
Классификация
Все причины почечной недостаточности, в том числе связанные с онкологическими заболеваниями, можно разделить на три большие группы:
- Преренальные — ухудшающие приток крови к почке и вызывающие поражение тканей органа в результате ишемии. К этим причинам относятся: уменьшение объема крови и сильное снижение артериального давления из-за кровотечения, рвоты, диареи, асцита и экссудативного плеврита, сдавление сосудов опухолью, тромбоз, сепсис, тяжелые осложнения во время операции и в послеоперационном периоде (шок).
- Ренальные — поражение непосредственно ткани почки опухолью, цитотоксичными препаратами.
- Постренальные — нарушение оттока мочи. К нему может привести опухолевая обструкция мочевыводящих путей, мочевые камни, асцит.
В зависимости от того, как меняется количество мочи, при острой почечной недостаточности выделяют три фазы:
- Продромальный период — нормальное количество мочи.
- Олигурический период — количество мочи уменьшается, обычно до 50-500 мл в сутки. У некоторых пациентов этого никогда не происходит, а у некоторых такое состояние сохраняется долго. Это зависит от причины почечной недостаточности, степени поражения ткани почек, времени начала лечения. У пациентов без олигурии лучше прогноз, и среди них ниже показатели смертности.
- Постолигурический период — постепенная нормализация количества мочи. После этого еще в течение нескольких дней сохраняются отклонения в лабораторных показателях: повышенный уровень мочевины, сывороточного креатинина.
В течении хронической почечной недостаточности выделяют следующие стадии:
- Стадия 1. Симптомы отсутствуют. Нарушение функции почек можно выявить только с помощью лабораторных анализов. Креатинин крови повышается, но не сильно — в пределах 440 мкмоль/л.
- Стадия 2. Появляются первые симптомы — повышенная утомляемость, сухость во рту, чувство жажды. Уменьшается объем мочи. Креатинин крови может повышаться до 880 мкмоль/л.
- Стадия 3. Состояние пациента ухудшается, он теряет в весе, пропадает аппетит. Креатинин крови повышается до 1320 мкмоль/л, развивается ацидоз — pH крови смещается в более кислотную сторону.
- Стадия 4. Нарушается работа сердца, легких, печени и других органов. Возникают отеки. Нарастает интоксикация.
Диагностика почечной недостаточности при раке
Цель обследования — диагностировать почечную недостаточность и разобраться в ее причинах.
При подозрении на острую почечную недостаточность врач в первую очередь осматривает пациента, выясняет, какими заболеваниями он страдает, какие принимает лекарства, проходил ли он исследования, во время которых внутривенно вводились йодсодержащие контрастные препараты. Проводят обследование, которое включает:
- анализ мочи с определением уровня белка;
- диагностические мочевые пробы;
- микроскопию мочевого осадка;
- определение остаточного объема мочи в мочевом пузыре;
- исследование креатинина в сыворотке крови;
- клиренс креатинина;
- исследование крови: в ней определяется анемия (снижение уровня эритроцитов, гемоглобина), повышение уровня калия, снижение уровня натрия, ацидоз (повышение кислотности).
В соответствии с рекомендациями KDIGO, острое поражение почек диагностируют, когда есть хотя бы один из следующих признаков:
- повышение уровня креатинина в сыворотке крови ≥ 26,52 мкмоль/л в течение 48 часов;
- увеличение уровня сывороточного креатинина в 1,5 раза или больше по сравнению с предшествовавшими 7 днями;
- объем мочи менее 0,5 мл/кг/час на протяжении 6 часов.
Чтобы установить причину острой почечной недостаточности, проводят дополнительные исследования, например, КТ, МРТ. В некоторых случаях прибегают к биопсии почек.
Лечение почечной недостаточности в первую очередь предусматривает борьбу с причиной, вызвавшей это состояние. Поэтому важно провести тщательное обследование, оценить влияние всех возможных факторов. Федеральная сеть клиник «Евроонко» располагает для этого всеми возможностями. У нас применяется новейшее диагностическое оборудование, мы сотрудничаем с ведущими лабораториями.
При хронической почечной недостаточности обследование включает общий анализ крови, исследование концентрации азота мочевины, уровней электролитов, креатинина, фосфатов, кальция, анализы мочи, микроскопию мочевого осадка, исследование белка мочи количественным методом, УЗИ почек, мочеточников, мочевого пузыря.
Лечение почечной недостаточности при онкологических заболеваниях
Лечение острой почечной недостаточности у онкологических больных обычно проводится в условиях стационара. Если возникают тяжелые, угрожающие жизни осложнения (отек легких, гиперкалиемия, тяжелые нарушения водно-электролитного, кислотно-щелочного баланса), пациента помещают в палату интенсивной терапии. Здесь проводятся экстренные мероприятия, жизненные функции пациента контролируют с помощью кардиомониторов и других аппаратов. В клиниках «Евроонко» функционируют отделения интенсивной терапии, оснащенные новейшим оборудованием. Здесь есть всё необходимое, чтобы в любое время суток, максимально оперативно оказать онкобольным с жизнеугрожающими состояниями все необходимые виды помощи.
В некоторых случаях возникают показания для гемодиализа или гемофильтрации (аппарат «искусственная почка»):
- тяжелые нарушения уровней электролитов, когда их не удается нормализовать другими способами;
- сохраняющийся отек легких на фоне медикаментозной терапии;
- ацидоз (снижение pH крови, ее «закисление»), с которым сложно бороться;
- признаки уремии — тяжелого состояния, связанного с накоплением в крови токсичных веществ: рвота, астериксис (непроизвольные движения кистью), эпилептические припадки, заторможенность, перикардит (воспаление околосердечной сумки).
В «Евроонко» применяется современный аппарат для высокоэффективной экстракорпоральной детоксикации Multifiltrate Fresenius (Германия).
Важно устранить причины, которые привели к почечной недостаточности, например, изменить схему терапии, если она включает нефротоксичные препараты, удалить опухоль или камень, которые мешают оттоку мочи, проводить эффективную противоопухолевую терапию, лечение синдрома распада опухоли.
Другие мероприятия при острой почечной недостаточности:
- Нормализация водного баланса. Если имеет место гиповолемия (уменьшение объема крови), проводят инфузионную терапию. Если, напротив, происходит задержка жидкости в организме, назначают диуретики (мочегонные препараты — но они не всегда эффективны).
- Высокий уровень калия в крови приводит к нарушению сердечного ритма, мышечной слабости. Для коррекции этого нарушения применяют внутривенные вливания кальция глюконата, сахара декстрозы и инсулина. Далее применяют натрия полистирена сульфонат, мочегонные препараты, при необходимости — диализ.
- Препараты кальция — при снижении его уровня в крови.
- Полноценное питание — 0,8 г белка на каждый килограмм массы тела в сутки.
- Потребление жидкости, адекватное ее потерям с мочой, стулом, рвотой, потом и пр.
- Ограничение натрия и калия.
При хронической почечной недостаточности, помимо лечения, направленного на причину, важно бороться с осложнениями. На ранних стадиях можно обойтись медикаментозной терапией. Назначают препараты, снижающие артериальное давление и уровень «плохого» холестерина в крови (при артериальной гипертензии и атеросклерозе), лекарства для борьбы с анемией, отеками, укрепления костей, диету с низким содержанием белка.
На более поздних стадиях хронической почечной недостаточности показан диализ, трансплантация почки.
Прогноз при почечной недостаточности у онкологических больных
Прогноз при острой почечной недостаточности зависит от причин, вызвавших это осложнение, степени поражения почечной ткани, тяжести состояния пациента в начале. Смертность от данной патологии в стационарах составляет 40-50%, а среди пациентов, оказавшихся в отделении интенсивной терапии и нуждающихся в диализе — 70-80%. Примерно 12,5% пациентов, оставшихся в живых, нуждаются в диализе, а у 19-31% имеется хроническое заболевание почек.
У онкологических больных острая почечная недостаточность существенно ухудшает прогноз, у многих впоследствии развиваются хронические болезни почек, повышается риск развития терминальной стадии почечной недостаточности.
Благодаря мультидисциплинарному подходу, в федеральной сети клиник «Евроонко» проводится эффективное лечение при различных осложнениях и сопутствующих заболеваниях у онкологических больных, в том числе таком грозном состоянии, как острая почечная недостаточность. Мы применяем передовой опыт мировой медицины, новейшее диагностическое и лечебное оборудование, оригинальные препараты последних поколений. Врачи в клиниках «Евроонко» работают в соответствии с современными международными рекомендациями, строго следуют принципам доказательной медицины, и при этом хорошо знают специфику работы с онкобольными. Пациенты, находящиеся в критических, угрожающих жизни состояниях, могут получить все необходимые виды помощи в полном объеме в отделении реанимации и интенсивной терапии. Для нас главная ценность — человеческая жизнь, и мы используем все возможности, чтобы ее сохранить.
Нефробластома
UPD 13.04.2021
Нефробластома, или опухоль Вилмса - опухоль почки, составляет 6% от всех злокачественных опухолей детского возраста. Опухоль названа по фамилии немецкого хирурга Макса Вильмса, впервые описавшего это заболевание в конце XVIII века.
Стандартом в лечении нефробластомы является комплексный подход: химиотерапия, туморнефроуретерэктомия и лучевая терапия. Прогноз заболевания при современных подходах к терапии благоприятный: выживаемость достигает 80%.
Распространенность нефробластом у детей
- Нефробластома - врожденная эмбриональная злокачественная опухоль почки.
- Заболеваемость составляет 1:100000 детей в возрасте до 14 лет.
- Опухоль выявляется преимущественно в возрасте 1-6 лет.
- Нет различий заболеваемости по полу.
- В 5% случаев наблюдаются двусторонние нефробластомы.

Точные причины возникновения опухоли Вильмса не установлены. Предполагается связь развития заболевания с мутацией в гене 1 опухоли Вильмса (WT 1), расположенного на 11 хромосоме. Этот ген важен для нормального развития почек и любые поломки в нем могут приводить к возникновению опухоли либо других аномалий развития почек. В 12-15% случаев опухоль Вильмса развивается у детей с врожденными аномалиями развития. Чаще всего имеют место аниридия (отсутствие радужной оболочки), синдром Беквита-Видемана (висцеропатия, макроглоссия, пупочная грыжа, грыжа белой линии живота, олигофрения, микроцефалия, гипогликемия, постнатальный гигантизм), урогенитальные аномалии, синдром WAIR (опухоль Вильмса, аниридия, мочеполовые аномалии, олигофрения), синдром Дениса-Драша (Опухоль Вильмса, нефропатия, аномалия гениталий, задержка роста, аномалии ушной раковины).
Если у кого-либо в семье уже была опухоль Вильмса, то у ребенка из этой семьи повышается вероятность заболеть нефробластомой. Частота «семейных» случаев, однако, не превышает 1%, при этом, как правило, опухолью поражаются обе почки.
Классификация опухолей почек у детей
Существует гистологическое и клиническое стадирование опухоли Вильмса:
I) Гистологическое стадирование по Smidt/Harms проводится после удаления новообразования и предусматривает выделение 3х степеней злокачественности, влияющих на прогноз заболевания (низкой, средней и высокой) в зависимости от строения опухоли.
II) Клиническое стадирование
В настоящее время используют единую систему стадирования нефробластомы, которая является определяющей для лечения:
I стадия - опухоль локализуется в пределах почки, возможно полное удаление
II стадия - опухоль распространяется за пределы почки, возможно полное удаление, в т.ч.:
- прорастание капсулы почки, с распространением в околопочечную клетчатку и/или в ворота почки,
- поражение регионарных лимфатических узлов (стадия II N+),
- поражение внепочечных сосудов,
- поражение мочеточника
III стадия — опухоль распространяется за пределы почки, возможно неполное удаление, в т.ч.:
- в случае инцизионной или аспирационной биопсии,
- пред- или интраоперационный разрыв,
- метастазы по брюшине,
- поражение внутрибрюшных лимфоузлов, за исключением регионарных,
- опухолевый выпот в брюшную полость,
- нерадикальное удаление
IV стадия - наличие отдалённых метастазов
V стадия - двусторонняя нефробластома
Классификация нефробластомы по системе TNM в настоящее время сохраняет, в основном, историческое значение и в клинической практике не используется.
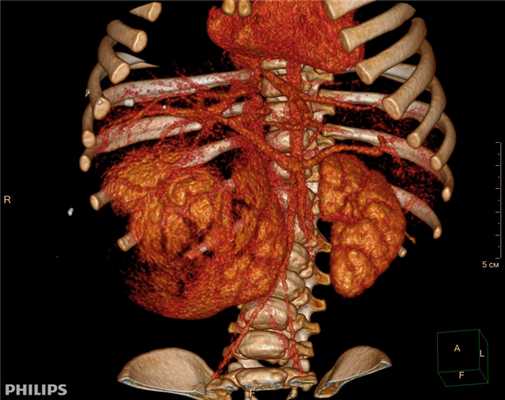
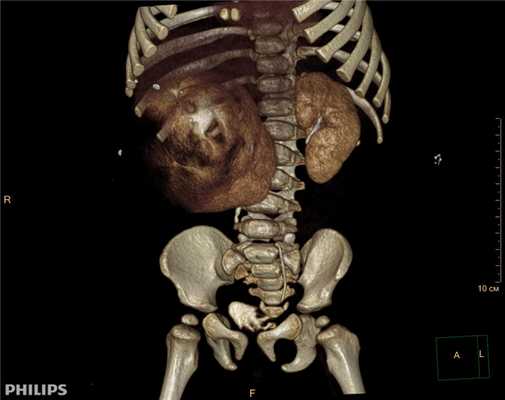
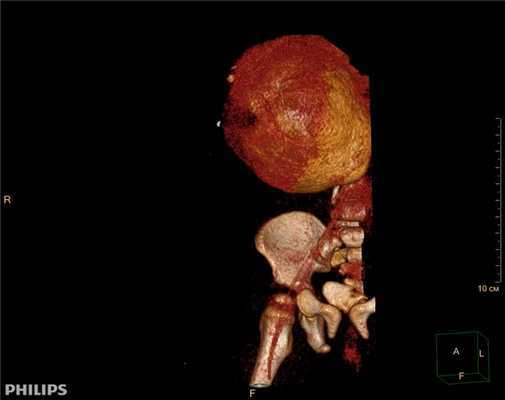
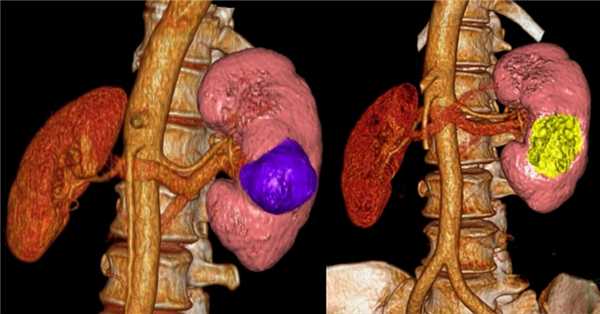
3D-реконструкции опухоли Вильмса пациентов детского отделения НМИЦ онкологии им. Н.Н. Петрова
Клинические симптомы опухоли почки у детей
Нефробластома может длительное время протекать бессимптомно. Первым признаком заболевания, который замечают родители, является увеличение размеров живота. Иногда ребенок жалуется на боли в животе. При микроскопическом исследовании мочи можно выявить микрогематурию.

Диагностика нефробластомы
Диагностические мероприятия при подозрении на опухоль Вильмса направлены, в первую очередь, на морфологическую верификацию диагноза и определение степени распространенности процесса в организме.
Основными инструментальными методами в диагностике опухоли почек у детей и подростков являются:
- и забрюшинного пространства.
- Компьютерная томография органов брюшной полости и забрюшинного пространства с оральным и внутривенным контрастированием.
- Магнитно-резонансная томография брюшной полости и забрюшинного пространства без и с контрастным усилением (даёт дополнительную информацию о распространённости и связи опухоли с окружающими органами).
- Радиоизотопное исследование почек - реносцинтиграфия позволяет оценить как суммарную функцию почек, так и отдельно функцию каждой из них.
- Для исключения метастатического поражения легких проводятся рентгенография и компьютерная томография органов грудной клетки.
Лабораторные исследования являются рутинными и включают в себя: клинический анализ крови, общий анализ мочи, биохимический анализ крови.
Непременным условием для постановки диагноза является выполнение тонкоигольной аспирационной биопсии опухоли под УЗИ-навигацией с проведением цитологического исследования полученного материала.
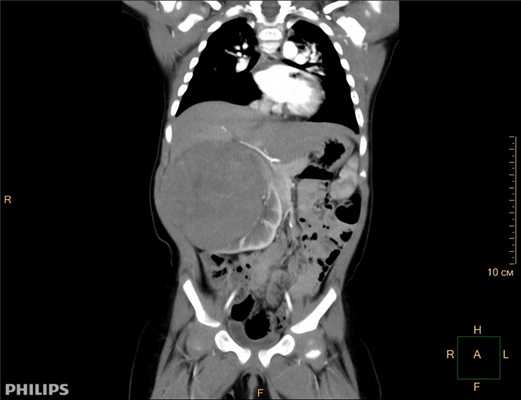
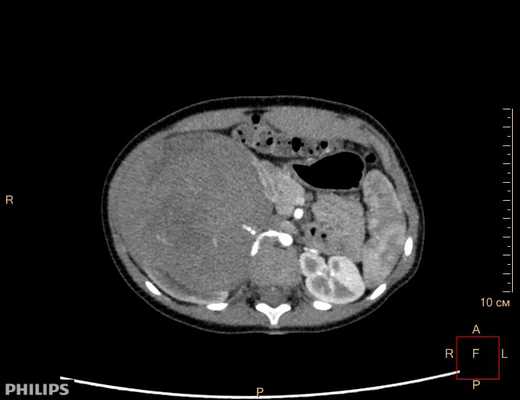
Опухоль Вильмса. Компьютерная томография
После удаления опухоли проводится ее морфологическое исследование. В зависимости от гистологического строения (мезобластическая нефрома, фетальная рабдомиоматозная нефробластома, кистозная частично дифференцированная нефробластома, классический» вариант без анаплазии, нефробластома с фокальной анаплазией, нефробластома с диффузной анаплазией) больные стратифицируются на группы риска.
Общие принципы лечения опухолей почки у детей и подростков
Лечение нефробластомы у детей проводится по стандартным методикам, принятым в европейских странах, и включает проведение неоадьювантного курса полихимиотерапии, операции - туморнефроуретерэктомии, послеоперационной химиотерапии и, по показаниям, лучевой терапии.
Предоперационный курс химиотерапии длится от 4 до 6 (при IV стадии) недель. Задача терапии - максимальное уменьшение размеров опухоли с целью предотвращения ее интраоперационного разрыва, т.е. во время операции и достижения максимальной резектабельности - возможности удалить больной орган. Базовыми препаратами, используемыми в данном курсе, являются винкристин и дактиномицин.
Оперативный этап лечения опухоли почки заключается в радикальном одномоментном удалении всей ткани опухоли. Туморнефроуретерэктомию проводят из срединного доступа. Обязательной является ревизия печени, контралатеральной почки и регионарных лимфатических узлов.
За последние десятилетия накоплен значительный опыт резекций почек при односторонней опухоли Вильмса, показавший сравнимые с классической нефрэктомией отдаленные результаты.
Лапароскопическая нефрэктомия при опухоли Вильмса впервые была выполнена в 2004 г. в университете Сан Пауло (Бразилия) у детей, получавших неоадъювантную терапию по протоколу SIOP-2001. К настоящему времени уже накоплен большой опыт ее применения, в том числе и в нашем Центре, позволяющий использовать минимально инвазивную хирургию не менее чем у 20% пациентов.
Метод лапароскопической ассистированной резекции почки возможен у пациентов с односторонней опухолью Вильмса только после неоадъювантной ПХТ и при соблюдении условий, оговоренных протоколом SIOP-RTSG 2016 «UMBRELLA»:
- объем первичной опухоли менее 300 мл;
- периферическая локализация и унифокальность;
- отсутствие инвазии в лоханку по данным предоперационной визуализации;
- отсутствие опухолевых тромбов и инвазии в соседние органы и ткани;
- отсутствие признаков разрыва капсулы, возможность радикального удаления опухоли при сохранении более 66% здоровой почечной ткани.
Послеоперационная химиотерапия проводится после разделения больных на группы риска в соответствии с гистологической структурой опухоли и стадии заболевания.
Лучевая терапия проводится параллельно послеоперационной полихимиотерапии, начинается на 2-3 неделе после удаления опухоли. Длительность лучевой терапии составляет 7-10 дней. Объем облучения зависит от результатов операции.
Диспансерное наблюдение при нефробластомах
Наблюдение за излеченными пациентами осуществляется для выявления рецидива и отдаленных последствий лечения.

В течение первых двух лет после окончания терапии пациенты обследуются каждые три месяца. Далее, до достижения пятилетнего срока наблюдения - каждые 6 месяцев. В алгоритм обследования включаются: УЗИ органов брюшной полости, рентгенография органов грудной клетки при каждом визите. При необходимости дополнительно рекомендуются проведение исследования функции почки (анализ мочи, биохимическое исследование крови, ренография), углубленное исследование сердечно-сосудистой деятельности (ЭКГ, ЭХО-КГ), исследование слуха методом аудиометрии.
После пяти лет наблюдения пациенты обследуются не чаще одного раза в год.
Все дети, закончившие программное лечение, могут продолжить посещение организованных детских коллективов (школа, детский сад).
Рак почки
Рак почки - это злокачественная опухоль, развивающаяся из почек. Почки - это парные органы, размерами примерно с кулак, располагающиеся на задней брюшной стенке справа и слева от позвоночника. Над каждой из почек находятся надпочечники.
Основная функция почек - фильтрация крови: удаление воды, солей и вредных веществ, попадающих в организм. Каждая из почек важна, однако, как правило, даже одной почки достаточно для нормального функционирования организма, и множество людей живут полноценной жизнью с одной почкой.
Почечноклеточный рак
Почечноклеточный рак (ПКР) является самым распространенным типом опухоли почки. Около 9 из 10 опухолей почки это ПКР.
Как правило, ПКР представлен одной опухолью почки, однако в некоторых случаях встречаются одновременно поражения обеих почек, или 2 или более опухоли в одном органе.
Существует несколько типов почечноклеточного рака, однако в основном отличить их друг от друга можно лишь под микроскопом. Несмотря на это, знание типа опухоли необходимо для помощи врачу выбрать тактику Вашего лечения.
Среди злокачественных опухолей почек, помимо почечноклеточного рака, существуют еще переходноклеточный рак, опухоль Вильмса и саркома почки.
Переходноклеточный рак
Из каждых 100 раков почки, около 5-10 будут представлять собой переходноклеточный (уротелиальный) рак. Эти опухоли представляют собой опухоли не собственно почки, а собирательной системы — чашек и лоханки. Этот тип рака, так же как и рак мочевого пузыря, очень часто связан с курением и воздействием токсических веществ (например, на производстве). Уротелиальный рак может проявлять себя, подобно почечноклеточному: болью в спине и, иногда, примесью крови в моче.
Переходноклеточный рак обычно лечится хирургически, операция предполагает удаление всей почки и мочеточника вместе с частью стенки мочевого пузыря, куда впадает мочеточник. Химиотерапия бывает необходима до или после операции, в зависимости от степени распространения опухоли.
Около 9 из 10 уротелиальных раков удается обнаружить на ранней стадии. Шансы на излечение снижаются в случае, если опухоль прорастает стенку мочеточника и врастает в почку, либо она выглядит агрессивнее при микроскопическом исследовании.
После лечения уротелиального рака необходимо наблюдаться у врача-онколога и выполнять следующие процедуры:
- цистоскопия — осмотр мочевого пузыря через специальный инструмент
- компьютерная томография
- магнитно-резонансная томографмя
Данная опухоль может появиться в мочевом пузыре и даже в других органах.
Опухоль Вильмса
Данная опухоль почти всегда поражает детей, и крайне редко возникает у взрослых.
Саркома почки
Саркома почки — это редкий тип опухоли, возникающий из стенок кровеносных сосудов или соеденительной ткани почки. Он составляет менее 1%от всех злокачественных опухолей почек
Какие факторы риска являются значимыми для рака почки?
Фактор риска - это что-то, что повышает шанс развития онкозаболевания. Различные опухоли могут иметь разные факторы риска. Некоторые факторы риска, такие как курение, можно предотвратить. Другие же, такие как возраст или наследственность, не могут быть предотвращены.
В случае рака почки, точная причина возникновения опухоли до сих пор не известна. Однако есть несколько путей снизить риск возникновения болезни:
- Курение сигарет ассоциировано с большим количеством случаев рака почки, и отказ от курения может снизить риск.
- Ожирение и высокое артериальное давление также являются факторами риска для рака почки. Контроль артериального давления и меры по снижению веса уменьшают шансы заболеть.
- И, наконец, необходима смена места работы в случае, если приходится контактировать с опасными веществами, такими как кадмий и органические растворители.
Симптомы и признаки рака почки
Опухоль почки на ранних стадиях, как правило, не вызывает никаких симптомов, однако чем больше стадия, тем больше риск появления различных симптомов, таких как:
- Примесь крови в моче (гематурия)
- Боль в пояснице с одной стороне
- Общая слабость
- Потеря аппетита
- Потеря веса, не связанная с диетой
- Повышение температуры на фоне отсутствия инфекционных заболеваний
- Анемия (снижение гемоглобина)
Эти признаки и симптомы могут быть вызваны раком почки, однако наиболее часто они вызываются другими, доброкачественными заболеваниями. Например, одной из основных причин появления крови в моче является мочекаменная болезнь. Таким образом, если появился один или несколько из вышеперечисленных симптомов, лучше посетить врача.
Диагностика
При подозрении на злокачественное образование в почках назначают ряд уточняющих обследований. С их помощью врач получает информацию о размере, границах, месте расположения опухоли в почке и оценивает общее состояние здоровья пациента.
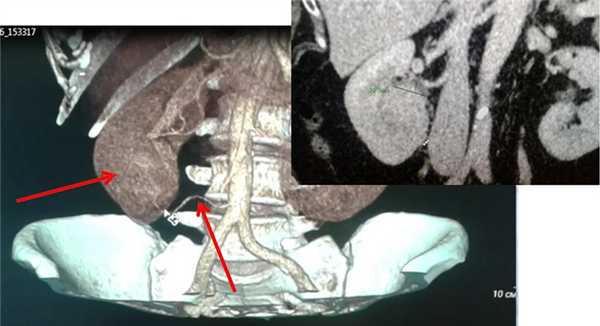
Комплекс исследований может включать в себя:
- Анализ мочи.
- Общий анализ крови.
- Биохимическое исследование крови.
- Компьютерная томография
- МРТ
- Ультразвуковое исследование
- Позитронно-эмиссионная томография (ПЭТ)
Некоторые другие исследования, такие как рентгенография или остеосцинтиграфия, будут полезны для определения распространения опухоли, т.е. метастазирования, в другие органы.
Стадирование рака почки
Лечение и прогноз заболевания определяются в зависимости от стадии опухоли почки. Наиболее широко для стадирования рака почки применяется система AJCC (Американского комитета по злокачественным заболеваниям), также известная как система TNM.
Стадия злокачественного образования зависит от его распространения: прорастания опухоли в близко расположенные ткани и органы, окружающие его лимфатические узлы, а также от наличия метастазов в отдаленных органах.
Стадирование основывается на результатах врачебного осмотра, биопсии и диагностических исследований.
Для злокачественной опухоли почки может быть 2 типа стадирования:
- Клиническая стадия, которая отражает клиническое представление врача о болезни
- Патологическая стадия, которая основана на тех же принципах, что и клиническая, плюс учитываются данные операции и исследования удаленного органа. Патологическая стадия считается более точной, чем клиническая.
Стадия может измениться после операции, например, если будет обнаружено распространение рака шире, чем предполагалось.
Стадия и прогноз
Выживаемость - это часто используемый показатель для оценки прогноза у пациента.
5-летняя выживаемость показывает на процент пациентов, кто прожил более чем 5 лет после установления диагноза. Разумеется, много людей живут намного дольше, чем 5 лет, и многие излечены от заболевания. Также, причиной смерти некоторых людей может быть не онкологическое заболевание.
Выживаемость пациентов с раком почки в зависимости от стадии заболевания
| Стадия | 5-летняя выживаемость |
| I | 81% |
| II | 74% |
| III | 53% |
| IV | 8% |
Эти цифры получены из национальной базы данных по злокачественным заболеваниям США, и могут отличаться для пациентов в РФ. Эти показатели включают в себя людей с установленным диагнозом рака почки, которые позже могли умереть от других причин, например, болезни сердца.
Лечение рака почки
Одним из самых важных факторов, имеющих значение для выбора плана лечения, является стадия заболевания. Также влияют такие факторы, как: общее состояние, возможные побочные эффекты от лечения, возможность полного исцеления, продления жизни или облегчения симптомов.
Варианты лечения рака почки могут включать в себя:
- Хирургию
- Абляцию
- Активное наблюдение
- Лучевую терапию
- Таргетную терапию
- Иммунотерапию
- Химиотерапию
Хирургическое лечение рака почки
Хирургия - это основное лечение рака почки. Шансы избавиться от заболевания без проведения операции очень малы. Даже пациенты с распространением рака на другие органы получают пользу от удаления опухоли почки. Удаление почки с опухолью может помочь некоторым пациентам продлить жизнь, а также убрать такие симптомы как боль и кровотечение.
В зависимости от стадии и расположения опухоли, хирургическим методом может быть удалена только опухоль с окружающей частью почки — так называемая резекция почки, либо целая почка с опухолью — нефрэктомия. Надпочечниковая железа и жировая ткань вокруг почки также может быть удалена вместе с почкой, если возникнет необходимость.
Нефрэктомия
Нефрэктомия - удаление почки, иногда вместе с надпочечником и окружающей жировой клетчаткой. Большинство людей с одной почкой живут обычной жизнью.
В условиях отделения онкоурологии и общей онкологии НИИ онкологии им. Н.Н. Петрова наиболее часто выполняется лапароскопический вариант данной операции. При этом вместо большого разреза используется несколько небольших разрезов 10-15 мм длиной, через которые устанавливаются специальные тонкие инструменты и лапароскоп с видеокамерой на конце. При помощи лапароскопии хирург видит происходящее на экране. После удаления почки для того, чтобы убрать ее из брюшной полости, производится разрез внизу живота, соответсвующий по размерам удаленному органу.
В случае, если опухоль распространяется в просвет почечной вены и/или в нижнюю полую вену, лапароскопический вариант операции возможен, однако он чаще, чем обычно, требует перехода на большой разрез при технических сложностях.
Резекция почки
В ходе данной процедуры, хирург удаляет только ту часть почки, которая содержит опухоль, оставляя оставшуюся ткань почки неповрежденной. В настоящий момент это предпочтительный метод лечения для пациентов с ранней стадией рака почки. Часто резекции вполне достаточно для удаления одиночных небольших опухолей до 4 см в диаметре.
Также этот метод может применяться у пациентов с бОльшими образованиями, до 7 см. Специалистами НИИ онкологии им. Н.Н. Петрова успешно выполнялись вмешательства на опухолях размерами 10 и более см, однако такие операции возможны только в отдельных случаях, с учетом анатомии опухоли.
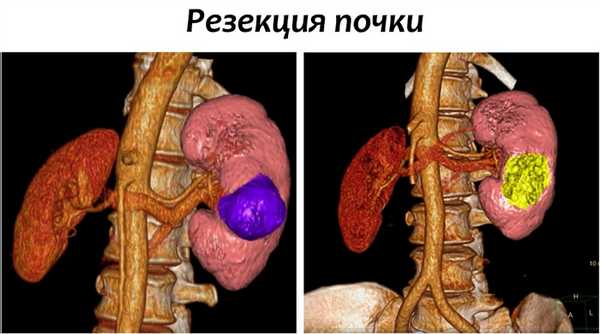
Современные исследования показали, что отдаленные результаты у пациентов, перенесших резекцию почки, почти такие же, как у пациентов, у которых почка была удалена. Однако несомненным плюсом остается сохранение большей части почечной функции.
По сравнению с открытой операцией после лапароскопии менее выражен болевой синдром и уже в первые сутки после операции больные более активны.
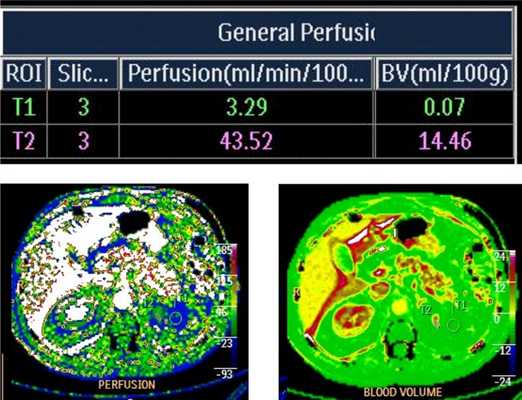
После резекции почки, для определения функционального состояния пациента в НИИ онкологии проводится перфузия почки.
Регионарная лимфаденэктомия (лимфодиссекция)
Эта операция предполагает под собой удаление ближайших к почке лимфатических узлов в случае, если имеется подозрение на их поражение. В настоящий момент не существует единого мнения, необходимо ли во всех случаях рака почки удалять лимфатические узлы. В основном считается, что необходимость удаления лимфоузлов возникает, если они выглядят увеличенными по данным КТ или МРТ, либо в ходе операции.
Удаление надпочечника (адреналэктомия)
Адреналэктомия является стандартной частью нефрэктомии, однако если опухоль расположена в нижнем сегменте почки, относительно далеко от надпочечника, и визуализационные методы не показывают поражения надпочечника, он может быть сохранен. Так же, как и удаление лимфоузлов, удаление надпочечника рассматривается индивидуально в каждом случае.
Удаление метастазов (метастазэктомия)
У около 25% больных раком почки на момент диагностики имеется распространение (метастазы) заболевания на другие органы. Наиболее часто к ним относятся легкие, кости, печень и головной мозг. В некоторых случаях при такой ситуации может помочь оперативное лечение. Наиболее часто оно может применяться в случаях, если имеется единичный метастаз, который может быть хирургически удален, либо в случаях, когда удаление метастаза может облегчить симптомы болезни, такие как боль.
Риск и побочные явления после операции
Оперативное вмешательство всегда предполагает риск возможных осложнений. К ранним осложнениям относятся: реакция на анестезию (наркоз), кровотечение, которое может потребовать переливание крови, формирование гематом и возникновение инфекции. У большинства пациентов после операции возникает боль, которая может быть снята применением обезболивающих препаратов.
Другие риски включают в себя:
- Повреждение в ходе операции других органов и кровеносных сосудов, таких как : селезенка, печень, поджелудочная железа, аорта, нижняя полая вена, кишечник.
- Пневмоторакс (появление воздуха в грудной полости)
- Послеоперационная грыжа в месте проведения разреза
- Истечение мочи в брюшную полость или в забрюшинную жировую ткань после выполнения резекции почки
- Почечную недостаточность (нарушение функции оставшейся почки или части резецированной почки)

Авторская публикация:
Джалилов Имран Бейрутович
врач хирург-онколог отделения онкоурологии
НИИ онкологии им Н.Н. Петрова
Читайте также:
