Появление III и IV тона сердца при тиреотоксикозе. Гиперфункция миокарда при тиреотоксикозе
Добавил пользователь Владимир З. Обновлено: 01.02.2026
Статья посвящается q-инфарктам миокарда у больной с тиреотоксикозом.
Ключевые слова
Для цитирования:
Рунов Г.П., Боровков Н.Н., Фурменкова Ю.В. Q-инфаркт миокарда у больной с тиреотоксикозом. Проблемы Эндокринологии. 2003;49(6):51-52.
For citation:
Runov G.P., Borovkov N.N., Furmenkova Yu.V. Q-infarction in a female patient with thyrotoxicosis. Problems of Endocrinology. 2003;49(6):51-52. (In Russ.)
Утверждение о том, что инфаркт миокарда у больных с тиреотоксикозом встречается крайне редко, общеизвестно. Эта закономерность связана со снижением склонности к тромбообразованию под действием тиреоидных гормонов (увеличение сосудистой скорости кровотока, снижение активности свертывающей системы крови и активация противосвертывающей системы, снижение уровня общего холестерина, p-липопротеидов, триглицеридов, холестерина липопротеидов низкой плотности) [2-4, 6, 7]. Установлено, что препараты гормонов щитовидной железы даже способствуют обратному развитию экспериментального атеросклероза [7].
В то же время большинство авторов утверждают, что избыток тиреоидных гормонов повышает активность симпато-адре- наловой системы, увеличивая несоответствие между доставкой и утилизацией кислорода миокардом. Это в свою очередь ведет к тяжелым обменно-дистрофическим повреждениям миокарда и развитию тиреотоксической кардиомиопатии 4.
По данным клиники, частота ангинозных болей при тиреотоксикозе достигает 20% [3]. Они могут возникнуть вследствие как метаболических изменений миокарда [4], так и относительной недостаточности коронарного кровообращения [3]. Однако случаи коронарной недостаточности, тем более инфаркта миокарда, единичны [3].
Больная Ч., 43 лет, находилась в эндокринологическом отделении Нижегородской областной клинической больницы (ОКБ) им. Н. А. Семашко с 19 02 по 05.03.02. При поступлении беспокоили нарушение сна, общая слабость, тревожность, раздражительность, похудание на 24 кг за 2 года, сердцебиение, одышка при ходьбе на расстояние более 300 м.
Считает себя больной с 1999 г., когда появилась общая слабость, потливость. При обследовании обращало на себя внимание увеличение щитовидной железы II степени. Заподозрен гипертиреоз. Исследование тиреоидных гормонов радиоиммунным методом в сентябре 1999 г.: Т4 220,8 нмоль/л, Т3 3,9 нмоль/
л. Тест поглощения со ”4: через 2ч - 49%, через 4ч - 65%, через 24 ч - 77%. Получала тиамазол 30 мг в сутки. После уменьшения дозы до поддерживающей прием препарата самостоятельно прекратила. Одновременно появились приступы сжимающих болей за грудиной при ходьбе на расстояние 300-400
м. Диагностирована ИБС: стабильная стенокардия напряжения II функционального класса, HKNA. 02.01.02 подняла груз общей массой 30 кг одномоментно, после чего почувствовала резкую слабость, головокружение, острую боль за грудиной. Госпитализирована в районную больницу по месту жительства, где после регистрации ЭКГ выявлена острая фаза Q-инфаркта переднеперегородочной области. На фоне соответствующего режима и лечения наблюдалась положительная ЭКГ-динамика. Однако усилилась клиническая симптоматика тиреотоксикоза, в связи с чем больная направлена в ОКБ для уточнения диагноза и тактики дальнейшего ведения.
При ультразвуковом исследовании щитовидной железы правая доля размером 20*21 *57 мм, объем 11,9 мл, левая доля размером 21*24*58 мм, объем 14,6 мл, перешеек 6 мм; структура умеренно неоднородна, узлов не выявлено. На ЭКГ 02.01.02: отсутствие зубца Я в отведениях V,- V3, подъем сегмента ST в отведениях V,-V4 на 2 мм, признаки полной блокады левой ножки пучка Гиса (см. рисунок). Назначены тиамазол 30 мг/сут, атенолол 50 мг/сут, феназепам 10 мг на ночь, кардикет 20 мг 2 раза в сутки.
Больная Ч., 43 лет, с диффузным токсическим зобом II степени, ЭКГ. Острая фаза Q-инфаркта миокарда переднеперегородочной области, полная блокада передней ножки пучка Гиса.
Поставлен диагноз: диффузный токсический зоб 11 степени средней тяжести с кардиальной, глазной и невротической симптоматикой. Ишемическая болезнь сердца: стабильная стенокардия напряжения II функционального класса, постинфарктный кардиосклероз (перенесенный Q-инфаркт переднеперегородочной области 02.01.02), НКИД (NYHA. II функциональный класс). Пациентке ограничен режим до полупостельного, увеличена доза нитратов до 40 мг кардикета 2 раза в сутки, к лечению добавлен аспирин 50 мг. На ЭКГ от 05.03.02 положительная динамика - отсутствие диагностированной ранее полной блокады левой ножки пучка Гиса. Больная выписана в удовлетворительном состоянии. Жалоб не предъявляла.
Данное наблюдение свидетельствует о том, что у пациентов с тиреотоксикозом физические перегрузки могут привести к развитию ишемического повреждения миокарда. Особой тщательности требует анализ ЭКГ у больных токсическим зобом при появлении жалоб стенокардического характера.
Тиреотоксический криз
Тиреотоксический криз - это ургентное осложнение диффузного токсического зоба, спровоцированное повышением активности тиреоидных гормонов в крови. Проявляется лихорадкой, потливостью, учащенным сердцебиением, одышкой, гипертонией, абдоминальными болями, приступами тошноты и рвоты, диареей, беспокойством и возбуждением. При тяжелом течении развивается кома, а затем смерть. Диагноз устанавливается по результатам опроса, осмотра, лабораторных тестов и ЭКГ. Лечение в основном медикаментозное, направлено на устранение тиреотоксикоза и восстановление жизненных функций.
МКБ-10

Общие сведения
По мнению большинства исследователей в области практической эндокринологии, тиреотоксический криз развивается только при базедовой болезни, в отдельных источниках указывается на возможность возникновения данного осложнения на фоне интоксикации при болезни Пламмера. Согласно различным статистическим данным, частота кризового состояния составляет от 0,5 до 9% случаев тяжелого тиреотоксикоза. Гендерное соотношение такое же, как при диффузном токсическом зобе: в женской популяции эпидемиологические показатели в 9 раз выше, чем в мужской. Средняя продолжительность тиреотоксикоза, который предшествует кризу - 2-4 года, развернутая симптоматика гипертиреоза наблюдается не менее 2-х лет.

Причины
Наиболее распространенным этиофактором развития криза является операция на щитовидной железе по поводу тиреотоксической аденомы либо диффузного тиреотоксического зоба. Для снижения риска осложнения необходима правильная подготовка пациентов к хирургическому вмешательству - достижение стабильного эутиреоза при помощи медикаментозной терапии. К менее частым причинам криза относятся:
- Операции на других органах. Хирургические процедуры способны спровоцировать усиление выработки йодированных гормонов. Риск повышается при использовании эфирного наркоза.
- Инфекционные болезни. Острое течение инфекций у людей с болезнью Грейвса увеличивает вероятность криза. Самыми опасными в этом плане являются бронхолегочные заболевания.
- Сахарный диабет. Провоцирующими факторами становятся метаболические осложнения сахарного диабета. Тиреоидные гормоны производятся активнее при кетоацидозе, гиперосмолярной коме и гипогликемии из-за введения больших доз инсулина.
- Провокация тиреотоксикоза. Обострение тиреотоксикоза может быть вызвано внешними факторами, стимулирующими секрецию йодсодержащих гормонов. К ним относятся самостоятельная отмена или изменение дозировки антитиреоидных лекарств, терапия радиойодом, рентгенологические обследования с использованием йодовых контрастов, лечение раствором йодида калия, травмирующая пальпация зоба.
- Тяжелые сопутствующие заболевания. Развитие криза бывает связано с нарушением мозгового кровообращения, тромбоэмболией легочной артерии, острым гастроэнтеритом, травмами. В группе повышенного риска беременные и роженицы.
Патогенез
Патогенетические механизмы остаются не до конца изученными. Распространена теория о развитии осложнения в связи с избыточной секрецией тироксина и трийодтиронина. Согласно исследованиям, активность щитовидной железы у больных действительно повышена, но не более, чем при обычном течении тиреотоксикоза без осложнений. Предположение о ведущей роли свободных (несвязанных) гормонов T3 и T4 также не нашло подтверждения.
Другая теория, которая продолжает разрабатываться, основана на гипотезе о гиперактивности катехоламинов как ключевом факторе манифестации криза. Концентрация адреналина и норадреналина в плазме не повышается, но в сердечной мышце существуют две раздельные системы, чувствительные к катехоламинам и тиреоидным гормонам, и сочетанное воздействие этих соединений проявляется кризом.
Сторонники третьей теории рассматривают как патогенетическую основу тиреотоксического криза усиление периферической реакции на влияние трийодтиронина и тироксина. В итоге увеличивается липолиз и теплопродукция, повышается температура, истощается устойчивость тканей к воздействию тиреоидных гормонов, развивается декомпенсация болезни Грейвса.
Симптомы тиреотоксического криза
В 90% случаев возникает расстройство функций центральной нервной системы. На первом этапе преобладают симптомы двигательного и психического возбуждения: пациенты тревожны, эмоционально неустойчивы (плачут, проявляют агрессию, смеются), гиперактивны и нецеленаправленны в поведении. Возможно развитие психоза. По мере прогрессирования криза такое состояние сменяется заторможенностью, апатичностью, эмоциональным отупением, крайней мышечной слабостью. Тиреотоксическая форма миопатии проявляется снижением тонуса и быстрой утомляемостью мышц шеи, лопаточной области, рук и ног, реже - лица и туловища. Могут наблюдаться боли, непроизвольные подергивания, судороги, гипокалиемический пароксизмальный паралич (приступообразная выраженная слабость мышц).
Симптомы расстройства желудочно-кишечного тракта включают тошноту, рвоту, снижение аппетита, спастические боли в животе, частую дефекацию, диарею и, как следствие, потерю веса. Нарушается работа почек, объем выделяемой мочи сокращается вплоть до полного ее отсутствия (анурии). У половины больных развиваются сердечно-сосудистые расстройства: тахикардия, аритмии. Повышается частота сердечных сокращений, возрастает артериальное давление, появляется одышка, затрудняется дыхание.
У лиц старше 60 лет повышается вероятность развития атипичной формы тиреотоксического криза. Для нее характерно скрытое течение либо доминирование симптомов патологии какой-либо одной системы организма, что значительно затрудняет диагностику. При латентном варианте криза больные находятся в летаргическом состоянии, заторможены, апатичны. Может определяться опущение верхнего века (блефароптоз), миопатия. При «маскированном» варианте разворачиваются изолированные симптомы нарушения нервной, сердечно-сосудистой, дыхательной или пищеварительной системы.
Осложнения
Диагностика
Обследование проводит врач-эндокринолог. Диагностика выполняется в экстренном порядке, включает набор процедур, позволяющих оценить анамнез и тяжесть текущего состояния пациента, выявить признаки, подтверждающие декомпенсацию тиреотоксикоза. При развернутой клинической картине дифференциальная диагностика не актуальна, при неравномерном проявлении симптомов может возникнуть необходимость исключения сердечной недостаточности, острой интоксикации. В комплексное исследование входит:
- Клинический опрос. У всех больных в анамнезе имеется диагноз «диффузный токсический зоб», у большинства присутствует провоцирующий фактор в недавнем прошлом - операция, лечение радиойодом, прием йодсодержащих препаратов и др. Пациенты сообщают о чувстве слабости, вялости, одышке, дрожи, потливости, нарушениях функций пищеварительного тракта.
- Осмотр. Наблюдается лихорадка, состояние нервного возбуждения. При пальпации живота отмечается болезненность. Измерение артериального давления дает повышенные и высокие показатели - от 130 до 300 мм рт. ст. Фонендоскопическое обследование выявляет тахикардию. Температура тела - от 38° до 41°C.
- Лабораторные анализы. Проводятся исследования гормонов и уровня глюкозы крови. Для криза характерно повышение содержания тироксина (Т4), трийодтиронина (Т3); уменьшение концентрации тиреотропина (ТТГ) и кортизола. Часто обнаруживается гипергликемия, сниженный уровень холестерина.
- ЭКГ. По данным электрокардиографического исследования диагностируется синусовая тахикардия и фибриляция предсердий, увеличение амплитуды зубцов T и QRS. Иногда определяется нарушенная внутрижелудочковая проводимость.
Лечение тиреотоксического криза
Терапия включает общие мероприятия, позволяющие восстановить жизненно важные функции организма, а также устранение состояния декомпенсации болезни. Неотложная помощь осуществляется на догоспитальном этапе и направлена на восстановление водно-электролитного баланса, поддержание дыхательной функции и работы сердца. После подтверждения диагноза разрабатывается индивидуальная схема лечения, которая включает следующие компоненты:
- Антитиреоидная терапия. Проводятся процедуры, снижающие уровень трийодтиронина и тироксина до нормы. Больным назначается прием тиреостатиков, йодидов, бета-блокаторов. Если медикаментозное лечение оказывается неэффективным, для удаления из крови Т3 и Т4 используется плазмаферез или гемосорбция.
- Восстановление функций организма. Всем больным показана инфузионная терапия раствором глюкозы и раствором натрия хлорида. Эти процедуры устраняют обезвоживание, нормализуют уровень электролитов. Артериальная гипертензия купируется гипотензивными средствами, гипотония - вазопрессорными препаратами, сердечно-сосудистая недостаточность - сердечными гликозидами. Пациентам в тяжелом состоянии бывают необходимы процедуры оксигенотерапии, искусственная вентиляция легких.
- Устранение сопутствующих заболеваний. Параллельно выполняется лечение патологических состояний, провоцирующих и поддерживающих криз. При бактериальных инфекциях используются антибиотики, при декомпенсации сахарного диабета - препараты инсулина. Пересматриваются назначения медикаментов, способных усилить выработку тиреоидных гормонов.
Прогноз и профилактика
При правильном лечении острое состояние удается устранить в течение 3-5 дней. В стабильном периоде требуется постоянный контроль уровня гормонов. Ключевым моментом в профилактике тиреотоксического криза является правильная подготовка пациентов к процедуре хирургического вмешательства и к лечению радиоактивным йодом: при помощи медикаментозной терапии должно быть достигнуто относительно стабильное состояние эутиреоза - нормальной концентрации гормонов щитовидной железы в крови. Помимо этого всем пациентам необходим регулярный контроль врача, внеплановые консультации и обследования при развитии инфекционного заболевания, после травм, перед операциями и родами, во время беременности.
1. Тиреотоксический криз. Редкие проявления и трудности своевременной диагностики/ Газизова Д.О., Васичкин С.В., Харкенен П.О , Фомин Д.К., Чупина Л.П., Кожокару А.Б., Шевченко Н.С.// Клиническая и экспериментальная тиреоидология. - 2015 - Т.11, №1.
2. Неотложные состояния в эндокринологии детского возраста: учебно-методическое пособие/ Козарезов С.Н. - 2014.
3. Неотложная эндокринология: учебник/ Жукова Л.А., Сумин С.А., Лебедев Т.Ю., Андреева Н.С., Гуламов А.А. - 2006.
Тиреотоксическое сердце
Тиреотоксическое сердце - это синдром поражения сердечно-сосудистой системы у пациентов с тиреотоксикозом. Патология в основном возникает при Базедовой болезни, реже ее причинами становятся тиреоидиты, ТТГ-продуцирующие гипофизарные опухоли, новообразование щитовидной железы. Симптомы заболевания включают тахикардию и другие нарушения ритма сердца, признаки сердечной недостаточности. Для диагностики назначается ЭКГ и ЭхоКГ, исследование гормонального профиля, сцинтиграфия щитовидной железы. Лечение предполагает коррекцию эутиреоза, прием бета-блокаторов, антиаритмиков и других препаратов патогенетической терапии.



Негативное влияние избытка гормонов щитовидной железы (ЩЖ) на работу сердца было впервые установлено английским врачом К. Парри в 1785 г. В 1835 г. ирландский доктор Роберт Грейвс и немецкий специалист Карл фон Базедов описали тахикардию, сопряженную с увеличением щитовидной железы. Проявления тиреотоксического сердца разной степени интенсивности возникают у всех пациентов с токсическим зобом, тяжелые сердечно-сосудистые болезни наблюдаются у 12-68% больных. Риск кардиоваскулярных осложнений имеет прямую корреляцию со стажем тиреотоксикоза.

Тиреотоксическое сердце чаще всего развивается при диффузном токсическом зобе (ДТЗ, Базедовой болезни). В редких случаях заболевание возникает при других патологиях ЩЖ, сопровождающихся гипертиреозом:
- Базедова болезнь. Патология имеет аутоиммунную природу, характеризуется постоянной иммунной стимуляцией клеток щитовидной железы. В результате в крови увеличивается количество тиреоидных гормонов, которые становятся причиной повреждения миокарда.:
- Тиреоидит. При воспалении железистой ткани на фоне вирусного подострого тиреоидита или аутоиммунного тиреоидита Хашимото происходит разрушение части клеток органа. В этом случае гипертиреоз длится несколько недель или месяцев, поэтому поражения сердца носят функциональный характер.
- Опухоли. Явления тиреотоксикоза наблюдаются на фоне ТТГ-секретирующих новообразований гипофиза, токсической аденомы щитовидной железы. Крайне редко кардиальные патологии возникают у женщин со струмой яичника, вырабатывающей тиреоидные гормоны.
К независимым факторам риска относят позднюю диагностику эндокринных патологий, низкую приверженность пациентов к лечению, неправильную схему приема тиреостатиков. Симптомы кардиоваскулярных нарушений возможны у людей, которые бесконтрольно принимают синтетические тиреоидные гормоны. Заболевание чаще наблюдается у женщин со склонностью к аутоиммунным нарушениям, отягощенным семейным анамнезом.
При тиреотоксическом сердце наблюдается дистрофия миокарда, которая развивается под влиянием двух основных механизмов. Во-первых, при тиреотоксикозе отмечается персистирующая гиперфункция сердечной мышцы на фоне активации симпатического отдела вегетативной нервной системы. Во-вторых, тироксин и трийодтиронин обладают прямым токсическим воздействием на миокард.
Тиреоидные гормоны оказывают влияние на миокард на уровне ядер, регулируют поток ионов через клеточные мембраны, изменяют активность митохондрий. Молекулярные механизмы токсического воздействия реализуются через фосфолипид-зависимые протеинкиназы, комплекс кальдомодулин-Са, цМАФ-протеинкиназу. Повышение общего сосудистого сопротивления при тиреотоксикозе усиливает тяжесть возникших нарушений.
Патоморфологически определяется мозаичное нарушений структуры кардиомиоцитов, наличие разрушенных и интактных митохондрий в пределах одной клетки. Тиреотоксические влияние обуславливают развитие внутриклеточного отека, увеличение числа гликогеновых включений. При длительном существовании болезни возникают необратимые очаги миокардиофиброза.

Классификация
Согласно рекомендациям ВОЗ, кардиальная дисфункция при тиреотоксикозе определяется как подвид метаболической кардиомиопатии. При отсутствии соответствующего лечения тиреотоксикоза нарушения сердечной деятельности носят неуклонно прогрессирующий характер. В клинической кардиологии выделяют 3 стадии ремоделирования сердца у пациентов с тиреотоксикозом:
- Гиперкинетическая. Наблюдается на первом этапе тиреотоксического поражения, проявляется усилением силы и частоты сердечных сокращений. Для гиперкинетической фазы характерно увеличение фракции выбора до 65% при отсутствии органических изменений в миокарде.
- Нормокинетическая. На втором этапе происходит постепенное увеличение массы миокарда левого желудочка и расширение полостей сердца. Показатели сердечного выброса и другие функциональные параметры находятся в пределах нормы.
- Гипокинетическая. На третьем этапе тиреотоксического сердца сократительная функция резко снижается, развивается хроническая сердечная недостаточность. Нарушения сопровождаются выраженной дилатацией левого желудочка.
Симптомы тиреотоксического сердца
Самым частым проявлением болезни считается ощущение сердцебиения, которое обусловлено постоянной синусовой тахикардией. Человек испытывает чувство тяжести и тупые боли в области сердца, сильную слабость, быструю утомляемость при ходьбе и привычных бытовых действиях. Зачастую возникает одышка, возможно появление головокружений и предобморочных состояний.
При прогрессировании синдрома тиреотоксического сердца возникают сильные боли в левой половине грудной клетки, появляются отеки нижних конечностей, бывают приступы удушья и кашля. Некоторые пациенты испытывают распирание и увеличение живота, боли и тяжесть в правом подреберье. Шейные и периферические вены набухают и хорошо контурируются сквозь кожу.
Кардиальная симптоматика сопровождается типичными проявлениями тиреотоксикоза. Пациенты становятся раздражительными, эмоционально неустойчивыми, испытывают трудности с засыпанием. Расстройства пищеварения представлены частыми поносами и снижением аппетита. Возможно возникновение мелкоразмашистого тремора конечностей, мышечной слабости, нарушений двигательной активности.
Высокая ЧСС в покое, которая наблюдается у всех пациентов с тиреотоксическим сердцем, является предиктором риска фатальных состояний. При постоянной тахикардии в 3 раза возрастает вероятность острых транзиторных ишемических атак, инсультов, летальных желудочковых фибрилляций. У пациентов с сопутствующей артериальной гипертензией и ИБС наблюдается утяжеление течения заболеваний, снижение фармакологического контроля.
Серьезным осложнением заболевания является мерцательная аритмия, которая развивается у 28% больных. До 68% пациентов с длительным стажем тиреотоксического сердца сталкиваются с проявлениями сердечной недостаточности (СН). Вначале развивается СН по правожелудочковому типу, поскольку правые отделы сердца быстрее истощают свой функциональный резерв. При отсутствии медикаментозной коррекции формируется тотальная форма сердечной недостаточности.

При физикальном обследовании пациента у врача-кардиолога определяется усиление сердечных тонов, систолические шумы, акцент второго тона на легочной артерии. Перкуторно обнаруживается расширение границ сердца. Для определения характера и степени тяжести органо-функциональных нарушений применяется комплексная программа обследования, которая включает следующие методы:
- ЭКГ. По результатам электрокардиографии на начальном этапе болезни определяется синусовая тахикардия, повышение амплитуды зубцов. На более поздних стадиях возникают атриовентрикулярные или внутрижелудочковые блокады, удлинение интервала QT, инверсия зубца Т, что отражает процесс ремоделирования миокарда.
- ЭхоКГ. При ультразвуковом исследовании сердца выявляется последовательное повышение и снижение фракции выброса крови, при динамическом наблюдении обнаруживается постепенное расширение полостей желудочков. При проведении ЭхоКГ на гипокинетической стадии определяются признаки миодистрофического кардиосклероза.
- Сцинтиграфия ЩЗ. Радиоизотопное сканирование железы назначается для определения ее функциональной активности. По распределению радиоактивных изотопов удается выявить диффузные изменения или очаговые гормонально активные образования.
- Анализ миокардиальных маркеров. Для исключения острых повреждений миокарда проводится тропониновый тест, определяется содержание креатинфосфокиназы и лактатдегидрогеназы. Целесообразно выполнять анализ острофазовых показателей крови.
- Гормональные исследования. Для подтверждения тиреотоксического характера кардиальной патологии назначаются анализы на гормоны Т3, Т4 (их количество повышено) и гипофизарный ТТГ, уровень которого чаще снижен.
Дифференциальная диагностика
Признаки тиреотоксического сердца необходимо отличать от токсико-аллергических миокардитов, ревматических пороков клапанного аппарата, других вариантов метаболических кардиомиопатий. Дифференциальная диагностика проводится с самостоятельными формами артериальной гипертензии, ишемической болезни сердца, туберкулезной интоксикацией.
Лечение тиреотоксического сердца
Медикаментозная терапия направлена на достижение эутиреоидного состояния и максимально возможное купирование кардиологических симптомов. Основная группа используемых препаратов - антитиреоидные (тиреостатики), которые блокируют синтез гормонов ЩЖ. По мере снижения уровней Т3 и Т4 уменьшаются их негативные влияния на миокард. Комплексное лечение включает следующие группы медикаментов:
- Бета-адреноблокаторы. Большинству пациентов назначаются неселективные блокаторы, которые способствуют ликвидации тахикардии и других видов аритмий. При субклиническом тиреотоксикозе имеет смысл назначение селективных бета-адреноблокаторов, которые имеют длительный период полувыведения.
- Антиаритмические препараты. Наибольшей активностью при тиреотоксической кардиомиопатии обладают ингибиторы реполяризации, которые имеют слабое инотропное свойство. Для усиления эффекта терапию дополняют кардиометаболическими препаратами, витаминно-минеральными комплексами.
- Диуретики. Мочегонные препараты добавляются в схему лечения запущенной формы тиреотоксического сердца, которая сопровождается сердечной недостаточностью. Для поддержки работы органа также могут использоваться сердечные гликозиды в строго контролируемых дозах.
- Антикоагулянты. На фоне аритмий существует повышенный риск тромбообразования, который требует профилактического назначения антиагрегантов и антикоагулянтов. Поскольку при ДТЗ увеличивается плазменный клиренс факторов свертывания, связанных с витамином К, дозы препаратов должны быть меньше стандартных.
Исход заболевания напрямую зависит от успешности лечения причины тиреотоксикоза, комплаенса пациента, своевременности диагностики сердечной патологии. При достижении стойкого эутиреоза удается устранить аритмию и снизить риск кардиоваскулярных кризов. При развитии тотальной сердечной недостаточности прогноз неблагоприятный. Профилактика заключается в предупреждении, ранней диагностике и комплексном лечении патологий щитовидной железы.
2. Особенности сердечно-сосудистых нарушений при тиреотоксикозе/ С.Т. Зубкова// Диабетология. Тиреоидология. Метаболические расстройства. - №20/1. - 2015.
4. Сердечно-сосудистая система при тиреотоксикозе/ Аметов А.С., Коншева М.Ю., Лукъянова И.В.// Consilium medicus. - 2003. - Том 3. - № 11.
Появление III и IV тона сердца при тиреотоксикозе. Гиперфункция миокарда при тиреотоксикозе
Кардиология:
Сердечно-сосудистые проявления тиреотоксикоза
Изменения сократимости миокарда и сердечно-сосудистой гемодинамики происходят при широком спектре тиреоидных заболеваний. Многочисленные исследования, включая эксперименты на животных, а также результаты инвазивных и неинвазивных исследований больных показали, что трийодтиронин регулирует инотронную и хронотропную функции сердца прямым и опосредованным способами.
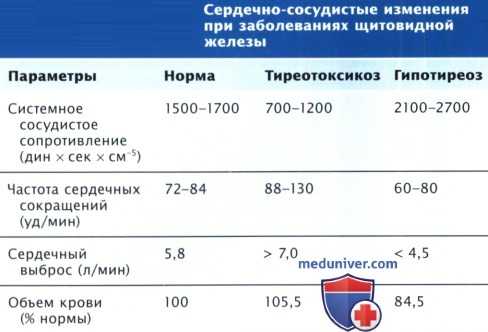
На рисунке ниже представлена интегральная схема действия Т3 на все ткани организма, приводящего к усилению гермогенеза. Прямые эффекты на гладкомышечные клетки снижают системное сосудистое сопротивление в периферических артериолах. Происходят уменьшение среднего АД и активация РААС, а также растет задержка натрия почками. Увеличение объема плазмы крови, связанное с повышением эритропоэтина, приводит к увеличению объема крови и преднагрузки. Такая комбинация низкого системного сосудистого сопротивления (снижение до 50%) в сочетании с увеличением венозного возврата и преднагрузки повышает СВ.
При тиреотоксикозе СВ может увеличиваться в 2 раза, а при гипотиреозе, напротив, снижаться до 30-40%. Недавние исследования с измерением метаболизма ацетата с помощью ПЭТ продемонстрировали, что значимое повышение СВ при тиреотоксикозе не сопровождается эффективным использованием энергии.
Трийодтиронин, по-видимому, уменьшает системное сосудистое сопротивление путем прямого действия на гладкомышечные клетки и за счет изменений в эндотелии сосудов, вероятно включая синтез и секрецию оксида азота. Т3 может оказывать вазодилататорный эффект в течение нескольких часов при введении больным после КШ и у больных ХСН. Податливость стенок артерий при тиреотоксикозе снижается, что может служить объяснением низкого среднего АД и ДАД и повышения пикового САД. Таким образом, повышение СВ и снижение податливости стенок артерий могут быть более выраженными у пациентов старшей возрастной группы с сосудистыми заболеваниями, что приводит к систолической АГ у 30% больных. При гипотиреозе системное сосудистое сопротивление может повышаться до 30%. Среднее АД повышено у 20% пациентов, имеющих значимую диастолическую АГ.
Даже мягкий гипотиреоз может уменьшать выброс эндотелием вазодилататорных факторов. Диастолическая АГ при гипотиреозе часто ассоциирована с низким уровнем ренина и снижением синтеза субстрата ренина в печени. Это обычно приводит к снижению чувствительности к соли, вновь подчеркивая важность увеличения системного сосудистого сопротивления, лежащего в основе диастолической АГ.
а) Сердечно-сосудистая система при тиреотоксикозе. Сердечно-сосудистые симптомы являются важной составной частью тиреотоксикоза и часто доминируют в клинической картине. Сердцебиение из-за увеличения частоты и силы сердечных сокращений беспокоит большинство пациентов и является следствием как усиления симпатической стимуляции, так и снижения парасимпатической стимуляции. Обычно у пациентов ЧСС > 90 уд/мин в покое и во время сна, вариабельность суточного ритма уменьшается, а при физических нагрузках ЧСС увеличивается чрезмерно. У многих пациентов с тиреотоксикозом снижается толерантность к физическим нагрузкам и появляется одышка, частично из-за слабости скелетных и дыхательных мышц. На фоне низкого сосудистого сопротивления и растущей преднагрузки функциональный резерв сердца не может увеличиваться в соответствии с субмаксимальной и максимальной физическими нагрузками.
У пациентов с тиреотоксикозом может возникать боль в сердце, подобная стенокардической. У пожилых пациентов с установленным или возможным поражением коронарных артерий повышение нагрузки сердца ассоциируется с увеличением СВ и сократимости миокарда, что может привести к его ишемии, чувствительной к лечению β-адреноблокаторами, или восстановлению эутиреоза. У небольшого количества больных, обычно молодых женщин, боли в груди могут сопровождаться ишемическими изменениями на ЭКГ. Катетеризация сердца у большинства из этих пациентов коронарной патологии не выявляет, однако может быть обнаружен вазоспазм, аналогичный таковому у пациентов с вариантной стенокардией. ИМ — редкая ситуация, организм пациентов хорошо реагирует на блокаторы кальциевых каналов или нитроглицерин.
б) Фибрилляция предсердий при тиреотоксикозе. Самой распространенной формой нарушения сердечного ритма при тиреотоксикозе является синусовая тахикардия, но наибольшее клиническое значеание имеет ФП. Частота встречаемости ФП и других форм наджелудочковой тахикардии при данном заболевании составляет 2-20%. В сравнении с контрольной группой пациентов с нормальной функцией щитовидной железы, в которой частота ФП составляет 2,3%, при явном тиреотоксикозе этот показатель равен 13,8%. В исследовании, включавшем более 13 тыс. пациентов с тиреотоксикозом, частота ФП была < 2% (возможно, вследствие ранней диагностики и лечения болезни).
При анализе частоты в зависимости от возраста больных выявили ступенчатое увеличение данного вида аритмии в каждой декаде, достигающей пика 15% у лиц старше 70 лет. Последнее исследование подтвердило факт увеличения частоты ФП при тиреотоксикозе с возрастом. В исследовании лиц с ФП явный тиреотоксикоз был ее причиной менее чем у 1% пациентов. Следовательно, аномальные показатели функции щитовидной железы, включая низкий уровень ТТГ в сыворотке, должны быть низкими у лиц с впервые возникшей ФП. Однако возможность восстановления эутиреоза и синусового ритма у больных тиреотоксикозом оправдывает необходимость определения ТТГ у большинства лиц с ФП и наджелудочковыми аритмиями неизвестной этиологии.
Терапия ФП при тиреотоксикозе включает использование β1-адреноблокаторов (селективных или неселективных) для контроля частоты сокращения желудочков. Симптоматическая терапия дает быстрый результат, но восстановление эутиреоза занимает значительно больше времени. Сердечные гликозиды можно использовать для контроля частоты сокращения желудочков при ассоциированной с тиреотоксикозом ФП, но в связи с повышением клиренса дигиталиса и снижением чувствительности к нему из-за высокой активности внутриклеточной Na + /K + -АТФазы и снижения тонуса парасимпатической нервной системы необходимы более высокие дозы. Единого мнения о необходимости антикоагулянтной терапии нет. Должны быть оценены возможность системной или мозговой эмболии, а также риск кровотечения и осложнений данной терапии.
Является ли тиреотоксикоз сам по себе ФР системной эмболии, до конца не установлено. В ретроспективном исследовании главным значимым фактором эмболизации был возраст, а не наличие ФП. Ретроспективный анализ больших групп пациентов не показал превышения риска тромбоэмболии над риском кровотечения вследствие назначения варфарина. У молодых пациентов с тиреотоксикозом и ФП в отсутствие других заболеваний сердца, гипертензии или независимых ФР эмболий польза антикоагулянтов не доказана и должна быть сопоставлена с риском их применения. В качестве альтернативы у молодых больных для снижения частоты эмболий можно достаточно безопасно использовать аспирин.
Успешное лечение тиреотоксикоза с помощью радиоактивного йода или тиреостатиков и восстановление нормальных уровней Т4 и Т3 в сыворотке ассоциировано с восстановлением синусового ритма у 60% пациентов в течение 2-3 мес. У пожилых больных или при длительной ФП частота восстановления синусового ритма ниже, может понадобиться электрическая или лекарственная кардиоверсия, но только после достижения эутиреоза. После кардиоверсии синусовый ритм восстанавливается в 90% случаев и у многих сохраняется в течение 5 и более лет. При использовании после кардиоверсии дизопирамида в дозе 300 мг/сут в течение 3 мес вероятность сохранения синусового ритма выше, чем без такого лечения.
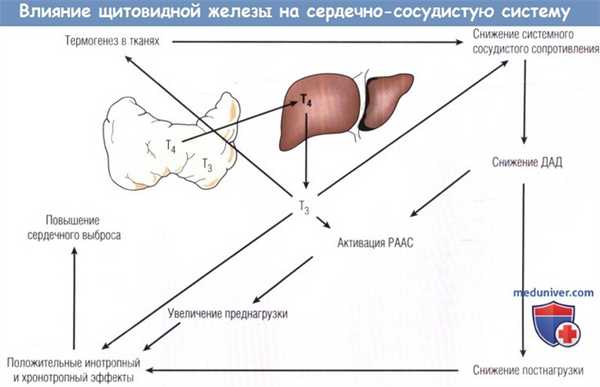
Схема метаболизма тиреоидных гормонов и действия трийодтиронина (Т3) на сердце и системный кровоток.
Т4 — тетрайодтиронин; ДАД — диастолическое артериальное давление; РААС — ренин-ангиотензин-альдостероновая система.
в) Сердечная недостаточность при тиреотоксикозе. Нарушения деятельности сердечно-сосудистой системы при тиреотоксикозе включают увеличение СВ в состоянии покоя и сократимости сердца. У меньшего количества больных с одышкой при нагрузках, ортопноэ, пароксизмальной одышкой во сне, а также у лиц с периферическими отеками, набуханием шейных вен и III тоном сердца отмечается СН. Данный симптомокомплекс в сочетании с неспособностью увеличить ФВ ЛЖ в ответ на нагрузку позволяет предположить развитие тиреотоксической КМП. Часто используемый термин «сердечная недостаточность с высоким выбросом» некорректен, поскольку, хотя СВ в покое превышает норму в 2-3 раза, нарушение толерантности к физическим нагрузкам является в большей степени следствием мышечной слабости, а не СН. Высокий СВ, однако, приводит к повышению реабсорбции натрия почками и объема плазмы крови, что, в свою очередь, вызывает периферические отеки, гидроторакс и венозную гипертензию.
Интересно, что, несмотря на снижение системного сосудистого сопротивления при тиреотоксикозе, легочное сосудистое русло изменяется противоположным образом: в результате повышения выброса крови растет давление в легочном артериальном русле. Все это приводит к увеличению среднего венозного давления, растяжению шейных вен, застою в печени и периферическим отекам в сочетании с легочной гипертензией или правожелудочковой недостаточностью.
У пациентов с длительным тиреотоксикозом и выраженной синусовой тахикардией или ФП возможно снижение СВ, нарушение сократимости миокарда и уменьшение фракции изгнания, появление III тона и застоя в легких, что соответствует клинической картине ХСН. Анализ таких наблюдений позволил прийти к выводу, что нарушение функции ЛЖ происходит вследствие длительной тахикардии с появлением частотно-зависимой СН. При дилатации ЛЖ может развиться митральная регургитация. Распознавание данной ситуации важно, поскольку лечение, направленное на урежение сердечного ритма, улучшает функцию ЛЖ уже до начала тиреостатической терапии. Пациенты в критическом состоянии должны получать лечение в отделениях интенсивной терапии. Некоторые из больных тиреотоксикозом (как и пациенты с ХСН) не переносят β-адреноблокаторы в полных терапевтических дозах, тогда лечение можно начать с низких доз короткодействующих β-адреноблокаторов в сочетании с классическими препаратами для лечения обострения ХСН, включая диуретики.
Увеличение двойного произведения и потребления кислорода вследствие тиреотоксикоза может нарушить функцию сердца у пожилых пациентов с возможной или верифицированной ИБС, гипертензией или поражением клапанного аппарата. Важна быстрая диагностика тиреотоксикоза у данной категории больных, поскольку риск сердечно-сосудистых и церебральных осложнений у них выше и до лечения, и в ходе лечения.
г) Лечение. Лечение больных с тиреотоксическим сердцем должно включать β-адреноблокаторы для снижения ЧСС до уровня 10-15% выше нормы. Это может уменьшить влияние тахикардии на развитие дисфункции желудочков сердца, хотя прямой инотропный эффект тиреоидных гормонов сохранится. Быстрое наступление эффекта и уменьшение многих признаков тиреотоксикоза подтверждают необходимость использования β-адреноблокаторов у большинства больных. Терапия может быть дополнена 131 I или тиреостатиками.
Тиреотоксикоз (гипертиреоз) - симптомы и лечение
Что такое тиреотоксикоз (гипертиреоз)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Курашова О. Н., эндокринолога со стажем в 28 лет.
Над статьей доктора Курашова О. Н. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Тиреотоксикоз (гипертиреоз) — гиперметаболический процесс, вызванный избытком тиреоидных гормонов в организме и их токсическим воздействием на различные органы и ткани. Клинически характеризуется увеличением щитовидной железы и поражением других систем и органов. [3] [5] [11]
Первые описания этой патологии были найдены в работах персидского врача Джурджани, созданных в 1100 году. [5] [11]
Данный синдром встречается как у женщин (до 2%), так и у мужчин (до 0,2%). Чаще он возникает у людей в возрасте 20-45 лет.
Причины тиреотоксикоза
Причин возникновения тиреотоксикоза множество. К основным относятся:
- повышение продукции гормонов щитовидной железой вследствие различных заболеваний (диффузно-токсический, узловой зоб и другие);
- избыточный приём препаратов, содержащих гормоны щитовидной железы (нарушение назначенной схемы лечения гипертиреоза).
Факторы риска
Провоцирующим фактором синдрома является дополнительное количество йода, поступающее в организм при самостоятельном использовании йодных добавок.
Состояние тиреотоксикоза при диффузно-токсическом зобе является аутоиммунным заболеванием. Обычно оно развивается в результате избыточной выработки антител к рецептору тиреотропного гормона (ТТГ), производимого гипофизом.
Возникновение тиреотоксического состояния возможно при возникновении функциональной автономии уже существующего узла щитовидной железы — одно- и многоузлового зоба. Это заболевание развивается достаточно долго, в основном у людей, старше 45 лет. Так, в отсутствие воздействия ТТГ — основного физиологического стимулятора [7] [8] — узлы синтезируют количество тиреогормонов, превышающее потребность организма. [5] [6] [11]
Тиреотоксикоз при беременности
Во время беременности потребность организма женщины в тиреоидных гормонах возрастает на 30-50 %, поэтому изменение работы щитовидной железы происходит уже с первых недель беременности. Вследствие этого у 2 % беременных развивается гестационный гипертиреоз. Беременным рекомендуется вовремя обратиться к лечащему врачу, провести диагностику и подобрать необходимое индивидуальное лечение.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы тиреотоксикоза (гипертиреоза)
При опросе пациентов с подозрением на повышенную функцию щитовидной железы выявляются:
- непредсказуемая возбудимость, эмоциональная неустойчивость, беспричинная плаксивость;
- беспокойство и нарушение концентрации внимания, возникающее при нахождении в обществе;
- ежедневное нарушение сна;
- суетливость при выполнении любой работы;
- слабость во время ходьбы;
- повышенная потливость диффузного характера, не зависящая от физического или эмоционального напряжения, ощущение «жара»;
- периодические сердцебиения;
- дрожь в теле и нарастающая потеря веса (наблюдаются редко).
Эмоциональные расстройства сочетаются с двигательно-волевыми: появляется необходимость в постоянном движении и хореоподобные подёргивания. Причём тремор конечностей и тела - типичный симптом тиреотоксикоза. [2] [3] [5] [11]
Читайте также:
