Причины эпилепсии и пароксизмальных расстройств у детей
Добавил пользователь Алексей Ф. Обновлено: 09.01.2026
К доброкачественным парциальным эпилепсиям детского возраста относятся:
- доброкачественная парциальная эпилепсия с центро-темпоральными спайками (роландическая эпилепсия);
- доброкачественная парциальная эпилепсия с затылочными пароксизмами;
- доброкачественная парциальная эпилепсия с аффективными симптомами (доброкачественная психомоторная эпилепсия). Обсуждается также вопрос о принадлежности к данной группе еще 2 форм:
- атипичная доброкачественная парциальная эпилепсия:
- доброкачественная парциальная эпилепсия с экстремальными соматосенсор-ными вызванными потенциалами.
Доброкачественная парциальная эпилепсия с центро-темпоральными спайками. (Роландическая эпилепсия)
Впервые заболевание описано Gastaut в 1952 г.
Частота. Роландическая эпилепсия встречается относительно часто и составляет 15% среди всех эпилепсий у детей до 15 лет. Частота встречаемости, в сравнении с абсансами, в 4-7 раз выше. Болеют преимущественно лица мужского пола.
Генетические данные. Наследственная отягощенность по эпилепсии прослеживается в 17-59% случаев (Blom et а1, 1972; Blom, Heijbel, 1982).
Клиническая характеристика. Роландическая эпилепсия наиболее часто манифестирует в возрасте 4-10 лет (Blom et а1, 1972). Приступ обычно начинается с односторонних сенсорных ощущений (онемение, покалывание) в орофациоман-дибулярной области. В дальнейшем может отмечаться тоническое напряжение в мышцах лица, реже наблюдаются клонические или тонико-клонические подергивания конечностей. При вовлечении в процесс мышц гортани и глотки отмечаются нарушения речи (нечленораздельные звуки, полная невозможность произнесения звуков). Приступы часто протекают при сохранном сознании, однако, при генерализации пароксизмов возможна потеря сознания (Nayrac, Beaussart, 1958). Одной из важных особенностей роландической эпилепсии является частое возникновение приступов ночью, преимущественно в фазу засыпания, либо- незадолго до пробуждения. Приступы обычно редкие. Они возникают, как правило, с интервалами в недели, месяцы, иногда бывают однократными. Лишь в 20% случаев частота приступов относительно высокая (Lerman, 1985). Интеллект обычно нормальный (Lerman, 1985; Dalla Bernardina et а1, 1992). Снижение интеллекта, изменения поведения наблюдаются лишь в единичных случаях (Beaumanoir et а1, 1974; Lerman, 1985). Нарушения поведения обусловлены не самой болезнью, а являются вторичными и связаны с родительской "гиперопекой" (Lerman, 1985). Тезис об абсолютном отсутствии при роландической эпилепсии патологических изменений со стороны центральной нервной системы дискуссионен (Morikawa et а1, 1979). Lerman (1985) обратил внимание на тот факт, что в 3% случаев при роландической эпилепсии отмечаются гемипарезы. Успеваемость в школе у детей с роландической эпилепсией, как правило, удовлетворительная, и профессиональные навыки даются легко.
Данные лабораторных и функциональных исследований. ЭЭГ является необходимым методом для верификации диагноза. Для роландической эпилепсии характерны наличие нормальной основной активности и спайков острых волн, локализующихся в центро-темпоральных областях. Частота спайков и острых волн во сне увеличивается. В фазу медленного сна возможно формирование билатеральных или независимых друг от друга очагов эпилептической активности (Blom et а1, 1972; Dalla Bernardina et а1, 1992), а в отдельных случаях-возникновение генерализованных вспышек комплексов "спайк-волна" частотой
3-4/сек (Lerman, 1985, 1992). Следует отметить, что в 30% случаев типичные для роландической эпилепсии ЭЭГ-паттерны регистрируются только во сне (Lerman, 1985). Вместе с тем, профиль сна при роландической эпилепсии обычно не изменен (Nayrac, Beaussart, 1958). Обращает на себя внимание тот факт, что "роландические спайки" иногда (1,2-2,4% случаев) отмечаются у здоровых людей (Cavazutti et а1, 1980) и у больных с некоторыми неврологическими заболеваниями (Degen et а1, 1988).
Дифференциальный диагноз следует, прежде всего, проводить с простыми и сложными фокальными приступами, наблюдаемыми при симптоматических парциальных эпилепсиях. При роландической эпилепсии, в сравнении с симптоматическими парциальными, интеллект обычно нормальный, отсутствуют выраженные нарушения поведения, не отмечается патологических изменений при нейрорадиологических исследованиях. На ЭЭГ регистрируются типичные паттерны- нормальная основная активность и спайки центро-темпоральной локализации.
Наиболее сложен дифференциальный диагноз роландической эпилепсии и сложных парциальных пароксизмов, сочетающихся с нарушением сознания (Lerman, 1985). Сложности дифференциальной диагностики связаны с ошибочной интерпретацией нарушений речи при роландической эпилепсии как расстройства сознания, а также с невозможностью адекватной оценки нарушений сознания. возникающих в ночное время. При височных и лобных эпилепсиях на ЭЭГ выявляются фокальные изменения в соответствующих областях, а при роландической эпилепсии-спайки центро-темпоральной локализации.
Лечение. Удовлетворительным эффектом при лечении роландической эпилепсии обладает сультиам (Doose et а1, 1988), Доза препарата определяется клиническими проявлениями заболевания. Необходимо отметить, что "подавлением эпил-птического очага на ЭЭГ не является обязательным, поскольку в пубертате он исчезает самостоятельно. Через 2-3 года при отсутствии приступов рекомендуется кон 1 рольное обследование и решение вопроса об отмене терапии. Прг наличии редких приступов терапия может не назначаться.
Атипичная доброкачественная эпилепсия детского возраста
Впервые предположение о нозологической самостоятельности атипичног доброкачественной эпилепсии детского возраста было высказано Aicardi, Chevru в 1982г. на основании обследования 7 больных. Однако, с нашей точки зрения ввиду небольшого числа наблюдений, вопрос о нозологической самостоятельности данной формы эпилепсии требует дальнейшего уточнения.
Клиническая характеристика. Заболевание манифестирует в раннем детскою возрасте. Примечательно, что у 3 из 7 больных, наблюдавшихся Aicardi, Chevru (1982), заболевание проявлялось ночными генерализованными и односторонним? приступами, сочетавшимися с редкими парциальными пароксизмами. Отмечались также и дневные приступы-абсансы, атонические и миоклонические пароксизмы. Приступы нередко частые, протекают в виде серий, по 30 пароксизме; в день. Однако, несмотря на разнообразие и высокую частоту приступов нервно-психическое развитие соответствует возрасту. В 9 лет приступы спонтан но исчезают.
Данные лабораторных и функциональных исследований. ЭЭГ-исследование в( время медленного сна выявляет продолжительные или почти постоянные комплексы "спайк-волна", а также роландические спайки с локализацией в центро-темпоральных или теменных областях. Кроме того, регистрируются нерегулярные комплексы "спайк-волна" частотой З/сек при пробуждении или генерализо-ванные медленные комплексы "спайк-волна".
Дифференциальный диагноз следует проводить с рядом прогностически серьезных эпилептических синдромов детского возраста-синдромом Леннокса-Гасто, миоклонически-астатической эпилепсией, а также с синдромом ESES. Наиболее частой диагностической ошибкой является рассмотрение атипичной доброкачественной эпилепсии как синдрома Леннокса-Гасто. При проведении дифференциального диагноза необходимо учитывать, что синдром Леннокса-Гасто сочетается с выраженной задержкой нервно-психического развития. Типичными для синдрома Леннокса Гасто являются ночные тонические приступы с характерными ЭЭГ-паттернами в виде генерализованных медленных комплексов "спайк-волна" частотой 2-2,5/сек. Увеличение частоты данных комплексов во время сна при синдроме Леннокса-Гасто является исключением.
Для миоклонически-астатической эпилепсии, в сравнении с атипичной доброкачественной парциальной эпилепсией, характерно снижение интеллекта, отсутствуют парциальные пароксизмы, а также медленные комплексы "спайк-волна" во время сна.
Дифференциальная диагностика атипичной доброкачественной парциальной эпилепсии и синдрома ESES основывается на результатах полисомнографического исследования, обнаруживающего типичные паттерны,
Лечение. Приступы, как правило, исчезают спонтанно. Поскольку при атипичной доброкачественной парциальной эпилепсии снижения интеллекта не наблюдается, комбинированная антиконвульсантная терапия не рекомендуется.
Доброкачественная парциальная эпилепсия детского возраста с затылочными пароксизмами
Доброкачественная парциальная эпилепсия детского возраста с затылочными пароксизмами впервые описана Gastaut в 1950 г.
Генетические данные. Роль генетических факторов в генезе заболевания несомненна. У многих больных прослеживается наследственная отягощенность по эпилепсии и мигрени (Kuzniecky, Rosenblatt, 1987).
Клиническая характеристика. Заболевание манифестирует преимущественно в возрасте 2-8 лет. Вместе с тем, описан и более ранний дебют болезни. Gastaut (1992) отмечал, что заболевание может проявляться в 5-17 лет. Наиболее типичными проявлениями приступов при данной форме эпилепсии являются зрительные нарушения - простые и сложные зрительные галлюцинации, иллюзии, амавроз (Gastaut, 1992). Данные симптомы могут быть изолированными или сочетаться с судорожными пароксизмами и преходящими гемипарезами. Нередко во время приступов отмечаются головная боль, рвота, поворот головы и глаз, в отдельных случаях дизестезия, дисфагия (Kivity, Lerman, 1992). Описаны приступы с длительным нарушением сознания - в течение 12 часов (Kivity, Lerman, 1992). Panayiotopoulos (1989) отметил, что наиболее часто приступы возникают ночью и сопровождаются различной степенью нарушения сознания, рвотой, девиацией глазных яблок.
Данные лабораторных и функциональных исследований. При ЭЭГ-исследовании регистрируются нормальная основная активность, высокоамплитудные (200-300 мВ) односторонние или билатеральные острые волны или комплексы "спайк-волна" с локализацией в затылочных областях. Данные изменения исчезают при открывании глаз. Гипервентиляция и фотостимуляция не оказывают влияния на частоту и характер эпилептических ЭЭГ-паттернов. В 38% случаев при ЭЭГ-исследовании обнаруживаются также генерализованные билатерально синхронные комплексы "спайк-волна" или "полиспайк-волна".
Дифференциальный диагноз следует проводить с простыми и сложными парциальными пароксизмами, синдромом Леннокса-Гасто, базилярной мигренью. Симптоматические парциальные эпилепсии, обусловленные структурными повреждениями затылочной доли, исключаются на основании анамнеза, неврологического статуса и нейрорадиологического исследования, обнаруживающих, как правило, патологические изменения. При симптоматических затылочных эпилепсиях, в сравнении с доброкачественной затылочной, открывание глаз не блокирует эпилептическую активность на ЭЭГ.
Дифференциальная диагностика с синдромом Леннокса-Гасто основывается на наличии тонических приступов и характерных для данного синдрома ЭЭГ-паттернах. При базилярной мигрени на ЭЭГ отсутствует эпилептическая активность. Лечение. Препаратом первой очереди выбора является карбамазепин.
Доброкачественная парциальная эпилепсия с аффективными симптомами. (Доброкачественная психомоторная эпилепсия)
Многие авторы предлагают рассматривать доброкачественную парциальную эпилепсию с аффективными симптомами как самостоятельную нозологическую форму (Plouin et а1, 1980; Dalla Bernardina et al, 1992).
Клиническая характеристика. Заболевание манифестирует в возрасте 2-9 лет. Ведущими симптомами являются приступы страха. Данные пароксизмы возникают, как днем, так и ночью. Отличий клинических проявлений дневных и ночных пароксизмов не отмечено. Наиболее типичными признаками приступов при доброкачественной психомоторной эпилепсии являются пароксизмы страха: больной внезапно пугается, может прижиматься к матери, иногда возникают глотательные и жевательные автоматизмы. Могут также наблюдаться смех, стоны, вегетовисцеральные нарушения (гипергидроз, слюнотечение, боли в животе), в отдельных случаях - остановка речи (Dalla Bernardina et а1, 1992). Следует подчеркнуть, что при данной форме эпилепсии тонические, тонико-клонические, атонические приступы не отмечаются.
Данные лабораторных и функциональных исследований. При ЭЭГ-исследовании регистрируются нормальная основная активность, ритмичные спайки или комплексы "острая-медленная волна" с преимущественной локализацией в лобно-височных или теменно-височных областях (Dalla Bernardina et а1, 1992). Частота эпилептических паттернов увеличивается в фазу медленного сна.
Дифференциальный диагноз следует проводить со сложными парциальными пароксизмами, роландической эпилепсией, ночными кошмарами.
Дифференциальная диагностика доброкачественной парциальной эпилепсии с аффективными симптомами со сложными парциальными пароксизмами основывается на характерных для данного заболевания критериях: дебют в раннем детском возрасте, нормальный интеллект, отсутствие изменений в неврологическом статусе и при нейрорадиологическом исследовании. Достаточно труден в отдельных случаях дифференциальный диагноз с роландической эпилепсией. Как известно, роландическая эпилепсия нередко сопровождается нарушением речи, гортанными звуками, слюнотечением. Подобный симнтомокомплекс отмечается иногда при доброкачественной парциальной эпилепсии с аффективными симптомами. В пользу доброкачественной парциальной эпилепсии с аффективными симптомами свидетельствует выраженная психомоторная симптоматика, всегда присутствующая при данном заболевании.
Ночные кошмары весьма сходны по клиническим проявлениям с приступами, наблюдаемыми при доброкачественной психомоторной эпилепсии. В сравнении с доброкачественной психомоторной эпилепсией ночные кошмары возникают исключительно ночью, характеризуются частыми приступами и отсутствием на ЭЭГ эпилептических паттернов.
Лечение. Удовлетворительным эффектом в лечении доброкачественной психомоторной эпилепсии обладают карбамазепин и фенитоин. Прогноз заболевания благоприятный.
Доброкачественная парциальная эпилепсия с экстремальными (гигантскими) соматосенсорными вызванными потенциалами
Dawson в 1947 г. впервые показал, что при соматосенсорном раздражении у отдельных больных с парциальными пароксизмами и поражением соматосенсорных регионов возникают высокоамплитудные (до 400 мВ) вызванные потенциалы. Данные потенциалы регистрируются на стороне, контралатеральной раздражению. Наиболее высокая амплитуда потенциалов отмечается в парасагиттальных и теменных областях. De Marco в 1971 г. опубликовал результаты уникального наблюдения, когда прикосновение к наружному краю стопы вызывало эпилептические паттерны на ЭЭГ. Позднее De Marco, Tassinari (1981) провели большое исследование, проанализировав 25000 электроэнцефалограмм у 1500 детей. Было установлено, что у 1% детей сенсорные раздражения пяток, кончиков пальцев, плеч, рук или бедер провоцируют гигантские соматосенсорные вызванные потенциалы. Примечательно, что 30% обследованных детей страдали эпилептическими пароксизмами, у 15% эпилептические пароксизмы возникли в более поздние сроки жизни.
Клиническая характеристика. Гигантские соматосенсорные вызванные потенциалы возникают в возрасте 4-6 лет, чаще у мальчиков. Нередко в анамнезе у больных имеются фебрильные судороги. В большинстве случаев приступы отмечаются днем. Наиболее часто пароксизмы проявляются моторными симптомами с версивным компонентом, но возможны и генерализованные тонико-клонические приступы без предшествующих фокальных нарушений. Эпилептические соматосенсорные потенциалы сохраняются даже после эпилептического пароксизма. Приступы относительно редкие, 2-6 раз в год. Интеллект не страдает.
Данные лабораторных и функциональных исследований. В возрасте 2,5-3,5 лет возникают гигантские соматосенсорные вызванные потенциалы, позднее на ЭЭГ регистрируются спонтанно возникающие фокальные эпилептические паттерны, наблюдаемые сначала только во сне, а затем и при бодрствовании. Через год после появления эпилептических паттернов на ЭЭГ возникают и клинически выраженные эпилептические пароксизмы.
Дифференциальный диагноз. Наиболее труден дифференциальный диагноз с роландической эпилепсией. Критериями, свидетельствующими в пользу диагноза "доброкачественная парциальная эпилепсия с гигантскими соматосенсорными вызванными потенциалами" являются: интактность в момент приступа мимической мускулатуры лица, парасагиттальная и теменная локализация ЭЭГ-паттернов, спонтанное исчезновение эпилептических соматосенсорных вызванных потенциалов.
Лечение. Антиконвульсантная терапия малоэффективна. Эпилептические приступы исчезают, как правило, спонтанно
Синдром Ландау Клеффнера
Синдром впервые описан Landau, Kleffner 1957 г. К настоящему времени описано около 200 случаев заболевания (Deonna, 1991).
Генетические данные. Согласно Beaumanoir (1992), наследственная отягощен-пость по эпилепсии наблюдается часто.
Клиническая характеристика. Заболевание манифестирует в возрасте 3- 7 лет (Deonna, 1991). Характерна триада симптомов афазия, эпилептические приступы, нарушения поведения. Ранними симптомами являются прогрессирующее нарушение речевой функции и вербальная агнозия (Pauquier et а1, 1992). Нарушения речи характеризуются появлением речевых персевераций, парафазий, жаргон-афазией. В большинстве случаев предшествующие развитию заболевания нарушения речевой функции отсутствуют (Echnne, 1990; Deonna, 1991). Афазические расстройства могут иметь флюктуирующее течение с кратковременными ремиссиями (Deonna et а1, 1989). В 2/3-3/4 случаев развиваются эпилептические пароксизмы. Приступы, как правило, простые парциальные моторные. Реже отмечаются генерализованные тонико-клонические, гемиклонические или сложные парциальные приступы и абсансы. Крайне редко наблюдаются атонические и тонические пароксизмы. У 1/3 больных эпилептические приступы редкие. Исключительно редко развивается эпилептический статус. Одной из особенностей эпилептических пароксизмов при синдроме Ландау-Клеффнера является их ночной характер. Приступы обычно короткие. Расстройства поведения проявляются агрессивностью, гиперактивностью, аутичностью.
Данные лабораторных и функциональных исследований. При ЭЭГ-исследовании регистрируются нормальная основная активность, фокальные или мультифокальные спайки, острые волны, комплексы "спайк-волна" с преимущественной локализацией в височных, теменно-височных или теменно-затылочных областях. В отдельных случаях при синдроме Ландау- Клеффнера на ЭЭГ обнаруживаются роландические спайки. Типичным ЭЭГ-паттерном при синдроме Ландау-Клеффнера является электрический эпилептический статус в фазу медленного сна (ESES) (Rodriguez, Niedermeyer, 1982).
При нейрорадиологическом исследовании патологические изменения отсутствуют. Спектральная позитронно-эмиссиопная томография выявляет уменьшение перфузии в левой средней лобной извилине и правой медиовисочной области (Mouridson et а1, 1993). При позитронно-эмиссионной томографии обнаруживаются метаболические расстройства в височной области (Maquet et а1, 1990), которые сохраняются и после клинического улучшения. Дифференциальный диагноз следует, в первую очередь, проводить с заболеваниями, сочетающимися с афазией, - опухолями, инфекциями, метаболическими расстройствами.
Лечение . Антиконвульсантная терапия в отношении речевых расстройств практически не эффективна (Marescaux et а1, 1990). Благоприятное действие оказывает АКТГ, однако, его длительное применение невозможно. Существенное внимание в комплексной терапии должно быть уделено логопедическим занятиям с целью коррекции речевых расстройств.
Эпилепсия
Эпилепсия — это состояние, характеризующееся повторными (более двух) эпилептическими приступами, не спровоцированными какими-либо немедленно определяемыми причинами. Эпилептический приступ — клиническое проявление аномального и избыточного разряда нейронов мозга, вызывающего внезапные транзиторные патологические феномены (чувствительные, двигательные, психические, вегетативные симптомы, изменения сознания). Следует помнить, что несколько спровоцированных или обусловленных какими-либо отчетливыми причинами (опухоль мозга, ЧМТ) эпилептических приступов не свидетельствуют о наличии у пациента эпилепсии.
МКБ-10
Общие сведения
Эпилепсия — состояние, характеризующееся повторными (более двух) эпилептическими приступами, не спровоцированными какими-либо немедленно определяемыми причинами. Эпилептический приступ — клиническое проявление аномального и избыточного разряда нейронов мозга, вызывающего внезапные транзиторные патологические феномены (чувствительные, двигательные, психические, вегетативные симптомы, изменения сознания). Следует помнить, что несколько спровоцированных или обусловленных какими-либо отчетливыми причинами (опухоль мозга, ЧМТ) эпилептических приступов не свидетельствуют о наличии у пациента эпилепсии.
Классификация
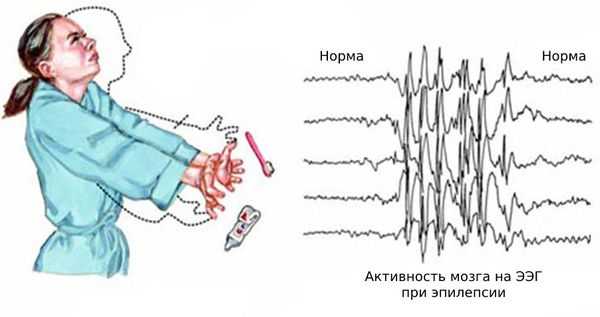
Согласно международной классификации эпилептических приступов выделяют парциальные (локальные, фокальные) формы и генерализированную эпилепсию. Приступы фокальной эпилепсии подразделяют на: простые (без нарушений сознания) — с моторными, соматосенсорными, вегетативными и психическими симптомами и сложные — сопровождаются нарушением сознания. Первично-генерализованные приступы происходят с вовлечением в патологический процесс обоих полушарий мозга. Типы генерализированных приступов: миоклонические, клонические, абсансы, атипичные абсансы, тонические, тонико-клонические, атонические.
Существуют неклассифицированные эпилептические приступы — не подходящие ни под один из вышеописанных видов приступов, а также некоторые неонатальные приступы (жевательные движения, ритмичные движения глаз). Выделяют также повторные эпилептические приступы (провоцируемые, циклические, случайные) и длительные приступы (эпилептический статус).
Симптомы эпилепсии
В клинической картине эпилепсии выделяют три периода: иктальный (период приступа), постиктальный (постприступный) и интериктальный (межприступный). В постиктальном периоде возможно полное отсутствие неврологической симптоматики (кроме симптомов заболевания, обусловливающего эпилепсию — черепно-мозговая травма, геморрагический или ишемический инсульт и др.).
Выделяют несколько основных видов ауры, предваряющей сложный парциальный приступ эпилепсии — вегетативную, моторную, психическую, речевую и сенсорную. К наиболее частым симптомам эпилепсии относятся: тошнота, слабость, головокружение, ощущение сдавления в области горла, чувство онемения языка и губ, боли в груди, сонливость, звон и/или шум в ушах, обонятельные пароксизмы, ощущение комка в горле и др. Кроме того, сложные парциальные приступы в большинстве случаев сопровождаются автоматизированными движениями, кажущимися неадекватными. В таких случаях контакт с пациентом затруднен либо невозможен.
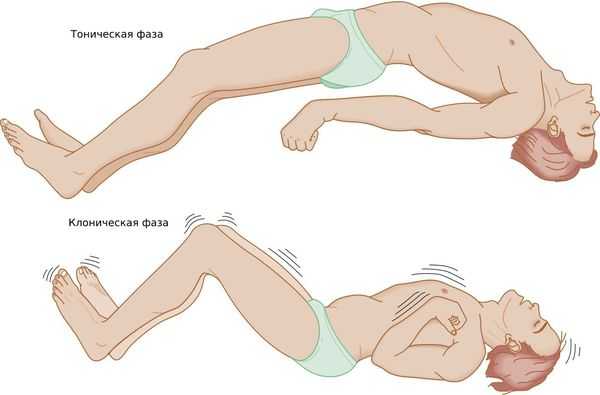
Вторично-генерализированный приступ начинается, как правило, внезапно. После нескольких секунд, которые длится аура (у каждого пациента течение ауры уникально), пациент теряет сознание и падает. Падение сопровождается своеобразным криком, который обусловлен спазмом голосовой щели и судорожным сокращением мышц грудной клетки.
Далее наступает тоническая фаза приступа эпилепсии, названная так по типу судорог. Тонические судороги — туловище и конечности вытягиваются в состоянии сильнейшего напряжения, голова запрокидывается и/или поворачивается в сторону, контралатеральную очагу поражения, дыхание задерживается, набухают вены на шее, лицо становится бледным с медленно нарастающим цианозом, челюсти плотно сжаты. Продолжительность тонической фазы приступа — от 15 до 20 секунд.
Затем наступает клоническая фаза приступа эпилепсии, сопровождающаяся клоническими судорогами (шумное, хриплое дыхание, пена изо рта). Клоническая фаза продолжается от 2 до 3 минут. Частота судорог постепенно снижается, после чего наступает полное мышечное расслабление, когда пациент не реагирует на раздражители, зрачки расширены, реакция их на свет отсутствует, защитные и сухожильные рефлексы не вызываются.
Наиболее распространенные типы первично-генерализированных приступов, отличающихся вовлечением в патологический процесс обоих полушарий мозга — тонико-клонические приступы и абсансы. Последние чаще наблюдаются у детей и характеризуются внезапной кратковременной (до 10 секунд) остановкой деятельности ребенка (игры, разговор), ребенок замирает, не реагирует на оклик, а через несколько секунд продолжает прерванную деятельность. Пациенты не осознают и не помнят припадков. Частота абсансов может достигать нескольких десятков в сутки.
Диагностика
Диагностирование эпилепсии должно основываться на данных анамнеза, физикальном обследовании пациента, данных ЭЭГ и нейровизуализации (МРТ и КТ головного мозга). Необходимо определить наличие или отсутствие эпилептических приступов по данным анамнеза, клинического осмотра пациента, результатам лабораторных и инструментальных исследований, а также дифференцировать эпилептические и иные приступы; определить тип эпилептических приступов и форму эпилепсии; ознакомить пациента с рекомендациями по режиму, оценить необходимость медикаментозной терапии, ее характер и вероятность хирургического лечения. Несмотря на то, что диагностика эпилепсии основывается, прежде всего, на клинических данных, следует помнить, что при отсутствии клинических признаков эпилепсии данный диагноз не может быть поставлен даже при наличии выявленной на ЭЭГ эпилептиформной активности.
Диагностикой эпилепсии занимаются неврологи и эпилептологи. Основным методом обследования пациентов с диагнозом «эпилепсия» является ЭЭГ, которая не имеет противопоказаний. ЭЭГ проводят всем без исключения пациентам в целях выявления эпилептической активности. Чаще других наблюдаются такие варианты эпилептической активности, как острые волны, спайки (пики), комплексы «пик — медленная волна», «острая волна — медленная волна». Современные методы компьютерного анализа ЭЭГ позволяют определить локализацию источника патологической биоэлектрической активности. При проведении ЭЭГ во время приступа эпилептическая активность регистрируется в большинстве случаев, в интериктальном периоде ЭЭГ нормальная у 50% пациентов.
На ЭЭГ в сочетании с функциональными пробами (фотостимуляция, гипервентиляция) изменения выявляют в большинстве случаев. Необходимо подчеркнуть, что отсутствие эпилептической активности на ЭЭГ (с применением функциональных проб или без них) не исключает наличие эпилепсии. В таких случаях проводят повторное обследование либо видеомониторинг проведенной ЭЭГ.
В диагностике эпилепсии наибольшую ценность среди нейровизуализационных методов исследования представляет МРТ головного мозга, проведение которой показано всем пациентам с локальным началом эпилептического припадка. МРТ позволяет выявить заболевания, повлиявшие на провоцированный характер приступов (аневризма, опухоль) либо этиологические факторы эпилепсии (мезиальный темпоральный склероз). Пациентам с диагнозом «фармакорезистетная эпилепсия» в связи с последующим направлением на хирургическое лечение также проводят МРТ для определения локализации поражения ЦНС. В ряде случаев (пациенты преклонного возраста) необходимо проведение дополнительных исследований: биохимический анализ крови, осмотр глазного дна, ЭКГ.
Приступы эпилепсии необходимо дифференцировать с другими пароксизмальными состояниями неэпилептической природы (обмороки, психогенные приступы, вегетативные кризы).
Лечение эпилепсии
Консервативная терапия
Все методы лечения эпилепсии направлены на прекращение приступов, улучшение качества жизни и прекращение приема лекарственных средств (на стадии ремиссии). В 70% случаев адекватное и своевременное лечение приводит к прекращению приступов эпилепсии. Прежде чем назначать противоэпилептические препараты необходимо провести детальное клиническое обследование, проанализировать результаты МРТ и ЭЭГ. Пациент и его семья должны быть проинформированы не только о правилах приема препаратов, но и о возможных побочных эффектах. Показаниями к госпитализации являются: впервые в жизни развившийся эпилептический приступ, эпилептический статус и необходимость хирургического лечения эпилепсии.
Одним из принципов медикаментозного лечения эпилепсии является монотерапия. Препарат назначают в минимальной дозе с последующим ее увеличением до прекращения приступов. В случае недостаточности дозы необходимо проверить регулярность приема препарата и выяснить, достигнута ли максимально переносимая доза. Применение большинства противоэпилептических препаратов требует постоянного мониторинга их концентрации в крови. Лечение прегабалином, леветирацетамом, вальпроевой кислотой начинают с клинически эффективной дозы, при назначении ламотриджина, топирамата, карбамазепина необходимо проводить медленное титрование дозы.
При назначении того или иного противоэпилептического препарата следует стремиться к минимально возможной частоте его приема (до 2 раз/сутки). За счет стабильной концентрации в плазме препараты пролонгированного действия более эффективны. Доза препарата, назначенная пожилому пациенту, создает более высокую концентрацию в крови, чем аналогичная доза препарата, назначенная пациенту молодого возраста, поэтому необходимо начинать лечение с малых доз с последующим их титрованием. Отмену препарата проводят постепенно, учитывая форму эпилепсии, ее прогноз и возможность возобновления приступов.
Хирургическое лечение
Фармакорезистентные эпилепсии (продолжающиеся приступы, неэффективность адекватного противоэпилептического лечения) требуют дополнительного обследования пациента для решения вопроса о оперативном лечении. Предоперационное обследование должно включать в себя видео-ЭЭГ регистрацию приступов, получение достоверных данных о локализации, анатомических особенностях и характере распространения эпилептогенной зоны (МРТ).
На основе результатов вышеперечисленных исследований определяется характер оперативного вмешательства: хирургическое удаление эпилептогенной ткани мозга (кортикальная топэтомия, лобэктомия, гемисферэктомия, мультилобэктомия); селективная операция (амигдало-гиппокампэктомия при височной эпилепсии); каллозотомия и функциональное стереотаксическое вмешательство; вагус-стимуляция.
Существуют строгие показания к каждому из вышеперечисленных хирургических вмешательств. Их проведение возможно только в специализированных нейрохирургических клиниках, располагающих соответствующей техникой, и при участии высококвалифицированных специалистов (нейрохирурги, нейрорадиологи, нейропсихологии, нейрофизиологи и др.).
Прогноз и профилактика
Прогноз на трудоспособность при эпилепсии зависит от частоты приступов. На стадии ремиссии, когда приступы возникают все реже и в ночное время, трудоспособность пациента сохраняется (в условиях исключения работы в ночную смену и командировок). Дневные приступы эпилепсии, сопровождающиеся потерей сознания, ограничивают трудоспособность пациента.
Эпилепсия оказывает влияние на все стороны жизни пациента, поэтому является значимой медико-социальной проблемой. Одна из граней этой проблемы — скудость знаний об эпилепсии и связанная с этим стигматизация пациентов, суждения которых о частоте и выраженности психических нарушений, сопровождающих эпилепсию, зачастую необоснованны. Подавляющее большинство пациентов, получающих правильное лечение, ведут обычный образ жизни без приступов.
Профилактика эпилепсии предусматривает возможное предотвращение ЧМТ, интоксикаций и инфекционных заболеваний, предупреждение возможных браков между больными эпилепсией, адекватное снижение температуры у детей с целью предотвращения лихорадки, последствием которой может стать эпилепсия.
Эпилепсия у детей
Эпилепсия у детей - это хроническое церебральное расстройство, характеризующееся повторяющимися, стереотипными припадками, возникающими без явных провоцирующих факторов. Ведущими проявлениями эпилепсии у детей служат эпилептические припадки, которые могут протекать в виде тонико-клонических судорог, абсансов, миоклонических судорог с нарушением сознания или без его нарушения. Инструментальная и лабораторная диагностика эпилепсии у детей включает проведение ЭЭГ, рентгенографии черепа, КТ, МРТ и ПЭТ головного мозга, биохимического анализа крови и спинномозговой жидкости. Общие принципы лечения эпилепсии у детей предполагают соблюдение охранительного режима, терапию антиконвульсантами, психотерапию; при необходимости - нейрохирургическое лечение.
Эпилепсия у детей - хроническая патология головного мозга, протекающая с периодически повторяющимися неспровоцированными судорогами или их вегетативными, психическими, сенсорными эквивалентами, обусловленными гиперсинхронной электрической активностью нейронов мозга. Согласно имеющейся в педиатрии статистике, эпилепсия встречается у 1-5% детей. У 75% взрослых, страдающих эпилепсией, дебют заболевания приходится на детский или подростковый возраст.
У детей, наряду с доброкачественными формами эпилепсии, встречаются злокачественные (прогрессирующие и резистентные к проводимой терапии) формы. Нередко эпилептические припадки у детей протекают атипично, стерто, а клиническая картина не всегда соответствует изменениям на электроэнцефалограмме. Изучением эпилепсии у детей занимается детская неврология и ее специализированный раздел - эпилептология.
Причины
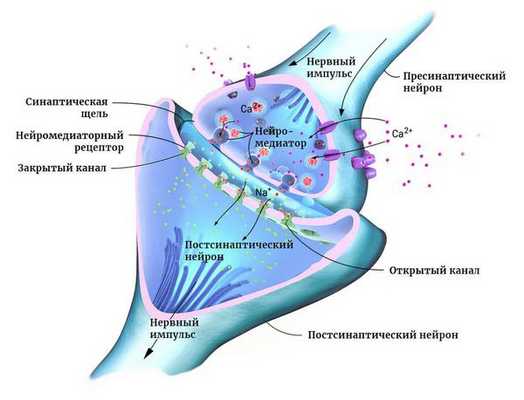
Фактором эпилептогенеза в детском возрасте выступает незрелость мозга, характеризующаяся преобладанием процессов возбуждения, необходимых для формирования функциональных межнейронных связей. Кроме этого, эпилептизации нейронов способствуют преморбидные органические поражения мозга (генетические или приобретенные), вызывающие повышенную судорожную готовность. В этиологии и патогенезе эпилепсии у детей немалую роль играют наследственная или приобретенная предрасположенность к заболеванию.
- Наследственный фактор. Развитие идиопатических форм эпилепсии у детей в большинстве случаев связано с генетически обусловленной нестабильностью мембран нейронов и нарушением нейромедиаторного баланса. При наличии идиопатической эпилепсии у одного из родителей, риск развития эпилепсии у ребенка составляет около 10%. Эпилепсия у детей может быть ассоциирована с наследственными дефектами обмена веществ (фенилкетонурией, лейцинозом, гиперглицинемией, митохондриальными энцефаломиопатиями), хромосомными синдромами (болезнью Дауна), наследственными нейрокожными синдромами (нейрофиброматозом, туберозным склерозом) и др.
- Пренатальное поражения головного мозга. Среди пренатальных факторов ведущую роль играют токсикозы беременности, гипоксия плода, внутриутробные инфекции, фетальный алкогольный синдром (ФАС), внутричерепные родовые травмы, тяжелая желтуха новорожденных.
- Раннее органическое поражение мозга. Может быть связано с врожденными аномалиями мозга, перенесенными ребенком нейроинфекциями (менингитами, энцефалитами, арахноидитами), ЧМТ; осложнениями общих инфекционных заболеваний (гриппа, пневмонии, сепсиса и др.), поствакцинальными осложнениями и пр. У детей с ДЦП эпилепсия выявляется в 20-33% случаев.
Криптогенные формы эпилепсии у детей имеют предположительно симптоматическое происхождение, однако их достоверные причины так и остаются невыясненными даже при использовании современных методов нейровизуализации.
В зависимости от характера эпилептических припадков, выделяют:
1. Фокальную эпилепсию у детей, протекающую с фокальными (локальными, парциальными) приступами:
- простыми (с двигательными, вегетативными, соматосенсорными, психическими компонентами)
- сложными (с нарушением сознания)
- с вторичной генерализацией (переходящими в генерализованные тонико-клонические приступы)
2. Генерализованную эпилепсию у детей, протекающую с первично-генерализованными приступами:
- абсансами (типичными, атипичными)
- клоническими припадками
- тонико-клоническими припадками
- миоклоническими припадками
- атоническими припадками
3. Эпилепсию у детей, протекающую с неклассифицируемыми припадками (повторными, случайными, рефлекторными, эпилептический статус и пр.).
Локализационно-обусловленные и генерализованные формы эпилепсии у детей с учетом этиологии подразделяются на идиопатические, симптоматические и криптогенные. Среди идиопатических фокальных форм заболевания у детей чаще всего встречается доброкачественная роландическая эпилепсия, эпилепсия с затылочными пароксизмами, эпилепсия чтения; среди генерализованных идиопатических форм - доброкачественные судороги новорожденных, миоклоническая и абсансная эпилепсия детского и юношеского возраста и др.
Симптомы эпилепсии у детей
Клинические проявления эпилепсии у детей многообразны, зависят от формы заболевания и типов приступов. В этой связи остановимся лишь на некоторых эпилептических припадках, встречающихся в детском возрасте.
В продромальном периоде эпилептического припадка обычно отмечаются предвестники, включающие аффективные нарушения (раздражительность, головную боль, страх) и ауру (соматосенсорную, слуховую, зрительную, вкусовую, обонятельную, психическую).
При «большом» (генерализованном) припадке ребенок, страдающий эпилепсией, внезапно теряет сознание и падает со стоном или криком. Тоническая фаза приступа длится несколько секунд и сопровождается напряжением мускулатуры: запрокидыванием головы, сжиманием челюстей, апноэ, цианозом лица, расширением зрачков, сгибанием рук в локтях, вытяжением ног. Затем тоническая фаза сменяется клоническими судорогами, которые длятся 1-2 минуты. В клоническую фазу приступа отмечается шумное дыхание, выделение пены изо рта, нередко - прикусывание языка, непроизвольное мочеиспускание и дефекация. После стихания судорог дети обычно не реагируют на окружающие раздражители, засыпают и приходят в себя в состоянии амнезии.
«Малые» припадки (абсансы) у детей, страдающих эпилепсией, характеризуются кратковременным (на 4-20 секунд) выключением сознания: замиранием взгляда, остановкой движений и речи с последующим продолжением прерванной деятельности и амнезией. При сложных абсансах могут иметь место моторные феномены (миоклонические подергивания, закатывание глазных яблок, сокращения мышц лица), вазомоторные нарушения (покраснение или побледнение лица, саливация, потливость), двигательные автоматизмы. Приступы абсансов повторяются ежедневно и с большой частотой.
Простые фокальные припадки при эпилепсии у детей могут сопровождаться подергиваниями отдельных мышечных групп; необычными ощущениями (слуховыми, зрительными, вкусовыми, соматосенсорными); приступами головных и абдоминальных болей, тошнотой, тахикардией, потливостью, повышением температуры; психическими нарушениями.
Осложнения
Длительное течение эпилепсии приводит к изменению нервно-психического статуса детей: у многих из них наблюдается синдром гиперактивности и дефицита внимания, трудности в обучении, нарушения поведения. Некоторые формы эпилепсии у детей протекают со снижением интеллекта.
Современный подход к диагностике эпилепсии у детей основывается на тщательном изучении анамнеза, оценке неврологического статуса, проведении инструментальных и лабораторные исследований. Детскому неврологу или эпилептологу необходимо знать частоту, продолжительность, время возникновения приступов, наличие и характер ауры, особенности течения припадка, постприступного и межприступного периодов. Особое внимание обращается на наличие перинатальной патологии, раннего органического поражения мозга у детей, эпилепсии у родственников. Инструментальная диагностика:
- Электроэнцефалография. Проводится с целью определения участка повышенной возбудимости в головном мозге и формы эпилепсии. Типичным для эпилепсии у детей служит наличие ЭЭГ-знаков: пиков, острых волн, комплексов «пик-волна», пароксизмальных ритмов. Поскольку эпилептические феномены не всегда обнаруживаются в покое, нередко возникает необходимость записи ЭЭГ с функциональными пробами (световой стимуляцией, гипервентиляцией, депривацией сна, фармакологическими пробами и т. д.) ночного ЭЭГ-мониторинга или длительного ЭЭГ-видеомониторинга, увеличивающих вероятность выявления патологических изменений.
- Методы нейровизуализации. Для определения морфологического субстрата эпилепсии у детей проводится рентгенография черепа, КТ, МРТ, ПЭТ головного мозга.
- ЭФИ сердца. С целью исключения пароксизмов кардиогенного происхождения выполняется электрокардиография и суточное мониторирование ЭКГ ребенку.
- Лабораторная диагностика. Для выяснения этиологического характера эпилепсии у детей может потребоваться исследование биохимических и иммунологических маркеров крови, проведение люмбальной пункции с исследованием цереброспинальной жидкости, определение хромосомного кариотипа.
Эпилепсию необходимо дифференцировать с судорожным синдромом у детей, спазмофилией, фебрильными судорогами и другими эпилептиформными приступами.
Лечение эпилепсии у детей
Первая помощь при эпилептическом приступе
Родители детей, страдающих эпилепсией, должны уметь оказать ребенку неотложную помощь при эпилептическом припадке. При возникновении предвестников приступа следует уложить ребенка на спину, освободив от тесной одежды и обеспечив свободный доступ воздуха. Во избежание западания языка и аспирации слюны голову ребенка необходимо повернуть набок. С целью купирования длительных судорог возможно ректальное введение диазепама (в виде суппозиториев, раствора).
При организации режима ребенка, больного эпилепсией, следует избегать перегрузок, волнений, в отдельных случаях - длительной инсоляции, просмотра телевизора или работы за компьютером.
Детям, страдающим эпилепсией, необходима длительная (иногда пожизненная) терапия индивидуально подобранными противосудорожными препаратами. Антиконвульсанты назначаются в режиме монотерапии с постепенным наращиванием дозы до достижения контроля над приступами. Традиционно для лечения эпилепсии у детей используются различные производные вальпроевой кислоты, карбамазепин, фенобарбитал, бензодиазепины (диазепам), а также антиконвульсанты нового поколения (ламотриджин, топирамат, окскарбазепин, леветирацетам и др.). При неэффективности монотерапии по назначению врача подбирается дополнительный противоэпилептический препарат.
Из немедикаментозных методов лечения эпилепсии у детей может применяться психотерапия, БОС-терапия. Положительно зарекомендовали себя при эпилепсии у детей, резистентной к противосудорожным препаратам, такие альтернативные методы, как гормональная терапия (АКТГ), кетогенная диета, иммунотерапия.
Нейрохирургическое лечение
Нейрохирургические методы лечения эпилепсии у детей пока не нашли широкого применения. Тем не менее, имеются сведения об успешном хирургическом лечении резистентных к терапии форм эпилепсии у детей посредством гемисферэктомии, передней темпоральной лобэктомии, экстратемпоральной неокортикальной резекции, ограниченной темпоральной резекции, стимуляции блуждающего нерва с помощью имплантируемых устройств. Отбор пациентов для оперативного лечения проводится коллегиально с участием нейрохирургов, детских неврологов, психологов с тщательной оценкой возможных рисков и предполагаемой эффективности вмешательства.
Прогноз
Успехи современной фармакотерапии эпилепсии позволяют добиться полного контроля над приступами у большинства детей. При регулярном приеме противоэпилептических препаратов дети и подростки с эпилепсией могут вести обычный образ жизни. При достижении полной ремиссии (отсутствии приступов и нормализации ЭЭГ) через 3-4 года врач может постепенно полностью отменить прием антиэпилептических препаратов. После отмены у 60% пациентов приступы в дальнейшем не возобновляются.
Менее благоприятный прогноз имеет эпилепсия у детей, характеризующаяся ранним дебютом приступов, эпилептическими статусами, снижением интеллекта, отсутствием эффекта от приема базовых лекарственных препаратов.
Профилактика
Профилактика эпилепсии у детей должна начинаться еще во время планирования беременности и продолжаться после рождения ребенка. В случае развития заболевания необходимо раннее начало лечения, соблюдении схемы терапии и рекомендованного образа жизни, наблюдение ребенка у эпилептолога. Педагоги, работающие с детьми, страдающими эпилепсией, должны быть информированы о заболевании ребенка и о мерах оказания первой помощи при эпилептических приступах.
Судорожный синдром у детей
Судорожный синдром у детей - неспецифическая реакция организма ребенка на внешние и внутренние раздражители, характеризующаяся внезапными приступами непроизвольных мышечных сокращений. Судорожный синдром у детей протекает с развитием парциальных или генерализованных судорог клонического и тонического характера с потерей или без потери сознания. Для установления причин судорожного синдрома у детей необходимы консультации педиатра, невролога, травматолога; проведение ЭЭГ, НСГ, РЭГ, рентгенографии черепа, КТ головного мозга и пр. Купирование судорожного синдрома у детей требует введения антиконвульсантов и проведения терапии основного заболевания.
Судорожный синдром у детей - частое ургентное состояние детского возраста, протекающее с развитием судорожных пароксизмов. Судорожный синдром встречается с частотой 17-20 случаев на 1000 детей: при этом 2/3 судорожных припадков у детей приходится на первые 3 года жизни. У детей дошкольного возраста судорожный синдром встречается в 5 раз чаще, чем в целом в популяции. Высокая распространенность судорожного синдрома в детском возрасте объясняется незрелостью нервной системы детей, склонностью к развитию общемозговых реакций и многообразием вызывающих судороги причин. Судорожный синдром у детей не может рассматриваться как основной диагноз, поскольку сопровождает течение большого круга заболеваний в педиатрии, детской неврологии, травматологии, эндокринологии.

Судорожный синдром у детей является полиэтиологическим клиническим синдромом. Неонатальные судороги, развивающиеся у новорожденных, обычно связаны с:
- тяжелым гипоксическим поражением ЦНС (гипоксией плода, асфиксией новорожденных);
- внутричерепной родовой травмой;
- внутриутробной или постнатальной инфекцией (цитомегалией, токсоплазмозом, краснухой, герпесом, врожденным сифилисом, листериозом и др.);
- врожденными аномалиями развития мозга (голопрозэнцефалией, гидроанэнцефалией, лиссэнцефалией, гидроцефалией и др.);
- алкогольным синдромом плода. Судороги могут являться проявлением синдрома абстиненции у детей, рожденных от матерей, страдающих алкогольной и наркотической зависимостью;
- редко у новорожденных возникают столбнячные судороги, обусловленные инфицированием пупочной ранки.
Среди метаболических нарушений, являющихся причиной судорожного синдрома, следует выделить следующие:
- электролитный дисбаланс (гипокальциемию, гипомагниемию, гипо- и гипернатриемию), встречающийся у недоношенных, детей с внутриутробной гипотрофией, галактоземией, фенилкетонурией.
- гипербилирубинемию и связанная с ней ядерная желтуха новорожденных.
- эндокринные нарушения - гипогликемию при сахарном диабете, гипокальциемию при спазмофилии и гипопаратиреозе.
В грудном и раннем детском возрасте в генезе судорожного синдрома у детей ведущую роль играют:
- нейроинфекции (энцефалиты, менингиты);
- инфекционные заболевания (ОРВИ, грипп, пневмония, отит, сепсис);
- ЧМТ;
- поствакцинальные осложнения;
- эпилепсия.
Менее частыми причинами судорожного синдрома у детей выступают опухоли мозга, абсцесс мозга, врожденные пороки сердца, отравления и интоксикации, наследственные дегенеративные заболевания ЦНС, факоматозы.
Определенная роль в возникновении судорожного синдрома у детей принадлежит генетической предрасположенности, а именно - наследованию особенностей метаболизма и нейродинамики, определяющих пониженный судорожный порог. Провоцировать судорожные припадки у ребенка могут инфекции, дегидратация, стрессовые ситуации, резкое возбуждение, перегревание и др.
По происхождению различают эпилептический и неэпилептический (симптоматический, вторичный) судорожный синдром у детей. К числу симптоматических относятся фебрильные (инфекционные), гипоксические, метаболические, структурные (при органических поражениях ЦНС) судороги. Следует отметить, что в некоторых случаях неэпилептические судороги могут перейти в эпилептические (например, при длительном, более 30 минут некупируемом судорожном припадке, повторных судорогах).
В зависимости от клинических проявлений различают парциальные (локализованные, фокальные) судороги, охватывающие отдельные группы мышц, и генерализованные судороги (общий судорожный припадок). С учетом характера мышечных сокращений судороги могут быть клоническими и тоническими: в первом случае эпизоды сокращения и расслабления скелетных мышц быстро сменяют друг друга; во втором имеет место длительный спазм без периодов расслабления. В большинстве случаев судорожный синдром у детей протекает с генерализованными тонико-клоническими судорогами.
Симптомы
Типичному генерализованному тонико-клоническому припадку свойственно внезапное начало. Внезапно ребенок теряет контакт с внешней средой; его взгляд становится блуждающим, движения глазных яблок - плавающими, затем взор фиксируется вверх и в сторону.
В тоническую фазу судорожного приступа голова ребенка запрокидывается назад, челюсти смыкаются, ноги выпрямляются, руки сгибаются в локтевых суставах, все тело напрягается. Отмечается кратковременное апноэ, брадикардия, бледность и цианотичность кожных покровов. Клоническая фаза генерализованного судорожного припадка характеризуется восстановлением дыхания, отдельными подергиваниями мимической и скелетной мускулатуры, восстановлением сознания. Если судорожные пароксизмы следуют один за другим без восстановления сознания, такое состояние расценивают как судорожный статус.
Наиболее частой клинической формой судорожного синдрома у детей служат фебрильные судороги. Они типичны для детей в возрасте от 6 месяцев до 3-5 лет и развиваются на фоне подъема температуры тела выше 38 °С. Признаки токсико-инфекционного поражения головного мозга и его оболочек при этом отсутствуют. Длительность фебрильных судорог у детей обычно составляет 1-2 минуты (иногда до 5 минут). Течение данного варианта судорожного синдрома у детей благоприятное; стойких неврологических нарушений, как правило, не развивается.
Судорожный синдром у детей с внутричерепной травмой протекает с выбуханием родничков, срыгиваниями, рвотой, расстройствами дыхания, цианозом. Судороги при этом могут носить характер ритмичных сокращений определенных групп мышц лица или конечностей либо генерализованный тонический характер. При нейроинфекциях в структуре судорожного синдрома у детей обычно доминируют тонико-клонические судороги, отмечается ригидности затылочных мышц. Тетания, обусловленная гипокальциемией, характеризуется судорогами в мышцах-сгибателях («рука акушера»), лицевой мускулатуре («сардоническая улыбка»), пилороспазмом с тошнотой и рвотой, ларингоспазмом. При гипогликемии развитию судорог предшествует слабость, потливость, дрожь в конечностях, головная боль.
Для судорожного синдрома при эпилепсии у детей типична предваряющая приступ «аура» (ощущение озноба, жара, головокружения, запахов, звуков и пр.). Собственно эпилептический приступ начинается с крика ребенка, следующей за этим потерей сознания и судорогами. По окончании приступа наступает сон; после пробуждения ребенок заторможен, не помнит произошедшее.
В большинстве случаев установление этиологии судорожного синдрома у детей только на основании клинических признаков невозможно.
В силу многофакторности происхождения судорожного синдрома у детей, его диагностикой и лечением могут заниматься детские специалисты различного профиля: неонатологи, педиатры, детские неврологи, детские травматологи, детские офтальмологи, детские эндокринологи, реаниматологи, токсикологи и др.
Решающим моментом в правильной оценке причин судорожного синдрома у детей является тщательный сбор анамнеза: выяснение наследственной отягощенности и перинатального анамнеза, предшествующих приступу заболеваний, травм, профилактических прививок и пр. При этом важно уточнить характер судорожного припадка, обстоятельства его возникновения, продолжительность, повторяемость, выход из судорог.
Важное значение в диагностике судорожного синдрома у детей имеют инструментальные и лабораторные исследования. Проведение ЭЭГ помогает оценить изменения биоэлектрической активности и выявить судорожную готовность мозга. Реоэнцефалография позволяет судить о характере кровотока и кровоснабжения головного мозга. При рентгенографии черепа у ребенка может выявляться преждевременное закрытие швов и родничков, расхождение черепных швов, наличие пальцевых вдавлений, увеличение размеров черепа, изменения контуров турецкого седла, очаги обызвествления и другие признаки, косвенно свидетельствующие о причине судорожного синдрома.
Уточнить этиологию судорожного синдрома у детей в ряде случаев помогают нейросонография, диафаноскопия, КТ головного мозга, ангиография, офтальмоскопия, проведение люмбальной пункции. При развитии судорожного синдрома у детей необходимо выполнить биохимическое исследование крови и мочи на содержание кальция, натрия, фосфора, калия, глюкозы, пиридоксина, аминокислот.
Лечение судорожного синдрома у детей
При возникновении судорожного приступа ребенка необходимо уложить на твердую поверхность, повернуть голову набок, расстегнуть воротник, обеспечить приток свежего воздуха. Если судорожный синдром у ребенка развился впервые и его причины неясны, необходимо вызывать скорую помощь.
Для свободного дыхания следует удалить из полости рта слизь, остатки пищи или рвотных масс с помощью электроотсоса или механическим путем, наладить ингаляции кислорода. Если причина судорог установлена, то с целью их купирования проводится патогенетическая терапия (введение раствор кальция глюконата при гипокальциемии, раствора магния сульфата - при гипомагниемии, раствора глюкозы - при гипогликемии, антипиретиков - при фебрильных судорогах и т. д.).
Однако, поскольку в ургентной клинической ситуации не всегда удается осуществить диагностический поиск, для купирования судорожного пароксизма проводится симптоматическая терапия. В качестве средств первой помощи используют внутримышечное или внутривенное введение сульфата магния, диазепама, ГОМК, гексобарбитала. Некоторые противосудорожные препараты (диазепам, гексобарбитал и др.) могут вводиться детям ректально. Кроме противосудорожных препаратов, для профилактики отека головного мозга детям назначается дегидратационная терапия (маннитол, фуросемид).
Дети с судорожным синдромом неясного генеза, судорогами, возникшим на фоне инфекционных и метаболических заболеваний, травм головного мозга, подлежат обязательной госпитализации.
Фебрильные судороги обычно прекращаются с возрастом. Для предупреждения их повторного возникновения не следует допускать выраженной гипертермии при возникновении у ребенка инфекционного заболевания. Риск трансформации фебрильных судорог в эпилептические составляет 2-10%.
В остальных случаях профилактика судорожного синдрома у детей включает предупреждение перинатальной патологии плода, терапию основного заболевания, наблюдение у детских специалистов. Если судорожный синдром у детей не исчезает после прекращения основной болезни, можно предположить, что у ребенка развилась эпилепсия.
Читайте также:
- Профилактика острого среднего отита. Острый мастоидит
- Морфология аспергилломы легких. Грибковые кисты легкого
- Выделительная функция печени и пищеварительного тракта. Выделительная функция желудка. Выделительная функция кишечника.
- Этапы и техника операции при разрыве ахиллова сухожилия
- Спинно-мозжечковые проводящие пути: нейроны, схема, функции
