Проблемы и модификации перфузии стекловидного тела при эндофтальмите
Добавил пользователь Дмитрий К. Обновлено: 21.01.2026
Эндофтальмит - это абсцедирующее воспаление внутренних структур глаза, приводящее к скоплению гнойного экссудата в стекловидном теле. При эндофтальмите отмечаются боли в глазном яблоке, отек и покраснение век и конъюнктивы, значительное понижение остроты зрения, гипопион. В диагностике эндофтальмита используется визометрия, исследование полей зрения, биомикроскопия глаза, диафаноскопия, офтальмоскопия, электроретинография, УЗИ глаза. Комплексное лечение эндофтальмита включает антибиотикотерапию, дезинтоксикационную, противовоспалительную, рассасывающую терапию; интравитреальные, парабульбарные или субконъюнктивальные инъекции, парацентез и промывание передней камеры; при тяжелом течении эндофтальмита - витрэктомию.
МКБ-10
Общие сведения
Гнойные воспаления тканей глазного яблока относятся к числу грозных состояний в офтальмологии, требующих оказания специализированной неотложной помощи. Гнойный процесс при эндофтальмите прогрессирует стремительно, иногда в течение нескольких часов приводя к развитию панофтальмита - тотального воспаления и расплавления всех оболочек глазного яблока и тканей орбиты. По различным данным, частота слепоты, функциональной и анатомической гибели глаза, приводящей к энуклеации, у пациентов с внутриглазной инфекцией достигает 28 - 89%. Данные обстоятельства ставят перед офтальмологами задачу своевременной профилактики, раннего выявления и адекватного лечения инфекций глазного яблока.
Причины эндофтальмита
Экзогенные причины
Экзогенные случаи инфицирования внутриглазных тканей преимущественно связаны со следующими факторами:
- проникающими ранениями глаз (95-97 %),
- операциями на глазном яблоке (2-4%),
- прободными гнойными язвами роговицы,
- инфицированными ожогами глаз.
В структуре механических повреждений глаз, сопровождающихся развитием эндофтальмита, преобладает детский травматизм (40 %), производственные (30%) и сельскохозяйственные (25-50%) травмы. Проникновение в глаз инородного тела значительно повышает риски возникновения эндофтальмита. Послеоперационный эндофтальмит чаще развивается вследствие экстракции катаракты с имплантацией заднекамерной ИОЛ.
При экзогенном инфицировании глаза выделяют первичную и вторичную микробную инвазию. В первом случае микробы попадают в глубокие структуры глаза в момент проникающего ранения или инвазивного вмешательства, а воспалительная реакция развивается уже в первые 2-3 суток. При вторичной микробной инвазии инфицирование развивается в поздние сроки вследствие неадекватной первичной обработки раны, ее зияния, размозжения краев и т. п.
Эндогенные причины
Эндогенный механизм развития эндофтальмита встречается в 1-2 % случаев и связан с гематогенным заносом микробных возбудителей в капилляры радужки и ресничного тела из отдаленных воспалительных очагов в организме при:
- фурункулах, абсцессах, флегмонах,
- синуситах, тонзиллите,
- пневмонии,
- остеомиелите,
- сепсисе,
- менингите,
- септическом эндокардите и др.
Возбудители экзогенного и эндогенного эндофтальмита многообразны. Наиболее часто при бактериологическом исследовании выявляются стафилококки, стрептококки, коринебактерии, протей, гемофильная палочка, синегнойная палочка, нейссерии, энтеробактерии, клебсиелла, пневмококки и различные полимикробные ассоциации. Опасную разновидность представляет грибковый эндофтальмит, который может вызываться более чем двадцатью разновидностями грибков (рода акремониум, кандида, аспергилл, цефалоспориум, нейроспора и др.).
Патогенез
Патогенез эндофтальмита при экзогенном инфицировании многоплановый. В случае нарушения целостности роговицы или склеры микроорганизмы проникают внутрь стекловидного тела, где беспрепятственно размножаются. Образуется внутриглазной очаг инфекции, который быстро распространяется на все оболочки глаза. В свою очередь, нарушение иммунологической изолированности глаза сопровождается аутоиммунной воспалительной реакцией, способствующей ослаблению сопротивляемости инфекции, и агрессивному течению эндофтальмита и панофтальмита.
Образующийся гнойный экссудат приводит к увеиту, расплавлению сосудистой и сетчатой оболочек, инкапсуляции с образованием шварт. Швартообразование в последующем вызывает тракции и отслойку сетчатки с исходом в гипотензию и атрофию глазного яблока.
Симптомы эндофтальмита
Эндофтальмит может протекать по типу отграниченного очага в глазу (абсцесса стекловидного тела) либо диффузного процесса; иногда встречается смешанная форма. По степени тяжести симптоматики выделяют легкую, среднюю и тяжелую степени эндофтальмита.
Экзогенный эндофтальмит развивается на 2-3 сутки после механического повреждения глаза. Прогрессирующее течение заболевания сопровождается болью в глазном яблоке, нарастающим снижением остроты зрения иногда до светоощущения, плавающими помутнениями в поле зрения. Внешние изменения глаза характеризуются умеренным отеком век и конъюнктивы, резкой смешанной инъекцией глазного яблока. Могут развиваться признаки иридоциклита. Характерной чертой эндофтальмита является формирование абсцесса в стекловидном теле, который просвечивает через зрачок желтоватым свечением.
Осложнения
При эндофтальмите тяжелой степени развивается выраженный хемоз, гипопион и гноетечение. Эндогенные эндофтальмиты, протекающие на фоне иммунодефицита или интоксикации, могут носить двусторонний характер. Прогрессирование эндофтальмита приводит к переходу в панофтальмит, что угрожает анатомической и функциональной гибелью глаза, риском развития менингита.
Диагностика
Комплексное офтальмологическое обследование при эндофтальмите позволяет оценить тяжесть процесса и выработать лечебную тактику. При подозрении на эндофтальмит проводится:
- Визометрия. Типичная офтальмологическая картина при эндоофтальмите характеризуется снижением остроты зрения: при легкой степени - частичным, при средней - выраженным, при тяжелой - значительным снижением или отсутствием зрения.
- Исследование полей зрения. Поле зрения сужено или отсутствует.
- Биомикроскопия. Проведение биомикроскопии выявляет смешанную инъекцию глазного яблока, наличие преципитатов на поверхности роговицы, гипопиона, гиперемию и инфильтрацию радужки, образование задних синехий
- Диафаноскопия глаза. Диафаноскопия глаза в проходящем свете позволяет обнаружить желтовато-серый зрачковый рефлекс, свидетельствующий об образовании абсцесса в стекловидном теле. При обратном развитии эндофтальмита ввиду формирования на месте гнойника соединительной ткани рефлекс приобретает молочно-белый оттенок.
- Офтальмоскопия. Проведение прямой и обратной офтальмоскопии при эндофтальмите затруднено и частично возможно только при легкой степени тяжести заболевания.
- Измерение ВГД. Внутриглазное давление при эндофтальмите обычно снижено.
- УЗИ глаза. Выявляет ограниченные или тотальные помутнения в стекловидном теле. Для верификации возбудителя проводится посев культуры из стекловидного тела и водянистой влаги.
- Элекрофизиологические исследования. Показатели электроретинографии могут соответствовать или быть близкими к норме (при очаговом эндофтальмите), значительно снижаться вплоть до исчезновения (при диффузном или смешанном эндофтальмите).
Последствия эндофтальмита у детей необходимо дифференцировать от злокачественной опухоли сетчатки - ретинобластомы.
Лечение эндофтальмита
Лечение эндофтальмита проводится в условиях отделения хирургической офтальмологии. Сразу же после установления диагноза назначается:
- Системная терапия: ударные дозы антибиотиков широкого спектра действия, сульфаниламиды, антимикотические средства, противовоспалительные препараты (НПВП, кортикостероиды), мощная дезинтоксикационная терапия, общеукрепляющая терапия (витаминотерапия, аутогемотерапия), рассасывающая терапия (ферменты).
- Внутриглазные инъекции. Для достижения максимальной концентрации антибактериальных препаратов внутри глаза проводится их внутривенное, внутримышечное, субконъюнктивальное, ретробульбарное, парабульбарное, супрахориоидальное, интравитреальное введение. Одновременно назначаются инстилляции противомикробных глазных капель и аппликации мазей.
- Пункция стекловидного тела. При витреите или гипопионе производится лечебно-диагностическая пункция стекловидного тела с забором экссудата для бактериального посева и введением антибиотика в стекловидное тело. При эндофтальмите возможно проведение внутриартериальной офтальмоперфузии лекарственных препаратов через надглазничную артерию. Для лечения эндофтальмита используются цефалоспорины, гликопептиды, пенициллины, аминогликозиды, фторхинолоны, макролиды и др.
При неэффективности интенсивной консервативной терапии эндофтальмита возникает необходимость хирургического удаления части стекловидного тела - витрэктомии. В послеоперационном периоде антибиотикотерапия должна быть продолжена.
Прогноз и профилактика
Своевременное комплексное лечение эндофтальмита, начатое в легкой стадии, позволяет сохранить зрительные функции. В более поздних стадиях зачастую удается сохранить глаз как анатомический орган, но спасти зрение практически невозможно. Исходом эндофтальмита чаще всего является субатрофия и атрофия глазного яблока. При прогрессировании эндофтальмита в панофтальмит приходится прибегать к энуклеации глазного яблока.
Профилактика экзогенного инфекционного эндофтальмита требует предупреждения травм глаза, проведения адекватной ПХО раны при проникающих ранениях, своевременного удаления инородных тел конъюнктивы и роговицы, грамотного проведения операций на структурах глаза. Для исключения развития эндогенного эндофтальмита необходима санация фокальных гнойных очагов и лечение общих септических состояний.
Деструкция стекловидного тела
Деструкция стекловидного тела - патология органа зрения, сопровождающаяся нарушением физико-химических свойств коллоидного геля стекловидного тела. Клинически заболевание проявляется «мушками» и другими «плавающими помутнениями» перед глазами. При прогрессировании возможно снижение остроты зрения. Диагностика основывается на результатах офтальмоскопии, биомикроскопии, УЗИ в режиме В-сканирования, оптической когерентной томографии, тонометрии и визометрии. Специфические методы лечения не разработаны. На ранних стадиях проводится консервативная терапия. Выраженная деструкция является показанием к оперативному вмешательству (витреолизису, витрэктомии).
Деструкцией стекловидного тела называют полное или частичное разрушение структуры данного анатомического образования. Патология наиболее распространена среди лиц пожилого возраста. У молодых людей обычно возникает в результате механического повреждения глаза или прогрессирования миопии. Представители мужского и женского пола болеют одинаково часто. Деструкция стекловидного тела статистически чаще встречается у жителей экономически развитых стран, что может быть обусловлено увеличением продолжительности жизни, чрезмерной нагрузкой на глаза в процессе профессиональной деятельности и рядом других факторов. Современные методы микрохирургии глаза позволяют не только устранить клинические проявления заболевания, но и отчасти восстановить зрительные функции.
Причины
Деструкция стекловидного тела происходит при изменении физико-химических характеристик его коллоидного геля в результате местного воспаления глаза и окружающих тканей (при эндофтальмите, кератите, блефарите, дакриоцистите). Состав коллоидов зависит от функционального состояния печени, почек и эндокринных желез. При дисфункции перечисленных органов нарушается физиологическое соотношение жидкости, протеогликанов, гликозаминогликанов и компонентов стромы. Расстройства метаболизма, патологические изменения сосудов сетчатки и головного мозга ухудшают кровообращение и провоцируют нейроциркуляторный спазм мышц глаз, предшествующий развитию деструктивных процессов. В преклонном возрасте реологические свойства коллоидного геля в центральных отделах ухудшаются, на периферии коллоид уплотняется. Под действием силы тяжести отложенные кристаллы или коллагеновые массы в области сетчатки отслаиваются и накапливаются в центре стекловидного тела.
Триггером данной патологии выступает миопия, при которой округлая форма глазного яблока сменяется эллипсоидной, что приводит к деформации внутриглазных структур. Заболевание может провоцироваться ударом в область глазницы. Механическая травма приводит к утрате целостности гелеобразной массы, нарушению первичной структуры коллагена и развитию гемофтальма на фоне повреждения сосудистого русла. В группу риска входят пациенты с декомпенсированным сахарным диабетом, астенопией и болезнью Паркинсона. Ятрогенная деструкция возможна при повреждении стекловидного тела во время оперативного вмешательства по поводу катаракты.
Патогенез и классификация
Различают полную и частичную деструкцию стекловидного тела. Чаще всего деструктивные процессы затрагивают центральные отделы коллоидного геля. Первым этапом является образование полости, содержащей жидкость и коагулированные массы коллагена. В последующем все больше фибриллярных белков поддается коагуляции и выходит за пределы образования, что приводит к разжижению студнеобразного вещества, заполняющего пространство между хрусталиком и сетчаткой. В нем образуются пленки и тяжи различной природы, которые могут фиксироваться к глазному дну, становясь причиной сморщивания и образования спаек. Стекловидное тело уменьшается в объеме и деформируется, что провоцирует натяжение витреоретинальных соединений с последующим отслоением сетчатки.
По форме выделяют нитевидную, зернистую и кристаллическую деструкцию. Триггером нитевидной формы выступает атеросклероз или прогрессирующая миопия. При развитии воспалительных процессов во внутреннем ретинальном слое формируются зернистые очаги поражения стекловидного тела. В редких случаях коллоидный гель повреждается отложенными кристаллами холестерина и тирозина.
Симптомы и диагностика
Пациенты отмечают фотопсии, гемофтальм, «пелену» перед глазами и снижение остроты зрения. Специфическим симптомом деструкции являются «мушки», которые чаще всего появляются при взгляде на небо или белый монитор. Попытка сфокусироваться на «мушках» приводит к их перемещению или исчезновению. Обычно патология развивается постепенно. Внезапное возникновение черных точек перед глазами является ранним симптомом отслоения сетчатки или стекловидного тела.
Для подтверждения деструкции стекловидного тела необходимо провести офтальмоскопию, УЗИ глазного яблока, биомикроскопию, оптическую когерентную томографию, визометрию и тонометрию. Методом офтальмоскопии определяются оптически пустые полости, которые зачастую имеют вид вертикальных щелей. Пограничная мембрана без специфических изменений, за ней визуализируются волокнистые структуры серого или белого цвета. Полная деструкция характеризуется образованием единой полости с обрывками фибрилл. Возможно разрушение пограничной мембраны, при котором наблюдается отсутствие ретролентального пространства. При локализации помутнения у края сетчатки специфические изменения не выявляются.
Используя щелевую лампу, при проведении биомикроскопии можно обнаружить изменение консистенции коллоидного геля и наличие хлопьеобразных помутнений. При нитчатой деструкции коллагеновые волокна приобретают петлеобразную структуру. Зернистая деструкция проявляется скоплением частиц небольшого размера серого или коричневого цвета. На поздних этапах болезни визуализируются скопления зерен в виде конгломератов.
Ультразвуковое исследование является более информативным методом. Методика рекомендована при сопутствующих кровоизлияниях в стекловидное тело, УЗИ следует проводить в режиме В-сканирования. Процедура позволяет выявить источник кровоизлияния и эхонегативные сигналы от кристаллических структур внутри коллоида. О разжижении стекловидного тела свидетельствует обнаружение подвижности кристаллов, зернистых конгломератов или скоплений коллагеновых волокон.
Оптическая когерентная томография (ОКТ) глаз выполняется при неинформативности других диагностических методик. При проведении исследования обнаруживается уменьшение размера и изменение формы стекловидного тела, его помутнение и неоднородность структуры. Противопоказанием к оптической когерентной томографии является массивный гемофтальм. Визометрия позволяет оценить степень снижения остроты зрения. Методом тонометрии определяется незначительное повышение внутриглазного давления.
Лечение
Специфические методы лечения деструкции стекловидного тела не разработаны. Тактика офтальмолога зависит от степени поражения коллоидного геля и снижения остроты зрения. При незначительном нарушении функций глаза и выявлении частичной деструкции рекомендована консервативная терапия и коррекция образа жизни. Пациентам следует нормализовать режим сна и бодрствования, выполнять гимнастику для глаз при работе за компьютером или продолжительном чтении. Консервативная терапия заключается в местном назначении йодистого калия для обеспечения рассасывающего эффекта и антиоксидантов для улучшения микроциркуляции глаз (метилэтилпиридинол). Перорально рекомендуется принимать винпоцетин и циннаризин, способствующие улучшению мозгового кровообращения. Показан прием ангиопротекторов и корректоров микроциркуляции (L-Лизина эсцинат).
Хирургическое лечение требуется при выраженной деструкции стекловидного тела. В современной офтальмологии для прицельного измельчения крупных фрагментов коллагена применяют витреолизис. Операцию проводят под местным обезболиванием. Перед использованием специального YAG-лазера зрачки расширяют при помощи мидриатиков короткого действия (тропикамид). Нарушений зрительной функции после витреолизиса коллагеновых структур стекловидного тела не наблюдается. Ход оперативного вмешательства затрудняется при высокой подвижности патологических скоплений внутри коллоидного геля.
Тотальная деструкция является показанием к проведению витрэктомии под местной или общей анестезией. В процессе хирургического вмешательства выполняют удаление стекловидного тела с использованием микрохирургической техники. На первом этапе коллоидный гель разделяют на небольшие участки, которые в дальнейшем подвергают аспирации. Внутриглазное давление нормализируют путем введения сбалансированного солевого раствора, силиконового масла или газа в полость глазного яблока.
Для профилактики деструкции стекловидного тела необходимо регулярно проходить осмотр офтальмолога с обязательным проведением офтальмоскопии, визометрии и тонометрии. Рекомендовано снизить зрительную нагрузку, выполнять лечебную гимнастику для глаз, употреблять витаминизированную пищу, исключить из рациона продукты питания с высоким содержанием животного жира. Всем пациентам с миопией следует своевременно осуществлять мероприятия по коррекции зрения. При диабетической ретинопатии консультация офтальмолога показана 2 раза в год.
Прогноз при деструкции стекловидного тела в случае своевременной диагностики и лечения благоприятный для жизни и работоспособности. Даже на поздних стадиях болезни при помощи витрэктомии можно значительно улучшить остроту зрения и качество жизни пациента.
Отслойка стекловидного тела
Отслойка стекловидного тела - это патологическое состояние, при котором нарушается взаимодействие между стекловидным телом и сетчаткой. Возникает в результате дегенеративных изменений в стекловидном теле, при наличии миопии высокой степени, воспалительных процессов или после травмы глаза. Выделяют полную или частичную отслойку. Клинически проявляется возникновением фотопсий, вспышек, молний при движении глазными яблоками. Для диагностики применяют офтальмометрию, визометрию, тонометрию, биомикроскопию, УЗИ глаза, измерение ПЗО. Лечение только хирургическое, заключается в проведении витрэктомии или энзимного витреолизиса.
Отслойка стекловидного тела - это заболевание стекловидного тела, при котором в результате дегенеративных изменений происходит прогрессирующее ослабление базальной витреоретинальной адгезии. Стекловидное тело расположено в непосредственной близости от сетчатой оболочки глаза, что определяет важность и актуальность данной патологии. При отслойке стекловидного тела, в зависимости от силы витреомакулярной тракции, может произойти повреждение макулярной области, что является грозным осложнением, сопровождается потерей зрения, снижением трудоспособности и инвалидизацией. Патология возникает в возрасте старше 50 лет, чаще диагностируется у женщин, чем у мужчин. Взаимосвязи с расовой принадлежностью или страной проживания не отмечается.
Этиология
К этиологическим факторам развития отслойки стекловидного тела в офтальмологии относят пожилой возраст и наличие миопии высокой степени - после 50 лет начинают происходить дегенеративные изменения в структурах глаза, значительно снижаются витреоретинальная адгезия и количество коллагена в стекловидном теле. В качестве предрасполагающего фактора также рассматривают частые воспалительные заболевания сетчатой и сосудистой оболочек глаза. При данных патологиях рН изменяется в кислую сторону, происходят нарушения в клеточных структурах стекловидного тела, снижается уровень адгезии между внутренней пограничной мембраной и задней гиалоидной мембраной.
Вероятность развития отслойки стекловидного тела повышается при некоторых общих заболеваниях, в том числе - сахарном диабете, синдроме Марфана, патологии щитовидной железы. В результате гормональных расстройств, связанных с данными заболеваниями, в организме нарушается синтез гиалуроновой кислоты и гликозаминогликанов, в итоге меняется структура стекловидного тела, происходит отслойка. Кроме того, к числу обстоятельств, повышающих риск возникновения отслойки стекловидного тела, относят проникающие ранения и оперативное лечение глазного яблока.
Основной причиной развития отслойки стекловидного тела является нарушение взаимодействия задней гиалоидной мембраны (ЗГМ) стекловидного тела и внутренней пограничной мембраны (ВПМ) сетчатки глаза. Гиалоидная мембрана стекловидного тела состоит из коллагеновых волокон, гиалоцитов, особого белка фибронектина и ламинина (являются основой межклеточного матрикса). Она образует наружный слой стекловидного тела, который прилежит к сетчатке глаза. Внутренняя мембрана сетчатки содержит коллагеновые волокна, гиалуроновую кислоту, плазматическую мембрану клеток Мюллера сетчатой оболочки. Толщина пограничной мембраны сетчатой оболочки различна. Наименьшая толщина и более прочное соединение со стекловидным телом отмечаются вокруг сосудов сетчатой оболочки, диска зрительного нерва и макулярной области. На остальном протяжении выявляется утолщение мембраны и менее крепкое соединение.
В зависимости от проникновения витреальных фибрилл в слои ретины с одной стороны, наличием фибронектина и ламинина - с другой определяется сила контакта между стекловидным телом и сетчаткой глаза. С возрастом (чаще после 50 лет) происходит утолщение пограничной мембраны сетчатой оболочки, что снижает способность мюллеровских клеток вырабатывать межклеточное вещество и поддерживать его нормальный уровень. Это приводит к ослаблению витреоретинальной связи с последующим отслоением пограничной мембраны от гиалоидной, в результате развивается отслойка стекловидного тела.
Классификация
В зависимости от характера отслойки выделяют полное и частичное отделение стекловидного тела. При полной отслойке происходит отслойка стекловидного тела от ДЗН с формированием перипапиллярного пространства. Данный вид отслойки чаще встречается в молодом возрасте, когда гель стекловидного тела имеет более оформленную структуру, а отделяемая глиальная мембрана прозрачна. Кроме того, этот вид отслойки возникает при отделении стекловидного тела от ДЗН в результате проникновения воспалительного экссудата из хориоретинального очага (возможно - при заднем увеите) или наличия кровоизлияния между стекловидным телом и сетчатой оболочкой глаза.
Частичная отслойка стекловидного тела может развиваться в результате воспалительных заболеваний сетчатой оболочки глаза (хориоидиты, ретиниты), кровоизлияний в сетчатке, тромбозов или проникающих ранений глаза. Отделение происходит от основания стекловидного тела, позади хрусталика либо от места выхода ДЗН (при сохранении контакта на остальном протяжении). Патологическую отслойку стекловидного тела определяют в случаях соприкосновения стекловидного тела с сетчаткой только на периферии глазного дна. Причинами могут быть осложнения после оперативного удаления хрусталика, воспалительные заболевания сетчатки (хориоретинит) либо проникающие травмы глаза.
Клинические проявления зависят от вида отслойки стекловидного тела. При полной отслойке пациент предъявляет врачу-офтальмологу жалобы на фотопсии, вспышки, молнии при движении глазными яблоками. В поле зрения могут возникать различные плавающие включения от «мушек» до крупных геометрических фигур. При частичной отслойке жалоб может не быть, иногда патология стекловидного тела становится случайной находкой. Поражение двустороннее, острота зрения не снижается. Из осложнений выделяют развитие регматогенной отслойки сетчатки или макулярного отверстия, которые происходят в результате патологической тракции стекловидного тела на область макулы. У пациентов с диабетической ретинопатией возможна полная отслойка сетчатой оболочки глаза.
Для диагностики используют стандартные методы обследования: определение остроты зрения, офтальмометрию, рефрактометрию, тонометрию, офтальмоскопию, биомикроскопию. Из дополнительных методик применяют определение переднезадней оси глаза (риск развития отслойки стекловидного тела увеличивается при ПЗО более 24 мм). Используют УЗИ глазного яблока (позволяет визуализировать структурные изменения в стекловидном теле, выявить наличие тракций или отслоек в сетчатой оболочке) и оптическую компьютерную томографию (дает возможность детально изучить состояние сетчатой оболочки, измерить толщину ЗГМ и ВПМ).
Лечение и профилактика
Лечение только хирургическое, проводится при наличии осложнений. Без клинических проявлений и жалоб пациента отслойка стекловидного тела не требует проведения специальных мероприятий. Развитие осложнений, таких как отслойка сетчатки, является показанием к оперативному вмешательству. Используют различные варианты витрэктомии с удалением задней гиалоидной мембраны. Кроме того, может применяться энзимный витреолизис - введение специального лекарственного вещества в стекловидное тело для изменения химических и физических свойств его молекул и ослабления витреоретинальной адгезии. Прогноз благоприятный только при своевременном обращении.
Профилактические мероприятия направлены на снижение риска развития осложнений. Необходимо адекватное лечение сопутствующих заболеваний, таких как сахарный диабет или патология щитовидной железы. Соблюдение диеты, отказ от алкоголя и курения благоприятно сказываются на прогнозе данной патологии. В список профилактических мероприятий также включают рациональный режим труда и отдыха для глаз, соблюдение техники безопасности для предупреждения травм органа зрения. При появлении симптомов отслойки стекловидного тела необходимо как можно скорее обратиться к офтальмологу для детального обследования.
Как лечить помутнение стекловидного тела глаза?
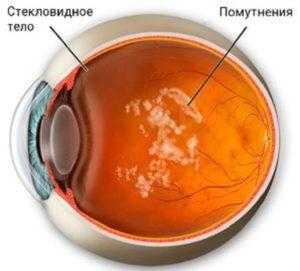
Часто в офтальмологической практике врачи сталкиваются с жалобами на появление перед глазами «плавающих мушек».
Возникновение данного дефекта зрения связано с дистрофическими процессами в стекловидном теле и его разрушением, которые можно выявить как у пациентов старшей возрастной группы, так и в более молодом возрасте.
Что такое стекловидное тело глаза?
Стекловидным телом называется структура глаза, расположенная между сетчаткой и хрусталиком.
К сведению! Оно обеспечивает сохранение правильной формы глазного яблока и тургор тканей, компенсирует колебания внутриглазного давления и участвует в преломлении световых лучей, идущих к сетчатке.
Стекловидное тело является самым большим структурным образованием органа зрения и занимает около 80% объема глазного яблока.
Оно состоит из воды, волокон коллагена и гиалуроновой кислоты и в норме является прозрачным.
Что такое помутнение стекловидного тела?
Нарушение прозрачности стекловидного вещества представляет собой утолщение некоторых волокон или разжижение отдельных его участков, приводящих к нарушению преломления световых лучей.
В результате потери прозрачности отдельных его участков, появляются плавающие в поле видимости пятна коричневого или серого цвета, возникающие из-за отбрасывания дополнительных теней на сетчатую оболочку глаза.
Пятна могут быть как единичными, так и множественными, и зависят от степени выраженности патологического процесса.
Имейте в виду! Лучше всего помутнения стекловидного тела глаза заметны при обращении взгляда на светлые яркие поверхности.
Деструктивные процессы могут проявляться в виде возникновения в поле зрения множества мелких точек, которые передвигаются одновременно с движением глазных яблок.
Такое явление называют золотым либо серебряным дождем.
И связывают его с нарушением обмена тирозина, холестерина и микроэлементов, приводящего к образованию в стекловидном теле кристаллов разного размера.
Чаще всего такая форма заболевания наблюдается в пожилом возрасте, а так же у лиц, страдающих сахарным диабетом и повышенным содержанием холестерина в крови.
Причины развития патологии
Нарушение нормальной структуры стекловидного тела, приводящее к возникновению помутнений, может быть связано с рядом физиологических процессов, проходящих в организме.
Стоит отметить! Так же с различными патология может быть вызвана следующими болезненными состояниями:
- возрастные изменения, встречающиеся у людей старше 40-45 лет;
- большая степень миопии;
- хронические воспалительные или часто рецидивирующие офтальмологические заболевания;
- эндокринная патология: сахарный диабет, гипотиреоз;
- атеросклероз сосудов шеи, головы, сетчатки глаза, гипертоническая болезнь;
- нарушение гормонального фона в период полового созревания, беременности, климакса, во время терапии гормональными препаратами;
- сильные зрительные нагрузки;
- травмы головы и органов зрения;
- гиповитаминозы;
- стрессовые состояния;
- перенесенная острая вирусная инфекция;
- воздействие на организм токсических соединений.
Опасен ли данный симптом?
Важно! В случае возникновения «плавающих мушек» в поле зрения следует обратиться к врачу-офтальмологу для установления причины их появления и определения тактики лечения.
Первичное нарушение прозрачности небольшого размера, развившееся вне связи с другими офтальмологическими заболеваниями, как правило, не представляет угрозы для остроты зрения и не требует специальных вмешательств.
Небольшие помутнения со временем могут рассосаться самостоятельно, что связано с обменными процессами в структурах глаза.
Увеличение количества помутнений, их размера или четкости свидетельствует о серьезных изменениях в структуре глаза, без необходимого лечения склонных к прогрессированию и серьезному влиянию на зрение и здоровье человека.
В таких случаях, необходимо как можно быстрее установить причину патологического состояния и начать соответствующую терапию.
Клинические проявления
Внимание! Основным проявлением данного патологического состояния служит возникновение в поле видимости плавающих пятен, точек и полос, которые становятся видимыми при направлении взгляда на светлые яркие объекты:
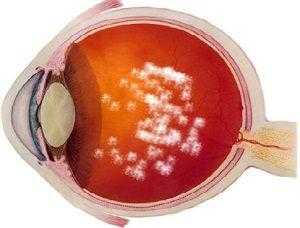
- «мушки» и помутнения носят постоянный характер, размеры и форму;
- такие оптические эффекты заметны при взгляде на светлые поверхности и не выявляются в темноте или с закрытыми глазами;
- при наличии множественных помутнений часто наблюдается повышенная утомляемость, головные боли, снижение контрастной чувствительности и постепенное ухудшение остроты зрения;
- при прогрессировании заболевания отдельные полосы и пятна могут сливаться между собой, образуя большие конгломераты, вызывающие выпадение отдельных участков полей зрения.
Методы диагностики
Основными методиками, используемыми для выявления деструктивных процессов в стекловидном теле, является офтальмологический осмотр с использованием офтальмоскопа и щелевой лампы, а также проверка остроты зрения и правильный и полный сбор анамнеза.
Также он может назначить дополнительные методы обследования, к которым относят:
- ультразвуковое исследование глаз;
- компьютерную томографию головы и шеи с целью визуализации сосудов;
- оптическую когерентную томографию.
Особенности лечения
В зависимости от тяжести заболевания и причин, вызвавших помутнение стекловидной структуры, существует несколько методик лечения: консервативное медикаментозное, хирургическое и лазерная терапия.
При выявлении деструкции назначаются следующие препараты:
- Лекарственные средства, улучшающие микроциркуляцию в сосудах глаза: Эмоксипин, Эмоксибел, Метилэтилпиридинол-Эском.
Такие препараты применяются короткими курсами 3-4 раза в год и вводятся в парабульбарную клетчатку. - Препараты, улучшающие кровообращение в головном мозге: Вобэнзим, Кавинтон, Циннаризин.
Они принимаются внутрь, улучшают проходимость кровеносных сосудов и обладают рассасывающими свойствами. - Местное применение рассасывающих лекарственных средств: инстилляции 2%-ого или 3%-ого раствора йодистого калия, Вита-Йодурол, Квинакс.
Будьте в курсе! В случае тяжелого течения болезни, когда одного медикаментозного лечения не достаточно, прибегают к хирургическому или лазерному вмешательству:
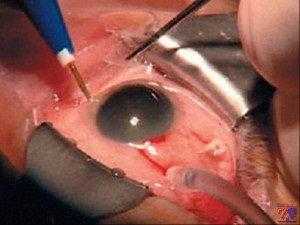
- Витреолизис.
Процедура, выполняемая при помощи YAG-лазера и направленная на разрушение образовавшихся помутнений.
К данному методу лечения прибегают в том случае, когда деструктивные процессы приводят к выраженной миопии высокой степени или возникает риск отслойки сетчатки. - Витрэктомия.
Хирургическое вмешательство, целью которого является полное или частичное удаление пораженного стекловидного тела и его замена на искусственную среду, схожую по своим преломляющим свойствам.
В качестве компонентов-заменителей выступают силиконовое масло, газовые пузырьки, солевой физиологический раствор.
Хирургическое лечение показано в случае отслоения сетчатки, критическом снижении зрения, выпадении из полей видимости больших участков.
При использовании газовых пузырьков или солевых растворов повторной операции не требуется, поскольку по прошествии времени они самостоятельно замещаются собственной внутриглазной жидкостью.
При замене стекловидного тела на силиконовое масло и другие полимеры необходимо повторное вмешательство через 5-8 лет, поскольку такие компоненты со временем теряют свои преломляющие свойства.
Профилактические меры
- Правильное сбалансированное питание, обогащенное белками, витаминами и микроэлементами;
- ежегодные профилактические осмотры у врача-офтальмолога;
- контроль степени и продолжительности зрительных нагрузок;
- своевременное лечение офтальмологической, эндокринной и соматической патологии;
- проведение мероприятий по коррекции остроты зрения в случае ее снижения.
Полезное видео
Из данного видео вы узнаете, как избавиться от «мушек» перед глазами:
Появление единичных оптических эффектов в виде плавающих перед глазами полос и мушек не являются угрозой полноценной жизни человека или его здоровью.
Но прогрессирование данного состояния требует постоянного контроля и лечения, поэтому не стоит откладывать визит к офтальмологу в случае нарастания клинических симптомов.
Послеоперационный эндофтальмит: современные методы профилактики и лечения
Ключевые слова: послеоперационный эндофтальмит, TASS-синдром, витрэктомия, антибиотики, стекловидное тело.
Эндофтальмит — (от греч. endo — внутри и ophthalmos — глаз) — это гнойное воспалительное заболевание внутренних оболочек глаза. Возникает вследствие инфицирования бактериями или грибами во время травмы, интраоперационно или в раннем послеоперационном периоде, в редких случаях — из-за распространения инфекции из эндогенных источников. Учитывая патогенез заболевания, время, необходимое для миграции патогенов в заднюю камеру глаза и накопления там медиаторов воспаления, составляет не менее 2 суток.
По механизму возникновения эндофтальмит подразделяют на:
- Острый послеоперационный (возникает в срок до 2 недель после выполненной операции)
Частота развития эндофтальмита после экстрации катаракты, по данным Европейского общества катаральных и рефракционных хирургов (ESCRS) [1], составляет 0,35 % без применения интракамерального введения цефуроксима, с применением — 0,05 %. В США, по данным Нила Шорстейна (Neal H. Shorstein) — 0,31 % и 0,014 % соответственно [8].
Этиология ипатогенез
По данным исследования Endophthalmitis Vitrectomy Study (EVS), основным источником инфицирования является микрофлора поверхности конъюнктивы пациента [7]. Самыми распространенными причинами развития острого послеоперационного эндофтальмита являются коагулазонегативные стафилококки, в частности Staphylococcus epidermidis (33-77 %); Staphylococcus aureus (10-21 %). При хроническом эндофтальмите наиболее вероятным возбудителем является Proprionibacterium acnes.
Микроорганизмы, часто встречающиеся при остром послеоперационном эндофтальмите [1]
Распространённость (%)
Виды микроорганизмов
КНС (коагулазонегативные стафилококки)
BHS (β-гемолитические стрептококки),
S. pneumoniae, ∂-гемолитические стрептококки, включая S. mitis и S. salivarius
Грамотрицательные бактерии, включая Ps. aeruginosa
Грибы (виды Candida, виды Aspergillus, виды Fusarium)
Микроорганизмы, часто встречающиеся при хроническом или позднем послеоперационном эндофтальмите [1]
К факторам риска развития эндофтальмита относятся:
- Увеличенное время операции у неопытного хирурга
- Повреждение задней капсулы хрусталика и стекловидного тела во время операции
- Наличие у пациента блефарита до операции
- Поверхность интраокулярных линз как среда для развития микроорганизмов
- Недостаточная стерилизация инструментов и операционного поля
Следует также отметить роль бесшовных оперативных методик в развитии послеоперационного эндофтальмита: использование туннельного бесшовного разреза роговицы способствует повышению частоты развития эндофтальмита после факоэмульсификации катаракты вследствие возможности всасывания в переднюю камеру слезной жидкости в раннем послеоперационном периоде.
По данным руководства ESCRS, у пациентов с роговичным туннелем вероятность развития эндофтальмита в 5,88 раз больше, чем при корнеосклеральном доступе [1].
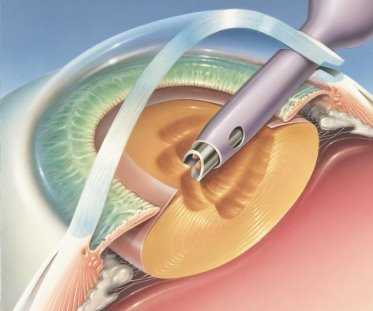
Рис. 1. Применение роговичного тоннельного доступа
В том же руководстве сообщается, что при имплантации силиконовых интраокулярных линз (ИОЛ) вероятность развития эндофтальмита в 3,13 раз выше в сравнении с линзами из акрила или другого материала, а хирургические осложнения сопровождались 4,95-кратным увеличением данного риска. Большинство имплантируемых ИОЛ на данный момент изготовлены из гидрофобного акрила, а силиконовые встречаются редко по причине инфекционных осложнений и риска повредить линзу при имплантации через разрезы менее 2,8 мм [15].
Клиника идиагностика
К основным клиническим проявлениям эндофтальмита, согласно исследованию EVS, относятся: нечёткость зрения (94 % пациентов), болевой синдром (74 %), отёк век (34 %), гипопион (80 %), покраснение глаза (82 %), помутнение сред глаза (74 %). Лизис стекловидного тела и замещение его гнойными массами вызывают жёлто-зелёный рефлекс с глазного дна.
По степени тяжести эндофтальмит может быть условно разделен на лёгкий, средней тяжести и тяжёлый:
- Лёгкий: слабо выраженный болевой синдром, умеренная инъекция глазного яблока, возможно проведение офтальмоскопии.
- Средней тяжести: выраженный болевой синдром и инъекция глазного яблока, невозможна офтальмоскопия, значительно снижена острота зрения, допускается наличие витреита, хемоза, отёка век.
- Тяжёлый: выраженный болевой синдром с иррадиацией в соответствующую половину черепа; выраженные: инъекция глазного яблока, хемоз, гипопион, витрит, отёк век; невозможна офтальмоскопия; снижение остроты зрения вплоть до светооощущения.
А. М. Южаков предложил классификацию в зависимости от формы развития:
- Очаговый эндофтальмит (абсцесс стекловидного тела), стадии I-II
- Диффузный эндофтальмит, стадии I-IV
- Смешанная форма, стадии I-IV
- Панофтальмит — конечный результат инфекционного процесса
При подозрении на послеоперационный эндофтальмит каждый час определяется острота центрального зрения, при ее резком снижении незамедлительно приступают к хирургическому лечению. Снижение зрительных функций до светоощущения является прогностически неблагоприятным фактором. Помимо визометрии, проводится биомикроскопия и офтальмоскопия для динамической оценки послеоперационного воспаления. Из инструментальных методов исследования обязательным является УЗИ (B-scan).
Дополнительно также проводятся периметрия и электрофизиологические исследования зрительного нерва и сетчатки (электроретинография). Снижение их показателей будет указывать на токсическое повреждение внутренних оболочек глаза и являться показанием для хирургического лечения.
Перспективным методом диагностики и контроля эффективности лечения является лазерная тиндалеметрия. Принцип работы основан на измерении интенсивности лазерного луча, отраженного от взвешенных во влаге передней камеры клеток и крупномолекулярных белков (альбуминов и макроглобулинов). Когда частица белка или клетка проходит через фокус лазера, происходит отражение излучения.
До начала лечения обязательным является предварительная пункция передней камеры глаза и биопсия стекловидного тела для проведения бактериологического анализа. Взятые пробы окрашивают по Граму (экспресс-метод) с дальнейшей идентификацией микроорганизмов и определением чувствительности к антибиотикам.
ПЦР с использованием праймеров широкого диапазона, нацеленных на высококонсервативные регионы эубактериальной 16S рДНК (18S рДНК для грибов), может выявлять и амплифицировать минимальные количества бактериальной ДНК, с их последующим секвенированием и идентификацией. Она обеспечивает намного лучшее выявление патогенов, особенно в случаях хронического эндофтальмита с малым количеством патогенов [9].
Дифференциальная диагностика сTASS-синдромом
Синдром токсического повреждения переднего сегмента глаза (TASS-синдром, экссудативно-воспалительная реакция) — состояние, сходное с эндофтальмитом по клиническим проявлениям, но имеющее другой патогенез. Синдром токсического повреждения переднего сегмента глаза (TASS-синдром) представляет собой стерильную послеоперационную воспалительную реакцию, вызываемую веществом неинфекционного происхождения, попавшим в передний сегмент глаза, что приводит к токсическому повреждению внутриглазных тканей.
Основные группы веществ, которые при попадании в передний сегмент могут вызвать TASS-синдром:
- Вещества извне, которые случайно проникают в переднюю камеру глаза во время или после операции (например, повидон-йод для местного применения).
- Продукты, вводимые в переднюю камеру глаза как часть хирургической процедуры, такие как сбалансированный солевой раствор из партии, произведенной с ошибочным рН или осмолярностью (или с лекарственными препаратами, добавленными в операционной) или анестетики (безопасным является только не содержащий консервантов 1 % лидокаин). Любой лекарственный препарат, вводимый в глаз, не должен содержать консервантов и должен использоваться в надлежащей концентрации, чтобы избежать развития токсических реакций.
- Раздражающие вещества на инструментарии, скопившиеся вследствие его неправильной очистки и/или стерилизации (например, денатурированные офтальмологические вискоэластики, оставшиеся на многоразовом инструментарии, стабильные к воздействию тепла эндотоксины, сульфатные примеси после автоклавирования паром).
К отличительным признакам TASS-синдрома относятся:
- Раннее начало (уже через 12-24 часа после операции)
- Отек роговицы от лимба до лимба, вторичный по отношению к распространенному повреждению слоя эндотелиальных клеток
- Повреждение радужной оболочки (фиксированный, расширенный или неправильной формы зрачок, дефекты просвечивания радужной оболочки)
- Высокое ВГД вследствие повреждения трабекулярной сети
- Отсутствие витрита (наиболее важная характеристика TASS-синдрома, поскольку он характеризуется главным образом воспалением переднего сегмента глаза, в то время как при эндофтальмите вовлекается задний сегмент).
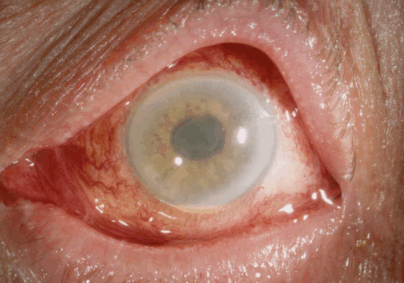
Рис. 2. Отёк роговицы, деформация зрачка и гипопион у пациента с TASS-синдромом [6]
Лечение TASS-синдрома включает в себя интенсивное применение местных кортикостероидов (и иногда пероральных).
Лечение острого послеоперационного эндофтальмита
Основными методами лечения являются витрэктомия и интравитреальное введение антибиотиков. ESCRS рекомендует при наличии витреоретинального хирурга и оснащенной операционной проводить стандартную трехпортовую центральную или полную витрэктомия по принципу «Ubi pus ibi evacuat» («Где гной, там очищай»). При центральной витрэктомии остается часть основы стекловидного тела, в то время как более полная витрэктомия сопровождается риском ятрогенного отслоения сетчатки, что является потенциальной катастрофой. Данный выбор остается за витреоретинальным хирургом.
После того, как витрэктомия выполнена, через один из разрезов склеры с использованием иглы диаметром 25-30G интравитреально вводятся антибиотики. В случае выполнения полной витрэктомии дозу следует уменьшить на 50 %. Данную инъекцию следует проводить медленно, в течение 1-2 минут, в середину стекловидного тела, направляя конец иглы вверх, подальше от макулы. Отдельные шприцы и отдельные иглы, для меньшей вероятности контаминации, вводятся через уже имеющееся отверстие. Затем интравитреально вводится дексаметазон (не содержащий консервантов).
Когда операцию «золотого стандарта» невозможно выполнить вследствие отсутствия витреоретинального хирурга и витреоретинальной операционной, приемлемым вариантом является проведение биопсии стекловидного тела с интравитреальным введением антибиотиков без последующей терапевтической витрэктомии («серебряный стандарт»). Поскольку простая аспирация с помощью иглы зачастую безуспешна, ее можно провести с помощью портативного витректора.
Дозы интравитреальных антибиотиков следует выбирать особо тщательно, потому что зазор для ошибки между терапевтической дозой и токсичностью является узким, особенно для аминогликозидов (гентамицин в дозе 200 мкг является эффективным, но в дозе 400 мкг может быть токсичным, вызывая макулярный инфаркт).
Комбинацией лекарственных средств первого выбора являются ванкомицин (1 мг) сцефтазидимом (2 мг).
Комбинация второго выбора: ванкомицин (1 мг) вкомбинации самикацином (0,4 мг), особенно у пациентов с чувствительностью к ß-лактамам. Несмотря на синергизм между ванкомицином и амикацином в отношении грамположительных микроорганизмов, многие хирурги избегают применения аминогликозидов для эрадикации грамотрицательных бактерий из-за риска ретинальной токсичности.
И. А. Фролычев предлагает введение раствора антибиотика в витреальную полость сочетать с тампонадой ПФОС [2], ввиду того, что раствор антибиотика активно перемещается с пузырем ПФОС в зависимости от положения тела пациента («на спине» — максимальное воздействие у зубчатой линии сетчатки, в положении стоя или сидя — воздействие на верхние отделы сетчатки, «на боках» — воздействие на назальную или височную половину сетчатки). При этом риск токсического локального воздействия растворов антибиотиков значительно снижается. При использовании ПФОС уменьшается риск токсического поражения макулярной зоны струей вводимого интравитреально АБ препарата. ПФОС, создавая противодействие вводимой струе препарата, препятствует токсическому повреждению макулы, освобождает хирурга от необходимости вводить раствор антибиотика медленно в течение 2-3 минут.
Тяжелый острый гнойный эндофтальмит следует лечить с использованием дополнительной системной антибиотикотерапии теми же лекарственными препаратами, которые используются для интравитреальной терапии. Такая схема лечения поможет поддерживать значимые интравитреальные концентрации лекарственного препарата на протяжении более длительного времени путем уравновешивания диффузии введенного препарата из глаза.
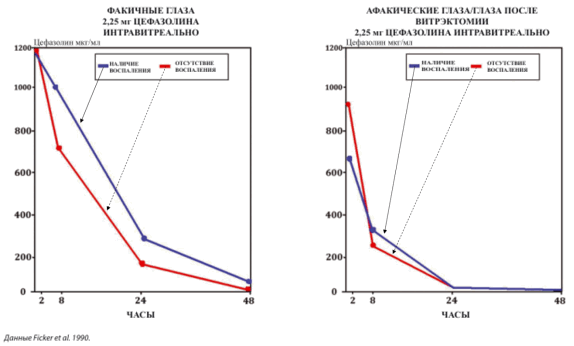
Рис. 3. Скорость выведения цефазолина из стекловидного тела [1]
Лечение хронического послеоперационного эндофтальмита
В отличие от острого послеоперационного эндофтальмита, представляющего собой неотложное состояние, в случае возможного хронического послеоперационного эндофтальмита имеется больше времени для правильной постановки диагноза и выбора вида лечения.
При хроническом эндофтальмите микроорганизмы изолированы в капсулярном мешке и защищены биопленкой; также они могут иметь внутриклеточную локализацию внутри макрофагов, где их не достигают антибиотики, часто используемые для лечения острого эндофтальмита. Однако некоторые антибиотики, такие как кларитромицин, хорошо абсорбируются при приеме внутрь, хорошо проникают в глаз, обладают антибиопленочными свойствами и концентрируются внутри нейтрофилов и макрофагов, где они в лучшей степени способны уничтожать внутриклеточные грамположительные бактерии.
Некоторые исследования [10,11] нашли применение кларитромицина эффективным и рекомендовали использовать дозу в 500 мг 2 раза в день на протяжении 2-4 недель. Добавление промывания ванкомицином капсулярного мешка повышало частоту ответа на лечение в случаях инфекции, вызванной видами Propionibacterium [13].
Для лечения хронического эндофтальмита существует несколько вариантов хирургических вмешательств:
- Промывание антибиотиком капсулярного мешка при первичной пункции передней камеры или при последующем вмешательстве в случаях положительного результата бакпосева
- Интравитреальная инъекция антибиотиков (ИИАБ)
- Витректомия рars plana (ВПП) с ИИАБ
- ВПП с частичной капсулэктомией (ЧК) и ИИАБ
- ВПП с тотальной капсулэктомией (ТК), ИИАБ, извлечением или заменой ИОЛ (зИОЛ)
Чем более агрессивным является лечение, тем ниже частота рецидивирования [14].
Профилактика
Основные этапы антисептики впредоперационном периоде
1. Обязательная обработка повидон-йодом роговицы и конъюнктивального мешка
2. Обязательная обработка повидон-йодом окологлазничной области
3. Использование медицинской спецодежды (халат, перчатки и пр.) и специального режима вентиляции в операционной
4. Обкладывание глаза салфетками,
заклеивание век и ресниц (не обрезать)
Основой профилактики послеоперационного эндофтальмита является соблюдение правил асептики и антисептики. Применение местных антибиотиков в каплях перед операцией не показано ввиду низкой эффективности и отсутствия доказательной базы [12].
Основные термины (генерируются автоматически): стекловидное тело, ESCRS, токсическое повреждение, EVS, передний сегмент глаза, антибиотик, выраженный болевой синдром, глазное яблоко, передняя камера глаза, лекарственный препарат.
Ключевые слова
Похожие статьи
Характер повреждения зрительного анализатора при алкогольной.
Глаза являются самой выразительной частью лица, и, как писал выдающийся русский писатель А. П. Чехов: «Глаза— это зеркало души».
Биомикроскопические исследования не выявили каких-либо особенностей в состоянии переднего отрезка глаза и стекловидного тела [3].
Современные подходы в лечении катаракты | Статья в журнале.
Деструкция стекловидного тела. Больные жалуются на постепенное снижение остроты зрения, как правило, возникающее на фоне воспалительных заболеваний глаза. При биомикроскопии хрусталик прозрачен, выявляется деструкция передних отделов стекловидноготела.
Влияние физических факторов окружающей среды на.
Передняя камера глаза — это пространство между роговицей и радужкой.
Стекловидное тело — гелеобразная прозрачная субстанция, расположенная в заднем отделе глаза.
Характер повреждения зрительного анализатора при алкогольной.
Дистрофия роговицы Когана: клиника, диагностика, лечение
5. Эндотелий является внутренней частью роговицы, обращенной в переднюю камеру глаза и омываемой внутриглазной жидкостью.
Симптоматическая клиника дистрофии связана с синдромом рецидивирующей эрозии роговицы и временным незначительным снижением.
Почему глаза двигаются вместе? | Статья в журнале.
Он находится в передней части глазного яблока. В преломлении света участвует также вещество, которым заполнена большая часть (2/3 объема) глазного яблока
Современные техники стабилизации изображения на сетчатке.
Первые способы фиксации стимуляции на сетчатке глаза включали в себя полное обездвиживание глаз [1]. Затем
Такие методы позволяли стабилизировать воспринимаемы объекты на глазном яблоке таким образом, что он перемещался вместе с движением взора с.
Клинические проявления, диагностика и исходы невритов.
Весь глаз по форме похож на шар и называется глазным яблоком (рис. 1). Рис. 1. Глазное яблоко. Когда свет достигает сетчатки, она
Основные термины (генерируются автоматически): поражение глаз, суставной синдром, ювенильный ревматоидный артрит, послеоперационный.
Офтальмологическая реабилитация больных ювенильным.
Деструкция стекловидного тела отмечалась у 9 (28 %), синехии почти у трети пациентов, катаракта — у 7 (22 %) больных.
Артикулярный синдром был вторичным по отношению к патологии глаз в 7 (22 %) случаях (артрит возник через 2-7 лет, в среднем 3,5 года).
Особенности течения и реабилитация больных ювенильным.
Артикулярный синдром был вторичным по отношению к патологии глаз в 7 (22 %) случаях (артрит возник через 2- 7 лет, в среднем 3,5 года).
Читайте также:
