Прочие патогенные виды вибрио. Прочие патогенные виды Vibrio. Галофильный вибрион. Парагемолитический вибрион. Vibrio parahaemolyticus.
Добавил пользователь Евгений Кузнецов Обновлено: 10.01.2026
ВИБРИОНЫ — род микроорганизмов Vibrio, включающий грамотрицательные с постоянным изгибом или прямые аспорогенные палочки с полярно расположенным жгутиком, индофенолоксидазоположительные, образующие кислоту без газа из D-глюкозы путем гликолиза по схеме Эмбдена — Мейергофа. Это временное определение было предложено в 1966 г. Подкомитетом по таксономии В. Международной ассоциации микробиол, обществ (IAMS).
Прежние определения рода Vibrio позволяли причислять к нему большое количество грамотрицательных микробов. Приведенное определение позволило исключить из рода Vibrio многие виды бактерий.
Согласно классификациям В. Д. Штибена и И. К. Бабича (1955), Брида (R. Breed, 1957), Уилсона и Майлса (G. Wilson, A. Miles, 1964), род Vibrio отнесен к сем. Spirillaceae; Эдди, Карпентер (В. Eddy, К. Carpenter, 1964) и Верон (М. Veron, 1965) полагают, что род Vibrio должен стать основой нового сем.— Vibrionaceae.
В связи с тем что В. очень сходны с негазообразующими представителями рода Aeromonas, который также предложено включить в сем. Vibrionaceae, Саказаки (R. Sakazaki) и соавт. (1967) дополнили определение рода Vibrio сведениями о наличии декарбоксилаз лизина и орнитина, отсутствии аргининдигидролазы, а также о способности расщеплять желатину, свойстве восстанавливать нитраты и неспособности образовывать сероводород. Остается спорным вопрос о таксономическом положении «штаммов С27» [Фергюсон, Хендерсон (W. Ferguson, N. Henderson), 1947], которые Габс, Шуберт (H.Habs, R. Schubert, 1962) предложили отнести к новому роду Plesiomonas (вид Shigelloides) сем. Pseudomonadaceae. Верон (1971) рассматривает эти микроорганизмы как В.— Vibrio shigelloides. Эдди и Карпентер (1964) считают, что упомянутые микроорганизмы следует исключить из сем. Pseudomonadaceae и отнести к сем. Vibrionaceae как род Plesiomonas.
В. приходится дифференцировать не только с Plesiomonas и негазообразующими представителями Aeromonas, но и с микробами родов Pseudomonas и Comamonas (последних ранее называли инактивными В.).
В связи с 7-й пандемией холеры род Vibrio неоднократно подвергался ревизии, но до сих пор общепринятой классификации В. не существует. В 1936 г. Хейберг (В. Heiberg) предложил биохим, классификацию В., к-рую в 1965 г. дополнили Смит и Гудиер, основанную на различном отношении В. к трем углеводам: сахарозе, арабинозе и маннозе (табл. 1). Схема Хейберга может быть использована для дифференциации В. только в комплексе с другими признаками.
Для медицины наибольшее значение имеют следующие представители рода Vibrio:

1. V. cholerae (биотип V. cholerae и биотип V. El Tor) — возбудитель холеры (рис.). От больных холерой и здоровых вибриононосителей, из сточных вод нередко выделяют атипичные В., в частности не агглютинирующиеся холерной OI-сывороткой. В одних случаях отсутствие агглютинабельности O-антигена связано с фенотипическим изменением; 2-часовое прогревание при 1100° восстанавливает агглютинабельность. В других случаях имеет место наследственное изменение строения О-антигена; возникающие мутанты называют НАГ-вибрионами. Для выяснения, являются ли такие атипичные В. холерными, используют типовые О-сыворотки. Описано 39 О-групп В., имеющих общий H-антиген. Признанные всеми возбудители холеры (см.) относятся к OI-группе.
Очень близок к холерным В. по морфол., культуральным, биохим, признакам и по способности давать перекрестный иммунитет Vibrio metchnikovi.
В., сходные с холерными по морфол., культуральными биохим, признакам, но не обладающие общими с ними О- и Н-антигенами, часто выделяют из объектов окружающей среды. Если видовая принадлежность В. не определена, их следует именовать Vibrio spp., но не НАГ-вибрионами.
2. V. parahaemolyticus — факультативно галофильный микроб, вызывающий дизентерие- и холероподобные заболевания, пищевые отравления, связанные с употреблением сырой и полусухой морской рыбы, крабов, моллюсков.
Парагемолитические В. широко распространены в морях и океанах, там, где имеются благоприятные температурные условия и вода богата органическими веществами. Одной из характерных особенностей V. parahaemolyticus является галофилия — неспособность к размножению в отсутствие хлорида натрия и устойчивость к его значительным концентрациям (7—8%).
Изучение антигенного строения этих В. показало, что, кроме термостабильного соматического О-антигена, они содержат термолабильные капсульный (К) и жгутиковый (Н) антигены. Описано 12 типов по О-антигену и 55 по К-антигену.
3. V. alginolyticus — галофильный микроб, обнаруживаемый в морской воде, гидробионтах и иногда в стуле больных гастроэнтеритами.
4. V. phosphorescens (син. V. albensis) — светящиеся В., обитающие в пресной и соленой воде открытых водоемов. 3. В. Ермольева (1924) впервые обнаружила его в испражнениях человека.
Дифференциальные признаки В. и сходных с ними бактерий представлены в табл. 2 и 3.
Таблица 1. БИОХИМИЧЕСКАЯ КЛАССИФИКАЦИЯ ВИБРИОНОВ ПО ИХ ОТНОШЕНИЮ К УГЛЕВОДАМ (Heiberg, 1936; Smith and Goodner, 1965)
13.7.1.2. Другие патогенные вибрионы
Парагемолитический вибрион (Vibrio parahaemolyticus) - галофильный вибрион, вызывающий острые гастроэнтериты. Распространен повсеместно в морской и пресной воде, эндемичен для Японии, вызванные им заболевания регистрируются также в странах Юго-Восточной Азии, Африки, Латинской Америке.
Основной метод диагностики - бактериологический с выделением возбудителя на ТЦБС-агаре, где V. parahaemolyticus образует зеленоватые колонии, т.к. не ферментирует сахарозу.
Идентификацию возбудителя проводят по серологическим и биохимическим свойствам.
Vibrio vulnificus распространен в прибрежных водах Тихого и Атлантического океанов. Возбудитель концентрируется в «природных фильтрах» - двухстворчатых моллюсках (устрицах, мидиях, гребешках и т.п.), вызывает 2 типа различных поражений - септицемии и раневые инфекции.
Заболевания чаще регистрируют у людей с иммунодефицитными состояниями, при нарушении функции печени, почек и сахарном диабете. Летальность у таких пациентов может достигать 50%. Наиболее тяжело инфекции протекают у лиц с гемохроматозом, т.к. возбудитель высокочувствителен к высоким концентрациям железа в сыворотке.
Раневые инфекции возникают при попадании контаминированной морской воды на поврежденные кожные покровы. Проявляются как целлюлиты, миозиты, некротизирующие васкулиты.
Факторы патогенности, которые продуцируют возбудитель, включают капсулу, комплекс ферментов (эластаза, коллагеназа, фосфолипаза), а также цитотоксин - гемолизин.
Лабораторная диагностика Проводится путем выделения V. vulnificus на TCBS-агаре (образует желтые колонии, т.к. ферментирует сахарозу). В отличие от холерного вибриона большинство штаммов V. vulnificus ферментируют лактозу.
Для лечения применяют антимикробные препараты (гентамицин, тетрациклины, хлорамфеникол).
XIV. Палочки грамположительные аэробные
14.1. Возбудитель сибирской язвы
Бактериальное происхождение заболевания было отмечено еще в середине XIX века (А. Полландер, 1849 г.; К. Давейн, 1850 г.) В чистой культуре возбудитель был выделен в 1876 г. Р. Кохом. Само заболевание приобрело название «сибирская язва» из-за обширной эпидемии в Сибири в 1786-1788 г.г., которая была детально изучена С. Андриевским.
Классификация
Семейство Bacillaceae является весьма многочисленным и объединяет более 30 родов. В свою очередь, род Bacillus также включает несколько десятков отдельных видов.
Основным возбудителем заболеваний у животных и человека является Bacillus anthracis, который вызывает сибирскую язву. Название вида произошло от греческого anthrax (антракс - уголь) по виду сибиреязвенного карбункула - черного гнойного первичного очага в коже.
Среди других бацилл Bacillus cereus может вызывать у человека пищевые токсикоинфекции.
Цепочки бактерий при микроскопировании напоминают «бамбуковую трость». При культивировании на средах с пенициллином палочковидные формы микробных клеток превращаются в глобулы (феномен «жемчужного ожерелья»).
Культуральные свойства
Неприхотливы к питательным средам. Хорошо растут на простых питательных средах. Вирулентны в R-форме - образуют крупные шероховатые колонии. Под микроскопом колонии напоминают «львиную гриву» или «голову медузы», имеют волокнистое строение.
Могут диссоциировать на S- (гладкие, авирулентные), М- (слизистые) и SM- (смешанные) колонии. При росте на жидких средах образуют осадок, напоминающий «комочки ваты».
Бактерии способны продуцировать гемолизин, но на кровяном агаре гемолиз либо отсутствует, либо проявляется очень медленно.
Биохимические свойства
Факультативные анаэробы. Биохимическая активность весьма выражена.
Разлагают глюкозу, мальтозу, сахарозу и другие углеводы, не разлагают лактозу, маннит и дульцит. Гидролизуют крахмал.
Восстанавливают нитраты в нитриты.
Белки разлагают до аммиака и сероводорода, желатин разжижают в виде «перевернутой елочки». Молоко свертывают на 3-5 сутки.
Выделяют ферменты каталазу, оксидазу, дегидрогеназу, лецитиназу.
Антигенная структура
Соматический антиген представляет собой полисахарид клеточной стенки; капсульный - полипептид D-глутаминовой кислоты, протективный антиген является рецепторной частью в токсическом комплексе возбудителя.
Факторы вирулентности
Гены патогенности возбудителя локализованы в двух плазмидах.
Одна из них кодирует синтез полипептидной капсулы, которая обладает выраженным антифагоцитарным действием. Бескапсульные штаммы обычно авирулентны
Другая плазмида определяет синтез двух основных экзотоксинов возбудителя - отечного токсина и летального токсина.
Эти токсины представляют собой сложные белковые комплексы, состоящие из рецепторной и ферментативной частей. По отдельности каждый из компонентов биологически неактивен.
Рецепторным компонентом обоих токсинов является протективный антиген, который обеспечивает связывание токсинов с клетками и их проникновение в цитоплазму.
В состав отечного токсина входит отечный фактор - фермент аденилатциклаза. В свою очередь, летальный токсин включает летальный фактор - фермент Zn-металлопротеиназу.
Начальные этапы действия токсинов зависят от протективного антигена. Он связывается с белковыми рецепторами на поверхности клеток. При этом протективный АГ расщепляется мембранными протеазами на 2 субъединицы. Большая субъединица полимеризуется с образованием полой структуры, которая приобретает свойства трансмембранного канала.
С этой структурой связывается несколько молекул отечного фактора (образуется отечный токсин) или летального фактора (образуется летальный токсин).
Сформированные токсины поступают в клетку посредством эндоцитоза. Летальный и отечный факторы выходят из эндосомы в цитоплазму через канал, образованный субъединицами протективного АГ.
Отечный фактор (фермент аденилатциклаза) увеличивает содержание цАМФ в клетке. Это подавляет функцию макрофагов, а также ведет к повышению проницаемости эндотелия и тканевому отеку с повреждением сосудов микроциркуляции.
Летальный фактор (фермент Zn-металлопротеиназа) гидролизует регуляторную внутриклеточную протеинкиназу (МАПК-киназу). Тем самым блокируется нормальный клеточный цикл, что приводит к апоптозу пораженных клеток.
Резистентность
Споры возбудителя сибирской язвы характеризуются крайней устойчивостью. В почве они могут сохранять жизнеспособность более 50 лет.
Вегетативные клетки погибают при 60 о С за 15 мин, при 100 о С - за 1-2 минуты. Споры гораздо более стабильны. Выдерживают кипячение в течение 15-20 минут и автоклавирование при 110 о С в течение 5-10 минут. Инактивируются под действием 1% формальдегида и 10% NaOH в течение 2-х часов
Патогенез и характеристика заболевания
Сибирская язва - острая бактериальная зоонозная особо опасная инфекция, характеризуется выраженной интоксикацией, серозно-геморрагическим воспалением кожи, лимфатических узлов, внутренних органов.
Источник инфекции - больные животные (дикие и домашние), выделяющие возбудителя с испражнениями и мочой. Поскольку споры бацилл могут сохраняться годами в почве, мерзлоте, трупах павших животных, факторы окружающей среды играют важную роль в передаче заболевания (сапронозная инфекция).
Также споры могут находиться длительное время в меховом и кожевенном сырье, изделиях из него.
Основные пути передачи: контактный - прямой контакт с больными животными или с изделиями из шерсти, кожи, щетины; алиментарный - через мясо от больных животных или продукты, инфицированные в процессе хранения; трансмиссивный - через кровососущих насекомых (слепни, мухи-жигалки); воздушно-пылевой.
В зависимости от места проникновения возбудителя, его вирулентности и восприимчивости организма у человека может быть 3 основных клинических формы сибирской язвы:
Кожная форма. Инкубационный период составляет 1-7 дней. У входных ворот возбудителя появляется красное пятно, переходящее в папулу медно-красного цвета, возникает зуд. Папула переходит в везикулу с серозным, затем геморрагическим содержимым. Образуется карбункул с черным струпом, присоединяется отек, интоксикация. Прогноз при своевременном лечении благоприятный.
Легочная форма. Развивается при попадании возбудителя или его спор через верхние дыхательные пути. Появляются катаральные явления со стороны верхних дыхательных путей, слезотечение, подъем температуры до 40 0 С.
Развивается пневмония, часто сменяющаяся токсическим отеком легких, в мокроте появляется кровь. Даже при назначении антибиотиков летальность при данной форме может превышать 40-50%. Без лечения возбудитель диссеминирует по организму, при этом летальность значительно увеличивается.
Абдоминальная (кишечная) форма. Развивается редко. Возникает при алиментарном пути заражения. Характерными признаками являются лихорадка, озноб, рвота, диарея с кровью, боли в животе, на коже геморрагии. Смерть может наступить через 3-5 дней от начала заболевания. Летальность при данной форме составляет 25-60%.
В связи с чрезвычайной устойчивостью спор возбудителя в окружающей среде, наличием высокоактивных экзотоксинов и возможностью ингаляционного распространения инфекции бацилла сибирской язвы представляет серьезную опасность как потенциальное средство биотерроризма.
В 2001 г. в США произошли неоднократные случаи заболевания сибирской язвой как результат биотеррористической атаки. Споры возбудителя распространялись в письмах при почтовых рассылках. Заражение происходило либо контактным, либо ингаляционным путем. Было подтверждено 22 случая заражения, 5 заболевших погибли. Предполагается, что реальное число пострадавших превышало 60 человек.
Иммунитет после заболевания стойкий, клеточный и гуморальный. В течение болезни развивается специфическая сенсибилизация, выявляется ГЧЗТ.
Лабораторная диагностика
Материал зависит от формы заболевания: кровь, моча, мокрота, кал, рвотные массы, отделяемое из сибиреязвенного карбункула.
Так как B. anthracis относится ко II группе патогенности, а заболевание относится к группе особо опасных инфекций, все работы по выделению возбудителя проводят в специализировнной лаборатории особо опасных инфекций. Материал от больного доставляется в особой упаковке (сосуды парафинируют, прикрепляют этикетку с обозначением материала, Ф.И.О. больного и лица, взявшего материал), сосуды с материалом заворачивают в салфетки, смоченные дезраствором и помещают в специальные контейнеры.
Бактериоскопический метод. Готовят мазок из вышеуказанного материала, окрашивают по Граму. Выявляют цепочки грамположительных палочек в общей капсуле.
Бактериологический метод - посев на МПА с последующей идентификацией возбудителей по морфологическим, культуральным, биохимическим свойствам.
Для диагностики инфекции также используют биопробу (заражение лабораторных животных).
Мышам вводят 0,1-0,2 мл исследуемого материала, кроликам и морским свинкам - 0,2-0,5 мл. Животные гибнут через 2-10 дней. Трупы вскрывают, делают протокольные посевы и микроскопируют мазки-отпечатки из внутренних органов трупов животных с целью выявления возбудителя и его идентификации.
Для ускоренной диагностики оценивают чувствительность к специфическому бактериофагу.
Необходима дифференциация возбудителя от сапрофитических бацилл. Основными отличительными признаками возбудителя являются наличие капсулы, характер роста на средах, феномен «жемчужного ожерелья» при культивировании с пенициллином, чувствительность лабораторных животных к инфекции (мышей, морских свинок, кроликов).
Иногда применяют кожно-аллергическую пробу с антраксином для выявления ГЧЗТ (вводят внутрикожно 0,1 мл антраксина).
Для обнаружения антигена в экстрактах из тканей трупного материала, кожевенном сырье, шерсти используют реакцию термопреципитации по Асколи.
Также для выявления антигена в материале применяют ИФА или РПГА с антительным диагностикумом.
Раннее назначение антибиотикотерапии является жизненно необходимым. Препараты назначают в высоких дозах.
Пенициллин используют для лечения случаев заболевания, вызванных чувствительными к нему штаммами B. anthracis. Также в терапии эффективны фторхинолоны, тетрациклины, ванкомицин.
Для экстренной профилактики и лечения возможно назначить противосибиреязвенный иммуноглобулин.
Профилактика
Специфическая профилактика: животных вакцинируют живой авирулентной вакциной из некапсулированного штамма Bacillus anthracis СТИ-1 и протективным антигеном.
Лица из групп профессионального риска (работники ветеринарной и лабораторной службы, скотоводы, доярки) вакцинируются протективным антигеном.
Неспецифическая профилактика включает изоляцию больных и подозрительных животных, сжигание их трупов, обеззараживание мест стоянок больных животных; необходим постоянный санитарный надзор за предприятиями, перерабатывающими животное сырье.
Холероподобные вибрионы не агглютинируются О1-сывороткой, их обозначают как НАГ-вибрионы (неагглютинирующиеся).
Основной метод диагностики - бактериологический с выделением возбудителя на TCBS-агаре, где V.parahaemolyticus образует зеленоватые колонии, т.к. не ферментирует сахарозу. В отличие от холерного вибриона не разлагает орнитин.
Заболевания чаще регистрируют у людей с иммунодефицитными состояниями, при нарушении функции печени, почек и сахарном диабете. Летальность - 50%. Септицемии развиваются после употребления моллюсков и проявляются буллезными поражениями кожи.
Факторы патогенности - капсула, защищающая бактерии от фагоцитоза, и комплекс ферментов (эластаза, коллагеназа, фосфолипаза), а также цитотоксин - гемолизин.
Наиболее тяжело инфекции протекают у лиц с гемохроматозом, т.к. возбудитель высокочувствителен к высоким концентрациям железа в сыворотке.
Диагностика проводится путем выделения V. vulnificus на TCBS-агаре (образует желтые колонии, т.к. ферментирует сахарозу). В отличие от холерного вибриона большинство штаммов V. vulnificus ферментируют лактозу.
Для лечения используют антимикробные препараты (гентамицин, тетрациклин, левомицетин).
14.1. Возбудитель сибирской язвы
Сибирская язва - острая бактериальная зоонозная особо опасная инфекция, характеризуется выраженной интоксикацией, серозно-геморрагическим воспалением кожи, лимфатических узлов, внутренних органов.
Заболевание приобрело название «сибирская язва» из-за широкого распространения в Сибири. В чистой культуре возбудитель был выделен в 1876 г. Р. Кохом. Название вида произошло от греческого anthrax (уголь) по виду карбункула - гнойного черного очага в коже.
Таксономия. Семейство Bacillaceae, род Bacillus, вид Bacillus anthracis.
Общие свойства
Морфологические. Крупные неподвижные грамположительные палочки, располагаются цепочками, окруженными общей капсулой. В неблагоприятных условиях вне организма образуют споры, которые чаще располагаются центрально.
Культуральные. Неприхотливы к питательным средам, факультативные анаэробы. На плотных средах растут в виде крупных шероховатых R-форм колоний.
Под микроскопом колонии напоминают «львиную гриву» или «голову медузы», имеют волокнистое строение. Могут диссоциировать на S- (гладкие, авирулентные), М- (слизистые) и SM- (смешанные) колонии. При росте на жидких средах образуют осадок, напоминающий «комочки ваты».
Биохимические. Разлагают глюкозу, фруктозу, мальтозу, декстрин до кислоты, не разлагают лактозу, маннит и дульцит. Гидролизуют крахмал. Выделяют лецитиназу. Молоко свертывают на 3-5 сутки. Белки разлагают до аммиака, желатин разжижают в виде елочки, перевернутой вниз верхушкой.
На средах с пенициллином образуют протопласты-шары в виде цепочки - феномен «жемчужного ожерелья», выявляемый при микроскопии.
Антигены: соматический - представляет собой полисахарид клеточной стенки, состоит из D-галактозы и N-ацетилглюкозамина; капсульный - полипептид D-глутаминовой кислоты, протективный (антигенный комплекс, обладающий высокой иммуногенностью).
Факторы патогенности. Основным фактором патогенности является токсин, который состоит из трех компонентов. Синтез токсина кодируется плазмидой pXO1. В плазмиду входят ген суа, определяющий синтез отечного фактора (ОФ); ген раg, кодирующий протективный антиген (ПА); ген lef, кодирующий синтез летального фактора (ЛФ).
Эти факторы действуют одновременно. ОФ является аденилатциклазой и катализирует накопление в клетках цАМФ, что вызывает повышение проницаемости сосудов. ПА индуцирует синтез защитных антител. ЛФ вызывает смерть животных.
Капсула защищает возбудителя от фагоцитоза и действия антител.
Характеристика заболевания
Источник инфекции - больные животные, выделяющие возбудителя с мочой, испражнениями. Споры возбудителя могут сохраняться длительное время в почве (десятки лет), в меховых и кожаных изделиях.
Пути передачи: контактный - прямой контакт с больными животными или с изделиями из шерсти, кожи, щетины; алиментарный - через мясо от больных животных или продукты, инфицированные в процессе хранения; трансмиссивный - через кровососущих насекомых (слепни, мухи-жигалки); воздушно - пылевой.
В зависимости от места проникновения возбудителя, его вирулентности и восприимчивости организма у человека может быть 3 клинических формы сибирской язвы:
Кожная форма. У входных ворот возбудителя появляется красное пятно, переходящее в папулу медно-красного цвета, зуд. Папула переходит в везикулу с серозным, затем геморрагическим содержимым. Образуется карбункул с черным струпом, присоединяется отек, интоксикация. Прогноз при своевременном лечении благоприятный.
Легочная форма. Развивается при попадании возбудителя или его спор через верхние дыхательные пути. Появляются катаральные явления со стороны верхних дыхательных путей, слезотечение, подъем температуры до 40 0 С, развивается пневмония, часто сменяющаяся отеком легких, в мокроте появляется кровь. Высокая летальность.
Абдоминальная (кишечная) форма. Развивается при алиментарном пути заражения. Характерными признаками являются лихорадка, озноб, рвота, диарея с кровью, боли в животе, на коже геморрагии. Смерть через 3-5 дней от начала заболевания.
Иммунитет стойкий, клеточный и гуморальный. В течение болезни развивается специфическая сенсибилизация, выявляется ПЧЗТ.
Патогенные для человека вибрионы, не относящиеся к виду V. cholerae
К роду Vibrio относится более 25 видов, из которых помимо V. cholerae по крайней мере следующие восемь способны вызывать заболевания у людей: V. parahaemolyticus, V. alginolyticus, V. vulnificus, V. fluvialis, V. furnissii, V. mimicus, V. damsela и V. hollisae. Признаки, по которым они различаются между собой, представлены в табл. 42. Все эти вибрионы являются обитателями морей и заливов. Заражение ими происходит либо при купании, либо при употреблении в пищу продуктов морского происхождения. Как выяснилось, холерные и нехолерные вибрионы могут вызывать не только гастроэнтериты, но и раневые инфекции. Эта способность обнаружена у V. cholerae O1- и не О1-групп, у V. parahaemolyticus, V. alginolyticus, V. mimicus,
Дифференциальные признаки патогенных видов рода Vibrio
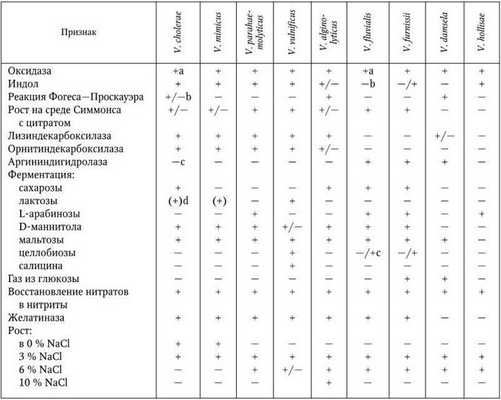
Примечание. +a - более чем 90 % штаммов позитивны; +/ - b - преобладающие реакции указаны в числителе; +c - более чем 90 % штаммов позитивны; - c - более чем 90 % штаммов негативны; (+)d - положительная реакция происходит в течение 3 дней.
V. damsela и V. vulnificus. Они вызывают воспалительные процессы в мягких тканях при повреждении их панцирем морских животных или при прямом контакте с инфицированной морской водой.
Из числа перечисленных патогенных нехолерных вибрионов наибольший практический интерес представляют V. parahaemolyticus, V. alginolyticus, V. vulnificus и V. fluvialis.
V. parahaemolyticus - парагемолитический вибрион - впервые был выделен в Японии в 1950 г. во время большой вспышки пищевой токсикоинфекции, вызванной употреблением полувысушенных сардин (летальность составила 7,5 %). Принадлежность возбудителя к роду Vibrio была установлена Р. Саказаки в 1963 г. Он разделил изученные штаммы на 2 вида: V. parahaemolyticus и V. alginolyticus. Оба вида обнаруживаются в прибрежной морской воде и у ее обитателей, они являются галофилами (греч. hals - соль); в отличие от обычных вибрионов, галофильные не растут на средах без NaCl и хорошо размножаются при высоких концентрациях ее. Видовую принадлежность галофильных вибрионов определяют по их способности ферментировать сахарозу, образовывать ацетилметилкарбинол, размножаться в ПВ с 10 % NaCl. Все эти признаки присущи виду V. alginolyticus, но отсутствуют у V. parahaemolyticus.
Парагемолитический вибрион имеет три типа антигенов: термолабильные жгутиковые Н-антигены, термостабильные, не разрушающиеся при нагревании до 120 °C в течение 2 ч О-антигены и поверхностные К-антигены, разрушающиеся при нагревании. Свежевыделенные культуры V. parahaemolyticus имеют хорошо выраженные К-антигены, которые предохраняют живые вибрионы от агглютинации гомологичными О-сыворотками. Н-антигены у всех штаммов одинаковы, но Н-антигены монотрихов отличаются от Н-антигенов перитрихов. По О-антигену V. parahaemolyticus разделяют на 14 серогрупп. Внутри серогрупп вибрионы подразделяют на серотипы по К-антигенам, общее количество которых составляет 61. Антигенная схема V. parahaemolyticus разработана применительно только к его штаммам, выделяемым от людей.
Патогенность V. parahaemolyticus связана с его способностью синтезировать гемолизин, обладающий энтеротоксическим свойством. Последнее выявляется с помощью метода Канагавы. Сущность его заключается в том, что патогенные для человека V. parahaemolyticus вызывают четкий гемолиз на кровяном агаре, содержащем 7 % NaCl. На кровяном агаре, содержащем менее 5 % NaCl, гемолиз вызывают многие штаммы V. parahaemolyticus, а на кровяном агаре с 7 % NaCl - только штаммы с энтеропатогенными свойствами. Парагемолитический вибрион обнаружен на побережьях Японского, Каспийского, Черного и других морей. Он вызывает пищевые токсикоинфекции и дизентериеподобные заболевания. Заражение происходит при употреблении в пищу сырых или полусырых морских продуктов, инфицированных V. parahaemolyticus (морская рыба, устрицы, ракообразные и т. п.).
Среди выше указанных восьми видов нехолерных вибрионов наиболее патогенным для человека является V. vulnificus, который впервые был описан в 1976 г. как Beneckea vulnificus, а затем в 1980 г. переклассифицирован в Vibrio vulnificus. Он часто обнаруживается в морской воде и ее обитателях и служит причиной различных заболеваний человека. Штаммы V. vulnificus морского и клинического происхождения не отличаются друг от друга ни фенотипически, ни генетически.
Раневые инфекции, вызываемые V. vulnificus, быстро прогрессируют и ведут к образованию опухолей с последующим некрозом ткани, сопровождаются лихорадкой, ознобом, иногда сильными болями, в некоторых случаях требуют ампутации. У V. vulnificus обнаружена способность продуцировать экзотоксин. В опытах на животных установлено, что возбудитель вызывает сильные местные повреждения с развитием отека и некроза ткани с последующим летальным исходом. Роль экзотоксина в патогенезе болезни изучается.
Помимо раневых инфекций, V. vulnificus может вызывать пневмонию у тонувших людей и эндометриты у женщин после пребывания их в морской воде. Наиболее тяжелой формой инфекции, вызываемой V. vulnificus, является первичная септицемия, связанная с употреблением в пищу сырых устриц (возможно, и других морских животных). Это заболевание развивается очень быстро: у больного появляются недомогание, лихорадка, озноб и прострация, затем сильная гипотония, являющаяся главной причиной смерти (летальность около 50 %).
V. fluvialis впервые как возбудитель гастроэнтерита был описан в 1981 г. Он относится к подгруппе нехолерных патогенных вибрионов, у которых есть аргининдигидролаза, но нет орнитин- и лизиндекарбоксилаз (V. fluvialis, V. furnissii, V. damsela, т. е. фенотипически сходных с Aeromonas). V. fluvialis - частый возбудитель гастроэнтеритов, которые сопровождаются сильной рвотой, поносом, абдоминальными болями, повышением температуры и сильной или средней тяжести дегидратацией. Главным фактором патогенности является энтеротоксин.
Лабораторная диагностика. Основным методом диагностики заболеваний, вызываемых нехолерными патогенными вибрионами, является бактериологический с использованием таких селективных сред, как TCBS, Мак-Конки и др. Принадлежность выделенной культуры к роду Vibrio определяют на основании ключевых признаков бактерий этого рода. Видовую принадлежность устанавливают с учетом признаков, указанных в табл. 39.
Читайте также:
- Зубные пасты. Методика чистки зубов.
- Заворот толстой кишки
- Связь шейного остеохондроза, ИБС и гипертонической болезни
- Техника наложения анастомоза между поджелудочной железой и тощей кишкой.
- Пищеварение в тонком кишечнике. Секреторная функция тонкой кишки. Бруннеровы железы. Либеркюновы железы. Полостное и мембранное пищеварение.
