Широкоугольные фотографии гемангиомы хориоидеи с четкими контурами
Добавил пользователь Morpheus Обновлено: 22.01.2026
Гемангиома хориоидеи - доброкачественное медленно развивающее сосудистое новообразование, которое чаще локализуется в заднем полюсе глаза и нередко сопровождается развитием экссудативной отслойки сетчатки со снижением зрительных функций. Диагностика и лечение данной патологии представляют большие сложности.
Цель. Разработка щадящей методики лазерного лечения гемангиомы хориоидеи, расположенной в центральных отделах глазного дна с минимизацией повреждения светочувствительных структур сетчатки и зрительного нерва.
Материал и методы. Методы обследования: визометрия, биомикроскопия, офтальмоскопия с помощью бесконтактной и контактной линз, оптическая когерентная томография, эхографическое исследование (В-скан), ангиография с флуоресцеином и индоцианином зеленым, микропериметрия с цветным фотографированием глазного дна.
Суть метода лечения заключается в том, что диод-лазерная ТТТ осуществляется селективно только в фокусах неоваскуляризации, определяемых методом ФАГ или ангиографии с индоцианином зеленым, в ранней артериальной фазе, исключая структуры макулы и зрительного нерва.
Результаты. При селективной лазерной ТТТ очагов неоваскуляризации, выявляемых в ранней артериальной фазе ангиографии, резорбция опухоли с прилеганием отслоенной сетчатки достигнута у всех 6 пациентов за 2-3 сеанса. Острота зрения улучшилось у 4-х и осталась без изменений - у 2-х пациентов.
Заключение. Таким образом, предложенная нами методика позволяет вылечивать больных с ограниченной формой гемангиомы без осложнений, минимизируя повреждения окружающих опухоль структур сетчатки и зрительного нерва, тем самым сохраняя, а иногда улучшая зрительные функции пораженного глаза.
Ключевые слова: гемангиома хориоидеи, транспупиллярная лазерная термотерапия.
Среди доброкачественных сосудистых новообразований хориоидеи особое место занимает ограниченная форма гемангиомы, которая обычно локализуется в заднем полюсе глаза, часто вовлекая центральную зону, что приводит к отеку и вторичной отслойке сетчатки с последующим снижением зрительных функций.
Диагностика данной формы гемангиомы хориоидеи - задача достаточно сложная, поэтому кроме осмотра глазного дна применяются специальные методы: ультразвуковые исследования (В-скан), ангиография с флуоресцеином (ФАГ) и с индоцианином зеленым (ИАГ) и дуплексное сканирование [3, 5, 7-9].
При ФАГ для гемангиомы хориоидеи характерны признаки неравномерной гиперфлуоресценции хориоидальных сосудов до заполнения артерий сетчатки, в ранней артериальной фазе - ретикулярная гиперфлуоресценция, в артериовенозной фазе - увеличение интенсивности окрашивания и в поздней фазе - нарастание мультифокальной флуоресценции. ИАГ позволяет выявить зоны флуоресценции и более четко определить фокальные скопления флуоресцеина в поздней стадии исследования, так называемые «горячие пятна».
Для лечения больных с данной патологией применяются лазеркоагуляция (ЛК), лазерная транспупиллярная термотерапия (ТТТ), брахитерапия, облучение протоновым лучом, а в тяжелых случаях прибегают к хирургическим вмешательствам - витрэктомии с выпусканием субретинальной жидкости и эндолазеркоагуляцией [1, 2, 4, 6, 7, 10].
Лазерное вмешательство преследует цель облитерации кровеносных сосудов опухоли с устранением выпота жидкости в окружающие структуры глаза, предотвращая при этом развитие отслойки сетчатки и витреоретинальных фиброзных изменений. При указанных методах светового или лучевого воздействия на всю поверхность опухоли невозможно обойтись без повреждения структур сетчатки и зрительного нерва в зоне поражения, когда новообразование локализуется в центральных отделах глазного дна. Ретроспективный анализ пролеченных нами 28 пациентов с гемангиомой хориоидеи методом лазеркоагуляции и лазерной ТТТ показал, что, несмотря на полную резорбцию опухоли, в 90% случаев отмечается в разной степени ухудшение зрения в связи с повреждением структур сетчатки и зрительного нерва.
Цель. Разработка щадящей методики лазерной термотерапии сосудистых новообразований хориоидеи, расположенных в центральных отделах глазного дна с минимизацией повреждения светочувствительных структур сетчатки и зрительного нерва.
Материал и методы. Изучена эффективность щадящей лазерной ТТТ при лечении 6 больных (6 глаз) с ограниченной формой гемангиомы хориоидеи в парамакулярной и юкстапапиллярной зонах.
Методы обследования: визометрия, биомикроскопия, офтальмоскопия с помощью бесконтактной и контактной линз, оптическая когерентная томография, эхографическое исследование (В-скан), ангиография с флуоресцеином и индоцианином зеленым, микропериметрия с цветным фотографированием глазного дна. Для ТТТ при гемангиоме хориоидеи мы использовали диод-лазерные офтальмологические установки: Nidek-3300 (810 nm) и Iridex-IQ (577 nm). Суть метода лечения заключается в том, что диод-лазерная ТТТ осуществляется селективно только в фокусах неоваскуляризации, определяемых методом ФАГ или ангиографии с индоцианином зеленым, в ранней артериальной фазе, исключая структуры макулы и зрительного нерва (рис. 1). В связи с тем, что гемангиома хориоидеи - опухоль доброкачественная и нет необходимости лечения ее в пределах здоровых тканей, достаточно селективное лазерное воздействие на фокусы патологической неоваскуляризации хориоидеи, оберегая светочувствительные и светопроводящие структуры окружающих тканей. При остаточной опухоли после первого сеанса лечения проводятся повторные сеансы лазерного воздействия строго в зонах роста хориоидальных сосудов. Применяемые нами лазерное излучение длиной волны 810 и 577 нм, в отличие от 514-532 нм, проникает глубже и почти не поглощается структурами сетчатки на поверхности опухоли.
Результаты. При селективной лазерной ТТТ очагов неоваскуляризации, выявляемых в ранней артериальной фазе ангиографии, резорбция опухоли с прилеганием отслоенной сетчатки достигнута у всех 6 пациентов за 2-3 сеанса. Острота зрения улучшилась у 4-х и осталась без изменений - у 2-х пациентов (рис. 2). При микропериметрии световая чувствительность в центральной зоне сетчатки улучшилась у 2-х пациентов, сохранилась без перемен у 3-х и ухудшилась у 1-го пациента.
Широкоугольные фотографии гемангиомы хориоидеи с четкими контурами
ФГБУ "НИИ глазных болезней" РАМН, Москва
ФГБУ "НИИ глазных болезней" РАМН, Москва;
ГБОУ ВПО "Первый Московский государственный медицинский университет им. И.М. Сеченова" Минздрава РФ
Диффузная гемангиома хориоидеи как проявление синдрома Sturge—Weber (клинический случай)
Журнал: Вестник офтальмологии. 2019;135(6): 108‑116
Энцефалотригеминальный ангиоматоз, или синдром Sturge—Weber — врожденное, спорадически возникающее заболевание, характеризующееся ангиоматозом сосудов мозговых оболочек, капилляров лица и глаз. В статье описан клинический случай, демонстрирующий сочетание односторонней кожной ангиомы с ангиоматозом конъюнктивы и диффузной гемангиомой хориоидеи на ипсилатеральной стороне без признаков нарушения офтальмотонуса. Интерес данного клинического случая обусловлен тем, что имеет место разновременное появление клинических признаков синдрома Sturge—Weber. Кожная ангиома у пациентки была с рождения, ангиома конъюнктивы появилась в возрасте 45 лет, тогда же у нее появился гиперметропический сдвиг рефракции, что может быть первым проявлением диффузной гемангиомы хориоидеи.
Энцефалотригеминальный ангиоматоз, или синдром Sturge—Weber — врожденное, спорадически возникающее заболевание, характеризующееся ангиоматозом сосудов мозговых оболочек, капилляров лица и глаз. Синдром Sturge—Weber, относится к группе наследственно дегенеративных заболеваний — факоматозам, или нейрокожным синдромам.
Факоматозы — группа наследственных заболеваний, при которых наблюдается сочетание поражений нервной системы, кожных покровов, глаз и внутренних органов. К наиболее распространенным факоматозам с поражением нервной системы относятся: нейрофиброматоз (тип 1: NF 1; тип 2: NF 2); туберозный склероз (болезнь Pringle—Bourneville); цереброретино-висцеральный ангиоматоз (болезнь Hippel—Lindau); энцефалотригеминальный ангиоматоз (синдром Sturge—Weber) [1].
Заболеваемость синдромом Sturge—Weber составляет 1 на 50 000, одинаково часто у мужчин и женщин. В отличие от большинства факоматозов, синдром Sturge—Weber является спорадическим без определенного наследственного маркера, который было бы возможно идентифицировать [2]. Ассоциированный ген мутации был выявлен в нуклеотидном переходе GNAQ хромосомы 9q21 [3]. Данный синдром обычно сочетает в себе кожный ангиоматоз на лице (чаще располагающийся на одной половине лица вдоль первой и второй ветвей тройничного нерва), ипсилатеральный лептоменингеальный ангиоматоз и поражение глаза [4—6]. Кожный ангиоматоз может быть врожденным или развиваться в раннем детстве. Окраска очагов в грудном возрасте розовая, затем становится синюшно-красной. Поражение, как правило, одностороннее, реже встречается двусторонний характер. Ангиомы формируются из остатков сосудистого сплетения, которое остается в области головной части нервной трубки, что обусловлено нарушением нормального эмбрионального развития на 6—9-й неделе. Триада симптомов (ангиомы кожи лица, органа зрения, головного мозга) выявляется в 1/5 случаев синдрома Sturge—Weber. В остальных случаях характерно моносимптомное проявление. Также в литературе описано сочетание односторонней гемангиомы кожи с двусторонней диффузной гемангиомой хориоидеи [7]. Реже синдром Sturge—Weber сочетается с окулодермальным меланозом (преимущественно у азиатов) [4].
Согласно классификации, предложенной А. Roach [4], выделяют 3 типа данного заболевания: тип 1 — гемангиома лица в сочетании с лептоменингеальной гемангиомой в сочетании с глаукомой или без нее; тип 2 — гемангиома лица в сочетании с глаукомой или без нее; тип 3 — лептоменингеальная гемангиома в сочетании с глаукомой или без нее.
Ангиоматоз лица может также захватывать веки и конъюнктиву. В 53% случаев на ипсилатеральной стороне выявляют диффузную гемангиому хориоидеи (дГХ), которая в 50—70% случаев сочетается с глаукомой [4, 8, 9]. Частыми симптомами дГХ являются отслойка сетчатки и вторичная глаукома [10, 11]. Риск развития вторичной глаукомы выше при вовлечении в патологический процесс кожи верхнего века [9]. Вторичная глаукома может развиться как на фоне повышения давления в эписклеральных венах [12], так и на фоне нарушения строения угла передней камеры (УПК) [10, 12]. С развитием вторичной глаукомы ассоциируют такие изменения переднего отрезка, как периферические передние синехии, гетерохромия радужки, расширение сосудов радужки [10].
При осмотре дГХ в первую очередь проявляется ярко-красным свечением зрачка в отличие от здорового глаза. При офтальмоскопии видно диффузное красно-оранжевое окрашивание хориоидеи на большом протяжении в постэкваториальной зоне, по сравнению с парной стороной [4, 12, 13]. Данное состояние чаще протекает бессимптомно, однако осложнения — субретинальное кровоизлияние и тотальная отслойка сетчатки — могут привести к потере зрения [5, 6, 13]. В некоторых случаях первым проявлением дГХ может быть гиперметропический сдвиг рефракции [14].
Гистологически дГХ обычно представлена смешанной формой — состоит из резко расширенных мелких сосудов, стенки которых выстланы одним слоем эндотелия. Границы у дГХ отсутствуют — она плавно переходит в нормальную хориоидею [11].
При проведении оптической когерентной томографии (ОКТ) за счет выраженного утолщения хориоидеи не всегда удается визуализировать склеро-хориоидальное сочленение [4, 5, 8]. Выявляют истончение наружных слоев сетчатки, локальные участки повреждения РПЭ-фоторецепторного слоя (включая РПЭ, промежуточную, элипсоидную и миоидную зоны) [5]. В ходе ОКТ-ангиографии могут быть выявлены хориоидальные сосуды, расположенные в форме мелких нитей [15].
Клинический случай
Пациентка К. 47 лет обратилась в ФГБНУ «НИИГБ» с жалобами на снижение зрения и покраснение левого глаза в течение двух лет.
Из анамнеза известно, что у пациентки с рождения имелось пятно ярко-розового цвета в области век, лба и ската носа слева. В детстве был поставлен диагноз: «диффузная гемангиома кожи левой верхней половины лица», лечение не проводили. В течение жизни пятно незначительно побледнело, потемнело и приобрело синюшный оттенок. Восемь лет назад пациентке было проведено несколько курсов лазерного лечения, на фоне которого отмечена выраженная положительная динамика в виде побледнения пятна и некоторого сокращения его площади. Два года назад пациентка заметила покраснение левого глаза, которое не зависело от каких-либо внешних факторов и не менялось в течение всего этого времени. Тогда же пациентка заметила снижение зрения левого глаза.
Объективно: Vis OD=1,0; Vis OS=0,6 sph+2,5 cyl-1,5 ax 86=1,0.
ВГД OD=15,3 мм рт.ст.; OS=12,7 мм рт.ст.
Периметрия обоих глаз — без патологических изменений.
При осмотре отмечается слабо заметное бледно-розовое окрашивание кожи в области век, ската носа и вокруг брови слева (пациентка не дала согласие на публикацию фотографий лица). При ближайшем рассмотрении визуализируются расширенные мелкие поверхностные сосуды в области изменения цвета кожи.
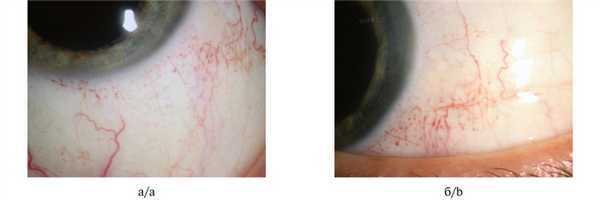
При биомикроскопии во всех отделах бульбарной конъюнктивы выявлены сосудистые изменения по типу диффузно расположенных расширенных капилляров ярко-красного цвета (рис. 1). Рис. 1. Фотография конъюнктивы левого глаза. а — при взгляде вверх; б — при взгляде вправо. Четко видны сосудистые изменения во всех отделах. Патологических изменений радужки и хрусталика не обнаружено.
При гониоскопии обоих глаз — угол передней камеры (УПК) открыт во всех отделах, патологических структур не выявлено.
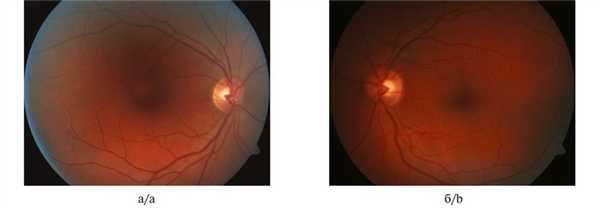
При офтальмоскопии: очаговой патологии на глазном дне обоих глаз выявлено не было, однако отмечено темно-красное окрашивание глазного дна левого глаза по сравнению с правым (рис. 2). Рис. 2. Фотография глазного дна правого (а) и левого (б) глаза.
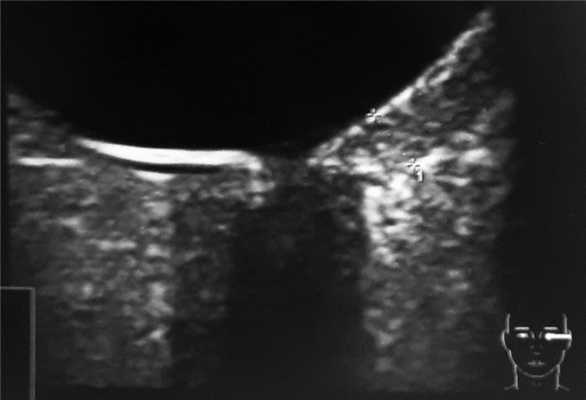
По данным ультразвукового исследования левого глаза выявлено диффузное (преимущественно в верхненаружной половине) утолщение хориоидеи до 2,2 мм по сравнению с правым (рис. 3), Рис. 3. Результаты ультразвукового исследования левого глаза. что обусловливало укорочение переднезадней оси (ПЗО) левого глаза, и, с нашей точки зрения, явилось причиной гиперметропического сдвига рефракции.
Пациентке была проведена ОКТ, в том числе в режиме EDI, и ОКТ-ангиография (OCT Spectralis, Heidelberg Engineering, Германия).
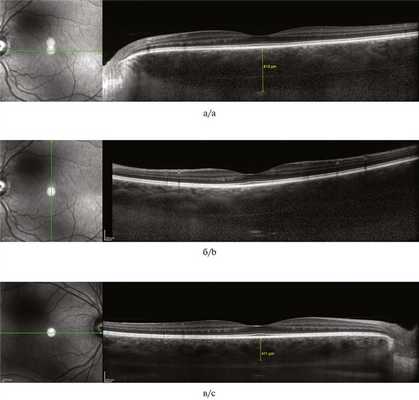
Визуализация склеро-хориоидального сочленения на левом глазу была возможна только в режиме исследования в глубине тканей (EDI). Было выявлено расширение хориоидеи до 815 мкм субфовеолярно и 872 мкм парафовеолярно снаружи в первую очередь за счет расширения наружных слоев хориоидеи. Данные изменения в большей степени были выражены кверху от фовеа (рис. 4, а, Рис. 4. Результат ОКТ. Срезы через фовеа: левого глаза — горизонтальный (а), вертикальный (б); правого глаза — горизонтальный (в). б).
Толщина хориоидеи на правом глазу также превышала нормальные значения для данной возрастной группы, однако ее структура изменена не была (см. рис. 4, в).
В режиме ОКТ-ангио выявлено изменение структуры хориоидеи выше фовеа — отмечено уменьшение плотности хориокапилляров и крупных сосудов хориоидеи (рис. 5). Рис. 5. Результат ОКТ-ангиографии. Срез на уровне хориокапилляров через фовеа правого (а) и левого (б) глаза. Зона обеднения сосудистого рисунка указана стрелками.
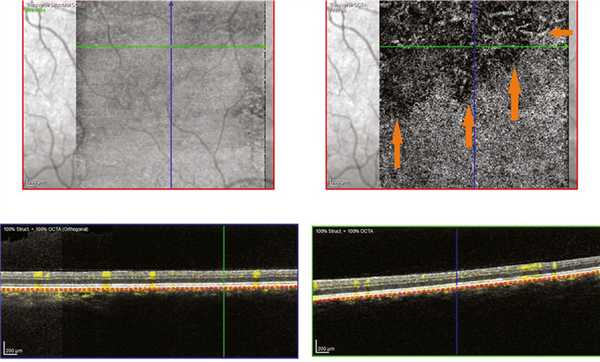
Аналогичная картина отмечена и в парафовеолярной зоне — в верхней половине выявлено обеднение хориоидального сосудистого рисунка на уровне хориокапилляров, что, с нашей точки зрения, может свидетельствовать о замедлении кровотока в расширенных сосудах хориоидеи (рис. 6). Рис. 6. Результат ОКТ-ангиографии левого глаза. Срез на уровне хориокапилляров парафовеолярно сверху. Зона обеднения сосудистого рисунка указана стрелками.
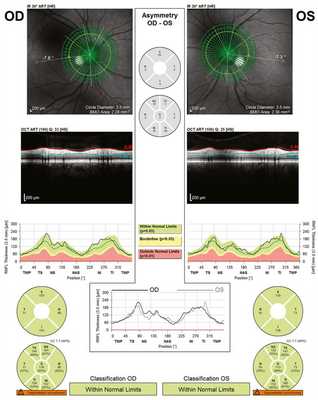
При проведении ОКТ диска зрительного нерва (ДЗН) изменения толщины перипапиллярного слоя нервных волокон сетчатки выявлено не было (рис. 7). Рис. 7. Результат ОКТ-исследования перипапиллярного слоя нервных волокон сетчатки.
Представленный клинический случай демонстрирует сочетание односторонней кожной ангиомы с ангиоматозом конъюнктивы и диффузной гемангиомой хориоидеи на ипсилатеральной стороне без признаков нарушения офтальмотонуса. Интерес данного клинического случая обусловлен тем, что имеет место разновременное появление клинических признаков синдрома Sturge—Weber.
Кожная ангиома была у пациентки с рождения, ангиома конъюнктивы появилась в возрасте 45 лет, тогда же у нее появился гиперметропический сдвиг рефракции, что, с нашей точки зрения, могло стать первым проявлением диффузной гемангиомы хориоидеи.
На момент обследования признаков повышения офтальмотонуса выявлено не было, однако, учитывая разновременное появление клинических симптомов, пациентка нуждается в дальнейшем динамическом наблюдении.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Сведения об авторах
ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздрава России, Москва
ФГБУ "Научно-исследовательский институт глазных болезней" РАМН, Москва
ГОУ ДПО РМАПО Минздрава России, ул. Баррикадная, 2/1, Москва, Российская Федерация, 125993
Гемангиома хориоидеи и возможности ее уточненной диагностики
Журнал: Вестник офтальмологии. 2016;132(4): 10‑19
Цель - выявить возможности оптической когерентной томографии (ОКТ) в уточненной диагностике гемангиомы хориоидеи (ГХ). Материал и методы. Обследованы 27 больных (22 женщины, 5 мужчин) с монолатеральной ГХ. Возраст на момент постановки диагноза составлял 30-76 лет (в среднем 53,7±5,29 года). Толщина опухолевого узла варьировала в пределах 0,9-5,3 мм (2,17±0,41 мм; медиана 1,9 мм), диаметр основания - 2,64-13,86 мм (медиана 7,7 мм). Результаты. Оценивая ОКТ-симптоматику ГХ, можно сказать, что нарушение архитектоники сетчатки, в том числе ее кистозная дистрофия, возникают при проминенции опухоли более 1,8 мм, а отек сетчатки - чаще при ее бо́льшей толщине. Следует отметить, что появившиеся морфофункциональные изменения в сетчатке при ГХ прогрессируют крайне медленно. При исследовании аутофлюоресценции опухоль была представлена участком обширной гипоаутофлюоресценции различной интенсивности. Локальный фиброз, гиперплазия и атрофия ретинального пигментного эпителия (PПЭ) также представлены зонами гипоаутофлюоресценции. Участки гипераутофлюоресценции соответствовали зонам скопления липофусцина. Вокруг самого узла опухоли в двух случаях наблюдали обширные зоны умеренной гипераутофлюоресценции за счет наличия свежей субретинальной жидкости с повреждением фоторецепторного слоя; точечные участки гипоаутофлюоресценции в этих зонах, по данным ОКТ, соответствовали участкам атрофии РПЭ. Заключение. Офтальмоскопическая картина ГХ представляет определенные трудности в уточненной диагностике. Наряду с получившей широкое распространение флюоресцентной ангиографией, современные методы диагностики, такие как спектральная ОКТ (в том числе в режиме углубленного сканирования с выявлением хориоидальных признаков), а также исследование аутофлюоресценции в режиме MultiColor позволяют уточнить диагноз гемангиомы.
Гемангиома хориоидеи (ГХ) - представитель группы гамартом, чаще представлена в виде отграниченного новообразования, реже - в виде диффузной формы, которая, как правило, сочетается с синдромом Стюрж-Вебера. Опухоль характеризуется торпидным течением, первые симптомы роста отграниченной ГХ возникают на 4-5-м десятилетии жизни. Клиническая картина ее многократно описана в литературе 1. Главная отличительная особенность - оранжево-красный или оранжево-желтый цвет опухоли. В то же время J. Gass в 1974 г. описал ГХ аспидно-серого цвета и объяснил это гиперплазией надлежащего ретинального пигментного эпителия (РПЭ). Такие случаи и делают трудной дифференциальную диагностику ГХ с другими опухолями и в первую очередь с меланомой хориоидеи.
Жалобы на зрительные расстройства при ГХ длительное время отсутствуют. Появление их связано с развивающимися изменениями в надлежащей сетчатке 4.
С целью уточнения диагноза ГХ достаточно широко используют флюоресцентную ангиографию (ФАГ), особенно с индоцианином зеленым [6], а также метод аутофлюоресценции (АФ) [7, 8].
Приводимые в литературе сведения о диагностической возможности визуализирующих методов исследования порой противоречивы, основное внимание уделено состоянию надлежащей сетчатки. Появление современных спектральных томографов, в том числе с функцией получения изображения в глубине тканей (EDI-OCT), позволило проводить более глубокое сканирование с оценкой хориоидального слоя [12]. При использовании EDI-OCT отграниченные гемангиомы выглядят как гипо- или среднерефлективные полосы с гомогенным сигналом и внутренними полостями. Они могут отличаться от нормальной окружающей хориоидеи, но их наружная граница может быть визуализирована только при толщине опухоли до 0,9 мм [6, 9].
Цель исследования - выявить возможности ОКТ в уточненной диагностике ГХ.
Материал и методы
Обследованы 27 больных (22 женщины, 5 мужчин) с монолатеральной Г.Х. Возраст на момент постановки диагноза составлял 30-76 лет (в среднем 53,7±5,29 года). У 10 пациентов исследование проводили в течение первого года после появления жалоб, у 4 человек - через 1,5-3 года, у 4 пациентов - через 3-8 лет, у 8 больных - через 9 лет и более (максимальный срок 16 лет). В одном случае ГХ была выявлена на амблиопичном глазу. В правом глазу ГХ диагностирована у 14 пациентов, в левом - у 13. Локализация во всех наблюдениях была ограничена задним полюсом глаза, в том числе макулярной (6 глаз) и парамакулярной (6 глаз) зоной. Толщина опухолевого узла варьировала в пределах 0,9-5,3 мм (2,17±0,41 мм, медиана 1,9 мм), диаметр основания - 2,64-13,86 мм (медиана 7,7 мм).
Всем пациентам проведены биомикроофтальмоскопия, цифровая фоторегистрация глазного дна, ультразвуковое исследование (УЗИ), ФАГ, ОКТ. Фоторегистрация глазного дна в режиме MultiColor (МС) выполнена у 7 больных, АФ - у 6. Повторно в процессе динамического наблюдения ОКТ проведена у 10 больных, из них у 3 - трехкратно (табл. 1).

Таблица 1. Временные параметры повторных исследований Примечание. * - амблиопия, скорее всего, обусловлена макулярной локализацией ГХ.
С целью выявления влияния толщины ГХ на состояние надлежащей сетчатки все опухоли были подразделены на группы с учетом ее толщины (табл. 2).
Таблица 2. Распределение глаз с учетом проминенции ГХ
ОКТ в стандартном режиме и в режиме получения изображения в глубине тканей (EDI-OCT), исследование АФ в режиме BluePeak и исследование в режиме MultiColor выполняли на приборе OCT Spectralis («Heydelberg Engineering», Германия), ФАГ - на фундус-камере FF 450 plus («Carl Zeiss», Германия). Фоторегистрацию глазного дна проводили во время ангиографии, а также с помощью фундус-камеры TRC-NW300 («Topcon», Япония). Ультразвуковые исследования выполнены на приборе UD 600 («Tomey», Япония).
Статистическую обработку результатов проводили с помощью Microsoft Excel 2007.
Результаты и обсуждение
Анализ томограмм начинали с оценки хориоидеи. Во всех случаях профиль хориоидеи проминировал в сторону надлежащей сетчатки, его величина не всегда совпадала с толщиной ГХ, уточненной по данным ультразвуковой биометрии хориоидальной зоны. Подобное несовпадение мы наблюдали при исследовании 6 глаз. В 4 случаях ГХ выявлена случайно, и, по данным УЗИ, высота ее варьировала от 1 до 2,33 мм, в то время как высота хориоидального профиля в зоне интереса по данным ОКТ оказалась в 2 раза меньше. Как свидетельствуют данные ОКТ, разница показателей обусловлена отслойкой нейроэпителия (ОНЭ) и интраретинальным отеком. Необходимо отметить, что при толщине ГХ более 2 мм (по данным ультразвуковой биометрии хориоидальной зоны) достоверно измерить толщину опухоли по ОКТ не представляется возможным.
При морфобиометрии хориоидального комплекса (зона интереса) следует помнить, что возможны отклонения от истинных границ ГХ, так как оптически плотные образования (рубцы, кровоизлияния, экссудат, сосуды) препятствуют прохождению световых лучей и визуализации глубжележащих структур [13].
В 8 наблюдениях (толщина ГХ 1-3,15 мм) в зоне интереса визуализировали ампулообразное утолщение хориоидеи с «выстоянием» в сторону склеры (рис. 1). Полосу склеры в проекции максимальной толщины ГХ удалось зафиксировать в 3 случаях (толщина опухоли 1; 1,25 и 1,3 мм) (см. рис. 1). При анализе томограмм в режиме оттенков серого в зоне патологического очага у 25 пациентов, независимо от высоты ГХ, практически сразу выявили очертания относительно крупных сосудов под мембраной Бруха, диаметр их просвета варьировал от 65 до 559 мкм, (рис. 2). Следует отметить, что в зоне максимальной проминенции ГХ имели место сосуды меньшего диаметра, а по периферии опухоли - сосуды большего диаметра.
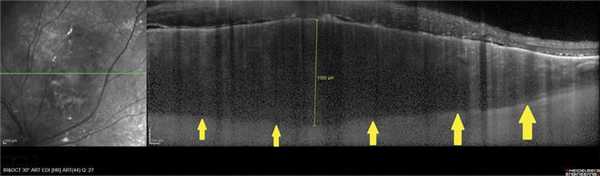
Рис. 1. ОКТ-горизонтальный срез через ГХ в зоне ее максимальной проминенции. Ампулообразное расширение хориоидеи (полоса склеры указана стрелками).
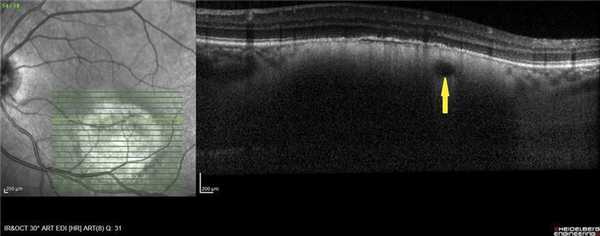
Рис. 2. ОКТ-горизонтальный срез. Крупный сосуд в толще ГХ (указан стрелкой).
Между мембраной Бруха и патологическим очагом в 9 случаях была видна гипорефлективная линия, разделяющая базальную мембрану и Г.Х. Эту полосу «самоотграничения» зафиксировали преимущественно при высоте опухоли до 1,9 мм (6 глаз) (рис. 3). В 3 случаях проминенция составляла 2,3; 3 и 4 мм. Не исключено, что она соответствует пространству между мембраной Бруха и псевдокапсулой гемангиомы, которую практически всегда находят при гемангиомах орбиты.
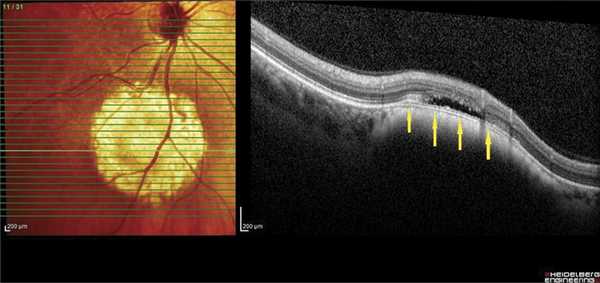
Рис. 3. ОКТ-горизонтальный срез. Зона «самоотграничения» ГХ (указана стрелками).

Рис. 4. ОКТ-горизонтальный срез. Уплощенная неровная поверхность ГХ, гиперрефлективная зона - фиброваскулярный рубец (отмечена звездочкой).
В 23 случаях поверхность РПЭ была неровной за счет его неравномерной гиперплазии, у 2 пациентов РПЭ имел вид «облысевшего» в результате его атрофии (длительность наблюдений 3 и 10 лет). У 7 пациентов при минимальной толщине ГХ 1 мм и максимальной 3,45 мм наряду с гиперрефлективностью РПЭ выявлены друзы, что проявляется на ОКТ неравномерной рефлективностью и отложением депозитов по РПЭ.
В 15 глазах были выявлены гиперрефлективные зоны (см. рис. 4), которые могут быть расценены как организовавшиеся субретинальные кровоизлияния или фиброваскулярные рубцы. Размер этих зон увеличивался по мере удлинения сроков заболевания. Таким образом, изменения РПЭ, расположенного на мембране Бруха, носили вторичный характер. Отслойка РПЭ зафиксирована у 8 пациентов (при толщине ГХ от 1 до 3,15 мм). При исследовании больных в динамике в сроки от 3 до 11 мес существенных изменений в РПЭ не выявлено.
ОНЭ с отеком и дезорганизацией дисков наружных фоторецепторов в макулярной зоне выявлена у 12 больных с ГХ со снижением зрения до 0,02-0,8, проминенцией опухоли 1-4,05 мм и анамнезом заболевания от 1 мес до 15 лет. Наиболее выраженное снижение зрения (до сотых) отмечали в случаях пара- и макулярного расположения ГХ и длительности анамнеза более 10 лет (рис. 5, а), минимальное снижение остроты зрения (до 0,6-0,8) - при длительности анамнеза до 1 года (см. рис. 5, б).
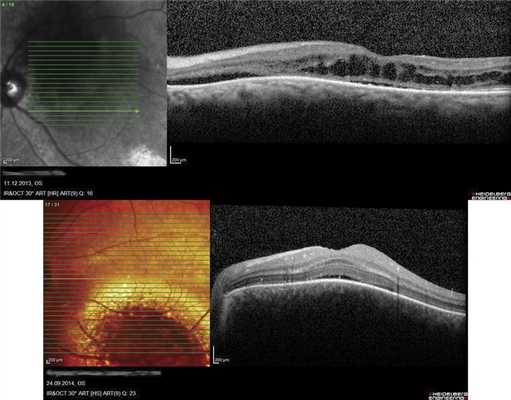
Рис. 5. ОКТ-горизонтальный срез через макулярную зону. а - пациентки Е., Vis OS =0,02, длительность анамнеза 11 лет (ОНЭ, кистозные изменения в макулярной зоне с разрушением фоторецепторов); б - пациентки С., Vis OS =0,7-0,8, длительность анамнеза 6 мес (отечность наружных сегментов фоторецепторов).
В 8 случаях выявили распространенную зону ОНЭ с дезорганизацией фоторецепторного слоя «на протяжении» от очага (рис. 6, а). В 2 случаях при анамнезе более 15 лет были выявлены зоны разрушения слоя фоторецепторов и наружных слоев сетчатки, соответствующие зонам ранее существовавшей ОНЭ (см. рис. 6, б).
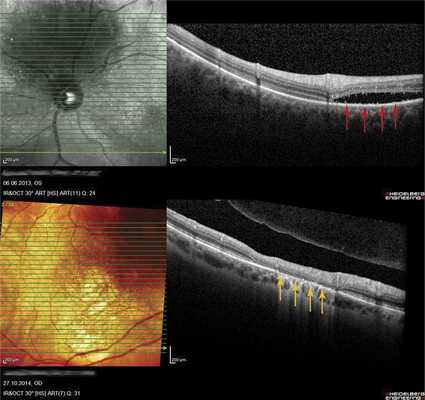
Рис. 6. ОКТ-горизонтальный срез «на протяжении» от ГХ. а - пациентки Х., длительность анамнеза 3,5 года (красными стрелками указана зона ОНЭ); б - пациентки К., длительность анамнеза 15 лет (желтыми стрелками указана зона разрушения слоя фоторецепторов и наружных слоев сетчатки на месте ранее существовавшей ОНЭ, атрофия РПЭ).
Следует отметить, что появившиеся морфофункциональные изменения в сетчатке при ГХ прогрессируют крайне медленно, что мы имели возможность подтвердить у 8 больных при повторных ОКТ с интервалами от 3 до 25 мес. Этот факт важен при планировании лечения больных с достаточно хорошим зрительным прогнозом. Ранние изменения в сенсорной части сетчатки (при анамнезе 3 мес) находили и другие авторы [10].
Оценивая ОКТ-симптоматику ГХ, можно сказать, что нарушение архитектоники сетчатки, в том числе ее кистозная дистрофия, возникают при проминенции опухоли более 1,8 мм, а отек сетчатки - чаще при ее бо́льшей толщине [15]. В то же время имеются сведения, что куполообразная элевация хориоидеи с фокальной гиперплазией надлежащего РПЭ может сочетаться с серозной отслойкой сетчатки над опухолью и сохранной архитектоникой сетчатки, нормальным слоем фоторецепторов и отсутствием интраретинального отека [9, 16], что расценивают как отражение остроты процесса [6].
Как показывают наши наблюдения, ГХ может быть подвержена саморегрессии. Мы имели возможность наблюдать больную 66 лет, у которой в 2005 г. была выявлена ГХ проминенцией 5,5 мм (рис. 7, а). Больная отказалась от лечения и находилась под наблюдением. При контрольном исследовании спустя 9 лет по данным ОКТ и УЗИ отмечено уменьшение толщины ГХ до 1,2 мм (см. рис. 7, б-г). Очаг, по данным ОКТ, «выстоял» в сторону склеры, куполообразная проминенция в сторону сетчатки отсутствовала. Аналогичный случай описан M. Munteanu и соавт. в 2013 г. [17].
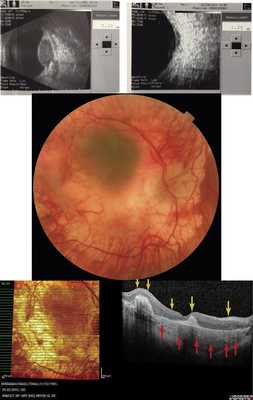
Рис. 7. Офтальмоскопическая картина глазного дна при саморегрессии ГХ (в) и соответствующие данные УЗИ в динамике (а - на момент выявления ГХ; б - при контрольном обследовании через 9 лет) и результат ОКТ (г) (красными стрелками отмечена область изменений в хориоидее, желтыми - в сетчатке).
Аутофлюоресценция исследована у 6 пациентов с ГХ, опухоль была представлена участком обширной гипоаутофлюоресценции различной интенсивности (рис. 8, а), в то время как по ФАГ ей соответствовали зоны гиперфлюоресценции собственных сосудов опухоли и сосудистых лакун (см. рис. 8, б). Локальный фиброз, гиперплазия и атрофия пигментного эпителия также представлены зонами гипоаутофлюоресценции. Участки гипераутофлюоресценции соответствовали зонам скопления липофусцина в виде пятен оранжевого пигмента, описанного J. Gass в 1974 г. Вокруг самого узла опухоли в 2 случаях наблюдали обширные зоны умеренной гипераутофлюоресценции за счет наличия свежей субретинальной жидкости с повреждением фоторецепторного слоя и/или альтерацией РПЭ, выявленными по данным ОКТ, точечные участки гипоаутофлюоресценции в этих зонах, по данным ОКТ, соответствовали участкам атрофии РПЭ (рис. 9).
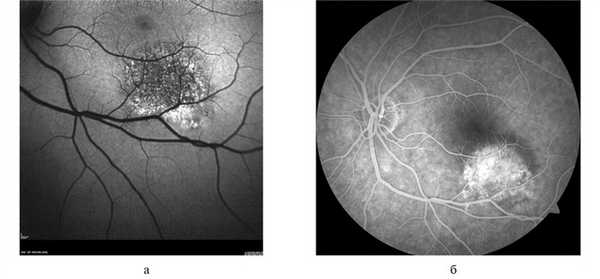
Рис. 8. Картина А.Ф. (а) и ФАГ (б) глазного дна при гемангиоме хориоидеи (объяснения в тексте).
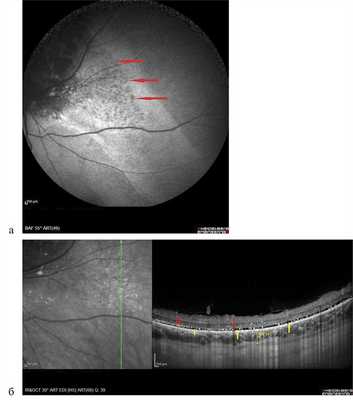
Рис. 9. Картина А.Ф. при гемангиоме хориоидеи и соответствующие данные ОКТ. Вертикальный срез через зону умеренной гипераутофлюоресценции, разрыв слоя фоторецепторов (указан желтыми стрелками, точечный блок АФ в зоне точечной атрофии пигментного эпителия указан красными стрелками).
Исследование глазного дна в режиме MC проведено в 7 случаях. Проанализированы как цветные, так и отдельные изображения, полученные при сканировании каждым из трех лазеров.
В исследованных случаях при получении цветного изображения гемангиомы выглядели в виде проминирующего участка зеленого цвета с четкими границами (рис. 10, б). При этом границы ГХ были представлены четче, чем на цветной фотографии глазного дна (см. рис. 10, а). Следует отметить, что в 5 случаях имели место беспигментные и слабопигментированные гемангиомы. Поля оранжевого пигмента определены во всех случаях. Следует отметить, что на МС липофусцин выглядел именно оранжевым (см. рис. 10, б), в то время как при офтальмоскопии на поверхности беспигментных опухолей он имел коричневую окраску и чаще совсем не выявлялся.
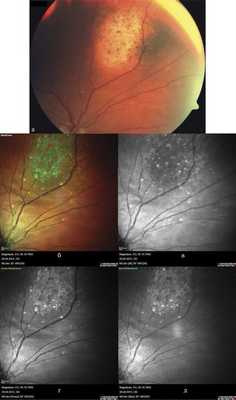
Рис. 10. Офтальмоскопическая картина глазного дна при гемангиоме хориоидеи (а) и соответствующие изображения глазного дна в режиме MultiColor (б), в инфракрасном свете (в), зеленом (г) и синем (д) отраженном свете (объяснения в тексте).
Анализ изображений, полученных отдельно от каждого лазера, показал, что зоны скопления липофусцина выявляются только на инфракрасном изображении, скопления твердого экссудата на поверхности сетчатки - на всех трех изображениях, но наиболее четко - на изображении в зеленом отраженном свете. Также на изображениях в зеленом и синем отраженном свете лучше всего видны участки эпиретинального фиброза (см. рис. 10, в-д).
Заключение
Офтальмоскопическая картина ГХ представляет определенные трудности в уточненной диагностике. Наряду с получившей широкое распространение флюоресцентной ангиографией, современные методы диагностики, такие как спектральная ОКТ (в том числе в режиме углубленного сканирования с выявлением хориоидальных признаков), а также исследование аутофлюоресценции и в режиме MultiColor позволяют уточнить диагноз гемангиомы.
Опухоли хориоидеи
Опухоли хориоидеи - это группа патологических образований сосудистой стенки, которая включает в себя невус, увеальную меланому и гемангиому. В течение длительного промежутка времени клинические симптомы отсутствуют. Снижение остроты зрения и страбизм возникают только при увеличении диаметра новообразования. Диагностика опухолей хориоидеи основывается на проведении офтальмоскопии, визометрии, ФАГ, биомикроскопии, ОКТ, УЗД. В зависимости от формы заболевания тактика лечения сводится к проведению лазерной коагуляции, криотерапии, брахитерапии, фотодинамической терапии, транспупиллярной термотерапии. При отсутствии эффекта или большом размере опухоли хориоидеи показана энуклеация.

Общие сведения
Опухоли хориоидеи - это доброкачественные или злокачественные новообразования сосудистой оболочки глазного яблока. Невус - наиболее распространённое доброкачественное образование органа зрения. Частота его выявления при офтальмоскопии составляет 2%. В тоже время, при аутопсии данную патологию диагностируют у 6,5-20% пациентов. У лиц женского и мужского пола невусы определяются в равной степени. Распространенность увеальной меланомы среди всех патологий глаз составляет 5%. Риск образования этой опухоли хориоидеи существенно увеличивается с возрастом больного и после 69 лет с каждым годом возрастает на 50 случаев (из расчета на 1 млн. населения). Общая заболеваемость гемангиомой глаза среди общего числа интраорбитальных патологических новообразований составляет 0,76%. Данный вид опухоли хориоидеи встречается во всех возрастных группах, но чаще диагностируется после 10 и до 60 лет.
Причины
Зачастую опухоли хориоидеи развиваются спорадически. Однако в литературе описаны семейные случаи увеальной меланомы, что позволяет отнести ее к числу генетически детерминированных патологий. Дисфункция генов-супрессоров опухолевого роста (CDKN2A, CDK4) приводит к развитию хромосомных мутаций, локализирующихся на коротком плече 21 или длинном плече 14 хромосомы. Каскад патологических процессов включает в себя нарушение синтеза белков p16 и p14ARF. Развитию данной опухоли хориоидеи может предшествовать окулодермальный меланоз или нарушение пигментного обмена. Нередко она возникает в результате малигнизации прогрессирующего невуса, но наиболее распространенная причина появления неоплазии - мутация «de novo». С учетом морфологической картины различают веретеноклеточный, эпителиоидный и смешанный варианты увеальной меланомы. Специфическая окраска опухоли хориоидеи обусловлена отложением липофусциновых зёрен.
Гемангиома относится к числу гамартом. Причина образования - тканевая аномалия развития. Состав новообразования имеет те же компоненты, что и окружающие ткани, но степень его дифференциации и строение резко нарушены. Риск развития опухолей хориоидеи возрастает при длительном контакте с ультрафиолетовым излучением или на фоне солнечных ожогов глаз. В популяции заболевание чаще встречается среди лиц, в фенотипе которых присутствуют голубые глаза, светлая кожа и волосы, множественные невусы (более 50).
Симптомы опухолей хориоидеи
С клинической точки зрения выделяют сосудистые и пигментные опухоли хориоидеи. Также различают доброкачественные и злокачественные новообразования. К пигментным формам относят невусы (стационарные и прогрессирующие). В большинстве случаев это врожденный вид опухолей хориоидеи, но интенсивность пигментной окраски усиливается после 30-летнего возраста. Их выявляют в заднем полюсе глазного яблока, реже в экваториальной области или перед ней. Описаны случаи бинокулярного поражения органа зрения. Как правило, течение заболевания бессимптомное. Увеличение в размере прогрессирующего невуса в редких случаях приводит к снижению остроты зрения.
Клинические проявления увеальной меланомы зависят от ее диаметра и степени вовлечения в патологический процесс окружающих сосудов. Ангиогенез в области опухоли хориоидеи и изменения сосудистой стенки (утолщение и уплотнение) приводят к разрыву внутренней оболочки глазного яблока. Зачастую симптоматика отсутствует. В редких случаях пациенты предъявляют жалобы на вспышки света, снижение зрительных функций, появление «мушек» или «чёрной занавеси» перед глазами. При большой распространенности опухолевого процесса у больных прогрессивно снижается острота зрения.
Гемангиома относится к группе доброкачественных опухолей хориоидеи. Для нее характерен быстропрогрессирующий рост, который очень часто приводит к полной отслойке сетчатки. Первый симптом заболевания у взрослых - нарушение зрительных функций. В детском возрасте данная опухоль хориоидеи становится причиной страбизма. С клинической точки зрения выделяют ограниченную и диффузную формы. При ограниченном варианте формируется небольшой узел с четко очерченными краями. Клинические проявления мало выражены. При диффузном распространении опухолевого процесса, заболевание осложняется энцефалофациальным ангиоматозом (синдром Стерджа-Вебера).
Диагностика
Диагностика опухолей хориоидеи основывается на результатах офтальмоскопии, визометрии, флуоресцентной ангиографии, биомикроскопии, оптической когерентной томографии (ОКТ), ультразвукового исследования (УЗД) в В-режиме. При офтальмоскопии невусы имеют вид плоских, приподнятых над уровнем окружающих тканей образований размером до 0,1 см. В зависимости от выраженности пигментации их цвет варьирует от сероватого до серо-коричневого. Границы зачастую неровные, но с четкими очертаниями. Неровность контуров обусловлена прилежащими сосудами. Для невусов, лишенных пигмента, характерна овальная или округлая форма с ровными, но менее очерченными контурами. В отличие от прогрессирующих невусов, на поверхности стационарных присутствуют друзы. Для их дифференциальной диагностики проводится офтальмоскопия с цветными фильтрами. Красная окраска фильтра позволяет визуализировать данный тип опухоли хориоидеи, при зеленой патологическое образование не определяется.
Методом флуоресцентной ангиографии при стационарной форме выявляется снижение флуоресценции на протяжении всего обследования. При этом в окружающей сосудистой оболочке изменения не выявляются. Об изменениях хориоидеи свидетельствует пропотевание и яркое свечение красителя. При офтальмоскопии увеальной меланомы обнаруживается небольшой узелок с постэкваториальной локализацией. Опухоль хориоидеи - желто-коричневой или аспидной окраски с друзами на поверхности или в окружающих тканях. Методом ОКТ устанавливается точная локализация, размеры, степень распространения на окружающие ткани. У большинства пациентом при визометрии диагностируется снижение остроты зрения.
При проведении офтальмоскопии отграниченная гемангиома имеет вид небольшого узелка округлой формы с ровными контурами диаметром 0,3-1,5 см. Средняя толщина патологического образования составляет 0,3-0,4 см. Цвет данной формы опухоли хориоидеи - от светло-серого до темно-красного. Для дифференциальной диагностики гемангиомы от меланомы следует провести флуоресцентную ангиографию. При гемангиоме средний диаметр сосудов опухоли соответствует таковому сосудов хориоидеи, также на ее поверхности могут появляться небольшие очаги кровоизлияния. Из-за прогрессирующего ангиогенеза при меланоме новообразованные капилляры имеют меньший калибр и более извитой ход. На УЗД опухоли хориоидеи определяется ток крови и характерная пульсация сосудов, что позволяет подтвердить диагноз. Наружный осмотр проводится для выявления типичной симптоматики страбизма.
Лечение опухолей хориоидеи
Тактика лечения при опухолях хориоидеи зависит от формы заболевания. При появлении признаков, свидетельствующих о трансформации стационарного невуса в прогрессирующий, показана лазерная коагуляция. При обнаружении увеальной меланомы большого размера следует провести энуклеацию глазного яблока. Если диаметр патологического новообразования незначительный, а опухоль не распространяется за пределы первичного очага, рекомендована контактная лучевая терапия (брахитерапия глаза). Преимущество данного метода лечения опухолей хориоидеи - местное воздействие на меланому максимальной дозой лучевой терапии. При этом на окружающие ткани и критические органы излучение не влияет. Альтернативный вариант - транспупиллярная диод-лазерная термотерапия. Данный метод относится к числу малоинвазивных техник. При этом вся процедура проводится под визуальным контролем.
Выявление гемангиомы - это показание к проведению оперативного вмешательства, что обусловлено большим риском экссудативной отслойки сетчатки и снижения зрительных функций. В лечении отграниченной формы опухоли хориоидеи используется криотерапия, брахитерапия, фотодинамическая терапия и транспупиллярная диод-лазерная термотерапия. Высокой эффективностью обладает лазерокоагуляция в желтом спектре излучения. Тактика лечения сводится к облитерации кровеносных сосудов. Преимущество этой методики - ликвидация выпота экссудата из новообразованных сосудов за счет адгезии пигментного слоя и сенсорной сетчатки. Субретинальная жидкость при этом резорбируется.
Прогноз и профилактика
Специфических мер по профилактике опухолей хориоидеи в офтальмологии не разработано. Все пациенты с установленным диагнозом доброкачественного или злокачественного новообразования сосудистой оболочки должны находиться на диспансерном учете у офтальмолога. После проведения оперативного лечения периодически необходимо проходить профилактическое обследование у специалиста, ограничить пребывание на солнце, избегать работы при высокой температуре окружающей среды.
Прогноз для жизни и трудоспособности при стационарной форме невуса благоприятный. Прогрессирующий вариант следует рассматривать как предраковое состояние. Наиболее злокачественная среди опухолей хориоидеи - меланома, прогноз для жизни определяется стадией развития. Гемангиома сосудистой оболочки - прогностически благоприятное заболевание, однако у отдельных больных возможна полная потеря зрения.
Гемангиома глаза
Гемангиома глаза - это доброкачественная сосудистая опухоль, располагающая на коже век или конъюнктиве и состоящая из патологических сосудистых сплетений. Причины возникновения гемангиомы глаза точно неизвестны. Различают капиллярные и кавернозные гемангиомы, а также смешанные варианты. Клинические проявления зависят от вида гемангиомы. Диагностику проводят с помощью визуального осмотра и биомикроскопии, из дополнительных методов используют УЗИ глаза, МРТ или КТ орбит, ангиографию. Лечение проводят консервативно или оперативно, в зависимости от размеров и места расположения гемангиомы. При раннем обращении и правильном лечении прогноз благоприятный.

Гемангиома глаза - доброкачественное сосудистое новообразование, возникающее из гиперплазированного эндотелия кровеносных сосудов, которое проявляется преимущественно в детском возрасте, характеризуется довольно быстрым ростом и частым прорастанием в окружающие ткани. Гемангиома глаза является одной из самых частых доброкачественных опухолей в детской офтальмологии. Встречается у новорожденных детей, чаще у недоношенных. Обнаруживается в первые дни после рождения ребенка или в первые месяцы жизни. Девочки болеют чаще, чем мальчики. Наиболее высокая заболеваемость наблюдается у детей из развитых стран. Если у ребенка появилась гемангиома глаза, то в течение первого полугодия жизни у таких детей возможно появление гемангиом на других участках тела. Являясь морфологически доброкачественными образованиями, гемангиомы часто отличаются неблагоприятным клиническим течением и характеризуются быстрым инфильтрирующим ростом, достигая максимальной величины в первые недели и месяцы жизни.
Причины гемангиомы глаза
Причины возникновения гемангиом глаза до сих пор вызывают много споров у офтальмологов. В настоящее время ещё не найдены специфические генные мутации, отвечающие за развитие гемангиомы глаза, наследственность не является фактором риска. Неизвестны точные механизмы, запускающие нарушения в ангиогенезе (процесс образования и развития новых сосудов). Имеются определённые доказательства, что гемангиома глаза у новорожденных детей образуется в результате повреждения ангиобластов (клетки сосудистой стенки). Эти процессы возникают в первом триместре беременности, между 7 и 10 неделей. Процесс внутриутробного развития сосудов достаточно сложен и окончательно не изучен. Любые изменения в ангиогенезе могут приводить к спонтанному росту кровеносных сосудов, отмечаемому при гемангиомах глаза у детей.
Симптомы гемангиомы глаза
Выделяют капиллярную и кавернозную гемангиому глаза, а также смешанные варианты. Капиллярная гемангиома, или «земляничный» невус, проявляется у новорожденных детей в виде ограниченного опухолевидного разрастания ярко-красного цвета. Выступает над уровнем кожи, бледнеет при надавливании и увеличивается в размерах во время крика или плача ребёнка. Чаще встречается на верхнем веке и может распространяться в орбиту. У данного вида гемангиомы активный рост отмечается в первый год жизни ребёнка и останавливается к двум годам. Затем происходит обратный регресс опухоли с полным исчезновением к 5-6 годам. В редких случаях гемангиома глаза может сочетаться с поражениями других органов и систем в виде синдрома Казабаха-Мерритта (характеризуется тромбоцитопенией, анемией и нарушением свёртывания крови), или синдрома Маффуччи (сочетается с хондроматозом рук, ног и искривлением трубчатых костей).
Кавернозная гемангиома, или пламенеющий невус, проявляется в виде пятна, чётко отграниченного, мягкого по консистенции, розового цвета, не бледнеющего при надавливании. Возникают также у новорожденных. С возрастом не увеличивается в размерах и не проходит самостоятельно, меняется цвет пятна до тёмно-красного или фиолетового. Кожа под образованием может грубеть, гипертрофироваться, становиться узловатой, рыхлой, кровоточить или воспаляться. Поражение носит сегментарный характер, но встречаются и двусторонние невусы. Сочетанные поражения возникают при обширных гемангиомах, затрагивающих ветви тройничного нерва. Проявляются в структуре синдрома Штурге-Вебера (характеризуется нарушением в развитии сосудов сетчатки и оболочек головного мозга).
Из осложнений гемангиом глаза выделяют: механический птоз (большой размер опухоли мешает нормальной работе мышц век), как результат птоза развивается обскурационная амблиопия; косоглазие (новообразование в области глаза мешает полноценному движению глазного яблока в какую-либо сторону). На месте регрессировавшей опухоли может оставаться рубец или гипопигменация. Гемангиомы глаза большого размера могут осложняться кровотечениями, инфицированием или нагноением.
Диагностика гемангиомы глаза
Диагностика всех видов гемангиом глаза обычно не вызывает затруднений и основывается на визуальном осмотре ребёнка офтальмологом с помощью метода биомикроскопии при помощи щелевой лампы. Для уточнения диагноза и дифференциальной диагностики с другими сосудистыми опухолями проводят дополнительные исследования, такие как УЗИ глазного яблока (для уточнения структуры и глубины распространения гемангиомы), КТ орбит или МРТ (при недостаточности данных УЗИ, для уточнения размеров новообразования и возможного поражения соседних органов).
При необходимости оперативного лечения гемангиомы глаза дополнительно проводят ангиографию для более точного определения границ опухоли и распространения патологических сосудов. При изменении поверхности гемангиомы, окраски или консистенции выполняют биопсию, для исключения злокачественного перерождения новообразования. Также могут назначаться консультации онколога, дерматолога, гематолога или инфекциониста.
Лечение гемангиомы глаза
При лечении гемангиомы применяют консервативный или хирургический метод. Консервативная терапия включает в себя использование препаратов из группы глюкокортикостероидов (препарат вводят перорально ребёнку при первых проявлениях новообразования), интерфероны (подкожное введение препарата используется при обширных гемангиомах). При малых размерах гемангиомы глаза для удаления используют метод криодеструкции или диатермокоагуляции (воздействие на гемангиому низкой или высокой температурой, в результате чего происходит разрушение и отторжение новообразования). Использование лазерных методик оправдано также при небольших размерах гемангиомы глаза. Оперативное лечение показано при обширных гемангиомах с расположением в анатомически сложных областях. Кроме того, хирургический метод используют для удаления косметических дефектов, оставшихся от гемангиом.
При своевременном обращении к офтальмологу с первыми признаками формирования гемангиом, правильно подобранной терапии - прогноз благоприятный, удается добиться полного исчезновения новообразования без видимых дефектов.
Профилактика гемангиомы глаза
Учитывая, что гемангиомы глаза закладываются на эмбриональном этапе, профилактические мероприятия включают в себя тщательный контроль и обследование женщин как в период беременности, так и на этапе подготовки к зачатию. За несколько месяцев до зачатия необходимо пройти лечение всех хронических очагов инфекции (ЛОР-органов, глаз, зубов). Обязательно информировать женщин о вреде курения и алкоголя в период беременности, своевременно освободить беременную от работы на вредных химических производствах или перевести на более лёгкий труд. У рожениц старше 35-40 лет необходимо тщательно контролировать артериальное давление для предотвращения возникновения эклампсии. При обнаружении у новорожденного гемангиомы глаза необходимо максимально быстро обратиться к офтальмологу для обследования и уточнения диагноза, а также строго соблюдать рекомендации врача.
Читайте также:
