Синдром Гебры (Hebra) - синонимы, авторы, клиника
Добавил пользователь Дмитрий К. Обновлено: 28.01.2026
Синдром Жильбера - самая распространенная форма наследственного пигментного гепатоза, характеризующаяся нарушением обмена билирубина вследствие генетического дефекта микросомальных ферментов печени. Часто заболевание протекает бессимптомно многие годы, но под действием провоцирующих факторов могут возникать интермиттирующая желтуха, диспепсические и астеновегетативные расстройства.
Диагностика требует сбора семейного анамнеза, проведения лабораторных и инструментальных исследований. В лечении синдрома Жильбера применяются медикаментозные препараты разных групп.
Синдрому Жильбера по МКБ соответствует код E80.4. Мужчины страдают данным заболеванием в четыре раза чаще женщин. В целом же распространенность патологии в европейских и азиатских странах не превышает 5%.
Причины появления
В норме у человека при распаде эритроцитов образуется токсичное для организма вещество - непрямой билирубин. Он нейтрализуется клетками печени, которые обеспечивают его связывание с глюкуроновой кислотой и превращение в водорастворимый прямой билирубин. В дальнейшем происходит выведение данного соединения через органы билиарной системы с калом и мочой.
Причина возникновения врожденного синдрома Жильбера - генетическая мутация микросомального фермента УДФ-глюкуронилтрансферазы, ответственного за связывание глюкуроновой кислоты с непрямым билирубином. Вторым механизмом развития болезни считается нарушение захвата билирубина микросомами сосудистого полюса клетки печени и его транспорта глутатион-S-трансферазой. Таким образом, концентрация токсичных продуктов метаболизма в сыворотке крови растет. В результате неконъюгированный билирубин накапливается в тканях, окрашивая их в желтый цвет. Наследование патологии происходит по аутосомно-доминантному типу.
- несбалансированное питание, строгая диета или голодание;
- потеря жидкости организмом, обезвоживание;
- стресс, физическое переутомление;
- менструальное кровотечение;
- инфекционные процессы;
- операции;
- прием алкоголя и некоторых лекарственных препаратов.
Симптомы синдрома Жильбера
Первые проявления синдрома Жильбера у детей начинаются в подростковом возрасте, после 11-12 лет, что связано с угнетающим влиянием половых гормонов на утилизацию билирубина. Однако дебют заболевания может случиться и намного позже, в срок до 30 лет.
- Интермиттирующая желтуха. Локализация и степень выраженности могут быть различными - от изменения цвета только склер глазных яблок до яркой желтушности кожи и слизистых по всему телу. Появление желтухи носит всегда внезапный характер, возникает после воздействия провоцирующих факторов и самопроизвольно исчезает.
- Ксантелазмы век. Единичные или множественные бляшки желтоватого цвета, возвышающиеся над кожей.
- Ощущение тяжести в правом подреберье, чувство дискомфорта в брюшной полости. Данные симптомы связаны с увеличением печени, селезенки, развитием холецистита, дискинезии желчевыводящих путей, желчнокаменной болезни.
- Астеновегетативные расстройства. Из-за интоксикации организма появляются быстрая утомляемость и подавленность, нарушение сна, избыточное потоотделение.
- Диспепсические проявления. Потеря аппетита, привкус горечи во рту, тошнота, отрыжка, вздутие живота и избыточное газообразование, нарушения стула.
Осложнения
Даже при благоприятном течении заболевания пациенту важно знать, чем опасен синдром Жильбера. При его наличии возрастает риск развития желчнокаменной болезни, внутрипеченочного и внепеченочного холестаза, дискинезии желчевыводящих путей, а также существенно отягощается течение других патологий гепато-билиарной системы, например, лекарственных и токсических гепатитов. Кроме того, развитие желтухи сопровождается снижением иммунитета.
Диагностика синдрома Жильбера
Постановка диагноза включает анализ имеющихся жалоб и клинических проявлений заболевания, уточнение наличия эпизодов желтухи и патологии гепато-билиарной системы у близких родственников, применение лабораторных и инструментальных методов исследования.
Дифференциальная диагностика синдрома Жильбера проводится с вирусным и хроническим гепатитом, механической и гемолитической желтухой, синдромом Криглера - Найяра, синдромом Дабина - Джонсона и синдромом Ротора, первичной шунтовой гипербилирубинемией, врожденными циррозами печени, атрезией желчных ходов. Главная отличительная особенность данного нарушения - повышение фракции неконъюгированного билирубина в сыворотке крови, не связанное с гемолизом эритроцитов, и наследственная отягощенность.
- . В ряде случаев отмечается повышение уровня гемоглобина или снижение числа тромбоцитов. . Основной признак заболевания - повышение концентрации общего билирубина до 34,2-85,5 мкмоль/л за счет его непрямой фракции. Показатели остальных печеночных ферментов крови, таких как АсАТ, АлАТ, ГГТП, ЩФ, как правило, находятся в пределах нормы. Возможно наличие диспротеинемии и повышение концентрации общего белка. . Проводится определение креатинина. . При синдроме Жильбера наличие Ig G к HBcAg, гепатиту А и С нехарактерно. . Анализ кала на стеркобилин при рассматриваемой патологии имеет отрицательный результат. В сложных случаях показано проведение функциональных лабораторных проб. Снижение уровня билирубина на фоне приема фенобарбитала и его повышение в 1,5-2 раза после голодания, низкокалорийной диеты или внутривенного введения никотиновой кислоты подтверждают диагноз.
Из инструментальных методов наиболее часто выполняется ультразвуковое исследование органов брюшной полости для исключения других патологий печени и желчнокаменной болезни. У детей можно пользоваться способом определения печеночно-селезеночного индекса по данным УЗИ.
Дополнительно возможно проведение дуоденального зондирования, тонкослойной хроматографии. Чрезкожная пункция печени с последующей морфологической оценкой полученного биоматериала выполняется при подозрении у пациента хронического гепатита или цирроза печени.
Лечение синдрома Жильбера
Само по себе наличие у детей и взрослых синдрома Жильбера еще не является показанием к медикаментозному лечению. Для предупреждения обострения заболевания и развития осложнений важны общие мероприятия: ограничение занятий тяжелыми видами спорта, продолжительного пребывания на солнце, употребления алкогольных напитков и гепатотоксических препаратов. Таким пациентам необходимо правильно питаться, избегать длительного голодания, а также продуктов, содержащих трудноусвояемые жиры - жирных сортов мяса, жареных и острых блюд, консервированной пищи.
- прием индукторов микросомальных ферментов (фенобарбитал, зиксорин);
- прием активированного угля;
- фототерапию.
Прогноз и профилактика
Прогноз заболевания в любом возрасте благоприятный. Гипербилирубинемия при синдроме Жильбера сохраняется пожизненно, но носит доброкачественный характер, не сопровождается прогрессирующими изменениями в печени и не оказывает влияние на продолжительность жизни.
Синдром Гийена — Барре - симптомы и лечение
Что такое синдром Гийена — Барре? Причины возникновения, диагностику и методы лечения разберем в статье доктора Жуйкова Александра Вячеславовича, невролога со стажем в 21 год.
Над статьей доктора Жуйкова Александра Вячеславовича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
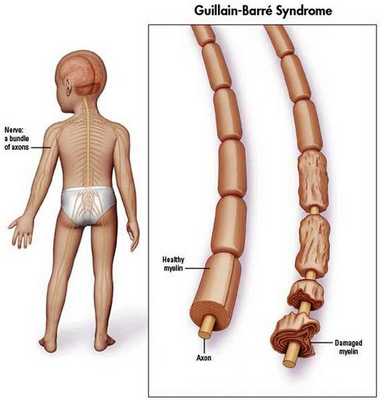
Синдром Гийена — Барре (ГБС) — острое аутоиммунное заболевание, которое охватывает группу острых нарушений периферической нервной системы. Характеризуется мышечной слабостью, а также болью и ползанием мурашек в начале болезни из-за поражения чувствительных волокон. Каждый вариант нарушений характеризуется особенностями патофизиологии и клинического распределения слабости в конечностях и черепных нервах.
Распространённость синдрома Гийена — Барре
Синдром Гийена — Барре встречается в 1-2 случаях на 100 000 населения в год. [10]
Причины синдрома Гийена — Барре
Точная причина синдрома Гийена — Барре неизвестна. Но у 70% пациентов с ГБС наблюдались предшествующие инфекционные заболевания: респираторные, желудочно-кишечные инфекции, вирус Зика. Также синдром Гийена — Барре может развиться после заражения коронавирусом. [9]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы синдрома Гийена — Барре
Симптомы ОРВИ или расстройства желудочно-кишечного тракта отмечаются у 2/3 пациентов. Первыми симптомами ГБС являются парестезии пальцев конечностей, за которыми следует прогрессирующая слабость мышц нижних конечностей и нарушения походки. Болезнь прогрессирует в течение нескольких часов или дней, возникает слабость верхних конечностей и развиваются паралич черепных нервов. Параличи обычно симметричны и носят, конечно, периферический характер. У половины пациентов боль может быть первоначальной жалобой, что затрудняет диагноз. Атаксия и боль чаще встречаются у детей, чем у взрослых. Задержка мочи наблюдается у 10%-15% больных. Поражение вегетативных нервов проявляются головокружениями, гипертонией, чрезмерным потоотделением и тахикардией.
При объективном обследовании выявляется восходящая мышечная слабость, а также арефлексия. Сухожильные рефлексы нижних конечностей отсутствуют, но рефлексы верхней конечности могут вызываться. Мышечная слабость может задействовать и респираторные мышцы. Поражение черепных нервов отмечается в 35-50%, вегетативная нестабильность в 26%-50%, атаксия — в 23%, дизестезия — в 20% случаев. [1]
Наиболее распространенными признаками вегетативной дисфункции являются синусовая тахикардия или брадикардия и артериальная гипертония. У пациентов с тяжелой вегетативной дисфункцией наблюдаются изменения периферического вазомоторного тонуса с гипотензией и лабильностью артериального давления.
Нечастые варианты клинического течения болезни включают лихорадку в начале неврологических симптомов, тяжелую сенсорную недостаточность с болью (миалгии и артралгии, менингизм, корешковая боль), дисфункции сфинктеров.
Возможность ГБС должна рассматриваться у любого пациента с быстрым развитием острой нервно-мышечной слабости. На ранней стадии ГБС следует отличать от других заболеваний с прогрессирующей симметричной мышечной слабостью, включая поперечный миелит и миелопатию, острую токсическую или дифтеритическую полиневропатию, порфирию, миастению и нарушения электролитного обмена (например, гипокалиемия).
Патогенез синдрома Гийена — Барре
Нейрофизиологические процессы, лежащие в основе ГБС, подразделяются на несколько подтипов. Наиболее распространенные подтипы включают:
- острую воспалительную демиелинизирующую полирадикулопатию;
- острую двигательную аксональную невропатию;
- острую моторную и сенсорную аксональную нейропатию;
- синдром Миллера-Фишера, как вариант ГБС, характеризуется триадой признаков: офтальмоплегия, атаксия и арефлексия.
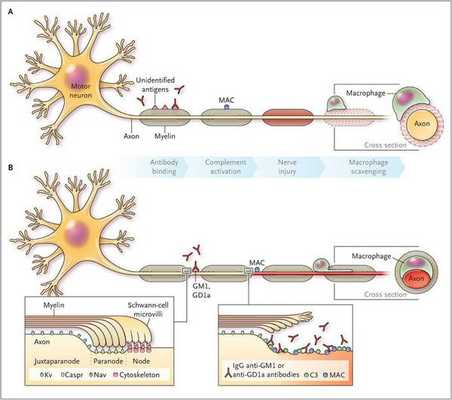
Считается, что ГБС развивается вследствие выработки антител против белка инфекционного агента, которые перекрестно реагируют с ганглиозидами нервных волокон человека. Аутоантитела связываются с миелиновыми антигенами и активируют комплемент, с формированием мембранно-атакующего комплекса на внешней поверхности клеток Шванна. Повреждение оболочек нервных стволов приводит к нарушениям проводимости и мышечной слабости (на поздней стадии может происходить и аксональная дегенерация). Демиелинизирующее поражение наблюдается по всей длине периферического нерва, включая нервные корешки.
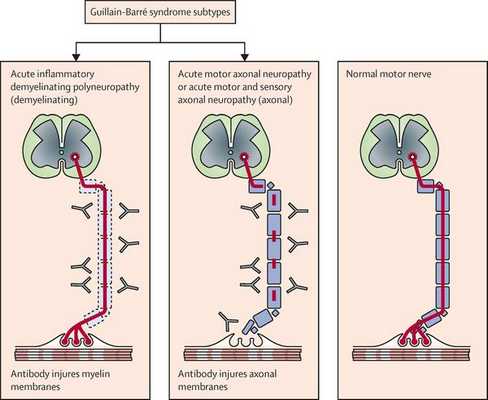
Поражаются все типы нервов, в том числе вегетативные, моторные и сенсорные волокна. Вовлечение двигательных нервов происходит значительно чаще, чем сенсорных.
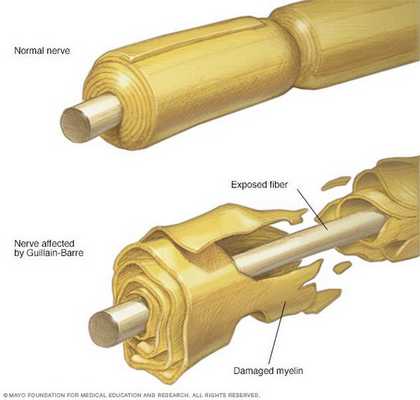
Классификация и стадии развития синдрома Гийена — Барре
В Международной классификации болезней (МКБ-10) синдром Гийена — Барре кодируется как G61.0.
Основные виды синдрома Гийена — Барре:
- Острая воспалительная демиелинизирующая полирадикулоневропатия (ОВДП) — самая распространённая форма в Северной Америке и Европе. Основным признаком ОВДП является мышечная слабость, которая сперва возникает в нижней части тела, а затем распространяется вверх.
- Синдром Миллера Фишера — проявляется параличом глаз и неустойчивостью походки. Эта форма более распространена в Азии.
- Острая моторная аксональная невропатия (ОМАН) и острая моторно-сенсорная аксональная невропатия (ОМСАН) — чаще встречаются в Китае, Японии и Мексике. [8]
Осложнения синдрома Гийена — Барре
Пациенты с ГБС подвержены риску опасных для жизни респираторных осложнений и вегетативных нарушений.
Показания для перевода в отделение интенсивной терапии включают:
- быстрое прогрессирование моторной слабости с поражением респираторных мышц;
- вентиляционную дыхательную недостаточность;
- пневмонию;
- бульбарные расстройства;
- тяжелую вегетативную недостаточность.
Осложнения проводимого лечения, требующие интенсивной терапии, включают перегрузку жидкостью, анафилаксию на введение внутривенного иммуноглобулина или гемодинамические нарушения при проведении плазмафереза.
У 15%-25% детей с ГБС развивается декомпенсированная дыхательная недостаточность, которая требует механической вентиляции легких. [2] Респираторные нарушения чаще встречается у детей с быстрым прогрессированием заболевания, слабостью верхних конечностей, вегетативной дисфункцией и поражениями черепных нервов. Интубация трахеи может потребоваться у больных для защиты дыхательных путей, проведения механической вентиляции легких. При ГБС быстрое прогрессирование, двусторонний паралич лицевого нерва и вегетативная дисфункция предопределяют повышенную вероятность интубации. Необходимо планирование ранней интубации для минимизации риска осложнений и необходимости проведения экстренной интубации.
Вегетативная дисфункция повышает риск эндотрахеальной интубации. С другой стороны, дисавтономия может увеличить риск гемодинамических реакций на препараты, используемые для индукции анестезии во время интубации.
Признаки, указывающие на необходимость механической вентиляции легких: [4]
- вентиляционная дыхательная недостаточность;
- увеличение потребности в кислороде для поддержания SpO2 выше 92%;
- признаки альвеолярной гиповентиляции (PCO2 выше 50 мм. рт. ст.);
- быстрое снижение жизненной емкости на 50% по сравнению с исходным уровнем;
- невозможность кашля
Вегетативная дисфункция является основным фактором смертности при ГБС. Фатальный сердечно-сосудистый коллапс из-за вегетативной дисфункции наблюдается у 2%-10% тяжелобольных пациентов. [3] Мониторинг частоты сердечных сокращений, артериального давления и электрокардиограммы следует продолжать до тех пор, пока пациенты нуждаются в респираторной поддержке. Чрескожная кардиостимуляция может потребоваться при выраженной брадикардии. Гипотония корректируется восполнением объема циркулирующей крови (ОЦК), и, если пациент невосприимчив к восполнению ОЦК, применяются α-агонисты, такие как норадреналин, мезатон, адреналин.
При нестабильной гемодинамике непрерывная регистрация артериального и центрального венозного давления должна проводиться для контроля объема инфузионной терапии.
Артериальная гипертензия может возникать, но это осложнение не требует специального лечения, если оно не осложняется отеком легких, энцефалопатией или субарахноидальным кровоизлиянием.
Диагностика синдрома Гийена — Барре
Сбор жалоб и анамнеза
На приёме врач в первую очередь обратит внимание на скорость распространения паралича и нарушение дыхания. Если эти признаки выражены, больному может потребоваться экстренная помощь.
Как правило, пациенты с синдромом Гийена — Барре жалуются на нарушение походки, онемение и зябкость ног, а затем и рук. Нередко пациенты рассказывают, что недавно перенесли ОРВИ.
Осмотр
Объективный неврологический осмотр — это основа диагностики при синдроме Гийена — Барре. Врач оценивает рефлексы, координацию движений, походку, чувствительность и мышечную силу.
Лабораторная диагностика
Основным видом лабораторной диагностики при синдроме Гийена — Барре является исследование спинномозговой жидкости, которую получают с помощью люмбальной пункции.
Инструментальная диагностика
ЭНМГ (Электронейромиография) — единственный инструментальный метод диагностики, позволяющий подтвердить диагноз ГБС и уточнить характер патологических изменений (демиелинизирующий или аксональный) и их распространенность. [3]
Игольчатая электромиография характеризуется наличием признаков текущего денервационно-реиннервационного процесса при полинейропатии. Исследуют дистальные мышцы верхних и нижних конечностей (например, переднюю большеберцовую мышцу, общий разгибатель пальцев), а при необходимости и проксимальные мышцы (например, четырёхглавую мышцу бедра).
ЭНМГ-исследование у больных с ГБС зависит от клинических проявлений:
- при дистальных парезах исследуются длинные нервы на руках и ногах: не менее четырех двигательных и четырех чувствительных (двигательные и чувствительные порции срединного и локтевого нервов; малоберцовый, большеберцовый, поверхностный малоберцовый и икроножный нервы с одной стороны).
Оценка основных ЭНМГ- параметров:
Первые признаки денервационного процесса появляются через две-три недели после начала заболевания, признаки реиннервационного процесса — через месяц.
Дифференциальная диагностика
Синдром Гийена — Барре следует отличать от следующих заболеваний:
- и клещевого энцефалита (чувствительность не нарушена, поражены преимущественно черепные нервы); (отягощённый эпидемиологический анамнез, например посещение эндемичных стран); (чувствительность не нарушена, рефлексы снижены незначительно);
- обменно-метаболических полиневропатий (течение хроническое).
Лечение синдрома Гийена — Барре
Показания для госпитализации
Практически во всех случаях требуется госпитализация. Экстренная госпитализация необходима пациентам с нарушениями дыхания — в таких случаях лечение проводят в условиях реанимации.
Общие принципы лечения синдрома Гийена — Барре
Лечение острой демиелинизирующей полирадикулоневропатии комплексное. Основа — плазмаферез, иммуноглобулины и кортикостероиды. В ряде случаев требуется искусственная вентиляция лёгких, коррекция нарушений кровообращения, профилактика инфекционных и тромбоэмболических осложнений. Обязательным условием успешного лечения является уход.
Общее поддерживающее лечение и уход
Пациенты, требующие интенсивной терапии, требуют тщательного общего ухода. Запор наблюдается более чем в 50% случаев пациентов с ГБС в результате динамической непроходимости кишечника. Может потребоваться искусственное питание.
Медикаментозное лечение и плазмаферез
В лечении ГБС предпринимаются различные виды иммуномодулирующей терапии. [1] [2]
Внутривенный иммуноглобулин назначают в виде ежедневной инфузии (в дозе 0,4 гр/кг/день) в течение 5 дней в первые 2 недели болезни. Второй курс иммуноглобулина может потребоваться 5%-10% пациентов, при отрицательной динамике после первоначального улучшения. Механизм действия внутривенного иммуноглобулина, вероятно, многофакторный и, как полагают, включает модуляцию активации комплемента, нейтрализацию идиотипических антител, подавление воспалительных медиаторов (цитокины, хемокины).
Побочные эффекты иммуноглобулина включают головную боль, миалгию и артралгию, гриппоподобные симптомы, лихорадку. У пациентов с дефицитом IgA может развиться анафилаксия после первого курса внутривенного иммуноглобулина.
Плазмаферез способствует удалению антител, вовлеченных в патогенез ГБС. В течение каждого сеанса 40-50 мл/кг плазмы заменяют смесью 0,9% раствора хлорида натрия и альбумина. Проведение плазмафереза приводит к сокращению времени выздоровления и снижению потребности в искусственной вентиляции. Эти преимущества очевидны, если плазмаферез проводится в течение первых двух недель после начала болезни. Осложнения, связанные с плазмаферезом, включают гематому в области венопункции, пневмоторакс после катетеризации подключичной вены и сепсис. Плазмаферез противопоказан пациентам с тяжелой гемодинамической нестабильностью, кровотечением и сепсисом. Комбинация плазмафереза и иммуноглобулина не показала клинических преимуществ.
Симптоматическое лечение синдрома Гийена — Барре:
- при боли применяют парацетамол;
- катадолон и трамадол применяют при выраженном болевом синдроме;
- при нейропатической боли эффективны карбамазепин и габапентин.
Оперативное лечение
При тяжёлом течении может потребоваться длительная респираторная поддержка и наложение трахеостомы. Если пациент находится на искусственном питании, то накладывают гастростому.
Прогноз. Профилактика
ГБС остается серьезным заболеванием, несмотря на улучшение результатов лечения. По сравнению со взрослыми, у детей чаще отмечается более благоприятное течение заболевания, с полным, а не частичным выздоровлением. Причинами неблагоприятного исхода при ГБС являются дыхательная недостаточность, осложнения искусственной вентиляции легких (пневмония, сепсис, острый респираторный дистресс-синдром и тромбоэмболические осложнения), остановка сердца, вторичная по отношению к дисавтономии.
Восстановление обычно начинается через две-четыре недели после прекращения прогрессирования симптомов. Среднее время от начала заболевания до полного выздоровления составляет 60 дней. Данные относительно долгосрочного исхода ГБС ограничены. 75% - 80% пациентов полностью выздоравливают. Около 20% пациентов не могут ходить через полгода.
Младшая возрастная группа (менее 9 лет), быстрое прогрессирование и максимальная мышечная слабость, потребность в искусственной вентиляции легких являются важными предикторами длительного двигательного дефицита. [4]
Почесуха гебры - prurigo Hebra
Пруриго Hebra обычно начинается в раннем детском возрасте или несколько позже с появления преимущественно на разгибательных поверхностях конечностей мелких бледно-розовых плотных сухих узелков, сопровождающихся очень сильным зудом. Иногда этому предшествуют высыпания характера папулезной крапивницы. Как уже было отмечено в статье о детской почесухе, в некоторых случаях как бы продолжением таковой является пруриго Hebra. Постепенно в процесс вовлекаются другие участки кожи — туловище, ягодицы, но почти всегда остаются свободными от сыпи лицо и сгибательные поверхности конечностей.
Вследствие очень сильного зуда большинство узелковых высыпаний находится в состоянии расчесов, покрыто кровянистыми корочками. Кожа утолщается, лихенифицируется, пигментируется. Иногда процесс осложняется вторичной инфекцией. Обычно значительно увеличиваются лимфатические узлы, главным образом паховые, подмышечные и локтевые; при этом говорят о «пруригинозных бубонах». Характерным для них является безболезненность и отсутствие тенденции к нагноению.
Французская дерматологическая школа во главе с Cazenave, Brocq и Jacquet считает, что при пруриго первичным является кожный зуд, узелки же возникают лишь в результате расчесов. В пользу этого взгляда говорит известный эксперимент Jacquet (1892): у пруригинозной больной на специально хорошо забинтованной руке не появлялись пруригинозные узелки, в то время как на коже другой руки и других мест таковые продолжали возникать. Венская и немецкая школы во главе с Hebra, Jarisch и Finger считают, что первичными являются пруригинозные узелки. По-видимому, были правы Neisser и Mac Leod, по мнению которых зуд и узелковая сыпь появляются одновременно и не представляется возможным рассматривать их отдельно.
Принято различать легкую форму пруриго (prurigo mitis) и тяжелую [prurigo aggria (от лат. agrius — тяжелый)], или prurigo ferox (лат. ferox — жесткий). При легкой форме общее состояние больных страдает незначительно, так как при этом бывает лишь небольшое количество высыпаний, зуд относительно небольшой, часты продолжительные ремиссии. При тяжелой форме этого заболевания зуд настолько мучительный, что больные буквально не находят себе места, лишаются аппетита, страдают бессонницей, у них постепенно развивается истощение. Болезнь длится десятилетиями, несколько стихая с возрастом.
Этиология неизвестна. Существуют две основные теории происхождения пруриго Hebra — нервнотрофическая и интоксикационная. В пользу первой теории, сторонниками которой являются А. Г. Поло-тебнов, П. В. Никольский, И. Ф. Зеленев, Т. П. Павлов, С. Т. Павлов и др., говорит наличие у больных стойкого белого дермографизма, расстройства кожных рефлексов, пониженного потоотделения, частое психическое недоразвитие больных (А. К. Шиперская и др.) и т. п. В отношении рефлексов Т. П. Павлов указал на то, что при щекотании подошв у больных пруриго Hebra не возникает обычный при этом рефлекс — сгибание пальцев и отдергивание конечностей. Продолжавший эти наблюдения С. Т. Павлов подметил, кроме того, отклонения от нормального и со стороны брюшного рефлекса.
Интоксикационная теория, сторонниками которой были А. И. Поспелов, А. П. Иордан, J. Jadassohn, Tommasoli и др., основывается на том, что нередко первое высыпание пруриго у детей возникает вслед за желудочно-кишечным расстройством. В то же время эта гипотеза основана на результатах многих исследований обмена веществ у больных этой формой почесухи, в частности отечественных авторов (И. Ф. Зеленев и Веллямович, П. П. Абрамычев, П. И. Фролов и др.), находивших при этом нарушения со стороны хлоридов, фосфатов, мочевой кислоты и др.
П. В. Никольский указывает, что один спазм сосудов в коже при пруриго Hebra был бы достаточен для того, чтобы возник зуд кожи, но к этому присоединяется увеличение порозности сосудистых стенок, которое образовалось, когда больные пруриго в детстве страдали еще только крапивницей, а также паралич потовых центров, в результате которого в коже скопляются также способствующие возникновению зуда токсические продукты обмена веществ. Видимо, правильнее рассматривать нервную и интоксикационную теорию как одно целое, и говорить о нервно-интоксикационном происхождении этого тяжелого заболевания.
Нужно, кроме того, отметить, что обычно даже при тяжелой форме почесухи Hebra на течение болезни благоприятно влияет перемена обстановки, в частности помещение больного в больницу. Надо думать, что благотворное действие при этом нередко оказывает улучшение окружающей обстановки, а также перемена пищевого режима. К сожалению, возвращение больного в привычную обстановку почти всегда ведет к новой вспышке заболевания.
Всегда нужно помнить о том, что иногда клиническая картина почесухи Hebra может развиться как проявление серьезного общего заболевания — prurigo lymphadenica dubrekilh (1905) или prurigo lymphatica Buschke (1902), но эти формы развиваются обычно у взрослых. Пруригинозная сыпь может быть и лимфогранулематозного характера.
Аргентинские дерматологи описывают так называемое меланотическое пруриго (prurigo melanotica), которое впервые появляется в возрасте 30—50 лет, преимущественно у брюнеток, чаще начинается на плечах и распространяется затем ниже, генерализуясь редко. Изменения кожи состоят в основном в пигментации. Заболевание сопровождается зудом. При этом находят заболевание печени или кишечное расстройство (амебиаз, лямблиоз и др.) (Pierini и Borda, I960). Этот своеобразный зудящий дерматоз можно определить как кожный зуд с резкой меланиновой пигментацией.
Прогноз для жизни большей частью благоприятный, но обычно заболевание, особенно его тяжелая форма, длится многие годы, несколько стихая с возрастом.
Лечение почесухи гебры состоит в применении разнообразных общеукрепляющих средств (железо, рыбий жир, витамины и др.)» средств, дезинфицирующих кишечник, антигистаминных препаратов, суховоздушных ванн с последующим укутыванием одеялом на 2 часа и питьем горячих напитков (П. В. Никольский), общих ультрафиолетовых облучений и др. Как уже было отмечено выше, большое значение имеет перемена обстановки, помещение в стационар, а также пребывание на курорте, морские купания, сульфидные ванны. Имеются отдельные указания на терапевтическую эффективность синтетических противомалярийных препаратов.
Местно применяют мази с противозудными и разрешающими инфильтрат средствами; лучше всего при этом пользоваться препаратами дегтя. В некоторых случаях хорошее влияние на зуд оказывают теплые ванны, причем во избежание последующего усиления сухости кожи нужно после водных процедур смазывать кожу жирными кремами.
При осложнении почесухи пиодермией или экзематизацией следует проводить соответствующую местную и общую терапию, водные процедуры при этом запрещаются.
Пруригинозные бубоны лечат теплом, ихтиоловыми компрессами и т. п. В тяжело протекающих случаях показаны кортикостероиды.
Самый простой способ записаться на прием к дерматологу, венерологу без очереди и анонимно - позвонить по телефону
8 903 618 8184 записаться по WhatsApp, через
Записаться на прием к врачу онлайн
Причин по которым пациенты не могут прийти в дерматологическую клинику очень много. Мы не будем их рассматривать, а просто предложим вызвать врача на дом или офис.
Вызвать врача дерматолога на дом в нашей клиники очень просто: позвоните по телефону: 8 903 618 8184 написать по WhatsApp или заполнить форму:
Вызвать врача на дом
Адрес венерологической клиники где можно пройти обследование, курс лечения, сдать анализы без очередей и анонимно
улица Большая Татарская, дом 35, строение 3
10 минут пешком от станций метро Павелецкая, Новокузнецкая, Третьяковская
Синдром Гебры (Hebra) - синонимы, авторы, клиника
Почесуха взрослых (prurigo adultorum) - заболевание, которое характеризуется наличием интенсивного, болезненного, долговременного зуда. На основании анамнеза пациентов, анализа наличия сопутствующих заболеваний и исследований экспертов разных стран можно предполагать, что возникает оно под воздействием негативных экзогенных и эндогенных раздражителей. Заболевание относится к группе нейродерматозов, с преимущественным возникновением высыпаний по типу папуловезикул. Кроме того, присутствуют признаки длительных и множественных расчесов, которые пациенты наносят себе сами ногтями или с помощью окружающих предметов с целью уменьшения зуда кожного покрова. Заболевание характеризуется многообразием клинических проявлений, включая папулы, узелки и бляшки. С точки зрения эпидемиологии неизвестно, какие именно народы и расы наиболее склонны к возникновению данного недуга. У некоторых пациентов наблюдаются зудящие линейные и пугающие царапины, превращающиеся в рубцы и шрамы. Пруриго значительно ухудшает качество жизни больных, приводя к нарушениям со стороны психики. Существует множество клинических признаков заболевания, с ними можно ознакомиться в нашей статье, где представлен анализ современных и наиболее значимых публикаций, посвященных клиническим особенностям почесухи взрослых.
1. Schedel F., Schürmann C., Metze D., Ständer S. Prurigo. Clinical definition and classification. Hautarzt. 2014. vol.65. no.8. P.684-690.
2. Скрипкин Ю.К., Кубанова А.А., Акимов В.Г. Кожные и венерические болезни. М.: ГЭОТАР-Медиа, 2011. 538 с.
3. Адаскевич В.П. Кожный зуд. Дерматологический и междисциплинарный феномен. М.: Издательство Панфилова. БИНОМ. Лаборатория знаний. 2014. 272 с.
4. Мухамадиева К.М., Исматуллоева С.С., Алмаамари А.М.А. Роль психовегетативных дисфункций в патогенезе почесухи // Вестник Авиценны. 2017. Т. 19. № 3. С. 407-412.
6. Федеральные клинические рекомендации. Дерматовенерология 2015: Болезни кожи. Инфекции, передаваемые половым путем. 5‑е изд., перераб. и доп. М.: Деловой экспресс, 2016. 768 с.
7. Weisshaar E., Dalgard F. Epidemiology of itch: adding to the burden of skin morbidity. Acta dermato-venereologica. 2009. vol.89. no.4. P.339-350.
8. Griffiths Christopher, Barker Jonathan, Bleiker Tanya O., Chalmers Robert, Creamer Daniel John. Rook’s Textbook of Dermatology. Wiley & Sons. 2016. Vol.2. Part.7.83. Р. 13-18.
9. Чеботарёв В.В, Тамразова О.Б., Чеботарёва Н.В., Одинец А.В. Дерматовенерология. М.: ГЭОТАР-Медиа. 2013. 345 с.
10. Обыденова К.В., Федоровская А.В. Почесуха. // Евразийский союз ученых. 2015. № 10-1 (19). С.106-108.
11. Бетехтин М.С., Завьялов А.И. Научный вклад Р.Виллана в развитие мировой научной дерматологии // Саратовский научно-медицинский журнал. 2017. Т. 13. № 3. С.681-685.
12. Бутова Ю.С., Скрипкина Ю.К., Иванова О.Л. Дерматовенерология. Национальное руководство. М.: ГЭОТАР-Медиа, 2013. 896 с.
13. Wolff Klaus, Johnson Richard. Fitzpatrick's Color Atlas and Synopsis of Clinical Dermatology. Sixth Edition. McGraw-Hill-Medical. 2009. P.1114-44.
15. Soutor Carol, Hordinsky Maria K. Clinical Dermatology. McGraw-Hill Education, LLC. 1st edition. 2013. P. 286.
16. James William D., Berger Timothy, Elston Dirk. Andrews' Diseases of the Skin: Clinical Dermatology. 11th Edition. Elsevier Inc. 2011. P.51.
18. Pereira M.P., Steinke S., Zeidler C., Forner C., Riepe C., Augustin M., Bobko S., Dalgard F., Elberling J., Garcovic S., Gieler U., Gonçalo M., Halvorsen J.A., Leslie T.A., Metz M., Reich A., Şavk E., Schneider G., Serra-Baldrich E., Ständer H.F., Streit M., Wallengren J., Weller K., Wollenberg A., Bruland P., Soto-Rey I., Storck M., Dugas M., Weisshaar E., Szepietowski J.C., Legat F.J., Ständer S. European academy of dermatology and venereology European prurigo project: expert consensus on the definition, classification and terminology of chronic prurigo. EADV. 2018. vol.32. no.7. P.1059-1065.
20. McAleer M.A, Irvine A.D. The multifunctional role of filaggrin in allergic skin disease. Allergy Clin. Immunol. 2013. vol.131. no.2. P.280-291.
21. Thomas P. Habif. Clinical dermatology: a color guide to diagnosis and therapy. Sixth edition. Saunders. 2016. P. 1008 -1117.
22. Schneider G., Hockmann J., Stumpf A.Hautarzt. Psychosomatic aspects of prurigo nodularis. Hautarzt. 2014. vol.65. no.8. P.704-708.
23. Brenaut E., Halvorsen J.A., Dalgard F.J., Lien L., Balieva F., Sampogna F., Linder D., Evers A.W.M, Jemec G.B.E, Gieler U., Szepietowski J., Poot F., Altunay I.K., Finlay A.Y., Salek S.S., Szabo C., Lvov A., Marron S.E., Tomas-Aragones L., Kupfer J., Misery L. The self-assessed psychological co morbidities of prurigo in European patients: a multicentre study in 13 countries. EADV. 2019. vol.33. no.1. P.157-162.
24. Ständer H.F., Elmariah S., Zeidler C., Spellman M., Ständer S. Diagnostic and treatment algorithm for chronic nodular prurigo. Journal of the American Academy of Dermatology. 2020. vol.82. no.2. P.460-468.
25. Rudolph C.M., Al-Fares S., Vaughan-Jones S.A., Müllegger R.R., Kerl H., Black M.M. Polymorphic eruption of pregnancy: clinicopathology and potential trigger factors in 181 patients. British Journal of Dermatology. 2006. vol.154. no.1. P.54-60.
26. Кочергин Н., Никитина Е., Цыкин А. Некоторые особенности дерматозов беременных // Врач. № 1. С.51-55.
27. Pereira M.P., Nau T., Zeidler C., Ständer S. Chronic prurigo. Hautarzt. 2018. vol.69. no.4. P. 321-330.
28. Zeidler C., Tsianakas A., Pereira M., Ständer H., Yosipovitch G., Ständer S. Chronic Prurigo of Nodular Type: A Review. Acta dermato-venereologica. 2018. vol.98. no.2. P. 173-179.
29. Ouattara I., Eholié S.P., Aoussi E., Bissagnéne E., Raffi F. Can antiretroviral treatment eradicate Prurigo nodularis in HIV infected patients? Med Mal Infect. 2009. vol.39. no.6. P. 415-416.
30. Pereira M.P., Ständer S. How to define chronic prurigo? Exp Dermatol. 2019. vol.28. no.12. P.1455-1460.
31. Zeidler C., Pereira M., Ständer S. The Neuromodulatory Effect of Antipruritic Treatment of Chronic Prurigo. Dermatol Ther (Heidelb). 2019. vol. 9. P.613-622.
32. Pereira M.P., Hoffmann V., Weisshaar E., Wallengren J., Halvorsen J.A., Garcovich S., Misery L., Brenaut E., Savk E., Potekaev N., Lvov A., Bobko S., Szepietowski J. C., Reich A., Bozek A., Legat F. J., Metz M., Streit M., Serra-Baldrich E., Gonçalo M., Storck M., Greiwe I., Nau T., Steinke S., Dugas M., Ständer S., Zeidler C. Chronic nodular prurigo: clinical profile and burden. A European cross-sectional study. EADV. 2020. vol.10. no. 2016-012 to MP. P.1111.
33. Inui K., Ugajin T., Namiki T., Yokozeki H. Chronic prurigo: A retrospective study of 168 cases. The journal of dermatology. 2020. vol. 47. no.3. P.283-289.
34. Курбачева О.М., Павлова К.С. Принципы диагностики и лечения больных с кожными проблемами, сопровождающимися зудом // Русский Медицинский Журнал. 2011. Т. 19. № 11. С. 682-687.
Почесуха взрослых, или пруриго - заболевание с хроническим течением, относящееся к группе нейроаллергодерматозов, основными симптомами которого являются интенсивный зуд и расчесы. Характеризуется возникновением на кожных покровах полушаровидных, уртикарных и узловатых элементов [1].
Корни возникновения данного недуга уходят далеко в прошлое. Так, индийский медик Сушрута в IV-VIII в. до н.э. в своих произведениях описывал средства лечения кожного зуда [2]. А «отец медицины» Гиппократ в 470-377 гг. до н.э. фиксировал клинические проявления пруриго, говоря, что это скорее не заболевание, а обезображивание человека. Дуранте дельи Алигьери в своих песнях «Ада» воспевал возникновение кожного зуда как воздействие кармы на мошенников, лжецов и клеветников: «…их ногти кожу обдирали сплошь, как чешую с крупночешуйной рыбы или с леща соскабливает нож…» [3]. Из этого следует, что попытки описать кожный зуд и этиологию данного недуга делались задолго до того, как Фердинанд Гебра, австрийский ученый, дерматолог, живший в 1816-1880 гг., описал симптомалогию синдрома Гебры (Hebra). Наряду с ним один из известных основателей современной дерматологии англичанин Роберт Виллан описал отдельную нозологическую единицу - пруриго. В основу легла классификация кожных болезней Йозефа Пленка [4].
Почесуха взрослых наблюдается чаще среди женщин в возрасте 18-30 лет, рецидив может наблюдаться во время менопаузы, а у мужчин - в возрасте 40-50 лет [5]. В Российской Федерации централизованная статистика и учет заболеваемости пруриго в настоящее время не ведутся [6]. Согласно исследованию, проведенному в 1976 г. в Великобритании, распространенность пруриго составляла 8,2% [7]. По современным оценкам исследователей, в США и Великобритании распространенность пруриго составляет 1-2,5 на 10 000 человек. При анализе 1037 пациентов с почесухой женщины страдали данным недугом значительно чаще (22%), чем мужчины (13,9%) [8].
В основе этиологии заболевания лежит воздействие эндогенных и экзогенных раздражителей. Эндогенные возникают вследствие эндокринных нарушений при сбое в работе желез внутренней секреции при сахарном диабете, гипотиреозе, тиреотоксикозе, гиперпаратиреоидизме, гиперальдостеронизме, феохромоцитоме, феохромобластоме, синдроме Нельсона; при хронических заболеваниях желудочно-кишечного тракта, таких как гастрит, холецистит, энтерит, колит, язвенная болезнь желудка и двенадцатиперстной кишки; при аутоинтоксикациях, возникающих вследствие непроходимости кишечника, перитонита, а также при распадах опухолевых образований и выделяемых ими токсических метаболитов при лейкозе, злокачественной лимфоме, миеломе; при инвазионных заболеваниях - гельминтозах, протозойных инфекциях (лейшманиозе, малярии, саркоцистозе, дизентерии) [3, 9, 10]. Пруриго часто отмечается у пациентов, страдающих ВИЧ-инфекцией [8], проявляя себя ближе ко II клинической стадии. В Нигерии, в зависимости от географической зоны, число заболеваний составляет от 11% до 46%. В Уганде у 28% пациентов, которые обратились за помощью к дерматовенерологу, выявили явления пруриго, в сопутствующих заболеваниях у 71% отмечалась ВИЧ-инфекция [3]. В 1886 г. профессор И.Ф. Зеленев высказывался о связи болезней нервной системы и дерматологических заболеваний: «Пруригинозный процесс в коже непосредственно зависит от изменений в нервных центрах и, таким образом, представляет собой только припадок заболевания нервной системы» [11]. Далее, в 1926 г. профессор Н.Н. Топорков доказал взаимосвязь неустойчивости нервной системы, которая отвечает сильным зудом в ответ на эмоциональное раздражение, с возникновением пруриго [4], что говорит о существенной роли в возникновении почесухи расстройств вегетативной нервной системы и негативных жизненных событий, таких как одиночество, стрессы, навязчивые состояния, неврозы, психозы. Наиболее подвержены заболеванию люди в депрессивном состоянии (18%), чем не страдающие депрессией (9%) [7].
Среди экзогенных раздражителей отмечают лекарственные средства, такие как витамины, опиоиды, противомалярийные препараты, гормоны. Взаимосвязь с возникновением почесухи и приемом групп других лекарственных средств пока недостаточно изучена. К пищевым аллергенам относят мед, орехи, острые, соленые, копченые продукты, экзотические фрукты, ягоды, грибы. Также отмечают инсектные раздражители при контакте, укусе, ужалении и вдыхании частиц насекомых [6, 10, 12].
В России в 1995 г. Юрий Константинович Скрипкин приводит последнюю общепринятую классификацию нейродерматозов, среди которых выделяет почесуху: детскую, взрослых, узловатую. В данной статье приводим клинические проявления взрослой почесухи, которая существует в двух формах: острой и хронической [6].
В литературе отмечаются случаи возникновения пруриго у беременных. Возможно, патогенез развития связан с тем, что при беременности организм, в том числе и кожный покров, претерпевает значительные изменения со стороны эндокринной, нервной, иммунной, сердечно-сосудистой, пищеварительной, выделительной, половой систем. Также исследователи связывают развитие заболевания с повышением массы тела матери, особенно при многоплодных беременностях, когда происходит сильное растяжение передней брюшной стенки под влиянием развития беременности. Заболевание возникает в последние недели первой беременности либо сразу после родоразрешения (в 15% случаев). На кожных покровах отмечаются самоограничивающиеся, зудящие высыпания - папулы, иногда сливающиеся в бляшки, с частотой встречаемости 1:160 беременностей. Почесуха берет начало в местах стрии живота, где мышцы брюшного пресса наиболее напряжены, плавно переходя на ягодицы и бедра, иногда могут распространяться. При этом возможно повреждение соединительной ткани в местах растяжения мышц, что способствует еще большему развитию воспалительного процесса и ухудшению течения заболевания. Высыпания в среднем разрешаются за 4-6 недель. Почесуха не оказывает негативного влияния на плод и его кожный покров, но может возникать при последующих беременностях матери [25, 26].
Отличительной особенностью хронической почесухи является тяжелое и длительное течение, более 6 недель, с эпизодами ремиссии и рецидивами. Отмечаются хронический, не прекращающийся ни днем, ни ночью интенсивный зуд, наличие единичных или множественных, обычно гиперкератотических, симметрично расположенных зудящих папул и узелков. Происходит распространение зудящих кожных высыпаний. При длительном, длящемся годами интенсивном зуде и на фоне цикла «зуд - царапина» развиваются эрозивные, гиперкератотические, иногда красные либо гиперпигментированные бляшки, узлы или папулы. Отмечаются шрамы от царапин, уродующие кожный покров пациентов. Общее состояние больных ухудшается, заболевание продолжается до конца жизни. Кожа приобретает грязновато-коричневую окраску [18, 27]. На спине участки, свободные от повреждений из-за невозможности пациента дотянуться до них и поцарапать, образуют так называемый знак бабочки. Хроническая форма почесухи вызывает сильнейший зуд, интенсивность по числовой шкале от 0 до 10 составляет 8. Кроме зуда, больные испытывают на травмированных участках кожи сочетание покалывания, жжения, жара и холода [28]. Ученые выявили, что тяжесть хронического пруриго коррелирует с более низким уровнем клеток CD4 при ВИЧ. После антиретровирусного лечения симптомы снижаются, состояние пациента улучшается [29].
С целью определения клинического профиля и тяжести хронической почесухи было проведено исследование с опросом пациентов в медицинских центрах Германии, Северной, Центральной, Восточной и Южной Европы. Всего участвовало 12 стран, были включены 509 пациентов. Они записали за предыдущие 24 часа оценку интенсивности зуда от умеренного до сильного. Результаты оценивались «высокими» у пациентов с более низким уровнем образования, а также у пациентов из Восточной или Южной Европы. Из них 71% больных испытывали зуд часто или всегда, 53% считали, что это явление отрицательно сказывается на их повседневной жизни. 49% пациентов считали интенсивность зуда наиболее обременительным аспектом заболевания, за которым следовали видимые кожные поражения в 21% случаев. Большинство пациентов не знали об этиологии заболевания, которое способствует появлению пруриго (64%). Психические заболевания стояли в сопутствующем диагнозе у 19% [32].
Эксперты Европейской дерматологии и венерологии говорят о необходимости определения классификации терминов для того, чтобы исключить путаницу среди дерматологов и специалистов других медицинских областей. Эксперты обосновывают это тем, что термин «пруриго», введенный более 200 лет назад Робертом Вилланом для описания зудящих папул, использовался без четких критериев для обозначения различных образований. В силу наличия множества возможных клинических проявлений существует и множество терминов, например «пруриго Бенье», «узловатое пруриго», «пигментное пруриго» и т.д. Эксперты Европейской дерматологии выделили хроническое пруриго с четырьмя подтипами: папулезный, узловой, бляшечный и пуповинный тип [18].
Два подтипа хронической почесухи - узловатую и мультиформную - выделили в Токийском медико-стоматологическом университете, где ретроспективно исследовали их клинические особенности. Исследователи сравнили возраст, пол, распространенность сопутствующих заболеваний и выяснили, что пациенты с мультиформным подтипом были старше, в основном страдали мужчины и пациенты, имеющие сопутствующим заболеванием сахарный диабет. Узловатым подтипом пруриго в равной степени страдали мужчины и женщины, а в этиологии наиболее часто значились хронические инфекции [33]. В Российской Федерации почесуху взрослых по Международной классификации болезней относят в код L28.2 другая почесуха, она имеет только две формы [6].
Таким образом, клинические проявления почесухи взрослых многообразны. Авторы медицинских работ утверждают, что очень важно выявить этиологию возникновения почесухи у пациента для дальнейшей тактики ведения, устранения первопричины возникновения заболевания, открытия новых эффективных лекарственных средств, для разработки реабилитационных программ и минимизации медикаментозного воздействия на пациента. Дополнительно потребуется совместная работа медицинских специалистов, таких как невропатолог, гастроэнтеролог, офтальмолог, оториноларинголог, гинеколог [34]. Осведомленность врачей о многообразии клинических проявлений почесухи взрослых открывает возможность выявить и провести дифференцировку заболевания, предупредить возникновение осложнений.
Синдром Гийена-Барре
Синдром Гийена-Барре относится к тяжелым аутоиммунным болезням, поражающим периферическую нервную систему. Наиболее частое проявление - острый тетрапарез, когда движения всеми четырьмя конечностями становятся практически невозможными. Прекращаются и другие движения, в том числе глотание, возможность поднимать веки и самостоятельное дыхание. Несмотря на это, течение болезни доброкачественное, большинство случаев заканчивается выздоровлением. Реже встречаются переход в хроническое течение или рецидивы. Синдром Гийена-Барре встречается во всех странах независимо от уровня их развития с одинаковой частотой - примерно 2 случая на 100 тыс. населения, зависимости от половой принадлежности нет. Болезнь может поражать пациентов самых разных возрастов.
Почему возникает синдром?
Ведущий механизм развития - аутоиммунный. В большинстве случаев начало болезни приходится на первые три недели после острой респираторной или кишечной инфекции. Так как с момента заболевания проходит достаточное количество времени, и характерные для инфекционного процесса симптомы успевают пройти, сами пациенты эти состояния, как правило, не связывают между собой. Причиной могут быть такие возбудители как:
- вирус Эпштейн-Барра или герпес человека 4 типа;
- микоплазма;
- кампилобактер, вызывающий инфекционную диарею;
- цитомегаловирус.

Исследователи обнаружили, что «оболочка» этих возбудителей имеет схожесть с миелиновой оболочкой аксона периферических нервов. Эта схожесть служит причиной атаки нервов антителами, которые изначально вырабатываются и циркулируют в крови в ответ на появление инфекционного агента. Это явление носит название «молекулярной мимикрии» и объясняет то, почему иммунные комплексы атакуют собственные ткани организма.
Описаны случаи, когда синдром возникает после вакцинации, после хирургических операций и абортов, переохлаждения, стресса. В некоторых случаях причину найти не удается.
Как проявляется синдром?
В течение нескольких дней, максимально до 1 месяца, нарастает мышечная слабость в ногах, возникают трудности при ходьбе. Далее слабеют руки, последней страдает мимическая мускулатура. Такие симптомы имеют отдельное название - восходящий паралич Ландри.
Но иногда паралич начинается сверху, с рук, распространяясь вниз, но всегда страдают все конечности.
Каждый пятый случай сопровождается параличом мускулатуры туловища, а именно диафрагмы и межреберных мышц. При таком параличе дыхание становится невозможным, требуется искусственная вентиляция легких.
Частое проявление - бульбарный синдром или двусторонний паралич мышц мягкого неба, когда невозможно глотание и четкая речь.
Вместе с двигательными волокнами иногда поражаются и сенсорные. Развиваются нарушения чувствительности, снижаются сухожильные рефлексы, беспокоят боли в конечностях. Боли носят выраженные «нейропатический» характер — жжение, чувство прохождения тока, покалывания. Тазовые расстройства встречаются редко, но чаще всего бывает задержка мочеиспускания, которая в ряде случаев сочетается с избыточной выработкой мочи.
Присоединяется вегетативная дисфункция, которая проявляется колебаниями артериального давления, сердцебиением, другими нарушениями ритма сердца, потливостью, отсутствием кишечной моторики.
Классификация
Выделяют несколько форм в зависимости от того, повреждается миелиновая оболочка или аксон, по тяжести течения и прогнозу:
- острая воспалительная демиелинизирующая полиневропатия или ОВДП, когда разрушению подвергается миелиновая оболочка;
- острая моторная или сенсорно-моторная аксональная невропатия, когда разрушаются аксоны;
- редкие формы - синдром Миллера-Фишера, острая пандисавтономия и другие, частота которых не превышает 3%.
Диагностические мероприятия
Диагностика основана на рекомендациях ВОЗ. Ведущих диагностических критериев два:
- мышечная слабость в конечностях, которая прогрессирует;
- снижение или отсутствие сухожильных рефлексов с первых дней болезни.
ВОЗ выделяет также дополнительные признаки, подтверждающие диагноз, к которым относятся:
- симметричность поражения;
- симптоматика нарастает не более 4-х недель;
- нарушения чувствительности по типу «перчаток и носков»;
- вовлечение черепно-мозговых нервов, особенно лицевого;
- возможное самопроизвольное восстановление функций после остановки прогрессирования болезни (так называемого «плато»);
- наличие вегетативных нарушений;
- отсутствие гипертермии (если лихорадка есть, то она вызвана другими инфекциями);
- повышение количества белка в спинномозговой жидкости, при этом клеточный состав ее не меняется (белково-клеточная диссоциация).
Окончательная диагностика невозможна без электронейромиографии или ЭНМГ. Это исследование выявляет, какая часть нерва повреждена - миелиновая оболочка или аксон. ЭНМГ также точно устанавливает протяженность поражения, его тяжесть и возможность восстановления.
Так как кроме синдрома Гийена-Барре существует целый ряд острых, подострых и хронических полинейропатий, элекронейромиография позволяет провести между ними дифференциальную диагностику и способствовать выработке правильной тактики лечения.
Нередко для диагностики необходима люмбальная пункция с последующим изучением ликвора, а также могут быть информативны такие анализы как:
- кровь на аутоантитела к структурам нейронов;
- крови на гаммаглобулины класса А (особенно если планируется проведение терапии иммуноглобулинами);
- биомаркеры нейрофиламента (часть цитоплазмы нейрона);
- маркеры тау-протеина (особый белок, разрушающий нейрон).
Специалисты клиники ЦЭЛТ дополнительно используют собственные алгоритмы дифференциальной диагностики, позволяющие достоверно отличить синдром Гийена-Барре от других болезней, вызывающих прогрессирующую мышечную слабость во всех конечностях или тетрапарез.
Наши врачи





Правила лечения
На сегодня известны два основных патогенетических метода лечения синдрома Гийена-Барре, и оба успешно используют специалисты ЦЭЛТ. Это плазмаферез и внутривенная иммунотерапия. Эти методы могут применяться изолированно или использоваться в комплексе, все зависит от конкретной клинической ситуации. Лечение направлено на удаление иммунных комплексов, циркулирующих в крови пациента, или их нейтрализацию. Оба метода лечения равноценны, практически всегда приводят к выздоровлению. Лечение останавливает процесс разрушения периферических нервов, сокращает длительность периода восстановления, способствует уменьшению неврологического дефицита.
Плазмаферез - это операция очищения крови. Чаще всего применяется аппаратный плазмаферез на сепараторах непрерывного действия, в ходе которого отобранная из организма кровь разделяется на форменные элементы (или клетки крови) и плазму (или сыворотку). Все токсические вещества находятся в плазме, поэтому она удаляется. Человеку возвращаются его же кровяные клетки, разведенные при необходимости плазмозамещающими растворами или донорской плазмой. Длительность процедуры - около полутора часов, весь курс состоит из 3-х или 5-ти сеансов. За один раз удаляется не более 50мл/кг массы тела плазмы.
В процессе лечения контролируются показатели крови: электролиты, гематокрит, время свертывания и другие.
Иммунотерапия внутривенная - это введение препарата человеческого иммуноглобулина класса G. Эти иммуноглобулины останавливают выработку антител к собственным нервам, попутно снижая продукцию веществ, поддерживающих воспаление. Эти препараты показаны для патогенетического лечения синдрома Гийена-Барре как у взрослых, так и у детей.
Одновременно с проведением специфического лечения обеспечивается тщательный уход за пациентом, включающий профилактику пролежней, пневмонии, контрактур. Часто требуется лечение сопутствующих инфекций. Выполняется профилактика венозного тромбоза, проводится кормление через зонд, контролируется выделительная функция. Лежачим пациентам выполняется пассивная гимнастика, а также ранняя вертикализация, позволяющая избежать расстройств кровотока. При угрозе развития контактуры (неподвижности суставов) возможны парафиновые процедуры. При необходимости используются двигательные тренажеры на основе биологической обратной связи.
Быстрее восстанавливаются пациенты с поражением миелиновых оболочек, аксональные же повреждения требуют более длительного периода реабилитации. Аксональные поражения часто оставляют за собой неврологический дефицит, трудно поддающийся коррекции.
Профилактика
Основной метод - полное излечение инфекций, которые мы считаем банальными, привычными. Синдром Гийена-Барре часто развивается при незначительном ослаблении иммунитета, который возможен у каждого человека.
Самый простой способ обезопасить себя - проверить текущий иммунный статус. Это займет всего несколько дней, а обнаруженные отклонения можно будет пролечить вовремя.
В распоряжении врачей клиники ЦЭЛТ не только новейшее диагностическое оборудование, но и новейшие лечебные методики, получившие мировое признание. Главная же роль в профилактике принадлежит пациенту, который обращается за обследованием и лечением своевременно.
Читайте также:
