Синдром Штаргардта (Stargardt) - синонимы, авторы, клиника
Добавил пользователь Алексей Ф. Обновлено: 21.01.2026
С Михаилом разговаривать приятно: он умный и начитанный, имеет множество увлечений, а о главном - автогонках - может рассказывать часами. Интеллигентное лицо - очки его украшают. Спокойный, уверенный в себе молодой человек 18 лет от роду. И тем страннее слушать то, что он говорит.
Дистрофия Штаргардта: дорога к слепоте
«Зрение у меня всегда было не очень. Я с детства наблюдался у офтальмолога. Относился к этому спокойно, очки мне не мешали. А в 16 лет начал замечать, что в темноте вижу всё хуже и хуже. К тому же стали выпадать некоторые участки зрения, буквально: здесь вижу, здесь не вижу. Честно говоря, испугался.
Точку поставил визит в военкомат. Медицинская комиссия вынесла вердикт: «абиотрофия сетчатки».
Дальнейшее обследование добавило переживаний. Диагноз звучал как приговор: желтопятнистая дистрофия сетчатки, она же макулодистрофия Штаргардта. Сказали: генетика, и сделать ничего нельзя, заболевание не лечится
Дома с родителями мы перевернул весь Интернет, через знакомых получили консультации нескольких профессоров-офтальмологов, нашли выходы на клиники в Изаиле, Германии, США… Везде, где мы думали, медицина может всё, нам сказали, что надежды на благополучный исход лечения нет.
Вариантов, кроме слепоты, у меня не было.»
«Абиотрофия Штаргардта - это довольно распространённое генетическое заболевание. По статистике она встречается у одного из 20 000 человек. Таким образом, только в России около 7 000 больных, которые по его причине теряют или уже потеряли зрение.
Желтопятнистое глазное дно, другое название этого синдрома, проявляется обычно как раз в подростковом и раннем юношеском возрасте - с 12 до 16 лет. Потеря зрения обычно идет очень резко - в случае Михаила процесс занял всего полгода.
В «УникаМед» Михаил попал в 18 лет, то есть через полтора года после постановки ему диагноза. К этому моменту он практически ничего не видел в темноте, наблюдались скотомы - выпадение участков зрения.
Без коррекции правый глаз видел 20%, левый — 15%. После коррекции оптикой правый глаз — 65%, левый — 55%.
Динамика развития процесса позволяла предположить полную потерю зрения уже к 20 годам».
Дегенерация Штаргардта - не приговор
То, о чём Миша рассказывает дальше, похоже на чудо.
«Мы продолжали искать, и на сайте «УникаМед» прочитали, что синдром Штаргардта они лечат! Поверить было сложно, но мы поехали в Москву.
Уже после первого сеанса регенеративной терапии я стал лучше видеть в темноте, зрение улучшилось. Ощущения такие, будто кто-то наконец помыл грязное лобовое стекло, закрывавшее обзор. Фантастика!
Всего я пока прошел три сеанса - сейчас у меня перерыв. Через 6 месяцев нужно будет пройти еще одну процедуру. Кстати, к автоспорту, в том числе к ночным заездам я уже вернулся!»
«Никаких чудес и никакой фантастики в случае Михаила, конечно же, нет.
Если совсем коротко, то в основе регенеративной терапии - уникальный клеточный аутологичный трансплантат, который стимулирует обновление сетчатки (приставка «ауто» обозначает трансплантат, клетки для которого берутся у самого человека и ему же пересаживаются).
Применение метода показывает положительный эффект практически у всех пациентов. Расширяется поле зрения, улучшается его острота. И если заболевание не является генетическим или сильно запущенным, мы всегда наблюдаем значительное улучшение остроты и качества зрения.
Сложные заболевания, как у Михаила, перестают прогрессировать. Состояние сетчатки и ее питание улучшается - соответственно, значительно улучшается и зрительная функция.
В случае Михаила через три месяца после первого сеанса регенеративной терапии скотомы исчезли, показатели зрения изменились таким образом:
Без оптики: правый глаз — 30%, левый — 25%
С подобранной оптикой: правый глаз — 85%, левый — 75%.
Сейчас, после трех сеансов лечения, Михаил пока не нуждается в дальнейшей терапии, но через 6-8 месяцев он должен снова приехать на осмотр: каким бы волшебным ни казался метод, перепрограммировать гены никто пока не научился, и для поддержания результата лечение нужно периодически повторять.»
Случай Михаила далеко не единичен: к нам в «УникаМед» обращаются люди, от которых отказались другие клиники. И даже на стадии невидения многие из них благодаря регенеративной терапии восстанавливают зрение.
Как проходит процедура
Для выполнения регенеративной терапии не требуется пребывания в стационаре. Пересадка клеточного материала выполняется амбулаторно в течение одного дня: пациент проводит в клинике 10-12 часов.
Но то, что со стороны кажется чудом, на самом деле - результат кропотливой работы.
Изготовление трансплантанта начинается с забора костного мозга. Потом его специальным образом подготавливают. Процедура подготовки клеток очень сложная. Она требует специального оборудования, одновременного участия в процессе нескольких классных специалистов по клеточной биологии и точного последовательного выполнения ряда операций.
Полученный материал по особой технологии вводится пациенту в зависимости от его заболевания и состояния органов зрения.
Вечером, после осмотра офтальмологом, вас выписывают домой до следующей процедуры. Интервал между процедурами определяется индивидуально, но их эффект имеет накопительный характер. И если между первой, второй и третьей процедурой требуется, допустим, три месяца, то между третьей и четвертой может пройти уже полгода. И так далее.
Между процедурами лечение болезни Штаргардта требует регулярного динамического наблюдения офтальмолога, чтобы вовремя «перехватить» возможные потери зрения.
Разумеется, получить эффект легче при лечении заболевания на самой ранней стадии, не дожидаясь потери зрения, полной или частичной. Если замечаете, что зрение становится хуже (особенно в темноте или в сумерках), если сузилось поле зрения, если цвета стали казаться вам менее яркими - найдите время показаться офтальмологу.
Неизлечимых заболеваний становится все меньше - и в клинике «УникаМед» у нас для этого есть все возможности. Регенеративная терапия показывает положительные результаты не только у пациентов с заболеванием Штаргардта, но и в лечении атрофии зрительного нерва, макулодистрофии разной природы, других форм дистрофии сетчатки глаза.
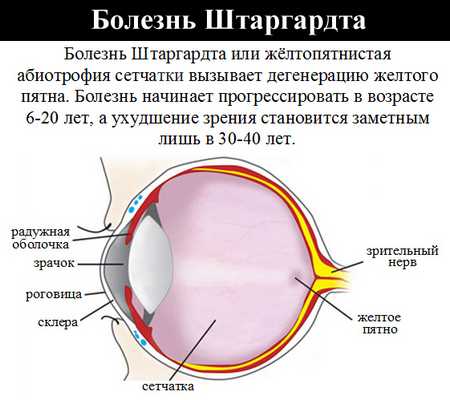
Болезнь Штаргардта
Болезнь Штаргардта - наследственное заболевание сетчатки, которое проявляется дистрофическими изменениями ее макулярной зоны и приводит к потере центрального зрения. Дебют заболевания приходится на детский или юношеский возраст. У пациентов отмечаются центральные скотомы и нарушения цветового зрения. Прогрессирование болезни Штаргардта приводит к полной слепоте. Диагностика проводится с помощью офтальмоскопии, флуоресцентной ангиографии и ЭФИ сетчатки. Для лечения применяется инъекционная терапия (витамины, антиоксиданты, ангиопротекторы), физиотерапия, проводятся реваскуляризирующие операции, разрабатывается методика аутологичной тканевой терапии.
Общие сведения
Другое название болезни Штаргардта - ювенильная макулярная дегенерация - отражает суть заболевания: оно начинается в юном (ювенильном) возрасте и характеризуется поражением макулы - рецепторного аппарата зрительного анализатора. Заболевание описал немецкий офтальмолог Карл Штаргардт в начале ХХ века как врожденное поражение макулярной области глаза, которое передавалось по наследству в одной семье. Типичные офтальмоскопические признаки болезни Штаргардта полиморфны: «атрофия хориоидеи», «бычий глаз», «битая (кованая) бронза». Патогенетическое название патологии - «желтопятнистая абиотрофия сетчатки» - отражает изменения в области глазного дна.
В 1997 году генетики обнаружили мутацию гена АВСR, вызывающую нарушение выработки белка, который должен переносить энергию фоторецепторным клеткам. Неполноценность переносчика АТФ приводит к гибели фоторецепторов сетчатки глаз. Различные виды наследственно обусловленной макулярной дистрофии встречаются в 50% случаев патологии глаз. Из них болезнь Штаргардта составляет около 7%. Нозологическая форма диагностируется с частотой 1:10000 и характеризуется прогрессирующим течением. Двусторонняя патология глаз начинается в молодом возрасте (от 6 до 21 года) и приводит к тяжелым последствиям, вплоть до полной потери зрения. Заболевание имеет социальную значимость, потому что приводит к инвалидности в молодом возрасте.
Причины развития болезни Штаргардта
Наследование не зависит от половой принадлежности пациента и родителей. Патология передается преимущественно по аутосомно-рецессивному типу, то есть наследование патологии не связано с полом (аутосомное - связано с неполовыми хромосомами) и не всегда передается будущему поколению (рецессивный путь наследования). По последним данным врачей-генетиков, патология гена может передаваться и по доминантному типу. При доминантном типе наследования дефектов гена - контролера синтеза белка-транспортера АТФ - заболевание протекает легче и нечасто приводит к инвалидности. Большинство рецепторных клеток макулы (верхушки) желтого пятна глазного дна функционируют. У пациентов с доминантным типом наследования болезнь протекает с минимумом проявлений. Больные сохраняют работоспособность и могут даже водить автотранспорт.
Основная причина дегенерации клеток макулы заключается в том, что они страдают от дефицита энергии. Дефект гена приводит к синтезу неполноценного белка, транспортирующего молекулы АТФ через мембрану клеток желтого пятна - центра сетчатки глаза, в котором фокусируется графическое и цветное изображение. В области желтого пятна нет кровеносных сосудов. Питание клеток-колбочек осуществляется за счет белков-переносчиков АТФ из близлежащей сосудистой оболочки (хориоидеи). Белки переносят через мембрану внутрь клеток-колбочек молекулы АТФ.
В нормальных условиях родопсин фоторецепторов поглощает фотон света, трансформируясь в транс-ретиналь и опсин. Затем транс-ретиналь под действием энергии АТФ, которую приносят белки-переносчики, превращается в ретиналь, который соединяется с опсином. Так восстанавливается родопсин. При наследственной мутации гена образуется неполноценный белок-переносчик. В результате нарушается восстановление родопсина и скапливается транс-ретиналь. Он превращается в липофусцин и оказывает прямое токсическое действие на клетки-колбочки.
Классификация болезни Штаргардта
Виды заболевания зависят от распространенности зоны поражения желтого пятна. В офтальмологии различают следующие формы болезни Штаргардта: центральную, перицентральную, центропериферическую (смешанную). При центральной форме поражаются клетки в центре желтого пятна. Это выражается в выпадении центрального зрения. У больного появляется центральная скотома (от гр. «скотос» - темнота). Выпадает из поля зрения центральная зона. Больной видит изображение с темным пятном в точке фиксации взгляда.
Перицентральная форма характеризуется появлением скотомы в стороне от точки фиксации. Человек способен фокусировать взгляд, но отмечает выпадения в одной из сторон от центра поля зрения в виде полумесяца. Со временем скотома приобретает вид темного кольца. Центропериферическая форма начинается с центра и стремительно распространяется к периферии. Темное пятно разрастается и полностью перекрывает поле зрения.
Симптомы болезни Штаргардта
Проявления заболевания начинаются в возрасте 6-7 лет. У всех пациентов, независимо от типа наследования, наблюдаются центральные скотомы. При благоприятном течении скотомы относительные: пациент видит яркие предметы с четкими контурами и не различает объекты со слабой цветовой гаммой. У многих больных отмечается нарушение цветового зрения по типу красно-зеленой дисхромазии, при которой человек видит светло-зеленый цвет как темно-красный. В то же время, некоторые пациенты не отмечают изменения восприятия цветной гаммы.
В начальной фазе заболевания не изменяются границы периферического зрения, при прогрессировании центральные скотомы расширяются, что приводит к полной слепоте. Одновременно с появлением выпадения центрального зрения уменьшается его острота. В завершающей стадии болезни Штаргардта зрительный нерв атрофируется. Человек полностью теряет зрение. Не наблюдается изменений других органов, как в начальной, так и в терминальной стадии заболевания.
Диагностика болезни Штаргардта
Заболевание начинается в детском возрасте - это один из главных признаков для дифференциальной диагностики. С помощью офтальмоскопии обнаруживается широкое кольцо пониженной пигментации, которое окружает темный центр. Вокруг бледного кольца отмечается следующее кольцо гиперпигментированных клеток. Картина напоминает «бычий глаз» или «кованую бронзу». Фовеолярный рефлекс отрицательный. Макулярное возвышение не определяется. При осмотре желтого пятна отмечаются желтовато-белые пятна разной величины и конфигурации. Со временем границы включений размываются, пятна приобретают серый оттенок либо полностью исчезают.
Во время проведения периметрии при болезни Штангардта отмечаются положительные или отрицательные (пациент их не ощущает) центральные скотомы. При центральной форме заболевания развивается красно-зеленая дейтеранопия. Для периферической формы не характерно нарушение цветового восприятия. Пространственная контрастная чувствительность изменяется по всему диапазону: отсутствует в области высоких частот (в центральном участке до 6-10 градусов) и снижается в области средних частот.
В начальной стадии заболевания отмечается снижение показателей макулярной электрографии при центральной форме дистрофии. При дальнейшем прогрессировании электрические потенциалы не регистрируются. При расположении дистрофии по средней периферической зоне в начальной стадии отмечается нормальная электрография и электроокулография. Затем значения колбочковых и палочковых компонентов элетроретинографии снижаются до субнормальрных. Заболевание протекает бессимптомно - без нарушения остроты зрения и восприятия цвета. Границы поля зрения находятся в пределах нормы. Незначительно снижена темновая адаптация.
С помощью флуоресцентной ангиографии на фоне «бычьего глаза» не обнаруживаются зоны гипофлуоресценции, просматриваются капилляры, «молчащая» или «темная» сосудистая оболочка. В зонах атрофии заметны гиперфлуоресцирующие участки клеток пигментного эпителия сетчатки. Гистологическое исследование в центральной зоне глазного дна определяет повышенное количество пигмента - липофусцина. Отмечается комбинация гипертрофированных и атрофированных клеток пигментного эпителия.
Молекулярно-генетический анализ позволяет заметить мутацию гена до начала проявлений болезни. Чтобы обнаружить замену нуклеотидов, проводится ПЦР в режиме реального времени при использовании нескольких ДНК-зондов - «молекулярных маяков». Дифференциальная диагностика болезни Штаргардта осуществляется с приобретенными лекарственными дистрофиями, пятнами сетчатки Кандори, семейными друзами, ювенильным ретиношизисом, доминантной прогрессирующей фовеальной, колбочковой, колбочно-палочковой и палочко-колбочковой дистрофией.
Лечение и прогноз болезни Штаргардта
Этиологического лечения нет. В качестве общего вспомогательного лечения применяются парабульбарные инъекций таурина и антиоксидантов, введение сосудорасширяющих средств (пентоксифиллин, никотиновая кислота), стероидных препаратов. Проводится витаминотерапия для укрепления сосудов и улучшения кровоснабжения (вит. группы В, А, С, Е). Показаны физиотерапевтические методы лечения: лекарственный электрофорез, ультразвук, лазерстимуляция сетчатки. Применяется методика реваскуляризации сетчатки путем трансплантации в зону желтого пятна пучка мышечных волокон. Разрабатывается патогенетическая регенерационная офтальмологическая технология аутологичной тканевой терапии с помощью стволовых клеток жировой ткани пациента.
Болезнь Штаргардта начинается в раннем возрасте и быстро приводит к инвалидности по зрению. В редких случаях, при доминантном типе наследования, зрение падает медленно. Пациентам рекомендуется наблюдение офтальмолога, прием витаминных комплексов и ношение солнцезащитных очков.
Синдром Штаргардта (Stargardt) - синонимы, авторы, клиника
ФГБУ "НИИ глазных болезней" РАМН
ФГБУ "НИИ глазных болезней" РАМН, Москва
ФГБНУ «Медико-генетический научный центр», ул. Москворечье, 1, Москва, Российская Федерация, 115478
Взаимосвязь структурных и функциональных изменений сетчатки при болезни Штаргардта
Журнал: Вестник офтальмологии. 2016;132(3): 42‑48
Цель — оценить взаимосвязь между структурными нарушениями в зоне раздела наружных и внутренних сегментов фоторецепторов (IS/OS) и функциональными изменениями. Материал и методы. В исследование были включены 45 пациентов (90 глаз) с болезнью Штаргардта. Всем больным проводили исследование цветового зрения, статическую периметрию в пределах 60° поля зрения, электрофизиологические исследования — ганцфельд-электроретинографию (гЭРГ) и мультифокальную электроретинографию (мфЭРГ), аутофлюоресценцию, оптическую когерентную томографию (ОКТ). Результаты. В работе были проанализированы данные 3 групп пациентов, разделенных на основании ОКТ в зависимости от повреждения зоны IS/OS. Установлена сильная прямая связь между степенью поражения IS/OS и показателем периметрии MD. В трех группах не была выявлена разница по показателям толщины сетчатки в фовеа, пара- и перифовеа, а также объема сетчатки в пределах 1, 3 и 6 мм. Во всех трех группах выявлены снижение амплитуд основных волн гЭРГ, а также в разной степени выраженные изменения параметров мфЭРГ. Наиболее постоянным отклонением, наблюдаемым во всех группах и во всех «кольцах», было снижение амплитуды (P1мкВ) и плотности биопотенциала сетчатки (P1 нв/град2). Заключение. Существует прямая корреляция между распространенностью и выраженностью структурных изменений IS/OS по данным ОКТ и зрительными функциями по данным периметрии, нарушением электрогенеза сетчатки по результатам мфЭРГ и гЭРГ.
На сегодняшний день клинический диагноз БШ, главным образом, основан на данных офтальмоскопии, аутофлюоресценции глазного дна, флюоресцентной ангиографии (ФАГ), которая долгое время считалась «золотым стандартом» в постановке диагноза заболевания [4]. Однако характерная картина затемнения сосудистой оболочки — «молчание хориоидеи» при проведении ФАГ наблюдается только у 85% пациентов с Б.Ш. Были описаны случаи пациентов с аутосомно-доминантным наследованием, которые не демонстрировали этот феномен [5, 6].
В настоящее время существует ряд современных технологий функциональной и структурной диагностики, которые обеспечивают количественную и качественную оценки сетчатки. Выявление морфофункциональных особенностей БШ имеет большую значимость для своевременной дифференциальной диагностики среди других центральных дистрофий сетчатки, оценки тяжести поражения и определения тактики ведения пациентов на разных стадиях заболевания.
Оценка функциональных нарушений при БШ основана на данных компьютерной периметрии, мультифокальной и общей электроретинографии [7]. Недавнее введение в практику спектральной оптической когерентной томографии (ОКТ) позволяет детально изучать слои сетчатки с высокой степенью разрешения, определять степень повреждения слоев сетчатки, варьирующую от начальной дезорганизации фоторецепторов до полной потери этого слоя в макулярной области и атрофии подлежащего П.Э. Томография сетчатки является важным методом в диагностике различных заболеваний глазного дна [8]. Характерными структурными нарушениями при БШ являются изменения в зоне раздела наружных и внутренних сегментов фоторецепторов (IS/OS), которые, очевидно, и определяют функциональные нарушения [9].
Цель работы — изучить морфофункциональное состояние сетчатки при БШ и исследовать взаимосвязь между структурными нарушениями в зоне раздела наружных и внутренних сегментов фоторецепторов (IS/OS) и функциональными изменениями.
Материал и методы
В исследование были включены 45 пациентов (90 глаз) с БШ, из них 22 женщины и 23 мужчины. Медиана (нижняя/верхняя квартили) возраста пациентов на момент обследования составляла 33 года (21/48), медиана дебюта заболевания — 15 лет (8/25,5), длительности заболевания — 14 лет (6/27).
Клинические исследования включали визометрию, стандартную кинетическую и статическую периметрию в пределах 60° поля зрения (программа macula examination, Octopus 900, Interzeag AG). Оценивали основные показатели статической периметрии: MD (mean defect) — средний дефект световой чувствительности, sLV (Loss variance), отражающий глубину скотом, и MS — среднее значение световой чувствительности.
Цветовое зрение исследовали по полихроматическим таблицам для исследования цветоощущения Е.Б. Рабкина, учитывали и суммировали неправильные ответы пациентов.
Электрофизиологические исследования включали регистрацию максимальной ганцфельд-ЭРГ (гЭРГ) и мультифокальной ЭРГ (мфЭРГ) и были выполнены на универсальной электрофизиологической установке Tomey ЕР-1000 Multifocal (Германия). При регистрации мфЭРГ использовали стимулирующую матрицу, состоящую из 61 гексагона, радиус стимулируемой зоны — 27,7 угловых градусов. Анализ результатов мфЭРГ проводили в режимах «3D» и «по кольцам», оценивали плотность и топографию биопотенциала центральной зоны сетчатки, латентность (T, мс), амплитуду (А, мкВ) и плотность (D, нв/град 2 ) компонентов N1 и P1.
ОКТ сетчатки проводили на спектральном томографе RTVue-100, протокол исследований MM5 (macula map 5×5 мм). Для оценки анатомо-структурных изменений слоев сетчатки использовали линейный скан (Cross Line), c помощью которого оценивали зону раздела наружных и внутренних сегментов фоторецепторов (IS/OS).
В группы контроля были набраны здоровые добровольцы для проведения ОКТ (17 человек, 33 глаза), электроретинографии (15 человек, 30 глаз). Группы пациентов и группы контроля были однородны по возрасту (критерий Колмогорова—Смирнова, p>0,1).
Аутофлюоресценцию выполняли на приборе Heidelberg Engineering GmbH (Германия).
Статистический анализ проведен с помощью программы Statistica 6.0.
Результаты и обсуждение
На основании офтальмоскопической и аутофлюоресцентной картины в зависимости от наличия дистрофического очага и распространенности желтопятнистой крапчатости пациенты были разделены на 3 группы в зависимости от типа БШ: БШ I типа — 23 пациента (46 глаз) с центральным атрофическим очагом; БШ II типа — 10 пациентов (20 глаз) с центральным атрофическим очагом и локализованными пара- и перифовеальными желтовато-белыми пятнами; БШ III типа — 12 пациентов (24 глаза) с центральным атрофическим очагом и многочисленными желтовато-белыми пятнами по всему глазному дну, а также с обширными атрофическими изменениями РПЭ. На рис. 1, а—в приведены примеры аутофлюоресцентной картины пациентов с тремя типами БШ, на которой дифференцированы участки гиперфлюоресценции, соответствующие отложениям липофусцина в клетках ПЭ, и участки гипофлюоресценции в зонах атрофии ПЭ.
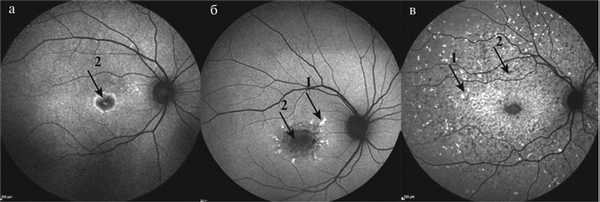
Рис. 1. Аутофлюоресцентная картина глазного дна пациентов с БШ. а — 1-й тип — пациент А. 26 лет; б — 2-й тип — пациент М. 48 лет; в — 3-й тип — пациент Ю. 12 лет; стрелка 1 — участки гиперфлюоресценции, стрелка 2 — участки гипофлюоресценции.
По данным ОКТ пациенты были разделены на 3 группы: 1-я группа (19 пациентов, 37 глаз) — потеря зоны IS/OS в макулярной зоне (горизонтальный и вертикальный размер потери составил 3,11±1,03 и 2,67±0,79 мм соответственно) и сохранение зоны IS/OS на всем остальном протяжении ОКТ-среза сетчатки (рис. 2); 2-я группа (14 пациентов, 26 глаз) — потеря зоны IS/OS в макулярной зоне (горизонтальный и вертикальный размер — 3,77±0,83 и 3,52±1,1 мм соответственно) с распространением дезорганизации IS/OS на всем остальном протяжении ОКТ-среза сетчатки; 3-я группа (13 пациентов, 26 глаз) — распространенная потеря зоны IS/OS на всем протяжении ОКТ-среза сетчатки. У 1 пациента ОКТ-картина сетчатки глаз соответствовала разным стадиям поражения IS/OS-слоя, соответственно они были отнесены к разным группам.
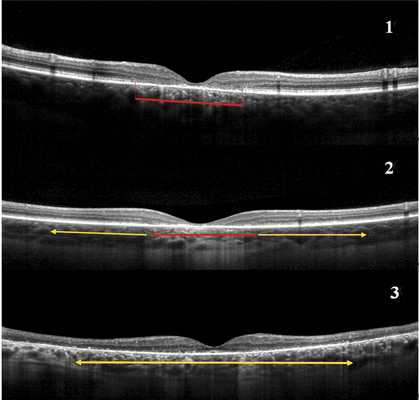
Рис. 2. ОКТ-сканы сетчатки пациентов. 1 — 1-й группы, потеря IS/OS в макулярной зоне (красный фрагмент), на всем остальном протяжении IS/OS-зона сохранена; 2 — 2-й группы, потеря IS/OS в макулярной зоне (красный фрагмент) с распространением дезорганизации IS/OS на всем остальном протяжении (желтая стрелка); 3 — 3-й группы, распространенная потеря зоны IS/OS на всем протяжении (желтая стрелка).
У 1 пациента (1 глаз) была выявлена дезорганизация IS/OS в макулярной зоне и на всем остальном протяжении сетчатки, за счет чего структурно-функциональные изменения были незначительны, острота зрения на данном глазу оставалась высокой (Vis OS=1,0) (рис. 3). В связи с единичным наблюдением данные этого глаза пациента не вошли в настоящее исследование. На парном глазу (OD) была выявлена характерная картина БШ, также в макулярной зоне были обнаружены тубуляции. Эти структурные образования локализуются в наружном ядерном слое сетчатки и визуализируются в виде округлого или овального гипорефлективного пространства, ограниченного вокруг гиперрефлективной каймой. Впервые подобные изменения были обнаружены у пациентов, страдающих возрастной макулярной дегенерацией [10], позже были описаны у пациентов с другой патологией сетчатки — колбочковой дистрофией, Х-сцепленным ретиношизисом и БШ [2, 11].
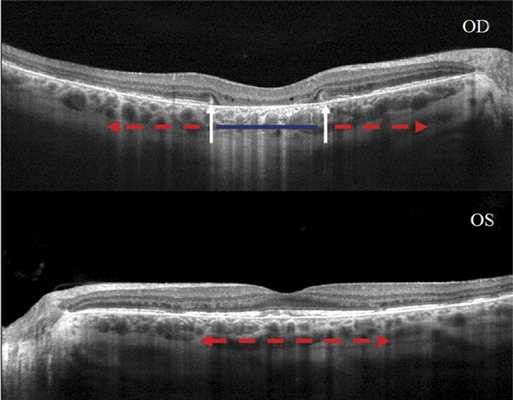
Рис. 3. ОКТ-сканы сетчатки пациента М. 53 лет. OD — потеря IS/OS слоя в макулярной зоне (синий фрагмент) и его дезорганизация на всем остальном протяжении (красные стрелки), тубуляции (белые стрелки); OS — дезорганизация IS/OS-слоя в макулярной области и на всем остальном протяжении (красная стрелка).
В работе были проанализированы данные 3 групп пациентов, разделенных на основании ОКТ в зависимости от повреждения зоны IS/OS. У пациентов с БШ не было выявлено зависимости между степенью повреждения зоны IS/OS и длительностью заболевания, что согласуется с рядом работ, в которых отмечают, что тяжесть БШ в основном определяется генетическим дефектом [12].
Была установлена прямая связь между степенью и размерами повреждения зоны IS/OS и I—III типом БШ (коэффициент гамма-корреляции R=0,5; p<0,05).
Максимально корригированная острота зрения в группах IS/OS составила: в 1-й группе — 0,22±0,27, во 2-й — 0,18±0,1, в 3-й — 0,13± 0,1 (p>0,05) (табл. 1). При исследовании цветового зрения была установлена прямая связь между степенью повреждения зоны IS/OS и количеством нечитаемых таблиц (коэффициент гамма-корреляции R=0,6; p<0,05).
Таблица 1. Характеристика заболевания, остроты зрения и показатели компьютерной периметрии пациентов с БШ по трем основным IS/OS группам Примечание. * — медиана (нижняя/верхняя квартили); ** — среднее значение ± стандартное отклонение.
По данным статической периметрии пациенты были разделены на 3 группы в зависимости от распространенности снижения пороговой световой чувствительности: изменения в пределах центральных 15° поля зрения были выявлены у 21 пациента (42 глаза), в пределах 30° — у 14 пациентов (28 глаз), в пределах 60° — у 10 пациентов (20 глаз). Была установлена сильная прямая связь между степенью повреждения зоны IS/OS и распространенностью периметрических изменений (коэффициент гамма-корреляции R=0,86; p<0,05). Однако площадь функциональных нарушений по результатам периметрии превышала размеры выявленных структурных ОКТ-изменений.
В трех IS/OS группах не была выявлена разница по показателям толщины сетчатки в фовеа, пара- и перифовеа, а также объема сетчатки в пределах 1, 3 и 6 мм (p>0,05), что свидетельствует о выраженных структурных потерях в макулярной зоне вне зависимости от распространенности повреждения IS/OS-зоны. Степень значимости различий показателей при сравнении с данными контрольной группы была высокой во всех IS/OS группах (p<0,001).
При анализе мфЭРГ сравнивали ее основные параметры в 3 группах пациентов и группе контроля (критерий Краскела-Уоллиса). Наиболее существенные различия в этих группах были получены при сравнении значений амплитуды и плотности биопотенциала компонента Р1 (P 1 мкВ, P 1 нв/град 2 ), уровень достоверности варьировал от pp
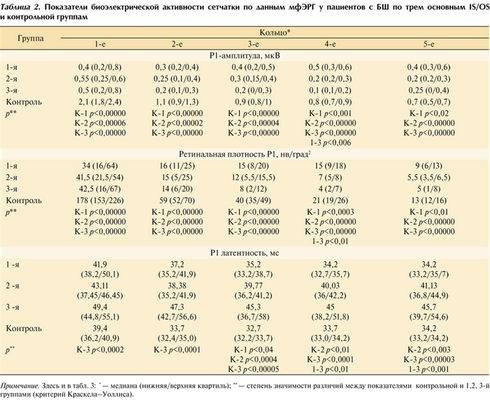
Таблица 2. Показатели биоэлектрической активности сетчатки по данным мфЭРГ у пациентов с БШ по трем основным IS/OS и контрольной группам Примечание. Здесь и в табл. 3: * — медиана (нижняя/верхняя квартиль); ** — степень значимости различий между показателями контрольной и 1,2, 3-й группами (критерий Краскела-Уоллиса).
При анализе мфЭРГ в режиме 3D выявлено нарушение топографии (нормального градиента) биопотенциала центральной зоны сетчатки у всех обследованных пациентов. В 1-й группе эти нарушения распространялись до наружной границы 4-го «кольца» (за пределы перифовеа), во 2-й и 3-й группах — на всю стимулируемую зону сетчатки.
При сравнительном анализе параметров мфЭРГ (P 1 мкВ, P 1 мс, P 1 нв/град 2 ) в трех группах пациентов (критерий Краскела—Уоллиса) в 1—3-х (центральных) «кольцах» мфЭРГ отсутствовали статистически значимые различия между показателями групп (р>0,05), что свидетельствует о примерно одинаковой степени выраженности изменения биопотенциала в этих кольцах независимо от группы. В 4-м и 5-м «кольцах» определялась статистически значимая разница всех анализируемых параметров мфЭРГ между группами (уровень достоверности различий варьировал от pp
Таблица 3. Показатели биоэлектрической активности сетчатки по данным гЭРГ у пациентов с БШ по трем основным IS/OS и контрольной группам
Таким образом, оценка зоны IS/OS, характеризующая целостность фоторецепторов, является важным критерием для анализа поражения сетчатки при Б.Ш. Спектральная ОКТ позволяет получать оптическое изображение поперечного среза сетчатки высокого разрешения, отражающее, как отмечают многие авторы, морфологическую картину, схожую с данными гистологического исследования [13]. Размеры и протяженность потерь и дезорганизации зоны IS/OS явились основой для разделения пациентов на 3 группы по структурному признаку. В данной работе только в одном случае наблюдали дезорганизацию IS/OS без потери этой зоны в макуле. Однако в ряде работ были описаны большие группы пациентов (до 40 человек) с относительно сохранным IS/OS слоем, у которых отмечали сильную корреляцию между целостностью IS/OS-зоны и высокими показателями остроты зрения [2, 14, 15].
Толщина и объем сетчатки в фовеа, пара- и перифовеа в трех исследуемых группах, разделенных по состоянию IS/OS, были значительно снижены по сравнению с показателями контрольной группой. Однако разница по этим показателям между 3 группами не была выявлена, эти результаты согласуются с работой других авторов [14]. У некоторых пациентов ОКТ макулярной зоны сетчатки демонстрировала, помимо характерных для классической БШ структурных нарушений, дополнительные изменения: отложение пигмента, мелкие кисты, утолщение внутренних слоев сетчатки. Как отмечают некоторые авторы, это может быть связано с аллельной гетерозиготностью и с более 600 разновидностью вариантов мутаций в гене ABCA4, что в свою очередь проявляется большим фенотипическим разнообразием БШ [16]. В других работах при длительном наблюдении пациентов авторы отмечают, что типичная для БШ офтальмоскопическая картина со временем может приобретать дополнительные черты, такие как отложение пигмента, выраженные атрофические хориоретинальные изменения, что, возможно, связано с наследуемой мутацией.
Картины аутофлюоресценции и ФАГ глазного дна, демонстрирующие зоны атрофии РПЭ и накопления липофусцина, также важны для оценки распространенности дистрофических изменений сетчатки. Была установлена прямая связь между структурными ОКТ-изменениями IS/OS-зоны и состоянием РПЭ.
Изучение состояния сетчатки с помощью статической периметрии и электроретинографии позволили установить корреляцию между степенью функциональных изменений и поражением IS/OS-зоны по группам. Однако изменения поля зрения, а также биопотенциала сетчатки превышают по площади ее структурные изменения, определяемые аутофлюоресценцией и ОКТ.
Заключение
Оценка зоны IS/OS является важным критерием для анализа поражения сетчатки при Б.Ш. Существует прямая корреляция между распространенностью и выраженностью структурных изменений IS/OS по данным ОКТ и зрительными функциями по данным периметрии, нарушением электрогенеза сетчатки по результатам мфЭРГ и гЭРГ.
Различные модификации электроретинографии при БШ позволяют объективно оценить изменения биоэлектрического потенциала сетчатки в целом и, прицельно, ее центральной зоны. Изменения поля зрения, а также биопотенциала сетчатки превышают по площади ее структурные изменения, определяемые при офтальмоскопии и ОКТ. Морфологические и функциональные (субъективные и объективные) исследования взаимно дополняют друг друга и позволяют получить наиболее полную клиническую картину, оценить степень и распространенность патологического процесса.
Что такое болезнь Штаргардта?
Болезнь Штаргардта — это очень редкая офтальмопатология, которая выявляется у 1-го человека из 20 тысяч. Вылечить ее в настоящее время не представляется возможным. Рано или поздно она приводит к слепоте. Есть лишь способы замедлить патологический процесс. Узнаем, из-за чего он возникает и как проявляется.

Патологию впервые описал врач-офтальмолог Карл Штаргардт. Он охарактеризовал ее как дистрофическое заболевание макулы — центральной области глаза, или желтого пятна. Также он установил, что недуг передается по наследству, а потому — врожденный. При этом дети больного человека не всегда наследуют данную болезнь. Внешние факторы практически не влияют на ее развитие.
В 1997 году была обнаружена мутация гена АВСR, в результате чего нарушается выработка белка, связанного с работой фоторецепторов, которые находятся в сетчатке. Он переносит энергию клеткам с рецепторами. Из-за недостаточной выработки этого белка клетки сетчатой оболочки гибнут.
Макулярная дистрофия внутренней оболочки глаза, обусловленная наследственностью, встречается в 50% случаев. Абиотрофия, или ювенальная макулодегенерация, составляет 7% из них.
изменение границ периферического зрения;
искажение очертаний предметов, прямые линии кажутся волнистыми;
размытость изображения, снижение остроты зрения;
расширение центральных скотом.
Нарушения цветового зрения возникают по типу дихромазии, при которой светло-зеленый цвет воспринимается как темно-красный. В конечном итоге пациент полностью теряет зрение. При этом болезнь может развиваться очень медленно, годами.

Симптоматика определяется типом заболевания. Всего выделяют три ее разновидности:
Центральная. Повреждаются клетки, которые находятся в самом центре макулы. Центральное зрение практически отсутствует. В середине картинки располагается большое пятно, перекрывающее обзор.
Перицентральная. Болезнь поражает клетки по краям макулы. Рассматривая какой-либо предмет, пациент замечает, что одна его сторона выпадает из обзора. Картинка выглядит как месяц темного или черного цвета. С годами он превращается в круг.
Смешанная. Пигментная абиотрофия сетчатой оболочки начинается в центре макулы и постепенно распространяется на ее периферию.
Предсказать скорость прогрессирования патологии невозможно.
Иногда зрение не изменяется на протяжении нескольких лет. Пациенты начинают верить, что болезнь отступила, но через некоторое время симптомы ее усиливаются и наступает слепота.
Диагностика болезни
Скотомы, нарушения цветового зрения — это признаки, которые бывают при различных глазных заболеваниях — катаракте, отслойке сетчатки и др. Чтобы поставить диагноз «Болезнь Штаргардта», назначается много диагностических процедур. В их числе стандартные офтальмологические:
тест на цветовое зрение по таблицам Рабкина;
Также применяются специальные методы, позволяющие получить более точные данные:
электроокулография — процедура, которая дает возможность оценить состояние фоторецепторов сетчатки;
электроретинография — изучение функций внутренней оболочки глаза;
кампиметрия — измерение центрального зрения;
ЭФИ (электрофизиологическое исследование) глаз — диагностический метод, позволяющий оценить функции сетчатой оболочки, зрительного нерва и состояние коры головного мозга;
флюоресцентная ангиография — изучение сосудов посредством введения в кровеносную систему светящегося раствора;
оптическая когерентная томография — процедура, применяемая для обнаружения патологий зрительного нерва и сетчатки.
Все эти методы позволяют выявить патологию, определить ее вид, характер повреждения сетчатки, скорость развития патологического процесса. После этого назначается лечение. Его можно рассматривать и как профилактику снижения зрения. Остановить прогрессирование патологии невозможно.
Болезнь Штаргардта: лечение
Этиологической терапии не существует. Офтальмопатология является наследственной. Ученые выявили мутацию гена, способы его передачи, но воздействовать на этот механизм не представляется возможным. Также нельзя скорректировать ухудшение зрения с помощью очков/контактных линз.
Все лечебно-профилактические мероприятия направлены на замедление прогрессирования патологии. Врачи пытаются отсрочить момент, когда больной полностью утратит зрительные функции. Немного улучшить состояние пациента помогают:
сосудосуживающие глазные капли;
уколы аминокислоты таурин;
витаминные комплексы, особенно с содержанием витаминов А, В, С, Е;
средства, улучшающие кровообращение.
Больным рекомендуется соблюдать диету с ограниченным потреблением ретинола — витамина А. Также рекомендуется носить солнцезащитные очки, защищающие от солнечного ультрафиолета. Все эти меры не помогут остановить болезнь. Однако лучше использовать все возможные средства.

Применяются и другие способы лечения болезни Штаргардта:
Первый метод предполагает установку мышечных волокон в пораженную дистрофией макулу. На определенное время это позволяет сохранить зрительные функции. Но с годами темное пятно расширяется, поэтому избежать слепоты не получается.
Аутологичная терапия — это одна из самых современных методик лечения, предусматривающая использование стволовых клеток, которые берутся непосредственно из жировой ткани пациента. Терапия абсолютно безопасна для пациента, так как осложнениями не сопровождается.
Она основана на замене разрушенных клеток новыми. Существует риск их отторжения, но он минимален в связи с тем, что применяется не донорские клетки, а ткани самого больного. На какое-то время удается восстановить утраченное зрения.
Такая терапия не дает 100-процентного результата, но пока она является максимально эффективной, так как позволяет временно восстановить остроту зрения даже при сильном его ухудшении.
В конечном итоге болезнь заканчивается для больного инвалидностью. Обычно ему присваивают вторую группу.
Болезнь Штаргардта — макулярная дистрофия сетчатки глаза — причины и лечение в Москве
Болезнь Штаргардта является наследственной патологией сетчатки глаза, сопровождающейся дегенеративными изменениями в ее центральной (макулярной) зоне, что влечет за собой утерю центрального зрения. Как правило, заболевание проявляет себя еще в детском или юношеском возрасте центральными скотомами и нарушением цветовосприятия. При прогрессировании болезни Штаргардта, исходом процесса становится полная слепота. В диагностике патологии, применяют офтальмоскопию, флуоресцентную ангиографию и ЭФИ сетчатки. В качестве лечения, назначается инъекционная терапия препаратами витаминов, ангиопротекторов, антиоксидантов, а также физиотерапия. Кроме того, проводятся реваскуляризирующие операции и применяется, находящаяся в разработке, методика аутологичной тканевой терапии.
Рис.1 Центральная (макулярная) зона сетчатки, которая поражается при болезни
О патологии
Болезнь Штаргардта носит и другое официалное название - ювенильная макулярная дегенерация. Именно оно наиболее полно отражает суть заболевания, которое начинается в раннем (ювенильном) возрасте. Патология характеризуется поражением области макулы сетчатки - рецепторного аппарата анализатора зрения. Второе свое название болезнь получила по имени, описавшего ее в начале ХХ века, немецкого ученого Карла Штаргардта. Патология описывалась, как врожденное поражение сетчатки в макулярной области, которое было характерно для представителей одного рода. Офтальмоскопические признаки заболевания полиморфны и типичны, это: атрофия хориоидеи, «битая (кованая) бронза», «бычий глаз». Патогенетически, заболевание обозначается, как «желтопятнистая абиотрофия сетчатки», что отражает визуализируемые изменения на глазном дне.
Болезнь вызывает мутация гена АВСR с нарушением синтеза белка, отвечающего за транспорт энергии клеткам-фоторецепторам. Это было выяснено учеными-генетиками в 1997 году. Тогда же удалось доказать, что патология переносчика АТФ становится причиной гибели фоторецепторов сетчатой оболочки.
Наследственно обусловленная макулярной дегенерация - заболевание довольно частое, ее различные виды встречаются практически в половине случаев патологии глаз. Болезнь Штаргардта, при этом, составляет примерно 7% всех случаев. Частота нозологической формы болезни, характеризующейся прогрессирующим течением, составляет 1:10000 в популяции.
Патология имеет двусторонний характер течения, дебютирует в молодом возрасте (до 21 года) и очень часто становится причиной полной потери зрения. Социальная значимость болезни Штаргардта весьма велика, так как она приводит к инвалидности людей молодого трудоспособного возраста.
Причины возникновения
Наследование патологии происходит вне зависимости от половой принадлежности детей и родителей. Преимущественно она передается аутосомно-рецессивным путем, то есть поражает потомков родителей-носителей заболевания, однако не в 100% случаев. Последние исследования врачей-генетиков выявили, что патология гена способна передаваться также и по доминантному пути.
В случае доминантного пути передачи болезни, она протекает легче и к инвалидности приводит довольно редко. Большинство клеток- рецепторов в макуле (не верхушке желтого пятна) остаются функциональными, поэтому патология имеет минимум проявлений. Люди сохраняют работоспособность, острота зрения позволяет даже водить автотранспорт.
Главная причина дегенерации макулярных клеток — дефицит энергии. Из-за дефекта гена, происходит синтез неполноценного белка, участвующего в транспорте молекул АТФ через мембрану клеток макулы - центра сетчатой оболочки, где и фокусируется цветное, графическое изображение. Желтое пятно не имеет кровеносных сосудов. В питании клеток-колбочек принимают участие белки-переносчики АТФ из прилегающей сосудистой оболочки (хориоидеи). Именно эти белки транспортируют через мембрану молекулы АТФ внутрь клеток-фоторецепторов.
Родопсин фоторецепторов в нормальных условиях поглощает фотоны света, с превращением в опсин и транс-ретиналь. Затем, под действием энергии АТФ, приносимой белками-переносчиками, транс-ретиналь превращается в ретиналь и соединяется с опсином. Это процесс восстановления родопсина. Наследственная мутация гена становится причиной синтеза неполноценного белка-переносчика. В итоге восстановление родопсина нарушается, происходит скопление транс-ретиналя. Он трансформируется в липофусцин, который и оказывает токсическое воздействие напрямую на клетки-колбочки.
Типы и виды болезни Штаргардта
Видовая изменчивость патологии объясняется распространенностью зоны поражения макулярной области. Специалисты классифицируют болезнь Штаргардта по следующим формам:
- Центральная.
- Перицентральная.
- Центропериферическая (смешанная).
Центральная форма характеризуется поражением клеток в центре области макулы. Процесс сопровождается выпадением центрального зрения. Человек отмечает появление центральной скотомы (темного пятна перед глазом). Происходит выпадение центральной зоны из поля зрения и видимое изображение в точке фиксации взгляда получается с темным пятном.
Перицентральная форма сопровождается возникновением в стороне от точки фиксации скотомы. Способность фокусировать взгляд остается, но с одной из сторон от центра поля зрения отмечает его выпадение в форме полумесяца. С прогрессом заболевания, скотома принимает вид темного кольца.
Для центрально-периферической формы характерно стремительное ухудшение зрения от центра к периферии. Постепенно разрастаясь, темное пятно полностью закрывает поле зрения.
Рис.2 Важность посещения врача-офтальмолога: чем раньше выявлена болезнь, тем выше шанс сохранить зрение
Признаки заболевания
Начало заболевания приходится на возраст 6-7 лет, тогда же возникают первые его симптомы. Вне зависимости от типа наследования, все пациенты отмечают возникновение центральных скотом. Ели, течение заболевания благоприятное, скотомы относительные. Те есть, человек способен четко видеть яркие предметы, но объекты, имеющие слабую окраску, различает хуже. Многие больные страдают нарушением цветовосприятия по типу красно-зеленой дисхромазии, когда человек воспринимает зеленый цвет, как красный. Правда, в некоторых случаях пациенты изменения цветового восприятия могут не отмечать.
В начальной стадии болезни, границы периферического зрения не изменены, но при прогрессировании центрально скотомы, они сужаются, что ведет к слепоте.
Одновременно с выпадением центрального зрения снижается и его острота. На итоговой фазе болезни Штаргардта происходит атрофия зрительного нерва и человек теряет зрение полностью. Изменений прочих глазных сред, на всех стадиях, не наблюдается.
Диагностика
Начало заболевания характерно для детского возраста. Это и является одним из главных диагностических его признаков.
При выполнении офтальмоскопии, выявляется широкое кольцо локализованное на сетчатке с пониженной пигментацией. Оно окружает темный центр здоровой ткани. Вокруг бледного кольца имеется следующее кольцо клеток с гиперпигментацией. Офтальмологи определяют такую картину, как «бычий глаз», «кованая бронза». Макулярное возвышение не определяется, нет фовеолярного рефлекса. При осмотре области макулы определяются бело-желтые пятна разной конфигурации и размера. Границы включений имеют тенденцию размываться со временем, пятна становятся сероватыми либо исчезают полностью.
Проведение периметрии при болезни Штангардта выявляет отрицательные (неощутимые) и положительные центральные скотомы. Определяется красно-зеленая дейтеранопия, если патологический процесс протекает в центральной форме, и отсутствие нарушения цветового восприятия в периферической форме. Изменение пространственной контрастной чувствительности по всему диапазону: ее отсутствие в зоне высоких частот (в центральном участке до 6-10 градусов), снижается в зоне средних частот.
Показатели макулярной электрографии в начальной стадии заболевания при центральной форме дистрофии снижены. Электрические потенциалы при дальнейшем прогрессировании процесса, не регистрируются. Если дистрофии расположена по средней периферической зоне, нормальная электрография регистрируется только в начальной стадии. Затем при электроретинографии, значения компонентов колбочек и палочек становятся субнормальными. Болезнь протекает без симптомов: нарушения остроты зрения и цветовосприятия не наблюдается. В норме границы поля зрения. Темновая адаптация снижена незначительно.
Флуоресцентная ангиография на фоне «бычьего глаза» зоны гипофлуоресценции не обнаруживает, капилляры просматриваются, сосудистая оболочка — «молчащая» или «темная».
Гиперфлуоресцирующие области клеток пигментного эпителия заметны лишь в зонах атрофии сетчатки. При гистологическом исследовании центральной зоны глазного дна выявляется излишнее количество липофусцина. Клетки пигментного эпителия гипертрофированы и атрофированы в комбинации.
Проведение молекулярно-генетического анализа выявляет мутацию гена, произошедшую до начала заболевания. Изменение нуклеотидов, обнаруживается в режиме реального времени при проведении ПЦР с применением нескольких «молекулярных маяков» — ДНК-зондов. Болезнь Штаргардта следует дифференцировать с приобретенными дистрофиями на фоне приема лекарств, пятнами Кандори, ювенильным ретиношизисом, семейными друзами, а также с прогрессирующей доминантной фовеальной колбочковой, палочко-колбочковой и колбочко-палочковой дегенерацией.
Рис.3 Осмотр глазного дна (офтальмоскопия) — основной метод диагностики заболевания
Лечение и прогноз
Как такового лечения, направленного на устранение заболевания нет. В качестве общей терапии показано внутриглазное введение таурина и антиоксидантов, расширяющих сосуды средств (никотиновая кислота, пентоксифиллин), гормональных препаратов. Также назначается витаминотерапия (вит. группы В, А, С, Е), направленная на укрепление сосудов, чтобы улучшить кровоснабжение и питание пораженной зоны сетчатки, ретинопротекторы (ретиналамин). Целесообразно проведение физиотерапии: ультразвук, лекарственный электрофорез, лазерстимуляция.
В домашних условиях пациенты могут смомостоятельно применять вакуумный массаж — прибор АМВО-01, разработанный специалистом по заболеваниям сетчатки у детей д.м.н., профессором Сидоренко Евгением Ивановичем, который не только стабилизирует процесс, но и даёт повышение остроты зрения и расширение полей.
Из хирургических методик нами применяется реваскуляризация заднего отдела глаза — процедура по активизации обменных процессов и улучшению кровоснабжения центральной области сетчатки.
В стадии разработки находится метод реваскуляризации сетчатки посредством пересадки в макулярную зону пучка мышечных волокон. Кроме того, на этапе исследования находится технология патогенетической регенерационной аутологичной тканевой терапии с использованием стволовых клеток жировой ткани пациента.
Для болезни Штаргардта характерно начало в детском возрасте и быстрый прогресс до состояния инвалидизации пациента по зрению. Зрение ухудшается медленно только в очень редких случаях доминантного пути наследования заболевания. В качестве профилактики, рекомендуется прием витаминных комплексов, длительное наблюдение офтальмолога, применение солнцезащитных очков.
Пациенты с болезнью Штаргардта нуждаются в динамическом наблюдении врача-ретинолога. Специалисты нашей клиники - признанные лидеры лечения заболеваний сетчатки. Применение инновационных технологий, новейшая аппаратура от лучших мировых производителей и индивидуальный подход к каждому пациенту, обеспечивают гарантированное получение максимально высоких результатов даже в самых сложных случаях.
Читайте также:
