УЗИ, МРТ при цитомегаловирусной инфекции у плода
Добавил пользователь Валентин П. Обновлено: 28.01.2026
Цитомегаловирусная инфекция (синонимы: цитомегалия, вирусная болезнь слюнных желез, инклюзионная цитомегалия, болезнь с включениями; salivarygland virus disease - англ.) хроническая антропонозная болезнь вирусной этиологии, характеризующаяся многообразием форм патологического процесса от латентной инфекции до клинически выраженного генерализованного заболевания [1,2].
Пользователи протокола: терапевты, врачи общей практики, инфекционисты, неврологи, дерматовенерологи, акушер-гинекологи, анестезиологи-реаниматологи, организаторы здравоохранения.
Класс I - польза и эффективность диагностического метода или лечебного воздействия доказана и и/или общепризнаны
Класс III - имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
• определение ДНК ЦМВ в ликворе, плевральной жидкости, отделяемого цервикального канала и уретры и т.д. в зависимости от органной патологии методом ПЦР;
• биохимическое исследование крови (билирубин и фракции, АЛТ, АСТ, тимоловая проба, амилаза, глюкоза);
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: не проводятся.
Жалобы: зависят от клинической формы инфекции, путей заражения и степени выраженности иммуносупрессии.
• отягощенный гинекологический анамнез (цервицит, эктопия шейки матки, хронический эндометрит и т.д.);
Физикальное обследование: зависит от клинической формы инфекции, путей заражения и степени выраженности иммуносупрессии.
У ВИЧ-инфицированных в 3 и 4 стадии: клиника манифестных форм с поражением легких, ЦНС, глаз (ретинит), ЖКТ, печени.
Иммунограмма: снижение CD4+, CD8+, снижение CD4\CD8.
• анти ЦМВ IgM -маркёры «свежей», первичной инфекции определяются от начала заболевания до 8- 12 нед после заражения;
• рентгенография органов грудной клетки (интерстициальная пневмония, фиброзирующий бронхиолит и альвеолит);
• спинномозговая пункция (лимфоцитарный плеоцитоз, повышение белка в ликворе при подозрении на менингит, энцефалит);
• офтальмоскопия (на сетчатке по периферии глазного дна очаги белого цвета с геморрагиями по ходу ретинальных сосудов, при прогрессировании инфильтрация с зонами атрофии и очагами кровоизлияний).
Дифференциальный диагноз
Алгоритм дифференциальной диагностики при цитомегаловирусной болезни
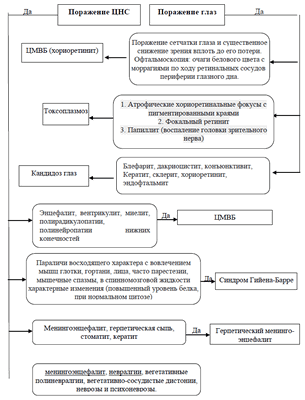
Лечение
• У иммунокомпроментированных - подавление репликации вируса, купирование клинических проявлений, профилактика осложнений.
Диета: стол № 15 с коррекцией в зависимости от клинической формы.
• интерферон рекомбинантный альфа 2 b 500 000 МЕ или 1 000 000 МЕ (виферон) по 1 свече 2 раза в сутки №10, далее 500 000 МЕ по 1 свече 2 раза в сутки через 12 часов 2-3 раза в неделю 1-12 месяцев в зависимости от клинической формы и течения болезни.
• меглюмина акридонацетат в таблетках: по 0,45 г (3 табл.) на прием 1 раз в сутки per os по схеме 1,2,4,6,8,11,14,17,21,23 дни., в инъекциях 12,5% - 2 мл в/м, 1 раз №10.
Латентная ЦМВИ: лечение не проводится.
• интерферон рекомбинантный альфа 2 b 500 000 МЕ или 1 000 000 МЕ по 1 свече 2 раза в сутки №10, далее 500 000 МЕ по 1 свече 2 раза 3 раза в неделю 1-12 месяцев;
• Панавир 0,004% раствор 5 мл в/в медленно №5 по схеме три инъекции с интервалом 48 часов, две последующие - с интервалом 72 часа и суппозитории ректальные Панавир 200 мкг, по 1 свече на ночь 3-х кратно в течении 1-ой недели с интервалом 48 часов и 2-х кратно в течении 2-ой недели с интервалом 72 часа. Курс лечения 11 дней.
• Валганцикловир 900 мг в сутки или Ганцикловир 5 мг/кг/сутки в течение месяца, перенёсшим ЦМВ - ретинит на фоне ВААРТ до повышения CD4 - лимфоцитов более 100 кл/мкл, сохраняющегося не менее 3 месяцев. Поддерживающий курс у этих больных при других манифестных формах ЦМВИ должен быть не менее одного месяца.
С целью дезинтоксикационной терапии: обильное питье из расчета 20-40 мл/кг массы тела, в тяжелых случаях - инфузионная терапия: кристаллоиды (физиологический раствор, ацесоль, лактосоль, ди- и трисоль и т.п.) и коллоиды (реополиглюкин) в соотношении 3:1 - 2:1;
С десенсибилизирующей, противотёчной, противовоспалительной целью при генерализованной ЦМВИ с поражением ЦНС: кортикостероидные препараты: преднизолон 2-5 мг\кг в сутки;
Антибактериальная терапия при наслоении бактериальной инфекции рекомендуется монотерапия одно нижеследующих препаратов:
С иммуномодулирующей и противовирусной целью рекомендуется монотерапия одно нижеследующих препаратов:
• интерферон рекомбинантный альфа 2b - суппозитории 150 000 МЕ, 500 000 МЕ, 1 000 000 МЕ, 3 000 000 МЕ;
• иммуноглобулин человека антицитомегаловирусный - раствор 500 ЕД (10мл), 1000 ЕД (20мл), 2500 ЕД (50мл);
• панавир - раствор для иньекций в ампулах по 5 мл с концентрацией 0,04 мг/м; суппозитории ректальные;
• Рингер раствор для инфузий, 200 мл и 400мл;
С профилактической целью - ганциклавир (реципиентам костного мозга, сердца, почек и печени; больным, получающим цитостатические препараты, беременным).
Препараты (действующие вещества), применяющиеся при лечении
| Валганцикловир (Valganciclovir) |
| Ганцикловир (Ganciclovir) |
| Декстран (Dextran) |
| Иммуноглобулин человека против цитомегаловируса (Immunoglobulin against human cytomegalovirus) |
| Интерферон альфа 2b (Interferon alfa-2b) |
| Калия хлорид (Potassium chloride) |
| Кальция хлорид (Calcium chloride) |
| Меглюмин (Meglumine) |
| Натрия хлорид (Sodium chloride) |
| Очищенный экстракт побегов растения Solanum tuberosum (The purified extract of plant shoots Solanum tuberosum) |
| Преднизолон (Prednisolone) |
| Цефепим (Cefepime) |
| Цефтриаксон (Ceftriaxone) |
| Ципрофлоксацин (Ciprofloxacin) |
Госпитализация
Показания для экстренной госпитализации: больные, в. т.ч. беременные с тяжелыми генерализованными формами цитомегаловирусной болезни.
Показания для плановой госпитализации: больные, в т.ч. беременные (в сроки до 30 недель беременности в инфекционный стационар, свыше 30 недель в родильные дома, перинатальный центр) с клинически выраженными формами ЦМВИ.
Информация
Источники и литература
Информация
1) Кошерова Бахыт Нургалиевна - доктор медицинских наук, профессор, РГП на ПХВ «Карагандинский государственный медицинский университет», проректор по клинической работе и непрерывному профессиональному развитию, главный внештатный инфекционист МЗСР РК, высшая квалификационная категория.
2) Кулжанова Шолпан Адлгазыевна - доктор медицинских наук, заведующая кафедрой инфекционных болезней и эпидемиологии, АО «Медицинский университет Астана», высшая квалификационная категория.
3) Нуралинова Гульнар Инжикановна - кандидат медицинских наук, РГП на ПХВ «Государственный медицинский университет города Семей», доцент кафедры неврологии, психиатрии и инфекционных болезней, высшая квалификационная категория.
4) Маукаева Сауле Боранбаевна - кандидат медицинских наук, РГП на ПХВ «Государственный медицинский университет города Семей», доцент кафедры неврологии, психиатрии и инфекционных болезней, высшая квалификационная категория.
5) Абуова Гульжан Наркеновна - кандидат медицинских наук, РГП на ПХВ «Южно-Казахстанская государственная фармацевтическая академия», заведующая кафедрой инфекционных болезней и дерматовенерологии, высшая квалификационная категория.
6) Ким Антонина Аркадьевна - кандидат медицинских наук, РГП на ПХВ «Карагандинский государственный медицинский университет» заведующая кафедрой инфекционных болезней.
7) Ихамбаева Айнур Ныгымановна - АО «Национальный центр нейрохирургии», врач - клинический фармаколог.
Рецензенты:
Шопаева Гульжан Амангельдыевна - доктор медицинских наук, РГП на ПХВ «Казахский национальный медицинский университет имени С.Д. Асфендиярова» профессор кафедры инфекционных и тропических болезней.
Указание условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Цитомегаловирусная инфекция у детей
Цитомегаловирусная инфекция у детей — это инфекционное заболевание, которое вызвано цитомегаловирусом и поражает слюнные железы, внутренние органы, ЦНС. В детстве патология чаще возникает при трансплацентарном или интранатальном заражении. Локализованные формы проявляются сиаладенитом, гепатитом, нефритом и т. д., распространенный вариант инфекции характеризуется поражением головного мозга, легких, почек и органов ЖКТ. Диагностика предполагает идентификацию возбудителя цитологическими, гистологическими, серологическими и молекулярно-биологическими методами. Лечение цитомегаловирусной болезни проводится специфическим иммуноглобулином и противовирусными препаратами.
МКБ-10
Общие сведения
Заражение цитомегаловирусной инфекцией (ЦМВИ) наблюдается у 20%‒60% всего детского населения, но в большинстве случаев оно протекает бессимптомно. Внутриутробное инфицирование вирусом от больной матери происходит в 30-50% случаев, при этом до 18% младенцев после рождения имеют клинические симптомы. Учитывая полиморфизм клинической картины, ранняя диагностика и лечение у детей затруднены. Цитомегаловирусная инфекция представляет серьезную опасность, особенно для плода и новорожденного, у которых заболевание, как правило, вызывает необратимые осложнения.
Причины
Болезнь вызвана герпесвирусом 5 типа — Cytomegalovirus hominis. Он имеет 6 штаммов: Davis, AD 169, Kerr, C-87, Esp, Towne, причем ребенок может быть инфицирован сразу несколькими подтипами возбудителя. Цитомегаловирус (ЦМВ) имеет ДНК-геном, отличается медленной репликацией и сравнительно низкой вирулентностью. Он термолабилен, уничтожается при температуре более 56°С, но длительно сохраняет жизнеспособность в комнатных условиях.
При врожденной ЦВМИ передача вируса к плоду происходит трансплацентарно, при перинатальной инфекции — путем контакта с вагинальными выделениями матери, грудным молоком или препаратами крови. Риск заражения увеличивается, если мать с острой формой болезни не получает специфическое лечение. В постнатальном периоде ребенок чаще всего заражается от ближайших родственников и сверстников воздушно-капельным или контактно-бытовым путем.
Патогенез
Попадая в кровь, вирус реплицируется в лейкоцитах, моноцитах и макрофагах и в дальнейшем он пожизненно сохраняется в лимфоцитарных органах. Зачастую процесс выражается в виде латентной инфекции, при которой у ребенка нет симптомов, и ему не требуется лечение. Активность цитомегаловируса зависит от состояния иммунитета: при физиологической иммунной недостаточности, которая наблюдается у детей раннего возраста, риск манифестной цитомегаловирусной инфекции возрастает в разы.
При угнетении защитных факторов организма (системы интерлейкинов, Т-лимфоцитов) возбудитель разносится с кровью к разным органам. К нему наиболее чувствительны клетки слюнных желез, где часто происходят специфические патоморфологические изменения. Заболевание характеризуется образованием крупных цитомегаловирусных клеток («совиный глаз»). Кроме того, при ЦМВИ возможен фиброз железистых органов, отложение кальцификатов.
В детской инфектологии различают врожденную (внутриутробную) и приобретенную формы патологии. По течению инфекция бывает острой (до 3 месяцев), подострой (3-6 месяцев), затяжной (6-12 месяцев) и хронической (более 1 года). По клиническим признакам выделяют локализованный (сиаладенит, нефрит, гепатит, энцефалит) и генерализованный вариант. С учетом тяжести течения цитомегаловирусную болезнь делят на 3 степени:
- Легкая. Отличается незначительными патоморфологическими изменениями во внутренних органах, которые не сказываются на их функциональной активности.
- Среднетяжелая. Проявляется выраженными органическими поражениями в сочетании с клиническими симптомами и расстройством функции некоторых внутренних органов.
- Тяжелая. Манифестирует тяжелыми органическими патологиями, резко выраженной интоксикацией и генерализованным характером поражения.
Симптомы
Врожденная ЦМВИ
У пациентов с манифестной врожденной форме цитомегаловирусной болезни признаки наблюдаются с первых дней жизни. Типичный комплекс симптомов у новорожденных детей включает недоношенность и/или низкую массу тела, поражение гепатобилиарной системы (увеличение печени, желтуха, гепатиты и циррозы), лимфаденопатии и геморрагическую сыпь на коже. Если инфицирование произошло на ранних сроках беременности, ребенок рождается с аномалиями — микроцефалией, гипоплазией легких, атрезией пищевода.
Приобретенная ЦМВИ
Приобретенная цитомегаловирусная болезнь обычно протекает в субклинической или латентной форме, когда у ребенка возникают гриппоподобные симптомы, субфебрильная температура без видимой причины. После заражения инфекция может длительное время себя не проявлять и давать обострения при снижении иммунного статуса, действии неблагоприятных эндо- или экзогенных факторов.
Течение манифестной приобретенной формы напоминает инфекционный мононуклеоз. У ребенка внезапно появляется слабость, повышается температура, беспокоят недомогание, головные боли, отсутствует аппетит. Позже присоединяются сильные боли в горле, увеличиваются подчелюстные и шейные лимфоузлы. Если цитомегаловирусная инфекция проявляется сиаладенитом, наблюдается резкое увеличение и болезненность слюнных желез на фоне фебрильной лихорадки.
Генерализованная ЦМВИ
При генерализованном варианте течения инфекции у детей поражается бронхолегочная система (пневмонии, дыхательная недостаточность), ЖКТ (энтероколит, мальабсорбция), печень (желтуха, цитомегаловирусный гепатит, билиарный цирроз). Особенно опасно вовлечение в процесс нервной системы, что проявляется судорожным синдромом, парезами и параличами, задержкой психомоторного развития.
Осложнения
Поражение клеток при цитомегаловирусной болезни создает благоприятные условия для возникновения аутоиммунных поражений — системной красной волчанки, рассеянного склероза, гломерулонефрита. Иногда после малосимптомной врожденной цитомегаловирусной инфекции осложнения наблюдаются в отдаленном периоде (в возрасте ребенка 2-5 лет). В основном они проявляются неврологическими расстройствами и поражением органов чувств.
Цитомегаловирусная инфекция отличается многообразием клинических признаков и часто протекает под маской других патологий, что затрудняет работу детского инфекциониста. На первичном приеме, помимо стандартного физикального осмотра, врач собирает детальный акушерский анамнез, чтобы выявить факторы риска антенатального инфицирования. Диагноз ЦМВИ правомочен только при лабораторном подтверждении, для чего используют следующие методы:
- Цитологические анализы. Для исследования берут мочу, слюну, мокроту и другие биологические жидкости. При анализе специально окрашенных препаратов под микроскопом врач выявляет цитомегалы, которые являются патогномоничным признаком цитомегаловирусной инфекции. Метод обладает недостаточной чувствительностью, поэтому его повторяют многократно в течение 3-5 дней.
- Гистологические исследования. «Золотой стандарт» диагностики врожденной инфекции у детей предполагает исследование образцов плаценты. Важными критериями считают очаговые ишемические инфаркты, некроз базальной пластинки, признаки продуктивно-пролиферативного виллузита. Обычно анализ выявляет типичные клетки типа «совиный глаз».
- Молекулярно-биологические методы. Информативно проведение ПЦР-диагностики для обнаружения генетического материала вируса в биологическом материале (слюне, моче, спинномозговой жидкости). Метод дает врачу возможность следить за уровнем вирусной нагрузки, чтобы корректировать противовирусное лечение и оценивать его эффективность.
- Серологические реакции. ИФА требуется для выявляется IgM и низкоавидных IgG, что характерно для острой фазы инфекционного процесса. По мере выздоровления и формирования иммунитета в крови появляются иммуноглобулины G с высокой авидностью. С помощью РИФ выявляют антигены в клеточных культурах или клетках периферической крови.
Инструментальные методы подбираются соответственно форме заболевания. Для оценки структурно-функциональных особенностей печени и билиарного тракта назначают УЗИ органов брюшной полости. КТ и МРТ головного мозга информативны для выявления врожденных пороков и кальцификатов. Рентгенография ОГК необходима при симптомах дыхательных расстройств. По показаниям ребенка направляют на консультации к профильным специалистам— кардиологу, неврологу, отоларингологу.
Лечение цитомегаловирусной инфекции у детей
Препаратом выбора у новорожденных и детей первого года жизни является специфический антицитомегаловирусный иммуноглобулин, который имеет повышенную концентрацию IgG. Лечение начинают при манифестных формах заболевания и проводят по схеме: вначале вводится высокая доза препарата, а спустя 9-10 дней дозировку постепенно уменьшают, контролируя степень ответа на терапию и активность процесса.
В старшем возрасте перечень препаратов, применяемых при цитомегаловирусной инфекции, значительно расширяется. Лечение включает противовирусные средства из группы нуклеозидов и нуклеотидов (ганцикловир, валганцикловир), производные ортофосфорной кислоты (фоскарнет). При легкой и среднетяжелой формах назначают интерфероны, иммуностимуляторы.
Для купирования интоксикации показано обильное питье (при легких формах), при среднетяжелых и тяжелых клинических вариантах рекомендована инфузионная терапия. Патогенетическая терапия подбирается в соответствии с характером течения болезни и может включать пищеварительные ферменты, ингибиторы протеиназ, гемостатики. Для предупреждения вторичных бактериальных осложнений используют антибиотики (макролиды, цефалоспорины, гликопептиды).
Прогноз и профилактика
При малосимптомных приобретенных вариантах цитомегаловирусная болезнь протекает без осложнений, зачастую у ребенка выявляется только латентное носительство. Угрозу для жизни и здоровья представляют тяжелые генерализованные инфекции, которые в 50-60% случаев сопровождаются осложнениями, несмотря на проводимое лечение. Особо опасно поражение цитомегаловирусом для детей с иммунодефицитными состояниями.
Основу профилактики врожденной ЦМВИ составляет обязательное лабораторное обследование женщин на носительство цитомегаловируса, которое проводится при планировании зачатия и во время беременности. Если в семье есть пациент с цитомегаловирусной инфекцией, необходимо ограничить его общение с ребенком и обеспечить лечение. Карантинно-изоляционные мероприятия в отношении заболевших и контактных лиц не производятся.
2. Клинические рекомендации (протокол лечения) оказания медицинской помощи детям больным цитомегаловирусной инфекцией. — 2015.
Цитомегаловирусная инфекция у беременных ( Цитомегалия )
Цитомегаловирусная инфекция у беременных — это клинически манифестное или латентно протекающее инфекционное заболевание, вызванное цитомегаловирусом, возникшее до зачатия или во время гестации. Проявляется гипертермией, катаральными симптомами, шейным и подчелюстным лимфаденитом, сиалоаденитом, общей интоксикацией, беловато-голубыми белями, реже — гепатомегалией, спленомегалией, генерализованной лимфаденопатией. Диагностируется с помощью серологических и молекулярных лабораторных методов. Лечение проводится специфическим человеческим иммуноглобулином, рекомбинантным альфа-2-интерфероном, при тяжелом течении — синтетическими аналогами нуклеозидов.
Цитомегаловирусная инфекция (цитомегалия, ЦМВИ) — одно из наиболее распространенных инфекционных заболеваний, внутриутробно поражающих плод и вызывающих различные врожденные аномалии. В зависимости от региона антитела к цитомегаловирусу определяются у 40-98% пациенток репродуктивного возраста. Цитомегалия чаще встречается в группах населения с низким уровнем социального и экономического развития. В России серопозитивными к ЦМВИ являются до 90% женщин, инфицированность среди беременных старше 30 лет достигает 97-98%. В европейских странах врожденная цитомегалия выявляется с частотой 3-5 случаев на 1000 родов, в других государствах этот показатель составляет от 0,2 до 2,2%.
Заболевание вызывается крупным ДНК-содержащим цитомегаловирусом (ЦМВ), принадлежащим к семейству герпес-вирусов. Специалисты выделяют три штамма возбудителя, каждый из которых может самостоятельно инфицировать организм одного и того же человека. Заражение происходит до зачатия либо во время беременности. Вирусы пожизненно персистируют в организме женщины, поражая практически все виды тканей. Часть инфекционистов считает ЦМВ условно-патогенным микроорганизмом, клинически значимая реактивация которого наблюдается только при значительном угнетении иммунитета.
Усиление патогенности цитомегаловируса в гестационном периоде связано с физиологической иммуносупрессией, защищающей генетически чужеродный плод от отторжения. Под влиянием эстрогенов, прогестерона, кортизола у беременной уменьшается абсолютное и относительное количество Т-лимфоцитов, непосредственно участвующих в элиминации вирусов и поврежденных клеток, снижается их цитотоксичность. В результате ускоряется репликация цитомегаловирусов, они быстрее распространяются по организму и при недостаточном уровне защитных антител преодолевают плацентарный барьер.
Особенностью цитомегаловирусной инфекции является множественность путей заражения. Вирус распространяется аэрогенным, контактным, фекально-оральным, гемотрансфузионным, половым, вертикальным способами, в том числе трансплацентарно от беременной к плоду. Из-за сравнительно низкой вирулентности для инфицирования важен тесный контакт с зараженным. Возбудитель ЦМВИ определяется практически во всех биологических средах: слюне, крови, моче, слезной жидкости, ликворе, грудном молоке, цервикальном, вагинальном, уретральном секрете, сперме, слизи из прямой кишки, околоплодных водах.
После попадания в организм цитомегаловирусы адсорбируются на поверхности клеток, проникают в них, проходят полный цикл репликации ДНК, после чего сформированные вирионы распространяются на соседние клетки, с кровью разносятся по организму. Наиболее чувствителен к вирионам протоковый эпителий слюнных желез, в первую очередь околоушных, других экзокринных желез.
После лимфогенной и гематогенной генерализации обычно наступает фаза непродуктивной инфекции (скрытого носительства) с длительным сохранением вирусной частицы внутри зараженной клетки и передачей при делении дочерним клеткам. У женщин с нормальным иммунитетом клиническая манифестация не происходит, заболевание сразу приобретает характер носительства. Цитомегаловирус может длительное время персистировать в неактивной форме в чувствительных клетках. Проникновение ЦМВ в лимфоциты и мононуклеары обеспечивает его защиту от противовирусных антител.
При падении иммунитета у беременных возможна реактивация цитомегаловирусной инфекции с разрушением ядер клеток, в которых персистировал вирус, гематогенной диссеминацией, поражением железистых органов, развитием васкулитов, индукцией специфического цитомегалического метаморфоза клеток разных тканей. При гестации вирусы из межворсинчатого пространства проникают через плаценту и гематогенно инфицируют плод. Установлено, что ЦМВ способен повреждать мембрану трофобласта.
Систематизация основных форм цитомегаловирусной инфекции у беременных проводится с учетом выраженности клинической картины и времени манифестации патологического процесса. Такой подход наиболее оправдан с точки зрения прогнозирования возможных осложнений заболевания и выбора оптимальной тактики ведения беременности. Специалисты в сфере акушерства и гинекологии, инфекционных болезней различают следующие варианты инфекции:
- Первично-манифестнаяЦМВИ. Самый неблагоприятный вариант течения патологии. Возникает в результате первичного инфицирования беременной, у которой отсутствуют специфические IgG. Отличается высокой вероятностью трансплацентарного переноса вируса (до 30-75%) и внутриутробного поражения плода. В период гестации выявляется не более чем у 4% пациенток. При заражении с острой симптоматикой в I триместре рекомендован аборт.
- Носительство. Наиболее частая форма цитомегаловирусной болезни у беременных. Носительницами являются женщины, у которых до зачатия была активная форма заболевания или инфекция на фоне сильного иммунитета сразу перешла в непродуктивную фазу. Иммуноглобулины G, циркулирующие в крови пациентки, защищают плод от заражения ЦМВ. При исключении иммуносупрессорных воздействий риск патологического течения гестации минимален.
- Реактивация латентной инфекции. При значительном снижении иммунитета у носительниц цитомегаловируса развивается характерная клиническая картина. Заболевание в той или иной степени обостряется у 40-50% серопозитивных беременных. В 0,15-0,36% случаев вирус передается трансплацентарно ребенку. Наибольший риск врожденных аномалий наблюдается при обострении цитомегаловирусной болезни на 7-12 неделях гестационного срока.
Симптомы ЦМВИ у беременных
Возможны беловато-голубые влагалищные выделения. При существенном снижении иммунитета определяется увеличение печени, селезенки с появлением тяжести, дискомфорта, распирания в правом и левом подреберьях, генерализованное увеличение лимфоузлов. Длительность острой фазы, как правило, составляет до 2-3 недель.
Осложненное течение гестации наблюдается преимущественно при острой или реактивированной инфекции. У таких пациенток чаще возникают спонтанные выкидыши, связанные с тяжелыми эмбрио- и фетопатиями, преждевременные роды, вызванные гипертонусом матки, замершие беременности, мертворождение. Из-за повреждения мембраны трофобласта ЦМВИ может осложниться приращением плаценты, гипертрофией и ранним старением плацентарной ткани, фетоплацентарной недостаточностью, внутриутробной гипоксией и задержкой развития плода.
Во время родов возможна преждевременная отслойка плаценты, массивная кровопотеря из-за атонического кровотечения. В послеродовом периоде отмечаются латентные эндометриты. В последующем повышается вероятность развития дисменореи.
При острой первичной цитомегаловирусной болезни существенно возрастает риск трансплацентарного инфицирования плода и развития многоводия. Дети зачастую рождаются недоношенными, с низкой малой тела. Особенно опасно заражение ЦМВ в 1-м триместре, часто вызывающее микроцефалию, хориоретинит, нейросенсорную тугоухость, другие аномалии развития.
Врожденная цитомегалия после внутриутробного инфицирования может протекать бессимптомно, проявляться тяжело протекающими манифестными формами или в виде последствий поражения отдельных органов (гепатомегалии, затяжной желтухи, нарушений сосания и глотания, стойкого снижения мышечного тонуса, тремора, анемии, тромбоцитопении, отставания в умственном и моторном развитии, пневмонии, миокардита, панкреатита, колита, нефрита). Отдаленными последствиями ЦМВИ у детей являются слепота, глухота, речевые нарушения, проявляющиеся на 2-5-м году жизни.
У беременных со значительной иммуносупрессией ЦМВИ протекает тяжелее, экстрагенитальные осложнения выявляются чаще. Неблагоприятными формами заболевания считаются цитомегаловирусные поражения легких (интерстициальная пневмония), мозга (менингит, энцефалит), периферической нервной системы (миелит, полирадикулоневрит), сердца (миокардит, перикардит), кроветворения (тромбоцитопения, гемолитическая анемия). Прямая угроза для жизни беременной возникает при быстрой генерализации инфекции с развитием сепсиса, инфекционно-токсического шока, ДВС-синдрома.
Сложность своевременного выявления ЦМВИ связана с отсутствием симптоматики у большинства беременных и полиморфностью клинической картины при манифестации. Учитывая повышенный риск перинатального заражения ребенка цитомегаловирусной инфекцией, в качестве скрининга рекомендовано проведение анализа на TORCH-комплекс. Ведущими методами диагностики являются лабораторные анализы, позволяющие верифицировать инфекционного агента, обнаружить серологические маркеры и определить остроту процесса. План обследования пациенток с подозрением на цитомегалию включает такие исследования, как:
- Иммуноферментный анализ. ИФА считается наиболее достоверным и информативным методом диагностики цитомегаловирусной болезни. Наличие активной инфекции подтверждает выявление IgM и более чем 4-кратное нарастание титра IgG. О давности инфицирования свидетельствуют данные об авидности иммуноглобулинов G (при показателе
- ПЦР-диагностика. Цитомегаловирусные нуклеиновые кислоты определяют в биологических секретах, которые могут содержать возбудителя. Обычно для анализа берут кровь, мочу, цервикальный секрет, буккальные мазки. Обнаружение вирусной ДНК подтверждает инфицированность, а количественные методы исследования позволяют контролировать течение инфекции.
Для оценки состояния плода, выявления фетоплацентарной недостаточности, возможных аномалий по показаниям проводятся:
- УЗИ плода и плаценты;
- допплерография маточно-плацентарного кровотока;
- фетометрия;
- КТГ;
- фонокардиография плода;
- биопсия хориона.
Цитомегалию дифференцируют с ВИЧ-инфекцией, инфекционным мононуклеозом, токсоплазмозом, листериозом, герпесом, вирусными гепатитами, бактериальным сепсисом, лимфогранулематозом, острым лейкозом. При необходимости пациентку консультирует инфекционист, вирусолог, иммунолог, онколог, онкогематолог.
Лечение ЦМВИ у беременных
Выбирая тактику ведения гестации, учитывают клиническую форму ЦМВИ и срок инфицирования. Женщинам с цитомегалией, первично-манифестировавшей в период 1 триместра, рекомендовано проведение аборта. Прерывание беременности по медицинским показаниям также показано пациенткам с клинически и лабораторно подтвержденной первичной инфекцией при обнаружении до 22 недели УЗ-признаков пороков развития плода. В остальных случаях возможна пролонгация гестации.
Беременным с носительством медикаментозное лечение не назначается. При отсутствии клинических и лабораторных признаков реактивации цитомегаловирусной болезни требуется коррекция образа жизни, направленная на предотвращение значительной иммуносупрессии. Больным необходимы достаточные отдых и сон, исключение чрезмерных физических и психологических нагрузок, полноценное питание, прием витаминно-минеральных комплексов, профилактика ОРВИ, осторожность при назначении препаратов, снижающих иммунитет.
Беременным с активной формой инфекции проводится лечение, направленное на купирование обострения и прекращение экскреции цитомегаловируса. Сложность выбора адекватной медикаментозной терапии связана с фетотоксичностью большинства противовирусных средств. С учетом возможных показаний и противопоказаний для лечения ЦМВИ при гестации применяются:
- Антицитомегаловирусный человеческий иммуноглобулин. Гипериммунные препараты позволяют восстановить титр специфических IgG, блокировать репликацию возбудителя и ограничить его диссеминацию. Использование иммуноглобулина человека существенно снижает риск внутриутробного инфицирования вирусом цитомегалии.
- Рекомбинантный α-2-интерферон. Препарат стимулирует Т-хелперы и Т-киллеры, повышая уровень Т-клеточного иммунитета. Усиливает активность фагоцитов и скорость дифференцировки В-лимфоцитов. Угнетает репликацию цитомегаловирусов и способствует их инактивации различными иммунными агентами. Рекомендован в виде ректальных свечей.
- Синтетические аналоги нуклеозидов. Назначаются только при тяжелых генерализованных формах цитомегаловирусной инфекции, когда риск токсических эффектов препаратов оправдан спасением жизни беременной. Противовирусные препараты ингибируют ДНК-полимеразу вирусных частиц и за счет этого тормозят синтез цитомегаловирусной ДНК.
Индукторы интерфероногенеза, иммуномодуляторы применяют крайне редко из-за возможного преждевременного прерывания гестации. В качестве немедикаментозных методов допустимо проведение эндоваскулярного лазерного облучения крови и плазмафереза.
Роды при ЦМВИ
Предпочтительным методом родоразрешения являются естественные роды. Кесарево сечение выполняется при наличии абсолютных акушерских или экстрагенитальных показаний или при сочетании относительных (внутриутробном инфицировании цитомегаловирусом, хронической гипоксии плода, II-III степенях задержки его развития, первичном и вторичном бесплодии в анамнезе).
Своевременное выявление латентной ЦМВИ и профилактика ее активации существенно улучшают исход беременности как для женщины, так и для плода. Прогноз неблагоприятен при генерализации первичной цитомегаловирусной инфекции. При установленном диагнозе цитомегалии показано планирование зачатия с учетом рекомендаций акушера-гинеколога, купирование активного процесса, прегравидарная иммунокоррекция с использованием пептидных иммуностимуляторов и рекомбинантных интерферонов.
Противовирусная терапия женщин с манифестной ЦМВИ на 75% снижает риск реактивации инфекции в наиболее опасном по возникновению осложнений 1 триместре. Общая профилактика заражения предполагает соблюдение правил личной гигиены с частым мытьем рук, отказ от близких прямых контактов с другими людьми.
1. Цитомегаловирусная инфекция и беременность/ Мельникова С.Е., Троик Е.Б.// Детская медицина Северо-Запада - 2012 - Т. 3, №3.
2. Цитомегаловирусная инфекция и беременность (прегравидарная подготовка и терапия)/ Короткова Н.А., Прилепская В.Н.// Эффективная фармакотерапия. - 2016 - №22.
3. Цитомегаловирусная инфекция. Этиология, эпидемиология, патогенез, клиника, лабораторная диагностика, лечение, профилактика/ Марданлы С.Г., Кирпичникова Г.И., Неверов В.А. — 2011.
4. Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ Извекова И.Я., Михайленко М.А., Краснова Е.И.// Лечащий врач. - 2018.
Цитомегаловирус ( Болезнь с включениями , Вирусная болезнь слюнных желез , Инклюзионная цитомегалия , Цитомегаловирусная инфекция (ЦМВ) )
Цитомегалия - это инфекционное заболевание вирусного генеза, передающееся половым, трансплацентарным, бытовым, гемотрансфузионным путем. Симптоматически протекает в форме упорной простуды. Отмечается слабость, недомогание, головные и суставные боли, насморк, увеличение и воспаление слюнных желез, обильное слюноотделение. Часто протекает бессимптомно. Опасна цитомегалия беременных: она может вызывать самопроизвольный выкидыш, врожденные пороки развития, внутриутробную гибель плода, врожденную цитомегалию. Диагностика осуществляется лабораторными методами (ИФА, ПЦР). Лечение включает противовирусную и симптоматическую терапию.
Другие названия цитомегалии, встречающиеся в медицинских источниках, - цитомегаловирусная инфекция (ЦМВ), инклюзионная цитомегалия, вирусная болезнь слюнных желез, болезнь с включениями. Цитомегалия является широко распространенной инфекцией, и многие люди, являясь носителями цитомегаловируса, даже не подозревают об этом. Наличие антител к цитомегаловирусу выявляется у 10—15% населения в подростковом возрасте и у 50% взрослых людей. По некоторым источникам, носительство цитомегаловируса определяется у 80% женщин детородного периода. В первую очередь это относится к бессимптомному и малосимптомному течению цитомегаловирусной инфекции.
Возбудитель цитомегаловирусной инфекции - цитомегаловирус - относится к семейству герпесвирусов человека. Клетки, пораженные цитомегаловирусом, многократно увеличиваются в размерах, поэтому название заболевания «цитомегалия» переводится как «клетки-гиганты». Цитомегалия не является высоко заразной инфекцией. Обычно заражение происходит при тесных, длительных контактах с носителями цитомегаловируса. Цитомегаловирус передается следующими путями:
- воздушно-капельным: при чихании, кашле, разговоре, поцелуях и т.д.;
- половым путем: при сексуальных контактах через сперму, влагалищную и шеечную слизь;
- гемотрансфузионным: при переливании крови, лейкоцитарной массы, иногда - при пересадке органов и тканей;
- трансплацентарным: во время беременности от матери плоду.
Нередко цитомегаловирус находится в организме многие годы и может ни разу не проявить себя и не нанести вреда человеку. Проявление скрытой инфекции происходит, как правило, при ослаблении иммунитета. Угрожающую по своим последствиям опасность цитомегаловирус представляет у лиц со сниженным иммунитетом (ВИЧ-инфицированных, перенесших трансплантацию костного мозга или внутренних органов, принимающих иммунодепрессанты), при врожденной форме цитомегалии, у беременных.
Попадая в кровь, цитомегаловирус вызывает выраженную иммунную реакцию, проявляющуюся в выработке защитных белковых антител - иммуноглобулинов М и G (IgM и IgG) и противовирусной клеточной реакцией - образованием лимфоцитов CD 4 и CD 8. Угнетение клеточного иммунитета при ВИЧ-инфекции приводит к активному развитию цитомегаловируса и вызываемой им инфекции.
Образование иммуноглобулинов М, свидетельствующих о первичной инфекции, происходит спустя 1-2 месяца после заражения цитомегаловирусом. Через 4-5 месяцев IgM заменяются на IgG, обнаруживающиеся в крови в течение всей последующей жизни. При крепком иммунитете цитомегаловирус не вызывает клинических проявлений, течение инфекции происходит бессимптомно, скрыто, хотя наличие вируса определяется во многих тканях и органах. Поражая клетки, цитомегаловирус, вызывает увеличение их размера, под микроскопом пораженные клетки похожи на «глаз совы». Цитомегаловирус определяется в организме пожизненно.
Даже при бессимптомном течении инфекции носитель цитомегаловируса является потенциально заразным для неинфицированных лиц. Исключение составляет внутриутробный путь передачи цитомегаловируса от беременной женщины плоду, который происходит в основном при активном течении процесса, и лишь в 5% случаев вызывает врожденную цитомегалию, в остальных же носит бессимптомный характер.
Симптомы цитомегалии
Врожденная цитомегалия
В 95% случаев внутриутробное инфицирование плода цитомегаловирусом не вызывает развития заболевания, а протекает бессимптомно. Врожденная цитомегаловирусная инфекция развивается у новорожденных, матери которых перенесли первичную цитомегалию. Врожденная цитомегалия может проявляться у новорожденных в различных формах:
- петехиальная сыпь - мелкие кожные кровоизлияния - встречается у 60-80% новорожденных;
- недоношенность и задержка внутриутробного развития плода - встречается у 30% новорожденных;
- желтуха;
- хориоретинит - острый воспалительный процесс в сетчатке глаза, часто вызывающий снижение и полную потерю зрения.
Летальность при внутриутробном инфицировании цитомегаловирусом достигает 20-30%. Из выживших детей большая часть имеет отставание в умственном развитии или инвалидность по слуху и зрению.
Приобретенная цитомегалия у новорожденных
При инфицировании цитомегаловирусом в процессе родов (при прохождении плода по родовым путям) или в послеродовом периоде (при бытовом контакте с инфицированной матерью или грудном вскармливании) в большинстве случаев развивается бессимптомное течение цитомегаловирусной инфекции. Однако у недоношенных младенцев цитомегаловирус может вызывать затяжную пневмонию, к которой часто присоединяется сопутствующая бактериальная инфекция. Часто при поражении цитомегаловирусом у детей отмечается замедление в физическом развитии, увеличение лимфоузлов, гепатит, сыпь.
Мононуклеозоподобный синдром
У лиц, вышедших из периода новорожденности и имеющих нормальный иммунитет, цитомегаловирус может вызывать развитие мононуклеозоподобного синдрома. Течение мононуклеазоподобного синдрома по клинике не отличается от инфекционного мононуклеоза, вызываемого другой разновидностью герпесвируса - вирусом Эбштейна-Барр. Течение мононуклеозоподобного синдрома напоминает упорную простудную инфекцию. При этом отмечается:
- длительная (до 1 месяца и более) лихорадка с высокой температурой тела и ознобами;
- ломота в суставах и мышцах, головная боль;
- выраженные слабость, недомогание, утомляемость;
- боли в горле;
- увеличение лимфоузлов и слюнных желез;
- кожные высыпания, напоминающие сыпь при краснухе (обычно встречается при лечении ампициллином).
В отдельных случаях мононуклеозоподобный синдром сопровождается развитием гепатита - желтухой и повышением в крови печеночных ферментов. Еще реже (до 6% случаев) осложнением мононуклеозоподобного синдрома служит пневмония. Однако у лиц с нормальной иммунной реактивностью она протекает без клинических проявлений, выявляясь лишь при проведении рентгенографии легких.
Длительность течения мононуклеозоподобного синдрома составляет от 9 до 60 дней. Затем обычно наступает полное выздоровление, хотя на протяжении нескольких месяцев могут сохраняться остаточные явления в виде недомогания, слабости, увеличенных лимфоузлов. В редких случаях активизация цитомегаловируса вызывает рецидивы инфекции с лихорадкой, потливостью, приливами и недомоганием.
Цитомегаловирусная инфекция у лиц с ослабленным иммунитетом
Ослабление иммунитета наблюдается у лиц, страдающих синдромом врожденного и приобретенного (СПИД) иммунодефицита, а также у пациентов, перенесших пересадку внутренних органов и тканей: сердца, легкого, почки, печени, костного мозга. После пересадки органов пациенты вынуждены постоянно принимать иммунодепрессанты, ведущие к выраженному подавлению иммунных реакций, что вызывает активность цитомегаловируса в организме.
У пациентов, перенесших трансплантацию органов, цитомегаловирус вызывает поражение донорских тканей и органов (гепатит - при пересадке печени, пневмонию при пересадке легкого и т. д.). После трансплантации костного мозга у 15-20% пациентов цитомегаловирус может привести к развитию пневмонии с высокой летальностью (84-88%). Наибольшую опасность представляет ситуация, когда инфицированный цитомегаловирусом донорский материал пересажен неинфицированному реципиенту.
Цитомегаловирус поражает практически всех ВИЧ-инфицированных. В начале заболевания отмечаются недомогание, суставные и мышечные боли, лихорадка, ночная потливость. В дальнейшем к этим признакам могут присоединяться поражения цитомегаловирусом легких (пневмония), печени (гепатит), мозга (энцефалит), сетчатки глаза (ретинит), язвенные поражения и желудочно-кишечные кровотечения.
У мужчин цитомегаловирусом могут поражаться яички, простата, у женщин - шейка матки, внутренний слой матки, влагалище, яичники. Осложнениями цитомегаловирусной инфекции у ВИЧ-инфицированных могут стать внутренние кровотечения из пораженных органов, потеря зрения. Множественное поражение органов цитомегаловирусом может привести к их дисфункции и гибели пациента.
С целью диагностики цитомегаловирусной инфекции проводится лабораторное обследование. Постановка диагноза цитомегаловирусной инфекции основана на выделении цитомегаловируса в клиническом материале или при четырехкратном повышении титра антител.
- ИФА-диагностика. Включает определение в крови специфических антител к цитомегаловирусу - иммуноглобулинов М и G. Наличие иммуноглобулинов М может свидетельствовать о первичном заражении цитомегаловирусом либо о реактивации хронической ЦМВИ. Определение высоких титров IgМ у беременных может угрожать инфицированию плода. Повышение IgМ выявляется в крови спустя 4-7 недель после заражения цитомегаловирусом и наблюдается на протяжении 16-20 недель. Повышение иммуноглобулинов G развивается в период затухания активности цитомегаловирусной инфекции. Их наличие в крови говорит о присутствии цитомегаловируса в организме, но не отражает активности инфекционного процесса.
- ПЦР-диагностика. Для определения ДНК цитомегаловируса в клетках крови и слизистых (в материалах соскобов из уретры и цервикального канала, в мокроте, слюне и т. д.) используется метод ПЦР-диагностики (полимеразной цепной реакции). Особенно информативно проведение количественной ПЦР, дающей представление об активности цитомегаловируса и вызываемого им инфекционного процесса.
В зависимости от того, какой орган поражен цитомегаловирусной инфекцией, пациент нуждается в консультации гинеколога, андролога, гастроэнтеролога или других специалистов. Дополнительно по показаниям проводится УЗИ органов брюшной полости, кольпоскопия, гастроскопия, МРТ головного мозга и другие обследования.
Лечение цитомегаловирусной инфекции
Неосложненные формы мононуклеазоподобного синдрома не требует специфической терапии. Обычно проводятся мероприятия, идентичные лечению обычного простудного заболевания. Для снятия симптомов интоксикации, вызываемой цитомегаловирусом, рекомендуется пить достаточное количество жидкости.
Лечение цитомегаловирусной инфекции у лиц, входящих в группу риска, проводится противовирусным препаратом ганцикловиром. В случаях тяжелого течения цитомегалии ганцикловир вводится внутривенно, т. к. таблетированные формы препарата обладают лишь профилактическим эффектом в отношении цитомегаловируса. Поскольку ганцикловир обладает выраженными побочными эффектами (вызывает угнетение кроветворения - анемию, нейтропению, тромбоцитопению, кожные реакции, желудочно-кишечные расстройства, повышение температуры и ознобы и др.), его применение ограничено у беременных, детей и у людей, страдающих почечной недостаточностью (только по жизненным показаниям), он не используется у пациентов без нарушения иммунитета.
Для лечения цитомегаловируса у ВИЧ-инфицированных наиболее эффективен препарат фоскарнет, также обладающий рядом побочных эффектов. Фоскарнет может вызывать нарушение электролитного обмена (снижение в плазме крови магния и калия), изъязвление половых органов, нарушение мочеиспускания, тошноту, поражение почек. Данные побочные реакции требуют осторожного применения и своевременной корректировки дозы препарата.
Прогноз
Особую опасность цитомегаловирус представляет при беременности, так как может провоцировать выкидыш, мертворождение или вызывать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с герпесом, токсоплазмозом и краснухой, относится к числу тех инфекций, обследоваться на которые женщины должны профилактически, еще на этапе планирования беременности.
Профилактика
Особенно остро вопрос профилактики цитомегаловирусной инфекции стоит у лиц, входящих в группу риска. Наиболее подвержены инфицированию цитомегаловирусом и развитию заболевания ВИЧ-инфицированные (особенно больные СПИДом), пациенты после трансплантации органов и лица с иммунодефицитом иного генеза.
Неспецифические методы профилактики (например, соблюдение личной гигиены) неэффективны в отношении цитомегаловируса, так как заражение им возможно даже воздушно-капельным путем. Специфическая профилактика цитомегаловирусной инфекции проводится ганцикловиром, ацикловиром, фоскарнетом среди пациентов, входящих в группы риска. Также для исключения возможности инфицирования цитомегаловирусом реципиентов при пересадке органов и тканей необходим тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Ультразвуковые особенности структурных изменений головного мозга новорожденных с внутриутробной герпес-цитомегаловирусной инфекцией
Лидер продаж в высоком классе. Монитор 21,5" высокой четкости, расширенный кардио пакет (Strain+, Stress Echo), экспертные возможности для 3D УЗИ в акушерско-гинекологической практике (STIC, Crystal Vue, 5D Follicle), датчики высокой плотности.
Введение
В настоящее время отмечается большой рост внутриутробной герпетической инфекции и увеличение числа инфицированных новорожденных. Среди инфекций герпетической этиологии наибольшую распространенность имеет цитомегаловирусная инфекция (ЦМВИ) и герпес-вирусная инфекция, вызываемая вирусами простого герпеса (ВПГ) I и II типов. У новорожденных 80% герпес-вирусной инфекции вызываются ВПГ II типа. Исходом даже бессимптомно протекающей во время беременности инфекции могут быть тяжелые последствия у плода: врожденные уродства, поражение различных органов и систем, наиболее серьезным из которых является повреждение головного мозга.
Клинические проявления в неонатальном периоде отмечаются лишь у 10% анте- или интранатально инфицированных детей, у остальных же внутриутробное инфицирование в периоде новорожденности протекает бессимптомно. Летальность у детей с генерализованной герпес-вирусной и цитомегаловирусной инфекцией при отсутствии химиотерапии составляет 90%; у 50% выживших отмечаются тяжелые психоневрологические исходы 2.
Быстрая и надежная расшифровка этиологии заболевания у новорожденного приобретает особую актуальность в связи с появляющейся в последние годы возможностью проведения этиотропной терапии.
Основным методом диагностики этих заболеваний является иммунологический метод. Но он далеко не всем доступен из-за дороговизны, трудоемкости, значительного времени, необходимого для постановки окончательного диагноза. Кроме того, этот метод не дает возможности установить вовлечение в патологический процесс головного мозга, что крайне важно для выбора лечебных мероприятий. Поэтому в настоящее время основным диагностическим методом на первом этапе помимо клинических методов является эхоэнцефалография, позволяющая оценить степень вовлечения головного мозга и других внутренних органов в инфекционный процесс.
На основании данных эхографии головного мозга и клинической картины заболевания у новорожденных можно начинать проводить лечение детей "по подозрению". В дальнейшем эти дети составят группу для комплексного иммунологического обследования, в результате которого диагноз будет уточнен.
Как свидетельствуют литературные данные, наиболее часто у детей с внутриутробной герпес-цитомегаловирусной инфекцией при эхоэнцефалографии выявляют кисты сосудистых сплетений боковых желудочков и (или) субэпендимальные кисты [4]. Показано, что при изолированных кистах сосудистых сплетений (без анализа причин их возникновения) прогноз психоневрологического развития детей в целом благоприятный [5]. При субэпендимальных кистах инфекционного происхождения прогноз неопределенный : от нормального развития до выраженного церебрального дефицита 7. В связи с этим цель настоящего исследования состояла в оценке психоневрологического статуса детей, имевших кисты сосудистых сплетений и (или) субэпендимальные кисты, с внутриутробной герпес-цитомегаловирусной инфекцией, подтвержденной данными комплексного иммунологического исследования.
Материалы и методы
Из многочисленной группы новорожденных (396 новорожденных с субэпендимальными кистами и 261 с кистами сосудистых сплетений) нами впоследствии (после завершения периода наблюдения) были отобраны 16 детей с подтвержденной иммунологическими методами герпес-цитомегаловирусной инфекцией, которые были подвергнуты динамической эхоэнцефалографии и клиническому обследованию в течение 2-12 мес. Показаниями для проведения иммунологического исследования на первом этапе являлись структурные изменения головного мозга, выявленные при эхографии, косвенно свидетельствующие о наличии внутриутробной инфекции.
Иммунологическая диагностика состояла в выявлении специфического антигена иммуноферментным и иммунофлюоресцентным методами, фрагментов ДНК вируса методом полимеразной цепной реакции, определении специфических антител в биологических средах. Материалом для исследования у детей служили кровь, моча и ликвор, у матерей - кровь. Обследование матерей проводили для повышения достоверности диагноза у их детей.
Всем детям проводили динамическую эхоэнцефалографию с первой недели до 2-9 мес. жизни. Эхографию головного мозга осуществляли с помощью различных ультразвуковых приборов, часть исследований выполнена на аппарате SA-8800 "GAIA" ("Medison", Южная Корея). Всего выполнено 59 эхографических исследований головного мозга.
Результаты и обсуждение
В клинической картине у 3 детей отмечался синдром угнетения функций ЦНС, который выражался в снижении церебральной и двигательной активности, мышечного тонуса и угнетении физиологических рефлексов новорожденных; у этих же детей выявлено вовлечение в патологический процесс органов дыхания с развитием пневмонии. У 2 новорожденных отмечена затянувшаяся желтуха с гепатоспленомегалией, у 2 - отечный синдром. У 4-го ребенка неврологическая симптоматика отсутствовала, у него были выявлены изменения со стороны внутренних органов в виде гепатоспленомегалии и затянувшейся желтухи.
При эхоэнцефалографии у детей I группы выявлено от 1 до 3 изолированных кистозных структур (не сочетающихся с другими структурными изменениями) диаметром от 0,2-0,5 см (рис. 1, 2), расположенных в верхушке или теле сосудистого сплетения левого бокового желудочка. У 3-х из этих детей исходные данные вентрикулометрии соответствовали нормальным значениям. У 1-го ребенка отмечено незначительное (до 0,6 см) расширение межполушарной щели и субарахноидальных пространств по конвекситальной поверхности мозга и умеренное симметричное увеличение ширины лобных рогов (преимущественно) и высоты тел боковых желудочков (до 0,7 см).
Рис. 1. Эхоэнцефалограмма ребенка Р. со смешанной герпес-цитомегаловирусной инфекцией, 7-е сут. жизни. Стрелками обозначена киста в верхушке сосудистого сплетения левого бокового желудочка.
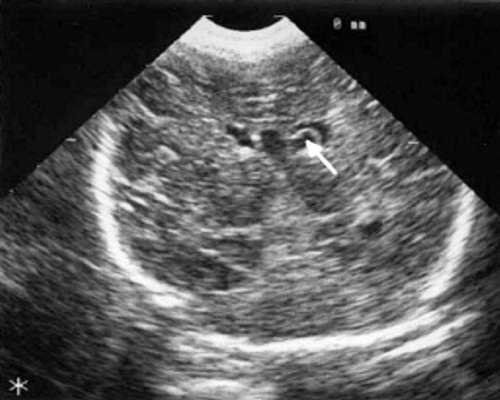
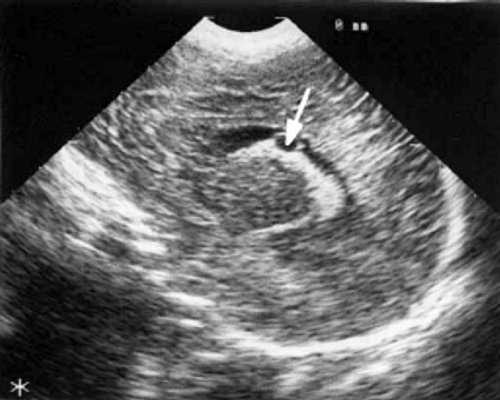
Рис. 2. Эхоэнцефалограмма ребенка Д. с цитомегаловирусной инфекцией, 2-е сут. жизни. Стрелками обозначены кисты в теле сосудистого сплетения левого бокового желудочка.
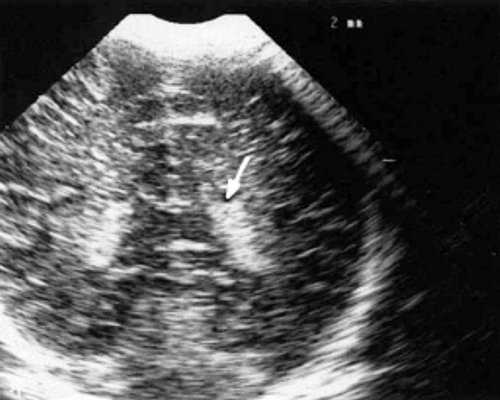
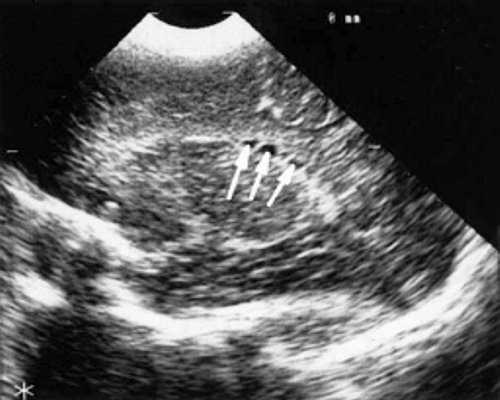
В конце периода наблюдения, который составлял от 2 до 7 мес., у 2 детей кисты сосудистых сплетений имели прежние размеры и число; у них данные вентрикулометрии, как при первом УЗИ, соответствовали возрастной норме. У одного ребенка киста сосудистых сплетений уменьшилась в размерах с 0,5 до 0,1 см; у него отмечено дальнейшее симметричное расширение боковых желудочков (ширина их лобных рогов и высота тел увеличилась с 0,7 до 0,9 см) и межполушарной щели и субарахноидальных пространств по конвекситальной поверхности мозга от 0,6 до 0,9 см. У одного ребенка этой группы при эхоэнцефалографии, проведенной в 7 мес. жизни, киста сосудистых сплетений не выявлялась, однако у него произошло симметричное увеличение ширины лобных рогов (преимущественно) и высоты тел боковых желудочков до 1 см и расширение субарахноидальных пространств по конвекситальной поверхности мозга до 0,7 см. При катамнестическом наблюдении только у этого ребенка выявлена незначительная задержка психомоторного развития, у 3 других детей I группы признаки церебрального дефицита не отмечены.
Всем детям этой группы проводилась иммунотерапия цитотектом и пентаглобином ("Biotest", Германия); в том числе 2 детям - иммунохимиотерапия (противоцитомегаловирусный иммуноглобулин - цитотект и виролекс). При анализе полученных данных какой-либо связи клинических проявлений заболевания, данных комплексного иммунологического обследования с локализацией кисты сосудистых сплетений, их числом, размерами и динамикой не выявлено.
По данным комплексного иммунологического обследования, у 6 детей была установлена смешанная герпес-цитомегаловирусная, у 3 - цитомегаловирусная и у 3 - герпес-вирусная инфекция. В клинической картине у этой группы больных выявлено полиморфное поражение с преобладанием признаков нарушений функций нервной системы у всех детей: преимущественно синдромом угнетения - у 9, гипервозбудимости - у 3. Вовлечение в патологический процесс органов дыхания отмечено у 5 новорожденных, затянувшаяся желтуха с гипербилирубинемией - у 9, гепатомегалия - у 2, отечный синдром - у 3 детей.
У детей этой группы при первом эхоэнцефалографическом исследовании были выявлены субэпендимально расположенные кистозные структуры на уровне таламо-каудальной вырезки (ТКВ) и (или) кпереди от нее диаметром от 0,3 до 1,1 см. У части новорожденных субэпендимальные кисты были представлены единой полостью с однородным или неоднородным содержимым, у других детей эти структуры напоминали соты, т. е. состояли из множества жидкостных включений, окруженных эхопозитивным ободком (рис. 3). Эти структурные особенности субэпендимальных кист, по-видимому, обусловлены разными стадиями резорбции. У 10 детей субэпендимальные кисты располагались в симметричных участках обоих полушарий, у 2 новорожденных - только в левом полушарии. У 3 детей, помимо субэпендимальных кист, расположенных в таламо-каудальной вырезке и (или) кпереди от нее, дополнительно выявлены субэпендимальные щелевидные кистозные структуры на уровне средних или передних отделов лобных рогов (см. рис. 3).
Рис. 3. Эхоэнцефалограмма ребенка Б. со смешанной герпес-цитомегаловирусной инфекцией, 5-е сут. жизни.
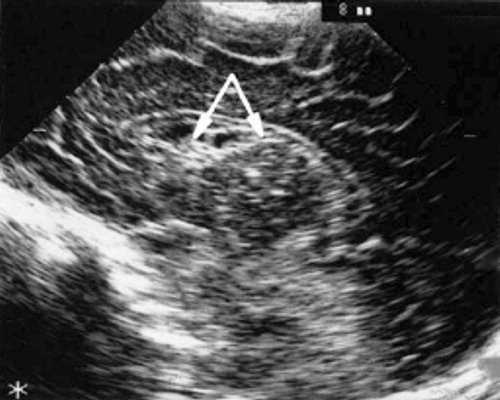
а) Правое полушарие. Стрелками обозначены субэпендимальные кисты, имеющие вид сот, расположенные в таламокаудальной вырезке и кпереди от нее.
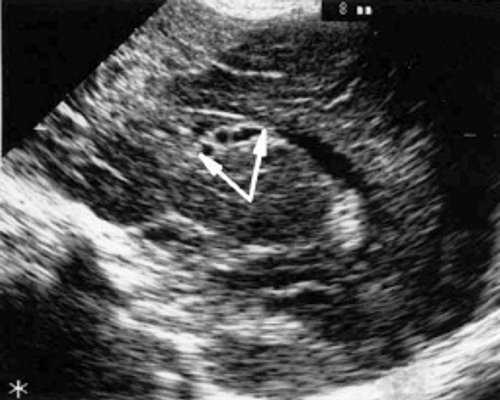
б) Левое полушарие. Стрелками обозначены субэпендимальные кисты, имеющие вид сот, расположенные в таламокаудальной вырезке и кпереди от нее.
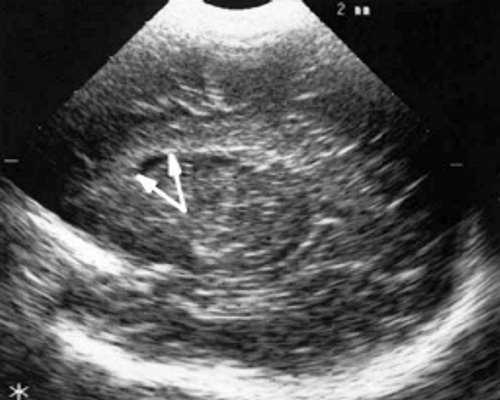
в) Правое полушарие. Стрелками обозначены субэпендимальные щелевидные кистозные структуры на уровне передних и средних отделов лобных рогов боковых желудочков.
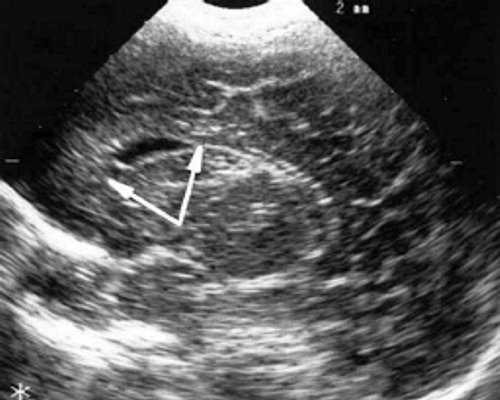
г) Левое полушарие. Стрелками обозначены субэпендимальные щелевидные кистозные структуры на уровне передних и средних отделов лобных рогов боковых желудочков.
У всех новорожденных этой группы исходные данные вентрикулометрии соответствовали нормальным значениям. В конце периода наблюдения, составляющего от 2 до 9 мес., размеры желудочковой системы у 9 детей оставались на нормальных значениях, у 3 детей отмечалось умеренное (до 0,9 см), симметричное увеличение ширины лобных рогов (преимущественно) и высоты тел боковых желудочков. Кроме того, у 1 ребенка выявлено расширение межполушарной щели и субарахноидальных пространств по конвекситальной поверхности мозга до 0,7 см. В течение периода наблюдения субэпендимальные кисты уменьшались в размерах у 11 детей (полностью резорбировались в конце периода наблюдения у 10 из них) и только у 1 ребенка односторонняя субэпендимальная киста увеличилась к 2 мес. жизни с 0,5 до 1 см.
Всем новорожденным II группы, как и детям I группы, проводилась иммунотерапия различными иммуноглобулинами (цитотект, пентаглобин), 3 детям - иммунохимиотерапия (цитотект, виролекс). Положительный терапевтический эффект отмечался у всех детей этой группы.
Эффективность лечения оценивалась по срокам выхода из тяжелого состояния, ликвидации или уменьшению явлений инфекционного токсикоза, нарастанию массы тела, данным динамической эхоэнцефалографии и лабораторным показателям. При катамнестическом наблюдении психоэмоциональное и моторное развитие у 6 детей II группы соответствовало возрастной норме. У других 6 детей этой группы в течение первого полугодия отмечено выраженное в различной степени отставание психомоторного развития (3-е из них имели вентрикуломегалию). К концу первого года жизни признаки церебрального дефицита у них отсутствовали.
Как и в I группе детей, мы не выявили отчетливой связи между числом, локализацией, динамикой субэпендимальных кист и данными комплексного иммунологического обследования, а также клиническими проявлениями заболевания как в раннем неонатальном периоде, так и в конце периода наблюдения.
Как известно, субэпендимальные кисты, возникающие при инфекции, являются результатом поражения субэпендимально расположенного герминативного матрикса инфекционным агентом. В начале процесса в зоне повреждения герминативного матрикса возникает участок некроза, который по мере его резорбции в течение 3-4 нед. трансформируется в кистозную полость [9]. Полная резорбция кисты, как показали наши исследования, происходит к концу 2-4 мес. жизни ребенка (чем больше кистозная полость, тем дольше идет процесс ее резорбции). Так как во всех приводимых нами наблюдениях уже при первом эхографическом исследовании головного мозга были выявлены субэпендимальные кисты, мы можем утверждать, что повреждение герминативного матрикса произошло в период внутриутробного развития.
Из 396 новорожденных с субэпендимальными кистами только один ребенок имел гестационный возраст 30 нед., подавляющее число новорожденных (88,9%) были доношенными. Зная время, необходимое на формирование субэпендимальной кисты в зоне некроза, можно предположить, что в подавляющем большинстве случаев повреждение матрикса произошло в конце II - начале III триместра беременности. При повреждении герминативного матрикса на стадии активной пролиферации его клеток (до 20 нед. гестации), обеспечивающей формирование серого вещества и глии [6], можно ожидать возникновения пороков развития головного мозга, обусловленных нарушением миграции, или внутриутробной гибели плода. Поскольку как первое, так и второе встречаются довольно редко, кроме того, учитывая, что субэпендимальные кисты в основном выявлены у доношенных детей, мы полагаем, что до 20 нед. гестации герминативный матрикс обладает определенной резистентностью к действию инфекционного агента.
Структурные же изменения головного мозга у новорожденных в виде субэпендимальных кист, по-видимому, являются исходом повреждения герминативного матрикса, находящегося в процессе регрессии (после завершения своей основной функции). Опровергнуть или подтвердить это предположение могут данные скринингового ультразвукового исследования головного мозга плода, проведенного в начале II триместра беременности, высококвалифицированным специалистом с использованием трансвагинального датчика.
Схожесть клинической картины заболевания у новорожденных I и II групп, этиологии процесса, установленной иммунологическим методом, а также высокий терапевтический эффект при использовании одних и тех же лекарственных препаратов свидетельствуют о том, что не кисты сосудистых сплетений и субэпендимальные кисты являются определяющими в клинической картине заболевания, а, по-видимому, сходные патоморфологические изменения, возникающие в головном мозге под влиянием инфекции, не обнаруживаемые при эхоэнцефалографии. Кисты сосудистых сплетений и субэпендимальные кисты - лишь маркеры этих патологических процессов. В то же время, выявление при эхографии головного мозга кист сосудистых сплетений и (или) субэпендимальных кист при клинической картине, характерной для внутриутробных вирусных инфекций, дает основание для проведения иммунохимиотерапии еще до получения результатов иммунологического исследования, что ведет к снижению тяжелых церебральных расстройств у детей раннего возраста.
Литература
- Кудашов Н.И., Озерова О.Е., Орловская И.В. Неврологические проявления при герпесвирусной инфекции у новорожденных // Педиатрия . - 1997. - N5. -С.42-45.
- Whitley R.T. Neonatal herpes Simplex infections // J. Med.Virol. - 1993. - V.1.- Suppl.- P.13-21.
- MurguiapdepSierra T., Florido J.,Minox T., Arriola M et al. Neonatal herpetic encephalitis . Current concepts concerning a case.// Rev. Invest. Clin. - 1996. - V.48. - N 1. - P. 35-41.
- Озерова О.Е., Кудашов Н.И., Орловская И.В. Особенности эхоэнцефалограммы у новорожденных с герпетической инфекцией // Ультразвуковая диагностика в акушерстве, гинекологии и педиатрии. - 1993. - N2. - С. 55-70.
- Озерова О.Е., Казьмин А.М., Дайхина Л.В., Кудашов Н.И., Орловская И.В. Клиническое значение кист сосудистых сплетений желудочков головного мозга у новорожденных // Акушерство и гинекология - 1993. - N 1. - вС. 31-33.
- Mito T., Ando Y.,Takeshita K.,Takada K., Takashima S. Ultrasonographical and morphological examination of subependimal cysts lesions in maturely born infants //Neuropediatrics. - 1989. - V.20. - N 4. - P. 211-214.
- Zorzi C., Angonese I. Subependimal pseudocysts in the neonate // Eur. J. Pediatr. - 1989. - V.148. - P. 462-464.
- Yamashita Y., Outani Y., Kawano Y., Horikawa M et al. Clinical analyses and short-term prognoses of neonates with subependimal cysts // Pediatr. Neurol. - 1990. - V.6. - N6. - P. 375378.
- Озерова О.Е., Казьмин А.М., Дайхина Л. В. Субэпендимальные кровоизлияния у новорожденных: эхографическая характеристика и психоневрологические исходы // Акушерство и гинекология. - 1991. - N3. - С. 40-43.
УЗИ аппарат HS40
Читайте также:
