УЗИ, МРТ при врожденной диафрагмальной грыже у плода
Добавил пользователь Владимир З. Обновлено: 28.01.2026
Рекомендовано
Экспертным советом
РГП на ПХВ «Республиканский центр
развития здравоохранения»
Министерства здравоохранения
и социального развития
Республики Казахстан
от «27» ноября 2015 года
Протокол № 17
Название протокола: Диафрагмальная грыжа у детей.
Врожденная диафрагмальная грыжа - это порок развития, при котором происходит перемещение органов брюшной полости в грудную через естественные или патологические отверстия в диафрагме, а также путем выпячивания ее истонченного участка [1,2].
Код протокола:
Код(ы) МКБ-10:
Q 79.0 Врожденная диафрагмальная грыжа
Сокращения, используемые в протоколе:
| АЛТ - аланинаминотрансфераза АСТ - аспартатаминотрансфераза ВИЧ - вирус иммунодефицита человека ИФА - иммуноферментный анализ ЖКТ - желудочно-кишечный тракт КЩС - кислотно-щелочное основание КАМЛ - кисто-аденаматозная мальформация легкого КТ - компьютерная томография МРТ - магнитно-резонансная томография НСГ - нейросонография ОАК - общий анализ крови ОАМ - общий анализ мочи CCC - сердечно-сосудистая система УЗИ - ультразвуковое исследование ЭхоКГ - эхокардиография Іg М - иммуноглобулин М ½ - одна вторая часть ¼ - одна четвертая часть |
Дата разработки протокола: 2015 год.
Категория пациентов: дети.
Пользователи протокола: врачи общей практики, педиатры, неонатологи, врачи и фельдшеры бригады скорой медицинской помощи, хирурги.
Примечание: в данном протоколе используются следующие классы рекомендаций и уровни доказательств ссылку:
Уровень I - Доказательства, полученные в ходе по крайней мере от одного должным образом разработанного случайного контролируемого исследования или мета-анализа
Уровень II - Доказательства, полученные в ходе по крайней мере от одного хорошо разработанного клинического испытания без надлежащей рандомизации, от аналитического когортного или исследования типа случай-контроль (предпочтительно из одного центра) или от полученных драматических результатов в неконтролируемых исследованиях.
Уровень III - Доказательства, полученные от мнений авторитетных исследователей на основе клинического опыта.
Класс А - Рекомендации, которые были одобрены по согласованию по крайней мере 75% процентов мультисекторной группы экспертов.
Класс B - Рекомендации, которые были несколько спорны и не встречали согласие.
Класс C - Рекомендации, которые вызвали реальные разногласия среди членов группы.

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Грыжи собственно диафрагмы
Выпячивание истонченной зоны диафрагмы (истинные грыжи):
· выпячивание ограниченной части купола
· выпячивание значительной части купола
· полное выпячивание одного купола (релаксация)
Дефекты диафрагмы (ложные грыжи):
· щелевидный задний дефект
· значительный дефект
· отсутствие купола диафрагмы
Грыжи переднего отдела диафрагмы
· передние грыжи (истинные грыжи)
· френоперикардиальные грыжи (ложные грыжи)
· ретроградные френоперикардиальные грыжи (ложные грыжи)
Грыжи пищеводного отверстия диафрагмы (истинные грыжи)
· эзофагеальные
· параэзофагеальные
По расположению:
· левосторонние (около 80%)
· правосторонние (около 20%) - передняя Морганьи
· двусторонние (менее 1%)
Клиническая картина
Cимптомы, течение
Диагностические критерии постановки диагноза:
Жалобы и анамнез:
· кашель;
· одышка;
· тахикардия;
· рвота после приема пищи;
· частые пневмонии.
Физикальное обследование:
· асимметрия грудной клетки с выбуханием на стороне поражения с отсутствием экскурсии;
· инспираторная одышка с участием вспомогательных дыхательных мышц;
· запавший «ладьевидный живот»;
· при перкусии отмечается тимпанит со смещением органов средостения имеющий не постоянный характер.
· при аускультации выслушиваются кишечные шумы в грудной клетке;
· на стороне поражения дыхание резко ослабленное или не прослушивается, на противоположной стороне дыхание ослаблено в меньшей степени.
Диагностика
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне:
· общий анализ крови
· общий анализ мочи
· биохимический анализ крови (общий белок и его фракции, мочевина, креатинин, остаточный азот, АЛТ, АСТ, глюкоза, общий билирубин, прямая и непрямая фракция, калий, натрий, хлор, кальций);
· обзорная рентгенография органов грудной полости в прямой и боковой проекциях.
Дополнительные диагностические обследования, проводимые на амбулаторном уровне:
· НСГ детей до 1 года для исключения патологии ЦНС;
· ЭхоКГ по показаниям.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию (стационарозамещающей помощи): согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Основные (обязательные) диагностические обследования, проводимые на стационарном уровне при экстренной госпитализации и по истечении сроков более 10 дней с момента сдачи анализов в соответствии с приказом МО:
· коагулограмма;
· определение газов крови;
· иммунограмма.
Дополнительные диагностические обследования, проводимые на стационарном уровне при экстренной госпитализации и по истечении сроков более 10 дней с момента сдачи анализов в соответствии с приказом МО:
· исследование крови на стерильность с изучением морфологических свойств и идентификацией возбудителя и чувствительности к антибиотикам;
· контрастное исследование ЖКТ для верификации смещения органов брюшной полости через дефекты диафрагмы;
· КТ/МРТ органов грудной клетки/органов брюшной полости позволяет убедительно поставить диагноз диафрагмальной грыжи, провести дифференциальный диагноз, а также правильно выбрать хирургический доступ;
Инструментальные исследования:
· обзорная рентгенография органов грудной клетки - наличие ячеистых полостей, смещение органов средостения в противоположную сторону обусловленных перемещенными в грудную полость органов брюшной полости;
· УЗИ органов грудной клетки - выявляется смещение органов брюшной полости (в частности печени, селезенки) в плевральную полость;
· ЭхоКГ - отмечается смещение сердца в противоположную от грыжи сторону с функциональными отклонениями показателей сердечной деятельности;
· контрастное исследование ЖКТ для верификации смещения органов брюшной полости через дефекты диафрагмы.
Показания для консультации узких специалистов:
· консультация педиатра для исключения сопутствующей соматической патологии;
· консультация кардиолога для исключения патологии ССС;
· консультация пульмонолога для исключения патологии дыхательной системы.
Лабораторная диагностика
Лабораторные исследования:
· специфичных для диафрагмальной грыжи изменений в лабораторных анализах не отмечаются.
Дифференциальный диагноз
Дифференциальная диагностика [4,5]
Таблица - 1. Дифференциальная диагностика диафрагмальной грыжи
| Ложная диафрагмаль-ная грыжа | КАМЛ | Опухоль средостения (или нейробластома) | Легочная секвестрация | Бронхогенная киста | Врожденная лобарная эмфизема |
| При даче контрастно-го вещества орально, через 2-3 часа позволяют выявить местораспо-ложения петель кишечника | В зоне пораже-ния тонко-стенные воздуш-ные кисты. | Тень (анэхогенная) с четкими контурами с локализацией в переднем или заднем средостении | Отсуст-вие анэхо-генного образования в структуре пораженного участка | Изолированное анэхоген-ного образования в структуре легкого, не сопровождающей повышение эхогенности окружающей ткани. | Перерастяжение легочной паренхимы без деструкции. |
Лечение
Цели лечения: низведение смещенных органов в брюшную полость с восстановлением целостности диафрагмы.
Тактика лечения:
Основным методом лечение является оперативное устранение диафрагмальной грыжи:
· устранение грыжи диафрагмы, фундопликация по Ниссену и другие модификации [5,6];
· торакоскопическое/лапароскопическое устранение диафрагмальной грыжи с фундопликацией 7.
Хирургическое вмешательство:
· устранение грыжи диафрагмы, фундопликация по Ниссену и другие модификации;
· торакоскопическое/лапароскическое устранение диафрагмальной грыжи с фундопликацией.
Хирургическое вмешательство, оказываемое в стационарных условиях:
Виды операции:
· устранение грыжи диафрагмы, фундопликация по Ниссену и другие модификации.
Показания:
· истинные грыжи;
· грыжи пищеводного отверстия диафрагмы;
· параэзофагельные грыжи и наличие признаков недостаточности кардии, рецидив диафрагмальной грыжи с выраженным спаечным процессом.
Виды операции:
· торакоскопическое/лапароскическое устранение диафрагмальной грыжи с фундопликацией.
Показания к торакоскопическому устранению диафрагмальной грыжи:
· истинные диафрагмальные грыжи;
· грыжа Богдалека и релаксация диафрагмы.
Показания к лапароскопическому устранению:
· ретростернальные грыжи и грыжи пищеводного отверстия диафрагмы.
В том числе противопоказания имеются абсолютные и относительные:
К абсолютным противопоказаниям относятся:
· тяжелое состояние больного, обусловленное тяжелой соматической;
· врожденной патологией сердечно-сосудистой системы;
· нарушение свертывающей системы крови.
К относительным противопоказаниям относятся:
· вирусно-бактериальные инфекции (катаральные явления);
· белково-энергетическая недостаточность II - III степени;
· анемия;
· белково- энергетическая недостаточность 2-3 степени;
· заболевания дыхательных органов;
· неудовлетворительное состояние кожных покровов (пиодермия, свежие явления экссудативного диатеза, инфекционные заболевания в остром периоде).
Немедикаментозное лечение:
Режим: I,II,III.
Стол: №1,15.
Другие виды лечения:
· дыхательная гимнастика;
· общеукрепляющий массаж.
Другие виды, оказываемые на стационарном уровне:
· дыхательная гимнастика;
· общеукрепляющий массаж.
Индикаторы эффективности лечения:
· восстановление целостности диафрагмы;
· отсутствие признаков гипоплазии, ателектаза и воспаления легких;
· отсутствие смещения органов брюшной полости в плевральную и перикардиальную полости;
· отсутствие смещения органов средостения в противоположную сторону.
Препараты (действующие вещества), применяющиеся при лечении
| Альбумин (Albumin) |
| Амброксол (Ambroxol) |
| Амикацин (Amikacin) |
| Декстроза (Dextrose) |
| Инсулин растворимый (человеческий генно-инженерный) (Insulin soluble (human biosynthetic)) |
| Калия хлорид (Potassium chloride) |
| Кальция хлорид (Calcium chloride) |
| Лоратадин (Loratadine) |
| Метоклопрамид (Metoclopramide) |
| Метронидазол (Metronidazole) |
| Натрия хлорид (Sodium chloride) |
| Плазма свежезамороженная |
| Преднизолон (Prednisolone) |
| Цефуроксим (Cefuroxime) |
| Эритроцитарная масса |
| Этамзилат (Etamsylate) |
Госпитализация
Показания для госпитализации с указанием типа госпитализации:
Показания для плановой госпитализации:
Грыжи собственно диафрагмы:
· выпячивание ограниченной части купола диафрагмы;
· грыжи переднего отдела диафрагмы;
· грыжи пищеводного отверстия диафрагмы (эзофагеальные, параэзофагеальные).
Показания для экстренной госпитализации:
Грыжи собственно диафрагмы:
· полное выпячивание одного купола диафрагмы со смещением органов средостения в противоположную сторону;
Ложные грыжи:
· щелевидный задний дефект диафрагмы;
· значительный дефект диафрагмы;
· отсутствие купола диафрагмы.
Грыжи переднего отдела диафрагмы:
· френоперикардиальные грыжи;
· ретроградные френоперикардиальные грыжи.
Профилактика
Профилактические мероприятия:
Первичной профилактики диафрагмальной грыжи не существует. Профилактика осложнений: ранняя диагностика, своевременная госпитализация и оперативное лечение снижают риск развития осложнений диафрагмальной грыжи 13.
Дальнейшее ведение:
· в послеоперационном периоде дети с диафрагмальной грыжей находятся в отделение интенсивной терапии и реанимации (2-3 суток), где проводится профилактика послеоперационной пневмонии, нарушение функции ССС, ЖКТ;
· постоянный контроль за сатурацией кислорода, КЩС, гемодинамики;
· парентеральное питание проводится до восстановления пассажа по ЖКТ;
· ежедневные перевязки послеоперационной раны;
· снятие швов на 7-10 сутки;
· всем детям, оперированным по поводу врожденной диафрагмальной грыжи, необходимо диспансерное наблюдение. Диспансеризация и объем лечебных мероприятий осуществляется на основании ближайших и отдаленных результатов оперативного вмешательства через 1-2 года.
Информация
Источники и литература
Информация
Список разработчиков протокола с указание квалификационных данных:
1) Карабеков Агабек Карабекович - доктор медицинских наук, профессор, РГП на ПХВ «Южно-Казахстанская государственная фармацевтическая академия», заведующий кафедрой детской хирургии.
2) Дженалаев Булат Канапьянович - доктор медицинских наук, профессор, РГП на ПХВ «ЗападноКазахстанский государственный медицинский университет им. Марата Оспанова», руководитель кафедры детской хирургии.
3) Ботабаева Айгуль Сапарбековна - кандидат медицинских наук, исполняющая обязанностями доцента кафедры детской хирургии АО «Медицинский Университет Астана».
4) Калиева Шолпан Сабатаевна - кандидат медицинских наук, доцент РГП на ПХВ «Карагандинский государственный медицинский университет», заведующая кафедрой клинической фармакологии и доказательной медицины.
Указание на отсутствие конфликта интересов: нет.
Рецензент: Марденов Аманжол Бакиевич - доктор медицинских наук, профессор кафедры детской хирургии РГП на ПХВ «Карагандинский государственныйо медицинский университет»
Указание условий пересмотра протокола: Пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Врожденная диафрагмальная грыжа
Врожденная диафрагмальная грыжа - это порок развития диафрагмы, приводящий к нарушению разделения брюшной полости и грудной клетки, а так же к смещению желудка, селезенки, кишечника и печени в грудную полость.
Врожденная диафрагмальная грыжа может быть изолированным пороком, а также сочетаться с пороками развития других органов и систем. Большинство случаев врожденных диафрагмальных грыж спорадические.

Частота встречаемости 1 на 4000 живорожденных, соотношение полов 1:1
Диафрагмальная грыжа может сочетаться с пороками сердца, на которые приходится около 20%. Сочетания с пороками центральной нервной системы и мочевыделительной системы составляют по 10,7%. Около 10-12% врожденных диафрагмальных грыж, диагностированных пренатально, являются составной частью различных наследственных синдромов (пентада Кантрелла, синдромы Фринзе, Ланге, Марфана, Элерса-Данлоса и т.д.) или проявлением хромосомных аномалий и генных нарушений. Частота хромосомных аномалий в среднем составляет 16 %. Еще раз следует подчеркнуть, что хромосомные аномалии чаще выявляются только в тех случаях, когда врожденная диафрагмальная грыжа сочетается с другими пороками развития. Следовательно, пренатальное кариотипирование показано во всех случаях наличия сочетанной патологии, для уточнения генеза порока.
Относительно сторон поражения все врожденные диафрагмальные грыжи делятся на:
- Левосторонние около 80%
- Правосторонние около 20%.
- Двусторонние менее 1%.
Большинство новорожденных с врожденной диафрагмальной грыжей разворачивают картину дыхательной недостаточности непосредственно в родовом зале сразу после рождения. Очень быстро прогрессирует острая дыхательная недостаточность. При осмотре обращает на себя внимание ассиметрия грудной клетки с выбуханием стороны поражения (обычно слева) и отсутствием экскурсии грудной клетки с этой стороны. Очень характерный симптом - запавший ладъевидный живот.
Главным методом дородового выявления врожденной диафрагмальной грыжи является эхография. При ультразвуковом исследовании подозрение на этот порок возникает при аномальном изображении органов грудной клетки. Одним из основных эхографических признаков, является смещение сердца, а также появление в грудной клетке желудка и петель тонкого кишечника. Пренатальное ультразвуковое исследование может выявить наличие содержимого брюшной полости в грудной клетки уже на 12 неделе беременности. Тем не менее, обычно диагноз ставится на 16-неделе беременности.
Ранняя диагностика ВДГ дает возможность провести кариотипирование, для исключения сочетанной хромосомной аномалии. Так же по данным УЗИ в I и II-м триместре беременности есть возможность определиться в необходимости фетальных вмешательств для стабилизации плода с ВДГ.
После рождения диагноз ВДГ подтверждается после проведения комплексного УЗИ и рентгенографии органов грудной и брюшной полости.
При рождении ребенка с диафрагмальной грыжей врачи должны быть готовы к проведению расширенной сердечно-легочной реанимации. Интубация трахеи и ИВЛ показана с первой минуты жизни. Уже в родзале ребенок с ВДГ может потребовать введение лекарственных препаратов, стабилизирующих работу сердца. Только достигнув стабильного состояния, возможна транспортировка ребенка из родзала, она выполняется в условиях транспортного кувеза на ИВЛ с мониторингом жизненных функций.
В условиях реанимационного блока отделения продолжается интенсивная терапия, направленная на стабилизацию состояния и подготовке к операции: подбор методов и параметров ИВЛ, кардиотоническая поддержка, седативная и обезболивающая, антибактериальная терапия.
По мере стабилизации состояния решается вопрос о возможности оперативного лечения.
В случае нестабильности состояния в нашем отделении есть возможность использовать методику экстракорпоральной методики поддержки работы сердца и легких - ЭКМО.
Оперативное лечение детей с ВДГ осуществляется преимущественно малоинвазивным эндоскопическим методом. Через минимальные проколы грудной клетки (3 мм) осуществляется бережное погружение содержимого из грудной полости в брюшную. После чего оценивается дефект диафрагмы: в случае достаточно развитой собственной диафрагмы пластика дефекта осуществляется собственными тканями, а при выраженном дефиците тканей - дефект замещается имплантом (используется синтетический материал Гор-Текс и биологический материал Пермакол).
В послеоперационном периоде продолжается интенсивная терапия, направленная на коррекцию дефицитов, которые сохраняются, пока гипоплазированное легкое не восстановится.
В ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России Вы получаете уникальную возможность получить БЕСПЛАТНО оперативное стационарное лечение по квотам на высоко-технологическую медицинскую помощь (ВМП по ОМС).
Руководство по диагностике и лечению врожденной диафрагмальной грыжи (Canadian Medical Association Journal, январь 2018)

В журнале Canadian Medical Association Journal 29 января 2018 г. опубликовано Канадское руководство по диагностике и лечению врожденной диафрагмальной грыжи.
Пренатальная диагностика
- УЗИ измерение наблюдаемого-к-ожидаемому легочно-головного отношения (O/E LHR) должно выполняться между 22 и 32 неделями гестационного возраста для прогнозирования тяжести легочной гипоплазии при изолированной врожденной диафрагмальной грыже.
- Для оценки объема лёгких и вовлечения печени в грыжеобразование при умеренной и тяжелой врожденной диафрагмальной грыже необходимо использовать МРТ плода (при наличии МРТ).
Вентилирование
- Новорожденные с врожденной диафрагмальной грыжой и с немедленным расстройством дыхания должны предпочтительно быть интубированы при рождении. Необходимо избегать искусственной вентиляции легких мешком Амбу.
- Необходимо обеспечить седацию всем новорожденным с врожденной диафрагмальной грыжой на ИВЛ. Глубокая седация и нейромышечная блокада должны выборочно проводиться детям с большей необходимостью в вентиляции или кислороде.
- Необходимо использовать Т-переходник (T-piece) с аппаратом ИВЛ, чтобы избежать пиковое давление на вдохе > 25 см Н2О.
- У всех новорожденных с врожденной диафрагмальной грыжой должны быть следующие целевые значения: артериальное рСО2 между 45 и 60 мм рт ст, и рН между 7,25 и 7,40 .
- Необходимо титровать подачу кислорода чтобы достичь уровня предуктальной сатурации как минимум 85 %, но не более 95 %.
- Изначальным режимом ИВЛ для новорожденных с врожденной диафрагмальной грыжой, которым требуется дыхательная поддержка, должен быть щадящяя перемежающаяся принудительная вентиляция (intermittent mandatory ventilation). Высокочастотная осцилляторная ИВЛ (High-frequency oscillatory ventilation) или высокочастотная струйная ИВЛ (high-frequency jet ventilation) должна применяться когда пиковое давление на вдохе, необходимое для контроля гиперкапнии при перемежающейся принудительной вентиляции, превышает 25 см Н2О.
Гемодинамическая поддержка
- Лечение плохой перфузии (время капиллярного наполнения > 3 сек, лактат > 3 ммоль/Л, выделение мочи < 1 мл/кг/час) и снижение АД ниже норм по возрасту должно включать:
-- разумное применение кристаллоидов, обычно не превышая 20 мл/кг;
-- инотропные препараты, такие как допамин или адреналин;
-- гидрокортизон.
- Если плохая перфузия продолжается, необходимо произвести оценку функции сердца (ЭХОКГ, сатурацию в центральных венах).
ЭХОКГ
- Две стандартные ЭХОКГ, одна в течение 48 часов после рождения и вторая на 2 - 3 неделе жизни, необходимы для оценки лёгочного сосудистого сопротивления, функции левого и правого желудочка. При наличии показаний могут понадобиться дополнительные обследования.
Лечение легочной гипертензии
- Ингаляция закиси азота показана при подтвержденной супрасистемной легочной артериальной гипертензии без левожелудочковой дисфункции и с адекватной мобилизацией легких (lung recruitment). При отсутствии клинического ответа или ответа на ЭХОКГ ингаляция закиси азота должна быть прекращена.
- Можно рассмотреть применение Силденафила у пациентов с рефрактерной легочной гипертензией (например не реагирующей на закись азота), либо как дополнение при снятии с закиси азота.
- Милринон должен применяться для лечения дисфункции сердца, особенно если дисфункция сердца связана с легочной гипертензией.
- Простагландин Е1 может применяться для сохранения артериального протока открытым и для снижения правожелудочковой постнагрузки у пациентов с легочной гипертензией с правожелудочковой недостаточностью, либо при наличии закрывающегося артериального протока.
Экстракорпоральная поддержка жизнеобеспечения
- Возможность экстракорпоральной поддержки жизнеобеспечения должна обсуждаться во время пренатальных консультаций по поводу врожденной диафрагмальной грыжи и обсуждение должно включать информацию, что имеющиеся доказательства не показали преимущества по выживаемости при применении экстракорпоральной поддержки жизнеобеспечения.
Операция
Следующие физиологические критерии должны соответствовать до операции:
- выделение мочи > 1 мл/кг/час.
- FiO2 < 0,5 .
- предуктальная сатурация кислорода между 85 % и 95 %.
- нормальное среднее АД в соответствии с гестационным возрастом.
- лактат < 3 ммоль/Л.
- оцененное давление в легочной артерии меньше системного давления.
Если данные критерии не соответствуют в течение 2х недель, то необходимо рассмотреть попытку хирургического лечения, либо паллиативный подход.
- Применение заплатки: для диафрагмальных дефектов, которые не подходят для первичного хирургического лечения, то необходимо применить заплатку большого размера без натяжения из политетрафторэтилена/гортэкс.
- Сравнение открытой операции с минимально инвазивной операцией: минимально инвазивный подход или техника не должна быть использована для хирургической коррекции неонатальной врожденной диафрагмальной грыжи ввиду высокой частоты рецидивов.
- У пациентов на экстракорпоральной поддержке жизнеобеспечения: операцию необходимо избегать до деканюляции. Если пациента не возможно снять с экстракорпоральной поддержки жизнеобеспечения, то необходимо рассмотреть попытку хирургического лечения, либо паллиативный подход.
Ведение (контроль) в длительном периоде
- Рекомендуется стандартизованное мульти-дисциплинарное ведение (контроль) детей с врожденной диафрагмальной грыжей для обеспечения наблюдения и скрининга, оптимальной и своевременной диагностики и лечения, подходящего для уровня риска.
- Рекомендуется выявлять подгруппу выживших пациентов с врожденной диафрагмальной грыжей с высоким риском заболеваемости в долгосрочном периоде, таких как: которым потребовалась экстракорпоральная поддержка жизнеобеспечения, которым для лечения применили заплатку, или которым требовалась респираторная поддержка на 30й день жизни.
Подробнее смотрите в прикрепленном файле .
Посмотреть другие обзоры
Автор обзора
Автор обзоров мировой медицинской периодики на портале MedElement - врач общей практики, хирург Талант Иманалиевич Кадыров.
Закончил Киргизский Государственный медицинский институт (красный диплом), в совершенстве владеет английским языком. Имеет опыт работы хирургом в Чуйской областной больнице; в настоящий момент ведет частную практику.
Регулярное повышение квалификации: курсы Advanced Cardiac Life Support, International Trauma Life Support, Family Practice Review and Update Course (Англия, США, Канада).
Новые ультразвуковые технологии в оценке постнатального прогноза при диафрагмальной грыже у плода
Курс пренатальной диагностики РМАПО, Москва.
Кафедра детской хирургии РНИМУ им. Н.И. Пирогова, Москва.
Детская клиническая больница им. Н.Ф. Филатова, Москва.
Кафедра акушерства и гинекологии ФППОВ I МГМУ им. И.М. Сеченова, Москва.

УЗИ аппарат HM70A
Экспертный класс по доступной цене. Монокристальные датчики, полноэкранный режим отображения, эластография, 3D/4D в корпусе ноутбука. Гибкая трансформация в стационарный сканер при наличии тележки.
Введение
Диафрагмальная грыжа - это корригируемый порок развития, который хорошо диагностируется до родов. Главная проблема заключается в составлении постнатального прогноза. Около 40% новорожденных с диафрагмальной грыжей погибают от гипоплазии легочной ткани и легочной гипертензии, поэтому точность дородовой оценки размеров легких плода и функциональных резервов компрессированной легочной ткани играет важную роль в этом процессе [1, 2]. Целью настоящей работы явилось изучение возможностей применения трехмерного УЗИ в оценке состояния легких при диафрагмальной грыже и прогнозировании постнатальных исходов при дородовой диагностике этого порока развития.
Материалы и методы
С целью улучшения пренатального консультирования беременных с корригируемыми пороками развития у плода, в том числе, с диафрагмальной грыжей, в течение года (с августа 2011 г. по август 2012 г.) на базе отделения ультразвуковой диагностики многопрофильной детской клинической больницы проводились совместные консультации детского хирурга и врача ультразвуковой диагностики. На консультацию приглашались пациентки, у которых при ультразвуковом обследовании в учреждениях второго уровня было заподозрено и/или подтверждено наличие у плода пороков развития хирургического профиля. Всего на консультативном приеме обследовано 18 женщин с диафрагмальной грыжей у плода, что составило 14,8% от общего количества проконсультированных за этот период и 57,2% от всех новорожденных, оперированных в отделении хирургии по поводу диафрагмальной грыжи за указанный период. Срок консультации варьировал от 16 до 37 нед и в среднем составил 31 нед 2 дня. До 22 нед обратились 2 (12%) пациентки, в 22-31 нед - 4 (24%), после 32 нед - 11 (64%). Средний срок диагностики диафрагмальной грыжи на первом этапе составил 26,0 нед (13-36 нед), при этом до 14 нед было диагностировано 2 (12%) случая, до 22 нед - 2 (12%), в 22-31 нед - 7 (41%), после 32 нед - 6 (35%).
Всем беременным проведено экспертное ультразвуковое исследование с измерением размеров легких, а также изучение взаиморасположения органов брюшной и грудной полости. Особое внимание уделялось положению печени и степени ее смещения в грудную полость. Во всех случаях была получена объемная информация и сохранена в памяти ультразвукового аппарата для дальнейшего анализа в режиме off line (без пациента). Основные исследования проводились на современных ультразвуковых приборах, включая Accuvix-V20 (Samsung Medison).
При пролонгировании беременности пациентки получали направление на родоразрешение в специализированный акушерский стационар. Всем новорожденным на первом этапе оказывалась реанимационная помощь в родовспомогательных учреждениях и после стабилизации состояния они переводились в хирургическое отделение для оперативного лечения.
В конечный анализ включены 14 из 18 случаев пренатальной диагностики диафрагмальной грыжи. В 2 клинических наблюдениях беременность по желанию семьи была прервана по медицинским показаниям, в 1 диагноз диафрагмальной грыжи снят, еще в 1 при консультативном осмотре у плода дополнительно были выявлены множественные пороки развития (плод антенатально погиб в III триместре беременности). В 7 из 14 случаев новорожденные погибли на этапе оказания помощи в родовспомогательных учреждениях, в 7 - оперированы: из них 2 закончились летальным исходом в связи с осложнениями, связанными с гипоплазией и гипертензией легких; 5 - выписаны в удовлетворительном состоянии после операции.
Результаты и обсуждение
В пренатальном периоде легкие находятся в сжатом состоянии и не выполняют своей основной функции (дыхание), поэтому провести до родов объективную оценку их функционального состояния нельзя. Даже в случае нормального развития плода и отсутствия каких-либо анатомических изменений в легких с уверенностью предсказать их абсолютную функциональную полноценность в периоде новорожденности невозможно. При наличии диафрагмальной грыжи степень внутриутробной компрессии легочной ткани значительно возрастает, что еще более затрудняет прогноз.
Объем легких теоретически можно оценить в режиме 2D, однако с введением в клиническую практику новых ультразвуковых технологий появилась надежда, что теперь это измерение можно делать точнее и проще. Действительно, использование программы VOCAL (Virtual Organ Computer-aided AnaLysis) позволяет получить фактически виртуальный "слепок" легких (рис. 1). Для этого объем грудной клетки следует получить в 3D режиме в сагиттальной плоскости, когда плод расположен лицом к датчику. Желательно соблюдать следующие правила: датчик слегка наклонить к голове для лучшей визуализации диафрагмы, использовать высокое качество изображения и гармоники, величина угла захвата изображения от 40 до 85º в зависимости от срока.
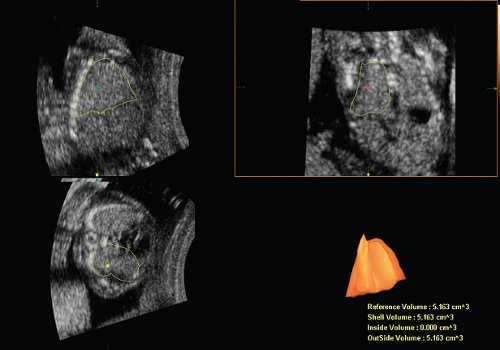
Рис. 1. Реконструкция здорового правого легкого и расчет его объема с применением программы VOCAL.
Далее формирование объемного изображения необходимо производить путем последовательных поворотов изображения легкого, каждый из которых составляет 30º. Ось вращения должна проходить через верхушку легкого и точку, максимально близкую к диафрагме. Контур легкого лучше обводить вручную. Стартовой позицией для вращения следует выбирать максимальный переднезадний диаметр легкого [2].
На первый взгляд, эта методика не очень сложна, однако правильно провести все этапы объемной реконструкции можно только при высоком качестве первично полученного объема. Даже при отсутствии патологии легких существует много факторов, затрудняющих визуализацию этого органа и влияющих на качество объемной информации. Прежде всего это срок беременности. До 32 нед неудачными для дальнейшей обработки являются 3-7% от всех сохраненных объемов, тогда как после этого срока - около 30%. Кроме того, к таким факторам относятся маловодие, плохая визуализация плода при ожирении пациентки, неудобное (например, поперечное) положение плода. Диафрагмальная грыжа сама по себе резко ухудшает визуализацию легких в связи с их компрессией (рис. 2) [3].
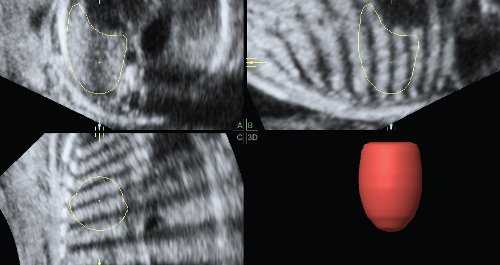
Рис. 2. Измерение объема контралатерального легкого при левосторонней диафрагмальной грыже. Тень от ребер мешает визуализации границ компрессированного легкого.
В нашем исследовании большинство консультаций (64%) было проведено после 32 нед в связи с поздней (средний срок 26 нед) диагностикой диафрагмальной грыжи, поэтому качество объемной информации в целом оказалось невысоким. Тем не менее в 11 из 14 случаев мы имели возможность получить дополнительные сведения при ретроспективном анализе.
Даже при нормальной анатомии органа и при отсутствии факторов, затрудняющих визуализацию, расхождение в оценке объема легких между специалистами и даже между измерениями одного и того же врача может быть очень существенным. Так, на предварительном этапе подготовки к этой работе разница в результатах при оценке объема нормального легкого одним врачом достигала 17,7%, а при реконструкции контралатерального легкого при диафрагмальной грыже - 25,2%. Кроме того, сам процесс реконструкции объема требует серьезных навыков и немалого свободного времени, что ограничивает возможность его клинического применения.
В рамках настоящего исследования мы использовали более традиционные методы оценки легких. Еще в середине 90-х гг. ХХ века была предложена методика пренатального прогнозирования сердечнолегочных осложнений при наличии диафрагмальной грыжи по степени компрессии контралатерального, т.е. условно здорового, легкого. Наиболее популярным критерием оценки постнатального прогноза при диафрагмальной грыже с тех пор стал LHR (lung-head ratio, легочноголовное отношение или ЛГО). Первоначально правое (условно здоровое) легкое при левосторонней диафрагмальной грыже измеряли в срок до 25 нед путем умножения максимальных диаметров, и полученный показатель соотносили с окружностью головы, измеренной при сканировании в стандартной аксиальной плоскости для оценки бипариетального размера (четкая визуализация М-эхо и задних рогов боковых желудочков, расположение полости прозрачной перегородки на расстоянии 1/3 от лобной кости) [4].
В течение последующих лет были проведены многочисленные исследования, направленные на изучение возможностей предложенного метода не только во II, но и в III триместре беременности. Результаты, полученные многими исследователями, существенно отличаются в связи с разными сроками обследования, небольшим количеством пациентов в нескольких сериях исследований, с затруднениями при оценке легкого при правосторонней диафрагмальной грыже и при перемещении в грудную полость печени, что вызывает более сильную компрессию. Несмотря на определенные расхождения в результатах, во многих работах было установлено, что при ЛГО≤1,5 прогноз для новорожденного можно расценить как неблагоприятный или крайне сомнительный, тогда как показатель >2 свидетельствует о хорошем постнатальном прогнозе 6.
Для уменьшения расхождения в оценке ЛГО в норме и при диафрагмальной грыже группой авторов под руководством С. Peralta и K. Nikolaides [2] произведено сравнение возможных методов измерения легких. Было доказано, что метод трассировки (длина контура) дает наименьшие расхождения в измерениях между специалистами; метод двух перпендикуляров (перемножение максимальных диаметров) является наиболее популярным, но в неопытных руках может существенно (до 45%) завышать размеры легкого, метод с включением в расчет переднезаднего размера легкого наименее воспроизводим, поскольку нет точных ориентиров установки калиперов переднезаднего размера (рис. 3).
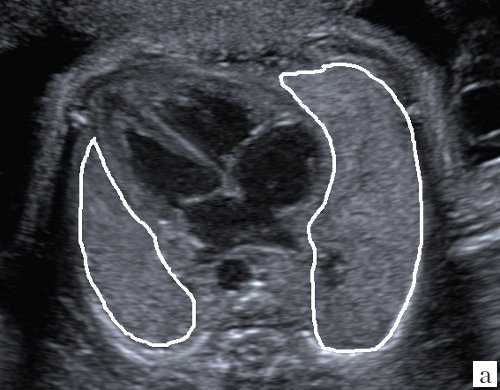
а) Метод трассировки.
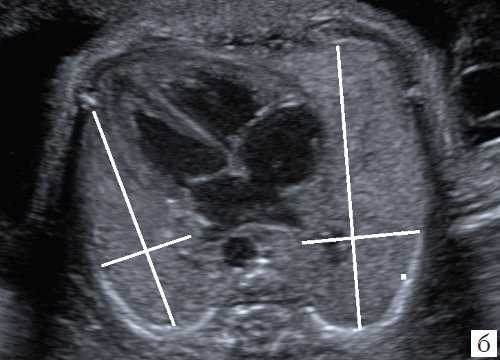
б) Метод двух перпендикуляров (метод максимальных диаметров).
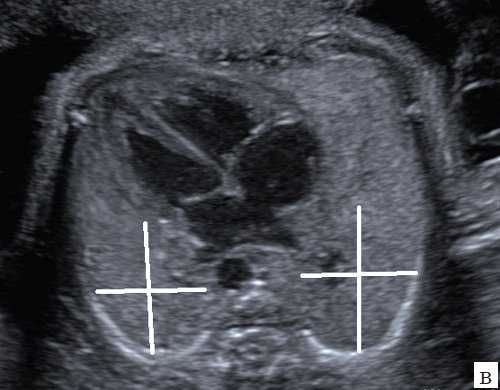
в) Метод оценки переднезаднего размера.
Этими же авторами были разработаны номограммы площади и ЛГО для правого и левого легкого в норме для каждой недели беременности с 12 нед до 32 нед (табл. 1) и дополнительно предложены формулы для расчета нормальной для срока площади легкого при любом из указанных трех способов измерения (табл. 2).
Таблица 2. Формула расчета ожидаемого для срока ЛГО при правосторонней и левосторонней диафрагмальной грыже с использованием разных методов оценки площади легкого [2].
| Метод измерения | Правое легкое при левосторонней диафрагмальной грыже | Левое легкое при правосторонней диафрагмальной грыже |
|---|---|---|
| Метод двух перпендикуляров (метод максимальных диаметров) | -3,4802+(0,3995xСБ)- -(0,0048xСБxСБ) | -2,5957+(0,3043xСБ)- -(0,0042xСБxСБ) |
| Метод оценки переднезаднего диаметра | -3,1597+(0,3615xСБ)- -(0,0041xСБxСБ) | -1,0224+(0,1314xСБ)- -(0,0011xСБxСБ) |
| Метод трассировки | -2,3271+(0,27xСБ)- -(0,0032xСБxСБ) | -1,4994+(0,1778xСБ)- -(0,0021xСБxСБ) |
Кроме того, были определены правила стандартизации измерений легких плода при диафрагмальной грыже.
- Измерение должно проводиться на уровне четырехкамерного среза сердца.
- Условно здоровое легкое должно располагаться ближе к датчику, чем легкое со стороны грыжи.
- Датчик следует располагать так, чтобы ультразвуковой сигнал шел параллельно ребрам по межреберному пространству во избежание тени, падающей на легкое.
- По получению оптимального среза для измерения (хорошо видны все опознавательные точки) изображение должно быть зафиксировано и затем увеличено так, чтобы аксиальный план занимал весь экран.
- Контралатеральное легкое можно измерить одним из трех способов, перечисленных выше, и затем полученный результат разделить на значение окружности головы для расчета ЛГО. Предпочтение следует отдавать методу трассировки, как наиболее воспроизводимому, особенно в условиях плохой визуализации легкого при диафрагмальной грыже. Необходимо следить за тем, чтобы миокард не входил в измеряемую часть изображения.
- После получения ЛГО следует разделить его на значение ЛГО, соответствующее средним нормативным значениям для срока, при котором проводится исследование.
- Минимальное количество измерений легких для достижения стабильного результата должно быть не менее 70. Желательно, чтобы врач, проводящий измерения, прошел курс специальной подготовки у врача-эксперта.
В нашем исследовании во всех случаях проводилась оценка контралатерального легкого по описанной выше методике двух перпендикуляров с использованием 2D режима и сохранялось двухмерное изображение с положением калиперов, фиксирующих размеры легкого. При получении значений ЛГО≤1,5 постнатальный прогноз расценивался как крайне сомнительный. В момент исследования объемная информация фиксировалась в архиве ультразвукового аппарата, но не обрабатывалась.
У 14 пациенток, включенных в исследование, ЛГО варьировало от 0,7 до 2,7, среднее значение составило 1,67. В 6 случаях ЛГО было менее 1,5 и 4 детей умерли на дооперационном этапе, 2 - после операции, в 3 случаях показатель превышал 1,5, но дети умерли до перевода в хирургический стационар. В 5 случаях ЛГО было более 1,5 и все дети были успешно прооперированы. Случаев, когда ЛГО было ≤1,5 и дети хорошо перенесли операцию, не было зафиксировано. Таким образом, чувствительность составила 66,7%, специфичность 100%, ложноположительный результат 0%, ложноотрицательный результат 33,3%.
Учитывая, что группа обследования была небольшой, нельзя полученные данные считать статистически достоверными. Кроме того, срок пренатальных консультаций значительно варьировал (16-36 нед), т.е. требовалось введение корректировки на срок беременности.
В исследовании, результаты которого приведены выше [2], было доказано, что в норме объем легких в течение беременности увеличивается в 16 раз, тогда как размеры головы только в 4 раза. В связи с такими особенностями роста органов плода в ходе беременности было рекомендовано не только измерять ЛГО, но и соотносить полученные данные со средними нормативными значениями ЛГО для того срока беременности, при котором проводится исследование. Согласно данным, приведенным выше (см. табл. 1), нижняя граница нормы для ЛГО для правого легкого в 12 нед составляет 0,21, в 20 нед - 1,26, в 22 нед - 1,45, в 32 нед - 2,03. Это означает, что при использовании для составления постнатального прогноза фиксированного значения ЛГО≤1,5 все здоровые плоды до 32 нед формально можно отнести к группе риска по гипоплазии легких.
На втором этапе настоящей работы ретроспективно в каждом случае был рассчитан показатель соотношения измеренного и ожидаемого (по средней границе нормы для срока) ЛГО (Из. ЛГО / Ож. ЛГО). Прогноз расценивался как неблагоприятный если этот показатель был ≤0,5. После введения поправки на срок беременности оказалось, что в 9 случаях коэффициент Из. ЛГО / Ож. ЛГО был меньше 0,5 и дети умерли, в 1 наблюдении он также был менее 0,5, но ребенок выжил, в 3 случаях, при показателе более 0,5, прогнозировали благоприятный прогноз и дети выжили. Случаев, когда коэффициент был более 0,5, но дети умерли, не было выявлено. Таким образом, чувствительность достигла 100%, специфичность - 75%, ложноположительные результаты составили 25%, ложноотрицательных результатов не отмечено.
При анализе показателей в двух группах (расчет ЛГО и расчет Из. ЛГО / Ож. ЛГО) больше всего нас заинтересовали 4 случая, когда мы ошиблись в прогнозе. Было решено повторно провести измерения, используя сохраненную объемную информацию. Во всех 4 случаях были выведены срезы легких на уровне четырехкамерного среза сердца и проведена оценка контралатерального легкого (табл. 3).
Таблица 3. Результаты перерасчета оценки ЛГО и Из. ЛГО / Ож. ЛГО после ретроспективного анализа объемной информации.
| ЛГО | ЛГО после коррекции | Изменение постнатального прогноза по величине ЛГО после корректировки измерений в режиме 3D | Из. ЛГО/ Ож. ЛГО | Из. ЛГО/ Ож. ЛГО после коррекции | Изменение постнатального прогноза по величине Из. ЛГО/ Ож. ЛГО после корректировки измерений в режиме 3D |
|---|---|---|---|---|---|
| 1,73 | 1,54 | - | 0,36 | 0,32 | - |
| 1,68 | 2,41 | - | 0,45 | 0,52 | + |
| 1,62 | 1,69 | - | 0,39 | 0,41 | - |
| 1,77 | 1,59 | - | 0,41 | 0,36 | - |
Во всех 4 случаях новые размеры отличались от первоначальных, но в 3 из них корректировка не изменила прогноз. В 1 наблюдении, по данным откорректированного ЛГО, группа риска не изменилась, а по данным откорректированного показателя Из. ЛГО/ Ож. ЛГО, постнатальный прогноз был пересмотрен. Таким образом, после ретроспективного пересчета данных была получена 100% чувствительность и специфичность, однако при небольшом количестве наблюдений нельзя сделать однозначный вывод об абсолютной надежности такого прогностического критерия при диафрагмальной грыже, как отношение измеренного к ожидаемому ЛГО.
При сравнении изображения в 2D режиме, по которому производились первоначальные измерения, и ультразвукового среза, полученного ретроспективно из сохраненного объема видны ошибки, допущенные при измерениях (рис. 4), и прежде всего отсутствие четкой картины четырехкамерного среза сердца и небольшое увеличение снимка. На этом этапе работы использование новых технологий позволило нам более объективно оценить ранее полученные данные.
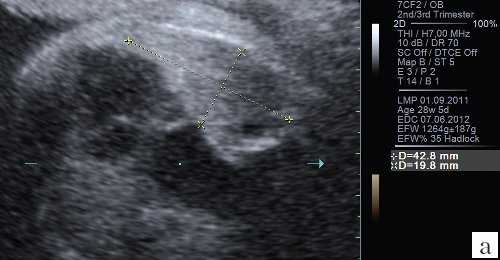
а) Нарушены правила оценки: нет четкого изображения четырехкамерного среза сердца.
Случай пренатальной ультразвуковой диагностики сочетания порока Арнольда-Киари с диафрагмальной грыжей, микрогенией и гипотелоризмом
Отделение пренатальной диагностики родильного дома №1, медико-генетическая консультация, Астана, Казахстан.

Журнал "SonoAce Ultrasound"
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Врожденные пороки центральной нервной системы (ЦНС) достаточно часто диагностируются при ультразвуковом исследовании плода. Точная частота синдрома Арнольда-Киари неизвестна, однако менингомиелоцеле встречается в 1-4 случаях на 1000 рождений, занимая одно из первых мест в структуре аномалий ЦНС [1, 2]. Известны три основных типа этой аномалии: I - проникновение миндалин мозжечка в шейный отдел позвоночного канала; II - вклинение дисплазированного мозжечка в большое затылочное отверстие в сочетании с удлинением ствола мозга; III - изолированное тотальное смещение структур заднего мозга в расширенное затылочное отверстие, сопровождаемое образованием грыжи. В доступной нам литературе мы не нашли описания сочетания порока Арнольда-Киари с диафрагмальной грыжей, микрогенией и гипотелоризмом, за исключением только одного случая сочетания с диафрагмальной грыжей [2]. В связи с этим приводим собственное клиническое наблюдение.
Материал и методы
Пациентка К., 22 лет, проходила скрининговое обследование в сроке 22 недель беременности. Настоящая беременность первая, на учет по беременности взята в 18 недель. Соматический анамнез и наследственность не отягощены.
Ультразвуковое обследование проводилось на сканере SonoAce-9900 (Medison, Южная Корея) с использованием конвексного объемного датчика.
Результаты
При ультразвуковом исследовании в полости матки определялся один живой плод в головном предлежании, показатели фетометрии соответствовали 22 недель беременности. В результате эхографического обследования головного мозга в горизонтальной плоскости обнаружена вентрикуломегалия, отмечено увеличение ширины задних рогов боковых желудочков и отсутствие изображения большой цистерны. Кроме этого, была выявлена ромбовидная структура в области цистерны четверохолмия.
При горизонтальных сканированиях выявлена характерная, заостренная кзади ("ланцетоподобная"), форма задних отделов тела бокового желудочка. Отмечена также асимметрия расположения сосудистых сплетений боковых желудочков, отсутствие изображения прозрачной перегородки (рис. 1). При фронтальных сканированиях через лобные доли у плода выявлено их атипичное изображение, которое проявилось в полном отсутствии изображения латеральных субарахноидальных пространств. При сагиттальном сканировании обнаружено увеличение расстояния между задней поверхностью валика мозолистого тела и верхней поверхностью червя мозжечка (рис. 2).
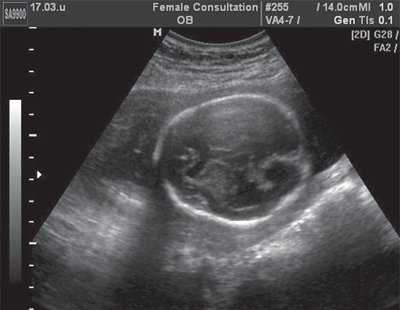
Рис. 1. Поперечное сечение головы плода, горизонтальное сканирование. Изображение прозрачной перегородки отсутствует.
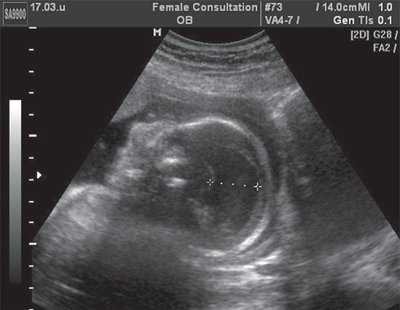
Рис. 2. Сагиттальное сканирование головы плода. Выраженное увеличение высоты тела бокового желудочка.
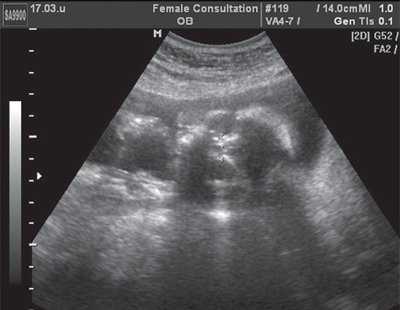
Рис. 3. Эхограмма глазниц плода. Гипотелоризм.
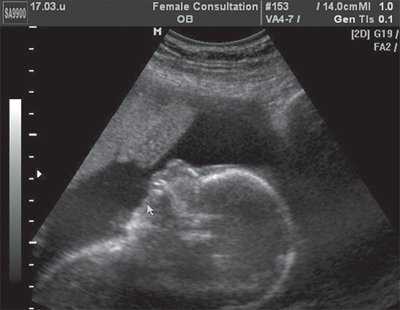
Рис. 4. Эхограмма профиля плода. Микрогения.
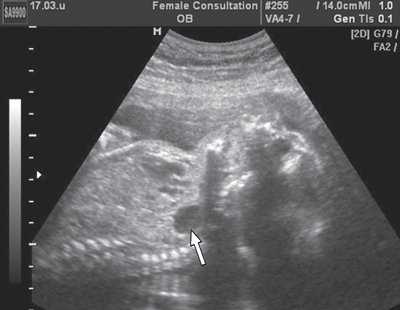
Рис. 5. Эхограмма продольного сечения грудной клетки плода. Стрелкой указан желудок плода, расположенный в его грудной клетке.
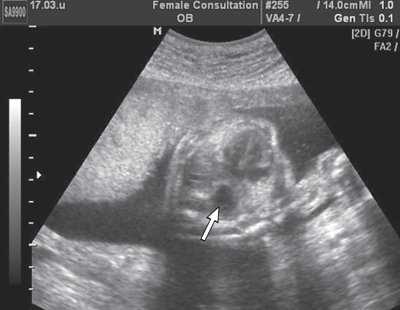
Рис. 6. Эхограмма поперечного сечения грудной клетки плода. Стрелкой указан желудок плода, расположенный в его грудной клетке.
Немаловажное значение для оценки лицевых структур плода и четкой идентификации выявленных изменений имело дополнительное использование трехмерной эхографии [3]. Специфические изменения лица плода были заметны "с первого взгляда". При анализе объемных реконструкций была четко видна гипоплазированная нижняя челюсть и близко расположенные глазные яблоки (гипотелоризм) (рис. 7, 8). Аномалий развития других органов не выявлено.
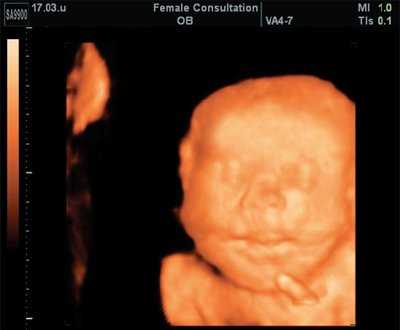
Рис. 7. Гипотелоризм плода в 22 недель беременности (поверхностная реконструкция).
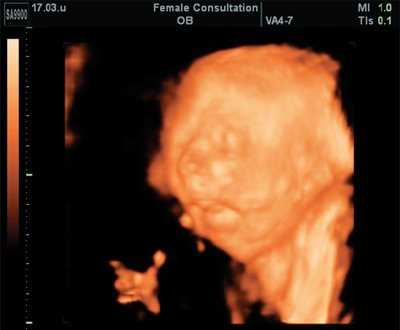
Рис. 8. Микрогения плода в 22 недель беременности (поверхностная реконструкция).
На основании данных эхографического исследования был поставлен диагноз: беременность 22 недели. Множественные пороки развития (сочетание порока Арнольда-Киари II с диафрагмальной грыжей, микрогенией и гипотелоризмом).
От рекомендованного пренатального кариотипирования пациентка отказалась. По желанию женщины, беременность была прервана путем интраамниального введения энзапроста.
При патологоанатомическом исследовании были обнаружены вклинение мозжечка в большое затылочное отверстие, левосторонняя диафрагмальная грыжа, микрогения и гипотелоризм.
Литература
Читайте также:
- Вкусовое восприятие. Обонятельная сенсорная система. Макросматики. Микросматики.
- КТ, МРТ при периневральной кисте дуральной воронки
- Диагностика отдаленного кровоизлияния в мозжечок по КТ, МРТ
- Диагностика беременности. Ранняя диагностика беременности. Поздняя диагностика беременности.
- Темы разговора с девушкой. О чем поговорить?
