УЗИ при раке эндометрия
Добавил пользователь Владимир З. Обновлено: 22.01.2026
Рак шейки матки и матки занимают лидирующие позиции по частоте встречаемости среди всех злокачественных новообразований женских органов репродукции.
Наибольший процент заболеваемости раком шейки матки регистрируется у женщин от 35 до 55 лет. На долю патологии шейки 4 стадии приходится до 50% случаев онкопатологии. Рак шейки у женщин после 65-летнего возраста встречается в 20% случаев.
Рак эндометрия чаще встречается в период менопаузы, но видеть патологию можно в любом возрасте. Видеть онкологический процесс возможно на УЗИ или кольпоскопии. На ультразвуковом аппарате можно визуализировать рак эндометрия, а рак шейки матки только на 3, 4 стадии.
Рак шейки и тела матки
Рак шейки матки представляет собой злокачественное образование, которое поражает цервикс. Рак тела матки, или рак эндометрия, является злокачественным образованием слизистой оболочки матки.
Причины
Среди факторов риска, которые могут провоцировать развитие злокачественного новообразования шейки, выделяют:
- раннюю половую жизнь в возрасте до 16 лет;
- частую смену половых партнеров, в среднем от 2 и более за год;
- раннюю беременность и роды до 16-летнего возраста;
- аборты;
- хронические воспалительные заболевания гениталий;
- бесконтрольный прием КОКов;
- курение;
- изменения иммунного статуса женского организма;
- воздействие химических или радиационных канцерогенов;
- эрозия;
- дисплазия;
- наличие ВПЧ, или вируса папилломы человека.
В основе рака эндометрия находится мутация, что приводит к появлению атипично делящихся клеток.
Среди основных факторов риска рака эндометрия выделяют:
- наследственность;
- гормональный дисбаланс в виде гиперэстрогенэмии;
- раннее менархе до 12 лет;
- позднее наступление климакса в возрасте позже 52 - 55 лет;
- отсутствие родов;
- избыточная масса;
- бесплодие;
- НМЦ, которые сопровождаются ановуляцией;
- СПКЯ;
- гормональная терапия гинекологических или сопутствующих заболеваний;
- эстрогензависимые новообразования;
- гормональная терапия при раке молочной железы;
- хронические воспалительные заболевания репродуктивных органов;
- ослабленный иммунитет;
- курение;
- сахарный диабет;
- гиперплазия эндометрия в анамнезе;
- синдром Линча, или наследственный рак толстой кишки без полипоза.
При наличии в анамнезе гиперпластических процессов выделяют 4 основных типа гиперплазии.
- Простая без атипии.
- Сложная или аденоматозная, без атипии.
- Простая атипическая.
- Сложная или аденоматозная, атипическая.
Простая и сложная атипические формы относятся к предраковым заболеваниям и требуют постоянного медицинского контроля.
При сложной атипической форме гиперплазии риск малигнизации составляет 80%.
Риск при эрозии
Эрозия шейки матки провоцирует малигнизацию при наличии благоприятных условий:
- раннее начало половой жизни;
- беспорядочная половая жизнь;
- отсутствие барьерного метода контрацепции;
- гормональный дисбаланс;
- ослабленный иммунный ответ;
- курение;
- наследственность;
- наличие ВПЧ.
На фоне эрозии наблюдается хронический воспалительный процесс. Отсутствие лечения и длительный промежуток времени без терапии могут провоцировать малигнизацию эрозии.
Видеть эрозивный процесс можно визуально. Для лучшей детализации рекомендовано комплексное обследование в виде кольпоскопии и УЗИ ежегодно.
Классификация
Международная классификация злокачественных новообразований TNM позволяет видеть степень онкологии:
- T представляет собой распространение раковых клеток и размер новообразования;
- N означает степень поражения лимфатических узлов;
- M обозначает метастатическое поражение органов.
Поражение лимфатических сосудов бывает:
- Nx - неизвестно о поражении лимфоузлов;
- N1 - опухоль не обнаружена в близлежащих лимфоузлах;
- N2 - опухолевые клетки имеются в близлежащих лимфоузлах.
Метастазы при раке бывают:
- M0 - метастазы отсутствуют;
- M1 - имеются отдаленные метастазы.
По размерам и распространению атипии рак шейки классифицируется.
- Tis - атипичные клетки определяются на поверхности органа, не проникая глубже.
- T1 - раковые клетки находятся в пределах шейки: T1a — размер не более 7 мм; T1b - размер более 7 мм.
- T2 - опухолевые клетки обнаруживаются за пределами цервикса и матки, без прорастания стенок малого таза и нижней трети влагалища: T2a - опухолевых клеток нет в тканях околоматочного пространства; T2b - поражены ткани околоматочного пространства.
- T3 - прорастание опухолевых клеток в нижнюю треть влагалища, стенки малого таза или мочеточники: T3a - стенки малого таза не поражены; T3b - имеется нарушение проходимости мочеточников.
- T4 - рак выходит за пределы малого таза, может поражаться мочевой пузырь и прямая кишка.
Рак тела матки классифицируется следующим образом.
Tis - преинвазивный рак.
- T1 - рак находится в пределах органа: T1a - инфильтрация опухоли менее ½ от толщины эндометрия; T1b - инфильтрация на ½ толщины эндометрия; T1c - инфильтрация более чем на ½ толщины эндометрия.
- T2 - опухоль находится в пределах органа и переходит на шейку: T2a - в опухолевый процесс вовлечен эндоцервикс; T2b - отмечается инвазия в строму.
- T3 - отмечается местное или региональное прорастание рака: T3a - метастазы в яичники, серозную оболочку; T3b - метастазы отмечаются во влагалище.
- T4 - метастазы рака в прямую кишку или мочевой пузырь.
Симптомы
Начальная стадия рака шейки протекает бессимптомно. Зачастую патология становится находкой по результатам цитологического или кольпоскопического исследований.
Среди характерных для патологии симптомов выделяют:
- Кровянистые выделения из половых путей, не связанные с менструациями. Могут возникать во время полового акта. Связаны с разрушением капилляров.
- Бели.
- Водянистые выделения. Неприятный запах появляется во время распада опухоли.
- Боль. Возникает при сдавливании нервных сплетений в крестцовой области при вовлечении в процесс лимфоузлов и тазовой клетчатки.
При опухоли шейки видеть патологический процесс возможно визуально.
Рак тела матки длительное время протекает бессимптомно. Симптомы, которые должны вызвать подозрение делятся на:
- нарушение менструального цикла;
- бесплодие;
- маточные кровотечения;
- кровянистые выделения из половых путей в климактерическом периоде;
- межменструальные кровянистые выделения;
- лейкорея или выделения водянистого характера;
- гнойные выделения;
- боли внизу живота и поясничной области.
Среди неспецифических симптомов выделяют:
- кахексию;
- слабость;
- общее ухудшение состояния;
- анемию.
Продолжительность жизни
Продолжительность жизни при раке шейки матки зависит от степени, когда было начато лечение и от наличия метастатических поражений. На начальных стадиях выживаемость женщин в течение 5 лет составляет более 80%. На второй стадии выживаемость находится в пределах 60% в течение 5 лет. Третья стадия рака характеризуется снижением выживаемости до 35% за 5 лет. При четвертой стадии прогноз минимален и составляет 10% за 5 лет.
Средняя выживаемость с опухолью находится в пределах 55%.
УЗИ при подозрении на рак
УЗИ при подозрении на рак является одним из основных методов исследования. УЗИ позволяет выявить наличие патологического образования, видеть его размеры и локализацию.
Возможность определения
Возможность определения злокачественного новообразования зависит от стадии патологии. На начальных стадиях при отсутствии жалоб УЗИ менее информативно при раке шейки, чем проведение кольпоскопии и цитологического исследования.
Современное оборудование УЗИ позволяет видеть наличие патологии от 3 мм в диаметре.
Трансвагинальный и абдоминальный способ выполнения
УЗИ при подозрении на рак проводится двумя способами:
Для абдоминального доступа при УЗИ необходимо наполнение мочевого пузыря, а для трансвагинального - мочевой пузырь необходимо опорожнить.
Для более точной диагностики проводится комплексное обследование двумя датчиками УЗИ.
Расшифровка результатов
При подозрении на рак на УЗИ врач может видеть характерные изменения в виде:
- изменения лимфоузлов;
- неровности контура органа, цервикса, полости матки;
- изменения в сосудах;
- изменения в шейке;
- метастатические поражения других органов.
Рак шейки при УЗИ имеет следующие признаки:
- неровные контуры;
- прорастание стенок цервикса;
- бочкообразный вид;
- прорастание соседних органов: мочевого пузыря или прямой кишки;
- бугристость.
Рак тела матки на УЗИ имеет следующие симптомы:
- неровность полости;
- бугристость;
- прорастание стенок органа.
Возможные ошибки
Возможные ошибки при диагностике рака шейки или тела матки методом УЗИ заключаются в сложности видеть патологию на ранних стадиях при маленьком размере опухоли. Кроме того, посредством УЗИ не всегда можно провести дифференциальную диагностику заболеваний.
При УЗИ возможно определение локализации и размеров образования. Для выставления диагноза необходимо проведение дополнительных методов исследования кроме УЗИ.
Альтернативные методы диагностики
Среди альтернативных методов УЗИ-диагностики при раке шейки и тела матки выделяют:
- исследование мазков на онкоцитологию;
- исследование на ИППП, ВПЧ;
- кольпоскопия простая и расширенная, которая позволяет видеть клеточный состав шейки;
- биопсия шейки матки;
- гистероскопия, которая позволяет видеть полость матки.
Исследование проводится комплексное.
Лечение
Лечение рака шейки и тела матки зависит от степени патологического процесса и бывает:
- хирургическим;
- лучевым;
- химиотерапевтическим;
- гормональным.
Чаще терапия комбинированная.
При выявлении у женщины преинвазивного рака шейки матки производится удаление цервикса с сохранением детородной функции. При первой стадии патологии удаляется матка вместе с шейкой. На второй и третьей стадиях производится комплексная химиотерапия и лучевая терапия. При четвертой стадии опухолевого процесса назначается паллиативная химиотерапия. Дополнительно проводится симптоматическая терапия в виде обезболивания.
При раке тела матки основным методом лечения является гистерэктомия. Дополнительно проводится химиотерапия и лучевая терапия.
Операция
Операция при раке шейки или тела матки зависит от стадии патологии, наличия поражения лимфатических сосудов и метастазов в другие органы. При раке шейки матки операция проводится при первой степени патологии, реже - при второй. При этом проводится экстирпация матки с придатками.
При раке тела матки оперативное лечение является основным. При операции производится гистерэктомия матки с придатками, биопсия сальника и лимфоузлов.
Объем операции может включать в себя:
- экстирпацию матки с придатками;
- радикальную экстирпацию матки с придатками и лимфаденэктомией или удалением лимфатических сосудов тазовой и паховой областей;
- радикальная операция с удалением большого сальника.
Онкология при беременности
Онкология при беременности ведется индивидуально для каждой пациентки. При этом учитываются:
- срок гестации;
- степень рака;
- локализация опухоли;
- решение о сохранении беременности.
Лечение рака может начинаться со второго - третьего триместра беременности. При выявлении рака шейки матки ранних стадий проводится наблюдение за женщиной и лечение после родов.
До 12 недель гестационного срока женщине рекомендовано прерывание беременности и проведение необходимого лечения.
При раке шейки матки возможно проведение хирургического лечения в виде конизации или ампутации шейки матки. Родоразрешение при этом осуществляется путем кесарева сечения.
Химиотерапия может проводиться по строгим медицинским показаниям во 2-ом и 3-ем триместрах беременности. Лучевая терапия используется крайне редко из-за негативного влияния на плод.
Значение поликлинического эхографического скрининга в снижении заболеваемости раком эндометрия
Точная и уверенная диагностика. Многофункциональная ультразвуковая система для проведения исследований с экспертной диагностической точностью.
Введение
По данным Я.В. Бохмана [6], пик заболеваемости раком эндометрия приходится на 59 лет и только в 16% случаев он встречается в репродуктивном возрасте [7]. Смертность при раке эндометрия остается высокой и, по сводным данным 69 клиник, пятилетняя выживаемость составляет 66,6% [2]. Определенный практический интерес представляют сведения о 5-летней выживаемости пациенток в зависимости от стадии заболевания. По сводным данным 120 клиник МФГА (1994), при I стадии она составила 76, при II - 59, при III - 29 и при IV - 10% [1].
Ежегодно в мире на 100 000 женщин от рака тела матки умирает 9-10, а в нашей стране 7-8 женщин [8].
В настоящее время установлено, что в большинстве случаев рак эндометрия является вторичным и возникает на фоне предраковых заболеваний. Так, Г.М. Савельева и В.Н. Серов [9] наблюдали переход доброкачественных новообразований эндометрия в рак у 79% женщин, Я.В. Бохман - у 73%, В.Ф. Савинова с соавт. [10] - у 26%. Г.М. Савельева и В.Н. Серов [9] к предраковым заболеваниям относят атипическую гиперплазию, аденоматозные полипы, железисто-кистозную гиперплазию в менопаузе (особенно рецидивирующую) или развившуюся на фоне нейроэндокринных нарушений. Т.В. Харитонова [1] к потенциально злокачественным новообразованиям также относит атипическую гиперплазию и аденоматоз, которые при отсутствии соответствующего лечения, по мнению автора, могут трансформироваться в рак. Другие виды патологии эндометрия переходят в рак крайне редко [9].
Следовательно, представленные данные свидетельствуют, что в большинстве случаев рак тела матки является вторичным и возникает вследствие злокачественной трансформации доброкачественных новообразований эндометрия. Поэтому для его профилактики основное внимание должно быть сосредоточено в первую очередь на диагностике доброкачественных новообразований эндометрия.
Материалы и методы
С целью выяснения возможностей эхографии в снижении заболеваемости раком эндометрия было проведено клиникоультразвуковое исследование в одной из поликлиник Москвы. Обследование осуществляли в течение последних 7 лет. Общая численность прикрепленных к поликлинике женщин составила 14 500 человек. Обследовано 13 088 женщин, у которых проведено более 40 тыс. ультразвуковых исследований. Возраст пациенток варьировал от 16 до 87 лет и составил в среднем 52,8 лет. В репродуктивном возрасте находилось 3582 женщины, в климактерическом - 5283 и в постменопаузальном - 5815.
Исследование осуществляли с помощью ультразвуковых приборов с использованием трансабдоминальных и трансвагинальных датчиков частотой 3,5 и 5 МГц. Обследование женщин репродуктивного возраста осуществляли только в первые 2-3 дня после менструаций, когда эндометрий еще не выражен. Особое внимание обращали на состояние срединного маточного эха (М-эха). За срединное маточное эхо принимали отражения, возникающие от стенок полости матки и эндометрия. При выявлении патологического образования в зоне срединного маточного эха определяли его размеры, локализацию, оценивали характер контуров и внутреннюю структуру. Измеряли также размеры матки и яичников, оценивали их эхоструктуру. Обращали внимание на состояние смежных органов.
Результаты исследований
Патология эндометрия при патоморфологическом исследовании установлена в 304 наблюдениях, однако клинические проявления заболевания отмечены только у 18% из них. Гиперплазия эндометрия имела место у 53 больных (железисто-кистозная - 48 и атипическая - 5), полипы - у 199 (железисто-кистозные - 15, железисто-фиброзные - 180 и аденоматозные - 4) и рак - у 36. При анализе распространенности злокачественного процесса установлено, что IA стадия заболевания констатирована у 10 пациенток, IB стадия - у 24 и II стадия - у 2. В целом, точность ультразвукового выявления патологии эндометрия (специфичность) в наших наблюдениях составила 92,2% и ее отсутствие (чувствительность) - 97,3%. При этом правильность диагностики гиперплазии эндометрия оказалась возможной - в 86,4%, полипов - в 87,9% и рака - в 25%.
Учитывая достаточно высокую информативность эхографии в диагностике патологии эндометрия, естественно, возникает вопрос об эффективности ее применения в профилактике рака эндометрия. Для решения поставленной задачи мы проанализировали результаты эхографии у тех женщин, у которых она либо вообще не применялась, либо с момента ее проведения прошло более 1 года (I группа). Рак тела матки в этой группе установлен у 31 больной. Интенсивный показатель онкологической заболеваемости составил 52,1. Во II группу вошло 5 женщин с раком эндометрия, но у которых с момента проведения ультразвукового исследования прошло менее 1 года. Интенсивный показатель рака эндометрия - 11,9. Следовательно, эти данные свидетельствуют о том, что применение эхографии и проведение соответствующих лечебных мероприятий позволило снизить частоту рака эндометрия в 4,4 раза.
Представленные нами данные свидетельствуют о высокой информативности эхографии в выявлении патологии эндометрия, а также таких доброкачественных ее форм, как гиперплазия и полипы. В то же время определение нозологической принадлежности рака оказалось низким и составило только 25%. Последнее, с нашей точки зрения, в первую очередь обусловлено тем, что в значительном числе случаев (28%) имелась IА стадия заболевания, при которой в связи с частым отсутствием характерных эхографических признаков рак нередко ошибочно принимается в основном за гиперплазию эндометрия. Это, в частности, подтверждают наши исследования, проведенные у стационарных больных, у которых точность определения нозологической принадлежности рака оказалась значительно выше и составила 82,8% [11]. Последнее объясняется тем, что рак поздних стадий у стационарных больных встречался чаще, чем у поликлинических, что значительно облегчало установление его нозологической принадлежности.
Важный аспект эхографического скрининга - более раннее выявление рака эндометрия. Это впервые нами было отмечено при применении трансабдоминальной [12], а затем и трансвагинальной эхографии (таблица). Представленные в таблице данные свидетельствуют, что в условиях эхографического скрининга произошло значительное увеличение частоты диагностики I стадии рака эндометрия и выраженное уменьшение выявления других стадий заболевания.
Таблица. Частота выявления рака эндометрия, %, в условиях поликлинического эхографического скрининга.
| Эхография | Стадия заболевания | |||
|---|---|---|---|---|
| I | II | III | IV | |
| Не применялась | 50 | 32 | 10 | 8 |
| Трансабдоминальная | 75 | 20 | 5 | 0 |
| Трансвагинальная | 95 | 5 | 0 | 0 |
Известно [1, 6, 9, 10], что из всех доброкачественных новообразований эндометрия наибольшей потенциальной способностью к злокачественному перерождению обладают атипическая гиперплазия и аденоматозные полипы. Однако в связи с тем, что в проведенном нами исследовании они наблюдались в относительно небольшом числе случаев (9) и встречались значительно реже, чем рак, то их выявление и своевременное удаление не могло иметь решающего значения в уменьшении частоты возникновения этой патологии. Другой, по-видимому, более важной причиной снижения онкологической заболеваемости было своевременное выявление железисто-кистозной гиперплазии, которая встречается значительно чаще, чем атипическая гиперплазия и аденоматозные полипы.
Определенный практический интерес представляют данные исследования 5 женщин, у которых, несмотря на применение эхографии, был установлен злокачественный процесс.
Наблюдение 1. Больная, 58 лет. Последнее ультразвуковое исследование - норма. Оперирована через 8 мес после ультразвукового исследования в связи с появлением кровяных выделений из половых путей. При патоморфологическом исследовании установлена IА стадия рака эндометрия. Патологический процесс ограничивался поражением только слизистой тела матки.
Наблюдение 2. Больная, 53 года. При первом ультразвуковом исследовании в январе 1996 г. установлен полип эндометрия (железисто-фиброзный) размерами 0,9x1,8x1,8 см, который был удален при гистерографии. Через 1 год (1997/I) - данные эхографии в пределах нормы. Через 3 мес при ультразвуковом исследовании установлено утолщение эндометрия до 6 мм. Высказано предположение о наличии железисто-кистозной гиперплазии эндометрия. При патоморфологическом исследовании установлен рак IБ стадии с инвазией в мышцу матки на глубину 2 мм.
Наблюдение 3. Больная, 49 лет. При ультразвуковом исследовании в июле 1996 г. патологии со стороны эндометрия не обнаружено. Через 5 мес проведено повторное ультразвуковое исследование в связи с жалобами на прекращение менструаций и схваткообразные боли внизу живота. При ультразвуковом исследовании установлено фрагментарное утолщение М-эха до 6 мм, гематоцервикс и гематометра. На операции и при патоморфологическом исследовании установлен рак матки IА стадии.
Наблюдение 4. Больная, 64 года. В мае 1998 г. в связи с однократными кровяными выделениями из половых путей произведено ультразвуковое исследование. При его проведении патологии со стороны эндометрия не обнаружено. Через 1 мес произведено диагностическое выскабливание и надвлагалищная ампутация матки. При патоморфологическом исследовании обнаружена злокачественная опухоль диаметром 2 мм без инвазии в миометрий. Заключительный диагноз: рак матки IА стадии.
Наблюдение 5. Больная, 53 года. При предыдущем исследовании в другой поликлинике медицинского центра патологии о стороны эндометрия не обнаружено. При исследовании, спустя 11 мес, отмечено, что матка имеет нормальные размеры, полость ее фрагментарно расширена до 3 мм. Эндометрий утолщен до 7 мм. Непосредственно к нему в области задней стенки матки примыкает участок повышенной эхогенности с неровными контурами толщиной 0,9 см. Высказано предположение о наличии рака эндометрия с прорастанием задней стенки матки. Патоморфологический диагноз - рак тела матки IБ стадии.
Отрицательные результаты эхографии у этих больных, с нашей точки зрения, могут быть обусловлены следующими причинами: возникновением патологии эндометрия после проведения эхографии; недостаточно высокой разрешающей способностью современной ультразвуковой аппаратуры и невозможностью обнаружить небольшие, а также малоотличающиеся по эхогенности от мышцы матки образования; появлением злокачественного процесса на фоне нормального или атрофического эндометрия. Последнее, по данным Я.В. Бохмана [6], наблюдается у каждой четвертой больной.
Важное практическое значение имеет решение вопроса о том, через какие временные интервалы необходимо проводить ультразвуковое исследование с тем, чтобы до минимума снизить неблагоприятные исходы при рассматриваемой патологии. Результаты проведенного исследования дают основание полагать, что оно должно производиться не реже 1 раза в 1-1,5 года. Это, с одной стороны, позволит своевременно выявлять доброкачественные новообразования и в связи с этим даст возможность избежать их злокачественной трансформации, а с другой - диагностировать рак эндометрия на ранних стадиях в случае его возникновения не на фоне доброкачественных заболеваний, т.е. de novo.
Таким образом, полученные данные свидетельствуют, что эхография представляет собой ценный метод, массовое использование которого в сочетании с проведением соответствующего лечения может способствовать значительному снижению заболеваемости раком тела матки. Для этого необходима четкая организация системы диспансеризации, совершенная аппаратура и достаточный опыт врача.
Литература
- Харитонова Т.В. Рак тела матки // Онкогинекология. - 2000. - Т. 2. - N2. -С. 44-48. Ашрафян Л.А. Стандартизированная диагностика рака эндометрия. / Дисс. . д-ра мед. наук. - М. - 1989. - 278 с.
- Максимова Н.А. Некоторые аспекты ультразвуковой диагностики рака эндометрия // Ультразвуковая диагностика в акушерстве, гинекологии и педиатрии. - 1999. - N3. - С. 196-201.
- Пурде М.К., Хинт Э.К. Заболеваемость раком тела матки в Эст. ССР //Матер. симп. "Карцинома эндометрия". - Тбилиси. - 1988. - С. 13-14.
- Черквиани Т.Л., Чачанидзе Н.И., Робакидзе З.О. и др. Особенности распространения рака тела матки в Грузии за 23 года (1965- 1987) // Матер. симп. "Карцинома эндометрия". - Тбилиси. - 1988. - С. 13-14.
- Бохман Я.В. Лекции по онкологии. - Ташкент: Медицина, 1985.- 304 с.
- Чекалова М.А., Миронова Г.Т., Шолохов В.М., Карпов С.А. Возможности ультразвуковой диагностики в гинекологии // Ультразвуковая диагностика в акушерстве, гинекологии и педиатрии. -1993. -N4. -С. 107-116.
- Черквиани Л.И., Черквиани Т.Л. Состояние и перспективы развития проблемы карциномы эндометрия // Матер. симп. "Карцинома эндометрия". - Тбилиси. - 1988. - С. 3-9.
- Савельева Г.М., Серов В.Н. Предрак эндометрия. М.: Медицина, 1980. -168 с.
- Савинова Т.В. Рак эндометрия начальной стадии //Акуш. и гинек. - 1988. - С. 19-21.
- Демидов В.Н., Гус А.И. Ультразвуковая диагностика гиперпластических и опухолевых процессов эндометрия // Клиническое руководство по ультразвуковой диагностике / Под ред. В.В. Митькова и М.В. Медведева). - М.: Видар, 1997. - С. 120-130.
- Демидов В.Н., Красикова С.П. Рак эндометрия - возможные пути его профилактики //Клинические лекции по ультразвуковой диагностике в акушерстве, гинекологии и неонатологии. - М. - 1991. - С. 66-78.
УЗИ сканер HS70
Цветовое допплеровское картирование в диагностике рака эндометрия
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Рак эндометрия является доcтаточно частой патологией и занимает второе место среди всех злокачественных заболеваний женских половых органов. Статистические данные последних лет свидетельствуют о существенном возрастании заболеваемости раком эндометрия - в нашей стране ежегодное увеличение составляет приблизительно 6% в год [1]. За последние 20 лет заболеваемость раком эндометрия увеличилась в России в 2 раза [2]. Максимальная заболеваемость раком тела матки отмечается в возрасте 50-59 лет [3,4].
В большинстве случаев рак эндометрия является вторичным и возникает на фоне предраковых заболеваний. Г.М. Савельева и В.Н. Серов наблюдали переход доброкачественных неопластических процессов в рак у 79% больных, Я.В. Бохман - у 73% и Т.В. Савинова - у 26% [5,3,6]. К предраковым заболеваниям относят атипическую гиперплазию, аденоматозные полипы, железистокистозную гиперплазию в менопаузе (особенно рецидивирующую) или развившуюся на фоне нейроэндокринных нарушений [3,5,6]. Наиболее частый клинический признак рака эндометрия - аномальные кровяные выделения из половых путей. Несмотря на то, что рак эндометрия требует как можно более раннего проведения терапии, тем не менее от появления первых признаков заболевания до постановки окончательного диагноза проходит приблизительно 6 мес [1].
Стандартным методом дифференциальной диагностики злокачественных и доброкачественных изменений является гистопатологическое исследование ткани, полученной при раздельном диагностическом выскабливании матки с гистероскопическим контролем. Сегодня актуален вопрос изыскания возможностей неинвазивной типизации тканей с помощью цветового допплеровского картирования, энергетического допплера, импульсной допплерометрии. Согласно данным литературы, систематическое использование эхографии способствует более ранней диагностике рака эндометрия, повышению частоты встречаемости рака I стадии на 50% и уменьшению заболеваемости раком III-IV стадий в 1,5 раза [7,8].
По мнению большинства авторов, применение комплексного ультразвукового исследования с анализом кривых скоростей кровотока является высокоинформативным методом неинвазивной диагностики карциномы эндометрия, так как в подавляющем большинстве случаев заболевания отмечаются патологические кривые скоростей кровотока, характерные для сосудистой сети с низким уровнем периферического сопротивления. Индексы резистентности и пульсации позволили доказать отсутствие мышечной оболочки в стенке артериальных сосудов в бассейне неоваскуляризации при злокачественном росте опухоли. Индекс резистентности (RI) при карциноме эндометрия составляет 0,42+0,02, тогда как в норме, при атрофии эндометрия и при простой гиперплазии, эндометриальный кровоток не регистрируется [9,10-14]. Однако ультразвуковых исследований, позволяющих выявить возможности цветовой допплерографии в диагностике рака эндометрия, крайне недостаточно.
Цель работы - изучение возможностей комплексного ультразвукового исследования с использованием цветового допплеровского картирования, энергетического допплера, импульсной допплерометрии в дифференциальной диагностике доброкачественной и злокачественной патологии эндометрия в определении стадии, степени дифференцировки и глубины инвазии опухолевого процесса в миометрий.
Нами обследовано 40 больных в пре- и постменопаузальном периоде с патологией эндометрия. Использован стандартный алгоритм обследования этой группы больных. Диагноз был верифицирован при морфологическом исследовании удаленного препарата. Обнаружено 17 (42,5%) случаев гиперпластических и 23 (57,5%) случая злокачественны nх процессов эндометрия. Средний возраст больных при доброкачественной патологии составил 46,8±8,1 года, при раке эндометрия - 58,5±7 лет. Данные морфологического исследования больных представлены в табл. 1.
| Морфологическая форма | Количество | % |
|---|---|---|
| Гиперпластические процессы | 17 | 42,5 |
| Железисто-кистозная гиперплазия Железисто-фиброзные полипы Атрофический эндометрий Атипическая гиперплазия | 9 4 1 3 | 22,5 10 2,5 7,5 |
| Злокачественная патология | 23 | 57,5 |
| Аденокарцинома Плоскоклеточный рак Аденоакантома Сочетание аденокарциномы и эндометриальной стромальной саркомы | 17 3 2 1 | 42,5 7,5 5 2,5 |
| Итого | 40 | 40 |
У 10 (58,8%) больных с гиперпластическими процессами и у 14 (60,9%) больных с аденокарциномой эндометрия наблюдалась сопутствующая миома матки небольших размеров (5-9 недель беременности). Длительное существование миомы матки (6-10 и более 10 лет) отмечено у всех пациентов с аденокарциномой.
Ультразвуковое исследование в сочетании с цветовым допплеровским картированием, энергетического допплера и импульсной допплерометрии выполнены всем пациентам на современных ультразвуковых аппаратах трансабдоминальным (конвексным датчиком с частотой 3,5 МГц) и трансвагинальным (конвексным датчиком с частотой 6,5 и 7 МГц) доступом. При эхографии оценивали размеры матки, величину, структуру, состояние полости матки и яичников. Допплеровский анализ включал определение: характера кровотока (артериальный или венозный), количества цветовых сигналов от сосудов в каждой опухоли, локализации внутриопухолевого кровотока (центральная или периферическая), наименьшего и среднего индекса резистентности (RImin и RImed) в маточных, аркуатных и опухолевых сосудах, максимальной скорости артериального (VAmax) и венозного кровотока (VVmax).
Для исключения субъективизма в оценке интенсивности внутриопухолевого кровотока нами предложена шкала. В 5-6 стопкадрах регистрировали количество цветовых сигналов от сосудов новообразования:
- "бедный" внутриопухолевый кровоток был представлен единичными цветовыми сигналами от сосудов - не более 5;
- умеренно выраженный - 5-10 цветовых сигналов;
- интенсивный, выраженный кровоток - более 10 цветовых сигналов от сосудов.
Для маточных артерий использовался частотный фильтр 100 и 50 Гц, для аркуатных и внутриопухолевых сосудов при размере "пробного объема" допплеровского луча 4 и 2 мм соответственно.
Результаты и их обсуждение
1 группа - гиперпластические процессы эндометрия (n=17). Клинически доброкачественная патология эндометрия проявлялась нарушениями менструального цикла по типу менометроррагии, анемией I-II степени у 47,1% больных. Их обследование выявило увеличение толщины М-эхо при доброкачественной патологии эндометрия в среднем - 13,8 мм (колебания 6-23 мм). При трансвагинальной эхографии железисто-кистозная гиперплазия определялась как образование повышенной эхогенности, однородной губчатой структуры с множественными точечными анэхогенными включениями и эффектом акустического усиления. При атипической гиперплазии в полости матки обнаруживалась неоднородная гиперэхогенная структура. Полипы отмечались как овальные или округлые гиперэхогенные образования, деформирующие полость матки, с небольшим количеством жидкости. При доброкачественных новообразованиях эндометрия выявлялся четкий и ровный наружный контур М-эхо.
Цветовая допплерография не зарегистрировала внутриопухолевый кровоток у 23,5% больных: при атрофическом эндометрии и в 3 случаях железисто-кистозной гиперплазии. У 76,5% пациенток обнаружен различной интенсивности периферический кровоток со средними значениями индекса резистентности. При железисто-кистозной гиперплазии отмечались единичные цветовые сигналы от сосудов, расположенные по периферии, со средними и высокими значениями индекса резистентности. При фиброзно-железистых полипах визуализировался умеренно выраженный венозный и артериальный периферический кровоток со средними показателями периферического сосудистого сопротивления. При атипической гиперплазии регистрировался интенсивный центральный и периферический внутриопухолевый кровоток со средним уровнем резистентности сосудов.
Минимальный индекс резистентности (RImin) при гиперпластических процессах эндометрия составил 0,56+0,05; максимальная скорость артериального кровотока - 9,3 см/с (колебания 5-13 см/с), максимальная скорость венозного кровотока-5 см/с (колебания 3-5 см/с).
2 группа - злокачественная патология эндометрия (n=23). Злокачественная трансформация эндометрия в большинстве случаев сопровождалась кровянистыми выделениями в постменопаузе, анемией различной степени у 73,9% пациенток.
Определение стадии рака осуществлено согласно Международной классификации рака тела матки (FIGO,1988). Сопоставление стадии и гистотипа представлено в табл. 2.
| Стадия | Аденокарцинома | Другие* | Всего | |
|---|---|---|---|---|
| высоко- дифферен- цированная | умеренно-дифферен- цированная | |||
| Ia | 4 | - | 1 | 5 |
| Ib | 4 | 4 | 4 | 12 |
| Ic | - | - | - | - |
| II | - | 2 | 1 | 3 |
| III | - | 2 | - | 2 |
| IVc | - | 1 | - | 1 |
| Итого: | 8 | 9 | 6 | 23 |
Примечание. * Аденоакантома Ia, Ib стадий - 2 случая, плоскоклеточный рак Ib стадии - 3 случая, сочетание аденокарциномы и эндометриальной стромальной саркомы II стадии - 1 случай.
В нашем исследовании степень дифференцировки опухоли коррелировала со стадией заболевания: высокодифференцированный процесс ограничивался телом матки, при умеренно дифференцированной аденокарциноме отмечены II, III и IV стадии (распространение опухоли за пределы органа). Обследование больных с подозрением на рак эндометрия выявило увеличение толщины М-эхо до 18,1 мм (колебания 7-38 мм). При Ia стадии - толщина М-эхо составила 11,6 мм (колебания 7-20 мм), при Ib стадии - 16,5 мм (колебания 7-38 мм), при II стадии - 31 мм (колебания 27-33 мм), при III стадии-17,5 мм (колебания 16-19 мм), при IV стадии - 29 мм.
Ультразвуковыми признаками злокачественной патологии эндометрия были: неоднородость внутренней структуры образования, более высокая эхогенность по сравнению с миометрием, повышенная звукопроводимость ткани, неровный, "изъеденный" контур, проникающий в миометрий на различную глубину, наличие гипоэхогенного ободка вокруг новообразования.
У 30,4% больных с карциномой эндометрия при трансвагинальной эхографии обнаруживались локальные гиперэхогенные образования неоднородной внутренней структуры с преимущественной инвазией в определенном направлении одной из стенок матки или локализация в области дна либо одного из трубных углов. При морфологическом исследовании выявлена экзофитная форма роста опухоли I стадии. В остальных 69,6% клинических наблюдениях отмечалась эндофитная форма роста с равномерной инвазией в миометрий. У этих больных обнаружены неровные, "изъеденные" контуры опухоли, проникающей в миометрий на различную глубину, стертая граница между новообразованием и миометрием. Некроз опухоли с деформацией полости матки и наличие некоторого количества жидкости выявлены при III и IV стадиях процесса.
Неоваскуляризация эндометрия имела место у 91,3% (21) больных. Из них "бедный" и умеренно выраженный кровоток с низкими цифрами индекса резистентности наблюдался в 13% наблюдений высокодифференцированной аденокарциномы Ia стадии. Такой тип неоваскуляризации отмечен при экзофитной форме роста опухоли.
Интенсивность кровотока зависела от формы роста опухоли: при экзофитной форме отмечен интраопухолевый тип неоваскуляризации, при эндофитной - интенсивный интра- и периопухолевый тип кровотока, богатая васкуляризация миометрия (рис. 1).
Возможности современных ультразвуковых методик в диагностике рака эндометрия
ФГУ Российский научный центр радиологии и хирургических технологий Росмедтехнологии, Санкт-Петербург.
УЗИ сканер HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Согласно мировой статистике, рак тела матки занимает 7-е место среди злокачественных заболеваний. Анализ онкологической ситуации в последнее десятилетие в России свидетельствует о неуклонном росте заболеваемости раком эндометрия, который к 2007 г. занял 2-е место среди всех злокачественных опухолей у женщин. Доля рака тела матки в структуре заболеваемости злокачественными новообразованиями на 100 000 женского населения России в разных регионах колеблется от 4,5 до 22,5. Прослеживается неуклонное возрастание частоты заболеваемости с 9,8 в 1990 г. до 13,9 в 2005 г., что соответствует 3-му месту по величине показателей прироста заболеваемости злокачественными новообразованиями [1]. В настоящее время увеличение числа впервые выявленных случаев рака тела матки не уступает таковому при опухолях молочной железы. В странах третьего мира риск развития рака тела матки в целом ниже, при этом уровень смертности остается высоким. В странах Северной Америки и Европы данное заболевание встречается значительно чаще, являясь наиболее распространенной злокачественной опухолью женской половой системы, и занимает 4-е место среди всех злокачественных новообразований после рака молочной железы, легких и толстой кишки. Заболеваемость раком эндометрия в возрасте от 40 до 54 лет резко повышается, пик заболеваемости приходится на возраст 60-64 года. Частота распространения рака эндометрия и ее динамика в разных странах с учетом влияния миграционных процессов и возраста указывают на специфические особенности заболевания и зависимость его возникновения от комплекса причин эндо- и экзогенной природы [2].
Среди факторов риска развития рака тела матки обращают на себя внимание малое число родов или бесплодие, ожирение, поздняя менопауза, сахарный диабет, преимущественно 2-го типа. В большинстве случаев риск развития рака эндометрия ассоциируется с различными формами гиперплазий эндометрия - 81,3%, дисфункцией на фоне поликистоза яичников - 25%, полипозом эндометрия - 5,3-25%, миомой матки - 1,6-8%. В последнее время отмечается существенное увеличение местнораспространенных форм рака эндометрия, что связано с неэффективными мероприятиями первичной диагностики. Вопросы уточняющей диагностики рака эндометрия являются предметом пристального изучения [3].
В патогенезе заболевания ведущее значение имеет теория избыточной эстрогенной стимуляции эндометрия, сочетающейся с недостаточностью прогестерона. Как полагают, избыточное влияние эстрогенов может приводить к гиперплазии эндометрия, которая способна прогрессировать в атипический вариант и в 20-25% случаев к переходу в аденокарциному. В то же время существующая зависимость между степенью пролиферации эндометрия и концентрацией эстрогенов в крови отмечается до определенного, порогового значения и даже интенсивная пролиферация не во всех случаях сопровождается злокачественной трансформацией эндометрия. Обнаруженная корреляция между содержанием эстрогенов и повреждением ДНК в нормальном и малигнизированном эндометрии заставляет обращать больше внимания на роль молекулярногенетических и морфологических факторов при формировании разных типов рака тела матки. Рак эндометрия характеризуется гетерогенной природой, что проявляется на уровне как факторов риска, так и его патогенеза, чем определяются особенности формирования групп риска при данном заболевании.
В настоящее время для выявления патологии эндометрия в основном используются диагностическое выскабливание полости матки, гистероскопия и аспирационноцитологическое исследование, а также методы лучевой диагностики, среди которых ведущее значение имеет ультразвуковое исследование (УЗИ) 4. При этом отсутствуют единые методически обоснованные эхографические критерии инвазивного роста опухоли. Внедрение в программы интегрированного обследования больных новых ультразвуковых технологий, таких как импульсная допплерометрия, ультразвуковая ангиография и трехмерная реконструкция изображений, позволило существенно повысить эффективность первичной диагностики и мониторинга больных раком эндометрия в процессе специфической терапии [7, 8].
Целью настоящей работы было изучение возможностей комплексного УЗИ с применением цветового допплеровского и энергетического картирования (ЦДК и ЭК), импульсной допплерометрии и трехмерной реконструкции изображений в первичной и уточняющей диагностике рака эндометрия.
Материал и методы
Обследованы 139 пациенток в возрасте от 21 года до 87 лет с подозрением на рак эндометрия в пери- и постменопаузальном периоде. У 34 больных были выявлены гиперпластические процессы эндометрия, у 105 - злокачественные процессы эндометрия. Средний возраст больных с доброкачественной патологией составил 42,6±7,2 года, больных раком эндометрия - 65,4±7 лет. Во всех случаях получена гистологическая верификация диагноза.
Все больные были комплексно обследованы ультразвуковым методом с использованием трансабдоминального (конвексным датчиком 3,5 МГц) и трансвагинального (датчиком 6,5-7 МГц) доступов на современных ультразвуковых аппаратах Logiq S6 (GE, Healthcare) и Accuvix-XQ (Medison) по определенной программе с применением новейших ультразвуковых методик, включающих допплерометрию маточных сосудов, ЦДК и ЭК с трехмерной реконструкцией изображений. При трансабдоминальном исследовании у пациенток с наполненным мочевым пузырем оценивали состояние матки и яичников, определяли объемы тела и шейки матки, ширину М-эхо. При трансвагинальном УЗИ (ТВУЗИ) методами допплерометрии проводили измерение кровотока и индекса резистентности в маточных артериях, оценивали интенсивность внутриопухолевого кровотока. На всех этапах исследования определяли состояние структуры эндо- и миометрия, их взаимоотношение и однородность. При выявлении очаговых изменений определяли их размеры, степень распространенности и взаимоотношение с окружающими органами и структурами, проводили сравнительную оценку толщины маточной стенки в зоне опухоли и вне зоны локализации опухолевого очага. По возможности точно определяли линейные и объемные параметры опухоли, четкость ее контуров, оценивали состояние прилежащей к ней слизистой оболочки. Основным параметром оценки эндометрия остается изменение его толщины [9]. Объем эндометрия также используется для наиболее ранней диагностики заболевания. Его значения более достоверны в дифференциальной диагностике рака и доброкачественных гиперпластических процессов, чем измерения ширины эндометрия. Критериями злокачественного поражения эндометрия являются значения объема эндометрия превышающие 13 см 3 . При этом обеспечиваются 100% чувствительность и 92% предсказуемость положительного теста в диагностике рака эндометрия [10].
Важнейшими характеристиками новообразования эндометрия являлись степень и характер его васкуляризации, которую с целью получения наиболее полного и наглядного представления оценивали в режиме кино-петли. Проводили качественную оценку кровоснабжения по количеству цветовых сигналов от сосудов новообразования: гиповаскулярный, умеренноваскулярный, гиперваскулярный. Нами использовалась технология Multi-Slice View c преобразованием объемных данных в серию последовательных срезов толщиной до 0,5 мм. Целенаправленный выбор определенных сечений из 3D объемных данных позволял выделить оптимальные срезы тела и полости матки и максимально точно оценить их размеры, определить взаимосвязь выявленных изменений с состоянием окружающих органов и тканей. Технология Volume CT View позволяла на основе 3D сканирования оценить контуры и структуру эндометрия, характер его кровоснабжения, а применение опции гистограммы - точно определить индекс васкуляризации [11].
Особое внимание уделяли оценке глубины миометральной инвазии, возможному переходу злокачественного процесса на цервикальный канал и состоянию регионарных лимфатических узлов, что имело решающее значение при определении стадии заболевания и выборе тактики лечения [12].
Результаты и обсуждение
В результате проведенного исследования у 34 пациенток выявлены гиперпластические процессы эндометрия, которые были выделены нами в отдельные нозологические формы, соответствующие рекомендациям ВОЗ. В табл. 1 представлено распределение больных в зависимости от морфогенеза выявленных гиперпластических процессов эндометрия.
| Количество больных | ||
|---|---|---|
| абс. | % | |
| Морфологическая форма гиперпластических процессов эндометрия | 34 | 100 |
| Железисто-кистозная гиперплазия | 19 | 56 |
| Железисто-фиброзные полипы | 5 | 15 |
| Атипическая гиперплазия | 10 | 29 |
Гиперпластические процессы эндометрия проявлялись нарушениями менструального цикла по типу менометроррагии, анемией I-II степени. При доброкачественной патологии эндометрия у 24 (71,4%) пациенток методом УЗИ в режиме серой шкалы определялось увеличение толщины М-эхо в среднем 14,6±3,2 мм. При трансвагинальной эхографии железисто-кистозная гиперплазия определялась как образование повышенной эхогенности, однородной структуры, с множественными точечными гипо- или анэхогенными включениями до 1,5 мм, иногда с эффектом акустического усиления. При атипической гиперплазии в полости матки выявлялась неоднородная гиперэхогенная солидная структура. Полипы определялись как округлые, овальные или продолговатые, в ряде случаев на длинной ножке, гиперэхогенные образования разных размеров, деформирующие полость матки и отчетливо дифференцирующиеся на фоне жидкостного содержимого полости матки. С помощью импульсного допплеровского режима были количественно оценены показатели гемодинамики в маточных артериях, которые составили: МСС - 9,3±2,1 см/с, индекс резистентности - 0,56±0,05 [13].
Методикой цветовой допплерографии внутриопухолевый кровоток при железисто-кистозной гиперплазии регистрировался в виде единичных сигналов от сосудов, расположенных по периферии. При фиброзно-железистых полипах визуализировался умеренно выраженный венозный и артериальный периферический кровоток со средними показателями периферического сосудистого сопротивления. У 2 пациенток с железистой гиперплазией определялась выраженная гиперваскуляризация эндометрия. При атипической гиперплазии регистрировался центральный и периферический внутриопухолевый кровоток умеренной интенсивности. У 5 больных с железисто-кистозной гиперплазией при атрофическом эндометрии кровоток не регистрировался. Характерными признаками доброкачественности новообразования даже при наличии множественных полиповидных разрастаний являлись сохранение формы полости матки, четкое определение наружного контура эндометрия и равномерное распределение сосудов миометрия (рис. 1 и 2).
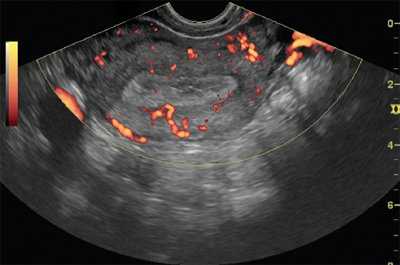
Рис. 1. ТВУЗИ, режим энергетического картирования. Железисто-кистозная гиперплазия эндометрия.
Рак эндометрия (рак тела матки) - симптомы и лечение
Что такое рак эндометрия (рак тела матки)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Ильина Антона Алексеевича, онколога-гинеколога со стажем в 13 лет.
Над статьей доктора Ильина Антона Алексеевича работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Маргарита Тихонова
Определение болезни. Причины заболевания
Рак эндометрия (endometrial cancer) — это злокачественная опухоль, которая развивается из клеток внутреннего слоя матки. Основным симптомом, который появляется уже на начальной стадии болезни, являются кровянистые выделения из половых путей.
Рак эндометрия ещё называют раком тела матки и аденокарциномой эндометрия.
Распространённость
Рак эндометрия — это самая частая злокачественная опухоль женских половых органов. Но если болезнь выявлена своевременно и проведено адекватное лечение, большинство пациенток выздоравливает [1] .
В основном раком эндометрия заболевают женщины в постменопаузе: более 90 % случаев диагностируются после 50 лет. Чаще всего болезнь встречается среди пациенток в возрасте 65-69 лет — заболеваемость среди них составляет 98,1 на 100 тыс. женщин. Средний возраст на момент начала болезни — 63 года. До 49 лет рак эндометрия встречается относительно редко: в 4-5 % от всех случаев [11] .
Факторы риска
Около 5 % случаев рака эндометрия имеют наследственный характер. Злокачественная опухоль эндометрия может развиться при наследственном неполипозном колоректальном раке (синдроме Линча) [12] . Болезнь возникает из-за поломки генов MLH1, MSH2, MSH6 или PMS2. При таких мутациях риск развития рака эндометрия и колоректального рака составляет 24-51 %, рака яичников — 11-15 % [13] .
Помимо генетической предрасположенности, на заболеваемость влияют следующие факторы:
- лишний вес (риск развития рака эндометрия повышается в 1,32 раза); (в 2,54 раза); (в 2,1 раза);
- раннее начало и позднее прекращение менструаций: до 10-12 и после 55 лет (в 2,1 раза); (в 2,9 раза);
- приём Тамоксифена — гормонального препарата для лечения рака молочной железы (в 2,5 раза);
- монотерапия эстрогенами более пяти лет (в 10-30 раз); ;
- лучевая терапия на органы малого таза.
Ожирение является одним из основных факторов риска. Жировая ткань преобразует в эстрогены другие гормоны — андрогены. Если уровень эстрогенов значительно повышен, то риск развития опухолей эндометрия также увеличивается. Получается, чем больше жировой ткани, тем выше вероятность заболеть раком эндометрия.
Тамоксифен — это препарат, который используется при лечении рака груди. В ткани молочной железы он действует как антиэстроген, но в матке механизм действия иной, аналогичный гормону эстрогену. При лечении Тамоксифеном рекомендуется ежегодно наблюдаться у гинеколога.
При синдроме поликистозных яичников значительно повышается уровень андрогенов и эстрогена, а также снижается уровень прогестерона. Изменение соотношения эстрогена и прогестерона является одной из основных причин развития рака эндометрия.
Предшествующая лучевая терапия. Радиация используется для лечения некоторых типов опухолей. При облучении сложно, а иногда невозможно не затронуть смежные органы. Радиация повреждает ДНК здоровых тканей и может приводить к развитию рака в прежде здоровых органах.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы рака эндометрия
Эффективных программ скрининга рака эндометрия пока не существует. Единственный способ обнаружить заболевание на ранней стадии — это ежегодно посещать гинеколога. Также к доктору нужно обратиться, если болит низ живота или появились кровянистые выделения из половых путей между менструациями или в постменопаузе. Кровянистые выделения при раке эндометрия встречаются у 90 % пациенток. Чаще всего выделения слабые или умеренные, их характер зависит от распространения опухоли.
Признаком злокачественной опухоли также может быть изменение характера выделений, даже без примеси крови [2] . Боль, потеря веса и тяжесть в животе появляются уже на поздних стадиях болезни.
Патогенез рака эндометрия
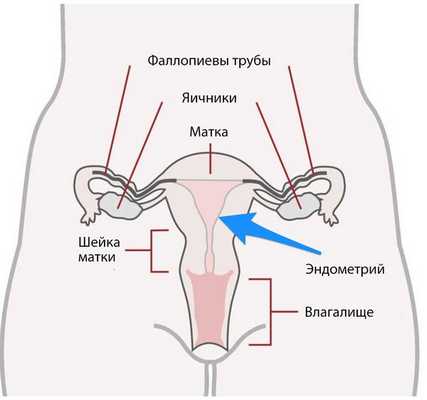
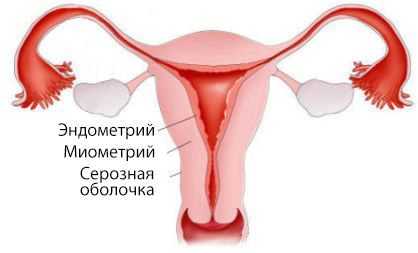
Матка состоит из двух частей: тела и шейки. В теле матки выделяют три слоя:
- наружный — серозная оболочка;
- средний — миометрий, или мышечный слой;
- внутренний — эндометрий, который частично отторгается вместе с кровью при каждой менструации.
Аденокарцинома развивается непосредственно из эндометрия.
В 1963 году была предложена и обоснована теория о двух основных типах аденокарциномы матки. Первый вариант наблюдается у 60-70 % пациенток и протекает с нарушениями углеводного и жирового обмена на фоне избыточного количества эстрогенов [14] [15] . Женщины с этим типом рака страдают маточными кровотечениями, бесплодием, ожирением и сахарным диабетом. У них поздно наступает менопауза и развиваются гиперпластические процессы в эндометрии (качественно-количественное изменение его клеток).
Второй патогенетический вариант болезни встречается у 30-40 % пациенток. У них описанные выше нарушения выражены слабо или отсутствуют [14] [15] . Изменения в эндометрии носят атрофичный характер, развиваются полипы, атипическая гиперплазия и рак.
Отнести заболевание к первому типу можно в следующих случаях:
- присутствует более половины перечисленных признаков;
- симптомы гиперэстрогении (болезненные менструации и маточные кровотечения вне их) сочетаются с обменными нарушениями, например с ожирением и сахарным диабетом.
Согласно другому разделению, к первому типу рака эндометрия относят эндометриоидный рак, ко второму — неэндометриоидный (серозный или светлоклеточный). Они встречаются в 80-90 % и 10-20 % случаев соответственно [3] . Такое разделение связано с различиями в молекулярном профиле опухолей, методах лечения и прогнозе.
Чаще всего раковые опухоли образуются из-за повреждения гена-супрессора PTEN, который подавляет развитие и рост раковых клеток. Данная аномалия встречается у 83 % пациенток с раком эндометрия [4] .
Болезнь также может развиваться при поломке в системе репарации (т. е. исправления) ошибок спаривания нуклеотидов. Эта система отвечает за важный этап нормального деления здоровых клеток. Рак эндометрия первого типа, как правило, связан с мутациями в генах KRAS и CTNNB. Второй тип часто протекает на фоне хромосомной нестабильности, генетических расстройств и мутации в гене р53.
Классификация и стадии развития рака эндометрия
В онкологии существуют две системы TNM, т. е. стадирования рака — FIGO (International Federation of Gynecology and Obstetrics) и AJCC (American Joint Committee on Cancer). Обе системы используют следующие ключевые параметры для описания рака и установки стадии:
- размер опухоли (Tumor);
- наличие или отсутствие опухоли в лимфатических узлах (Node);
- наличие или отсутствие метастазов опухоли (Metastasis) [5] .
Исходя из этих признаков, выделяют четыре основные стадии. Чем меньше стадия, тем лучше прогноз. Рак обычно стадируется дважды. Первый раз — до лечения, такое стадирование называется клиническим. Второй раз — после операции, такое стадирование называется патологоанатомическим и считается более точным и окончательным. Со временем опухоль может расти или распространяться на органы, в которых её раньше не было, а также повторно развиваться после полного излечения. В этом случае стадия, установленная однажды, меняться не будет.
Стадии рака эндометрия по системе TNM
Более схематично стадии рака эндометрия отражены на рисунке:
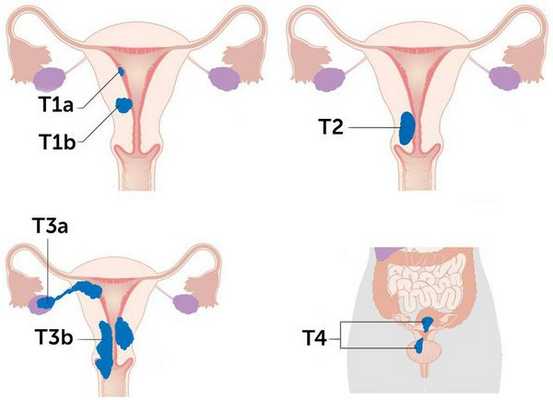
Согласно международной гистологической классификации рака тела матки, выделяют несколько видов опухолей:
- Злокачественные эпителиальные опухоли. В эту группу входят различные виды рака, среди которых эндометриальная аденокарцинома, серозный и светлоклеточный рак.
- Злокачественные смешанные эпителиальные и мезенхимальные опухоли — аденосаркома и карциносаркома.
- Мезенхимальные опухоли — леймиосаркома, эпителиоидная и миксоидная леймиосаркома, эндометриальная стромальная саркома низкой и высокой степени злокачественности.
Лучший прогноз имеет эндометриоидная форма, худший — серозная и светлоклеточная, но основным прогностическим критерием является стадия заболевания. Например, выживаемость с IV стадией эндометриоидного рака ниже, чем с I стадией светлоклеточного.
Рак тела матки также классифицируется на основании вида клеток, из которых он развился. Чтобы установить разновидность рака и его дифференцировку, исследуются удалённые органы или их части. Тип опухоли устанавливает эксперт-патолог, работающий с тканями под микроскопом.
Дифференцировка — это схожесть раковой клетки со здоровой. Она отражает, насколько быстро опухоль может расти и распространяться. Описаны три степени дифференцировки: G1, G2, G3, где G3 — самая неблагоприятная с быстрым ростом опухоли. Сейчас чаще выделяют только два класса: низкой злокачественности (low grade) и высокой (high grade). Low grade включает G1 и G2, a high grade — G3.
Осложнения рака эндометрия
Без специализированного лечения рак эндометрия неизбежно прогрессирует: боль и кровотечение из половых путей усиливаются, мочевой пузырь и прямая кишка сдавливаются, их функции нарушаются. У пациенток учащается мочеиспускание и стул либо, наоборот, возникают запоры.
Если опухоль проросла в мочевой пузырь и кишку, в моче и кале может появиться кровь. Очаги опухоли могут также образоваться в других органах и тканях: печени, лёгких и брюшной полости. При метастазах в лёгких появляется кашель, боль в грудной клетке и одышка; метастазы в печени проявляются болью в правом подреберье [6] .
Диагностика рака эндометрия
В отличие от рака шейки матки для рака эндометрия не существует программ скрининга. Диагноз устанавливается после комплексного обследования, которое включает:
- осмотр на гинекологическом кресле;
- подтверждение наличия опухолевых клеток;
- магнитно-резонансную томографию (МРТ) с контрастированием;
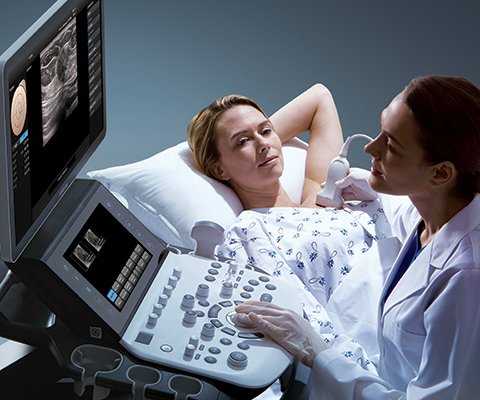
- ультразвуковое исследование (УЗИ);
- компьютерную томографию (КТ).
Осмотр на гинекологическом кресле позволяет оценить, где расположена и насколько распространилась опухоль, а также выявить, поражены ли смежные органы малого таза.
Подтверждение наличия опухолевых клеток, или верификация, — это необходимый компонент обследования. Получить клетки можно двумя способами:
- Пайпель-биопсия — процедура, при которой эндометрий забирается из полости матки с помощью тонкого зонда. Не требует общего наркоза и специальных условий.
- Гистерорезектоскопия — операция, при которой перед забором эндометрия врач может осмотреть полость матки. Гистероскопия предпочтительна при безоперационном лечении, проводится под наркозом и редко занимает более 15 минут. Точность гистероскопии выше, чем пайпель-биопсии, и составляет около 72 % [7] .
Ультразвуковое исследование может быть выполнено через брюшную стенку и интравагинально, т. е. через влагалище. Интравагинальное УЗИ позволяет лучше оценить состояние эндометрия, аномальное утолщение которого может косвенно указывать на онкологическое заболевание. Данная процедура является относительно простой и не требует специальной подготовки, поэтому часто назначается пациенткам на первом этапе диагностики. Правильно интерпретировать результаты УЗИ может только врач-онкогинеколог.
Магнитно-резонансная томография с контрастированием является более точным методом диагностики по сравнению с УЗИ. МРТ назначается при планировании лечения и позволяет определиться с объёмом операции.
Компьютерную томографию (КТ) с контрастированием применяют, чтобы определить, есть ли метастазы в органах грудной клетки и брюшной полости.
Специфических онкомаркеров для диагностики рака эндометрия не существует. Один из немногих маркеров с относительной чувствительностью — Са-125, но такой анализ не входит в стандартное обследование. Этот онкомаркер выявляется при лимфоме, раке яичников, поджелудочной и молочной железы. Также его уровень может повышаться при беременности, различных воспалительных заболеваниях или доброкачественных образованиях, например кистах яичников и миоме матки.
Лечение рака эндометрия
Основной метод лечения рака эндометрия — это операция, при которой удаляются тело и шейка матки с придатками.
Операция может проводиться через три вида доступа:
- лапаротомный (разрез передней брюшной стенки);
- лапароскопический (через проколы 5-10 мм);
- влагалищный.
Чаще всего применяется лапароскопия, так как после неё пациентки быстрее всего восстанавливаются.
Необходимость лимфодиссекции (удаления лимфатических узлов) зависит от наличия факторов риска метастазирования опухоли, результатов морфологического заключения и данных инструментальной диагностики. При удалении лимфатических узлов важно оценить, есть ли в них опухолевые клетки, что имеет решающее значение при планировании лечения после операции.
Чем больше объём операции, тем выше риски послеоперационных осложнений. При удалении лимфоузлов примерно в половине случаев образуются лимфокисты — отграниченные скопления лимфатической жидкости в малом тазу [8] . Чтобы минимизировать риски их развития и избежать лимфодиссекции, в некоторых клиниках используется технология определения сигнальных лимфоузлов (СЛУ). Во время процедуры в шейку матки вводится краситель, который по лимфатическим сосудам попадает в лимфоузлы. Затем хирург находит лимфоузлы, в которых накопился краситель, и удаляет узел, расположенный ближе всего к матке. Далее, непосредственно во время операции, проводится гистологическое исследование, позволяющее подтвердить или исключить наличие метастазов в СЛУ и избежать их полного удаления.
Если женщина планирует беременность, то в некоторых случаях допустимо безоперационное лечение. Оно возможно при эндометриоидном типе рака, стадии IA и высокой дифференцировке. Лечение проводится гормональными препаратами, которые блокируют работу яичников и оказывают терапевтический эффект на опухоль. Применяются два основных препарата: Мегестрола ацетат и Медроксипрогестерон.
Продолжительность гормонального лечения, как правило, составляет 6-12 месяцев. Затем при хорошем эффекте врач может разрешить беременность. После родов зачастую рекомендуется удалить матку, так как опухоль часто развивается повторно.
Лучевая терапия или химиотерапия на первом этапе менее эффективны, чем хирургическое лечение. Они назначаются, если нельзя провести операцию, например при тяжёлых хронических заболеваниях, распространённости опухоли и лечении рецидивов.
Чтобы предотвратить повторное появление опухоли, после операции могут проводиться дистанционное облучение малого таза и брахитерапия (контактная лучевая терапия, при которой источник излучения вводится внутрь поражённого органа).
Метод подбирается врачом в зависимости от типа и стадии рака, состояния лимфатических узлов. Например, при неэндометриоидном раке после операции назначается химиотерапия в сочетании с брахитерапией, а при эндометриальном раке I стадии может быть достаточно брахитерапии или наблюдения.
Прогноз. Профилактика
Без лечения рак эндометрия неизбежно прогрессирует и со временем приводит к гибели пациентки.
Для оценки прогнозов в онкологии используется термин «пятилетняя выживаемость», который сравнивает пациентов с конкретной стадией болезни с людьми из общей популяции. Например, если пятилетняя выживаемость при первой стадии болезни достигает 95 %, то такие пациенты по сравнению со здоровыми людьми с вероятностью 95 % проживут пять лет.
При своевременном выявлении и лечении рак эндометрия имеет самые благоприятные прогнозы среди всех злокачественных опухолей женских половых органов:
- для I стадии пятилетняя выживаемость составляет 85-95 %;
- для II — 65-70 %;
- для III — 29 % [9] .
Стадия болезни является самым значимым фактором при определении прогноза, но далеко не единственным. Онкологи оценивают гистологический тип опухоли, её дифференцировку, размеры, расположение в матке, прорастание или метастазирование в другие органы и лимфатические узлы. Точный прогноз врач сможет дать только после всестороннего анализа этих параметров.
Читайте также:
