УЗИ при тромбозе почечной вены трансплантата почки
Добавил пользователь Дмитрий К. Обновлено: 09.01.2026
Почечная недостаточность — это неспособность почек удалять отходы из крови. Начальные признаки — боли в пояснице или животе, тошнота, рвота, анемия, головные боли. Позже нарушается мочеотделение — полиурия, олигурия или анурия. В моче могут появиться лейкоциты, бактерии, гной, кровь, белок. В крови повышены калий, мочевина и креатинин.
При острой почечной недостаточности резко снижается функция почек. Главные причины ОПН: острое нарушение гемодинамики; резкое снижение почечного кровотока; остро возникшая двусторонняя обструкция мочевыводящих путей; токсическое воздействие, реже - острый воспалительный процесс в почках. Прогноз при ОПН зависит от того, как быстро был восстановлен нормальный почечный кровоток. При ОПН почка может быть нормального размера или увеличена, эхогенность паренхимы часто повышена.
Хроническая почечная недостаточность нарастает медленно и необратимо. Частые причины ХПН: инфекции, диабет, гипертоническая болезнь, сосудистые, врожденные и наследственные болезни, токсическая нефропатия, обструктивная нефропатия. На ранних стадия ХПН протекает без видимых симптомов. Позже появляется недомогание, усталость, пониженный аппетит, тошнота, артериальная гипертензия. В анализах крови повышен калий, мочевина и креатинин. Из-за низкой продукции эритропоэтина больными почками нарастает анемия. При ХПН изначально обе почки увеличены, но позже значительно уменьшаются.
При подозрении на почечную недостаточность с помощью УЗИ нужно оценить размеры и эхоструктуру почек. Подробнее смотри Нормальная почка. Следует искать признаки непроходимости, опухоли, камни, анатомические нарушения, инфекции. Чтобы проверить проходимость почечных сосудов используйте доплер. Подозрительные доплер-сигналы: высокий систолический пик скорости, низкий уровень или отсутствие диастолического потока, турбулентность и tardus-parvus эффект. Подробнее смотри Доплер сосудов почки.
Важно. Высокий риск развития почечной недостаточности при гидронефрозе, остром гломерулонефрите, папиллярном некрозе, стенозе почечной артерии, остром тубулярном некрозе, почечной и других инфекциях.
Острый и хронический гломерулонефрит на УЗИ
Острый гломерулонефрит — это двустороннее воспаление почечных клубочков. Воспаление и склероз клубочков нарушает функции почек и в конечном итоге может привести к почечной недостаточности. Гломерулонефрит возникает как позднее осложнение инфекции глотки. Чаще встречается у детей, чем у взрослых.
Могут быть жалобы на недавнюю температуру, боль в горле и суставах, отеки лица и лодыжек, мутная моча, олигурия, повышенное давление. В крови анемия, высокие мочевина и креатинин. В моче эритроциты, белок, снижение скорости клубочковой фильтрации.
Острый гломерулонефрит часто переходит в хронический гломерулонефрит. Медленно идет необратимый последовательный фиброз клубочков, снижется скорость клубочковой фильтрации, в крови накапливается мочевина и креатинин, наступает интоксикация. Спустя 20-30 лет хронический гломерулонефрит приводит к хронической почечной недостаточности и в конечном итоге к смерти.
Острый гломерулонефрит не имеет никаких специальных узи-признаков. Можно заметить небольшое двустороннее увеличение почек, почечные пирамиды хорошо визуализируются, эхогенность корковой зоны несколько повышена. При хроническом гломерулонефрите на УЗИ небольшие, ровные, гиперэхогенные почки.
Некроз почечных сосочков на УЗИ
Сосочки — это конусовидные верхушки пирамид почек. Они обращены к синусу и состоят из собирательных трубочек нефронов. Строение почки смотри здесь. Частые причины некроза почечных сосочков
- Нарушение кровоснабжения почечного сосочка вследствие отёка, воспаления и склеротических изменений в почке;
- Нарушение оттока мочи — моча скапливается в лоханке, растягивает её и сдавливает почечную ткань;
- Гнойно-воспалительные процессы в мозговом веществе почки;
- Воздействие токсинов на почечную паренхиму;
- Нарушение текучести крови.
Некроз сосочков обычно двусторонний. Существует две формы заболевания: папиллярная и медуллярная форма некроза сосочков пирамид. Пациенты с сахарным диабетом, серповидноклеточной анемией более подвержены некрозу сосочков почечных пирамид. Женщины страдают заболеванием в 5 раз чаще, чем мужчины.
Жалобы при некрозе сосочков неспецифичны: температура, боли в пояснице или животе, высокое давление (от ишемии почек), нарушение мочеиспускания. В ОАМ протеинурия, пиурия, бактериурия, гематурия, низкий удельный вес мочи. У 10% больных с мочой выделяются некротические массы — серые, мягкой консистенции, слоистого строения, нередко содержат комочки солей извести. Это указывает на значительный деструктивный процесс в мозговом веществе почки. Нередко отвалившиеся сосочки закупоривают чашечки или мочеточники, что приводит к непроходимости и развитию гидронефроза.
При своевременном лечении прогноз благоприятный. После отхождения некротических масс раневая поверхность эпителизируется, функции почек восстанавливаются. В почечных пирамидах на месте исчезнувших сосочков формируются округлые или треугольные кисты. Если некротические массы отходят не полностью, то идет их кальцификация, и вокруг почечного синуса в области сосочков появляется гиперэхогенные включения. В некоторых случаях папиллярный некроз может привести к смерти вследствие острой почечной недостаточности.
УЗИ почки трансплантата (лекция на Диагностере)
Статья находится в разработке.
УЗИ трансплантата почки проводили методом УЭСВ, а также использовали стандартные режимы сканирования:
1) серошкальное сканирование: оценка состояния и топометрия трансплантата (размеры трансплантата, толщина коркового слоя, величина чашечно-лоханочной системы и т.д.), оценка состояния околопочечного пространства;
2) цветовое доплеровское картирование скорости и энергии кровотока;
3) спектральное доплеровское исследование.
При пересадке почки методом УЗИ оценивают возможные осложнения в пересаженной почке.
Обычно первое УЗИ проводят через 24-48 часов после трансплантации.
Часто выполняемый с помощью радионуклидной визуализации (йод-131 ортойодогиппурат, Tc-99m MAG3).
Важно знание хирургической техники, отчета об операции часто улучшает интерпретацию исследования.
Трансплантированная почка обычно располагается забрюшинно в подвздошной ямке, чаще справа.
При трансплантации трупной почки основную почечную артерию забирают с прикрепленной частью донорской аорты.
Затем анастомозируется из стороны в сторону к наружной подвздошной артерии реципиента.
Трансплантация живых доноров включает прямой сквозной трансплантат почечной артерии к наружной подвздошной артерии или сквозной анастомоз с внутренней подвздошной артерией.
Основная почечная вена почти всегда пересаживается реципиентной наружной подвздошной вене сквозным образом.
Мочевой дренаж обычно восстанавливается путем имплантации донорского мочеточника в купол мочевого пузыря (уретеронеоцистостомия).
Хотя он также может быть имплантирован в нативный мочеточник или почечную лоханку.
Структурная оценка
Общая структурная оценка включает: эхогенность, кортикомедуллярная дифференциация должна быть сохранена, размер почек.
Увеличение может указывать на отек, который неспецифичен, но изменение размера между исследованиями является признаком основного заболевания.
Хирургические осложнения: Обструктивная уропатия, гидронефроз,проксимальный гидроуретер
Коллекции жидкостей
Характер сбора жидкости после трансплантации не может быть надежно определен только по внешнему виду ультразвука, так как большинство из них безэховые с различными внутренними акустическими характеристиками.
Лучше всего это делать на основе шкалы времени, поскольку разные сборы жидкости имеют тенденцию представлять в разное время в послеоперационном периоде:
сразу после операции: гематома
1-2 недели после операции: уринома
3-4 недели после операции: перинефритический абсцесс
2-й месяц и далее: лимфоцеле
Оценка сосудов
тромбоз почечной вены или стеноз
изменение диастолического кровотока в почечной артерии
тромбоз почечной артерии или стеноз
высокие скорости потока в месте стеноза
пиковая систолическая скорость ≥2 м / с
разница скоростей между пре- и постстенотическими сегментами 2:1
постстенотическое расширение спектра
Форма волны Парвуса и Тардуса дистальнее стеноза
обычно развивается через месяцы или недели
псевдоаневризма: обычно после биопсии или другой почечной пункции
внутрипочечный артериовенозный свищ
Медицинские осложнения
Существует ряд медицинских причин дисфункции или отказа почечного трансплантата:
острый тубулярный некроз
отказ
сверхострый: сразу после операции
острый: 1-3 недели после пересадки
хронический:> 3 месяца после пересадки
лекарственная нефротоксичность
рецидивирующее заболевание, например рецидивирующая IgA нефропатия
пиелонефрит
встречается у 80% получателей в первый год
Ультразвуковое исследование при медицинских осложнениях трансплантата неспецифично и может включать:
повышенный резистивный индекс (RI)> 0,8
очаговый или диффузный паренхиматозный отек
В конечном счете, пациенты с подозреваемыми медицинскими причинами дисфункции трансплантата подвергаются биопсии для окончательного диагноза.
Главная » Методы диагностики заболеваний » Ультразвуковая диагностика »
Дергачев А.И., Котляров П.М., Абдоминальная эхография .Справочник, 2003
« предыдущая
к содержанию
следущая »
Трансплантация почки Ультразвуковое исследование трансплантированной почки
Трансплантированная почка обычно располагается вдоль поверхности подвздошнопоясничной мышцы, ее эхогенность совпадает с эхо- генностью обычной почки. Эхографические признаки отторжения трансплантата включают: патологическое увеличение размеров почки, гидронефроз, паранефральное скопление жидкости, гематомы, абсцессы и экстраренальные накопления мочи. При допплерографии почечного кровотока обычно определяется увеличение сосудистого сопротивления или полное прекращение кровотока в главной почечной артерии, междолевых артериях, дугообразных артериях (для исключения отторжения), почечной вене (для исключения перегиба почечной вены).
Способ диагностики острого отторжения пересаженной почки
Способ диагностики острого отторжения пересаженной почки путем определения в послеоперационном периоде индекса периферического сопротивления сосудистого русла трансплантата при допплеросонографии и, дополнительно, эхосканировании, определяют объем трансплантата, толщину его паренхимы, индекс примамид мозгового вещества,а индекс периферического сопротивления сосудистого русла пересаженной почки определяют по отношению разницы максимального пикового систолического допплеровского частотного сдвига в конце диастолы к максимальному пиковому систолическому допплеровскому частотному сдвигу и при индексе периферического сопротивления сосудистого русла пересаженной почки более 0,79, или объеме почки более 300 см3, или толщине паренхимы более 2 см и индексе пирамид мозгового вещества более 2,1, или толщине паренхимы меньше или равной 2,0 см и индексе пирамид мозгового вещества более 2,8 диагностируют острое отторжение пересаженной почки (Арутюнян С. М. и соавт., 1990).
Тромбоз почечных вен
Тромбоз почечных вен — это острая или хроническая окклюзия венозной сети почек. Проявляется болью в животе и пояснице, макрогематурией, олигоанурией, интоксикационным синдромом. При хроническом течении может протекать моносимптомно со стойким повышением АД. Диагностируется с помощью магнитно-резонансной, компьютерной, селективной почечной флебографии, дуплексного сканирования почечных вен. Консервативная терапия предполагает длительное введение прямых и непрямых антикоагулянтов. При угрозе ТЭЛА интракавально устанавливается сетчатый фильтр. По показаниям выполняется регионарный тромболизис, чрескожная или открытая тромбэктомия, нефрэктомия.
МКБ-10
Общие сведения
Закупорка ренальных вен традиционно рассматривается как казуистически редкое патологическое состояние, которое обычно развивается у больных с нефротическим синдромом, реже — с другими сопутствующими заболеваниями. По мнению современных урологов, информация о низкой (до 5%) частоте венозного ренального тромбоза при нефрологической патологии не соответствует действительности.
По данным последних исследований, хроническая окклюзия почечных вен обнаруживается у трети пациентов, длительное время страдающих протеинурией. Тромбоз чаще бывает односторонним, реже поражает обе почечные вены. Актуальность своевременной диагностики заболевания обусловлена его частым осложнением острой или хронической почечной недостаточностью.
Причины
Венозная окклюзия сосудов почек является полиэтиологической патологией, возникающей при нарушении целостности сосудистого эндотелия, замедлении кровотока, коагуляционном дисбалансе. По наблюдениям специалистов в сфере практической урологии, нефрологии и ангиологии, основными причинами тромботической закупорки одной или обеих почечных вен являются:
- Гиперкоагуляция при нефротическом синдроме. В группу повышенного риска входят пациенты с мембранозной нефропатией, у которых риск тромбирования венозных сосудов достигает 50%, мембранозно-пролиферативным гломерулонефритом, амилоидозом почек, липоидным нефрозом. Тромбозом могут осложняться диабетическая нефропатия, поражения почек при серповидно-клеточной анемии, системной красной волчанке.
- Другие расстройства коагуляции. Вероятность венозного тромбоза почек возрастает при врожденном дефиците противокоагуляционных факторов (антитромбина III, протеинов S и C), мутациях протромбина, лейденовского фактора V. Вторичная гиперкоагуляция с окклюзией вен почек возможна при приеме эстрогенов, оральных контрацептивов, гестозах, ДВС-синдроме, трансплантации почек, обезвоживании.
- Неопластический процесс. Нарушение кровотока в почечных сосудах с последующим тромбозом может наблюдаться при прорастании злокачественных опухолей (преимущественно почечно-клеточной карциномы), внешнем сдавлении нижней полой и ренальных вен увеличенным лимфоузлами, объемными новообразованиями, расположенными в забрюшинном пространстве. Усугубляющим фактором при неоплазиях является гиперкоагуляция.
- Сосудистая патология. В основе тромбообразования лежит повреждение эндотелия при почечных васкулитах, травмах. У некоторых больных тромботический процесс распространяется на ренальные сосуды из яичниковой, нижней полой вены, возникает при сдавлении аневризмой аорты. Иногда тромбоз становится следствием мигрирующего тромбофлебита при миеломе, лимфогранулематозе, аллергии и др.
Патогенез
Пусковым моментом тромбоза почечных вен обычно является увеличение активности коагулирующих факторов в сочетании с угнетением ингибиторов свертывания и фибринолитических агентов. Усилению свертываемости способствуют характерные для нефротического синдрома гипоальбуминемия (критический уровень — менее 25-30 г/л), диспротеинемия, повышение уровня фибриногена, протромбина, тромбоцитов. Отдельными звеньями патогенеза ренального венозного тромбоза становятся замедление почечного кровотока при прорастании сосудов опухолями или сдавлении объемными новообразованиями, повреждение сосудистой стенки вследствие воспалительных процессов, во время травм, операций.
Частичная или полная обтурация просвета вены тромбом вызывает ишемию с обратимой или необратимой деструкцией почечной паренхимы. При благоприятном исходе флеботромбоза наблюдается фибринолиз, асептический аутолиз сгустка, организация тромба с его обызвествлением, петрификацией. При медленном развитии тромботического процесса и постепенном прекращении кровотока зачастую происходит разрастание компенсационных коллатералей.
Симптомы
При одномоментной окклюзии одной или двух почечных вен выявляется клиническая картина острого повреждения почек, характеризующаяся такими признаками, как резкая боль в области поясницы и боковых отделах живота, появление крови при мочеиспускании, уменьшение объема мочи вплоть до анурии. Вследствие накопления в организме продуктов азотистого обмена развиваются симптомы интоксикации — тошнота и рвота, слабость, сонливость, головокружение. Может повышаться температура тела.
При наличии системной гиперкоагуляции наблюдаются проявления тромбоза глубоких вен: боли, отечность и пастозность нижних конечностей, видимое расширение венозных коллатералей. У пожилых пациентов болезнь зачастую протекает в стертой форме, единственным симптомом является стойкая артериальная гипертензия, устойчивая к гипотензивным препаратам.
Осложнения
Выраженный венозный стаз в результате тромбоза может привести к инфаркту и разрыву почки. При повышении концентрации азотистых соединений в крови вследствие интоксикационного поражения головного мозга возникают нарушения психической деятельности: чередование периодов возбуждения и заторможенности, дезориентация, спутанность сознания, бред, галлюцинации. Накопление ионов калия при острой почечной недостаточности провоцирует вялые парезы мышц, брадикардию.
Частым осложнением тромбоза является угнетение иммунитета, сопровождающееся присоединением тяжелых бактериальных и вирусных инфекций со склонностью к генерализации. Задержка мочи и электролитов ведет к внеклеточной гипергидратации, асциту, отеку мозга. В редких случаях отмечаются профузные кровотечения из образовавшихся язв желудочно-кишечного тракта. Нестабильные тромбы могут стать причиной тромбоэмболии легочной артерии.
Диагностика
Постановка диагноза при тромбозе почечных вен зачастую затруднена вследствие полиморфности клинической картины. Подозревать венозную окклюзию необходимо у всех пациентов со стойким ухудшением функций почек невыясненной этиологии, тяжелой степенью нефротического синдрома. Наиболее информативными в диагностическом плане являются следующие исследования:
- УЗИ. УЗДС НПВ и ее ветвей часто используется как стартовый способ диагностики заболевания, при помощи которого можно обнаружить тромбоз вен. При дуплексном сканировании существует риск получения ложноположительных и ложноотрицательных результатов. Во время ультразвукового исследования выявляется изменение контуров мочеточников — характерный признак, который возникает при чрезмерном развитии венозных коллатералей.
- Магнитно-резонансная флебография. МРТ является неинвазивным безопасным методом диагностики, позволяющим получить детальные послойные изображения с достаточным для верификации диагноза увеличением. Проведение магнитно-резонансного исследования показано, если скорость клубочковой фильтрации составляет не менее 30 мл/мин. Преимуществом МРТ является выполнение без введения в организм контрастных веществ.
- КТ флебография. Важные преимущества методики — быстрота проведения, обеспечение хорошей детализации анатомических структур, высокая специфичность, чувствительность, безболезненность. Исследование хорошо выявляет точное место тромбоза. Однако при окклюзии почечных вен КТ флебография применяется с осторожностью из-за нефротоксичности рентгеноконтрастных препаратов, которые необходимы для исследования.
- Селективная почечная флебография. Метод считается наиболее информативным для подтверждения тромбоза. Исследование проводится путем направленного введения рентгеновского контраста через нижнюю полую вену, в результате чего врач получает достаточное заполнение основного ствола и дополнительных ветвей венозных сосудов почек. При катетеризации ренальных вен существует риск развития тромбоэмболии.
Дополнительно проводится клинический анализ мочи, в котором обнаруживают признаки нарушения работы почек — протеинурию, умеренную лейкоцитурию, цилиндрурию, снижение удельного веса, гематурию. В биохимическом анализе крови наблюдается повышение уровней креатинина, мочевины, снижение концентрации ионов калия, натрия, анемия. Для комплексной оценки состояния мочеполовой системы выполняют экскреторную урографию, КТ брюшной полости.
Дифференциальную диагностику проводят с аневризмой почечной вены, опухолью почки, острым и злокачественным гломерулонефритом, хроническим пиелонефритом, нефропатиями при аутоиммунных заболеваниях, системных васкулитах, подагре, остром канальцевым, медуллярным, кортикальным некрозом, артериальным тромбозом, гемолитико-уремическим синдромом, кровоизлияниями в ткани надпочечников. Кроме осмотра врача-нефролога пациенту рекомендованы консультации сосудистого хирурга, гематолога, онколога, онкогематолога, инфекциониста.
Лечение тромбоза почечных вен
Основными врачебными задачами являются терапия основного заболевания, вызвавшего образование тромба, устранение окклюзии, коррекция существующих клинических проявлений. Лечение патологии, осложнившейся тромбозом, проводится по стандартным протоколам для соответствующей нозологической единицы. Для восстановления кровотока в тромбированной почечной вене используются:
- Антикоагулянтные средства. Предпочтительным методом терапии тромбоза является консервативное ведение пациента с применением противосвертывающих препаратов в течение 6-12 месяцев, а при наличии гиперкоагуляционных расстройств — пожизненно. Наиболее эффективны низкомолекулярные гепарины, непрямые антикоагулянты из группы полусинтетических производных кумарина. Фармакотерапия позволяет предотвратить дальнейшее тромбообразование, реканализировать тромбированные венозные сосуды, улучшить функциональные способности почек.
- Операции на почечных сосудах и почках. При остром двухстороннем тромбозе ренальных вен возможно проведение регионарного тромболизиса через ангиографический катетер. Если противокоагулянтная терапия оказывается неэффективной, тромб не удается растворить фибринолитическими средствами, существует угроза тромбоэмболических осложнений, рекомендована супраренальная установка кава-фильтра, чрескожная катетерная либо открытая тромбэктомия. Массивный венозный инфаркт с поражением всей почки служит показанием для нефрэктомии.
Поскольку острое нарушение тока крови в почечных венах зачастую сопровождается развитием почечной недостаточности, с учетом тяжести состояния пациента показана инфузионная терапия для коррекции метаболических расстройств, устранения гемодинамических нарушений. При выраженной ОПН возможно назначение заместительной почечной терапии (гемодиализа, перитонеального диализа, гемофильтрации, гемодиафильтрации). Больным с почечной артериальной гипертензией рекомендованы гипотензивные средства.
Прогноз и профилактика
Вероятность полного выздоровления зависит от тяжести основной патологии, послужившей причиной закупорки почечных вен. Прогноз благоприятный для молодых пациентов, у которых нет необратимых изменений в почках. Длительное течение болезни у людей с интеркуррентными патологиями приводит к стойкому снижению скорости клубочковой фильтрации.
Специфическая профилактика не разработана. Для предотвращения тромбоза вен необходимо проводить своевременную комплексную терапию состояний, которые закономерно осложняются гиперкоагуляцией. Больным нефротическим синдромом профилактическая антикоагулянтная терапия назначается при снижении концентрации альбумина меньше 30,0 г/л.
1. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений (ВТЭО) - 2015.
2. Диагностика тромбозов почечных вен и НПВ у новорожденных/ Ольхова Е. Б., Полякова Е. В., Эмирова Х.М., Румянцева И., Попа А.В., Жукова И.А., Мстиславская С.А.// Радиология - Практика. - 2001 - №3.
3. Опухолевый тромбоз почечных вен и нижней полой вены при нефробластоме у детей: клиника, диагностика, лечение: Автореферат диссертации/ Сухарев А.В. - 2008.
Осложнения трансплантации почки
Осложнения трансплантации почки — это расстройства, этиологически связанные с пересадкой нефротрансплантата. В раннем периоде проявляются гипертермией, олигоанурией, артериальной гипертензией, болью в области трансплантата. Поздние осложнения длительно протекают бессимптомно, в последующем превалируют признаки почечной недостаточности и нарушений в работе других органов. Патология диагностируется с помощью исследований крови и мочи, УЗИ, УЗДГ, МРТ почек, пункционной биопсии. Для лечения применяют иммуносупрессоры, антибиотики, антиагреганты, антикоагулянты, проводят хирургическую ревизию раны, оперативные вмешательства на мочеточниках, нефротрансплантатэктомию.
Выживаемость пациентов, перенесших трансплантацию почки, на протяжении первого послеоперационного года достигает 94-98%, однако развитие осложнений существенно влияет на функциональность пересаженного органа и качество жизни реципиентов. В раннем и позднем посттрансплантационном периоде могут возникать как урологические заболевания, так и повреждения других органов, способные спровоцировать гибель пациента.
По результатам наблюдений, 33,2% смертей после трансплантации почек вызваны кардиальными причинами, из них 11,3% — острым инфарктом миокарда, 17,8% — инфекционными заболеваниями, 11,9% — опухолевым процессом, 6,9% — нарушением мозгового кровообращения, 30,3% — другими факторами. В течение первых 12 месяцев после вмешательства отторгается от 6 до 12% нефротрансплантатов, что требует возобновления заместительной почечной терапии и проведения повторной пересадки. До 36% реципиентов переносят инфекционные заболевания мочевыделительных органов и оппортунистические инфекции.
Несмотря на накопленный опыт и внедрение эффективных стандартов проведения операции, техническая сложность ее выполнения и использование аллотрансплантата повышают риск осложненного течения послеоперационного периода. Специалисты в сфере современной урологии, нефрологии и трансплантологии выделяют следующие группы причин, провоцирующих возникновение осложнений после нефротрансплантации:
- Возраст и состояние здоровья реципиента. Кроме абсолютных противопоказаний, при которых проведение трансплантации в большинстве случаев завершается неблагоприятным исходом, существуют относительные, существенно повышающие вероятность осложнений. В группу риска входят пациенты старше 65-70 лет, а также страдающие рядом сопутствующих заболеваний — активным гепатитом, циррозом печени, СКВ, васкулитом, гемолитико-уремическим синдромом, системными заболеваниями в активной фазе, сахарным диабетом, острыми инфекционными процессами, ХСН IIБ ст.
- Особенности трансплантируемой почки. Осложнения чаще возникают при AB0 и HLA-несовместимости тканей, пресенсибилизации реципиента. Приживление органа ухудшается при длительной (более 24 ч) холодовой ишемии почки, по результатам некоторых наблюдений этот фактор оказывается более значимым, чем гистосовместимость. Функциональность трупной почки зависит от причин смерти донора, электролитных нарушений, степени и длительности гипотонии, других особенностей агонального периода. На течение посттрансплантационного периода также влияет техника забора органа.
- Медицинские факторы. Исход трансплантации зависит от полноты предоперационного обследования реципиента и прижизненного донора, правильности оценки выявленных противопоказаний, проведения предтрансплантационной подготовки при обнаружении гистологической несовместимости тканей. На качество приживления почки оказывают влияние техническая точность пересадки, соблюдение требований асептики и антисептики, профилактика ишемического повреждения органа, качество наблюдения за пациентом, выбор оптимального режима иммуносупрессии (ИСТ).
- Иммунодефицит. Ряд постнефротрансплантационных осложнений связан с медикаментозным угнетением иммунитета реципиента. Назначение иммуносупрессивных препаратов — важное условие профилактики отторжения трансплантата. Однако на фоне иммунодефицита повышается вероятность возникновения ранних и отдаленных инфекционных заболеваний. Кроме того, иммуносупрессия является фактором риска онкогенеза. У части пациентов нарушения гуморального и клеточного иммунитета стимулируют возникновение аллергических и аутоиммунных реакций.
Механизм развития осложнений трансплантации почек зависит от этиологических факторов, спровоцировавших патологическое состояние. Зачастую в основе расстройства лежит иммунное или инфекционное воспаление. В первом случае наблюдается отторжение нефротрансплантата вследствие Т-клеточного ответа или гуморальной реакции типа антиген-антитело. При попадании в рану инфекционных агентов воспалительная деструкция тканей происходит под действием бактериальных эндо- и экзотоксинов.
Ситуация часто усугубляется ишемическими нарушениями, возникшими на фоне расстройств микроциркуляции, артериальной окклюзии, венозного тромбоза. Отдельную роль в патогенезе постнефротрансплантационных осложнений играет иммуносупрессия, снижающая или извращающая нормальную защитную реакцию организма на действие повреждающих факторов. В отдаленные сроки преобладают процессы склерозирования почечной паренхимы.
Классификация
Систематизация вариантов осложнений после трансплантации почки создана с учетом времени возникновения, причин, механизма развития и клинической симптоматики расстройства. Такой подход соответствует принципам своевременной диагностики и адекватной этиопатогенетической терапии постнефротрансплантационных нарушений. Осложнения при нефротрансплантации могут быть ранними, возникшими остро в ходе операции или в первые месяцы после пересадки, и поздними, с постепенным нарастанием симптомов. Различают следующие формы патологии:
Ранние острые нарушения обычно отличаются бурной клинической картиной. Вскоре после трансплантации у пациента возникает ярко выраженный интоксикационный синдром с высокой температурой, ознобом, суставными и мышечными болями, тошнотой, рвотой, кожным зудом, резкой слабостью. При внутреннем кровотечении наблюдается головокружение, бледность кожных покровов, возможна потеря сознания.
У большинства реципиентов о появлении осложнений свидетельствует значительное уменьшение мочеотделения вплоть до его полного прекращения в сочетании с высоким артериальным давлением. В области трансплантированной почки может пальпироваться болезненное уплотнение. Распространенным признаком инфекционного воспаления является наличие обильного раневого отделяемого. При вовлечении в воспалительный процесс брюшины и развитии перитонита возникает резкая боль в брюшной полости, живот становится напряженным, доскообразным, отмечается учащение пульса, резкое падение АД, часто отсутствует стул.
Проявлением поздних осложнений обычно становится прогрессирующее снижение фильтрационной способности почек. Клиническая симптоматика длительное время отсутствует. В последующем пациент начинает предъявлять жалобы на быструю утомляемость, снижение работоспособности. Уменьшается суточный диурез. Утром на лице преимущественно в области век появляются отеки, которые по мере развития почечной недостаточности сохраняются в течение дня и распространяются на другие части тела. Часто повышается артериальное давление.
Возникают и нарастают симптомы уремии — заторможенность, апатичность, бледность и сероватый оттенок кожи, интенсивный кожный зуд, жажда, нарушения сна, низкая температура тела, отсутствие аппетита, тошнота, рвота, диарея. При сочетанном поражении других органов и систем отмечается соответствующая симптоматика. Из-за угнетения иммунитета реципиенты часто болеют ОРВИ, у них развиваются тяжелые длительные бронхиты, пневмонии. Возможны различные формы пиодермий.
Нарушение всасывания кальция приводит к остеопорозу, гиперплазии паращитовидных желез. Из-за недостаточного синтеза эритропоэтинов часто формируется анемия. У пациентов, длительно принимающих иммуносупрессоры, могут диагностироваться онкологические заболевания. При этом преобладают новообразования предположительно вирусного происхождения — плоскоклеточная (сквамозная) и базальноклеточная карциномы, лимфопролиферативная болезнь (преимущественно В-клеточная неходжкинская лимфома), аногенитальные неоплазии, в том числе рак шейки матки, саркома Капоши.
Диагностический поиск при подозрении на осложнение трансплантации почки направлен на уточнение характера расстройства, оценку жизнеспособности и функциональной состоятельности почечного трансплантата, выявление критических органных и метаболических нарушений, угрожающих жизни реципиента. Наиболее информативными методами обследования являются:
- Общий анализ крови. Вероятное развитие острых осложнений подтверждается значительным повышением уровня лейкоцитов, падением содержания тромбоцитов, ускорением СОЭ. В отдаленном периоде часто наблюдается снижение концентрации эритроцитов, гемоглобина, на фоне иммуносупрессии возможно возникновение лейкопении.
- УЗИ почечного трансплантата. Эхография почки является безопасным скрининговым методом, позволяющим выявить изменение размеров пересаженного органа, деструкцию паренхимы, наличие патологических изменений в паранефральном пространстве. Исследование дополняют УЗДГ почечных сосудов для комплексной оценки состояния кровотока.
- Биохимический анализ крови. О нарушении фильтрационной функции клубочков свидетельствует нарастание уровней креатинина, остаточного азота, мочевины, калия. Поражение гломерулярного аппарата подтверждается данными пробы Реберга, нефрологического комплекса. Характерен высокий уровень ЛДГ, С-реактивного белка.
В зависимости от типа осложнения в общем анализе мочи может обнаруживаться повышение или снижение удельной плотности, наличие эритроцитов, лейкоцитов, цилиндров, бактерий. Для исключения отторжения нефротрансплантата рекомендовано проведение расширенного комплексного иммунологического исследования, пункционной биопсии с последующим гистологическим анализом полученного материала. Исследования с введением рентгеновского контраста (экскреторная урография, КТ, МСКТ почек) производятся с осторожностью из-за возможного усугубления клинической ситуации за счет развития контраст-индуцированной нефропатии.
В качестве дополнительных методов может назначаться МРТ для выявления возможных структурных нарушений в тканях трансплантата и нефросцинтиграфия, позволяющая уточнить функциональность пересаженной почки. Для мониторинга состояния пациента в раннем посттрансплантационном периоде оценивают волемический статус (гемогидробаланс, уровень ЦВД), электролитное состояние (уровни калия, натрия, кислотно-щелочного равновесия), коагулограмму, обеспечивают контроль диуреза, суточное мониторирование АД, регулярно выполняют ЭКГ.
Дифференциальную диагностику обычно проводят между различными видами осложнений. При поздних урологических последствиях трансплантации исключают развитие возвратного гломерулонефрита, рецидивирующей волчаночной нефропатии, пиелонефрита, гидронефроза. По назначению врача-нефролога или уролога пациента консультирует трансплантолог, анестезиолог-реаниматолог, абдоминальный хирург, инфекционист, ревматолог, иммунолог, онколог.
Лечение осложнений трансплантации почки
Основными врачебными задачами являются скорейшая коррекция возникших расстройств и поддержание основных жизненных функций реципиента. При отсутствии острых хирургических осложнений лечение обычно представлено комплексной медикаментозной терапией. С учетом выявленных нарушений пациентам, перенесшим трансплантацию почки, назначаются:
- Коррекция иммуносупрессорной терапии. Применение пульс-методов, изменение дозировки ингибиторов кальциневрина, антиметаболитов, глюкокортикоидов, ингибиторов интерлейкинов, биологических антилимфоцитарных агентов, замена одних препаратов другими зачастую позволяет купировать эпизод отторжения. Коррекция назначений также может потребоваться при связи осложнений с принимаемыми иммунодепрессантами.
- Лечение ишемии пересаженной почки. При возникновении сосудистых и тромботических нарушений используются дезагреганты, антикоагулянты, антигипоксанты, цитопротекторы, синтетические простагландины. С их помощью удается эффективно улучшить почечный кровоток, микроциркуляцию, перфузию тканей. Для увеличения кислородной емкости крови может назначаться гипербарическая оксигенация.
- Антибактериальные препараты. Показанием к проведению активной антибиотикотерапии служит наличие инфекционно-воспалительных осложнений. Предпочтительны противобактериальные средства с минимальным риском нефротоксического эффекта — хинолоны, комбинации диаминопиримидинов с синтетическими сульфаниламидами. При лечении оппортунистических инфекций учитывается чувствительность микроорганизмов.
Инфузионная терапия под контролем диуреза проводится при возникновении острых, угрожающих жизни состояний, метаболических расстройств. С учетом клинической картины реципиенту почки могут вливаться коллоидные и кристаллоидные растворы, отдельные электролиты, цельная кровь и ее компоненты. При нарастании признаков почечной недостаточности возобновляется заместительная терапия (гемодиализ, перитонеальный диализ, гемофильтрация, гемодиафильтрация). Лечение заболеваний, спровоцированных трансплантацией почки, осуществляется согласно протоколам для соответствующей патологии.
Оперативные методы лечения требуются при выявлении хирургических осложнений, деструкции мочеточника или почечного трансплантата. Объем вмешательств зависит от особенностей осложнения. Может выполняться ревизия и дренирование раны, ушивание поврежденных сосудов, лапароскопическая марсупиализация лимфоцеле. При повреждении мочеточника возможно проведение эндоскопического рассечения уретероцеле, уретеропластики, уретерокутанеостомии, наложение неоуретероцистоанастомоза. Необратимая деструкция трансплантированной почки служит показанием для нефротрансплантатэктомии с последующим назначением ЗПТ и возможной повторной пересадкой органа.
Возникновение осложнений ощутимо ухудшает показатели выживаемости пациентов, однако своевременное выявление и грамотная коррекция расстройств делают прогноз более благоприятным. Профилактика возможных осложнений начинается с комплексного обследования больного перед операцией для определения всех абсолютных и относительных противопоказаний, оценки гистосовместимости с донором. При предстоящей AB0-несовместимой трансплантации требуется проведение предоперационной десенсибилизации. По показаниям на предтрансплантационном этапе может назначаться превентивная антибиотикотерапия.
С учетом вероятной компрометации заживления раны на фоне иммуносупрессивной терапии важна прецизионная хирургическая техника, повышенное внимание к деталям, строгое соблюдение правил асептики, тщательный гемостаз. После трансплантации ключевую роль играет правильный выбор индукционной и поддерживающей ИСТ, послеоперационный мониторинг состояния реципиента.
2. Инфекции после трансплантации почки (Обзор литературы)/ Кабулбаев К.А.// Нефрология и диализ. - 2009 - Т.11, №4.
3. Инфекционные осложнения раннего послеоперационного периода у пациентов после трансплантации почки/ Барканова О.Н., Перлин Д.В., Шепелева Ю.Б., Реброва Е.В., Ильченко О.В. // Вестник Волгоградского государственного медицинского университета. - 2016.
4. Этиология возбудителей инфекционных осложнений после трансплантации печени и почек и их резистентность к антибиотикам/ Габриэлян Н.И.// Российский медицинский журнал. - 2016.
Доплер сосудов почки (лекция на Диагностере)
Почечные артерии отходят от брюшной аорты чуть ниже верхней брыжеечной артерии — на уровне II поясничного позвонка. Кпереди от почечной артерией располагается почечная вена. В воротах почки оба сосуда находятся кпереди от лоханки.
ППА проходит позади нижней полой вены. ЛПВ проходит через «пинцет» между аортой и верхней брыжеечной артерией. Иногда встречается кольцевидная ЛПВ, тогда одна ветвь располагается впереди, а другая — позади аорты.
Нажимайте на картинки, чтобы увеличить.
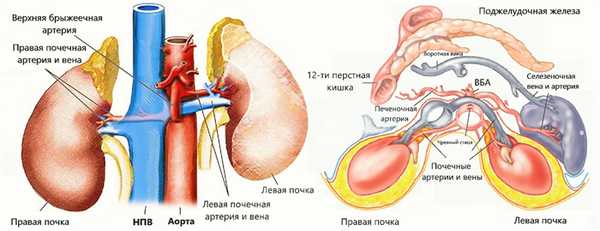
Для исследования сосудов почки используют конвексный датчик 2,5-7 МГц. Положение пациента лежа на спине, датчик располагают в эпигастрии. Оцените аорту от чревного ствола до бифуркации в В-режиме и ЦДК. Проследите ход ППА и ЛПА от аорты до ворот почки.
Рисунок. В режиме ЦДК на продольном (1) и поперечном (2) срезах от аорты отходят ППА и ЛПА. Сосуды направляются к воротам почки. Кпереди от почечной артерии располагается почечная вена (3).
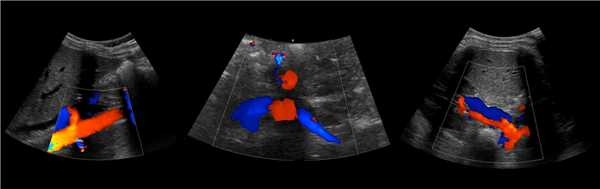
Рисунок. Почечные вены впадают в нижнюю полую вену (1, 2). Аортомезентериальный «пинцет» может сдавливать ЛПВ (3).
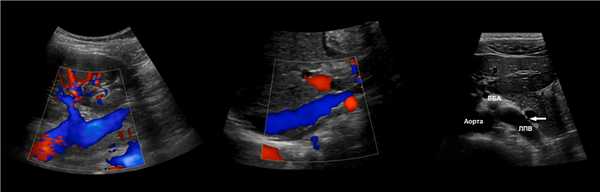
Рисунок. В воротах почки главная почечная артерия делится на пять сегментарных: задняя, верхушечная, верхняя, средняя и нижняя. Сегментарные артерии разделяются на междолевые артерии, которые располагаются между пирамидками почки. Междолевые артерии продолжаются в дугообразные → междольковые → приносящие артериолы клубочков → капиллярные клубочки. Кровь от клубочка отходит по выносящей артериоле в междольковые вены. Междольковые вены продолжаются в дугообразные → междолевые → сегментарные → главную почечную вену → нижнюю полую вену.
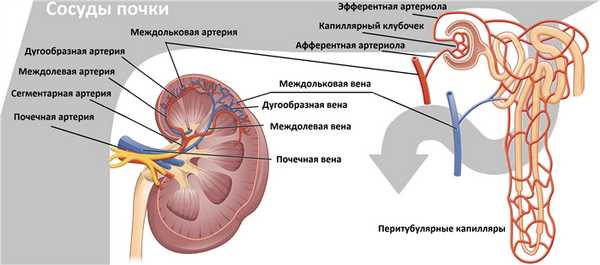
Рисунок. В норме при ЦДК сосуды почек прослеживаются до капсулы (1, 2, 3). Главная почечная артерия входит через ворота почки, добавочные артерии из аорты или подвздошной артерии могут подходить у полюсов (2).
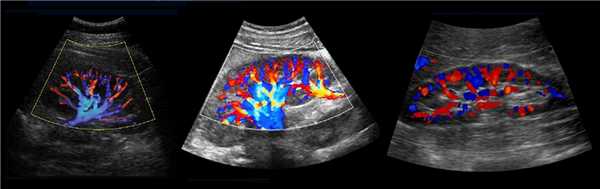
Рисунок. На УЗИ здоровая почка: вдоль основания пирамид (кортикомедуллярный переход) определяются линейные гиперэхогенные структуры с гипоэхогенной дорожкой в центре. Это дугообразные артерии, которые ошибочно расценивать как нефрокальциноз или камни.
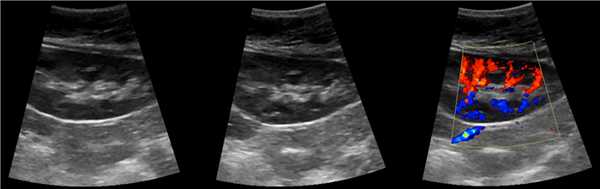
Видео. Дугообразные артерии почки на УЗИ
Доплер сосудов почки в норме
Почечную артерию следует оценивать в семи точках: при выходе из аорты, в проксимальном, среднем и дистальном сегментах, а так же верхушечную, среднюю и нижнюю сегментарные артерии. Оцениваем пиковую систолическую (PSV) и конечно-диастолическую (EDV) скорости кровотока, индекс резистивности (RI), время ускорения (АТ), индекс ускорения (PSV/АТ). Подробнее смотри Доплер сосудов.
Нормальный спектр почечных артерий имеет выраженный систолический пик с антеградным диастолическим потоком на протяжении всего сердечного цикла. У взрослых в норме на главной почечной артерии PSV 100±20 см/сек, EDV — 25-50 см/сек, у детей раннего возраста PSV 40-90 см/сек. В сегментарных артериях PSV падает до 30 см/сек, в междолевых до 25 см/сек, в дуговых до 15 см/сек и междольковых до 10 см/сек. RI в воротах почки
Рисунок. Нормальный спектр почечных артерий — высокий систолический пик, антеградный диастолический поток, низкое периферическое сопротивление — RI в норме
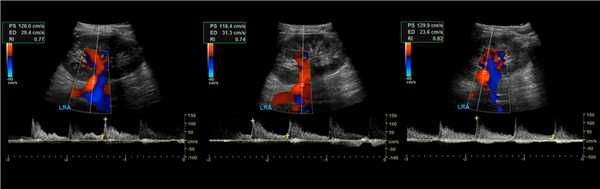
Рисунок. Спектр сосудов почки у новорожденных: почечная артерия — выраженный систолический пик и антеградным диастолический поток (1); высокое сопротивление на внутрипочечных артериях считается нормальным для новорожденных — RI 0,88 (2); почечная вена — поток антеградный с постоянной скоростью на протяжении всего сердечного цикла, минимальные дыхательные колебания (3).
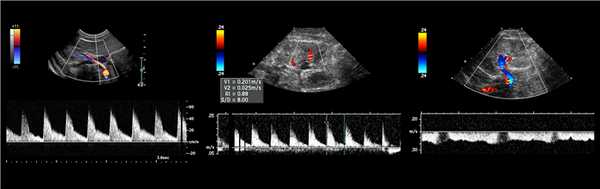
Доплер при стенозе почечной артерии
Стеноз почечной артерии можно встретить при атеросклерозе или фибромышечной дисплазией. При атеросклерозе чаще страдает проксимальный сегмент почечной артерии, а при фибромышечной дисплазии — средний и дистальный сегменты.
Прямые признаки стеноза почечной артерии
Элайзинг указывает место турбулентного высокоскоростного потока, где следует производить измерения. В зоне стеноза PSV >180 см/сек. У молодых на аорте и ее ветвях в норме может быть высокая PSV (>180 см/сек), а у пациентов с сердечной недостаточностью PSV низкая даже в области стеноза. Эти особенности нивелирует почечно-аортальное соотношение RAR (PSV в зоне стеноза/PSV в брюшной аорте). RAR при стенозе почечной артерии >3,5.
Таблица. Критерии стеноза почечной артерии на УЗИ
| Стеноз почечной артерии | PSV в месте стеноза | RAR |
| Норма | ||
| >180 см/сек | ||
| ≥60% | >180 см/сек | ≥3,5 |
| Окклюзия | Нет сигнала | — |
Косвенные признаки стеноза почечных артерий
Прямые критерии является предпочтительными, диагноз не должен быть основан исключительно на косвенных признаках. В постстенотическом отделе поток затухает — tardus-parvus эффект. При стенозе почечной артерии на внутрипочечных артериях PSV слишком поздний (tardus) и слишком маленький (parvus) — АТ >70 мс, PSV/АТ 0,05 и PI >0,12.
| Признаки | Главная почечная артерия | Сегментарные или междолевые артерии |
| Прямые | PSV >180 см/сек, RAR >3,5 | |
| Косвенные | AT >70 мс, AI | |
| Сочетание | PSV в междолевых артериях 5 | |
Рисунок. Пациентка 60-ти лет с рефрактерной артериальной гипертензией. PSV на брюшной аорте 59 см/сек. В проксимальном отделе ППА при ЦДК элайзинг (1), PSV значительно повышен 366 см/сек (2), RAR 6,2. В среднем сегменте ППА при ЦДК элайзинг, PSV 193 см/сек (3), RAR 3,2. На сегментарных артериях без существенного увеличения времени ускорения: верхняя — 47 мс, средняя — 93 мс, нижняя — 33 мс. Заключение: Стеноз в проксимальном отделе правой почечной артерии.
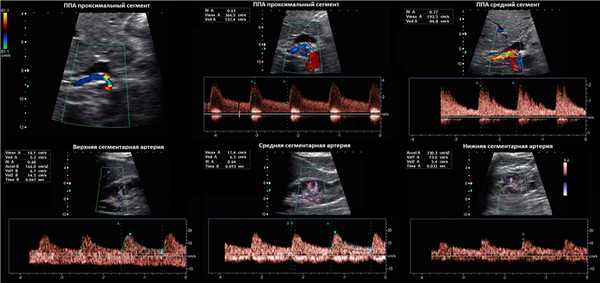
Рисунок. Пациент с острой почечной недостаточностью и рефрактерной артериальной гипертензией. УЗИ брюшной аорты и почечной артерий затруднено из-за газа в кишечнике. На сегментарных артериях слева RI о,68 (1), справа RI 0,52 (2), разница 0,16. Спектр правой сегментарной артерии имеет форму tardus-parvus — время ускорения увеличено, PSV низкий, вершина округлая. Заключение: Косвенные признаки стеноза правой почечной артерии. КТ-ангиография подтвердила диагноз: в устье правой почечной артерии атеросклеротические бляшки с кальцификацией, стеноз умеренной степени.
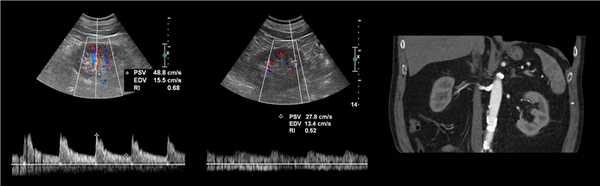
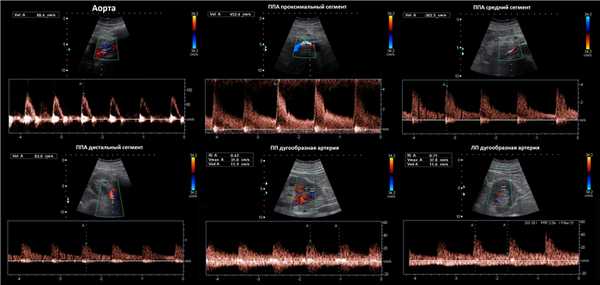
Рисунок. Пациент с артериальной гипертензией. PSV в аорте 88,6 см/сек (1). В проксимальном отделе ППА элайзинг, PSV 452 см/сек, RAR 5,1 (2). В среднем отделе ППА элайзинг, PSV 385 см/сек, RAR 4,3 (3). В дистальном отделе ППА PSV 83 см/сек (4). На внутрипочечных сосудах tardus-parvus эффект не определяется, справа RI 0,62 (5), слева RI 0,71 (6), разница 0,09. Заключение: Стеноз в проксимальном отделе правой почечной артерии.
Доплер почечных вен
Левая почечная вена проходит между аортой и верхней брыжеечной артерией. Аортомезентериальный «пинцет» может сдавливать вену, что ведет к венной почечной гипертензии. В положении стоя «пинцет» сжимается, а в положении лежа — раскрывается. При синдроме Щелкунчика затрудняется отток по левой яичковой вене. Это фактор риска развития левостороннего варикоцеле.
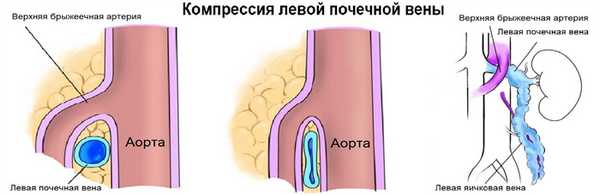
Из-за сдавления спектр ЛПВ похож на воротную вену — спектр выше базовой линии, постоянная низкая скорость, контур плавными волнами. Если соотношение диаметра ЛПВ перед и в зоне сужения более 5 или скорость потока менее 10 см/сек выносим заключение о повышении венозного давления в левой почке.
Задача. На УЗИ левая почечная вена расширена (13 мм), участок между аортой и верхней брыжеечной артерией заужен (1 мм). Кровоток в зоне стеноза с высокой скоростью (320 cм/сек), реверс кровотока в проксимальном сегменте. Заключение: Компрессия левой почечной вены аортомезентериальным «пинцетом» (синдром Щелкунчика).
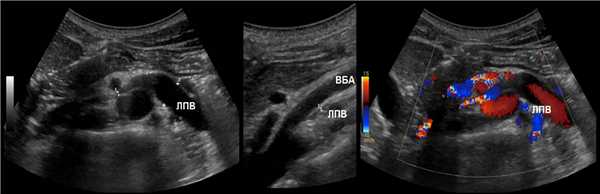
Сдавление почечной вены возможно из-за аномального расположения позади аорты. Соотношение диаметра и скорость потока оценивают по вышеуказанным правилам.
Характер кровотока в правой почечной вене приближается к кавальному. Форма кривой меняется при задержке дыхания может быть более пологой. Скорость кровотока 15-30 см/сек.
Читайте также:
- Техника тотальной панкрэктомии. Методика операции при карциноме поджелудочной железы.
- Характеристика митохондриального наследования. Особенности
- Техника, этапы операции реконструкции латеральной локтевой коллатеральной связки
- Боли в груди при инфаркте миокарда. Характеристика болей при инфаркте миокарда.
- Диагностика, лечение травм, ожогов и обморожений наружного уха
