Влияние менструального цикла на течение ревматоидного артрита и хирургических заболеваний
Добавил пользователь Cypher Обновлено: 09.01.2026
Ревматоидный артрит (РА) является наиболее распространенным заболеванием соединительной ткани. Оно неуклонно прогрессирует, рано приводит к утрате трудоспособности и снижает продолжительность и качество жизни пациентов. В первые 3 года болезни трудоспособность утрачивают 37,5% больных, а через 5 лет более чем 50% больных РА уже не способны продолжать работу.
Возможности улучшения прогноза при РА связаны с применением адекватной иммуноактивной терапии до начала развития деструктивного процесса в суставах. Минимальная продолжительность этого периода времени составляет около 3 месяцев с момента дебюта болезни. Однако на практике почти в половине случаев диагноз РА ставится больным лишь тогда, когда у них выявляются рентгенологические признаки достоверных, а следовательно, уже необратимых, суставных деструкций. Причин несвоевременной постановки диагноза РА на этапе первой врачебной помощи несколько.
Главной является недостаточное знаком-ство докторов общей практики с дифференциальным диагнозом заболеваний суставов. РА и другие ревматические болезни схожи на начальных этапах развития. Современная медицина пока не располагает абсолютным критерием, позволяющим на 100% отличать РА от другой суставной патологии. В связи с этим диагноз РА ставится по совокупности признаков, каждый из которых имеет различную степень достоверности. Для диагностики РА повсеместно применяют предложенные в 1987 году Американской коллегией ревматологов (AКР) классификационные критерии (табл.). Критерии 1—4 должны наблюдаться не менее 6 недель. Диагноз РА устанавливается при наличии не менее 4 критериев. Чувствительность критериев — 91,2%, специфичность — 89,3%. В развернутой стадии болезни эти критерии действительно имеют высокую чувствительность и специфичность (около 90%).
Ранняя диагностика крайне важна
Однако при раннем РА эффективность диагностики гораздо ниже. Например, подкожные ревматоидные узелки редко выявляются на первом году заболевания. Рентгенологические изменения в ранние сроки РА неспецифичны или могут отсутствовать. То же относится и к присутствию у пациентов в крови ревматоидного фактора. Тогда основное значение в постановке диагноза имеет симметричный артрит с вовлечением кисти и запястья, сопровождающийся продолжительной утренней скованностью.
Относительно последнего признака мы хотели бы заострить внимание читателя. Скованность — тугоподвижность суставов, связанная со снижением уровня эндогенных кортикостероидов в утренние часы, а не боль является достоверным диагностическим критерием РА.
По данным зарубежных исследователей, одной из главных причин отсроченной постановки диагноза РА является позднее направление больного к ревматологу. Для уменьшения потери времени на этапе первичного контакта с врачом общей практики и своевременного направления пациента к ревматологу Emery P. и соавт. (2002 г.) предложили критерии «впервые выявленного» РА (см. табл.).
Следующий этап — признаки воспаления
Лабораторные признаки РА — следующий этап алгоритма, это, конечно, признаки воспаления. Однако оценка СОЭ, С-реактивного белка (СРБ), белковых фракций имеет второстепенное значение в диагностическом процессе на ранних этапах. И отсутствие их изменений не должно препятствовать постановке диагноза. В первые 2—3 месяца величины этих параметров не менее чем у 50% больных не выходят за пределы нормы. Кроме того, изменения острофазовых показателей типичны и для других заболеваний суставов.
Тем не менее дебют РА у лиц пожилого возраста (старше 55 лет) сопровождается выраженной клинико-лабораторной активностью болезни — высоким уровнем СОЭ, СРБ, альфа 2 и гамма-глобулинов. В клиническом течении преобладает острое начало с лихорадочным синдромом без четкого продромального периода, стойкий полиартрит, нередко торпидный к терапии. Вышесказанное важно и потому, что эти проявления манифестируют на фоне уже имеющихся других суставных заболеваний, в первую очередь, остеоартроза, что также затрудняет верификацию РА, традиционно считающегося «болезнью молодого возраста». Именно высокие, нетипичные для остеоартроза, показатели СОЭ и уровня острофазовых белков должны навести врача на мысль о дебюте РА у пожилого больного.
Большее значение имеет обнаружение в крови ревматоидного фактора (РФ) в диагностических титрах. Однако примерно у 20% больных РА РФ в сыворотке крови отсутствует. Кроме того, РФ обнаруживают примерно у 5% здоровых людей, у 5—25% лиц пожилого возраста, а также у значительного числа больных с хроническими заболеваниями (системной красной волчанкой, системной склеродермией и др.).
Иммунологический тест улучшил диагностику
Указанных ограничений лишен недавно внедренный в клиническую практику новый иммунологический тест — определение антител к циклическому цитруллинированному пептиду (анти-ЦЦП-АТ), что повысило эффективность лабораторной диагностики РА на ранних стадиях. У больных с РА было выявлено несколько аутоантител, направленных против белков, содержащих цитруллин. Первым таким аутоантителом был антиперинуклеарный фактор. Специфичность анти-ЦЦП-АТ при диагностике РА на ранних стадиях составляет 86%, комбинации анти-ЦЦП-АТ + СОЭ — 95%, анти-ЦЦП-АТ + РФ — 91%, анти-ЦЦП-АТ + СРБ — 97%, анти-ЦЦП-АТ + полиартрикулярная боль — 95%, анти-ЦЦП-АТ + утренняя скованность — 99%. Особенно диагностически значимо определение анти-ЦЦП-АТ у лиц с низкими титрами ревматоидного фактора.
Рентгенография суставов — достоверный, но на ранних стадиях заболевания имеющий низкую диагностическую ценность, метод исследования. Околосуставной остеопороз как признак первой рентгенологической стадии РА развивается как минимум в течение нескольких недель. А костные эрозии и узуры — наиболее важный симптом РА — являются поздним признаком и могут обнаруживаться лишь спустя много месяцев. Тем не менее рентгенография суставов обязательна при любом подозрении на РА.
В первую очередь выполняется снимок кистей вне зависимости от степени субъективных и объективных признаков их поражения. Эрозии и сужение суставной щели проксимальных межфаланговых суставов обеих кистей рук наиболее типичны для РА. Они могут прогрессировать субклинически и, следовательно, их обнаружение дополняет картину даже при нерезко выраженных признаках воспаления. Рентгенологические изменения в крупных суставах считаются менее специфичными для РА. Тем не менее, особенно при серонегативных формах болезни, исследование костей таза может быть диагностически значимым.
На ранних стадиях РА наиболее чувствительным методом для выявления диагностически значимых изменений в суставах является МРТ. Этот метод позволяет обнаружить изменения в мягких тканях. Более доступным для клинической практики является метод допплеровского ультразвукового исследования суставов, который, как и МРТ, обладает большей, по сравнению с рентгенографией, чувствительностью в выявлении характерных для РА изменений в суставах. В первые месяцы заболевания, помимо визуализации синовита и тендовагинита, большое значение для постановки диагноза имеет обнаружение паннуса, который выглядит как гроздевидное утолщение синовиальной оболочки до 4—6 мм с усиленной васкуляризацией. На поздних стадиях толщина паннуса может достигать 10—12 мм, при этом выраженность его васкуляризации значительно варьирует. Этот метод имеет преимущества при исследовании плечевых и тазобедренных суставов, хуже доступных для физикального обследования. При других распространенных заболеваниях суставов (реактивных артритах, остеоартрозе) паннус не образуется. Напротив, в суставах характерен синдром «минус ткань», когда визуализация фиксирует разрушение хряща, расширение суставной щели и дефекты костной ткани без наличия пролиферирующей синовии.
Итак, дебют РА возможен как в молодом, так и в пожилом возрасте. В последнем случае болезнь имеет более агрессивный и прогностически менее благоприятный характер. Как мы показали выше, «классические» критерии диагностики РА на ранних стадиях имеют существенные дополнения. Оценка уровня антицитруллиновых антител, подключение ультразвукового и МРТ-исследования суставов расширяют возможности ранней диагностики этого тяжелого и социально значимого заболевания.
Диагностика ревматоидного артрита на ранних стадиях представляет самостоятельную клиническую проблему, которая является ключевой для своевременного назначения препаратов, предотвращающих прогрессирование болезни.
Перспективы улучшения прогноза при ревматоидном артрите связаны с применением адекватной иммуноактивной терапии до начала развития деструктивного процесса в суставах.
Экстрагенитальная патология в акушерстве: Ревматоидный артрит
Ревматоидный артрит (РА) - хроническое системное соединительнотканное заболевание с прогрессирующим поражением преимущественно периферических (синовиальных) суставов по типу эрозивно-деструктивного полиартрита с быстрым развитием функциональных нарушений в них.
Этиология и патогенез РА.
Этиология РА не установлена, существует множество факторов, которые могут расцениваться как предрасполагающие к РА: половой, возрастной, семейный, эндокринные, метаболические, социально-экономические, инфекционные (стрептококки группы В, микоплазмы и особенно вирус Эпштейна-Барр). В развитии болезни важное значение имеет и генетическая предрасположенность к РА, обусловливающая повышенную частоту заболевания среди родственников больных.
Основой патогенеза РА является нарушение гуморального иммунитета -гиперпродукция аутоантител к различным типам коллагена, в том числе и к тем, которые обнаруживаются в хряще. Особое значение при этом придается наличию ревматоидных факторов, являющихся антителами к Fc-фрагментам IgG, поскольку с их наличием связывается тканевое повреждение при РА.
Наиболее изучены механизмы основного проявления РА - синовита. Гипотетический этиологический фактор повреждает клетки синовиальной оболочки сустава, что приводит к развитию клеточной пролиферации, паннуса, костных эрозий и характерных клинических признаков хронического прогрессирующего артрита.
Патогенез большинства внесуставных (системных) проявлений РА связан с развитием иммунокомплексного васкулита, а также, возможно, с непосредственным повреждением тканей сенсибилизированными лимфоцитами или аутоантителами.
Основу клинической картины РА составляет суставной синдром. Ревматоидный процесс локализуется преимущественно в периферических суставах в виде симметричных артритов конечностей и часто сопровождается поражением околосуставных тканей (связок, сумок и капсулы сустава, сухожилий и мышц). Суставной процесс носит рецидивирующий и прогрессирующий характер. С каждым последующим обострением в процесс вовлекаются новые суставы, вследствие чего один сустав находится в более ранней, а другой - в более поздней стадии поражения. При РА могут поражаться и внутренние органы (легкие, сердце, сосуды, почки, нервная система), а также глаза, кожа и др.
В диагностике РА широкое распространение получили критерии Американской ревматологической ассоциации (пересмотр 1987г.), включающие 7 признаков:
1) утренняя скованность в течение 1 час. в последние 6 нед.;
2) припухлость 3 и более суставов в течение 6 нед.;
3) припухлость запястий, пястно-фаланговых и проксимальных межфаланговых суставов в течение 6 нед. и более;
4) симметричность припухания суставов;
5) наличие подкожных ревматоидных узелков;
6) обнаружение ревматоидного фактора в сыворотке крови;
7) типичные рентгенологические изменения суставов кистей (эрозии, околосуставной остеопороз).
Наличие по крайней мере четырех из семи критериев позволяет диагностировать РА.
Влияние беременности на ревматоидный артрит
Изучение влияния беременности на РА позволило установить, что беременность у больных РА способствует развитию ремиссии заболевания, которая встречается в 54-95% случаев (в среднем у 77% больных). Клиническое улучшение отмечается уже в течение первых трех месяцев беременности и на протяжении всего гестационного периода. При этом уменьшаются не только явления артритов, боль и скованность в суставах, но и улучшаются другие клинические параметры, отражающие активность заболевания. Улучшение течения заболевания при береременности связывают как с изменением иммунологического статуса, так и с гормональной перестройкой (образованием ряда специфических связанных с беременностью факторов, повышением уровней различных гормонов) в организме беременной.
Отсутствие ремиссии и ухудшение течения РА в гестационном периоде можно ожидать у больных тяжелым вариантом заболевания с выраженными системными проявлениями болезни (поражением легких, почек, сердца и др.). С окончанием беременности у 80% больных в течение первых 3 месяцев наблюдается рецидив РА по активности аналогичный таковому до гестации. Подобная тенденция изменения активности РА прослеживается и при последующих беременностях больной.
Влияние ревматоидного артрита на беременность и плод
У больных РА часто развивается субфертильность, что объясняют, главным образом, самим заболеванием.
Причиной осложненного течения беременности может быть высокая активность РА в течение гестации, потребовавшая “агрессивной” терапии, которая, в свою очередь, может оказывать негативное влияние на развитие гестации и родов. Неблагоприятные исходы беременности могут наблюдаться и у больных РА серопозитивных по антифосфолипидным антителам и/или Ro/Lа-антителам, с которыми (как ранее указывалось) связано формирование вторичного антифосфолипидного синдрома и синдрома Шегрена. Осложнения гестации при этом аналогичны расмотренным у беременных с СКВ (см. выше).
Несомненно однако, что при отсутствии активности РА в течение беременности случаи срочных неосложненных родов с рождением здорового доношенного ребенка часты.
Акушерская и терапевтическая тактика
1. Беременность у женщин больных РА возможна при низкой активности заболевания.
2. Противопоказаниями для беременности при РА являются высокая активность заболевания с системными поражениями (почек, легких, сердца и признаками их функциональной недостаточности), амилоидоз почек. Относительным противопоказанием является асептический некроз головок бедренных костей.
3. Диспансерное наблюдение предусматривает выделение в группу риска беременных с РА и сопутствующим АФС, а также с синдромом Шегрена (последних - из-за повышенного риска неонатальных осложнений). Осмотр беременной с РА ревматологом проводится не реже одного раза в каждом триместре, после родоразрешения и через 2-3 месяца после родоразрешения.
4. При стойкой ремиссии заболевания в период беременености возможно уменьшение дозы принимаемых лекарственных препаратов и их временная отмена до окончания гестации.
5. Сроки госпитализации в родильный дом определяются совместно акушером и терапевтом (ревматологом).
6. Показанием для родоразрешения кесаревым сечением может быть наличие поражения тазобедренных суставов с нарушением их функции.
7. Методом выбора контрацепции у больной РА может быть применение оральных контрацептивов, благодаря установленному факту, что применение женщинами противозачаточных гормональных средств снижает заболеваемость РА в 2 раза, а у больной РА способствует ремиссии заболевания. Для предупреждения беременности возможно использование и механических барьерных, и внутриматочных средств.
СПИСОК ЛИТЕРАТУРЫ
1. Насонов Е.Л. Противовоспалительная терапия ревматических болезней.— М.: М-СИТИ, 1996; 345 стр.
2. Насонов Е.Л., Чичасова Н.В. / / Ревматоидный артрит: терапевтические перспективы.— Врач, 1999; 5:7—10.
3. Решетняк Д.В., Насонов Е.Л. //Новые направления лечения ревматоидного артрита: механизмы действия и клиническая эффективность лефлюномида.— Научно-практическая ревматология, 2001; 5:39-45.
4. Сигидин Я.А., Лукина Г.В. //Ревматоидный артрит— М.; АНКО, 2001; стр.328.
5. Чичасова Н.В., Насонова М.Б., Степанец О.В., Насонов Е.Л. //Современные подходы к оценке активности ревматоидного артрита.— Терапевт. Архив, 2002; 5: 57-60.
6. American College of Rheumatology Ad Hoc Committee on Clinical Guidelines. Guidelines for the management of rheumatoid arthritis. Arthritis Rheum., 1996; 39:713—722.
7. American College of Rheumatology Subcommittee on Rheumatoid Arthritis Guidelines. Guidelines for the Management of Rheumatoid Arthritis. 2002 Update. Arthritis Rheum., 2002; 46:328—346.
8. Amrett F.C., Edworth S.M., Bloch D.A„ et al. The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis
9. Breedveld F.C., Dayer J-M. Leflunomide: mode of action in the treatment of rheumatoid arthritis. Ann. Rheum. Dis., 2000; 59:841-849.
10. Dinarello C.A., Moldawer L.L. Proinflammatory and antiinflammtory cytokines т rheumatoid arthritis. A primer for clinicians. 2 nd ed., 2000; Amgen Inc.282 pp.
11. Emery P., Breedveld F.C., Dougados М., Kalden J.R., Schiff M.H., Smolen J.S. Early ref feral recommendation for newly diagnosed rheumatoid arthritis: evidence based development of a clinical guide. Ann. Rheum. Dis., 2002; 61: 290-297.
12. Emery P, Foster W., Suarez-Almazor M. Rheumatoid arthritis, evidence, com /.
13. Feldman М., Brennan F., Maini R.N. Role of cytokines in rheumatoid arthritis. Annu.Rev.Immunol, 1996; 14:397—440.
14. Felson D.T., Anderson J.J., Boers М., et al. American College of Rheumatology preliminary definition of improvement in rheumatoid arthritis. Arthritis Rheum., 1993; 36:729-740.
15. Felson DT, Anderson J.J, Meenan R.F. Use of short-term efficacy /toxicity trade offs to select second-line drugs in rheumatoid arthritis. A metaanalysis of published clinical trials. Arthritis Rheum., 1992;35:1117-25.
16. Fries J.F., Spitz P.W., Young D.Y. The dimensions of health outcomes: the Health Assesment Questionnaire, Disability Pain Scale. J. Rheumatol., 1982; 9:789-793.
17. Harris E, D. Jr. Rheumatoid Arthritis: pathophysiology and implications for therapy. N. Engl. J. Med., 1990; 322:1277-1289.
18. O'Dell J.R. Treating rheumatoid arthritis early: a window of opportunity? Arthritis Rheum., 2002; 46: 283—285.
19. Management of Early Rheumatoid Arthritis. A National Clinical Guideline. Scotish Intercollegiate Guidelines Network.
20. Maetzel A., Wong A., Strand V., et al. Me analysis of treatment termination r. among rheumatoid arthritis patients receiving disease-modifying antirheuma: drugs. Rheumatology, 2000; 39: 975—981.
21. Pinals RS. Drug therapy in Felty's syndrome. UpToDate, 2002; 20:2.
22. Pincus Т., Ferraccioli G., Sokka Т., et al. Evidence from clinical trials and longterm observational studies that disease-modifying anti-rheumatic drugs slow radiographic progression in rheumatoid arthritis: updating a 1983. Rheumatology, 2002;42:1346-1356.
23. Quin MA, Conaghan PC, Emery P. The therapeutic approach of early intervention for rheumatoid arthritisL what is the evidence? Rheumatology, 2001; 40: 1211— 1230.
24. Ritchie D.M., Boyle J.A., Mclnnes J.M., et al. Clinical studies with an articular index for assessment of joint tenderness in patients with rheumatoid arthritis. Q.J.Med., 1968; 37:393-406.
25. Van der Heijde D.M.F.M, van’t Hof M.A., van Riel P.L.C.M, van Leeuwen M.A, vas. Rijswijk M.H, van de Putte L.B.A. Validity of single variables and composite indices for measuring disease activity in rheumatoid arthritis. Ann. Rheum. Dis., 1992; 51:177-181.
26. Van Gestel A.M., Prevoo M.L.L, van’t Hof M.A, van Rijswijk M.H, van de Putte L.B., van Riel P.L.C.M. Development and validation of the European League Against Rheumatism response criteria for rheumatoid arthritis. Arthritis Rheum., 1996; 39:34—40.
27. Mandil L.A., Esdaile J.M. Adult Still's disease. UpTodate 2003;ll, No.3 \
28. Yamaguchi М., Ohta A., Tsunematsu Т., et al. Preliminary criteria for classification of adult Stills disease. J. Rheumatol., 1992;29:424-435.
Ревматоидный артрит: новые подходы к старой проблеме
Р. М. Балабанова, профессор, доктор медицинских наук, руководитель отдела изучения и коррекции аутоиммунных нарушений ГУ Института ревматологии РАМН
Е. В. Шекшина, кандидат медицинских наук, младший научный сотрудник
Хроническое системное иммуноопосредованное воспалительное заболевание с преимущественным поражением периферических (синовиальных) суставов по типу симметричного эрозивнодеструктивного полиартрита, сопровождающегося пролиферацией синовиоцитов и ангиогенезом (что сближает его с онкологическими заболеваниями), называют РЕВМАТОИДНЫМ АРТРИТОМ (РА).
Распространенность РА среди взрослого населения различных климато-географичеcких зон - в среднем 0,6-1,3%. Ежегодная заболеваемость за последние годы сохраняется на высоком уровне - 0,02%. Для РА характерен половой диморфизм: женщины болеют в 3-4 раза чаще, чем мужчины. Во время беременности нередко развивается ремиссия. У женщин пик заболеваемости РА приходится на 35-55 лет, у мужчин - на 40-60 лет.
Этиология и патогенез заболевания
До настоящего времени причина возникновения РА не уточнена. В его развитии равнозначна роль как генетических, так и внешнесредовых факторов, среди которых предполагается участие инфекции, иммунизации, питания, переливания крови, курения, УФО-облучения и др.
О генетической предрасположенности к заболеванию свидетельствует его высокая агрегация в семьях больных РА. Заболеваемость им в раннем возрастезначительно чаще встречается в семьях, где были родственники с РА. Роль генетической предрасположенности к этому заболеванию подтверждена и его более высокой частотой среди монозиготных близнецов (12-32%) по сравнению с дизиготными (3,5-9%).
Из эндогенных факторов в развитии РА определенную роль играют половые гормоны, что подтверждается большой частотой заболевания среди женщин, а также положительным влиянием беременности на течение РА и его обострением после родоразрешения или ее прерывания. У женщин, больных РА, выявлен дефицит андрогенов - тестостерона и дегидроэпиандростерона, у мужчин также низок уровень тестостерона.
Участие половых гормонов в развитии РА подтверждает влияние экзогенных эстрогенов (оральных контрацептивов), снижающих риск развития РА.
Среди внешнесредовых факторов возникновения этого заболевания в первую очередь предполагается роль инфекции. Классических эпидемиологических доказательств инфекционной этиологии РА нет, но это не исключает ее участия в генетически предрасположенном организме, о чем свидетельствуют результаты исследований на животных.
Специфический (инфекционный) триггер РА не установлен, но есть много претендентов: микоплазма, парвовирус В19, цитомегаловирус (ЦМВ), вирус простого герпеса 6-го типа, Эпстайна - Барр вирус (ЭБВ). Один из механизмов развития так называемых аутоиммунных заболеваний, к которым относится и РА, - “молекулярная мимикрия”. Микробы и вирусы могут содержать белковые структуры (аминокислотные последовательности), сходные с белками хозяина. Иммунный ответ на патоген с целью его элиминации может “изменить направление”, в результате чего возникает перекрестная реакция с собственными антигенами, структурно схожими с чужеродными.
В сыворотке больных РА содержатся в повышенных титрах антитела к латентному или репликативному антигену ЭБВ. Тлимфоциты периферической крови больных РА не способны контролировать ЭБВ-позитивные В-лимфобластоподобные линии, и это объясняет частоту ЭБВ-инфицированных периферических В-лимфоцитов при РА в сравнении с контролем. Длительная экспозиция одного или нескольких вирусов, что нередко имеет место при РА, может играть триггерную роль в инициации иммунного воспаления, так как антигены вируса не только перекрестно реагируют с антигенами хозяина, но и выполняют адъювантный эффект.
Патогенез
ЭФ РА(?) > Трансформация IgG в АутоАГ > IgM,A,G-ревматоидные факторы + АутоАГ = ЦИК > синовиальная ткань > повышение активности медиаторов воспаления, проницаемости микрососудов, хемотаксис лейкоцитов, фагоцитоз ЦИК > повреждение лизосом лейкоцитов и макрофагов > высвобождение лизосомальных ферментов > повреждение клеточных структур > образование новых АутоАГ > цепная реакция
Неизвестный этиологический фактор ревматоидного артрита вызывает первичную иммунную реакцию в виде образования антител в виде IgG. По неизвестной причине они трансформируются и превращаются в аутоантигены, которые в условиях иммунодефицита по Тсупрессорам инициируют выработку В-лимфоцитами антител групп Ig M, A, G (ревматоидные факторы). Они образуют с аутоантигеном циркулирующие иммунные комплексы (ЦИК), оседающие главным образом в синовиальной оболочке суставов и вызывающие повышение активности медиаторов воспаления, нарушение микроциркуляции, активацию хемотаксиса лейкоцитов.
В процессе фагоцитоза повреждаются лизосомы нейтрофилов и макрофагов, высвобождаются лизосомальные ферменты, повреждающие клеточные структуры. Образуются новые аутоантигены, новые аутоантитела, и патологический процесс приобретает характер цепной реакции. На какое-то время она может затихать, но затем вновь возобновляется под влиянием специфических и неспецифических факторов.
Исход воспалительного процесса характеризуется редукцией, а затем и прекращением миграции клеток в воспаленную ткань с последующим повышением апоптоза клеток и восстановлением тканей. Постоянная активация моноцитов и макрофагов приводит к неспособности их блокировать эти процессы, что способствует переходу острого воспаления в хроническое.
Важную роль в патогенезе РА играют простагландины.
Другой механизм, участвующий в воспалении и деструкции хряща, - усиление новообразования сосудов. Этот ангиогенез в синовии связывают с действием провоспалительных цитокинов, который приводит к усилению проникновения воспалительных клеток в ткани сустава, что обеспечивает поступление питательных веществ, необходимых для нормального функционирования воспалительных и пролиферирующих клеток. Важная роль отводится нейтрофилам, увеличение количества которых в синовиальной жидкости приводит к гиперпродукции хемоаттрактантов. Дегрануляция нейтрофилов сопровождается высвобождением протеиназ, реактивных форм кислорода, продуктов метаболизма арахидоновой кислоты.
Процессы, происходящие в синовии при РА, напоминают локальное злокачественное новообразование. Масса вновь образованных клеток и соединительной ткани во много раз превышает массу нормальной синовиальной оболочки. Образующийся при РА паннус обладает способностью к инвазии и деструкции хряща, субхондральной кости и связочного аппарата. Синовиоциты больных РА обладают фенотипическими свойствами трансформированных опухолевых клеток. В синовиальной жидкости и тканях обнаружено увеличение уровня факторов роста - тромбоцитарного и фибробластного. Сходство ревматоидного синовита и локализованного злокачественного новообразования проявляется и на молекулярном уровне. Ряд цитокинов обладает способностью вызвать длительно сохраняющиеся фенотипические изменения клеток.
Патологический процесс при РА в первую очередь развивается в суставах и околосуставных тканях и имеет свои особенности в зависимости от стадии заболевания.
Синовит выявляется рано, даже в клинически неизмененном суставе. Нарушения в синовиальной мембране обусловлены иммунологическими процессами. В начальных стадиях процесса строма скудно инфильтрирована лимфоцитами, плазматическими клетками, лаброцитами (тучными клетками) и макрофагами. Т-лимфоциты имеют морфологические и иммунологические характеристики антигензависимых клеток. В-лимфоциты как предшественники плазматических клеток и сами плазматические клетки синтезируют иммуноглобулины in situ.
На ранней стадии имеет место пролиферация кроющих синовиоцитов типа В, имеющих морфологическое сходство с фибробластами. Клетки формируют несколько слоев с очаговым “частоколом”. Встречаются капилляриты и продуктивные васкулиты. На этой стадии выявляется преобладание экссудативных и альтернативных процессов в синовиальной мембране - отек, полнокровие и очаги фибриноидных изменений.
Для развернутой стадии характерна картина хронического пролиферативного процесса. При этом отмечаются выраженная гиперплазия и гипертрофия ворсинок. Становится более очевидной пролиферация кроющих синовиоцитов с формированием нескольких слоев и наличием гигантских клеток.
В морфогенезе ревматоидного синовита важное место занимает поражение сосудов микроциркуляторного русла - васкулиты и ангиоматоз. В стенках сосудов выявляются отложения иммуноглобулинов. На этой стадии в синовиальной мембране могут формироваться ревматоидные узелки, а в случае присоединения амилоидоза - амилоидные массы.
Особенность позднего периода - выраженный ангиоматоз, сочетающийся с продуктивными васкулитами и тромбозами. Волнообразное течение болезни находит отражение и в морфологии синовиальной мембраны.
Под ней в перихондральной ее части формируется синовиальный паннус - сосудистая и фиброзная ткань. В процессе развития он врастает в хрящ, разрушая его.
Специфический морфологический признак при РА - ревматоидный узелок. Его можно увидеть в различных органах и тканях, но наиболее частая локализация - кожа и синовиальная мембрана. Узелок представлен очагом фибриноидного некроза, окруженного палисадообразно расположенными макрофагами, лимфоцитами и плазматическими клетками. Нередко в нем видны гигантские многоядерные клетки. С помощью моноклональных антител удалось подтвердить участие иммунопатологических реакций в развитии ревматоидных узелков.
Особое место в прогрессировании ревматоидного процесса занимают васкулиты, которые выявляютсяво всех органах, но не имеют специфических морфологических признаков. Исследование сосудов кожи у больных РА с признаками кожного васкулита показало, что изменения микроциркуляторного русла носят генерализованный характер.
При этом заболевании обнаруживают продуктивные, деструктивные и деструктивно-продуктивные васкулиты. Сосуды поражены генерализованно и полиморфно - от умеренной пролиферации эндотелия и инфильтрации наружной оболочки до некроза средней оболочки стенки сосуда. Преобладают поражения сосудов мелкого калибра - кожи, скелетной мускулатуры, внутренних органов. Наиболее типичны продуктивные васкулиты и тромбоваскулиты, реже встречается панваскулит типа узелкового полиартериита с очаговым или тотальным некрозом средней оболочки.
Изменения в сосудах крупного и среднего калибра могут быть обусловлены поражением vasa vasorum и развивающейся в связи с этим ишемией сосудистой стенки. Иногда наблюдается картина аортита с последующим склерозом и расширением устья аорты.
Поражение серозных оболочек проявляется чаще всего сухим плевритом с незначительным фибринозным выпотом, что ведет к образованию спаек. В легочной ткани процесс развивается по типу хронической межуточной пневмонии, очагового или диффузного пневмосклероза с образованием ревматоидных узелков.
Поражение почек обусловлено гломерулонефритом (мембранозным или мембранозно-пролиферативным), нефроангиосклерозом, хроническим интерстициальным нефритом, ангиитом. Часто нефропатия обусловлена отложением амилоидных масс. В латентной стадии амилоид обнаруживают периваскулярно в ткани пирамид и некоторых артериолах клубочков, в нефротической стадии в большинстве клубочков, стенках сосудов, пирамидах отложения амилоида массивные.
В желудочно-кишечном тракте выявляют признаки гастрита, энтерита, колита, которые достаточно часто обусловлены иммунокомплексным процессом, что подтверждается обнаружением в подслизистой основе иммуноглобулинов, фибрина. Наиболее тяжелые изменения желудочно-кишечного тракта связаны с отложением амилоидных масс в слизистой оболочке, стенке сосудов с развитием лимфоидно-плазмоцитарной инфильтрации, атрофией слизистой оболочки и подслизистой основы.
В биоптатах печени отмечают изменения в портальной соединительной ткани с продуктивными васкулитами, лимфоидно-гистиоцитарной или плазмоцитарной инфильтрацией, склеротические изменения, а также дистрофию, некроз гепатоцитов. При амилоидном поражении отложения амилоида наблюдают в ретикулярной строме долек печени по ходу внутридольковых капилляров, в стенке сосудов. Амилоид нередко замещает большую часть паренхимы.
В селезенке выявляют гиперплазию и плазматизацию лимфоидной ткани, пролиферацию эндотелия синусов, отложения белковых преципитатов.
При РА поражаются различные отделы нервной системы и ее элементы (сосуды, соединительная ткань, нервные волокна). Периферическая система в основном поражена за счет vasa nervorum. В соединительной ткани нервной системы выявляют фибриноидные изменения, лимфоидные и плазмоклеточные инфильтраты, а также отложения амилоида, микронекрозы.
Клиническая картина РА
Суставной синдром - ведущий в клинической картине РА. Начало заболевания чаще всего подострое (55-70%), как правило, спровоцированное перенесенной острой инфекцией или обострением хронической, охлаждением, травмой, стрессовой ситуацией.
Развитию артрита за несколько недель или месяцев предшествует продромальный период, признаки которого - усталость, похудание, периодически возникающая боль в суставах (часто на изменение атмосферного давления), снижение аппетита, повышенная потливость, субфебрильная температура, небольшая анемия, увеличение СОЭ.
По данным В. А. Насоновой и М. Г. Астапенко (1989), в продромальном периоде у 32% больных развивается утренняя скованность, особенно в суставах конечностей, которая при активном движении проходит. Среди причин возникновения этого симптома - нарушение нормального ритма выработки гормонов надпочечниками со смещением на более поздний период суток, а также аккумуляция цитокинов в отечной жидкости воспаленных суставов во время сна.
В начальном периоде РА у 1/3 больных отмечают артралгии, усиливающиеся при движении, у 2/3 - симметричный артрит мелких суставов кистей и стоп. Боль и скованность наибольшие в утренние часы, постепенно убывающие к вечеру. Интенсивность и длительность этих проявлений коррелирует с прогрессивностью болезни, сохраняясь при выраженной активности до обеда, а у отдельных больных проходит только к вечеру.
У 8-15% страдающих РА заболевание начинается остро в течение нескольких дней. При этом пациент может указать время и движение, спровоцировавшее боль. Артралгии могут сопровождаться такой же резкой болью в мышцах, длительной утренней скованностью, лихорадкой, что приводит больного к обездвиженности.
В 15-20% случаев РА начинается незаметно с медленным прогрессированием артрита без повышения температуры тела, ограничения движений.
Поражение суставов в ранней стадии РА может быть нестойким и самопроизвольно исчезать на несколько месяцев и даже лет. Стойкий полиартрит с прогрессированием воспалительного процесса отмечен у 70% больных. Первыми, как правило, при РА вовлекаются вторые-третьи пястно-фаланговые, проксимальные межфаланговые и суставы запястья, реже - плюсне-фаланговые. Затем по частоте поражения следуют коленные, локтевые, голеностопные. Позднее вовлечение крупных суставов некоторые авторы объясняют более высоким соотношением поверхности синовиальной мембраны к суставному хрящу. По нашим данным, у 87% заболевших все началось с поражения мелких суставов кистей, у 9,7% - крупных (коленные, плечевые). Стойкий прогрессирующий полиартрит имел место у 43%, у 57% больных он носил волнообразное течение с периодами ремиссии. У 20,4% пациентов развился ишемический некроз головок бедренных костей.
Некоторые суставы в дебюте болезни остаются интактными (“суставы исключения”) - дистальные межфаланговые, первый пястнофаланговый сустав большого пальца кисти, проксимальный межфаланговый мизинца.
Ранняя фаза РА характеризуется преобладанием экссудативных явлений симметрично пораженных суставов кистей с наличием выпота, определяемого по симптому флюктуации, воспалительному отеку периартикулярных тканей, резкой болезненности при пальпации, положительному симптому сжатиякисти.
Над мелкими суставами может быть слегка гиперемирована кожа, а над крупными - повышенная температура. Вследствие воспаления суставных тканей и рефлекторного спазма мышц резко ограничивается движение в пораженных суставах, что ведет к развитию мышечной атрофии. Артрит сопровождается воспалительным поражением влагалищ сухожилий, чаще разгибателей, реже - сгибателей кисти и стопы.
У 15-20% заболевших в первый год болезни может произойти спонтанное затухание симптомов артрита и развиться ремиссия болезни. Но у большей части больных процесс принимает прогрессирующий характер с переходом в экссудативно-пролиферативную фазу.
Наряду с общими симптомами (слабость, астения, похудание, ухудшение сна, аппетита, субфебрильная температура) прогрессирует суставной синдром. Преобладание пролиферативных процессов в суставных тканях приводит к их утолщению, стойкой плотной или пружинящей припухлости периартикулярных тканей, что вызывает изменение конфигурации суставов, в первую очередь мелких - кистей и стоп, запястья, лучезапястных, коленных, локтевых. Плечевые, тазобедренные суставы поражаются при РА редко, еще реже вовлекаются суставы позвоночника.
Классификация РА
Первая была предложена А. И. Нестеровым в 1961 году, после чего неоднократно уточнялась в связи с появлением новых данных о клинике и вариантах течения РА. Последний был одобрен на I Всероссийском конгрессе ревматологов в 2003 году.
Выделено 2 клинико-иммунологических варианта: серопозитивный и серонегативный РА. Полиартрит как основное проявление этого заболевания включает в себя оба варианта. Внесуставные проявления в основном отнесены к серопозитивному варианту и представлены лишь там, где ревматоидная принадлежность не вызывает сомнений. Сюда же отнесена особая форма РА - синдром Фелти. Серонегативный вариант РА имеет свои клинико-лабораторные особенности, к нему отнесен и синдром Стилла взрослых.
Характеризуя активность заболевания, выделяют 4 степени: 0 - ремиссия, 1 - низкая, 2 - средняя, 3 - высокая. Определение активности базируется на наиболее лабильных клинических и лабораторных признаках:
- выраженность боли по визуальной аналоговой шкале (ВАШ), где ее отсутствие приравнивается к нулевой отметке, а максимальное значение - к 10 см
- длительность утренней скованности в минутах
- показатели СОЭ и СРБ
Определение СРБ в нашей стране не стандартизировано, поэтому мы взяли за исходное значение норму, а далее - ее 2-3- и более кратное превышение.
Зарубежными ревматологами предложено для оценки активности РА применять DAS (счет активности болезни).
По МКБ Х принята такая классификация РА: Воспалительные полиартропатии
Влияние менструального цикла на течение ревматоидного артрита и хирургических заболеваний
Почему при месячных болят ноги: причины, симптомы, терапия
Течение ревматоидного артрита часто облегчается в лютеиновой фазе с максимальным синтезом стероидов яичников. Аналогичным образом улучшение наступает во время беременности, а обострение наступает в послеродовой период. Субъективная утренняя скованность и боли в суставах возникают во время менструации и в начале фолликулярной фазы. Rudge et al. Объективно продемонстрировали колебания тяжести симптомов ревматоидного артрита, связанных с менструальным циклом.
Они подтвердили значительное снижение средней силы сжатия кулаков с началом менструации. Кроме того, максимальное увеличение суставов пальцев было достигнуто в течение 6 дней после начала менструации, что во многих случаях сопровождалось увеличением веса.
Причина «менструального артрита» (редкое состояние, при котором воспаление суставов возникает только во время менструации), как полагают, вызвана резким снижением синтеза гормонов яичников в результате инволюции лютеиновой кислоты. Циклические изменения проявления ревматоидного артрита могут быть проявлением измененного иммунного ответа в результате цикличности менструации.
И эстрогены, и прогестерон обладают противовоспалительными свойствами и поэтому благотворно влияют на симптомы артрита. Предменструальные изменения тяжести симптомов также объясняются изменением восприятия боли, связанным с предменструальными колебаниями настроения.
Некоторым женщинам с ревматоидным артритом помогают эстрогены сами по себе или в составе комбинированного перорального контрацептива. Оральные противозачаточные таблетки могут отсрочить начало ревматоидного артрита, но не полностью. Терапия эстрогенами у женщин в постменопаузе не защищает от ревматоидного артрита.
Имеются данные о том, что острый аппендицит чаще развивается в лютеиновой фазе, хотя это может быть связано с ошибочно диагностированной болью в правом нижнем квадранте живота в результате кисты желтого тела, ведущей к ненужной аппендэктомии. Другие расстройства, которые ухудшаются после овуляции и в предменструальной фазе менструального цикла, включают: угри, аллергию и эндокринную анафилаксию, наследственный ангионевротический отек, многоформную эритему, крапивницу, афтозную язву, синдром Бехчета, острую перемежающуюся порфирию, пароксизмальную глаукомовентарную пароксизмальную глаукомовентарную опухоль.
Агонисты люлиберина использовались для лечения некоторых из этих состояний (в основном рецидивирующей анафилаксии, острой перемежающейся порфирии), когда симптомы становятся особенно тяжелыми или приводят к инвалидности. В отличие от этих состояний течение миастении имеет тенденцию к облегчению перед менструацией. Хотя одно раннее исследование показало, что операция на груди более эффективна в лютеиновой фазе, ученые не нашли дальнейшего подтверждения этого открытия.
Обострение определенных дискомфортов в определенные периоды менструального цикла - явление хорошо известное. Невозможно переоценить важность проспективных записей симптомов в контексте менструального цикла для облегчения диагностики и лечения. Часто для лечения таких обострений достаточно соответствующей циклической смены симптоматической терапии. Если эти меры окажутся неэффективными, следует попытаться фармакологически подавить овуляцию. При отсутствии положительных результатов имеет смысл продолжить терапию агонистами люлиберина со «стероидной добавкой» или более дешевой альтернативой - медроксипрогестероном или даназолом.
Если по разным причинам эта лечебная тактика не может применяться в течение длительного времени и женщина больше не собирается выполнять репродуктивные функции, последним методом остается гистерэктомия и двусторонняя овариэктомия с последующей гормональной заместительной терапией (ЗГТ).
Кратко о современных представлениях о влиянии менструального цикла и предменструального синдрома на женский организм:
- Термин ПМС должен относиться к комплексу довольно тяжелых симптомов, в основном психиатрических, существенно нарушающих повседневную деятельность и поддерживающих нормальные отношения с другими людьми.
- Врач может с уверенностью поставить диагноз ПМС только при наличии предполагаемой записи симптомов в течение 1-2 месяцев.
- В наиболее тяжелой степени ПМС симптомы начинаются вскоре после овуляции (за 2 недели до менструации) и исчезают в конце менструации.
Считается, что у некоторых восприимчивых женщин нормальные колебания уровня половых гормонов вызывают изменения в активности центральных нейромедиаторов, особенно серотонина, что, в свою очередь, приводит к значительным перепадам настроения и изменениям поведения.
Контролируемые клинические испытания показали, что прогестерон и масло примулы вечерней неэффективны при лечении ПМС.
- Ряд новых антидепрессантов, которые увеличивают активность серотонина в ЦНС, облегчают тяжелые симптомы ПМС.
- У женщин с менструальной мигренью начало головной боли вызвано резким снижением уровня эстрогена в сыворотке крови, а не изменениями других гормонов.
- Женщинам с менструальной мигренью, у которых не наблюдается достаточного облегчения симптомов, показана профилактическая гормональная терапия для стабилизации уровня эстрогена.
- Все типы припадков могут обостриться во время менструации, хотя фокальная эпилепсия встречается чаще, чем генерализованная эпилепсия.
- У некоторых женщин с инсулинозависимым сахарным диабетом наблюдаются изменения гликемического профиля в лютеиновой и предменструальной фазах.
- Симптомы ревматоидного артрита часто менее выражены в лютеиновой фазе, когда синтез стероидов в яичниках максимален.
Редактор: Искандер Милевски. Дата публикации обновления: 18.3.2021
Болят ноги перед месячными
Многие женщины испытывают боли внизу живота и пояснице во время менструации. Некоторые люди обращаются к гинекологам с жалобами, говоря, что у них болят ноги во время менструации. Дискомфорт может возникнуть в конце цикла и длиться до начала менструации.
Могут ли болеть ноги во время месячных
Пациенты любого возраста борются с возникновением болей в нижних конечностях во время менструации. К гинекологам приходят с недугами:
- матери с дочерьми в подростковом возрасте девочек; женщины детородного возраста; женщины в пременопаузе.
Неприятные ощущения возникают в результате гормональной перестройки. У некоторых женщин ноги болят незначительно, в то время как другие жалуются, что не могут ходить из-за боли, даже когда находятся в состоянии покоя.
Симптоматика болей в ногах при месячных
В зависимости от причин боли в ногах выраженность симптомов различается. Пациенты могут жаловаться на тянущую боль или чувство боли. Неприятные ощущения концентрируются вокруг щиколоток, колен и бедер.
Боль вызывается естественными физиологическими изменениями, происходящими в организме, т. Е. Кровеносными сосудами, заболеваниями суставов и неврологическими расстройствами.

Во время месячных болят суставы
Боль в суставах - один из симптомов тяжелой дисменореи. При вышеуказанном диагнозе одновременно появляются сильные боли внизу живота, поясницы, вегетативные и эмоциональные расстройства.
Чтобы узнать причины болей в суставах перед месячными, нужно пройти комплексное обследование. Во время менструации дискомфорт может усиливаться у пациенток, страдающих дегенеративно-дистрофическими изменениями суставной ткани. Обратите внимание, что сопровождающие симптомы:
- боль с пальпацией; отек, покраснение; Подвижность с ограниченными возможностями.
Некоторые пациенты начинают болеть суставами даже при отсутствии заболевания. Дискомфорт вызван избытком простагландина, отсутствие эндогенных опиатов в сочетании с порогом низкого боли. Это симптом припоминающегося синдрома натяжения.
Тянет ноги перед месячными
Потягивание часто встречается в подростках. Их внешний вид вызван изменениями, происходящими в организме. Кости и мышцы во время полового созревания растут быстро, сосудистая и нервная система не отстает от их развития. Нервные наконечники становятся более чувствительными, сильно реагирующими на любые раздражительские факторы, простагландин становится более яснее.
Репродуктивные женщины могут сообщать гинекологу с жалобой, что их ноги болят до менструации. Если боль охватывает нижнюю часть спины, живота, тошнота появляются, слабость, головокружение, врач может диагностировать дисменорею.

Чувство потянув часто встречается у пациентов с воспалением хронического использования. Замедленное преимущество воспаление вызывает боль в нижних путях, которые излучают поясничную зону, нижние конечности. Также болезненные конечности у женщин, которые имеют тенденцию к отеку.
Ломит ноги перед месячными
Ощущение мышечной боли и суставов накануне менструации редко. Сильные боли ногой у женщин, которые имеют чрезмерное разделение тазовых костей перед доставкой, перемещенные круги во время беременности. Изменения в форме скелета провоцируют сужение кровеносных сосудов, нервных окончаний. С появлением менструации под воздействием гормонов чувствительность тела увеличивается.
Чувство боли в ногах происходит у женщин, страдающих дегенеративными изменениями, позвоночникам. Когда окончание нервов в кросс-зоне угнетены, конечности начинают болеть. Боль распространяется на бедрах, нижние ноги.
Во время месячных болит бедро
Чаще всего женщины чувствуют боль в матке, придатки. Некоторые пациенты докладывают гинекологу с жалобами на дискомфорт в пах, бедер. Они появляются в первый день менструации или за несколько дней до его начала. Характеристика для дисменореи - распространение боли во всем нижнем теле. В случае таких заболеваний сначала необходимо исключить совместные заболевания, кровеносные сосуды, неврологические расстройства.

Почему при месячных болят ноги
Чтобы объяснить причины боли ног во время менструации, она будет получена после комплексного исследования. Появление ощущений боли может быть вызвано физиологическими или патологическими причинами. Чтобы определить точную причину, необходимо проверить репродуктивные органы, кровеносные сосуды, суставы, определить, нет проблем с позвоночником, воспалением. Ноги могут болеть после родов, хирургических процедур.
Физиологические причины боли в ногах перед месячными
Гинекологи часто встречаются с пациентами с четкой синдромом прембрель, который жалуется, что их ноги болят во время менструации. Доктор может предположить, что боль вызывается PMS, если из интервью, кажется, что из менструальной женщины
- Повышенная раздражительность; Увеличивает аппетит; Изменить вкусовые предпочтения; Опухание очевидно.
Под воздействием гормонов вены в ногах расширяются, что приводит к чувству тяжести, побаловать себя.
Тело активно производит простагландины, необходимые для миометрического сокращения при подготовке к менструации. Их концентрация крови увеличивается, существует сокращение кровеносных сосудов и развитие состояния ишемии. Гемодинамические барьеры нарушаются, в клетках развивается голод кислорода, поэтому боль увеличивается.

Возникновение физиологической боли характерно для девочек во время полового созревания. При отсутствии заболеваний репродуктивных органов дискомфорт суставов проходит в течение 1-2 лет с начала менструации. Гормональный фон нормализует, между разработкой опорно-двигательного, сосудистой, нервной системы не существует равновесия.
Во время пременопаузы гормональных изменений ноги начинают болеть. Если этот симптом возникает до менопаузы, убедитесь, что нет сердечно-сосудистых заболеваний, суставов.
Патологические причины
Чтобы определить причины боли ноги перед менструалом, в первые дни менструации гинекологи проводят визуальный обзор, двуручный осмотр матки, руководство по ультразвуку. Боль может возникнуть из-за хронического применения придатков, матки, эндометриоза, других заболеваний репродуктивной системы.
При отсутствии проблем с репродуктивными органами ноги начинают болеть из-за прогресса сосудистых заболеваний, опорно-двигательного аппарата:
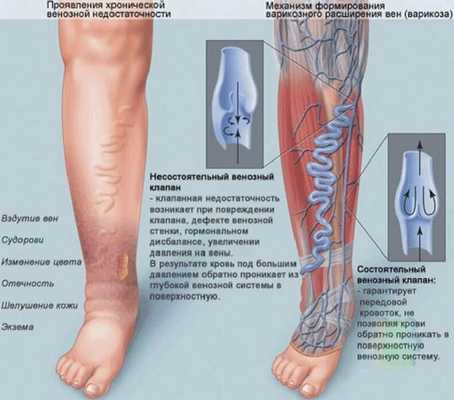
- остеохондроз; тромбофористое воспаление вен; артрит; Оплодотворение межпозвоночной грыжи; опухоли; дегенеративные, воспалительные заболевания пруда; венозный провал.
Эндокринологическое заболевание приводит к ослаблению иммунной системы, появления полиневропатии.
Когда нужно обратиться к врачу
Чувствующее, что периодически повредить нижние конечности, женщины начинают принимать обезболивающие, применять мази. Самоцепляющие приводят к прогрессу базовой болезни, что является причиной боли.
Если ноги периодически болят, увеличивая дискомфорт во время менструации или перед его запуском, вы должны проконсультироваться с гинекологом. При отсутствии проблем будет необходим консультация с флебогутом, неврологом, эндокринологом, ревматологом, травматологом и другими специалистами с узким профилем.
Диагностика
- Биохимические, общие анализы крови; МРТ; гистероскопия; Ультразвук; Сосудистое обследование.
Каждый врач выбирает тесты, которые помогают найти недостаток или наличие проблем с профилем. Доктор Гинеколог, в дополнение к исследованию, ручным половым органам, дает реферал к ультразвуку. Если обнаружены опухоли или кисты, можно рекомендовать терапевтическую и диагностику лапароскопии.
В случаях, когда колени болят во время менструации, докторские заказы на радиография, артрография, диагноз подвижности суставов. В случае заболевания вены рекомендуется ультразвуковое ангизисканирование, флебография с рентгеновским, CT или MRI контрастностью.
Лечение
Тактика терапии пациентов с лирикой боли выбираются в зависимости от причин дискомфорта. Если болевой синдром представляет собой симптом PMS, агенты, которые нормализуют гормональный фон, полезны.
Врачи могут выбрать лекарства для улучшения состояния суставов или увеличить тонус проживания. При необходимости предписаны седативные, обезболивающие и многовитаминовые комплексы.
Возможные осложнения
Пациенты, которые начали испытывать боль в ноге во время менструации, должны пройти всеобъемлющее исследование. Важно выявить основное заболевание, которое вызывает болезненные чувства. Если причина не удалена, условие постепенно ухудшается.
Гинекологическое заболевание в развитой форме приводит к бесплодию. Заболевания пруда, от позвоночника усложняют жизнь. Отсутствие лечения приводит к нарушению подвижности конечностей, возникают проблемы с ходьбой. Из-за нарушения венозного тона, кровоток к конечностям ухудшается.
Профилактические меры
Предотвращение возникновения болезненных чувств во время менструации будет возможно, если вы обратите внимание на вашу диету, физическую активность. Боль в ногах чаще начинается с пациентов с избыточным весом. Это связано с увеличением нагрузки пруда, тенденция к варикозному вену.
Превентивные меры также включают в себя:
- Носить удобную обувь; Контрастные ноги; Регулярная автоматическая.
Питание во время второй фазы цикла очень важна. С тенденцией к появлению боли придется отказаться от алкоголя, еда, которые провоцируют отек, уменьшают количество кофе.
Заключение
Ввиду того, что мои ноги болят во время менструации, идут в гинеколог. При отсутствии заболеваний репродуктивной системы при условии комплексного исследования. Необходимо быстро определить причину боли и удалить ее. Возникновение боли вызвано физиологическими или патологическими факторами.
Читайте также:
